第5讲 晶体场理论2 颜色成因教学课件
大学二年级结晶化学-课件-第七章
时间。 (1)萤光:余辉时间(ta) ≤ 10-8秒者, 即激发一停,发光立即停止。发光基 本不受温度影响。 (2)磷光:余辉时间 ≥ 10-8秒者,即 激发停止后,发光还要继续一段时间。 根据余辉的长短,磷光又可分成短期 磷光(ta ≤10-4秒)和长期磷光(ta ≥10-4 秒)。磷光的衰减强烈地受温度影响。
萤光和磷光的发光机理示意图
§ 7.2 晶体的力学性质
1 . 晶体的密度 密度(D):单位体积的晶体质量,单位g/cm3。 晶体密度与构成离子的原子量和晶体结构的堆积密度直接
有关。 晶体密度分成理论密度和实测密度。
晶体的理论密度(X光密度)表达式:
D=MZ/NAV M:晶体化学式的分子量,Z:单位晶胞中的分子数, NA=Avogadro常数=6.023×1023mol-1,V:单位晶胞的体积(实测 晶胞参数 计算)
SiO2同质多象变体的密度与n的关系
光在晶体中的传播特点
高级晶族晶体:一个折射率:n ,光性均质体;发生单折 射现象,不发生双折射。
中级晶族晶体:两个主折射率:ne和no,光学一轴晶;
(ne-no)>0,正光性晶体(+) (ne-n级晶族晶体:三个主折射率: ng,nm,np ,光学二轴
n=折射率,k=吸收系数 表面光滑的银(n=0.18,k=3.6)R=95%
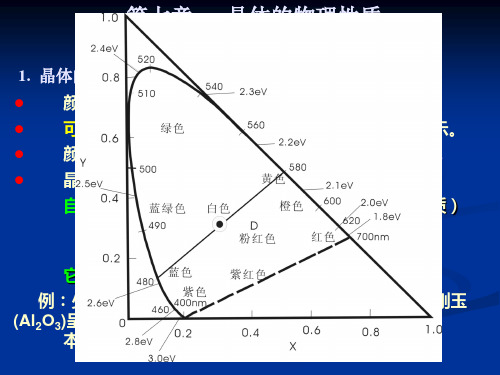
半导体、绝缘体的带隙宽度(Eg)决定晶 体的颜色
晶体吸收能量E>Eg的所有可见光,透过E <Eg的可见光。
例: 金刚石Eg=5.4eV,可见光的E<5.4eV 而全部透过晶体,故金刚石无色透明。
磷化镓(Eg=2.4eV)吸收绿色以上色光, 晶体呈橙色。
蓝宝石偏振吸收光谱图
第一节晶体场理论ppt课件

释了配合物的空间构型等问题。
为了较好地解释配合物的磁性和高自旋和低自旋等问
题,1935年培特和冯弗莱克提出了晶体场理论(CFT)。
晶体场理论认为:配合物中央离子(原子)和配体之
间的相互作用,主要来源于类似于离子晶体中正负离子间
的静电作用;在此作用下,中心离子的原子轨道可能发生
分裂。
z
Hans Albrecht Bethe
——2006年高中化学竞赛试题
6-2 某钒的配合物具有 VO(N2O2)配位结构形式,所有的氮、氧原子都为配 位原子。且配合物只检测到一种 V-N键,两种 O-V键。
美国著名化学家,因阐明化学 键的本质,并以此解释了复杂分子 结构,1954年获诺贝尔化学。
看法。 他认为:所有配合物都是以共价配键结合的。并结合杂化轨道理论对
配合物的构型加以解释。
严格执行突发事件上报制度、校外活 动报批 制度等 相关规 章制度 。做到 及时发 现、制 止、汇 报并处 理各类 违纪行 为或突 发事件 。
相对较多;
npx npy
☆pz 轨道受配体静电的排斥相对
较小,其能级升高相对较少。
E’
npz
np
四方配位场
严格执行突发事件上报制度、校外活 动报批 制度等 相关规 章制度 。做到 及时发 现、制 止、汇 报并处 理各类 违纪行 为或突 发事件 。
⑶ d轨道
中央离子的 d 轨道有五种取向(dxy、dyz、dxz、dx2-y2、dz2),当四 个配体沿±x、±y 方向靠近中央离子时,中央离子 d 轨道受配体静电的 排斥,其能级升高,并发生能级分裂。
点平面方向。
z
z
x
y
y
x
dxz
dyz
第二章 晶体场理论

3 配体的性质
将一些常见配体按光谱实验测得的分裂能从 小到大次序排列起来,就得到光谱化学序列。 I-Br-Cl-SCN-F-~(NH2)2CO~OH-~ONOHCOO-C2O42-H2OCH2(COO)22- NCSNH2CH2COO-EDTApy~NH3 NH2C2H4NH2~(NH2CH2CH2)2N-SO32-dipy phen NO2-H-CH3-CN-CO 以配位原子分类: I Br Cl S F O N 离子半径(pm) 216 195 181 184 136 132 170
6H2O
HS
HS
LS HS
LS HS
根据P和△的相对大小可以对配合物的高、低 自旋进行预言: ①在弱场时, 由于△值较小, 配合物将取高自旋构 型; 相反, 在强场时, 由于△值较大, 配合物将取 低自旋构型。 ②对于四面体配合物, 由于△t=(4/9)△0, 这样小 的△t值, 通常都不能超过成对能值, 所以四面体 配合物通常都是高自旋的。 ③第二、三过渡系金属因△值较大, 故他们几乎 都是低自旋的。 ④由于P(d5)>P(d4)>P(d7)>P(d6), 故在八面体场 中d6离子常为低自旋的 (但Fe(H2O)62+和CoF63-例 外),而d5离子常为高自旋的(CN-的配合物例外)。
d轨道在四面体场中的能级分裂
y
x
dx2-y2
z
y
dz2
z
x
y
dxy
x
y
x
dyz(dxz)
设四个配体只在x、y平面上沿±x和±y 轴方 向趋近于中心原子, 因dx2-y2轨道的极大值正好处 于与配体迎头相撞的位置, 受排斥作用最强, 能级 升高最多。其次是在xy平面上的dxy轨道。而dz2 仅轨道的环形部分在xy平面上, 受配体排斥作用 稍小, 能量稍低, 简并的dxz、dyz的极大值与xy平 面成45°角, 受配体排斥作用最弱, 能量最低。 总之, 5条d轨道在Sq场中分裂为四组, 由高到 低的顺序是: ①dx2-y2, ②dxy, ③dz2, ④dxz和dyz
配位化学讲义 第四章(1) 价键理论、晶体场理论

第三章配合物的化学键理论目标:解释性质,如配位数、几何结构、磁学性质、光谱、热力学稳定性、动力学反应性等。
三种理论:①价键理论、②晶体场理论、③分子轨道理论第一节价键理论(Valence bond theory)由L.Pauling提出要点:①配体的孤对电子可以进入中心原子的空轨道;②中心原子用于成键的轨道是杂化轨道(用于说明构型)。
一、轨道杂化及对配合物构型的解释能量相差不大的原子轨道可通过线性组合构成相同数目的杂化轨道。
对构型的解释(依据电子云最大重叠原理:杂化轨道极大值应指向配体)二、AB n型分子的杂化轨道1、原子轨道的变换性质考虑原子轨道波函数,在AB n分子所属点群的各种对称操作下的变换性质。
类型轨道多项式sp x xp p y yp z zd xy xyd xz xzd d yz yzd x2-y2x2-y2d z22z2-x2-y2(简记为z2)*s轨道总是按全对称表示变换的。
例:[HgI3]- (D3h群)平面三角形A1′:d z2、sE′:(p x、p y )、(d x2-y2、d xy)A2″:p zE″:(d xz、d yz)2、σ轨道杂化方案1)四面体分子AB4(Td)[CoCl4]2-以四个杂化轨道的集合作为分子点群(Td)表示的基,确定该表示的特征标:E 2 -1 2 0 0 (z2, x2-y2)T1 3 0 -1 1 -1T2 3 0 -1 -1 1 (xy,xz,yz) (x,y,z)a(A1)=1/24(1×4+8×1×1+3×1×0+6×1×0+6×1×2)=1a(A2)=1/24 [1×4+8×1×1+3×1×0+6×(-1)×0+ 6×(-1)×2]=0a(E)=1/24 [2×4+8×(-1)×1+3×2×0+6×0×0+ 6×0×2]=0a(T1)=1/24 [3×4+8×0×1+3×(-1)×0+6×1×0+6×(-1)×2]=0a(T2)=1/24 [3×4+8×0×1+3×(-1)×0+6×(-1)×0 +6×1×2]=1约化结果Γ=A1+T2由特征标表:A1T2s (p x、p y、p z)(d xy、d xz、d yz)可有两种组合:sp3(s、p x、p y、p z)、sd3(s、d xy、d xz、d yz)* 以一组杂化轨道为基的表示的特征标的简化计算规则:Γ 5 2 1 3 0 3约化结果:Γ= 2A1′+A2〞+E′A1′A2〞E′s p z (p x、p y)d z2(d xy、d x2-y2)两种可能的组合:(s、d z2、p z 、p x、p y)( s、d z2、p z、d xy、d x2-y2)约化得:Γ=A1g+B1g+E uA1g B1g E us d x2-y2(p x、p y)d z2两种类型:dsp2(d x2-y2、s、p x、p y)、d2p2(d z2、d x2-y2、p x、p y)5)八面体AB6(O h) 例:[Fe(H2O)6]3+(d z2、d x2-y2、s、p x、p y、p z) 3、π成键杂化方案在AB n分子中,原子A上要有2n个π型杂化轨道和在B原子上的2n个π原子轨道成键。
《晶体场理论》课件

03
通过实验测量可以获得晶体的各种物理性质数据,如通过硬度测试了解晶体的机械性能,通过电导率测试了解晶体的导电性能等。
03
CHAPTER
晶体场理论的基本概念
晶体场中电子由于受到周期性势场作用而产生的能级分裂,产生的能量差值即为晶体场稳定化能。
晶体场稳定化能
晶体场分裂能
随着晶体场强度的增加,分裂能级的间距逐渐增大。
强晶体场中分裂能级较为稳定,弱晶体场中分裂能级不稳定。
在晶体场作用下,电子云会发生变形,以适应周围势场的分布。
电子云变形
光谱线分裂
磁有序现象
化学键合作用
由于晶体场作用,光谱线会分裂成多个子线,子线的数目和位置取决于晶体场的对称性和强度。
在强晶体场中,由于电子自旋和轨道磁矩的相互作用,可导致磁有序现象的出现。
常用的数值计算方法包括有限差分法、有限元法、蒙特卡洛方法等。这些方法可以根据具体问题选择合适的数值计算方法,以获得更准确的结果。
05
CHAPTER
晶体场理论的应用
磁性材料设计
利用晶体场理论预测和解释不同材料的磁学性质,为磁性材料的设计和优化提供理论支持。
催化剂设计
通过晶体场理论模拟催化剂的电子结构和活性位点,优化催化剂的性能,提高化学反应效率。
晶体场效应
由于晶体场作用导致能级分裂的能量差值,反映了晶体场对电子的束缚强弱。
晶体场对电子的相互作用和影响,包括电子云变形和能级分裂等。
03
02
01
能级分裂类型
分裂能级数量
分裂能级间距
分裂能级的稳定性
01
02
03
04
根据晶体场强度和对称性,能级分裂可分为弱场分裂、中等强度场分裂和强场分裂。
晶体场理论

①金属离子的电荷和电子构型; ②金属离子d轨道的主量子数; ③配体的本性.
3
表 1 某些正八面体配合物的Δ值(×100cm-1)
nd
n
Mn+
Br-
Cl-
配体 OX2- H2O NH3 CN-
en
Edta4-
3d1 Ti2+
当金属离子的正电荷增大时,与同一配体生 成的配合物的Δ值增大。例如第一过渡系的三价 离子的Δ值一般比二价离子大4060%。金属离子 的电荷增大与配体作用增强,分裂能增大。
2 金属离子的主量子数
在同一副族不同过渡系列金属的对应配合物 中,Δ值随着d轨道主量子数的增大而增加。
第四周期过渡元素3dn到第五周期过渡元素 4dn, Δ约增加40~50%,由第五周期过渡元素 4dn到第六周期5dn,Δ约增加20~25%。这是因 为随主量子数的增加,d轨道在空间伸展的范围 增大,受配体的作用更强烈。
由于配体的作用,d轨道能级发生分裂,体 系d电子进入分裂的轨道比处于未分裂轨道时的 总能量降低,这样获得的能量称为晶体场稳定化 能,用符号CFSE表示。
CFSE的影响因素:中心离子的d电子数目、 配体场强弱、 晶体场类型。
CFSE的计算: (以八面体场为例)
令 nn12::te2gg轨轨道道中中的的电电子子数数
§ 晶体场理论(CFT)
在1929年由Bethe提出, 30年代中期为 Van Vleck等所发展, 与Pauling的价键理论 处于同一时代, 但当时并未引起重视, 到50 年代以后又重新兴起并得到进一步发展, 广 泛用于处理配合物的化学键问题。
晶体场理论是一种静电
晶体场理论_图文

高
高
低
低
高
高
⑴八面体络合物中d电子的排布
当△0﹥P时,即强场的情况下,电子尽可能占据 低能的t2g轨道。
注意:d1,d2,d3,d8,d9和d10无高低自旋之分,仅d4,d5d6和d7有
。
△
eg
t2g
d1 d2 d3 d4 d5 d6 d7 d8 d9 d10
但是
当△0<P时,即弱场的情况下,电子尽可能分占 五个轨道。
-
-
4911
-
-
-
-
-
2597
-
-
-
2597
-
-
-
1903
-
-
-
1476
-
363
-
-
-
500
-
-
-
403
-
-
-
371 306 3283
-
347
-
-
323
从表中的实验数据来看,一般说有:
10000cm-1<△0<30000cm-1
这样的d-d跃迁常常发生在可见光或紫外区。
从表中的实验数据来看,相应络合物中的△t 值,显然比△0的值小的多.
又例如
在四面体场中,均为弱场高自旋 ,d6为e3 t23,如图:
(2/5)△t
△t=(4/9)×10Dq
(3/5)△t
可求
(3) 络合物的热力学稳性
用CFSE可解释放络合物热学稳定性的事实 。 以第一系列过渡元素二价离子的水合物 [M(H2O)6]2+的水化(-△H)为例:
M:Ca2+…… Zn2+ d:d0 …….. d10
第6讲 配位场理论2 颜色成因教学课件

蓝宝石 (2)二者在垂直c轴方向上以棱相接 此时两离子的距离比较大(0.297nm),两离子的分子轨道 的叠加程度变小,结果电荷转移吸收带向红光区移动,吸收 中心在620nm,在非常光中,刚玉呈蓝绿色。
电荷转移类型
M→M:异核原子价态之间
宝石学实例: Fe2+→Ti4+ 蓝色(刚玉、蓝晶石、蓝锥矿、矽线石)、褐色(镁电 气石、钙铁榴石、红柱石、符山石)、黄-黑色(黑榴 石)、绿色(绿柱石) Mn2+→Ti4+ 绿黄色(电气石)
a* 1gb<t1ub<egb<t2g<eg*<a1g*<t1u
配位场例子:六配位的八面体[ML6]
电荷转移:电子从一个分子轨道跃迁到另一个 分子轨道。
在这类跃迁中,电子从主要定域在配体L上的 轨道跃迁到主要定域在金属M上的轨道上,或 相反。
通常电荷迁移跃迁比d-d跃迁具有较高的能量, 吸收峰一般出现在近紫外和紫外区。吸收强度 也比大d-d跃迁大得多。
《宝石颜色成因理论》
第6讲 配位场理论2
石斌 中国地质大学(武汉)珠宝学院
2020/10/3
原子 结构
原子电子轨道
原子轨道理论
物
晶体场理论
质
微
配位场理论
观
结
分子电子轨道
分子轨道理论
构
分子 结构
能带理论 色心
能带(色心)理论
分子振动转动
分子振转理论
在晶体场理论中,它所假设的前提是:在中心阳离子 与配位体之间的化学键是离子键,彼此间不存在电子 轨道的重叠,亦即没有共价键的形成;同时,配位体 被作为点电荷来处理。但这种假定的前提条件在共价 性强的化合物,例如硫化物、含硫盐及其类似化合物 中,显然是不能适用的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第5讲 晶体场理论2
石斌
中国地质大学(武汉)珠宝学院
基本概念与知识
配位化合物
基本概念与知识
d轨道
基本概念与知识
能量换算 1cm-1=1.24×10-4eV
可见光范围
波长:380nm – 760nm 波数:26,316cm-1 – 13,158cm-1 电子伏特:3.16eV – 1.63eV
能级分裂
能级分裂
能级分裂
晶体场理论的应用
Cr3+离子在不同宝石中呈现的颜色
红宝石
变石 祖母绿
Cr3+
晶体场理论的应用
Cr3+离子在不同宝石中呈现的颜色
Cr3+离子电子组态3d3
基谱项为4F,在八面 体晶体场作用下分裂 为三项:4A2,4T1,4T2
晶体场理论的应用
Cr3+离子在不同宝石中呈现的颜色
3 Dt
5
正四面体场
e
晶体场的分裂能及其影响因素
4)配体的对称性(几何构型) ➢ 平面正方形
d x2y2
Es
自由离子d轨道
dxy
d z2
dxz、dyz
能级分裂
在八面体环境中单电子能级的分裂
能级分裂
在不同对称性类型的环境中单电子能级分裂
能级分裂
在不同对称性 类型的环境中 自由离子能级 分裂
能级分裂
能级分裂
在八面体对称中d2-d8组态的能级(分裂)图
dn(八面体)≡ d10-n(四面体)
能级分裂
Oh
Td
S A1g
A1
P T1g
T1
D Eg, T2g
E, T2
F A2g , T1g, T2g
A2 , T1, T2
G A1g , Eg, T1g , T2g
A1 , E, T1 ,T2
H Eg, 2T1g , T2g,
➢ dxy, dyz, dxz 轨道由于未正对配体,而是指向两坐标轴 夹角的平分线上,因而受到配体的排斥作用较小,能量 较低。
定性解释:八面体晶体场下d轨道分裂
自由离子 E0
Es = 0Dq 球形场
d x 2- y 2 d z 2
二重简并eg
6Dq Δ 0=10Dq
-4Dq
d xy d xz d yz 三重简并t2g
E, 2T1 , T2
I A1g , A2g, Eg, T1g , A1 , A2, E, T1 ,
2T2g
2T2
D4h
A1g A2g, Eg A1g , B1g , B2g , Eg A2g, B1g, B2g , 2Eg 2A1g , A2g , B1g , B2g , 2Eg A1g , 2A2g , B1g , B2g , 3Eg 2A1g, A2g, 2B1g, 2B2g , 3Eg
八面体场
晶体场的分裂能及其影响因素
分裂能Δ0:是指在晶体场中d轨道分裂后的最高能 量的d 轨道与最低能量的d轨道之间的能量差。 一般将八面体场中d 轨道分裂后的两组轨道能 量差Δ0 分为10 等分。用Δ0=10Dq表示。
Δ0=Eeg - Et = 10Dq
影响分裂能的因素主要有中心离子的电荷、元素 所在周期和配体的性质及对称性,其变化规律 大体如下:
当配合物构型相同时,各种配体对同一中心离子产生的分
裂能值由小到大的顺序如下:
I-<Br-<Cl-<S2-<SCN-<NO3-<F-<(NH)CO~OH– ~ONO-~HCOO-<C2O42-<H2O<NCS-<EDTA<NH3< en<CN–
这一顺序称为光谱化学序,即配体产生的晶体场从弱到强 的顺序。
Cr 3+
自由离子谱项
为 3d3 组态,自由 离子基谱项是4 F, 在八面体晶体场中, 4F基谱项一步分裂 为:4A2,4T2,4T1。
在分裂能级之 间,d 电子从低能 级吸收一定的能量 后,跃迁至高能级 上,由此产生与之 对应的吸收光谱, 使宝石呈色。
Cr3+离子在不同宝石中呈现的颜色
晶体场的分裂能及其影响因素
4)配体的对称性(几何构型) ➢ 正八面体场
dz2, d(x2-y2)
eg
自由离子d轨道
Es
球形场
10Dq
dxz,dxy,dyz
t2g
晶体场的分裂能及其影响因素
4)配体的对称性(几何构型) ➢ 正四面体场
t2
自由离子d 轨道
Es
球形场
D D 52 D t
4 410Dq t 90 9
晶体场理论的基本要点
➢ 晶体场理论是静电作用模型,把中心离子 (M)和配位体(L)的相互作用看作是类似 离子晶体中正负离子的静电作用;
➢ 当L接近于M时,M中的d轨道受到L负电荷的 静电微拢作用,使原来能级简并的d轨道发 生分裂。
➢ 分裂类型与化合物的空间构型有关;晶体 场相同,L不同,分裂程度也不同。
Fe3+ 13700 cm-1 Fe2+ 10400 cm+
9300 cm-1
晶体场的分裂能及其影响因素
2)元素所在周期 对于相同配体、带相同正电荷的同族金属离子形
成配合物时,分裂能△0值随中心离子所在周期 数的增加而增大。(约增加30%至50%) 随周期增加,同族电荷相同的中心离子半径增加, d轨道伸展离核越远,越易受到配体负电场的排 斥作用,因此,分裂能△0增大。
[Co(en)2]3+: △0 = 23000 cm-1 [Rh(en)2]3+: △0 = 34400 cm-1 [In(en)2]3+: △0 = 41200 cm-1
晶体场的分裂能及其影响因素
3)配体的性质
对于同一中心离子、不同配体的配合物,其分裂能随配体 形成的晶体场的强弱不同而不同。场的强度越大,分裂 能越大。由光谱数据统计出。
晶体场的分裂能及其影响因素
1)中心离子电荷
同一过渡元素形成的配合物,当配体相同时,
中心离子正电荷越高,分裂能越大。
因为中心离子正电荷越高,对配体引力越大,
导致中心离子与配位原子核间距减小,配体产
生的晶体场对d电子的斥力越大,分裂能越大。
[M(H2O)6]n+: Mn3+ 21000 cm-1 Mn2+ 7800 cm-1
晶体场的定性解释:八面体晶体场下d
轨道分裂
定性解释:八面体晶体场下d轨道分裂
➢ 自由原子中的d轨道是五重简并轨道。中心原子所受配 位体静电场作用可分为球对称和场对称两种,前者对所 有的d轨道产生同样的作用,能量升高,能级不分裂; 后者产生能级分裂,在八面体晶体场影响下,d轨道分 裂成两组;。
➢ dx2–y2 及dz2 轨道由于在坐标轴上正指向配体,因而受 配体的排斥作用较大,能量较高。
