化学必修二 实验清单
高中化学实验目录

高中化学实验目录以下是一份高中化学实验目录的示例:
1. 酸碱中和反应实验
- 确定酸、碱的浓度
- 酸、碱的中和反应
2. 金属活动性实验
- 排列金属活动性的实验
- 金属与酸的反应实验
3. 氧气制备实验
- 过氧化氢分解制备氧气的实验
- 高锰酸钾分解制备氧气的实验
4. 集气法制备气体实验
- 羟基磷酸分解制备氢气的实验
- 碳酸氢钠与酸反应制备二氧化碳的实验
5. 气体的溶解度实验
- 观察二氧化碳、氧气、氮气的溶解度实验
6. 非金属氧化物与水反应实验
- 碳、硫、磷等非金属氧化物与水反应的实验
7. 电解质与非电解质实验
- 测试不同物质的电解性实验
8. 精馏实验
- 分离混合物中的液体成分实验
9. 燃烧实验
- 不同物质的燃烧实验
10. 过滤实验
- 过滤混合物实验
请注意,这只是一个示例目录,实际的高中化学实验目录可能会根据教材和教学内容的不同而有所变化。
建议根据教学需要和实验设备条件,选择适合的实验项目。
高中化学必修2实验汇总

第一章物质结构元素周期律实验1-1 卤素氧化性强弱P9药品:新制氯水、溴水、NaBr溶液、KI溶液、四氯化碳仪器:试管、滴管实验备注1. 将少量新制的饱和氯水分别加入盛有NaBr溶液和KI溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置2. 将少量溴水加入盛有KI溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置实验1-2 化学键中的离子键P21药品:金属钠、氯气(必修1制取)仪器:滤纸、石棉网、酒精灯实验备注取一块绿豆大的金属钠(切去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热。
待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方。
观察现象。
第二章化学反应与能量实验2-1 放热反应P32药品:6mol/L的盐酸、铝条仪器:温度计、试管、砂纸实验备注在一支试管中加入2~3 mL 6mol/L的盐酸,再插入用砂纸打磨过的铝条。
观察现象,并用温度计测量溶液温度的变化。
实验2-2 吸热反应P32药品:Ba(OH)2•8H2O、NH4Cl仪器:烧杯、玻璃片、玻璃棒实验备注将约20g Ba(OH)2 •8H2O晶体研细后与约10gNH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片或小木板上,用玻璃棒快速搅拌,闻气味,用手触摸悲壁下部,试着用手拿起烧杯,观察现象。
实验2-3 酸碱中和热P32药品:2mol/L 的盐酸、2mol/L NaOH溶液仪器:烧杯、量筒、玻璃棒、温度计实验备注在50mL烧杯中加入20mL 2mol/L的盐酸,测其温度。
另用量筒量取20mL 2mol/LNaOH溶液,测其温度,并缓慢地倾入烧杯中,边加边用玻璃棒搅拌。
观察反应中溶液温度的变化过程,并作好记录。
实验2-4 化学能与电能的转换P37药品:锌片、铜片、稀硫酸仪器:导线电流表、烧杯实验备注将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸的烧杯中,观察现象。
实验2-5 温度对化学反应速率的影响P44药品:5%的H2O2溶液、1mol/L FeCl3溶液仪器:试管、滴管、烧杯、火柴实验备注在2支试管大小相同的试管中,装入2~3mL 约5%的H2O2溶液,分别滴入1~2滴1mol/L FeCl3溶液。
高中化学实验目录

高中化学实验目录一、必修一1、粗盐的提纯实验目的:掌握溶解、过滤、蒸发等基本操作,除去粗盐中的杂质。
实验用品:粗盐、蒸馏水、烧杯、玻璃棒、漏斗、滤纸、蒸发皿、酒精灯、三脚架、坩埚钳等。
实验步骤:(1)溶解:将粗盐逐渐加入盛有蒸馏水的烧杯中,并用玻璃棒搅拌,直至粗盐不再溶解。
(2)过滤:制作过滤器,将烧杯中的液体沿玻璃棒倒入过滤器中,进行过滤。
(3)蒸发:将滤液倒入蒸发皿中,用酒精灯加热,同时用玻璃棒不断搅拌,当有大量晶体析出时,停止加热,利用余热蒸干。
2、萃取和分液实验目的:了解萃取和分液的原理,学会用萃取和分液的方法分离混合物。
实验用品:碘水、四氯化碳、分液漏斗、烧杯等。
实验步骤:(1)加液:将碘水和四氯化碳加入分液漏斗中,盖好玻璃塞。
(2)振荡:用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来振荡,使两种液体充分接触。
(3)静置:将分液漏斗放在铁架台上静置。
(4)分液:待液体分层后,将分液漏斗颈上的玻璃塞打开,或使塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下,上层液体从上口倒出。
3、一定物质的量浓度溶液的配制实验目的:学会配制一定物质的量浓度溶液的方法。
实验用品:容量瓶、托盘天平、药匙、烧杯、玻璃棒、胶头滴管、蒸馏水、溶质。
实验步骤:(1)计算:根据所需溶液的浓度和体积,计算所需溶质的质量。
(2)称量:用托盘天平称量溶质的质量。
(3)溶解:将称好的溶质放入烧杯中,加入适量蒸馏水溶解,并用玻璃棒搅拌。
(4)转移:将溶解后的溶液冷却至室温,沿玻璃棒小心地转移到容量瓶中。
(5)洗涤:用少量蒸馏水洗涤烧杯和玻璃棒 2-3 次,洗涤液也转移到容量瓶中。
(6)定容:向容量瓶中加入蒸馏水,至液面离刻度线 1-2 厘米时,改用胶头滴管滴加蒸馏水至液面与刻度线相切。
(7)摇匀:盖好瓶塞,反复上下颠倒摇匀。
4、金属钠与水的反应实验目的:观察金属钠与水的反应现象,了解钠的性质。
高中化学必修2实验通知单
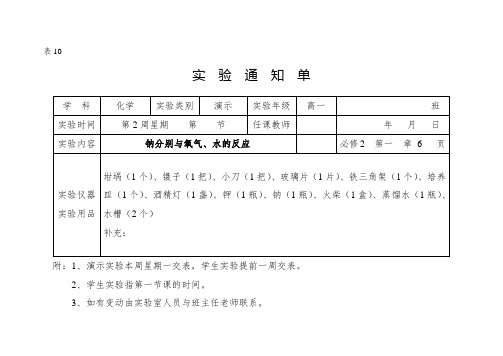
表10实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
实验通知单附:1、演示实验本周星期一交表,学生实验提前一周交表。
2、学生实验指第一节课的时间。
3、如有变动由实验室人员与班主任老师联系。
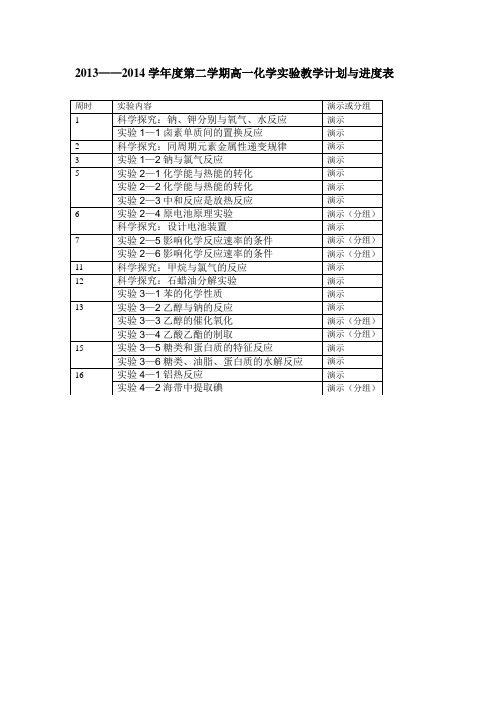
高中化学必修2实验一览表
15
实验3—5糖类和蛋白质的特征反应
演示
实验3—6糖类、油脂、蛋白质的水解反应
演示
16
实验4—1铝热反应
演示
实验4—2海带中提取碘
演示(分组)
2013——2014学年度第二学期高一化学实验教学计划与进度表
科学探究:设计电池装置
演示
7
实验2—5影响化学反应速率的条件
演示(分组)
实验2—6影响化学反应速率的条件
演示(分组)
11
科实验
演示
实验3—1苯的化学性质
演示
13
实验3—2乙醇与钠的反应
演示
实验3—3乙醇的催化氧化
演示(分组)
实验3—4乙酸乙酯的制取
周时
实验内容
演示或分组
1
科学探究:钠、钾分别与氧气、水反应
演示
实验1—1卤素单质间的置换反应
演示
2
科学探究:同周期元素金属性递变规律
演示
3
实验1—2钠与氯气反应
演示
5
实验2—1化学能与热能的转化
演示
实验2—2化学能与热能的转化
演示
实验2—3中和反应是放热反应
演示
6
实验2—4原电池原理实验
演示(分组)
化学必修二实验计划
4
实验1—2名称:钠与氯气实验
钠、滤纸、石棉网、酒精灯、氯气
3
5
实验(2—1、2—2、2—3)认识和感受化学能与热能的相互转化实验
盐酸、砂纸、铝条、温度计、氢氧化钡晶体、氯化铵晶体、烧杯、玻璃片、小木板、氢氧化钠溶液
4
6
实验2—4原电池原理实验
原电池装置、锌片、铜片、导线、稀硫酸、电流表
5
7
科学探究实验:水果电池和各种原电池
15
16
实验4—1名称:铝热反应
纸、铁架台、铁圈、蒸发皿、氧化铁、铝粉、氯酸钾、镁条
16
17
实验4—2名称:海带提取碘
海带、刷子、剪刀、酒精、稀硫酸、双氧水、淀粉
16
笨、溴水、酸性高锰酸钾
11
12
实验3—2名称:乙醇的性质实验
乙醇、钠、配有注射器针头单孔塞、澄清石灰水
12
13
实验3—3名称:乙醇的催化氧化实验
乙醇、铜丝
13
14
实验3—4名称:乙酸的酯化实验
试管、乙醇、浓硫酸、乙酸、酒精灯、饱和碳酸钠溶液
14
15
实验3—5、3—6名称:糖类和蛋白质性质实验
葡萄糖、新制的氢氧化铜、碘酒、土豆、面包、鸡皮、蔗糖、稀硫酸、氢氧化钠
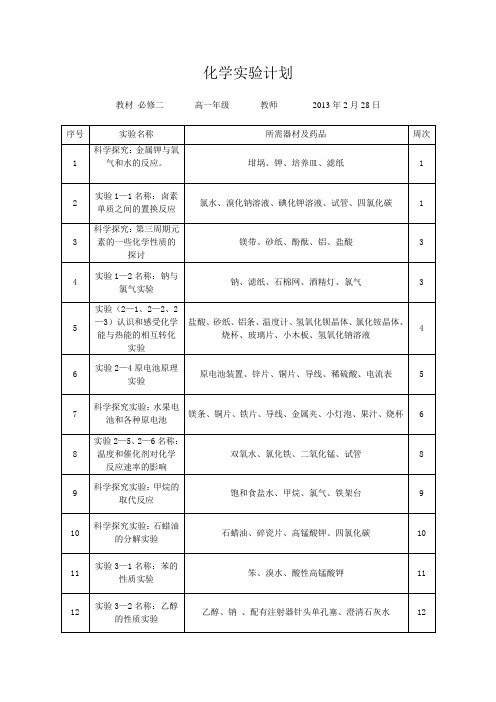
化学实验计划
教材必修二高一年级教师2013年2月28日
序号
实验名称
所需器材及药品
周次
1
科学探究:金属钾与氧气和水的反应。
坩埚、钾、培养皿、滤纸
1
2
实验1—1名称:卤素单质之间的置换反应
氯水、溴化钠溶液、碘化钾溶液、试管、四氯化碳
1
3
科学探究:第三周期元素的一些化学性质的探讨
高中化学(必修2)实验目录
序号实验名称实验药品及仪器备注1 卤素单质间的互相置换氯水、NaBr溶液、KI溶液、溴水、四氯化碳溶液、试管。
2 钠、镁、铝与水反应的比较镁带、铝片、酚酞、1mol/L盐酸、砂纸、小试管。
3 钠在氯气中燃烧金属钠、氯气、滤纸、石棉网、酒精灯、铁架台(带铁圈)、4 化学反应中的吸热,放热现象6mol/L的盐酸、铝条、Ba(OH)2·8H2O晶体、NH4Cl晶体、2mol/L的盐酸、2mol/L的NaOH溶液、砂纸、烧杯、玻璃棒、玻璃片、温度计。
5 Cu—Zn稀硫酸原电池锌片、铜片、稀硫酸、导线、烧杯、电流表。
6 外界条件对反应速率的影响5%的H2O2溶液、1mol/LFeCl3溶液、MnO2粉末、烧杯、试管、热水。
7 石蜡油的分解石蜡油、酸性高锰酸钾、溴的四氯化碳溶液、石棉、碎瓷片、酒精灯、铁架台、试管、单孔橡胶塞、导气管。
探究8 苯的性质苯、溴水、酸性高锰酸钾溶液、试管。
9 乙醇与金属钠的反应无水乙醇、金属钠、滤纸、大试管、小试管、试管夹、医用注射针头、单孔橡胶塞、小烧杯。
10 乙醇的催化氧化无水乙醇、10-15cm长的铜丝、酒精灯、试管。
11 酯化反应无水乙醇、浓硫酸、无水乙酸、饱和碳酸钠溶液、酒精灯、铁架台、试管、单孔橡胶塞、导气管。
12 糖类、蛋白质的特征反应葡萄糖、CuSO4溶液、2%的NaOH溶液、碘酒、土豆片、鸡皮、浓硝酸、蒸发皿、酒精灯、试管。
13 蔗糖的水解20%的蔗糖溶液、稀硫酸、氢氧化钠溶液、新制备的Cu(OH)2、烧杯、试管。
14 铝热反应Fe2O3粉末、铝粉、氯酸钾固体、镁带、砂纸、滤纸、蒸发皿、火柴、铁架台(带铁圈)。
15 海带提纯市售干海带、稀硫酸、H2O2溶液、淀粉溶液、酒精、坩埚钳、酒精灯、铁架台(带铁圈)、石棉网、玻璃棒、小烧杯、普通漏斗、滤纸、蒸馏水。
序号实验名称实验药品及仪器备注1 化学反应中的吸热,放热现象6mol/L的盐酸、铝条、Ba(OH)2·8H2O晶体、NH4Cl晶体、2mol/L的盐酸、2mol/L的NaOH溶液、砂纸、烧杯、玻璃棒、玻璃片、温度计。
高中化学必修2实验总结
《化学必修2》实验汇编实验一:钾与水的反应:实验内容实验现象实验结论钾与水反应钾与水剧烈反应,浮在水面上,熔化成小球,不停地滚动,有气体产生,甚至发生轻微的爆炸。
钾能与水反应,反应产生气体、放热钠与水反应钠浮在水面上,熔化成小球,不停地滚动,发出“吱吱”响声,有气体产生向反应后的溶液里加入2滴酚酞试液,立即显红色。
练习1.BD实验二:金属与水、酸的反应1.现象镁与冷水不反应,加热后,镁条表面有气泡产生,一段时间后溶液变红。
化学方程式Mg+2H2O=Mg(OH)2+H2↑2.Mg Al现象产生气泡速率较快铝片表面有气泡产生化学方程式Mg+2HCl=Mg(OH)Cl2+H2↑2Al+6HCl=2AlCl3+3H2↑结论:金属与水或同浓度的酸反应的难易程度、剧烈程度可以用于比较金属的活泼性。
实验三:钠与氯气反应:现象钠在氯气中剧烈燃烧,产生大量白烟化学方程式2Na+Cl2=2NaCl实验四:化学反应与能量1.现象与解释:手有温暖的感觉,温度计测量的温度升高。
说明该反应是放热反应。
2.现象与解释:玻璃片上的水结成冰。
说明该反应是吸热反应。
实验五:催化剂对化学反应速率的影响。
(注意对比实验的设计方法)现象结论加入MnO2有大量气泡冒出MnO2对H2O2的分解有催化作用加入FeCl3有大量气泡冒出FeCl3对H2O2的分解有催化作用不用其它试剂没有明显现象结论:许多过渡金属的氧化物或盐类对H2O2的分解有催化作用。
练习2.(1)催化剂(或催化),2H2O22H2O+O2↑(2)2HIO+H2O2=I2+2H2O+O22H2O22H2O+O2↑(3)不正确,O元素和I元素的化合价均上升,没有化合价降低的元素(或违背电荷守衡原理)H2O2+2I-+2H+=2H2O+I22H2O22H2O+O2↑实验六:甲烷与氯气的反应(注意反应条件的控制) 现象包黑纸 没有明显变化没包黑纸①量筒内气体颜色变浅。
②量筒内壁出现黄色油状液滴。
高中化学必修2实验汇总
�性酸�质性学化的醇乙 性和饱有具否是苯验检
3 ..............................................................................物合化机有 3 ............................ 44P 2 ................................ 44P 响影的率速应反学化对剂化催 响影的率速应反学化对度温 换转的能电与能学化 热和中碱酸 应反热吸 应反热放
6-2 验实 5-2 验实 4-2 验实 3-2 验实 2-2 验实 1-2 验实 章二第
2 ............................................ 73P
2 ........................................................... 23P 1 ............................................................... 23P 1 ............................................................... 23P
17P
应反化酯的酸乙 4-3 验实
。味气的生产体液 中管试闻心小 �化变的丝铜察观 。次几复反 �中醇乙入插�热红至烧灼上灯精酒在�状 旋螺城绕端下�丝铜的长 mc Lm51~01 根 一取�醇乙 Lm5~3 入加中管试支一向 注 备 验 实
5
。象现察观�液溶粉淀滴几入加 。象现察观� �%3 为数分量质�2O2H Lm1 约 入加再� �L/lom3�酸硫稀滴几入滴中液滤在 。滤过�nim3~2 沸煮、拌搅�水馏蒸 Lm01 入加中其向�中杯烧到移转灰带海将 .2 。却冷 �热加止停�烬灰成变全完至带海烧灼�灯精 酒燃点。中埚坩入放�湿润精酒用�后碎剪 刀剪用� �洗冲水用要不�净刷子刷用物着附 的面表带海干把 �带海干的右左 g3 取 .1 注 备 验 实
高中化学实验目录 (2)[001]
高中化学实验目录实验一:酸碱中和反应的观察与测定实验目的观察和测定酸碱中和反应的现象,并学会利用指示剂进行酸碱中和滴定。
实验步骤1.准备所需实验器材和试剂:盛有酸性溶液的容器、酸性溶液、碱性溶液、酸碱指示剂、滴定管、滴定管夹等。
2.将酸性溶液倒入一个容器中。
3.将碱性溶液倒入另一个容器中。
4.用滴定管取一定量的酸性溶液滴入碱性溶液中,同时不断地加入酸碱指示剂。
5.当试液变色,且一滴酸性溶液能使试液保持新颜色时,记录滴定的酸碱溶液的体积。
6.重复实验步骤4和5,直至试液彻底转变为另一种颜色。
7.计算酸性溶液和碱性溶液的摩尔浓度差异,得到滴定的酸碱溶液的浓度。
实验结果与分析通过观察实验现象,我们发现酸性溶液与碱性溶液滴定反应后,试液的颜色会发生变化。
根据变色点的出现,我们可以判断滴定溶液的反应是否达到中和的状态。
通过记录滴定的酸碱溶液的体积,并计算酸碱溶液摩尔浓度的差异,我们可以推断酸碱溶液的浓度。
实验结论本实验通过酸碱中和反应的观察与测定,学会了利用指示剂进行酸碱中和滴定,通过记录滴定溶液的体积,并计算酸碱溶液摩尔浓度差异,可以确定酸碱溶液的浓度。
实验二:氧化还原反应的观察与测定实验目的观察和测定氧化还原反应的现象,并学会利用氧化还原指示剂进行氧化还原滴定。
实验步骤1.准备所需实验器材和试剂:盛有氧化剂的容器、氧化剂、还原剂、氧化还原指示剂、滴定管、滴定管夹等。
2.将氧化剂倒入一个容器中。
3.将还原剂倒入另一个容器中。
4.用滴定管取一定量的还原剂滴入氧化剂中,同时不断地加入氧化还原指示剂。
5.当试液变色,且一滴还原剂能使试液保持新颜色时,记录滴定的氧化剂和还原剂的体积。
6.重复实验步骤4和5,直至试液彻底转变为另一种颜色。
7.计算氧化剂和还原剂的摩尔浓度差异,得到滴定的氧化还原溶液的浓度。
实验结果与分析通过观察实验现象,我们发现氧化剂与还原剂滴定反应后,试液的颜色会发生变化。
根据变色点的出现,我们可以判断滴定溶液的反应是否达到滴定终点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验4-2(91)
蒸馏水、稀硫酸、3%H2O2、淀粉溶液
坩埚、酒精灯、小烧杯、玻璃棒
实验2-6(48)
5% H2O2溶液、MnO2粉末、1mol/L FeCl3溶液
试管
烯烃性质实验(67)
石蜡油、碎瓷片、酸性KMnO4溶液、溴的四氯化碳溶液
酒精灯、试管、试管、单孔塞
实验3-1(69)
苯、溴水、酸性高锰酸钾溶液
试管
实验3-2(73)
无水乙醇、钠、澄清石灰水
配有医用注射针头的单孔塞、小试管、烧杯
化学必修二实验清单
实验名称(页码)
实验药品实验仪器钠、钾 Nhomakorabea质对比(6)
钾
坩埚、培养皿
实验1-1(8)
氯水、溴水、NaBr溶液、KI溶液、四氯化碳、
试管
镁、铝性质对比(15)
镁带、铝、1mol/L盐酸、酚酞溶液
砂纸、试管、酒精灯
实验1-2(21)
钠、氯气
铁架台、石棉网、滤纸、集气瓶
实验2-1(33)
6mol/L盐酸、铝条
实验3-3(74)
乙醇、铜丝
酒精灯、试管
实验3-4(75)
乙醇、浓硫酸、乙酸、饱和碳酸钠溶液
酒精灯,单孔塞、试管、导管
实验3-5(79)
葡萄糖、氢氧化铜、碘酒、浓硝酸
试管、酒精灯、蒸发皿
实验3-6(79)
20%蔗糖、稀硫酸、氢氧化钠溶液、新制备的氢氧化铜
pH试纸、酒精灯
实验4-1(89)
氧化铁粉末、铝粉、氯酸钾、镁带
试管、砂纸、温度计
实验2-2(34)
Ba(OH)2.8H2O、NH4Cl晶体
烧杯、玻璃片、玻璃棒
实验2-3(34)
2mol/L盐酸、2mol/L NaOH溶液
量筒、玻璃棒、温度计
实验2-4(40)
锌片、铜片、稀硫酸
导线、电流表、烧杯
实验2-5(48)
5% H2O2溶液、1mol/L FeCl3溶液
试管、烧杯、火柴
