高中化学必修2 专题02 氮及其化合物专项训练新解析版)
人教版高中化学必修第二册第五章《第二节 第1课时 氮气和氮氧化物》练习题(解析版)

第二节 氮及其化合物第1课时 氮气和氮氧化物[核心素养发展目标] 1.能从分子结构的角度认识氮气的化学稳定性,熟知氮气与镁、氧气、氢气的化学反应及其条件,了解氮的固定和自然界中氮的循环。
2.能从物质类别和氮元素的化合价认识氮氧化物的性质与转化,熟知工业制硝酸的反应原理,促进“证据推理与模型认知”化学核心素养的发展。
一、氮气与氮的固定1.氮元素(1)结构氮原子一般通过共用电子对与其他原子相互结合构成物质。
(2)氮元素在自然界中的存在 2.氮气 (1)物理性质 通常情况下,氮气是无色、无味的气体,密度比空气的稍小,难溶于水。
(2)化学性质氮分子内两个氮原子间以共价三键(N ≡N)结合,断开该化学键需要较多的能量,所以氮气的化学性质很稳定,通常情况下很难与其他物质发生化学反应,但在高温、放电等条件下,氮气也可以与镁、氧气、氢气等物质发生化合反应。
写出氮气与下列物质反应的化学方程式。
①金属镁:N 2+3Mg=====点燃Mg 3N 2,氮气表现氧化性;②氢气:N 2+3H 2高温、高压催化剂2NH 3,氮气表现氧化性;③氧气:N 2+O 2=======放电或高温2NO ,氮气表现还原性。
(3)用途①氮气常用作保护气,如焊接金属、填充灯泡、保存食品等。
②氮气是合成氨、制硝酸的重要原料。
③液氮可用作制冷剂,应用于医学、科技等领域。
3.氮的固定(1)含义:将大气中游离态的氮转化为氮的化合物的过程。
(2)分类(1)氮原子与其他原子只能形成共价键,不能形成离子键(×)(2)氮的固定中氮元素一定被氧化(×)(3)工业上将NH3转化为其他铵态化肥属于人工固氮(×)(4)N2和足量的O2在放电条件下会生成NO2(×)(5)镁条在空气中燃烧时,可以与O2、N2、CO2等反应生成MgO、Mg3N2、C(√)氮在自然界中的循环如下图所示。
(1)过程①称为________,写出合成氨反应的化学方程式:_____________________________,该反应中氮气显__________(填“氧化”或“还原”,下同)性。
2024年人教版高中化学同步精品讲义(必修二)第04讲 5.4氮气和氮氧化物(含答案解析)

第1课时 氮气和氮氧化物1.了解氮的固定和自然界中氮的循环。
2.了解氮气的主要化学性质。
3.认识氮氧化物的性质与转化。
一、氮气与氮的固定 1.氮元素的原子结构和性质(1)氮元素的原子结构氮元素位于元素周期表的第二周期第ⅤA 族,氮原子最外层有5个电子,既不容易得到3个电子,也不容易失去5个电子。
氮原子一般通过共用电子对与其他原子相互结合构成物质。
(2)氮元素在自然界中的存在①游离态:主要以氮气分子的形式存在于空气中,约占78%(体积分数)。
②化合态:存在于动植物体内的蛋白质中,土壤、海洋的硝酸盐和铵盐中。
2.氮气的性质(1)物理性质通常情况下,氮气是无色、无味的气体,密度比空气的稍小,难溶于水。
(2)化学性质氮分子内两个氮原子间以共价三键(N ≡N)结合,断开该化学键需要较多的能量,所以氮气的化学性质很稳定,通常情况下很难与其他物质发生化学反应,但在高温、放电等条件下,氮气也可以与镁、氧气、氢气等物质发生化合反应。
写出氮气与下列物质反应的化学方程式。
①金属镁:N 2+3Mg=====点燃Mg 3N 2,氮气表现氧化性; ②氢气:N 2+3H 2高温、高压催化剂2NH 3,氮气表现氧化性;③氧气:N 2+O 2=======放电或高温2NO ,氮气表现还原性。
(3)用途①氮气常用作保护气,如焊接金属、填充灯泡、保存食品等。
②氮气是合成氨、制硝酸的重要原料。
③液氮可用作制冷剂,应用于医学、科技等领域。
3.氮的固定(1)含义:将大气中游离态的氮转化为氮的化合物的过程。
(2)分类:①自然固氮:大自然通过闪电释放能量将氮气转化为含氮的化合物(高能固氮),或者通过豆科植物的根瘤菌将氮气转化为氨(生物固氮)。
②人工固氮:工业合成氨。
二、一氧化氮和二氧化氮1.一氧化氮、二氧化氮的物理性质氧化物颜色状态气味水溶性NO无色气态无味难溶NO2红棕色气态刺激性气味与水反应2.一氧化氮、二氧化氮的相互转化操作一:在一支50 mL的注射器里充入20 mL NO,观察颜色,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器。
人教高中化学氮及其化合物 复习题含答案解析

人教高中化学氮及其化合物复习题含答案解析一、选择题1.硝酸钾是一种无氯氮钾复合肥,宜在种植水果、蔬菜、花卉时使用。
关于KNO3的说法中,不正确的是()A.从其阳离子看,属于钾盐B.从其阴离子看,属于硝酸盐C.它属于纯净物中的无机化合物D.因为含有氧元素,故它属于氧化物【答案】D【详解】A.硝酸钾含有的阳离子为钾离子,则硝酸钾属于钾盐,故A正确;B.硝酸钾含有的阴离子为硝酸根离子,则硝酸钾属于硝酸盐,故B正确;C.硝酸钾是由三种元素组成的盐,是纯净的无机化合物,故C正确;D.氧化物是由两种元素组成,并且一种元素为氧元素的纯净物,硝酸钾是由三种元素组成的盐,不属于氧化物,故D错误;故选D。
2.某些离子的检验及结论一定正确的是()A.加入氢氧化钠溶液并加热,产生气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ B.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则一定有CO32-C.加入氯化钡溶液有白色沉淀产生,再加入盐酸沉淀不消失,一定有SO42-D.某溶液加入稀盐酸酸化的AgNO3产生白色沉淀,则原溶液中一定含有Cl-【答案】A【详解】A. 加入氢氧化钠溶液并加热,产生气体能使湿润的红色石蕊试纸变蓝,则说明该气体为氨气,推出原溶液中一定有NH4+,A项正确;B. 原溶液中若含HCO3-,加入稀盐酸后也会产生无色无味能使澄清石灰水变浑浊的气体,故原溶液中不一定有CO32-,B项错误;C. 产生不溶于盐酸的白色沉淀也可能是AgCl,则原溶液中不一定有SO42-,C项错误;D. 加入盐酸酸化的AgNO3溶液时,则引入了Cl-,故不能证明是原溶液中是否含有Cl-,D项错误;答案选A。
3.对于硫酸和硝酸的比较中,下列叙述不正确的是()A.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装B.稀硫酸和稀硝酸都具有氧化性C.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性D.硫酸和硝酸都是重要的化工原料【答案】C【详解】A. 铝、铁与冷的浓硫酸和浓硝酸发生的钝化,因此冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装,故A正确;B. 稀硫酸和稀硝酸都具有氧化性,稀硫酸和金属反应生成氢气,表现氧化性,稀硝酸和金属反应生成硝酸盐和一氧化氮表现氧化性,故B正确;C. 浓硫酸和浓硝酸都具有很强的腐蚀性,浓硫酸具有脱水性,浓硝酸不具有,故C错误;D. 化工生产中用硝酸、硫酸生产化肥、农药、炸药、燃料,金属加工前的酸洗等,故D正确。
高一化学必修二氮及其化合物练习题含答案解析
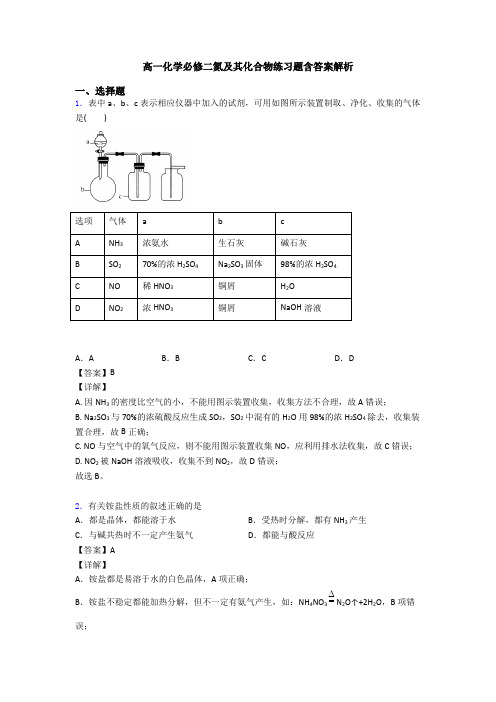
高一化学必修二氮及其化合物练习题含答案解析一、选择题1.表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是()选项气体a b cA NH3浓氨水生石灰碱石灰B SO270%的浓H2SO4Na2SO3固体98%的浓H2SO4C NO稀HNO3铜屑H2OD NO2浓HNO3铜屑NaOH溶液A.A B.B C.C D.D【答案】B【详解】A. 因NH3的密度比空气的小,不能用图示装置收集,收集方法不合理,故A错误;B. Na2SO3与70%的浓硫酸反应生成SO2,SO2中混有的H2O用98%的浓H2SO4除去,收集装置合理,故B正确;C. NO与空气中的氧气反应,则不能用图示装置收集NO,应利用排水法收集,故C错误;D. NO2被NaOH溶液吸收,收集不到NO2,故D错误;故选B。
2.有关铵盐性质的叙述正确的是A.都是晶体,都能溶于水B.受热时分解,都有NH3产生C.与碱共热时不一定产生氨气D.都能与酸反应【答案】A【详解】A.铵盐都是易溶于水的白色晶体,A项正确;B.铵盐不稳定都能加热分解,但不一定有氨气产生,如:NH4NO3N2O↑+2H2O,B项错误;C.铵盐都能与碱反应生成氨气,C项错误;D.铵盐不都能与酸反应,例如硝酸铵不能与酸反应,D项错误;答案选A。
3.除去铝制品表面的铜镀层,宜选用的试剂是()A.稀盐酸B.氯化钠溶液C.水D.浓硝酸【答案】D【详解】室温下,铜和浓硝酸反应生成硝酸铜而溶解,铝在冷的浓硝酸中钝化而不溶解,因此除去铝制品表面的铜镀层,宜选用的试剂是浓硝酸,故D正确;答案选D。
4.下列对于硝酸的认识中不正确的是()A.浓硝酸和稀硝酸都具有强氧化性B.铜与HNO3的反应属于分解反应C.金属与HNO3反应一般不产生氢气D.可用铁或铝制的容器盛装浓硝酸【答案】B【详解】A. 浓硝酸和稀硝酸中氮元素化合价降低可以表现出都具有强氧化性,A正确;B. 铜与HNO3反应生成硝酸铜、一氧化氮或二氧化氮和水,不属于分解反应,B不正确;C. 金属与HNO3反应中氮元素化合价降低,生成一氧化氮或二氧化氮等含氮化合物,一般不产生氢气,C正确;D. 铁或铝在冷的浓硝酸中钝化,可用铁或铝制的容器盛装浓硝酸,D正确;答案选B。
高考化学易错题专题训练-氮及其化合物练习题含详细答案

高考化学易错题专题训练-氮及其化合物练习题含详细答案一、氮及其化合物练习题(含详细答案解析)1.人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:(1)将N2转化为含氮化合物的过程称为固氮①人工固氮,将N2→NH3, N2发生_________反应②自然界固氮,可将少量N2转化为Ca(NO3)2等氮肥,转化途径如下(转化所需试剂及条件已略去):N2→NO→NO2→HNO3M−−→Ca(NO3)2。
写出NO→NO2→HNO3的化学方程式__________、__________。
将HNO3转化为Ca(NO3)2,列举三种不同类别......的化合物M_______(写化学式)。
(2)科学合理地保存、施用氮肥① NH4HCO3需阴凉处保存,原因是__________(写化学方程式)。
②铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式________。
(3)过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。
(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去):① X可能是______、_______。
Y是___________。
②尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3则尿素中C 元素化合价为__________。
【答案】还原 2NO + O2= 2 NO2 3NO2 + H2O = 2HNO3 + NO CaO、Ca(OH)2、CaCO3NH4HCO3ΔNH3↑+CO2↑+ H2O NH4++ OH-= NH3↑+ H2O SO3 H2SO3 H2SO4 +4【解析】【分析】本题主要考察含N物质的化学性质,运用所学知识答题即可。
【详解】(1)①N2→NH3,N的化合价由0变为了-3,则N2作氧化剂,发生还原反应;②NO→NO2的化学方程式为:2NO+O2=2NO2;NO2→HNO3的化学方程式为:3NO2+H2O=2HNO3+NO;HNO3M−−→Ca(NO3)2,M可以是CaO、Ca(OH)2、CaCO3;(2)①NH4HCO3需阴凉处保存,是因为该物质对热不稳定,受热易分解,相关的化学方程式为:NH4HCO3ΔNH3↑+CO2↑+H2O;②该离子方程式为:NH 4++OH -=NH 3↑+H 2O ;(3)①根据图可知,Y 为H 2SO 4;在自然环境中,SO 2变为H 2SO 4的途径有两种:2H O [O]2324SO SO H SO −−→−−−→、22H O O 22324SO H SO H SO −−−→−−→,故X 为SO 3或H 2SO 3;②尿素CO(NH 2)2缓慢与H 2O 发生非氧化还原反应释放出NH 3,说明尿素中N 呈-3价,由于O 呈-2价,H 呈+1价,故可算得C 呈+4价。
完整版高一化学必修二提高题专题复习氮及其化合物 练习题

完整版高一化学必修二提高题专题复习氮及其化合物练习题一、选择题NH+,你认为下列试纸和试剂可用到的是1.为了检验某固体物质中是否含有4①蒸馏水②NaOH 溶液③红色石蕊试纸④蓝色石蕊试纸⑤稀硫酸A.①②④B.②③C.①②③D.①③⑤【答案】C【详解】NH+时,为便于反应,通常将固体先溶于水,然后加入强碱溶液、加检验固体物质中的4热,逸出的NH3用湿润的红色石蕊试纸检验,所以应选择①②③,故选C。
2.四支试管中分别充满NO、SO2、NO2、Cl2中的一种,把它们分别倒置于盛有水的水槽中,放置一段时间后的现象如图所示。
其中原试管充满NO2的是A.B.C.D.【答案】B【详解】NO不溶于水,对应D图像,SO2在水中的溶解度为1体积水溶解40体积SO2,对应图像A,根据化学方程式3NO2+H2O=2HNO3+NO,剩余气体是反应前的1/3,对于图像B,Cl2+H2O =HCl+HClO,HClO2HCl+O2↑,对应图像C,所以其中原试管充满NO2的是B,答案选B。
3.对于硫酸和硝酸的比较中,下列叙述不正确的是()A.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装B.稀硫酸和稀硝酸都具有氧化性C.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性D.硫酸和硝酸都是重要的化工原料【答案】C【详解】A. 铝、铁与冷的浓硫酸和浓硝酸发生的钝化,因此冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装,故A正确;B. 稀硫酸和稀硝酸都具有氧化性,稀硫酸和金属反应生成氢气,表现氧化性,稀硝酸和金属反应生成硝酸盐和一氧化氮表现氧化性,故B正确;C. 浓硫酸和浓硝酸都具有很强的腐蚀性,浓硫酸具有脱水性,浓硝酸不具有,故C错误;D. 化工生产中用硝酸、硫酸生产化肥、农药、炸药、燃料,金属加工前的酸洗等,故D正确。
综上所述,答案为C。
4.取三张蓝色石蕊试纸放在玻璃棒上,然后按顺序分别滴加65%的浓HNO3、98.3%的浓H2SO4和新制氯水,三张试纸最后的颜色为A.红、红、红B.白、黑、白C.红、黑、红D.红、黑、白【答案】B【详解】硝酸具有强氧化性,将试纸中的有色物质氧化成无色,最后试纸呈现白色;浓硫酸具有脱水性,试纸和其中的有色物质都是有机物,浓硫酸夺取其中的H、O,只剩下黑色的碳,最后试纸呈黑色;新制氯水具有漂白性,将试纸漂白,最后试纸呈白色;即三张试纸最后呈现的颜色依次为白、黑、白;答案选B。
新高一化学必修二化学氮及其化合物 试题及答案
新高一化学必修二化学氮及其化合物 试题及答案一、选择题1.四支试管中分别加入少量不同的无色溶液进行如下操作,现象和结论正确的是( )操作现象 结论A 先滴加2BaCl ,再滴加HCl 溶液 生成白色沉淀 原溶液中有24SO -B 先滴加稀盐酸再滴加3AgNO 溶液 生成白色沉淀 原溶液中有Cl - C用洁净铁丝蘸取溶液进行焰色反应 火焰呈黄色溶液中有Na +,不确定有无+K D加稀NaOH 溶液,将湿润红色石蕊试纸置于试管口试纸不变蓝原溶液中无4NH +A .AB .BC .CD .D【答案】C 【详解】A .白色沉淀可能为AgCl ,则原溶液中不一定有SO 42-,故A 错误;B .白色沉淀可能为硫酸银,则原溶液中不一定有Cl -,故B 错误;C .钠的焰色反应为黄色,观察K 的焰色反应需要透过蓝色的钴玻璃,则原溶液中有Na +,不确定有无K +,故C 正确;D .滴加稀NaOH 溶液,可能生成一水合氨,则原溶液中可能含NH 4+,故D 错误; 故答案为C 。
2.除去铝制品表面的铜镀层,宜选用的试剂是( ) A .稀盐酸 B .氯化钠溶液C .水D .浓硝酸【答案】D 【详解】室温下,铜和浓硝酸反应生成硝酸铜而溶解,铝在冷的浓硝酸中钝化而不溶解,因此除去铝制品表面的铜镀层,宜选用的试剂是浓硝酸,故D 正确; 答案选D 。
3.下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( ) A .在空气中敞口久置的浓硫酸,溶液质量增大难挥发性 B .在加热条件下铜与浓硫酸反应强氧化性、酸性 C .蔗糖与浓硫酸反应中有海绵状的炭生成吸水性D .浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色脱水性【答案】B【详解】A.浓硫酸具有吸水性,则在空气中敞口久置的浓硫酸,会吸收空气中的水分而使溶液的质量增大,表现的是浓硫酸的吸水性,故A错误;B.在加热条件下铜与浓硫酸反应生成硫酸铜和二氧化硫和水,硫元素化合价部分变化,体现浓硫酸的强的氧化性和酸性,故B正确;C.蔗糖与浓硫酸反应中有海绵状的炭生成,体现浓硫酸的脱水性,故C错误;D.硫酸与少量胆矾晶体混合,晶体由蓝色变成白色,体现浓硫酸的吸水性,故D错误。
高考化学推断题综合题专题复习【氮及其化合物】专题解析及答案解析
高考化学推断题综合题专题复习【氮及其化合物】专题解析及答案解析一、氮及其化合物练习题(含详细答案解析)1.某课外兴趣小组探究利用废铜屑制取CuSO4溶液,设计了以下几种实验方案。
完成下列填空:(1)方案一:以铜和浓硫酸反应制备硫酸铜溶液。
方案二:将废铜屑在空气中灼烧后再投入稀硫酸中。
和方案一相比,方案二的优点是________________________;方案二的实验中,发现容器底部残留少量紫红色固体,再加入稀硫酸依然不溶解,该固体为________。
(2)方案三的实验流程如图所示。
溶解过程中有气体放出,该气体是________。
随着反应的进行,生成气体速率加快,推测可能的原因是_______________________________________________________________________________ _。
(3)设计实验证明你的推测:______________________________。
方案四的实验流程如图所示。
(4)为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为________;(5)对方案四进行补充完善,设计一个既能防止污染,又能实现物料循环的实验方案(用流程图表示)__________________________________。
【答案】不产生污染空气的SO2气体,制取等量的CuSO4溶液,消耗的硫酸量少Cu O2反应产生的Cu2+对H2O2分解有催化作用取H2O2溶液,向其中滴加CuSO4溶液,观察产生气泡的速率是否加快3∶2【解析】【详解】(1)第一个方案中放出的有毒气体二氧化硫会造成空气污染;第二个方案中铜和氧气加热生成氧化铜,氧化铜和硫酸反应产生硫酸铜和水,因此反应过程中没有污染物,且原料的利用率高。
方案二的实验中,发现容器底部残留少量紫红色固体为铜,不溶于稀硫酸;(2)方案三中H2O2发生还原反应生成O2;随着反应的进行,生成气体速率加快,可能是反应产生的Cu2+对H2O2分解有催化作用;(3)取H2O2溶液,向其中滴加CuSO4溶液,如果产生气泡的速率加快,则证明Cu2+对H2O2分解有催化作用;(4)根据离子方程式:3Cu+2NO+8H+===3Cu2++2NO↑+4H2O,反应消耗2 mol硝酸,生成3 mol硫酸铜,故为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为3∶2;(5)设计实验方案时,为防止NO污染空气,应通入空气氧化NO为NO2,用水吸收后,生成的HNO3再循环利用:。
高一化学必修二氮及其化合物 知识点-+典型题及答案
高一化学必修二氮及其化合物知识点-+典型题及答案一、选择题1.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是()A.洗气瓶中产生的沉淀是碳酸钡B.洗气瓶中产生的沉淀是硫酸钡C.在Z导管出来的气体中没有二氧化碳D.在Z导管口排出无色气体【答案】B【详解】C与浓硫酸共热反应生成CO2、SO2和H2O,产生的气体X中含CO2、SO2;Cu与浓HNO3反应生成Cu(NO3)2、NO2和H2O,气体Y中含NO2;将X、Y同时通入足量BaCl2溶液中,发生的反应有3NO2+H2O=2HNO3+NO、3SO2+2HNO3+2H2O=3H2SO4+2NO、H2SO4+BaCl2=BaSO4↓+2HCl。
A. 根据上述分析,洗气瓶中产生的沉淀是BaSO4,CO2与BaCl2溶液不反应,A项错误;B. 根据上述分析,洗气瓶中产生的沉淀是BaSO4,B项正确;C. CO2不能被BaCl2溶液吸收,从Z导管出来的气体中含CO2,C项错误;D. 反应中有NO生成,在Z导管口NO遇空气中氧气变为红棕色的NO2气体,D项错误;答案选B。
2.X、Y、Z、W 有如图所示的转化关系,则 X、W可能的组合有( )①C、O2②Na、O2③Fe、HNO3④S、O2 ⑤N2、O2 ⑥H2S、O2 ⑦NH3、O2A.四项B.五项C.六项D.七项【答案】A【详解】①氧气不足时,碳燃烧生成一氧化碳,一氧化碳能在氧气中燃烧生成二氧化碳,碳在足量氧气中燃烧生成二氧化碳,①符合;②常温下,钠与氧气反应生成氧化钠,加热时氧化钠可与氧气反应生成过氧化钠,钠在氧气中燃烧生成过氧化钠,②符合;③过量的铁与稀硝酸反应生成硝酸亚铁,硝酸亚铁与稀硝酸反应转化为硝酸铁,铁与足量的稀硝酸反应生成硝酸铁,③符合;④硫在氧气中燃烧生成二氧化硫,在催化剂和高温条件下二氧化硫与氧气反应生成三氧化硫,硫与氧气不能直接反应生成三氧化硫,④不符合;⑤氮气与氧气在放电或高温条件下反应生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,氮气与氧气不能直接生成二氧化氮,⑤不符合;⑥氧气不足时,硫化氢燃烧生成硫,硫在氧气中燃烧生成二氧化硫,硫化氢在足量氧气中燃烧生成二氧化硫,⑥符合;⑦在催化剂和加热条件氨气与氧气反应生成一氧化氮,一氧化氮与氧气化合生成二氧化氮,氨气与氧气不能直接生成二氧化氮,⑦不符合;所以,符合图示转化关系的有:①②③⑥,故答案为:A。
人教版高中化学必修二《第二节氮及其化合物》同步练习及答案解析
《第二节氮及其化合物》同步练习第1课时氮及其氧化物一、单选题(本大题共13小题,每题4分,共52分)1.反应3N()2 + H20 = 2HNO3 + NO中,当有6moie-发生转移时,被氧化与被还原的物质的物质的量之比为()A. 1: 1B. 1: 2C. 2: 1D. 3: 1【答案】C【解析】【分析】本题考查氧化还原反应计算、氧化还原反应概念,难度中等,理解基本概念,关键根据产物中化合价判断氧化剂与还原剂中的NO2的物质的量之比。
【解答】NO2与水反应3NO2 +H20= 2HNO3 + NO,反应中只有氮元素的化合价发生变化,-2 X LI q由+4价升高为+5价,山+4价降低为+2价,如图,得左•所以NO2既是氧化剂也是还原剂,氧化剂被还原,还原剂被氧化,由产物中氮元素的化合价,可知起始氧化剂与还原剂的NO?物质的量之比为1: 2, 所以被氧化的NO?与被还原的NO2的物质的量之比为2: 1,故选C2.将装有60mLN()2、NO混合气的量筒倒立于水槽中,反应后气体体积缩小为40mL,则混合气体中NO2和N0的体积比是()A. 5: 3B. 2: 3C. 1: 1D. 2: 1【答案】C【解析】【分析】本题考查了根据方程式的计算,根据二氧化氮和气体体积减少的体积的关系,利用差量法来分析解答,难度不大。
【解答】60mLNO 2ffl NO 的混合气体通入倒立于水槽中盛满水的试管中发生反应为剩余40mL 气体,反应前后气体体积减少20mL,设 二氧化氮气体的体积为V,20mL3: 2 = V(NO 2): 20mL,\ 3X20mL TV(NO 2) — —--= 30m L,原气体中V(NO) = 60mL - 30mL = 30mL,所以原混合气体中NO 和NO2的体积比为为V(N()2): V(NO) = 30mL : 30mL = 1: lo 故选Co3. 谚语“雷雨发庄稼”不包括下列哪个化学反应()A. N 2 + 02 = 2NOB. N 2 + 3H 2 = 2NH 3C. 2NO+ O 2 = 2NO 2D. 3NO 2 + H 2O = 2HNO 3 + NO T【答案】B【解析】【分析】 本题主要考查了雷雨肥田原理,氮气、一氧化氮、二氧化氮的化学性质,理解反 应原理、正确书写化学方程式是解答的关键,题目难度不大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题02 氮及其化合物专项训练1.下列用途中应用了氮气的稳定性的是:()A.以氮气为原料之一制造硝酸B.合成氨气后,制氮肥C.金属焊接时的保护气D.镁可以和氮气反应【答案】C【详解】A、利用N2制备硝酸,发生的反应为N2+3H22NH3、4NH3+5O24NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO,与N2的稳定性无关,故A不符合题意;B、根据A选项分析,合成氨气,制备氮肥,与N2的稳定性无关,故B不符合题意;C、单质氮的化学性质相对稳定,因此氮气常作金属焊接时的保护气,与氮气的稳定性有关,故C符合题意;D、Mg能与N2反应生成Mg3N2,与N2的稳定性无关,故D不符合题意。
2.下列关于氮及其化合物,说法不正确的是( )A.氮的固定是将N2转化成含氮化合物B.氮元素在自然界中既有游离态又有化合态C.NO和NO2都可稳定存在于空气中D.N2既可作氧化剂又可做还原剂【答案】C【详解】A.氮的固定是将空气中游离态的氮转化为含氮化合物的过程。
如豆类植物共生的根瘤菌。
它们能吸收大气中的氮气分子,将其转变成氨及铵离子,A正确;B.自然界中N有游离态,如N2,也有化合态,如铵盐、硝酸盐等,B正确;C.NO不稳定,易与O2反应生成NO2,C错误;D.N2中N元素处于中间价态,既可以升高又可以降低,N2既可以做氧化剂又可以做还原剂,D正确;故答案选C。
3.下列叙述正确的是()A.液氨用作制冷剂发生的是化学反应B.氨气溶水得到氨水发生的只是物理变化C.分离液态空气制取氮气属于氮的固定D.氮气与氢气化合生成氨气属于人工固氮【答案】D【详解】A. 液氨用作制冷剂,是因为它汽化时会吸收大量的能量,汽化是物理变化,A错误;B. 氨气溶水得到氨水,大部分氨气和水反应生成了一水合氨,发生的既有物理变化又有化学变化,B错误;C. 氮的固定是把空气中的氮气转变成含氮化合物的过程,分离液态空气制取氮气是物理变化,不属于氮的固定,C错误;D.氮的固定有自然固氮和人工固氮,氮气与氢气化合生成氨气属于人工固氮,D正确;答案选D。
4.酸雨被称为“天堂的眼泪”,会造成水土酸性化、建筑物加速腐蚀等危害。
下列说法正确的是( ) A.酸雨不会对动植物产生任何影响B.使用新型能源不会对酸雨的防治产生效果C.酸雨指的是pH小于7的雨水D.NO2和SO2的过度排放是形成酸雨的主要原因【答案】D【详解】A.酸雨中含有硫酸和硝酸,因此酸雨会造成水土酸性化、建筑物加速腐蚀、污染水源,危害人体健康,使农作物和植物的生长遭到破坏,故A错误;B.使用新型能源,可以减少污染物的排放,有利于酸雨的防治,故B错误;C.pH小于5.6的雨水为酸雨,故C错误;D.人类超量排放的NO2和SO2,是形成酸雨的主要原因,故D正确;故选D。
5.目前,我国是世界三大酸雨区之一,治理酸雨对我国的可持续发展有着重大意义,下列有关酸雨的说法错误..的是A.开发能替代化石能源的新能源,如氢能、太阳能等B.利用石灰石对含硫燃料进行脱硫处理C.空气质量指数(AQI)监测SO2、NO2、PM2.5、PM10、O3、CO2检测项目D.利用熟石灰处理酸化土壤【答案】C【详解】A.化石燃料的燃烧产物往往含有氮、硫等氧化物,其产物是造成酸雨的主要原因之一,利用氢能、太阳能等清洁能源可以减少污染物的排放,故A正确;B.高温条件下石灰石分解为氧化钙,氧化钙可以与硫的氧化物结合,故B正确;C.空气质量指数(AQI)监测不包括二氧化碳,二氧化碳不是空气污染物,应该为一氧化碳,二氧化,故C 错误;D.熟石灰的主要成分为氢氧化钙,显碱性,能与酸性土壤发生中和反应,从而改善土壤,故D正确;故答案为C。
6.下列说法正确的是( )A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在B.NH3汽化时吸收大量的热,因此,氨常用作制冷剂C.CO2、NO2或SO2都会导致酸雨的形成D.活性炭、SO2、Na2O2都能使品红溶液褪色,原理相同【答案】B【详解】A.NO能够和氧气反应,不能在空气中稳定存在,故A错误;B.液氨变为氨气需要吸收周围环境的热量,导致周围环境的温度迅速降低,因此氨常用作制冷剂,故B正确;C.二氧化碳不会导致酸雨的形成,二氧化硫和二氧化氮都会导致酸雨的形成,故C错误;D.活性炭是吸附品红溶液导致褪色;二氧化硫与品红化合生成无色物质,体现了二氧化硫的漂白性;过氧化钠具有强氧化性,把品红氧化褪色,虽然都能使品红褪色,但是原理不相同,故D错误;故选B。
7.下面是实验室制取氨气的装置和选用的试剂,其中正确的是A.B.C.D.【答案】D【详解】A.实验室制取氨气用氯化铵和氢氧化钙混合固体加热,产生的氨气用碱石灰干燥,氯化铵受热分解为氨气和氯化氢,遇冷又结合成氯化铵,得不到氨气,不能直接加热氯化铵分解制氨气,故A错误;B.氨气能被浓硫酸吸收,应该用碱石灰干燥氨气,故B错误;C.固体+固体加热制气体时,试管口应向略向下倾斜,否则会有炸裂试管的可能,故C错误;D.氨水易挥发,可采用加热浓氨水的方法制取氨气,用碱石灰干燥氨气,故D正确;故选:D。
8.下列关于浓硝酸的说法不正确的是( ) A .常温下铜在浓硝酸中发生钝化 B .光照易分解C .能与碳反应说明其具有强氧化性D .露置于空气中溶液浓度降低 【答案】A 【详解】A .常温下铝、铁在浓硝酸中发生钝化,铜不能,A 错误;B .浓硝酸见光易分解生成二氧化氮、氧气和水,B 正确;C .浓硝酸能与碳反应生成二氧化碳、二氧化氮和水,这说明浓硝酸具有强氧化性,C 正确;D .浓硝酸易挥发,露置于空气中溶液浓度会降低,D 正确; 答案选A 。
9.下列关于硝酸正确的是( )A .稀硝酸能与Fe 发生反应,浓硝酸不能B .浓硝酸和稀硝酸都是强氧化剂C .稀硝酸是弱酸,浓硝酸是强酸D .稀硝酸与Cu 反应,生成NO ,而浓硝酸与Cu 反应只生成NO 2 【答案】B 【详解】A .稀硝酸、浓硝酸都能与Fe 反应,A 错误;B .浓硝酸、稀硝酸都有很强的氧化性,都是强氧化剂,B 正确;C .浓硝酸、稀硝酸都是强酸,C 错误;D .浓硝酸与铜反应,若铜过量,则随着反应的进行硝酸的浓度减小,还会生成NO ,D 错误; 答案选B 。
10.碳酸氢铵是中国主要生产的氮肥品种之一,它属于铵态氮肥(铵盐)。
下列有关铵盐的叙述说法正确的是( )A .所有铵盐受热均可以分解,产物均有NH 3B .所有铵盐中氮元素均呈-3价C .NH 4Cl 溶液中加入NaOH 溶液共热时,反应的离子方程式为4NH+OH -ΔNH 3↑+H 2OD .NH 4Cl 和NaCl 的固体混合物可用升华法分离 【答案】C 【详解】A .铵盐不稳定,受热会分解,但受热分解不一定都产生NH 3。
如氯化铵、碳酸氢铵等分解可生成NH 3;而NH 4NO 3受热分解可能产生N 2O 、H 2O ,而不产生NH 3,A 错误;B .铵盐中4NH +的N 元素化合价为-3价,若不是4NH +的N ,则N 元素就不是-3价,如NH 4NO 3中3NO -所含氮元素显+5价,B 错误;C .铵盐与碱共热时,反应产生的NH 3·H 2O 会发生分解反应产生NH 3,该反应的离子方程式为:4NH ++OH -ΔNH 3↑+H 2O ,C 正确;D .NaCl 稳定,加热不分解,NH 4Cl 不稳定,加热分解产生NH 3、HCl 气体逸出,因此可通过加热二者混合物进行分离。
但NH 4Cl 受热分解产生NH 3、HCl ,遇冷二者重新化合形成NH 4Cl ,该过程中有新物质生成,因此发生的是化学变化,不是升华,D 错误; 故合理选项是C 。
11.依据图中氮元素及其化合物的转化关系,判断下列说法不正确的是( )A .X 是N 2O 5B .工业上以NH 3、空气、水为原料生产硝酸C .可用排空气法收集NO 气体D .由NH 3→N 2,从原理上看,NH 3可与NO 2反应实现 【答案】C 【详解】A.X 中氮元素为+5价,是氧化物,则化学式是N 2O 5,选项A 正确;B.氨气催化氧化生成一氧化氮和水,一氧化氮和氧气反应生成二氧化氮,二氧化氮溶于水生成硝酸,故工业上以NH 3、空气、水为原料生产硝酸,选项B 正确;C.NO 能与空气中的氧气发生反应生成NO 2,不可用排空气法收集NO 气体,选项C 错误;D. NH 3与NO 2反应生成氮气,发生氧化还原反应8NH 3+6NO 2=7N 2+12H 2O ,选项D 正确; 答案选C 。
12.某化学反应在催化剂条件下的转化过程的微观示意图如图所示。
下列有关说法不正确的是A.该反应中,氧化性:NO>CO2B.该反应可表示为2NO+2CO催化剂N2+2CO2C.该反应中,被氧化与被还原的元素的质量之比为7:6D.每生成标准状况下2.24LN2,转移的电子数为0.4N A【答案】C【分析】根据图像可知,该反应为2NO+2CO催化剂N2+2CO2。
【详解】A.该反应中,NO为氧化剂,CO2为氧化产物,则氧化性:NO>CO2,A说法正确;B.分析可知,该反应可表示为2NO+2CO催化剂N2+2CO2,B说法正确;C.该反应中,被氧化的元素是碳元素,被还原的元素是氮元素,则被氧化与被还原的元素的质量之比为6:7,C说法错误;D.每生成标准状况下2.24LN2,转移的电子0.4mol,即电子数为0.4N A,D说法正确;答案为C。
13.我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图:以下说法中不正确...的是A.向饱和食盐水中先通入足量的NH3,再通入足量的CO2B.沉淀池中得到的沉淀为碳酸钠C .使原料氯化钠的利用率从70%提高到90%以上,主要是设计了循环1D .循环2中的气体X 为CO 2 【答案】B 【分析】焦炭和水在高温下反应生成CO 2和H 2,H 2和从空气中分离出来的N 2合成氨,氨和CO 2通入盛有饱和食盐水的沉淀池中生成溶解度较小的NaHCO 3沉淀和NH 4Cl ,分离出NaHCO 3,煅烧得到纯碱,生成的CO 2可以循环使用;母液中通入氨可以分离出NH 4Cl ,剩余的含NaCl 的溶液可以送回沉淀池中循环使用。
【详解】A .CO 2在水中的溶解度比较小,NH 3在水中的溶解度很大,所以先向饱和食盐水中通入氨,使溶液呈碱性,再向碱性溶液中通入CO 2,可以得到更多的3HCO -,从而生成更多的溶解度较小的NaHCO 3,故A 正确; B .由以上分析可知,沉淀池中得到的沉淀为NaHCO 3,故B 不正确;C .母液分离出NH 4Cl 后,剩下的主要是NaCl ,循环Ⅰ将分离出NH 4Cl 的溶液送回沉淀池中,提高了NaCl 的利用率,故C 正确;D .煅烧炉中发生反应:2NaHCO 3ΔNa 2CO 3+H 2O+CO 2↑,生成的CO 2可以再进入沉淀池中循环使用,故D正确; 故选B 。
