高三常见气体制备吸收装置
高三化学一轮复习——常见气体的制备

B.ADG D.BCF
有机物制备
气体连接
利用如图所示装置进行下列实验,能得到相应实验结论的是
选项 ①
②
③
A 浓硫酸 Na2SO3 KMnO4溶液退色
实验结论 SO2有漂白性
B 浓盐酸 KMnO4 FeBr2溶液变为黄色 氧化性:Cl2>Br2
√C
稀硫酸
碳酸钠
CaCl2溶液无明显 变化
CO2不与CaCl2反应
D 浓硫酸 蔗糖
溴水退色
浓硫酸具有脱水 性、吸水性
强海行纳者 百有川志有。容乃大壁立千仞无欲则刚 心一志个要 人坚如,果意胸趣无要大乐志。,既使再有壮丽的举动也称不上是伟人。 治死天犹下 未者肯必输先心立去其,志贫。亦其能奈我何! 虽与长其不 当满一七辈尺子,乌而鸦心,雄莫万如丈当。一次鹰。 心燕志雀要 安坚知,鸿意鹄趣之要志乐哉。 并虽非长神 不仙满才七能尺烧,陶而器心,雄有万志丈的。人总可以学得精手艺。 志有之志所 始趋知,蓬无莱远近勿,届无,为穷总山觉复咫海尺不远能。限也;志之所向,无坚不摧。 顶海天纳立 百地川奇有男容子乃,大要壁把立乾千坤仞扭无转欲来则。刚 雄胸心无志 大四志海,,枉万活里一望世风。尘。 不卒怕子路 过远河,就意怕在志吃短帅。
试剂乙 CaCO3 Na2SO3 MnO2 KMnO4
试剂丙
Na2SiO3溶液 BaCl2溶液 酸性 KI-淀粉溶液
Na2S溶液
丙中的现象 有白色沉淀生成 有白色沉淀生成 溶液变为蓝色 有淡黄色沉淀生成
微诊断 判断正误,正确的画“√”,错误的画“×”。
1.因为氢气无毒,制备氢气时多余的尾气可以直接排放到空气中。( × )
找杂质?
实验原理:反应方程式
如何测量气 体体积?
高中化学:常见气体的实验室制备

高中化学:常见气体的实验室制备1.掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)。
(高频)2.能绘制和识别典型的实验仪器装置图。
(高频)气体的实验室制法1.O2的实验室制法2.CO2的实验室制法3.H2的实验室制法4.NH3的实验室制法5.Cl2的实验室制法6.SO2的实验室制法气体的收集方法收集方法排水法向上排空气法向下排空气法收集原理收集的气体不与水反应且难溶于水收集的气体密度比空气大,与空气密度相差较大,且不与空气中的成分发生反应收集的气体密度比空气小,与空气密度相差较大,且不与空气中的成分发生反应收集装置适用的气体H2、O2、NO、CH4Cl2、CO2、NO2、SO2H2、NH31.易误诊断(正确的打“√”,错误的打“×”)。
(1)Cl2收集可用排饱和NaCl溶液方法不能用排水法()(2)CO2、H2的制备可以选用相同的发生装置()(3)Cl2、SO2、NH3均可用NaOH溶液吸收尾气()(4)除去CO2中的HCl可以将混合气通入饱和的Na2CO3溶液中()(5)Cl2、SO2、CO2、NH3均可用浓H2SO4作干燥剂()(6)Cl2、SO2的验满均可用湿润的品红试纸()【答案】(1)√(2)√(3)×(4)×(5)×(6)√2.在实验室中制取H2、CO2、NH3、NO、NO2、SO2、Cl2、O2是否均可以用如图所示装置来制取?答:_____________________________________________________________________ ___。
【答案】可以。
因为制取上述八种气体均可用固体与液体,且不需要加热的反应来制取3.据下图所示的实验装置回答问题:(1)实验室用高锰酸钾制取比较干燥的氧气应选用的发生装置是________,收集装置为________。
(2)实验室用双氧水制取并收集较纯的氧气时应选用的发生装置是________,收集装置为________。
常见气体的实验室制法

择 吸 收 剂
气 体 的 毒 性 选
装置连接顺序
2、操作顺序一般包括: 操作顺序一般包括: 仪器 连接 查气 密性 装 药 品 防倒吸 等措施 仪器拆 卸等
①装配仪器时:从下向上;从左往右 装配仪器时:从下向上; ②在连接导管时: 在连接导管时: 对制气装置、洗气瓶的导气管应“长进短出” a 对制气装置、洗气瓶的导气管应“长进短出”; 干燥管应大口进气 大口进气, b 干燥管应大口进气,小口出气 ; 量气装置的导管应“短进长出” c 量气装置的导管应“短进长出”; 有易挥发液体反应或生成时,要设计冷凝回流装置。 冷凝回流装置 d 有易挥发液体反应或生成时,要设计冷凝回流装置。
固体----圆底烧瓶 固体 圆底烧瓶 石棉网
MnO + 4HCl ∆ MnCl + Cl2 ↑ +2H2O 2 2 2KMnO +16HCl = 2MnCl + 2KCl + 5Cl2 ↑ +8H2O 4 2
∆ NaCl + H 2 SO4(浓) = Na2 HSO4 + HCl ↑
Na2SO + 2H2SO (浓) = 2NaHSO+ SO ↑ +H2O 3 4 2 4
△
氨气
(2)氧气的制备 传统方法:固+固→气( KClO3、MnO2 共热) 变析:固+液→气(Na2O2+H2O→O2 或 H 2O 2
MnO2
O 2)
(3)氯气的制备 传统方法:固+液→气( 浓HCl、MnO2 共热) 变析:固+液→气(不加热) (2KMnO4+16HCl=2KCl+2MnCl2+5Cl2 ↑ +8H2O)
2025届高三化学一轮复习+之常见气体和金属的制备+

2025届高考复习之常见气体和金属的制备-2019人教版一、气体制备1.Cl2制备原理:实验室加热:4HCl(浓)+MnO2MnCl2+2H2O+Cl2↑实验室不加热:16HCl(浓)+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O注:实验室还可通过浓盐酸与KClO3的反应、浓盐酸与K2Cr2O7的反应、PbO2和浓盐酸的反应制备Cl2。
工业制Cl2:2NaCl+2H2O 2NaOH+Cl2↑+H2↑考点:①涉及HCl的反应往往要除杂。
②两处的“浓”含义不一样,MnO2与稀HCl不反应,MnO4-与Cl-任何情况都反应,用浓溶液是为了加快V。
典型例题1.某学习小组利用下图装置制备84消毒液。
下列说法正确的是A .湿润的蓝色石蕊试纸褪色,说明2Cl 有漂白性B .Ⅱ中溶液出现浑浊,说明2Cl 降低了NaCl 的溶解度C .若无装置Ⅱ,制取的84消毒液中NaClO 的纯度下降D .该装置条件下,若用2MnO 代替4KMnO 也可制取84消毒液 2.在实验室采取如图装置和下列各组试剂,能使纸蝴蝶只变色不褪色的是 选项 液体A+C 固体BA稀硝酸+紫色石蕊溶液CuB 浓盐酸+紫色石蕊溶液4KMnOC 稀盐酸+品红溶液 FeSD 醋酸+酚酞溶液3CaCOA .AB .BC .CD .D2.SO2制备原理:实验室加热:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O实验室不加热: Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O考点:①SO2有四性:漂白性,还原性,氧化性,酸性。
检验酸性:把气体通到氢氧化钠的酚酞溶液中,会褪色;检验漂白性:把气体通到品红溶液中,会褪色,加热会恢复红色,这是可逆型漂白。
检验还原性:把气体通到酸性高锰酸钾溶液或溴水中,均会褪色。
(通到液溴中不反应)检验氧化性:通到硫化氢的水溶液中会看到黄色浑浊。
②SO2能漂白品红和有色布条的漂白性可逆,加热可恢复颜色。
(完整版)高中化学气体制备大全
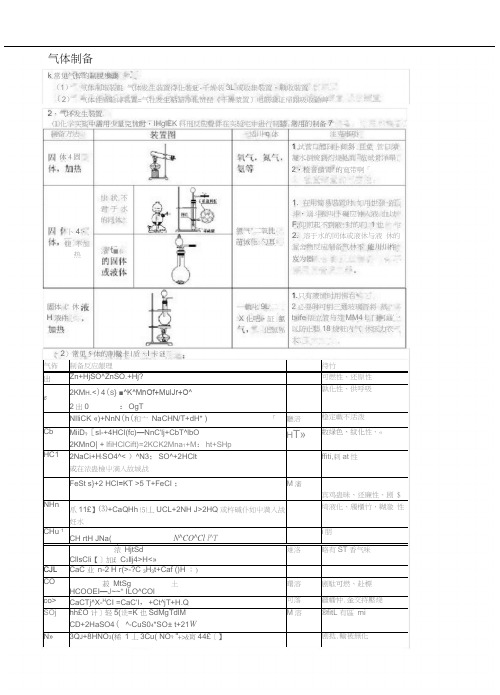
制备方法 适川q 休注克事项 氯气"二氧比 苗诫化:勺耳快状不 君于水 的同体灌t ■水固体( 休H 液件卜4•腹 不加热休4固1.只有液怵时用怫右*2必耍时可用三通玻璃晋将 蒸t»ife 版立管与芬MM4 I. 门柯通’以防止藝18烧粧内气 休压力衣大.軌叱9L 二 X 化吧・証 氯化氢% 1试营口醴向卜倾斜.且免 管口障凝水倒流到灼烧处而 览试骨洋舉.2•检音饋胃'的寬带啊「1. 在用简易裝置时.如用世颈 蹈斗•溺斗颈叫卜礙应伸入液 血以F,仰则起不到液:封的门 1也2. 溶于水的同体或液休与液 休的渥舍物反应制备气林不 能川川杵岌为器气体制备k 常见气悴的制脱歩骤(1) 气体制取装氈 气体发生装置待化装迓-千燥装3L 或收集裝置・戰收裝置(2)气体性质验诽裳置=气牡发生粘笳净化赞琵《干燥漿置)电筋验证帰跟吸收爺艸2、气坏发生装置⑴化学实鲨中需用少量完怵时・IHglEK 料刑反应聲件在实验宅中进行制牆.常用的制备7气佈制备反应龈理待竹出Zn+HjSO^ZnSO.+Hj?可燃性、还原性62KM H .<)4(S } ■^K^MnOf+MulJr+O^2出0:OgT孰化性、供呼吸NIliCK «)+NnN (h (和亠 NaCHN/T+dH* )「 廳涪稳定載不活泼 CbMiiD ?[sl-+4HCI(fc)—NnC'lj+CbT^lbO2KMnO| + lfiHClCift)=2KCK2Mna 1+M :ht+SHpH T»数绿色、紋化性、«HC1 2NaCi+H :SO4^< )^N3;SO^+2HClt或在浓蛊檢屮滴入故城战ffiti,剌at 性FeSt s}+2 HCI =KT >5 T+FeCI ;M 瀋宾鸡蛊昧、还廉性、剧 $NHn 爪11£】⑶+CaQHh ⑸丄UCL+2NH J>2HQ 或杵碱仆如屮満入战妊水埼液化、斶櫃竹,糊激 性CHu 1CH rtH JNa( N^CO^Cl l^Ti 朋1浓 HjtSdCllsCli 【]加£ C 3llj4>H<»难洛略有ST 香气味CJL CaC 业 n-2 H r(>-?C 3H 3t+Caf ()H ;)CO 菽 MtSg土HCOOEI —J ~~* ILO^COl曙溶 剧駄可燃、赴標 co> CaCTj^X-H CI =CaC'l ,+Ct^jT+H.Q 可落疆幡忡.金交持壓烧SOj hh£O 计]轻5(诜=K 也SdMgTdlM CD+2HaSO4( ^-CuS04*SO± t+21W M 溶®fitL 有區 miN»3Q J +8HNO 3(稀 1 丄3Cu( NO ? ”+>&肓44£〔】剧抵.輸被無化,〉常见5体的制儆卡|质、卡谜•验室制备的气体常常幣有恢券和水汽.仃时需要祎化和I•燥.酸雾“川水或物质的水溶液除去・k ;:・计I质选用浓硫酸.无水氯化纵碱石灰等吸收水汽。
高中化学必修二 学习笔记 第5章 第2节 第3课时 NH3及常见气体的制备方法

第3课时NH3及常见气体的制备方法[核心素养发展目标] 1.掌握实验室制取NH3的方法。
2.掌握实验室制取常见气体的原理、装置、收集、净化方法及制备方法的比较。
一、氨的实验室制法1.氨的实验室制法制备原理实验装置收集NH3极易溶于水,可以用________________________收集验满把湿润的红色石蕊试纸置于试管口,试纸变____________;或将蘸有浓盐酸的玻璃棒置于试管口,有______________产生思考(1)此装置存在的弊端是什么?如何进行改进?________________________________________________________________________ (2)收集NH3时,试管口处为什么加一团棉花?________________________________________________________________________ 2.氨的简易制法方法及装置原理及化学方程式氨水具有________和______,受热易分解。
化学方程式为____________________________NaOH固体具有吸水性,溶于水放出大量的热,促使氨水分解。
CaO与水反应,使溶剂(水)减少;反应放热,促使氨水分解。
化学方程式为____________________________________1.判断正误(1)实验室中可以利用加热NH4Cl分解的方法制取NH3()(2)由于氨极易溶于水,所以不能用排水法收集氨,只能用向下排空气法收集()(3)氨不能用浓硫酸进行干燥,但可以用无水CaCl2干燥()(4)为加快产生NH3的速率,实验室中可以用NaOH和NH4Cl反应制NH3()(5)由于氨极易溶于水,所以多余的氨可以用导管直接插入水中进行吸收() 2.(2023·江苏盐城高一联考)下列装置用于实验室中制取干燥氨气的实验,其中能达到实验目的的是()A.用装置甲制备氨气B.用装置乙除去氨气中的少量水C.用装置丙收集氨气D.用装置丁吸收多余的氨气(1)制氨气所用的铵盐不能用NH4NO3、NH4HCO3、(NH4)2CO3等代替,NH4NO3加热时爆炸,而NH4HCO3、(NH4)2CO3极易分解产生CO2气体使制得的NH3不纯。
气体的制备和实验装置的连接

化学实验小型化训练——常见气体的制备及实验装置的连接一、常见气体的实验室制法所用试剂、反应原理:气体所用试剂反应原理H2O2Cl2NH3C2H4C2H2CO2SO2NONO2二、常见气体的实验室制取、净化、收集及尾气处理装置:1、制备装置的选择:根据反应物的状态、反应条件进行选择固+固气固+液→气固(或液)+液气制、制、、制、、、制、、。
【思考】上图制Cl2右侧替代装置中的玻璃管起到什么作用?2、气体的除杂和干燥:干燥装置一般放在其它除杂装置之后洗气瓶(盛装液态试剂)干燥管(盛装固态试剂)3、防倒吸装置吸收易溶于水的气体时防倒吸气体连接装置中的防倒吸装置(安全瓶)【思考】以下装置能防倒吸的是:()A B C D4、气体收集装置:根据气体密度、溶解性及能否与空气中的某种成分反应等方面进行选择。
排水(或其它液体)法向上排空气法向下排空气法可收集气体有:可收集气体有:可收集气体有:5、量气装置排水(或其它液体)法测体积测吸收装置的增重量洗气瓶或干燥管等装置读取气体的体积之前必须①使试管和量筒(或量气管)内的气体都冷却至室温;②调整量筒(或量气管)内外液面高度使之相同【思考】在盛水的广口瓶和量筒之间的导管中应该先充满水,为什么?6、尾气处理装置:需要处理的气体为有毒、有害及可燃性气体在水中溶解度较小的气体易溶于水的气体可燃性气体贮气瓶处理气体:三、实验方案的设计和仪器的连接:综合实验制备题的一般思考顺序:反应原理→反应物的选择→除杂试剂的选择→仪器的选择→完整实验的组合。
1、连接仪器:一般顺序为气体发生装置→除杂装置→干燥装置(是否必需)→性质检验装置→气体收集装置(如有必要)→尾气处理装置,具体实验会有不同的步骤组合。
【注意】导管在装置连接中的使用方法2、检查装置的气密性:①先要审清题目是检测全套装置,还是其中部分装置气密性;②操作时一定要先将被检测装置变成一个密封体系(如关闭开关、导管出口插入水中等),然后改变气压(如加热、注水等),观察现象;③回答问题时应先叙述操作方法、步骤,再说观察到的现象,最后由现象得出结论。
2014高三化学考试说明全解全析5化学实验基础(7)

(7)了解常见气体和一些简单化合物的制备原理和实验室制备方法。
例1.下图Ⅰ、Ⅱ、Ⅲ是常见的气体发生装置;Ⅳ、Ⅴ、Ⅵ是气体收集装置,根据要求回求答下列问题(装置图填序号):(1)气体发生装置的选择:若用CaCO 3与盐酸反应制CO 2,则可选择 ; 若用NH 4Cl 和Ca(OH)2反应制NH 3,则可选择 ; 若用MnO 2与浓盐酸反应制取氯气,应选用装置 ;用离子方程式表示制取氯气的反应原理是 。
(2)收集装置的选择:若选用V 为氯气收集装置,则氯气应从 口通入。
用化学方法检验氯气收集满的方法是 。
(3)气体的吸收:若经试验发现,现1体积的水已吸收336体积的HCl ,且得到的溶液的密度为1.08g·cm -3,则所得溶液中溶质的物质的量浓度为 mol·L -1。
【解析】2实验装置的选取和安装③加入药品;④排尽装置内的空气;⑤验纯;⑥反应;⑦拆除装置。
a b ca导管作用:平衡气压b要求:不溶性块状固体c温度计位置:水银球在反应液内(3)气体净化与干燥的先后顺序①若采用溶液除杂,实验室制取下列气体:①H2,②O2,③Cl2,④CO,⑤SO2,⑥HCl,⑦NH3,⑧NO,⑨NO2。
用如图所示的装置,位置不可变动:(1)若烧瓶是干燥的,则由A口进气可收集的气体有。
(2)若烧瓶是干燥的,则由B口进气可收集的气体有。
(3)若烧瓶充满水,应从B 口进气收集气体,可收集的气体有。
(4)若烧瓶内装入浓硫酸作干燥剂,可用此装置来干燥的气体有,此时气体应从口进口出。
(5)请选用最合适的试剂装入洗气瓶,用此装置除杂(括号内的气体为杂质)。
CO2(HCl) 饱和NaHCO3溶液;CO2(SO2) 。
SO2(HCl) 饱和NaHSO3溶液;H2S (HCl) 。
Cl2(HCl) ;H2S (H2O) P2O5固体。
【关注高考】1.(2008·江苏·6)下列装置或操作能达到实验目的的是()2.(2010·江苏·7)下列有关实验原理或操作正确的是()A.选择合适的试剂,用图1所示装置可分别制取少量的CO2、NO和O2B.制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸.C.洗涤沉淀时(见图2)自漏斗中加适量水,搅拌并滤干D.用广泛pH试纸测得0.10 mol·L-1NH4Cl溶液的pH =5.23.(2011·江苏·7)下列有关实验原理或实验操作正确的是()A.用水润湿的pH试纸测量某溶液的pHB.用量筒量取20 mL 0.5000 mol·L-1H2SO4溶液于烧杯中,加水80 mL,配制成0.1000mol·L-1H2SO4溶液C.实验室用图2所示装置制取少量氨气D.实验室用图3所示装置除去Cl2中的少量HCl.4.(2012·江苏·6)用下列实验装置进行相应实验,能达到实验目的的是()图1 图2 图3 图4 A.用图1所示装置除去Cl2中含有的少量HClB.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体C.用图3所示装置制取少量纯净的CO2气体D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层.5.(2014·江苏·5)下列装置应用于实验室制取氯气并回收氯化锰的实验,能达到实验目的的是()A.用装置甲制取氯气B.用装置乙除去氯气中的少量氯化氢C.用装置丙分离二氧化锰和氯化锰溶液. D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O6.(2013·江苏·16)(4)煅烧过程存在以下反应:2MgSO 4+C 800℃ 2MgO+2SO 2↑+CO 2↑ MgSO 4+C 800℃ MgO+SO 2↑+CO ↑ MgSO 4+3C 800℃ MgO+S ↑+3CO ↑利用下图装置对煅烧产生的气体进行分步吸收或收集。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大家好
10
[例5]铜与浓硝酸反应和铜与稀硝酸反应,产物
不同,实验现象也不同。
⑴某课外活动小组为了证明并观察到铜与稀
硝酸反应的产物为NO,设计了如左图所示
的实验装置。请你根据他们的思路,选择下
列药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、锌粒、碳酸钙固体
步骤:①检查装置的气密性;
② 向试管中加入一定量碳酸钙固体
(4)若烧杯是干燥的,不能用此装置来收集的 气体是___。
【答】(1) ②④⑦⑧ (2)①③⑥,A
(3)①②③④⑥⑧,B (大家4好)⑥
9
[例4]:
某集气瓶中充满了HI气体,试设计一个装置表 示:将这种气体排出烧瓶,并粗略证明它确实是HI 气体,写出有关反应的离子方程式。
【答】:往装有气体的瓶中注入浓磷酸,使气体排出, 用盛有适量水的烧杯吸收排出的气体(玻璃管下端接一个 倒置漏斗),一段时间以后,取少量烧杯中的溶液,测得 PH值小于7;加入用硝酸酸化的硝酸银溶液,如发现有黄 色沉淀生成,则可说明原气体是HI气体。
4、尾气处理装置
▪总原则 ▪(1)有毒、污染环境的气体不能直接排放。 ▪(2)尾气吸收要选择合适的吸收剂和吸收装置。
•直接吸收:Cl2、H2S、NO2 防倒吸:HCl、NH3、SO2 •常用吸收剂:NaOH溶液,硫酸铜溶液 ▪(3)可燃性气体且难用吸收剂吸收:燃烧处理或袋装。
大家好
1
4、尾气处理装置
(1)若烧瓶是干燥的,则由A口进气,在B口可收集的气体 有(用数字表示,下同)________________.
(2)若烧瓶充满水,可收集的气体有________,这时气体 由________口进入。
(3)若在烧瓶内装入浓硫酸进行干燥气体,则 可用此装置的气体有____________,这时气体 由________口进入。
;
向试管中到入过量的稀硝酸,并迅速盖上带铜丝
③ 和导管的橡皮塞
;
④ 待反应完全后,将右边导管插入试管内接近液面 ;
⑤ 将铜丝插入到溶液中
;
⑥用注射器向试管内推入氧气(或空气)
大家好
11
谢谢
大家好
12
浓硫酸、稀硫酸、浓硝酸、稀硝酸、浓盐酸、稀盐酸、浓 氨水、稀氨水、蒸馏水、饱和氢硫酸溶液、饱和石灰水
请回答:A、B、C、D、E各是什么物质?
【答】:A是氯化氢气体,B是浓盐酸,C、D、E均是浓硫酸
大家好
8
[例3]:
利用下图所示装收集以下8种气体(图中烧瓶位置不得移 动):①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
关随停的CO2气体发生装置。应选用的仪器是(填入仪器
的编号)
。
(2)若用上述装置制取CO2气体,而实验室只有稀硫酸、 浓硝酸、水、块状纯碱、块状大理石,比较合理的方案应
选用的药品是
。
大家好
7
[例2]:
为制取纯净的气体A可用下图所示的装置,生成A的速度 可通过滴液的速度控制,图中B、C、D均为液体,且为下列 试剂中某一种:
5、气体性质实验装置
▪ 5.1 装置分类
▪ (1)常温反应装置
▪ (2)加热反应装置
▪ (3)冷却反应装置
▪ 5.2 判断原则 大家好
5
6、排水量气装置
标准 装置
注意事项: 左端水位与右 端水位相平
变化 装置
注意事项: 量筒内的水位与 水槽中水位相平 .
大家好
6
[例1]:
(1)在没有现成的CO2气体发生器的情况下,请你选用 下图中的部分仪器,装配成一个简易的、能随开随用、随
(1)水溶解法 如:HCl、NH3等。 (2)碱液吸收法
如:Cl2、H2S、CO2、 SO2、NO2、NO等。
(3)燃烧或袋装处理法
如 : CH4 、 C2H4 、 C2H2 、 H2、CO等。
大家好
2
4、尾气处理装置
(4)防倒吸吸收
标准装置
安全瓶装置
大家好
3
②防倒吸吸收
图 5-27-1
大家好
4
