二苯甲醇的制备的一些问题

实验三 二苯甲醇的制备
【实验目的】
1.掌握由NaBH4还原二苯甲酮制备二苯甲醇的方法,了解酮的还原反应机理、还原剂的种类及特点。
2.进一步熟悉用TLC 判定反应终点的方法。 【实验的准备】
仪 器:圆底烧瓶(100ml 1个);水银温度计(150℃ 1支);回流管(1个);吸滤瓶(1个);布氏漏斗(1个);水泵(公用)。
药 品:二苯甲酮 1.0 g (5.49mmol); NaBH4 0.4 g (10.57 mmol); TLC 板,环己烷,乙酸乙酯,10%HCl 。
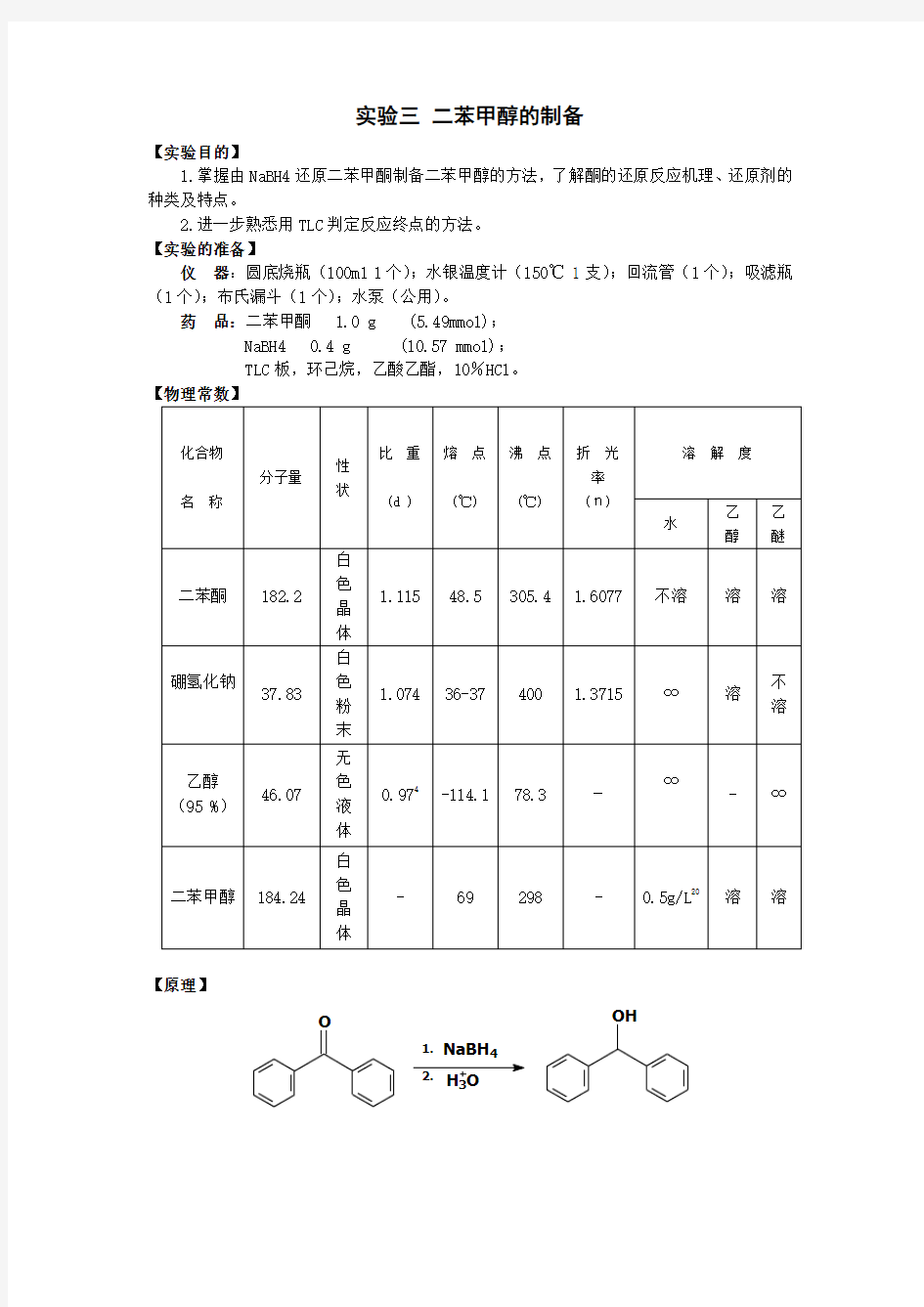
【原理】
O
1.NaBH 4OH
Na BH 4
+Ph Ph
O
Na B(O CH Ph
Ph )4
Na B(O CH Ph
Ph
)4+H 2O 3+H
Ph
Ph
OH +B(OH)3
4
【操作】
100mL 烧杯中加入1.0g 二苯甲酮(5.49mmol),3mL 水,20mL95%乙醇,再加入0.4gNaBH4
(10.57mmol ),室温下(反应温度<500
C)搅拌反应20min 左右,TLC 跟踪到终点(展开剂:环己烷:乙酸乙酯=10:1)。然后加入100mL 水,滴加10%HCl1mL ,搅拌均匀后吸滤,得二苯甲醇。
【本实验的成败关键】 TLC 判断终点。 注意:
1、NaBH 4的用量 答:理论上NaBH4:二苯甲酮=1:4,但实际上NaBH4的用量要多得多,一般而言需NaBH4:二苯甲酮=1.25:1。本实验比例NaBH4:二苯甲酮=1.9:1
2、所用溶剂
可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇 对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。 3、水的作用
水的作用是水解硼酸脂 。水的用量也不宜过多,在40ml 时,恰好能使过量的硼酸脂水解。
4、浓盐酸的作用
① 分解过量的硼氢化钠,此时滴加速度不宜过快,有大量气泡放出,严禁明火。 ② 水解硼酸脂的配合物。
制备二苯甲醇的最佳实验条件的探讨
学生:杨丽指导教师:张耀文
(太原师范学院化学系1211班030031)
摘要硼氢化钠是一个负氢试剂,能选择性的将醛酮还原成醇,它操作方便,反应可以在含水的醇中进行,1mol硼氢化钠理论上能还原4mol醛酮,但是硼氢化钠的实际用量远比理论值多,本文将讨论制备二苯甲醇的最佳实验制备条件。
关键词负氢试剂选择性还原硼氢化钠还原法
由醛或酮还原生成相应的醇是研究的最多的一类还原反应,可以用于醛和酮还原的催化活性组分也很多,以过渡金属元素居多,但是所需的条件比较苛刻,如需要在高温条件下进行,不易操作,且在操作过程中温度不易控制,另外,利用酶作为催化剂的生物催化法也有较多的研究。与传统的化学催化剂相比,酶具有非常独特的催化性能。概括起来有以下五点,即高效性,高选择性,常压室温,接近中性PH值条件等温和条件下反应,催化活性可以自动调节。同时具有物相和多相催化的特点。尽管酶的这些特点非常突出,诱人,但是目前这些特点的许多作用机理还是不很清楚。此外还有大量的采用金属氢化物,硼(氢)化物等,如LiAlH4,NaBH4.其中LiAlH4作为还原剂选择性能差,往往是羰基和其他官能团都被还原;另一方面LiAlH4,价格昂贵对试剂的无水处理要求非常严格,使其应用受到限制,而较LiAlH4 ,NaBH4还原能力较弱,选择性高,本文仅关注使用NaBH4作为还原剂来还原二苯甲酮制备二苯甲醇,其中实验条件和药品用量将是本文讨论的课题。
一实验部分
1.1主要化学反应
1.2实验流程
1.3 试剂和实验仪器
二苯甲酮硼氢化钠蒸馏水甲醇95%乙醇浓盐酸石油醚50ml圆底烧瓶电子天平100ml烧杯胶头滴管玻璃棒真空泵
1.4实验过程
(1)NaBH4的用量
①50ml圆底烧瓶中加入20ml95%乙醇和1.5g二苯甲酮,缓慢振动,使二苯甲酮溶解于乙醇中,然后称取0.08g硼氢化钠,此时硼氢化钠和二苯甲酮的用量比为1:4,为理论值.把称好的硼氢化钠缓慢倒入圆底烧瓶中,振荡,在加药品过程中,温度始终低于50℃,待加完药品后,放置20min,使其充分反应,直到有沉淀物出现为止,此时将圆底烧瓶中的液体连同沉淀物一起倒入盛有40ml冷水的烧杯中,滴几滴浓盐酸,搅拌混合,抽滤,分离出二苯甲醇,用8ml/次水洗涤两次,用10ml石油醚重结晶,得二苯甲醇晶状体,将其置于烘箱中恒温烘干后用电子天平称量,产品质量为0.43g,测其熔点为64.8℃
②照上述实验,其他条件不变,称取0.16g硼氢化钠,缓慢倒入圆底烧瓶中,此时硼氢化钠与二苯甲酮的用量比为1:2,所得产品质量为0.98g,熔点为64.9℃。
③照上述条件不变,称取0.40g硼氢化钠, 缓慢倒入圆底烧瓶中,此时硼氢化钠与二苯甲酮的用量比为1.25:1,所得产品质量为1.41g,熔点为65.3℃。
(2) 溶剂的选择
①50ml圆底烧瓶中加入20ml95%乙醇和1.5g二苯甲酮,缓慢振动,使二苯甲酮溶解于乙醇中,然后称取0.4g硼氢化钠,把称好的硼氢化钠缓慢倒入圆底烧瓶中,振荡,在加药品过程中,温度始终低于50℃,待加完药品后,放置大约20min,使其充分反应,直到有沉淀物出现为止,此时将圆底烧瓶中的液体连同沉淀物一起倒入盛有40ml冷水的烧杯中,滴几滴浓盐酸,搅拌混合,抽滤,分离出二苯甲醇,用8ml/次水洗涤两次,用10ml石油醚重结晶,得二苯甲醇晶状体,将其置于烘箱中恒温烘干后用电子天平称量,产品质量为1.41g,测其熔点为65.3℃。
②把上述实验中的溶剂95%乙醇换成20ml甲醇后,在实验过程与上述实验条件相同的情况下,发现二苯甲酮固体更易溶于甲醇中,反应速度也比用95%乙醇作为溶剂时的速度更快,所得产品的质量为1.42g,熔点为65.1℃。
⑶蒸馏水的用量
①50ml圆底烧瓶中加入20ml95%乙醇和1.5g二苯甲酮,缓慢振动,使二苯甲酮溶解于乙醇中,然后称取0.40g硼氢化钠,把称好的硼氢化钠缓慢倒入圆底烧瓶中,振荡,在加药品过程中,温度始终低于50℃,待加完药品后,放置20min,使其充分反应,直到有沉淀物出现为止,此时将圆底烧瓶中的液体连同沉淀物一起倒入盛有20ml冷水的烧杯中,滴几滴浓盐酸,搅拌混合,抽滤,分离出二苯甲醇,用8ml/次水洗涤两次,用10ml石油醚重结晶,得二苯甲醇晶状体,将其置于烘箱中恒温烘干后用电子天平称量,产品质量为1.03g,测其熔点为65.2℃。
②50ml圆底烧瓶中加入20ml95%乙醇和1.5g二苯甲酮,缓慢振动,使二苯甲酮溶解于乙醇中,然后称取0.40g硼氢化钠.把称好的硼氢化钠缓慢倒入圆底烧瓶中,振荡,在加药品
过程中,温度始终低于50℃,待加完药品后,放置20min,使其充分反应,直到有沉淀物出现为止,此时将圆底烧瓶中的液体连同沉淀物一起倒入盛有40ml冷水的烧杯中,滴几滴浓盐酸,搅拌混合,抽滤,分离出二苯甲醇,用8ml/次水洗涤两次,用10ml石油醚重结晶,得二苯甲醇晶状体,将其置于烘箱中恒温烘干后用电子天平称量,产品质量为1。41g,测其熔点为65.3℃。
实验①②
蒸馏水20ml 40ml
产量 1.03 g 1.41 g
熔点65.2℃65.3℃
二结果与讨论
硼氢化钠是一种负氢转移试剂,还原的本质是氢原子携带电子向被还原底物的羰基碳原子转移,然后带有负电荷的羰基氧原子与硼结合,形成还原的中间产物,最后经过水解而生成醇,此法试剂较昂贵,通常只用于小量合成。
(1) 理论上1molNaBH4能还原4mol二苯甲酮,但是硼氢化钠的实际用量要比理论值多,那多多少呢?通过上述实验很明显,硼氢化钠与二苯甲酮的物质的量比为1.25:1时,产品质量要比它们物质的量为1:2多,而硼氢化钠与二苯酮物质的量比为1:4时,产品质量很少,由此说明,在实际实验过程中,还原试剂NaBH4的用量远比理论值大。
(2) 该实验中溶剂可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。
(3) 在该实验中水的作用是水解硼酸脂,在上述两个实验的对比中,很明显得知,用40ml的冷水所得二苯甲醇的量要比用20ml的冷水时多。这说明用20ml冷水时没有完全水解了硼酸脂。所以应该用过量的冷水,但是同时水的用量也不宜过多,在40ml时,恰好能使过量的硼酸脂水解。
(4) 浓盐酸在这个实验中所起到的作用主要有两点:
①分解过量的硼氢化钠,此时滴加速度不宜过快,有大量气泡放出,严禁明火。
②水解硼酸脂的配合物。
二苯甲醇的红外光谱图
参考文献:
[1]李需良<<微型半微型有机化学实验>> 高等教育出版社2003
[2]曾绍琼<<有机化学实验>> 高等教育出版社1986
[3]兰州大学复旦大学化学系有机化学教研室主编<<有机化学实验>> 1978
[4][美] L.F费塞尔K.L.威廉森<<有机化学实验>> 1968
Preparation Aenzoin Methyl Alcohol Best Experimental Condition Discussion
Yang Li instructor Zhang Yaowen
(Taiyuan normal school chemistry department,class 1211,Taiyuan 030031)
Abstract The boron sodium hydride is negative hydrogen reagent,Can selective be mellow the aldehyde ketone reduction,Its ease of operation, The response may mellow carry on in the watery, the 1mol hydroboration sodium theoretically can return to original state the 4mol aldehyde ketone, But the hydroboration sodium actual amount used are far more than the theoretical value,This article will discuss will prepare the benzoin methyl alcohol the best experiment to prepare the condition.
Key words Negative hydrogen reagent selectivity return to original state boron sodium hydride reducing process.
实验十苯甲醇和苯甲酸的制备
实验十苯甲醇和苯甲酸的制备 一、实验目的 1.学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法。 2.进一步熟悉机械搅拌器的使用。 3.进一步掌握萃取、洗涤、蒸馏、干燥和重结晶等基本操作。 4.全面复习巩固有机化学实验基本操作技能。 二、基本原理 无α-H的醛在浓碱溶液作用下发生歧化反应,一分子醛被氧化成羧酸,另一分子醛则被还原成醇,此反应称坎尼扎罗反应。本实验采用苯甲醛在浓氢氧化钠溶液中发生坎尼扎罗反应,制备苯甲醇和苯甲酸,反应式如下: CHO + NaOH 2CH2OH + COONa COONa + HCl COOH + NaCl 三、主要试剂与仪器 1.试剂苯甲醛10 mL(0.10 mol),氢氧化钠8g (0.2mol),浓盐酸,乙醚,饱和亚硫酸氢钠溶液,10%碳酸钠溶液,无水硫酸镁。 2.仪器100mL 圆底烧瓶,球形冷凝管,分液漏斗,直形冷凝管,蒸馏头,温度计套管,温度计(250℃),支管接引管,锥形瓶,空心塞,量筒,烧杯,布氏漏斗,吸滤瓶,表面皿,红外灯,机械搅拌器。 四、主要物料的物理常数
五、实验装置 本实验制备苯甲醇和苯甲酸,采用机械搅拌下的加热回流装置,如图1所示。乙醚的沸点低,要注意安全,蒸馏低沸点液体的装置如图2所示。 图1 制备苯甲酸和苯甲醇的反应装置图图2 蒸乙醚的装置图 六、实验步骤 1.在250mL三口烧瓶上安装机械搅拌及回流冷凝管,另一口塞住,如图1。 2.加入8g氢氧化钠和30mL水,搅拌溶解。稍冷,加入10 mL新蒸过的苯甲醛。 3.开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。 4.停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温。 5.反应物冷却至室温后,倒入分液漏斗,用乙醚萃取三次,每次10mL。水层保留待用。 6.合并三次乙醚萃取液,依次用5 mL饱和亚硫酸氢钠洗涤,10mL 10%碳酸钠溶液洗涤,10 mL 水洗涤。 7.分出醚层,倒入干燥的锥形瓶,加无水硫酸镁干燥,注意锥形瓶上要加塞。 8.如图2安装好低沸点液体的蒸馏装置,缓缓加热蒸出乙醚(回收)。 9.升高温度蒸馏,当温度升到140℃时改用空气冷凝管,收集198℃~204℃的馏分,即为苯甲醇,量体积,回收,计算产率。 10.将第5步保留的水层慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。 11.冷却,抽滤,得到粗苯甲酸。 12.粗苯甲酸用水作溶剂重结晶,需加活性炭脱色。产品在红外灯下干燥后称重,回收,计算产率。 七、注意事项 1.本实验需要用乙醚,而乙醚极易着火,必须在近旁没有任何种类的明火时才能使用乙醚。蒸乙醚时可在接引管支管上连接一长橡皮管通入水槽的下水管内或引出室外,接受器用冷水浴冷却。 2.结晶提纯苯甲酸可用水作溶剂重,苯甲酸在水中的溶解度为:80℃时,每100 mL水中可溶解苯甲酸2.2g。
二苯甲醇的制备
现代有机合成实验实验报告 实验名称:二苯甲醇的制备 一、实验目的 (1)学习制备二苯甲醇的实验原理和方法; (2)巩固重结晶的操作方法; (3)进一步练习半微量实验。 二、实验原理 二苯甲酮可以通过多种还原剂还原得到二苯甲醇。在碱性醇溶液中用锌粉还原,是制备二苯甲醇常用的方法,适用于中等规模的实验室制备,对于小量合成,硼氢化钠是更理想的试剂。本实验采用锌粉还原。 三、实验步骤 (1)仪器:搅拌器(标准口)、铁架台、球形冷凝管(标准口)、油浴锅、100℃温度计、250ml 三颈瓶、100ml量筒、减压抽滤装置、天平、干燥器、烧杯、玻璃棒、表面皿、滤纸。(2)试剂:二苯甲酮 1.0g ; NaOH 1.0g ;无水乙醇 10ml;石油醚 10ml;乙酸乙酯:环己烷 =1:2(10ml);硅胶G 适量 二苯甲醇反应装置
实验步骤实验现象解释原因 1、在250ml三颈瓶中依此加入1.0g研细的NaOH,1.0g 二苯甲酮和10ml无水乙醇,最后加入1g锌粉,充分振摇约20min。明显感觉三颈瓶外部变热,即 反应放热。 NaOH溶于水放热。 2、在80℃的热水浴上加热15-20min后取样,在薄层板上二苯甲酮溶液对照点样,展开剂选择(乙酸乙酯:环己烷 =1:2),晾干后放在紫外分析仪下观察反应进行的情况。在紫外分析仪下观察发现,只 有二个紫色的亮斑。Rf二苯甲 醇=0.32,Rf二苯甲酮=0.63 一个亮斑为原料点二苯甲酮 的荧光现象,另一亮斑为产物 二苯甲醇的荧光现象,说明实 验已反应完全。 3、用布氏漏斗抽滤,固体用少量乙醇洗涤。将滤液倒入成有80ml预先用冰水浴冷却的水中,摇匀后用浓HCl小心酸化,使PH为5-6。抽滤过程中,发现抽滤瓶中溶 液呈现淡淡的灰色;冷却过程 中,加酸并不断搅拌发现,溶 液上层出现白色絮状的物质。 液体呈现淡淡的灰色,可能因 为抽滤时漏入了少量的锌粉; 4、真空抽滤析出固体,粗品于烘箱(50℃)中干燥、称重。然后用石油醚(60-90℃)约10ml重结晶,抽滤、干燥、称重。用石油醚重结晶过程冷却时, 发现只有少量结晶析出。 可能原因:石油醚用量不够 四、数据处理 经重结晶,抽滤、干燥后,称得针状结晶的二苯甲醇为0.53g,产率为53%。 五、实验结论 1、二苯甲酮和氢氧化钠必须研碎,否则反应很难进行。 2、锌粉最好后加,便于振摇。
实验七__二苯甲醇的制备
实验七二苯甲醇的制备 一、实验原理、方法、注意事项 1、原理 (一)锌粉还原 (二)硼氢化钠还原 该反应副反应较多,在氢氧根和乙氧负离子的亲核作用下,能够生成 PhC(OH)2Ph和Ph2C(OH)OC2H5;也可能发生苯环上的亲核取代反应生成酚和芳醚。二苯酮可以通过多种还原剂还原,得到二苯甲醇。在碱性溶液中用锌粉还原,是制备二苯甲醇的常用方法,适用于中等规模的实验室制备;对于少量合成,硼氢化钠是更理想的试剂。硼氢化钠是一个选择性地将醛酮还原为相应醇的负氢试剂,它操作方便,反应可在醇溶液中进行,1 mol硼氢化钠理论上能还原4 mol 醛酮。 2、实验方法 图15 用带电动搅拌装置的回流装置进行实验 3、注意事项 (1)采用硼氢化钠还原法,实验开始前应干燥仪器。 (2)可用硼氢化钠或氢化锂铝负氢还原剂还原,也可用其它一些还原剂,如过渡金属催化氢化,乙硼烷还原,醇铝还原等。 二、实验——二苯甲醇的制备 (一)实验目的 1、掌握酮还原制备醇的方法和机理。 2、熟悉回流、重结晶等的基本操作。 (二)药品和仪器 主要药品:二苯酮、锌粉、氢氧化钠、95%乙醇、浓盐酸、60~90 °C石油醚; 主要仪器:三口烧瓶? 温度计球冷凝管搅拌器等 (三)实验原理 (参见本节一、1、) (四)实验步骤 1、锌粉还原法
(1)在装有冷凝管的100 mL的三颈瓶中见图15,依次加入3.0 g mol) NaOH、2.79 g mmol) C6H5COC6H5 (diphenyl ketone, . 48.5 °C, . 305.4 °C/760 mmHg)、3.0 g mol) Zn粉和30 mL 95 %的乙醇。 (2)充分振摇(电动搅拌),反应微微放热,约30 min后,在80 °C的水浴上加热搅拌2 h,使反应完全(多数情况下,在加热40分钟左右体系开始变成棕黄色或棕色)。 (3)冷却,减压抽滤,固体用少量乙醇洗涤。滤液倒入150 mL事先用冰水浴冷却的水中,摇荡混匀后用浓盐酸小心酸化(~5 mL),使溶液的PH值为5~6,减压抽滤见图16析出固体。粗产物在空气中晾干。 图16 减压抽滤装置 (4)晾干后的粗产物用适量石油醚(60~90 °C,根据制备的粗产物的量来定)重结晶,干燥,得二苯基甲醇(无色针状晶体,. 69 °C)。鉴于实验过程中,二苯甲醇很难溶于石油醚,改用石油醚:无水乙醇=3:1的混合溶液进行重结晶。 2、硼氢化钠还原法 (1)在装有回流冷凝管的100 mL的圆底烧瓶中,加入3.66 g mmol) 二苯酮和16 mL甲醇,摇动使其溶解。 (2)迅速称取0.46 g mmol) 硼氢化钠加入瓶中,摇动使其溶解。反应物自然升温至沸,然后室温下放置20 min,并不时振荡。 (3)加入6 mL水,在水浴上加热至沸,保持5 min。冷却,析出结晶。抽滤,粗品干燥后用石油醚(沸程60~90 °C,每克粗品约需3 mL石油醚)重结晶。(五)注意事项 硼氢化钠或氢化锂铝负氢还原剂是比(Zn+ROH)强的还原剂,在操作上,前者形成了均相溶液,不用过滤;后者仍有部分金属锌还原剂未溶解,需要过滤除掉。另外,后者在碱性条件下进行,需要用酸中和才能析出产物结晶。 (六)思考题 1、用硼氢化钠还原,反应后加水并加热至沸的目的是什么? 2、锌粉还原法中,为什么要电动搅拌? 为什么要用水浴加热?温度为什么要控制在80 °C,高点低点如何? 为什么要减压抽滤?滤液为什么要倒入事先用冰水浴冷却的水中?
二苯甲醇的合成实验报告
竭诚为您提供优质文档/双击可除二苯甲醇的合成实验报告 篇一:二苯甲醇的制备 篇二:二苯甲醇的制备 实验三二苯甲醇的制备 【实验目的】 1.掌握由nabh4还原二苯甲酮制备二苯甲醇的方法,了解酮的还原反应机理、还原剂的种类及特点。 2.进一步熟悉用TLc判定反应终点的方法。【实验的准备】 仪器:圆底烧瓶(100ml1个);水银温度计(150℃1支);回流管(1个);吸滤瓶(1个);布氏漏斗(1个);水泵(公用)。 药品:二苯甲酮1.0g(5.49mmol); nabh40.4g(10.57mmol);TLc板,环己烷,乙酸乙酯,10%hcl。 【原理】 o
1.oh nabh4 o 4 +phph )4+3h2o+h ph 4ph ph ph )4 phohph +b(oh)3 【操作】 100mL烧杯中加入1.0g二苯甲酮(5.49mmol),3mL水,20mL95%乙醇,再加入0.4gnabh4 (10.57mmol),室温下(反应温度【本实验的成败关键】TLc判断终点。注意: 1、nabh4的用量答:理论上nabh4:二苯甲酮=1:4,但实际上nabh4的用量要多得多,一般而言需nabh4:二苯甲酮=1.25:1。本实验比例nabh4:二苯甲酮=1.9:1 2、所用溶剂可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易
溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。3、水的作用水的作用是水解硼酸脂。水的用量也不宜过多,在40ml时,恰好能使过量的硼酸脂水解。 4、浓盐酸的作用 ①分解过量的硼氢化钠,此时滴加速度不宜过快,有大量气泡放出,严禁明火。②水解硼酸脂的配合物。 篇三:二苯甲醇的制备的一些问题 实验三二苯甲醇的制备 【实验目的】 1.掌握由nabh4还原二苯甲酮制备二苯甲醇的方法,了解酮的还原反应机理、还原剂的种类及特点。 2.进一步熟悉用TLc判定反应终点的方法。【实验的准备】 仪器:圆底烧瓶(100ml1个);水银温度计(150℃1支);回流管(1个);吸滤瓶(1个);布氏漏斗(1个);水泵(公用)。 药品:二苯甲酮1.0g(5.49mmol); nabh40.4g(10.57mmol);TLc板,环己烷,乙酸乙酯,10%hcl。 【原理】
二苯甲醇的制备的一些问题
实验三 二苯甲醇的制备 【实验目的】 1.掌握由NaBH4还原二苯甲酮制备二苯甲醇的方法,了解酮的还原反应机理、还原剂的种类及特点。 2.进一步熟悉用TLC 判定反应终点的方法。 【实验的准备】 仪 器:圆底烧瓶(100ml 1个);水银温度计(150℃ 1支);回流管(1个);吸滤瓶(1个);布氏漏斗(1个);水泵(公用)。 药 品:二苯甲酮 1.0 g (5.49mmol); NaBH4 0.4 g (10.57 mmol); TLC 板,环己烷,乙酸乙酯,10%HCl 。 【原理】 O 1.NaBH 4OH
Na BH 4 +Ph Ph O Na B(O CH Ph Ph )4 Na B(O CH Ph Ph )4+H 2O 3+H Ph Ph OH +B(OH)3 4 【操作】 100mL 烧杯中加入1.0g 二苯甲酮(5.49mmol),3mL 水,20mL95%乙醇,再加入0.4gNaBH4 (10.57mmol ),室温下(反应温度<500 C)搅拌反应20min 左右,TLC 跟踪到终点(展开剂:环己烷:乙酸乙酯=10:1)。然后加入100mL 水,滴加10%HCl1mL ,搅拌均匀后吸滤,得二苯甲醇。 【本实验的成败关键】 TLC 判断终点。 注意: 1、NaBH 4的用量 答:理论上NaBH4:二苯甲酮=1:4,但实际上NaBH4的用量要多得多,一般而言需NaBH4:二苯甲酮=1.25:1。本实验比例NaBH4:二苯甲酮=1.9:1 2、所用溶剂 可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇 对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。 3、水的作用 水的作用是水解硼酸脂 。水的用量也不宜过多,在40ml 时,恰好能使过量的硼酸脂水解。 4、浓盐酸的作用 ① 分解过量的硼氢化钠,此时滴加速度不宜过快,有大量气泡放出,严禁明火。 ② 水解硼酸脂的配合物。
最新实验七二苯甲醇的制备
实验七二苯甲醇的制 备
实验七 二苯甲醇的制备 一、实验原理、方法、注意事项 1、原理 (一)锌粉还原 C 6H 5COC 6H 5 C 6H 5CH(OH)C 6H 5 2 NaOH Zn +Zn 2+H H Zn 2+H H 2CHOH (二)硼氢化钠还原 H C O H +H 3B OCH 3H 3B OCH 343BH 4(CH 3O)4B +C 6H 5COC 6H 5 6H 5CH(OH)C 6H 5CH 3OH, NaBH 4 该反应副反应较多,在氢氧根和乙氧负离子的亲核作用下,能够生成 PhC(OH)2Ph 和Ph2C(OH)OC2H5;也可能发生苯环上的亲核取代反应生成酚和芳醚。二苯酮可以通过多种还原剂还原,得到二苯甲醇。在碱性溶液中用锌粉还原,是制备二苯甲醇的常用方法,适用于中等规模的实验室制备;对于少量合成,硼氢化钠是更理想的试剂。硼氢化钠是一个选择性地将醛酮还原为相应
醇的负氢试剂,它操作方便,反应可在醇溶液中进行,1 mol硼氢化钠理论上能还原4 mol醛酮。 2、实验方法 图15 用带电动搅拌装置的回流装置进行实验 3、注意事项 (1)采用硼氢化钠还原法,实验开始前应干燥仪器。 (2)可用硼氢化钠或氢化锂铝负氢还原剂还原,也可用其它一些还原剂,如过渡金属催化氢化,乙硼烷还原,醇铝还原等。 二、实验——二苯甲醇的制备 (一)实验目的 1、掌握酮还原制备醇的方法和机理。 2、熟悉回流、重结晶等的基本操作。 (二)药品和仪器 主要药品:二苯酮、锌粉、氢氧化钠、95%乙醇、浓盐酸、60~90 °C石油醚; 主要仪器:三口烧瓶温度计球冷凝管搅拌器等
苯甲醇的制备实验报告
三苯甲醇的制备 实验目的:学习利用Grignard反应合成醇 练习无水操作反应 学习水蒸气蒸馏操作 认识三苯甲基碳正离子 反应原理: 试剂药品:镁屑,,溴苯(新蒸),,苯甲酸乙酯,无水乙醚,氯化铵,乙醇 实验步骤: 1.苯基溴化镁的制备 如图在50mL三颈瓶上分别装置搅拌器、冷凝管及滴液漏斗,在冷凝管及滴液漏斗的上口装置氯化钙干燥管。瓶内放置镁屑及一小粒碘片,在滴液漏斗中混 合溴苯及8mL无水乙醚。先将三分之一的混合液滴入烧瓶中,数分 钟后即见镁屑表面有气泡产生,溶液轻微混浊,碘的颜色开始消失。 若不发生反应,可用水浴或手掌温热。反应开始后开动搅拌,缓缓 滴入其余的溴苯醚溶液,滴加速度保持溶液呈微沸状态。加毕后, 在水浴继续回流,使镁屑作用完全。 2.三苯甲醇的制备 将已制好的苯基溴化镁试剂置于冷水浴中,在搅拌下由滴液漏斗滴加苯甲酸乙酯和3mL无
水乙醚的混合液,控制滴加速度保持反应平稳地进行。滴加完毕后,将反应混合物在水浴回流,使反应进行完全,这时可以观察到反应物明显地分为两层。将反应物改为冰水浴冷却,在搅拌下由滴液漏斗慢慢滴加由9mL水和氯化铵配成的溶液,以分解加成产物。 将反应装置改为蒸馏装置,在水浴上蒸去乙醚,再将残余物进行水蒸气蒸馏,以除去未反应的溴苯及联苯等副产物。瓶中剩余物冷却后凝 为固体,抽滤收集。得三苯甲醇粗产品(淡黄色 固体)。用80%的乙醇进行重结晶,干燥后得白色 颗粒状晶体。 3.三苯甲基碳正离子的检验 在一洁净的干燥试管中,加入三苯甲醇和2mL 冰醋酸,温热使其溶解,向试管中滴加2滴浓硫 酸,立即生成橙红色溶液,然后加入2mL水,颜色消失,并有白色沉淀生成。 产率:以苯甲酸乙酯(M260)的量为基准计算产率:ⅹ260)=68%
实验七二苯甲醇的制备.doc
实验七 二苯甲醇的制备 一、实验原理、方法、注意事项 1、原理 (一)锌粉还原 Zn + NaOH C 6H 5 COC 6 H 5 C 6H 5CH(OH)C 6 H 5 H H 2 NaOH + Zn 2+ Zn Ph O C + Ph H H Ph 2CHOH Zn 2+ (二)硼氢化钠还原 CH 3 OH, NaBH 4 C 6 H 5CH(OH)C 6 H 5 C 6 H 5 COC 6 H 5 C O C O + H 3BOCH 3 H 3 B H OCH 3 H H H 4 H 3BOCH 3 3BH 4 + (CH 3 O) 4B 该反应副反应较多,在氢氧根和乙氧负离子的亲核作用下,能够生成 PhC(OH)2Ph 和 Ph2C(OH)OC2H5 ;也可能发生苯环上的亲核取代反应生成酚和芳醚。二苯酮可以通过多种 还原剂还原,得到二苯甲醇。在碱性溶液中用锌粉还原, 是制备二苯甲醇的常用方法, 适用 于中等规模的实验室制备; 对于少量合成, 硼氢化钠是更理想的试剂。 硼氢化钠是一个选择 性地将醛酮还原为相应醇的负氢试剂,它操作方便,反应可在醇溶液中进行, 1 mol 硼氢化 钠理论上能还原 4 mol 醛酮。 2、实验方法
图 15用带电动搅拌装置的回流装置进行实验 3、注意事项 (1)采用硼氢化钠还原法,实验开始前应干燥仪器。 (2)可用硼氢化钠或氢化锂铝负氢还原剂还原,也可用其它一些还原剂,如过渡金属催化氢化,乙硼烷还原,醇铝还原等。 二、实验——二苯甲醇的制备 (一)实验目的 1、掌握酮还原制备醇的方法和机理。 2、熟悉回流、重结晶等的基本操作。 (二)药品和仪器 主要药品:二苯酮、锌粉、氢氧化钠、95%乙醇、浓盐酸、60~90 °C 石油醚; 主要仪器:三口烧瓶温度计球冷凝管搅拌器等 (三)实验原理 (参见本节一、1、) (四)实验步骤 1、锌粉还原法 ( 1)在装有冷凝管的100 mL 的三颈瓶中见图15,依次加入 3.0 g (0.076 mol) NaOH 、2.79 g (15.3 mmol) C 6H 5COC6 H5 (diphenyl ketone, m.p. 48.5 C, b.p. 305°.4 C/760° mmHg) 、 3.0 g (0.046 mol) Zn 粉和30 mL 95 % 的乙醇。 ( 2)充分振摇(电动搅拌),反应微微放热,约30 min 后,在80 °C 的水浴上加热搅拌 2 h,使反应完全(多数情况下,在加热40 分钟左右体系开始变成棕黄色或棕色)。 ( 3)冷却,减压抽滤,固体用少量乙醇洗涤。滤液倒入150 mL 事先用冰水浴冷却的水中, 摇荡混匀后用浓盐酸小心酸化(~5 mL ),使溶液的 PH 值为 5~6,减压抽滤见图16 析出固
实验七__二苯甲醇的制备
实验七 二苯甲醇的制备 一、实验原理、方法、注意事项 1、原理 (一)锌粉还原 C 6H 5COC 6H 5 C 6H 5CH(OH)C 6H 5 2 NaOH Zn +Zn 2+H H Zn 2+H H 2CHOH (二)硼氢化钠还原 H C O H +H 3B OCH 3H 3B OCH 343BH 4(CH 3O)4B +C 6H 5COC 6H 5 6H 5CH(OH)C 6H 5CH 3OH, NaBH 4 该反应副反应较多,在氢氧根和乙氧负离子的亲核作用下,能够生成Ph C(OH )2Ph 和Ph2C(OH )OC2H 5;也可能发生苯环上的亲核取代反应生成酚和芳醚.二苯酮可以通过多种还原剂还原,得到二苯甲醇。在碱性溶液中用锌粉还原,是制备二苯甲醇的常用方法,适用于中等规模的实验室制备;对于少量合成,硼氢化钠是更理想的试剂。硼氢化钠是一个选择性地将醛酮还原为相应醇的负氢试剂,它操作方便,反应可在醇溶液中进行,1 mo l硼氢化钠理论上能还原4 mol 醛酮。 2、实验方法
图15 用带电动搅拌装置的回流装置进行实验 3、注意事项 (1)采用硼氢化钠还原法,实验开始前应干燥仪器. (2)可用硼氢化钠或氢化锂铝负氢还原剂还原,也可用其它一些还原剂,如过渡金属催化氢化,乙硼烷还原,醇铝还原等。 二、实验-—二苯甲醇的制备 (一)实验目的 1、掌握酮还原制备醇的方法和机理。 2、熟悉回流、重结晶等的基本操作。 (二)药品和仪器 主要药品:二苯酮、锌粉、氢氧化钠、95%乙醇、浓盐酸、60~90 °C石油醚; 主要仪器:三口烧瓶温度计球冷凝管搅拌器等 (三)实验原理 (参见本节一、1、) (四)实验步骤 1、锌粉还原法 (1)在装有冷凝管的100 mL的三颈瓶中见图15,依次加入3。0g(0。076 mol) NaOH、2.79 g (15.3 mmol) C6H5COC6H5(diphenyl ketone, m.p。 48.5°C, b。p. 305.4 °C/760mmHg)、3.0 g (0.046 mol) Zn粉和30 mL 95%的乙醇. (2)充分振摇(电动搅拌),反应微微放热,约30 min后,在80 °C的水浴上加热搅拌2 h,使反应完全(多数情况下,在加热40分钟左右体系开始变成棕黄色或棕色). (3)冷却,减压抽滤,固体用少量乙醇洗涤。滤液倒入150 mL事先用冰水浴冷却的水中,
苯甲醇和苯甲的制备预习报告及思考题
苯甲醇和苯甲酸的制备 一.实验目的 1.学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法 2.巩固机械搅拌器的使用 3.进一步掌握萃取、洗涤、蒸馏、干燥和重结晶等基本操作 4.学会低沸点溶剂的处理 二.实验原理 无α-H的醛在浓碱溶液作用下发生歧化反应,一分子醛被氧化成羧酸,另一分子醛则被还原成醇,此反应称坎尼扎罗反应。本实验采用苯甲醛在浓氢氧化钠溶液中发生坎尼扎罗反应,制备苯甲醇和苯甲酸。反应物加水溶解后,用乙醚加以萃取,乙醚层经洗涤、干燥、蒸馏,得到苯甲醇;水层经酸化得到苯甲酸。反应式如下: CHO 2+NaOH CH2OH + COONa COONa +HCl COOH+NaCl 苯甲醛如果长时间放置,会被空气氧化,因此存在以下的副反应: CHO +O 2 COOH 三.实验准备 1.主要试剂及仪器 1)试剂 苯甲醛 10 mL (0.10 mol),氢氧化钠 8g (0.2mol),浓盐酸,乙醚,饱和亚硫酸氢钠溶液,10%碳酸钠溶液,无水硫酸镁。 2)仪器 100mL 圆底烧瓶,球形冷凝管,分液漏斗,直形冷凝管,蒸馏头,温度计套管,温度计(250℃),支管接引管,锥形瓶,空心塞,量筒,烧杯,布氏漏斗,吸滤瓶,表面皿,红外灯,机械搅拌器。
2.主要物料物理常数 化合物分子量比重(d)熔点(℃)沸点(℃)折光率(n) 溶解度 水乙 醇乙醚 苯甲醛105.12 1.046 -26 179.1 1.5456 0.3 溶溶苯甲醇108.13 1.0419 -15.3 205.3 1.5392 417∞∞苯甲酸122.12 1.2659 122 249 1.501 微溶溶溶 四.实验装置及操作要点 制备苯甲醇和苯甲酸采用回流搅拌装置,实验装置如图1所示。乙醚沸点低,要注意安全。蒸馏低沸点液体的装置如图2所示。 图1.制备苯甲醇和苯甲酸的反应装置 图2.蒸乙醚的装置图 【干燥操作要点】 1.干燥剂不是越多越好 2.干燥操作在干燥的带有塞子的锥形瓶中进行。加入干燥剂后,加塞旋摇,放置
二苯甲醇的制备
实验二苯甲醇的制备 一、实验目的 (1) 学习制备二苯甲醇的实验原理和方法; (3) 了解还原反应的类型及特点; (4) 练习半微量实验方法。 二、实验原理 在碱性溶液中用锌粉还原二苯甲酮得二苯甲醇。 反应机理: 三、仪器与试剂 (1) 仪器:搅拌器(标准口)、铁架台、球形冷凝管(标准口)、油浴锅、 100 ?C温度计、250 mL三颈瓶、100 mL量筒、减压抽滤装置、天平、干燥器、烧杯、玻璃棒、表面皿、熔点测定仪、牛角勺、滤纸。 (2) 试剂: 二苯甲酮 1.0 g (0.0055 mol) 无水乙醇10 mL 苯适量 锌粉 1.0 g (0.015 mol) 石油醚(b.p 60—90 ?C)10 mL 硅胶G 适量 四、实验步骤 实验步骤实验现象现象解释在装有冷凝管的50 mL 锥 形瓶中, 依次加入研细的 1.0 g 氢氧化钠、1.0 g二苯甲酮、1.0 g锌粉及10 mL无水乙醇, 充分反应微放热 发生氧化还原反应, 反应放热。
五、注意事项 (1) 称量NaOH时要将颗粒用研磨碾成粉末,称量迅速,防止潮解。 (2) 反应过程要不断搅动。 (3) 用浓HCl酸化时要有耐心,pH值调到5~6为佳,如果酸性太强,产物 会分解。 (4) 样品干燥时注意温度的控制,防止样品溶化。 (5) 烘干温度不大于45摄氏度,防止熔化。 六、思考题 (1) 用图示表明反应未进行完全和反应完全的薄层斑点示意图.
(2) 为什么反应后要加入10%盐酸进行酸化? 为什么酸化的酸性不能太强? 由于反应过程中,整个溶液呈碱性,产品溶于碱性溶液中,故要加入盐酸进行酸化。但是如果酸性太强的话,则会使产品发生取代反应,生成了二苯氯甲烷。反应如下:
苯甲酸和苯甲醇的制备
试验四十一苯甲酸和苯甲醛的制备 一、目的要求 1. 掌握Cannizzaro 反应制备苯甲酸和苯甲醇的原理与方法; 2. 熟练掌握萃取与蒸馏操作; 二、基本原理 无α-氢的醛类和浓的强碱溶液作用时,发生分子间的自氧化还原反应,一分子醛被还 原成醇,另一分子醛被氧化成酸,此反应称为Cannizzaro 反应。如: 按上述反应式只能得到一半的醇。如应用稍过量的甲醛水溶液与醛(1.3∶1mol)反应 时,则可使所有的醛还原至醇,而甲醛则氧化成甲酸。例如: 三、仪器药品 250mL锥形瓶、分液漏斗、刚果红试纸等 氢氧化钾18g(0.32mol)、饱和亚硫酸氢钠溶液、10%碳酸钠溶液、无水硫酸镁、 无水碳酸钾、浓盐酸 苯甲醛21g(20mL,0.2mol)、乙醚 四、实验步骤 在250mL锥形瓶中配制18g氢氧化钾(0.32mol)和18mL水的溶液,冷至室温后,加 入21g新蒸过的苯甲醛(20mL,0.2mol)。用橡皮塞塞紧瓶口,用力振摇,使反应物充分混 合,最后成为白色糊状物,放置24小时以上。 向反应混合物中逐渐加入足够量的水(约60mL),不断振摇使其中的苯甲酸盐
全部溶 解。将溶液倒入分液漏斗,每次用20mL乙醚萃取三次(萃取出什么?)。合并乙醚萃取液, 依次用5mL饱和亚硫酸氢钠溶液、10mL10%碳酸钠溶液及10mL水洗涤,最后用无水硫酸 镁或无水碳酸钾干燥。 干燥后的乙醚溶液,先蒸去乙醚,再蒸馏苯甲醇,收集204~206℃的馏分,产量8~8.5g (产率74~79%)。 乙醚萃取过的水溶液,用浓盐酸酸化直至刚果红试纸变蓝,冰水冷却使苯甲酸完全析 出,抽滤,用少量水洗涤,挤压去水分。将制得的苯甲酸放在沸水浴上干燥。若要得到纯产品,可用水重结晶提纯。 纯粹苯甲酸为无色针状晶体,熔点为122.4℃。 纯粹苯甲醇33333的沸点为205.5℃,d4 25 1.0413。 五、思考回答 1. 试比较Cannizzaro 反应与羟醛缩合反应在醛的结构上有何不同?怎样利用Cannizzaro 反应将苯甲醛全部转化成苯甲醇? 2. 本实验中两种产物是根据什么原理分离提纯的?用饱和的亚硫酸氢钠及10%碳酸钠 溶液洗涤的目的何在?
实验七二苯甲醇的制备
实验七二苯甲醇的制备集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)
实验七二苯甲醇的制备 一、实验原理、方法、注意事项 1、原理 (一)锌粉还原 (二)硼氢化钠还原 该反应副反应较多,在氢氧根和乙氧负离子的亲核作用下,能够生成PhC(OH)2Ph和Ph2C(OH)OC2H5;也可能发生苯环上的亲核取代反应生成酚和芳醚。二苯酮可以通过多种还原剂还原,得到二苯甲醇。在碱性溶液中用锌粉还原,是制备二苯甲醇的常用方法,适用于中等规模的实验室制备;对于少量合成,硼氢化钠是更理想的试剂。硼氢化钠是一个选择性地将醛酮还原为相应醇的负氢试剂,它操作方便,反应可在醇溶液中进行,1 mol硼氢化钠理论上能还原4 mol醛酮。 2、实验方法 图15 用带电动搅拌装置的回流装置进行实验 3、注意事项 (1)采用硼氢化钠还原法,实验开始前应干燥仪器。 (2)可用硼氢化钠或氢化锂铝负氢还原剂还原,也可用其它一些还原剂,如过渡金属催化氢化,乙硼烷还原,醇铝还原等。 二、实验——二苯甲醇的制备 (一)实验目的 1、掌握酮还原制备醇的方法和机理。 2、熟悉回流、重结晶等的基本操作。
(二)药品和仪器 主要药品:二苯酮、锌粉、氢氧化钠、95%乙醇、浓盐酸、60~90 °C 石油醚; 主要仪器:三口烧瓶? 温度计球冷凝管搅拌器等 (三)实验原理 (参见本节一、1、) (四)实验步骤 1、锌粉还原法 (1)在装有冷凝管的100 mL的三颈瓶中见图15,依次加入3.0 g (0.076 mol) NaOH、2.79 g (15.3 mmol) C 6H 5 COC 6 H 5 (diphenyl ketone, m.p. 48.5 °C, b.p. 305.4 °C/760 mmHg)、3.0 g (0.046 mol) Zn粉和30 mL 95 %的乙醇。 (2)充分振摇(电动搅拌),反应微微放热,约30 min后,在 80 °C的水浴上加热搅拌2 h,使反应完全(多数情况下,在加热40分钟左右体系开始变成棕黄色或棕色)。 (3)冷却,减压抽滤,固体用少量乙醇洗涤。滤液倒入150 mL事先用冰水浴冷却的水中,摇荡混匀后用浓盐酸小心酸化(~5 mL),使溶液的PH值为5~6,减压抽滤见图16析出固体。粗产物在空气中晾干。 图16 减压抽滤装置(4)晾干后的粗产物用适量石油醚(60~90 °C,根据制备的粗产物的量来定)重结晶,干燥,得二苯基甲醇(无色针状晶体,m.p.
苯甲醇的制备
相转移催化法合成苯甲醇 预习内容:请参考周科衍等编《有机化学实验》P108~109 一、实验目的 1.了解相转移催化反应的原理,学习利用相转移催化反应制取苯甲醇的方法。 2.复习巩固电动搅拌、加热回流、萃取、干燥、常压蒸馏等实验方法。 3.练习高温蒸馏和空气冷凝管的使用方法。 二、实验原理 用苯氯甲烷制苯甲醇是由卤代烃水解制备醇的一个实际例子。水解在碱性水溶液中进行。由于卤代烃均不溶于水,这个两相反应进行得很慢,并且需要强烈搅拌。如果加入相转移催化剂如四乙基溴化铵,反应时间可以大缩短。 反应式: 四乙基溴化铵 2CH2OH + 2KCl + CO2 CH2Cl + K2CO3 + H2O 无水碳酸钾9g(0.065mol) 溴化四乙基铵2mL(50%水溶液) 乙酸乙酯30ml 无水硫酸镁适量 四、实验步骤: 在装有电动搅拌器的250ml三口瓶里加入9g碳酸钾、70ml水,搅拌溶解,再依次加入2ml溴化四乙基铵和10ml苯氯甲烷。搅拌加热回流反应1-1.5h。冷却,转入125ml 分液漏斗中,分出油层,水层用乙酸乙酯萃取三次,每次10ml。合并萃取液和粗苯甲醇,用无水硫酸镁或碳酸钾干燥。 用一般的蒸馏装置蒸馏,回收乙酸乙酯后,将直形冷凝管改为空气冷凝管,继续蒸馏收集200-208?C的馏分。称重,计算产率。 五、掌握要点 本实验操作训练的重点是电动搅拌、相转移催化反应的操作。 要求要理解相转移催化反应的原理,为什么要用乙酸乙酯萃取?为什么要用空气冷凝管蒸馏? 六、实验装置图
分液漏斗 反应装置 蒸馏瓶 高温蒸馏装置 七、注意事项 [1] 相转移催化剂四乙基溴化铵可用三乙基苄基氯化铵代替。 [2] 苯氯甲烷有腐蚀性,加料时要细心,不要弄到皮肤上。一旦洒到皮肤上,要立即用水冲洗,再用肥皂水洗。 [3] 虽然加入了相转移催化剂,反应中仍然需要搅拌来加快相转移的速度。 [4] 反应结束后,冷却到30-40 C 为宜,过低的温度会有固体析出,影响下步的分离操作。 [5] 高温蒸馏时,空气冷凝管温度较高,小心烫伤。 八、回答思考题 1.苄基氯碱性水解的反应历程是什么? 2.简述相转移催化反应的原理? 3.乙酸乙酯萃取的作用是什么?能否用其它溶剂代替? 4.简答什么情况下才考虑用空气冷凝管蒸馏?
制备二苯甲醇
制备二苯甲醇 摘要硼氢化钠是一个负氢试剂,能选择性的将醛酮还原成醇,它操作方便,反应可以在含水的醇中进行,1mol硼氢化钠理论上能还原4mol醛酮,但是硼氢化钠的实际用量远比理论值多,本文将讨论制备二苯甲醇的最佳实验制备条件。 由醛或酮还原生成相应的醇是研究的最多的一类还原反应,可以用于醛和酮还原的催化活性组分也很多,以过渡金属元素居多,但是所需的条件比较苛刻,如需要在高温条件下进行,不易操作,且在操作过程中温度不易控制,另外,利用酶作为催化剂的生物催化法也有较多的研究。与传统的化学催化剂相比,酶具有非常独特的催化性能。概括起来有以下五点,即高效性,高选择性,常压室温,接近中性PH值条件等温和条件下反应,催化活性可以自动调节。同时具有物相和多相催化的特点。尽管酶的这些特点非常突出,诱人,但是目前这些特点的许多作用机理还是不很清楚。此外还有大量的采用金属氢化物,硼(氢)化物等,如LiAlH4,NaBH4.其中LiAlH4作为还原剂选择性能差,往往是羰基和其他官能团都被还原;另一方面LiAlH4,价格昂贵对试剂的无水处理要求非常严格,使其应用受到限制,而较LiAlH4 ,NaBH4
还原能力较弱,选择性高,本文仅关注使用NaBH4作为还原剂来还原二苯甲酮制备二苯甲醇,其中实验条件和药品用量将是本文讨论的课题。 一实验部分 1.1主要化学反应 1.2实验流程 1.3 试剂和实验仪器 二苯甲酮硼氢化钠蒸馏水甲醇 95%乙醇浓盐酸石油醚 50ml圆底烧瓶电子天平 100ml烧杯胶头滴管玻璃棒真空泵 1.4实验过程 (1)NaBH4的用量 ① 50ml圆底烧瓶中加入20ml95%乙醇和1.5g二苯甲酮,
实验室三苯甲醇的制备
三苯甲醇的合成 一、实验目的 1学习和掌握叔醇的制备原理和方法. 2进一步巩固Grignard 试剂的制备方法,技巧和应用. 3学习水蒸气蒸馏的基本操作. 二、实验原理 用溴苯和镁制得Grignard 试剂,通过苯基溴化镁可制备三苯甲 醇.本实验选用由二苯甲酮与苯基溴化镁反应制备. 纯三苯甲醇为无色棱状晶体,mp 为164.2°C 三、仪器和药品 玻璃仪器、冷凝管、滴液漏斗、电动搅拌机、蒸馏装置、水蒸 馏装置、真空泵、冰箱、镁屑、溴苯,二苯甲酮、无水乙醚、氯化铵、 乙醇 四、实验步骤、 1苯基溴化镁的制备 在干燥的三口瓶内放入0.75g(0.031mol)镁屑和一小粒碘片,装 上带干燥管的回流冷凝管[1],另用滴液漏斗中取3.4mL (5g 0.032mol) 溴苯和12mL 无水乙醚,.滴加约三分之一的溴苯乙醚溶液(滴加的速 度保持溶液呈微沸状态)。滴加完毕后水浴加热回流半小时,使镁屑 反应完全。得到苯基溴化镁。 2三苯甲醇的制备 将制备好的苯基溴化镁乙醚溶液置于冰浴中,在搅拌下滴加5.5g (0.030mol)二苯甲酮和15mL 无水乙醚的混合液。滴加完毕后将反应 混合物水浴加热继续回流0.5小时,使反应完全。在冰水浴中冷却, 在搅拌下慢慢滴加6g 氯化铵配成的饱和水溶液(用水22mL)分解加成 (C 6H 5)2C=O C H MgBr,Et O (C 6H 5)3COMgBr NH 4Cl,H 2O (C 6H 5)3COH
产物[2],再将反应装置改为蒸馏装置,在水浴上蒸去乙醚,再将残余物进行水蒸气蒸馏以除去未反应的溴苯和副产物联苯。瓶中的剩余物冷却后凝为固体,抽滤收集。粗产品用乙醇和水混合溶剂进行重结晶 [3],干燥后产量应有4-4.5g。. 五、注意事项 1.制备和使用Grignard试剂的反应体系必须充分干燥,溴苯用无水氯化钙干燥过夜,使用绝对无水乙醚为溶剂,冷凝管要安装干燥管。 2.如出现絮状氢氧化镁未全溶,可加入少量稀盐酸,促使之溶解. 3.重结晶时可先将粗产品加热溶于少量乙醇中,再逐滴加入预热的水,直至溶液刚好出现混浊为止,然后再加入一滴乙醇使之浑浊消失,冷却,结晶析出,这样保证溶解的刚完全而不至于溶液过多影响结晶速度和晶型。 六、思考 1. 溴苯加入太快或一次性加入会发生那些可能的副反应? 2.如何选择混合溶剂进行重结晶? 3.在该反应中乙醚如果含有乙醇对本反应有什么影响? 4.写出苯基溴化镁与碳酸二甲酯,甲酸乙酯反应的产物分别是什么?总结Grignard试剂在有机合成中的应用.
二苯甲醇的制备的一些问题
实验三二苯甲醇的制备 【实验目的】 1.掌握由NaBH4还原二苯甲酮制备二苯甲醇的方法,了解酮的还原反应机理、还原剂的种类及特点。 2.进一步熟悉用TLC判定反应终点的方法。 【实验的准备】 仪器:圆底烧瓶(100ml 1个);水银温度计(150℃1支);回流管(1个);吸滤瓶(1个);布氏漏斗(1个);水泵(公用)。 药品:二苯甲酮 1.0 g (5.49mmol); NaBH4 0.4 g (10.57 mmol); TLC板,环己烷,乙酸乙酯,10%HCl。 【物理常数】
【原理】 O 1.NaBH OH Na BH 4 +Ph Ph O Na B(O CH Ph Ph )4 Na B(O CH Ph Ph )4+H 2O 3+H Ph Ph OH +B(OH)3 4 【操作】
100mL烧杯中加入1.0g二苯甲酮(5.49mmol),3mL水,20mL95%乙醇,再加入0.4gNaBH4(10.57mmol),室温下(反应温度<500C)搅拌反应20min左右,TLC跟踪到终点(展开剂:环己烷:乙酸乙酯=10:1)。然后加入100mL水,滴加10%HCl1mL,搅拌均匀后吸滤,得二苯甲醇。 【本实验的成败关键】 TLC判断终点。 注意: 1、NaBH4的用量 答:理论上NaBH4:二苯甲酮=1:4,但实际上NaBH4的用量要多得多,一般而言需NaBH4:二苯甲酮=1.25:1。本实验比例NaBH4:二苯甲酮=1.9:1 2、所用溶剂 可用95%乙醇和甲醇,甲醇作为溶剂时虽然二苯甲酮易溶于它,且反应速度快,但与95%乙醇相比,甲醇的毒性要大比乙醇对人体的危害性要大,且甲醇的价格昂贵,故在制备二苯甲醇的时候,溶剂一般用95%的乙醇。 3、水的作用 水的作用是水解硼酸脂。水的用量也不宜过多,在40ml时,恰好能使过量的硼酸脂水解。 4、浓盐酸的作用 ①分解过量的硼氢化钠,此时滴加速度不宜过快,有大量气泡放出,严禁明火。 ②水解硼酸脂的配合物。
二苯甲醇的制备电子版本
二苯甲醇的制备
现代有机合成实验实验报告 实验名称:二苯甲醇的制备 一、实验目的 (1)学习制备二苯甲醇的实验原理和方法; (2)巩固重结晶的操作方法; (3)进一步练习半微量实验。 二、实验原理 二苯甲酮可以通过多种还原剂还原得到二苯甲醇。在碱性醇溶液中用锌粉还原,是制备二苯甲醇常用的方法,适用于中等规模的实验室制备,对于小量合成,硼氢化钠是更理想的试剂。本实验采用锌粉还原。 三、实验步骤 (1)仪器:搅拌器(标准口)、铁架台、球形冷凝管(标准口)、油浴锅、100℃温度计、250ml三颈瓶、100ml量筒、减压抽滤装置、天平、干燥器、烧杯、玻璃棒、表面皿、滤纸。 (2)试剂:二苯甲酮 1.0g ; NaOH 1.0g ;无水乙醇 10ml;石油醚 10ml;乙酸乙酯:环己烷 =1:2(10ml);硅胶G 适量
二苯甲醇反应装置 实验步骤实验现象解释原因 1、在250ml三颈瓶中依此加入 1.0g研细的NaOH,1.0g二苯甲酮和10ml无水乙醇,最后加入1g锌粉,充分振摇约20min。明显感觉三颈瓶外部变热, 即反应放热。 NaOH溶于水放热。 2、在80℃的热水浴上加热15-20min后取样,在薄层板上二苯甲酮溶液对照点样,展开剂选择(乙酸乙酯:环己烷 =1:2),晾干后放在紫外分析仪下观察反应进行的情况。在紫外分析仪下观察发现, 只有二个紫色的亮斑。Rf二 苯甲醇=0.32,Rf二苯甲酮=0.63 一个亮斑为原料点二苯甲酮 的荧光现象,另一亮斑为产 物二苯甲醇的荧光现象,说 明实验已反应完全。 3、用布氏漏斗抽滤,固体用少量乙醇洗涤。将滤液倒入成有80ml预先用冰水浴冷却的水中,摇匀后用浓HCl小心酸化,使PH为5-6。抽滤过程中,发现抽滤瓶中 溶液呈现淡淡的灰色;冷却 过程中,加酸并不断搅拌发 现,溶液上层出现白色絮状 的物质。 液体呈现淡淡的灰色,可能 因为抽滤时漏入了少量的锌 粉; 4、真空抽滤析出固体,粗品于烘箱(50℃)中干燥、称重。然后用石油醚(60-用石油醚重结晶过程冷却 时,发现只有少量结晶析 出。 可能原因:石油醚用量不够
(完整版)苯甲醇和苯甲酸的制备
学生姓名: 小田田 学号: 专业班级: 实验类型:□验证■综合□设计□创新 实验日期: 2013年4月24日 实验地点: 同组学生姓名: 指导教师: 实验成绩: 实验八 :苯甲醇和苯甲酸的制备 一、实验目的 1.学习由苯甲醛制备苯甲醇和苯甲酸的原理和方法。 3.进一步掌握萃取、洗涤、蒸馏和干燥等基本操作。 二、产品介绍 苯甲醇是最简单的芳香醇之一,可看作是苯基取代的甲醇。在自然界中多数以酯的形式存在于香精油中。中文别名 苄醇;。苄醇是极有用的定香剂,用于配制香皂;日用化妆香精。但苄醇能缓慢地自然氧化,一部分生成苯甲醛和苄醚,使市售产品常带有杏仁香味,故不宜久贮。苄醇在工业化学品生产中用途广泛;医药;合成树脂溶剂;可用作尼龙丝;纤维及塑料薄膜的干燥剂,染料;纤维素酯;酪蛋白的溶剂,制取苄基酯或醚的中间体。同时,广泛用于制笔(圆珠笔油);油漆溶剂等。 苯甲酸为具有苯或甲醛的气味的鳞片状或针状结晶,具有苯或甲醛的臭味。在100℃时迅速升华,它的蒸气有很强的刺激性,吸入后易引起咳嗽。微溶于水,易溶于乙醇、乙醚等有机溶剂。苯甲酸是弱酸,比脂肪酸强。它们的化学性质相似,都能形成盐、酯、酰卤、酰胺、酸酐等,都不易被氧化。苯甲酸的苯环上可发生亲电取代反应,主要得到间位取代产。 三:反应式 主反应: CHO + NaOH 2 CH 2OH + COONa COONa + HCl COOH + NaCl 副反应: CHO COOH +O 2
学生姓名: 小田田 学号: 专业班级: 实验类型:□验证■综合□设计□创新 实验日期: 2013年4月24日 实验地点: 同组学生姓名: 指导教师: 实验成绩: 四:主要试剂及产品的物理常数 名称 分子量 性状 相对密度 熔点 (℃) 沸点 (℃) 溶解度 水 醇 醚 苯甲醛 106.12 无色液体,有苦杏仁气味 1.04 -26 179.62 微溶 易溶 易溶 苯甲酸 122.1 鳞片状或针状结晶,具有苯的臭味 1.27 122.13 249 0.21g 46.6g 66g 苯甲醇 108.13 无色液体,有芳香味 1.04 -15.3 205.7 微溶 易溶 易溶 乙醚 74.12 无色透明液体。有特殊刺激气味 0.71 -116.3 34.6 不溶 易溶 -- 五:试剂与仪器 1、主要仪器 : 125mL 圆底烧瓶、分液漏斗,蒸馏装置、烧杯等。 2、主要试剂规格及用量: 名称 规格 用量 KOH 固体 13.5g 苯甲醛 新蒸的 15mL 乙醚 —— 45mL NaHSO 3 饱和 10mL Na 2CO 3 10% 10mL MgSO 4 无水 —— 盐酸 浓 ——
