实验一 硫酸铝钾大晶体的制备

实验一、硫酸铝钾大晶体制备
一、实验目的
1、了解制备硫酸铝钾的原理及过程
2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体,学会及时处理问题的技能。实验中细致摸索条件。
3、熟练掌握溶解、结晶、抽滤等基本操作。
二、试剂
铝片、NaOH(S)、H 2SO 4(3mol/L ,1:1)、K 2SO 4 (S) 、 尼龙线
三、实验原理
1、KAl (SO4)2的制备
2、明矾籽晶培养
保持溶液在一个适当的过饱和度,在一定温度下通过溶剂蒸发使晶体析出,静置一段时间使籽晶形成完整晶型。
3、大晶体制备
通过加热与溶解调解母液的浓度及温度至合适的值,将饱和溶液在室温下静置,靠溶剂的自然挥发来创造溶液的准稳定状态,人工投放晶种让之逐渐长成单晶。
↑+→++2423)(2622H OH NaAl O H NaOH Al 4223424)(2 SO H 2NaAl(OH)SO Na O H OH Al ++?→?+O H SO Al OH Al SO H 23423426)()(23+→+O H SO KAl O H SO K SO Al 22424234212)(224)(?→++
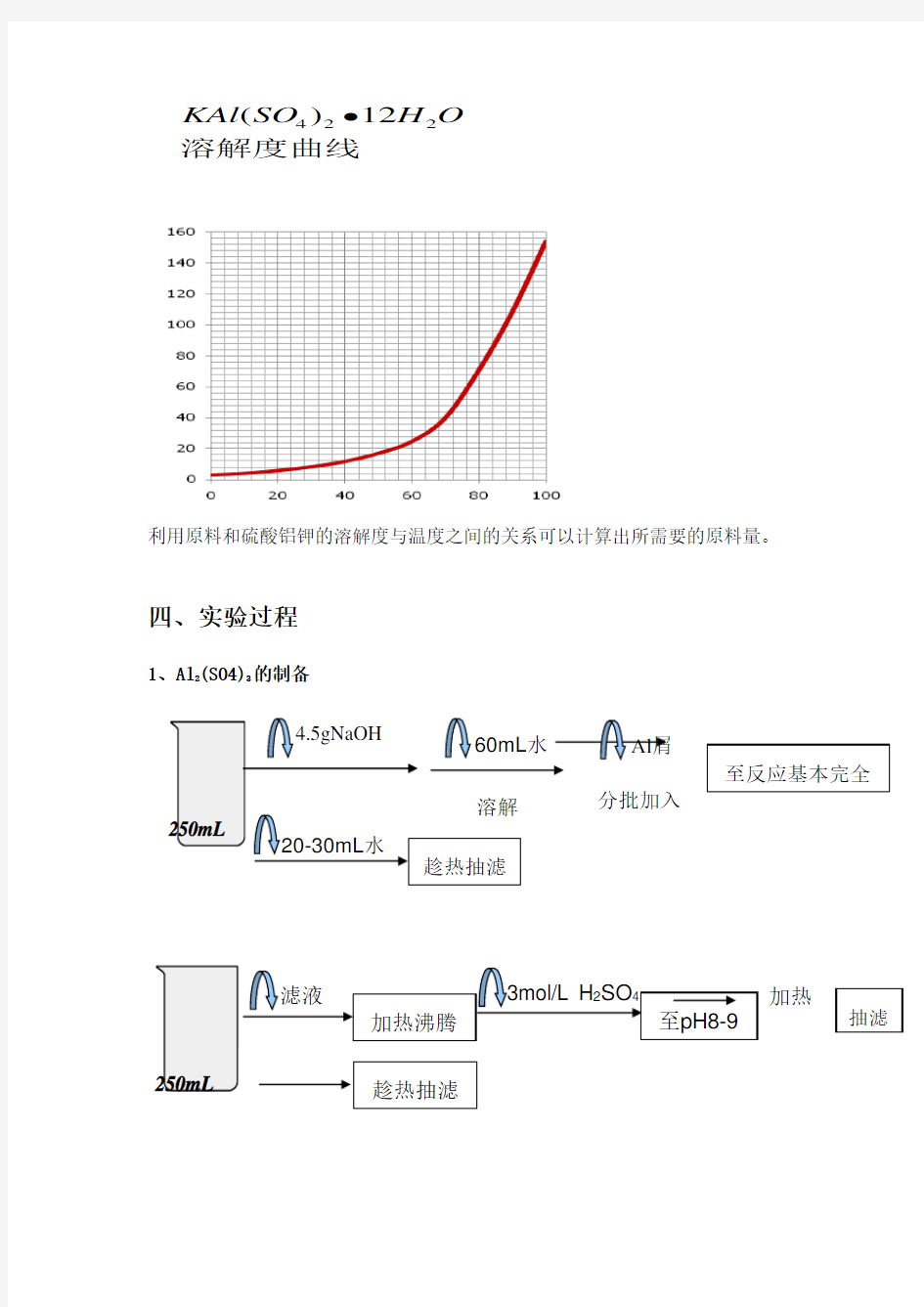
利用原料和硫酸铝钾的溶解度与温度之间的关系可以计算出所需要的原料量。
四、实验过程
1、Al 2(SO4)3的制备
溶解
250mL
4.5gNaOH
60mL 水 Al 屑
分批加入
至反应基本完全
20-30mL 水
趁热抽滤
250mL
滤液
3mol/L H 2SO 4
至pH8-9
趁热抽滤
加热沸腾
加热
抽滤
溶解度曲线
O H SO KAl 22412)(?
2. KAl(SO4)2·12H 2O 的制备
将Al 2(SO 4)3溶液与6.5g K 2SO 4 配成的饱和溶液相混合,搅拌均匀,充分冷却后,减压抽滤,尽量抽干,称量,计算产率(硫酸铝钾的理论产值为35.1g)。KAl(SO 4)2·12H 2O 易溶于水,抽滤时,不可再用水冲洗,以免损失KAl(SO 4)2·12H 2O 。
3.籽晶制备
I. 取20克产物放入烧杯中(在40摄氏度,一个标准大气压下,明矾溶解度
为11.7g),加入适量的水(理论值约为170ml ,实际加水约100mL ,若加水过多,蒸发结晶会比较耗时间)并加热至沸腾,在烧杯口上架一根玻璃棒,然后把一根尼龙线悬于溶液中间。 II. 把溶液置于不易振荡,易蒸发的地方,在烧杯口盖上一张滤纸以防止灰尘
的进入,静置1~2天。
III. 把线绳上较小,不规则的籽晶去掉,留下较大的,八面体形状的籽晶。
4.大晶体的培养
①把取出籽晶后的溶液加热,使烧杯底部的小晶体溶解,并持续加热一小段时间。 ②将溶液冷却至30~40℃,若溶液析出晶体,则过滤晶体,若溶液没有饱和则需加入 KAl(SO 4)2?12H 2O 再加热,直至把溶液配成30~40℃的饱和溶液。在此温度时有利于籽晶快速长大,同时不至于晶体在室温升高时溶解。 ③把籽晶轻轻吊在饱和液并处于溶液中间。
④多次重复①②③,直至得到无色、透明、八面体形状的硫酸铝钾大晶体。在晶体生长过程中,应经常观察,若发现籽晶上又长出小晶体,应及时去掉。若杯底有晶体析出也应及时滤去,以免影响晶体生长。
以下是在实验中的附图
铝与氢氧化钠的反应:
250m L
Al(OH)3
20mL 1:1H 2SO 4
Al 2(SO 4)3溶液
水浴加热
沉淀溶解
抽滤得到偏铝酸钠溶液
pH控制使氢氧化铝沉淀达到最大抽滤得到氢氧化铝沉淀
用浓硫酸溶解氢氧化铝并加入硫酸钾,得到硫酸铝钾晶体
实验结果
实验一-硫酸铝钾大晶体的制备
实验一-硫酸铝钾大晶体的制备
实验一、硫酸铝钾大晶体制备 一、实验目的 1、了解制备硫酸铝钾的原理及过程 2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体,学会及时处理问题的技能。实验中细致摸索条件。 3、熟练掌握溶解、结晶、抽滤等基本操作。 二、试剂 铝片、NaOH(S)、H 2SO 4(3mol/L ,1:1)、K 2SO 4 (S) 、 尼龙线 三、实验原理 1、KAl (SO4)2的制备 2、明矾籽晶培养 保持溶液在一个适当的过饱和度,在一定温度下通过溶剂蒸发使晶体析出,静置一段时间使籽晶形成完整晶型。 3、大晶体制备 通过加热与溶解调解母液的浓度及温度至合适的值,将饱和溶液在室温下静置,靠溶剂的自然挥发来创造溶液的准稳定状态,人工投放晶种让之逐渐长成单晶。 ↑+→++2423)(2622H OH NaAl O H NaOH Al 4223424)(2 SO H 2NaAl(OH)SO Na O H OH Al ++?→?+O H SO Al OH Al SO H 23423426)()(23+→+O H SO KAl O H SO K SO Al 22424234212)(224)(?→++
利用原料和硫酸铝钾的溶解度与温度之间的关系可以计算出所需要的原料量。 四、实验过程 1、Al 2(SO4)3的制备 溶解度曲线 O H SO KAl 22412)( ?
2. KAl(SO4)2·12H 2O 的制备 将Al 2(SO 4)3溶液与6.5g K 2SO 4 配成的饱和溶液相混合,搅拌均匀,充分冷却后,减压抽滤,尽量抽干,称量,计算产率(硫酸铝钾的理论产值为35.1g)。KAl(SO 4)2·12H 2O 易溶于水,抽滤时,不可再用水冲洗,以免损失KAl(SO 4)2·12H 2O 。 3.籽晶制备 I. 取20克产物放入烧杯中(在40摄氏度,一个标准大气压下,明矾溶解度 为11.7g),加入适量的水(理论值约为170ml ,实际加水约100mL ,若加水过多,蒸发结晶会比较耗时间)并加热至沸腾,在烧杯口上架一根玻 溶解 250mL 4.5gNaOH 60mL 水 Al 屑 分批加入 至反应基本完全 20-30mL 水 趁热抽滤 250mL 滤液 3mol/L H 2SO 4 至pH8-9 趁热抽滤 加热沸腾 加热 抽滤 250mL Al(OH)3 20mL 1:1H 2SO 4 Al 2(SO 4)3溶液 水浴加热 沉淀溶解
1生物学实验常用技术
生物学实验常用技术一、分子方面 1、基因工程 1)PCR (Polymerase Chain Reaction) (二楼PCR仪器全部会用) 2)RT-PCR;Q-PCR 3)琼脂糖凝胶电泳;胶回收 4)酶切/链接 5)转化 6)固体/液体LB培养基配制 (高压蒸汽灭菌锅使用方法) 7)质粒大/小抽原理及步骤 (手提、溶液I、II、III作用) 8)基因组DNA抽提 9)RNA提取; 2、蛋白质工程 1)蛋白收集 (蛋白裂解液+PMSF; 1×Loading 裂解(推荐)) 2)SDS-PAGE(电泳胶的配制) 2)考马斯亮蓝染色,银染 3)Western blot 4)蛋白定量常用的方法及原理, 以及熟练操作Bradford法蛋 白定量 (TRIZOL法原理、注意事项及步骤) 二、细胞方面 1)细胞培养、传代 2)细胞冻存与复苏 冻存液配制: (1)DMSO:血清=1:9(推荐)
(2)DMSO:培养基:血清=1:3:6 均可 DMSO为细胞专用型;现用现配,效果最好;冻存时细胞在-80℃中不要超过一周,最好在24-48h内放入液氮罐中保存。 3)细胞培养基配制(过滤除菌)、胰酶配制(过滤除菌),PBS配制(灭菌);(不同培养基的区别;谷氨酰胺(提供氮源),2周补充一次) 4)转染 5)MTT原理及操作(检测细胞存活率或死亡率) 6)碱性磷酸酶实验(ALP,检测细胞分化) (5、6 需学会SPSS软件及graphpad prism5软件使用) 7)Hoechst染色 8)结晶紫染色(不推荐) 9)苏木精/伊红染色 (9可以替代8,以后实验推荐使用9,图片漂亮) 10)荧光显微镜的使用 11)激光共聚焦显微镜样品制备(细胞固定,染色,洗脱) (7、8、9、10、11需学会Photoshop常用工具处理数据) 12)流式细胞仪样品制备(包括:转染效率与细胞凋亡染色标记)以及仪器操作(需学会FlowJo软件分析流式结果) 三、动物实验 1)小鼠的定制: 常见的小鼠: ICR小鼠(正常),9元/只
分组实验:硫酸铜晶体的制备和生长
分组实验:硫酸铜晶体的制备和生长 1.一定温度下,向饱和硫酸铜溶液中加入少量硫酸铜晶体,如图所示。所得溶液与原溶液相比(D) 饱和硯战铜溶液 硫酸铜晶怵 (第 1 题) A.溶剂的质量增加,颜色变浅 B.溶质溶解度不变,颜色变深 C.溶质的质量增加,颜色变深 D.溶质溶解度不变,颜色不变 2.硫酸铜 晶体含有结晶水,食盐没有结晶水,则暴露在空气中比较稳定的是(B)A.硫酸铜B.食盐 C.硫酸铜和食盐 D.无法确定 3.在“冷却热饱和溶液来制备硫酸铜晶体”的实验中需要用到的仪器是(B) A.铁架台、铁圈、烧杯、漏斗、玻璃棒、滤纸 B.烧杯、温度计、玻璃棒、酒精灯 C.铁架台、铁夹、铁圈、石棉网 D.冷凝管、酒精灯、蒸发皿、接收管 4.在t C时的硫酸铜饱和溶液中加入x克无水硫酸铜,可析出y克硫酸铜晶体。则x的差值表示的意义是(D) A.表示原溶液损失的溶剂质量 B.表示原溶液损失的溶质质量 C.表示原溶液增加的溶质质量 D.表示原溶液损失的饱和溶液的质量 5.实验一:用滴管吸取饱和蔗糖水溶液,将其滴在玻璃片上,放置在空气中晾干,观察实验现象。 实验二:在30毫升沸水中不断加入硝酸钾至不再溶解为止,将上层热的饱和溶液倒入另一只烧杯里,把盛有热饱和溶液的烧杯放在冷水中降温(如图所示),观察实验现象。 (第5题)
通过实验一和实验二的描述可知,使晶体析出通常有蒸发溶剂和冷却热饱和溶液两种方
法。 6.在20 C时,把5克硫酸铜晶体(CuS04 ? 5H2O)溶于95克水中,所得溶液的溶质质量分数(C) A.等于5% B.大于5% C.小于5% D.无法确定 【解析】5克硫酸铜晶体溶于水后,其中的结晶水变为溶剂,因此溶质小于5克。溶 液质量不变,所以溶质质量分数小于
晶体材料制备原理与技术
中国海洋大学本科生课程大纲 课程属性:公共基础/通识教育/学科基础/专业知识/工作技能,课程性质:必修、选修 一、课程介绍 1.课程描述: 晶体材料制备原理与技术是综合应用物理、化学、物理化学、晶体化学、材料测试与表征等先修课程所学知识的应用型专业课程,主要讲授晶体材料制备过程的基本原理和典型的晶体材料制备技术,为学生从事晶体材料制备工作提供理论基础和技术基础。 2.设计思路: 晶体材料是高新技术不可或缺的重要材料,晶体材料制备是材料科学与工程专业相关的重要生产领域。作为一门以拓展学生知识面为目的的选修课程,本课程分为三大部分:首先介绍典型的晶体材料制备方法和技术,通过课下查阅资料和课堂讨论加深学生对常见方法和技术的理解。此部分教师讲解和学生课堂讨论并重。然后介绍晶体材料制备过程中的一般原理,此部分主要由教师进行课堂讲授。最后,由学生自主查阅晶体材料制备最新文献,了解晶体材料制备技术最新进展,通过课下研读、课上汇报、讨论、教师点评等教学活动,加深学生对本课程中所学知识的理解及相关知识的综合运用。 - 3 -
3. 课程与其他课程的关系: 晶体材料制备原理与技术是综合应用物理、化学、物理化学、晶体化学、材料测试与表征等先修课程所学知识的应用型专业课程,是材料制备与合成工艺课程相关内容的细化和深入。 二、课程目标 本课程的目标是拓宽材料科学与工程专业学生的知识面,掌握晶体材料制备一般原理,了解晶体材料制备常见技术,加深对物理、化学、晶体化学以及材料表征等先修课程知识的理解,加强文献检索能力,学会分析晶体材料制备中遇到的问题,提高解决生产问题的能力,为毕业后从事晶体材料制备等生产和研究工作打下基础。 三、学习要求 晶体材料制备原理与技术是一门综合了物理、化学、物理化学、晶体化学、材料测试与表征等多学科知识的综合性课程。为达到良好的学习效果,要求学生:及时复习先修课程相关内容,按时上课,上课认真听讲,积极查阅资料,积极参与课堂讨论。本课程将包含较多的资料查阅、汇报、讨论等课堂活动。 四、教学进度 - 3 -
制备大晶体
制备大晶体 1概论 原理:利用不同物质溶解度随温度变化而产生不同变化的原理对物质进行分离,得到所需产品。 过程:晶核生成和晶体生长 仪器:布氏漏斗,抽滤瓶,电炉,蒸发皿,烧杯,玻璃棒, 方法 2蒸发结晶 定义:加热蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出 试用范围:溶解度随温度变化不大的物质 典型事例:Nacl 晶体的析出 操作过程:在蒸发皿中进行,蒸发皿放于铁架台的铁圈上,倒入液体不超过蒸发皿容积的2/3,蒸发过程中不断用玻璃棒搅拌液体,防止受热不均,液体飞溅。看到有大量固体析出,或者仅余少量液体时,停止加热,利用余热将液体蒸干。
注意事项及提高产率的方法:1保证要结晶的物质溶解度随温度都变化要大 2利用余热蒸发剩余的晶体有助于节约能源 2 冷却结晶 定义:即蒸发浓缩,冷却结晶,指在温度比较高的情况下饱和的溶液将其温度降低,使其析出晶体的过程。 适用范围:适用于溶解度随温度的升高而明显增大的物质。 典型事例:我们这两次做的硫酸亚铁铵晶体的制备 操作过程:先将溶液倒入蒸发皿中,水浴加热至溶液饱和,略微有固体析出(硫酸亚铁铵制备过程中是形成一层晶体膜,而硫酸四铵合铜制备过程中是有蒸气出现即可),然后盖上表面皿,冷却一段时间,待有大量晶体析出时进行抽滤即可。 蒸发浓缩冷却结晶 注意事项及提高产率的方法: 1要保证配合物配位数的一定,如硫酸四铵合铜中铵的系数是4,即配位数是四 2可以通过改变溶剂环境来改变溶解度的差,提高产率,如制备硫酸四铵合铜的过程中加入95%的氨水 3结晶开始后,溶液温度最好也不要太高,最好不要超过60度,建议40~50度(比室温高20度)
分子生物学实验技术考试题库
一、名词解释 1.分配常数:又称分配系数,是指一种分析物在两种不相混合溶剂中的平衡常数。 2.多肽链的末端分析:确定多肽链的两末端可作为整条多肽链一级结构测定的标志,分为氨基端分析和羧基端分析。 3.连接酶:指能将双链DNA中一条单链上相邻两核苷酸连接成一条完整的分子的酶。 4.预杂交:在分子杂交实验之前对杂交膜上非样品区域进行封闭,用以降低探针在膜上的非特异性结合。 5.反转录PCR:是将反转录RNA与PCR结合起来建立的一种PCR技术。首先进行反转录产生cDNA,然后进行常规的PCR反应。 6.稳定表达:外源基因转染真核细胞并整合入基因组后的表达。 7.基因敲除:是指对一个结构已知但功能未知或未完全知道的基因,从分子水平上设计实验,将该基因从动物的原基因组中去除,或用其它无功能的DNA片断取代,然后从整体观察实验动物表型,推测相应基因的功能。 8.物理图谱:人类基因组的物理图是指以已知核苷酸序列的DNA片段为“路标”,以碱基对(bp,kb,Mb)作为基本测量单位(图距)的基因组图。 9.质谱图:不同质荷比的离子经质量分析器分开后,到检测器被检测并记录下来,经计算机处理后所表示出的图形。 10.侧向散射光:激光束照射细胞时,光以90度角散射的讯号,用于检测细胞内部结构属性。
11.离子交换层析:是以离子交换剂为固定相,液体为流动相的系统中进行的层析。 12.Edman降解:从多肽链游离的N末端测定氨基酸残基的序列的过程。 13.又称为限制性核酸内切酶(restriction endonuclease):是能够特异识别双链DNA序列并进行切割的一类酶。 14.电转移:用电泳技术将凝胶中的蛋白质,DNA或RNA条带按原位转移到固体支持物,形成印迹。 15.多重PCR:是在一次反应中加入多对引物,同时扩增一份模板样品中不同序列的PCR 过程。 16.融合表达: 在表达载体的多克隆位点上连有一段融合表达标签(Tag),表达产物为融合蛋白(有分N端或者C端融合表达),方便后继的纯化步骤或者检测。 17.同源重组:发生在DNA同源序列之间,有相同或近似碱基序列的DNA分子之间的遗传交换。 18.遗传图谱又称连锁图谱(linkage map),它是以具有遗传多态性的遗传标记为“路标”,以遗传学距离为图距的基因组图。 19.碎片离子:广义的碎片离子为由分子离子裂解产生的所有离子。 20.前向散射光:激光束照射细胞时,光以相对轴较小角度向前方散射的讯号用于检测细胞等离子的表面属性,信号强弱与细胞体积大小成正比。 21.亲和层析:利用共价连接有特异配体的层析介质分离蛋白质混合物中能特异结合配体的目的蛋白或其他分子的一种层析法。(利用分子与其配体间特殊的、可逆性的亲和结合
制取硫酸铜晶体实验报告
制取硫酸铜晶体实验报告 .、八、- 刖言 冷却热的硫酸铜饱和溶液可以得到硫酸铜晶体,但晶体析出的情况、形状大小都会因实验用品的差异、实验过程中的变量有所不同。在本次实验中,我们通过参照初三化学【下册】课本 P40中明矶晶体的制取方法和借鉴往届学生制作硫酸铜晶体的经验,结合网上查找到的相关资料,进行制取硫酸铜晶体的实验,共耗时10天才成功完成。 一、实验仪器、药品、材料 线圈,碗一个,硬纸片一张、硫酸铜粉末若干。 二、实验步骤 1.在烧杯中放入比室温高10?20C的水,并加入足量硫酸铜; 2.用筷子搅拌,直到有少量晶体不能再溶解; 3?待溶液自然冷却到比室温略高3?5 C时,把模型放入碗中; 4.用硬纸片盖好,静置一夜; 5.取出线圈后往烧杯中加入温水,使其成为比室温高10?15°C的溶液,并补充适量硫 酸铜,使其饱和; 6.用硬纸片盖好,静置过夜;每天观察,重复5、6项的操作过程。 7.三、实验注意 1.所用试剂必须纯净,如含有杂质就很难获得完整的晶形。 2.控制溶液的浓度,如果溶液过浓,析晶速率太快,不易形成晶形完整的晶体;如 超过饱和溶液浓度不大,结晶速率太慢,小晶体慢慢长大。制备小晶体时,用高于室温 20C?30C的饱和溶液;以后添加的饱和溶液应是高于室温15C?20C的溶液,每次加入量约为原溶液的1/10,添加时要把晶体取出,等溶液温度均匀后再把晶体浸入。 3.注意环境温度的变化,应使饱和溶液缓慢冷却,可用布或棉花把烧杯包好。白天温 度较高时可把晶体取出,到晚上再放回溶液中。 4.所用容器必须洁净,要加盖以防灰尘落入。 四、实验过程 五、实验结论 (1)硫酸铜的溶解度随着温度的升高而增大,通过严格控制温度的变化,有利于加快晶 体的成形速率; (2)使用铁丝作为模型,不能使硫酸铜饱和溶液结晶,因为Fe的金属活动性比Cu强,能
制取硫酸铜大晶体探究实验报告
制取硫酸铜大晶体实验探究报告 学校:广州大学附属中学 班级:初三(4)班 组员:丘子贞、郑康维、谢广俊 作品名称:《蓝色妖姬》
实验名称:制取硫酸铜大晶体实验探究 实验目的:①培养化学实验中的动手能力和简单分析能力 ②探究如何制取形状规则的硫酸铜大晶体 实验用品:250ml烧杯两个、碗、玻璃棒、医用纱布、小水盆、保鲜膜、棉线、头发、笔、小刀、小盒子、透明指甲油、五水硫酸铜(分析纯)试剂一瓶(500g/瓶) 前期实验记录(准备期):
后期实验记录(培养期):
①晶体表面突起的薄片状小晶体被轻易切除 ③打磨晶体后刀刃变浅红,现疑似铁锈的痕迹。 ④晶体继续按菱形轮廓慢慢生长。 晶体慢慢长大。到第7天时晶体长约4.5cm。 几天后晶体表面开始泛白,再具有光泽。 几天后晶体仍保持原有光泽。
实验结论: 硫酸铜晶体的形状是一定的,但是在实际培养过程中,由于实验设备有限和外界影响等各种因素,想要培养出完全规则的硫酸铜晶体非常困难。我们只能尽自己所能,培养出形状相对规则的硫酸铜晶体。 实际形成的晶体形状受多方面因素的影响。经过归纳总结,想要培养出形状相对规则的硫酸铜晶体,在操作过程中需要注意以下几点: ①尽量挑选形状完整的小晶体作为晶核; ②使用头发绑晶核; ③等待热饱和溶液完全冷却并进行过滤后再把晶核放入; ⑤在溶液析晶的过程中要意防震防尘; ⑥取出晶体后要及时清理晶体上的各种突起。 制取硫酸铜晶体是一个繁琐的过程,只有具有持之以恒的毅力和耐心的操作,才有可能培养出理想的晶体。 实验体会: Part1:做探究实验最重要的就是多做对比实验。在实验过程中,我们应多留意细微的现象,做好实验记录并进行简单分析。遇到不懂的问题要及时通过咨询老师、查阅资料等方法解决。只有具有格物致知的精神和勤于动手动脑的意识,我们才能在实践中逐步提高自己的动手能力和分析能力。 Part2:本次探究实验耗时近一个月,期间我们因经验不足、操作疏忽等因素,经历了数十次失败。但我们不抛弃不放弃、不断总结经验,最终取得了一定的实验成果。这次探究实验经历也让我们懂得了:任何的成功都需要科学的方法和不懈的坚持。 改进建议: ①着手做实验前应先查阅大量资料,多向有经验的前辈请教,以免在实验前期因经验 不足耗费大量时间; ②实验过程中应更加严格把控外界因素介入,以免影响晶体生长; ③实验过程中应更勤于拍照记录。 成果展示: 作品名称:蓝色妖姬
本科生六个基本生物学实验
实验一:感受态细胞的制备 1.原理: 当实验室获得了一个新的质粒时,而这个质粒并未转化到宿主菌体内,则需要该技术进行细菌的转化,以大量获得这一质粒。转化细菌的方式有很多种,如电转化法、脂质体转染法、显微注射法、CaCl2处理法制备感受态细胞等。一般的实验室都应用CaCl2处理细菌,改变细胞膜的结构,使质粒DNA能穿过细菌细胞膜进入细胞。然后在选择培养基中培养转化处理过的细菌,转化成功的细菌可在抗菌素培养基上生长形成菌落。这一方法是分子生物学常用实验方法。 2.实验材料 2.1LB液体培养基 2.20.1mol/L CaCl2溶液:称取1.1g无水CaCl2,溶于90ml双蒸去离子水中, 定容至100ml,用0.22μm滤器过滤并装入灭菌试剂瓶中,4℃保存。 2.3 DH5α菌株,冰,牙签,无菌滤纸,50ml离心管,枪头(以上需灭菌); 移液器,摇床,冷冻离心机,涡旋震荡器,恒温摇床,恒温培养箱,超净工作台,普通冰箱,-70℃冰箱 3.操作方法 3.1从37℃培养12—16h的平板上,用无菌牙签挑取一个单菌落,转移到含有3ml LB培养基的试管内,37℃振摇过夜。次日取菌液1ml,接种到含有100ml LB培养基的500 ml烧瓶中,37℃剧烈振摇培养约2—3h(振摇速度为200—300r/min),待OD600值达到0.3—0.4时,将烧瓶取出立即置冰浴10—15min。 3.2自该步骤起皆需无菌操作。在无菌条件下将细菌转移到一个灭菌处理过的、冰预冷的50 ml离心管中。 3.34℃离心,4000g×5min回收细胞。 3.4弃去培养液,将离心管倒置于滤纸上1min,以使最后残留的培养液流尽。 3.5加入冰预冷的0.1mol/L CaCl2溶液10ml重悬菌体,置冰浴30min。 3.64℃离心,4000g×5min,弃去上清液,倒置于滤纸1min。 3.7再加4ml用冰预冷的0.1mol CaCl2重悬菌体(重悬时操作要轻)。 3.8置4℃冰箱置12—24h,即可应用于转化。 思考题: 制备感受态细胞时加入CaCl2的作用是什么? 钙离子结合于细胞膜上,使细胞膜呈现一种液晶态。在冷热变化刺激下液晶态的细胞膜表面会产生裂隙,细胞膜的通透性发生变化,使外源DNA进入。
小学科学-硫酸铜晶体制作
设备:100ml玻璃容器200ml烧杯搅拌棒加热装置一个密封塑料瓶漏斗滤纸等 STEP1你需要购买硫酸铜(分析纯)试剂 称取室温下溶解度多3g左右的硫酸铜,溶于100ml热水中(实验中所用的水不能是自来水,可以是饮用水,推荐屈臣氏蒸馏水),搅拌使其完全溶解。倒入干净的玻璃容器中,盖上盖子,静置一天 STEP4 如果你发现完全冷却后,容器底部有大量碎晶,没有完整的小晶体,那就重复STEP3,原因可能是冷却过快、水中有杂质或者在冷却过程中频繁扰动溶液。如果你得到了几个完整的小晶体(称为晶核)那请进行下一步 STEP5 得到了晶核,你就可以真正开始你的晶体培养了!首先你要配置较大量的饱和溶液(也就是溶解固体达到最大无法继续再溶的溶液)(200ml),当然你上一步剩余的溶液应该并入此步骤的溶液中。具体的配置常温饱和溶液的方法是:称取室温下溶解度多2g左右的硫酸铜,溶解在200ml热水中,完全冷却后过滤(这一步你也可能得到好的晶核),保留滤液,剩余的固体放入一个密封塑料瓶中,放入水。这个塑料瓶的目的是保存你以后分离得到的硫酸铜固体,并且可以同时得到室温下的饱和硫酸铜溶液。 STEP6 晶体培养一般有两种方法:杯底或者悬挂。如果你不想用细线挂住晶体,那么可以采用直接把晶核放在杯底的方法,但这种方法对硫酸铜来说会影响晶体的形状,所以建议采用悬挂的方法。(当然你也可以两种方法都试一试)将一个稍大一点的晶核(1-2cm)用细线栓紧,系死扣,并且将线的另一端系在一个细竹签上。系晶体的标准是:不能让晶体在自然状况下掉落,线长应该满足晶体全部浸入烧杯液面以下。 STEP7 系好了晶体,不要忙着放入溶液。因为这时你的溶液可能混入了大量的杂质,空气中的毛发、灰尘等,需要先进行过滤。(如果你的设备有限,可以不进行这一步,但一定要减少灰尘进入) STEP8 将拴好的晶核放入溶液,静置。盖上透气防尘的盖子(或者蒙上一层卫生纸) STEP9 如果发现杯底有小晶体出现,在不触碰到晶核的情况下可以先忽视,但如果碎晶很多,就需要及时清理。如果发现杯壁有攀援的晶体层,一定要及时小心清除。为了减少这种现象的发生,你在每次配置好饱和溶液准备静置的时候应该把烧杯壁上的硫酸铜液滴擦掉。如果在蒸发一段时间后溶液过少,应该添加常温下饱和溶液。 STEP10 这样放置一段之间,晶体长到足够大时,就可以取出晶体了。 STEP11保存需要涂上一层清漆或透明的指甲油。
大学化学实验 五水硫酸铜的制备
实验二五水硫酸铜的制备 一.实验目的 1. 学习由不活泼金属与酸作用制备盐的方法及重结晶法提纯物质。 2.练习和掌握台天平、蒸发皿、坩埚钳、表面皿的使用。 3.学会倾滗法,减压过滤,溶解和结晶;固体的灼烧。 二.实验原理 1.制备原理:Cu + 2HNO3 + H2SO4 =CuSO4 +2NO2(↑) + 2H 2O CuSO4 +5H2O = CuSO4·5H2O 铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到产物硫酸铜。 2.提纯原理: 未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在273K~373K范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩后析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。 硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过
滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。
T/K273293313333353373 五水硫酸 23.132.044.661.883.8114.0 铜 硝酸铜83.5125.0163.0182.0208.0247.0 三.主要仪器与试剂 1 仪器烧杯量筒热过滤漏斗减压过滤装置台称坩埚钳,蒸发皿。 2 试剂Cu (s) 、H2SO4、HNO3(2.5mol/L; 0.5mol/L) 四.操作步骤
五.实验结果及分析 结果:1.上述得到的粗产品的重量为:5.30g 2.重结晶后得到的产品重量为:2.39 g 分析:1. Cu —CuSO4 —CuSO4·5H2O(s) 64 160 250 1.5g 3.75g 5.86g 产率= 5.30g/5.86g×100% = 90.4% 2.理论重结晶率为:(8 3. 8g-27.5g)/83.8*100%=67.2% 实际重结晶率为:2.39 / 5.30 * 100% = 45.1% (在283K与353k时的溶解度分别为27.5g/100g水、83.8g/100g水) 六.讨论 ●:1.列举从铜制备的其他方法,并加以评述。 答:由铜制备硫酸铜时铜的价态升高了,因此各种制备方法的共同点是找一个氧化剂。氧化剂不同,制备上有差异,因此,每一种制备方法均有优缺点,请根据此思路考虑其他制备方法。同样由铜制备氯化铜、醋酸铜的关键也是找氧化剂,只是酸根不同而已。
硫酸铜晶体制作
以硫酸铜晶体制作为例研究人类行为活动和思想感对 周围无机环境的直接影响 作者单位:北京市第十七中学 作者:杜博文董磊 指导教师:蒋金海刘莉李锐 主题词:硫酸铜制作人类情感影响
内容提要 我们在上网查询的时候,发现有人做出这样的结论,在晶体结晶的过程中因为施加了感情因素,例如:谩骂、讽刺、表彰等,晶体的结晶出现明显不同,硫酸铜是一种晶体,我们希望通过我们的猜想证实或者证伪这种结论,从而得到一个更加符合实际的结果。此外我们通过改变其他的因素,如同噪音、轻音乐等来看一看外界环境对硫酸铜晶体制作中的影响,从而得出相应的结论。 中学化学是一门重要的课程,我们的研究方法将会找到一种有趣的实验方法,改变学习化学抽象、枯燥的方式,为学生学习化学提供一种动手与动脑的相结合的学习方式。
以硫酸铜晶体制作为例研究人类行为活动和思想感情对周围无机 环境的直接影响 序言 人的行为活动会改变周围的环境,如植物的生长,动物的繁殖……使相关环境条件为人类服务。那都是通过一定的科学技术利用已探求出的物理公式,化学变化,数学规律来实现的。那么人类的行为活动和思想感情会不会对周围无机环境有直接影响呢?在科幻故事中经常出现以人的念力(即人的思想)改变外界环境的情节。在人类理想化的生活中也希望可以凭思想来代替机械运动。由此我们以硫酸铜晶体制作过程利用不同人为活动的变化来研究人类行为活动和思想感情对非生物物质的影响。 我们所进行的实验有以下几个特点:实验仪器来源于中学实验室,简单易得;所选用的药品(即硫酸铜)成本较低;使学生在实践中充分利用书本知识,对中学教学有巨大意义;实验过程由学生自主设计,从中体会科学研究过程;所得数据真实,有全过程记录(图片,文字记录)。 二研究的问题 [提出问题] 1选取硫酸铜晶体制作过程的哪一步。 2如何控制试验中的变量(即不同条件)。 3如何使此实验中的对象不变条件完全相同。 4选取人类活动和思想感情中的什么行为(感情)进行实验研究。
硫酸铜的制备及结晶水的测定_
硫酸铜的制备及结晶水的测定一、实验目的 1.掌握利用废铜粉制备硫酸铜的方法; 2.练习减压过滤、蒸发浓缩和重结晶等基本操作;3.了解结晶水的测定方法,认识物质热稳定性和分子结构的关系。
二、实验原理 利用废铜粉灼烧氧化法制备CuSO 4·5H 2O :先将铜粉在空气中灼烧氧化成氧化铜,然后将其溶于硫酸而制得: 2Cu + O 2=== 2CuO (黑色) CuO + H 2SO 4=== CuSO 4+ H 2O 由于废铜粉不纯,所得CuSO 4溶液中常含有不溶性杂质和可溶性杂质FeSO 4、Fe 2(SO 4)3及其它重金属盐等。Fe 2+离子需用氧化剂H 2O 2溶液氧化为Fe 3+离子,然后调节溶液pH ≈4.0,并加热煮沸,使Fe 3+离子水解为Fe(OH)3沉淀滤去。其反应式为 2Fe 2++ 2H ++ H 2O 2=== 2Fe 3++ 2H 2O Fe 3++ 3H 2O === Fe(OH)3↓+ 3H +
CuSO 4·5H 2O 在水中的溶解度,随温度的升高而明显增大,因此粗硫酸铜中的其它杂质,可通过重结晶法使杂质在母液中,从而得到较纯的蓝色水合硫酸铜晶体。水合硫酸铜在不同的温度下可以逐步脱水,其反应式为 CuSO 4·5H 2O === CuSO 4·3H 2O + 2H 2O CuSO 4·3H 2O === CuSO 4·H 2O + 2H 2O CuSO 4· H 2O === CuSO 4+ H 2O 1 mol CuSO 4结合的结晶水的数目为:24 H O CuSO n n
三、实验仪器及试剂 托盘天平,瓷坩埚,泥三角,酒精灯,烧杯(50mL),电炉,布氏漏斗,吸滤瓶,精密pH试纸,蒸发皿,表面皿,水浴锅,量筒(10mL)。 废铜粉, H 2SO 4 (2mol·L-1), H 2 O 2 (3%), K 3[Fe(CN) 6 ](0.1mol·L-1), NaOH(2mol·L-1),无水乙醇。
材料常用制备方法
材料常用制备方法
材料常用制备方法 一.晶体生长技术 1.熔体生长法【melt growth method】(将欲生长晶体的原料熔化,然后让熔体达到一定的过冷而形成单晶) 1.1 提拉法 特点:a. 可以在短时间内生长大而无错位晶体 b.生长速度快,单晶质量好 c.适合于大尺寸完美晶体的批量生产 1.2 坩埚下降法 特点:装有熔体的坩埚缓慢通过具有一定温度梯度的温场,开始时整个物料熔 融,当坩埚下降通过熔点时,熔体结 晶,随坩埚的移动,固液界面不断沿 坩埚平移,至熔体全部结晶。 1.3 区熔法 特点:a.狭窄的加热体在多晶原料棒上移动,在加热体所处区域,原料变成熔 体,该熔体在加热器移开后因温度下 降而形成单晶
c.外延层的表面形貌一般不如气相外延的好。 2. 溶液生长法【solution growth method】(使溶液达到过饱和的状态而结晶) 2.1 水溶液法 原理:通过控制合适的降温速度,使溶液处于亚稳态并维持适宜的过饱和度,从而结晶 2.2 水热法【Hydrothermal Method】 特点:a. 在高压釜中,通过对反应体系加 热加压(或自生蒸汽压),创造一个 相对高温高压的反应环境,使通常难 溶或不溶的物质溶解而达到过饱和、 进而析出晶体 b. 利用水热法在较低的温度下实现 单晶的生长,从而避免了晶体相变引 起的物理缺陷 2.3 高温溶液生长法(熔盐法) 特点:a.使用液态金属或熔融无机化合物作为溶剂 b.常用溶剂: 液态金属 液态Ga(溶解As)
Pb、Sn或Zn(溶解S、Ge、GaAs) KF(溶解BaTiO3) Na2B4O7(溶解Fe2O3) c.典型温度在1000 C左右 d.利用这些无机溶剂有效地降低溶 质的熔点,能生长其他方法不易制备 的高熔点化合物,如钛酸钡BaTiO3二.气相沉积法 1. 物理气相沉积法(PVD)【Physical Vapor Deposition】 1.1 真空蒸镀【Evaporation Deposition】 特点:a.真空条件下通过加热蒸发某种物质使其沉积在固体表面; b.常用镀膜技术之一; c.用于电容器、光学薄膜、塑料等的镀膜; d.具有较高的沉积速率,可镀制单质和不易热分解的化合物膜 分类:电阻加热法、电子轰击法 1.2 阴极溅射法(溅镀)【Sputtering Deposition】 原理:利用高能粒子轰击固体表面(靶材),
实验一 硫酸铝钾大晶体的制备
实验一、硫酸铝钾大晶体制备 一、实验目的 1、了解制备硫酸铝钾的原理及过程 2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体,学会及时处理问题的技能。实验中细致摸索条件。 3、熟练掌握溶解、结晶、抽滤等基本操作。 二、试剂 铝片、NaOH(S)、H 2SO 4(3mol/L ,1:1)、K 2SO 4 (S) 、 尼龙线 三、实验原理 1、KAl (SO4)2的制备 2、明矾籽晶培养 保持溶液在一个适当的过饱和度,在一定温度下通过溶剂蒸发使晶体析出,静置一段时间使籽晶形成完整晶型。 3、大晶体制备 通过加热与溶解调解母液的浓度及温度至合适的值,将饱和溶液在室温下静置,靠溶剂的自然挥发来创造溶液的准稳定状态,人工投放晶种让之逐渐长成单晶。 ↑+→++2423)(2622H OH NaAl O H NaOH Al 4223424)(2 SO H 2NaAl(OH)SO Na O H OH Al ++?→?+O H SO Al OH Al SO H 23423426)()(23+→+O H SO KAl O H SO K SO Al 22424234212)(224)(?→++
利用原料和硫酸铝钾的溶解度与温度之间的关系可以计算出所需要的原料量。 四、实验过程 1、Al 2(SO4)3的制备 溶解 250mL 4.5gNaOH 60mL 水 Al 屑 分批加入 至反应基本完全 20-30mL 水 趁热抽滤 250mL 滤液 3mol/L H 2SO 4 至pH8-9 趁热抽滤 加热沸腾 加热 抽滤 溶解度曲线 O H SO KAl 22412)(?
生物学基础实验技能讲义
生物学基础实验技能 实验讲义 王玉倩冯晓英郭娟张潮汤晓辛唐婧编 贵州师范大学生命科学学院 2012年6月
目录 一、显微操作 (2) 实验一显微镜的使用方法与绘图 (2) 实验二简单临时装片的制作与观察,油镜的使用 (6) 实验三压片的制作,涂片的制作 (8) 实验四生物材料的解剖结构观察 (10) 二、溶液配制 (11) 实验五玻璃器皿的洗涤 (11) 实验六、溶液的配制Ⅰ (13) 实验七、溶液的配制Ⅱ (15) 实验八溶液pH值的调节 (18) 三、分光光度计的使用 (20) 实验九分光光度法的介绍及分光光度计的使用方法 (20) 实验十混合物中CuSO4的测定 (24) 实验十一分光光度法测定叶绿素的含量 (26) 四、无菌操作 (28) 实验十二无菌操作技术 (28)
一、显微操作 实验一显微镜的使用方法与绘图 一、实验目的 1、掌握显微镜的构造及原理,熟练使用光学显微镜。 2、了解显微镜使用的基本要求、注意事项及一般维护方法。 3、学习生物绘图的基本要求及方法。 二、实验原理 显微镜的原理是经过两次成像,成为倒立的虚像。第一次先经过物镜成像,在物镜的一倍焦距和两倍焦距之间成放大的倒立的实像。第一次成的物像,经过目镜的第二次成像,是一个虚像。倒置的像常常使初学者使用发生困难。 1、显微镜的构造 机械部分 (1) 镜座 显微镜最下面呈马蹄形或园形的部分,起稳定和支持镜身作用。 (2) 镜柱 从镜座向上直立的短柱。上连镜臂,下连镜座,可以支持镜臂和载物台。 (3) 镜臂 弯曲成马蹄形的部分,便于手持,下端与镜柱相连接的地方有一个倾斜关节,可使镜臂倾斜,便于观察。 (4) 载物台 自镜臂下端向前伸出,放置标本用的平台,其中央有一个园孔,叫通光孔。台上有一移动器(老式的左右各有一个压片夹),用以固定和移动标本。 (5) 镜筒 和镜臂上方连接的园筒部分。有的显微镜镜筒内有一抽管,可适当抽长,一般长度是160-170毫米。镜筒上端装有目镜,下端有一个可转动的园盘,叫物镜转换器(或叫物镜旋转盘,固着在镜筒下端,分两层,上层固着不动,下层可自由转动。转换器上有2~4个圆孔,用来安装不同倍数的低倍或高倍物镜)。作用是保护成像的光路与亮度。 (6) 调节器(也叫调节螺旋) 为镜壁上两种可转动的螺旋,一大一小,能使镜筒上下移动,调节焦距。大的叫粗准焦螺旋,位于镜臂的上方,可以转动,以使镜筒能上下移动,从而调节焦距,升降镜筒较快,用于低倍镜对焦;小的叫细准焦螺旋,位于镜臂的下方,它的移动范围较粗准焦螺旋小,升降镜筒较慢,可以细调焦距。 (7) 倾斜关节 镜柱和镜臂交界处有一个能活动的关节。它可以使显微镜在一定的范围内后倾(一般倾斜不得超过45°)便于观察。但是在使用临时封片观察时,禁止使用倾斜关节,尤其是装片内含酸性试剂时严禁使用,以免污损镜体。 (8) 载物台 从镜臂向前方伸出的金属平台。呈方形或圆形,是放置玻片标本的地方。其中央具有通光孔,在通光孔的左右有一个弹性的金属压片夹,用来压住载玻片。较高级的显微镜,在载物台上常具有推进器,它包括夹片夹和推进螺旋,除夹住切片外,还可使切片在载物台上移
硫酸铜晶体制作方法图文整理
首先您所需的设备:100ml的玻璃容器200ml烧杯搅拌棒能提供热水的装置一个密封塑料瓶漏斗滤纸等 STEP1您需要购买硫酸铜(分析纯)试剂 STEP2 查阅五水合硫酸铜的溶解度(这里给出部分) 0℃23、1 10℃27、5 20℃32 30℃37、8 40℃44、6 50℃不详60℃61、8 70℃不详80℃83、8 90℃不详100℃114 STEP3称取室温下溶解度多3g左右的硫酸铜,溶于100ml热水中(实验中所用的水不能就是自来水,可以就是饮用水,推荐屈臣氏蒸馏水),搅拌使其完全溶解。倒入干净的玻璃容器中,盖上盖子,静置一天 STEP4如果您发现完全冷却后,容器底部有大量碎晶,没有完整的小晶体,那就重复STEP3,原因可能就是冷却过快、水中有杂质或者在冷却过程中频繁扰动溶液。如果您得到了几个完整的小晶体(称为晶核)那请进行下一步 STEP5得到了晶核,您就可以真正开始您的晶体培养了!首先您要配置较大量的饱与溶液(也就就是溶解固体达到最大无法继续再溶的溶液)(200ml),当然您上一步剩余的溶液应该并入此步骤的溶液中。具体的配置常温饱与溶液的方法就是:称取室温下溶解度多2g左右的硫酸铜,溶解在200ml热水中,完全冷却后过滤(这一步您也可能得到好的晶核),保留滤液,剩余的固体放入一个密封塑料瓶中,放入水。这个塑料瓶的目的就是保存您以后分离得到的硫酸铜固体,并且可以同时得到室温下的饱与硫酸铜溶液。 STEP6晶体培养一般有两种方法:杯底或者悬挂。如果您不想用细线挂住晶体,那么可以采用直接把晶核放在杯底的方法,但这种方法对硫酸铜来说会影响晶体的形状,所以建议采用悬挂的方法。(当然您也可以两种方法都试一试)将一个稍大一点的晶核(1-2cm)用细线栓紧,系死扣,并且将线的另一端系在一个细竹签上。系晶体的标准就是:不能让晶体在自然状况下掉落,线长应该满足晶体全部浸入烧杯液面以下。 STEP7 系好了晶体,不要忙着放入溶液。因为这时您的溶液可能混入了大量的杂质,空气中的毛发、灰尘等,需要先进行过滤。(如果您的设备有限,可以不进行这一步,但一定要减少灰尘进入) STEP8将拴好的晶核放入溶液,静置。盖上透气防尘的盖子(或者蒙上一层卫生纸) STEP9如果发现杯底有小晶体出现,在不触碰到晶核的情况下可以先忽视,但如果碎晶很多,就需要及时清理。如果发现杯壁有攀援的晶体层,一定要及时小心清除。为了减少这种现象的发生,您在每次配置好饱与溶液准备静置的时候应该把烧杯壁上的硫酸铜液滴擦掉。如果在蒸发一段时间后溶液过少,应该添加常温下饱与溶液。 STEP10 这样放置一段之间,晶体长到足够大时,就可以取出晶体了。五水合硫酸铜晶体易风化,保存时应该涂上清漆或者透明的指甲油。不要忘记在这个过程中有任何疑问或者新发现都可以与吧友们交流哦! STEP1 首先我们需要这些东西,硫酸铜AR级,烧杯两只(一大一小),培养皿两只,玻璃棒一根,滤纸,以及水。
硫酸铝钾大晶体制备
硫酸铝钾大晶体制备 实验目的 1、了解制备硫酸铝钾的原理及过程 2、了解从水溶液中培养大晶体的方法,制备硫酸铝钾大晶体,学会及时处理问题的技能。实验中细致摸索条件。 3、熟练掌握溶解、结晶、抽滤等基本操作。 试剂 铝片 NaOH(S) H2SO4(3mol/L 1:1) 浓硫酸 K2SO4 (S) KOH(S) 实验原理 1、KAl (SO4)2的制备 2、明矾籽晶培养 保持溶液在一个适当的过饱和度,在一定温度下通过溶剂蒸发使晶体析出,静置一段时间使籽晶形成完整晶型。 3、大晶体制备 通过加热与溶解调解母液的浓度及温度至合适的值,将饱和溶液在室温下静置,靠溶剂的自然挥发来创造溶液的准稳定状态,人工投放晶种让之逐渐长成单晶。 ↑+→++2423)(2622H OH NaAl O H NaOH Al 4223424)(2 SO H 2NaAl(OH)SO Na O H OH Al ++?→?+O H SO Al OH Al SO H 23423426)()(23+→+O H SO KAl O H SO K SO Al 22424234212)(224)(?→++
利用原料和硫酸铝钾的溶解度与温度之间的关系可以计算出所需要的原料量。 实验过程 1、Al2(SO4)3的制备 加热 抽滤 至反应基本完全 溶解度曲线 O H SO KAl 224 12)(
2.籽晶制备 I. 取20克产物放入烧杯,加水200ml 并加热至沸腾,在烧杯口上架一根玻 璃棒,然后把一根尼龙线悬于溶液中间。 II. 把溶液置于不易振荡,易蒸发的地方,在烧杯口盖上一张滤纸以防止灰尘 的进入,静置1~2天。 III. 把线绳上较小,不规则的籽晶去掉,留 下较大的,八面体形状的籽晶。 3.大晶体的培养 ①把取出籽晶后的溶液加热,使烧杯底部的小晶体溶解,并持续加热一小段时间。 ②将溶液冷却至30~40℃,若溶液析出晶体,则过滤晶体,若溶液没有饱和则需加入 KAl(SO4)2?12H2O 再加热,直至把溶液配成30~40℃的饱和溶液。在此温度时有利于籽晶快速长大,同时不至于晶体在室温升高时溶解。 ③把籽晶轻轻吊在饱和液并处于溶液中间。 ④多次重复①②③,直至得到无色、透明、八面体形状的硫酸铝钾大晶体。在晶体生长过程中,应经常观察,若发现籽晶上又长出小晶体,应及时去掉。若杯底有晶体析出也应及时滤去,以免影响晶体生长。 以下是在实验中的附图 2SO 4 水浴加热 沉淀溶解
生物化学基本实验技术
Ⅰ生物化学基本实验技术 一、分光光度法 (一)原理 光线的本质是电磁波的一种,有不同的波长。肉眼可见的彩色光称为可见光,波长范围在400—760nm。短于400nm的光线称为紫外线(200—400nm为紫外光区),短于200nm 的叫远紫外线,再短的就是X射线和γ射线了。长于760nm的光线称为红外线(760—500000nm为红外区),再长的就是无线电波了。 可见光区的电磁波,因波长不同而呈现不同的颜色,这些不同颜色的电磁波称为单色光,单色光并非单一波长的光,而是一定波长范围内的光,太阳及钨丝灯发出的白光,是各种单色光的混合光,利用棱镜可将白光分成按波长顺序排列的各种单色光,即红、橙、黄、绿、青、蓝、紫等,这就是光谱。 当光线通过透明溶液介质时,其辐射的波长有一部分被吸收,一部分透过,因此光线射出溶液之后,部分光波减少。例如,可见光通过有色溶液后,或红外线通过多种气体后,部分光波被吸收。不同的物质由于其分子结构不同,对不同波长光线的吸收能力也不同,因此每种物质都具有其特异的吸收光谱,在一定条件下,其吸收程度与该物质浓度成正比,故可利用各种物质的不同的吸收光谱特征及其强度对不同物质进行定性和定量的分析。 在可见光范围内,利用溶液的颜色深浅来测定溶液中物质含量的方法,称为比色法。采用适当的光源、棱镜和适当的光源接受器,可使溶质浓度的测定范围不仅仅局限于可见光,尚可扩大到紫外光区和红外光区。这就是分光光度法。 分光光度法是生物化学中最有价值的测定方法之一。通过测定紫外、可见或红外的特征吸收光谱可以鉴定未知化合物;通过测量在某一波长的光吸收可以测定溶液中未知化合物的浓度。 分光光度法所依据的原理是Lambert和Beer定律。 1.Lambert定律一束单色光通过透明溶液时,一部分波长的光波被吸收,被吸收光波的量与溶液厚度有一定的比例关系。 即:
