溶解度表大全-无机盐-有机物

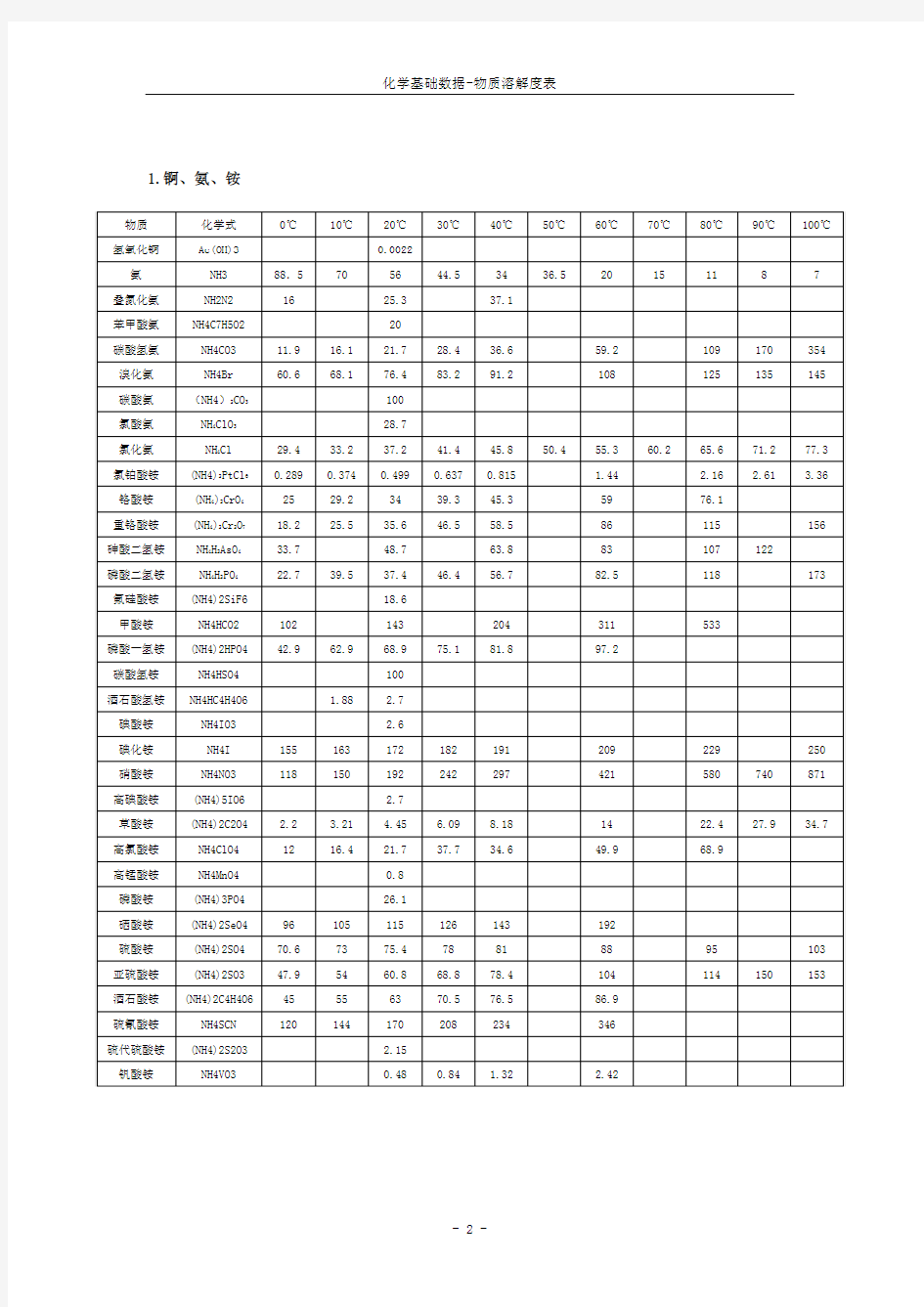
物质水溶液溶解度表
以化学品中特征元素的拼音顺序排列。所有数据都为1atm下水溶液溶解度的数据,单位为g/100cm3
1.锕、氨、铵 (2)
2.钯、钡、铋、铂、钚 (3)
3.氮、镝 (4)
4.铒 (4)
5.钒 (4)
6.钆、钙、锆、镉、铬、汞、钴、硅 (4)
7.铪、氦、钬 (7)
8.镓、钾、金 (7)
9.钪 (8)
10.镧、锂、硫、镥、铝 (9)
11.镁、锰 (9)
12.钠、镍、钕 (10)
13.硼、铍、钋、镨 (12)
14.氢、铅 (12)
15.铷 (13)
16.铯、钐、砷、铈、锶 (14)
17.铊、碳、铽、锑、铁、铜、钍 (15)
18.锡、氙、锌、溴 (17)
19.氩、氧、铟、钇、镱、银、铀、铕 (19)
20.有机化合物 (22)
21.酸碱盐溶解性表 (23)
1.锕、氨、铵
2.钯、钡、铋、铂、钚
3. 氮、镝
4.铒
5.钒
6.钆、钙、锆、镉、铬、汞、钴、硅
7.铪、氦、钬
8.镓、钾、金
9.钪
10.镧、锂、硫、镥、铝
11.镁、锰
12.钠、镍、钕
13.硼、铍、钋、镨
14.氢、铅
15.铷
16.铯、钐、砷、铈、锶
17.铊、碳、铽、锑、铁、铜、钍
18.锡、氙、锌、溴
19.氩、氧、铟、钇、镱、银、铀、铕
20.有机化合物
(完整版)溶解度计算题练习(答案)
三思培训学校溶解度计算题练习 (一)关于溶解度的计算的类型 1. 已知一定温度下,饱和溶液中溶质的质量和溶剂的质量。求该温度下的溶解度。 例如:把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。求20℃时硝酸钾 的溶解度。 解析:溶液的质量为溶质质量和溶剂质量之和,因此50克硝酸钾饱和溶液中含水的 质量是:50克-12克=38克 设:20℃时100克水里溶解硝酸钾达到饱和状态时所溶解的质量为x 溶质 溶剂 溶液 12g 38g 50g x 100g (x+100)g g g x g 1003812= 解得x=31.6g 答:20℃时硝酸钾的溶解度为31.6克 (1)把20℃时53.6克氯化钾饱和溶液蒸干,得到13.6克氯化钾。求20℃时,氯化 钾的溶解度? 设:20℃时氯化钾的溶解度为x 溶质 溶剂 溶液 13.6g 40g 53.6g x 100g (x+100)g g g x g 100406.13= 解得x=34g 答:20℃时氯化钾的溶解度为34克 (2)20℃时,把4克氯化钠固体放入11克水中,恰好形成饱和溶液。求20℃时,氯 化钠的溶解度? 设:20℃时氯化钠的溶解度为x 溶质 溶剂 溶液 4g 11g 15g x 100g (x+100)g g g x g 100114= 解得x=36.4g 答:20℃时氯化钠的溶解度为36.4克 2. 已知某温度时物质的溶解度,求此温度下饱和溶液中的溶质或溶剂的质量。 例如:把100克20℃时硝酸钾的饱和溶液蒸干,得到24克硝酸钾。则: (1)若配制350克20℃的硝酸钾的饱和溶液,需硝酸钾和水各多少克? (2)若将78克硝酸钾配成20℃时的饱和溶液,需水多少克? 解析:设配制350克20℃的硝酸钾的饱和溶液,需硝酸钾和水的质量分别为x 和y 。将78
常见有机溶剂的溶解性汇总
常用溶剂的沸点、溶解性和毒性 溶剂名称沸点(101.3kPa)溶解性毒性 液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、*****、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 ***** 34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶*****性 戊烷36.1 与乙醇、*****等多数有机溶剂混溶低毒性员?婷疋0? 二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,*****性强 二硫化碳46.23 微溶与水,与多种有机溶剂混溶*****性,强刺激性 溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大 丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性 氯仿61.15 与乙醇、*****、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强*****性甲醇64.5 与水、*****、醇、酯、卤代烃、苯、酮混溶中等毒性,*****性 四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、*****、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。*****性,刺激性 三氟代乙酸71.78 与水,乙醇,*****,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷74.0 与丙酮、、甲醇、*****、苯、四氯化碳等有机溶剂混溶低毒类溶剂 四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,*****性 乙醇78.3 与水、*****、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,*****性 丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、*****、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性 乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒 异丙醇82.40 与乙醇、*****、氯仿、水混溶微毒,类似乙醇 1,2-二氯乙烷83.48 与乙醇、*****、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌 乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。能溶解各种树脂,还是二氧化硫、氯代甲烷、乙烯等气体的优良溶剂吸入和经口低毒 三氯乙烯87.19 不溶于水,与乙醇.*****、丙酮、苯、乙酸乙酯、脂肪族氯代烃、汽油混溶有机有毒品_ 三乙胺89.6 水:18.7以下混溶,以上微溶。易溶于氯仿、丙酮,溶于乙醇、***** 易爆,皮肤黏膜刺激性强 丙睛97.35 溶解醇、醚、DMF、乙二胺等有机物,与多种金属盐形成加成有机物高度性,与氢氰酸相似 庚烷98.4 与己烷类似低毒,刺激性、*****性
溶解度的计算,物质的量的有关计算
溶解度的计算 溶解度的计算: 溶解度的计算公式:S=100m质/m剂(一定温度下的饱和溶液)溶解度曲线: 在平面直角坐标系里用横坐标表示温度,纵坐标表示溶解度,画出某物质的溶解度随温度变化的曲线,叫这种物质的溶解度曲线。 ①表示意义 a.表示某物质在不同温度下的溶解度和溶解度随温度变化的情况; b.溶解度曲线上的每一个点表示该溶质在某一温度下的溶解度; c.两条曲线的交点表示这两种物质在某一相同温度下具有相同的溶解度; d.曲线下方的点表示溶液是不饱和溶液; e.在溶解度曲线上方靠近曲线的点表示过饱和溶液(一般物质在较高温度下制成饱和溶液,快速地降到室温,溶液中溶解的溶质的质量超过室温的溶解度,但尚未析出晶体时的溶液叫过饱和溶液)。 ②溶解度曲线的变化规律 a.有些固体物质的溶解度受温度影响较大,表现在曲线“坡度”比较“陡”,如KNO 3 ; b.少数固体物质的溶解度受温度的影响很小,表现在曲线“坡度”比较“平”,如NaCl 。 c.极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如Ca(OH) 2 ③应用 a.根据溶解度曲线可以查出某物质在一定温度下的溶解度; b.可以比较不同物质在同一温度下的溶解度大小; c.可以知道某物质的溶解度随温度的变化情况; d.可以选择对混合物进行分离或提纯的方法; e.确定如何制得某温度时某物质的饱和溶液的方法等。 运用溶解度曲线判断混合物分离、提纯的方法: 根据溶解度曲线受温度变化的影响,通过改变温度或蒸发溶剂,使溶质结晶折出,从而 达到混合物分离、提纯的目的。如KNO 3和NaCl的混合物的分离。 (KNO 3 ,NaCl溶解度曲线如 图)
(完整版)初二溶解度的计算典型例题
有关溶解度的计算典型例题 [例1]已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾? [例2] 把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。 [例3]已知30℃时硝酸钾的溶解度为45.8g。在这温度时,某硝酸钾溶液500g中溶有硝酸钾137.4g。如果蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾? [例4]有60℃时A物质的溶液100g,若温度不变,蒸发掉10g水时,有4gA的晶体析出(不含结晶水),再蒸发掉10g水时,又有6gA的晶体析出,求60℃时A物质的溶解度是多少克。 [例5]在20℃时某物质的不饱和溶液50g,平均分成两等份。一份中加入0.7g该物质,另一份蒸发掉5g水,结果两份溶液都达饱和。那么该物质在此温度下的溶解度为多少克? [例6]一定温度下,取某固体物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半。给另一份溶液里加入原溶质的晶体(该晶体不含结晶水),当达饱和时,所加晶体的质量恰好是此份溶液质量的1/8,求此温度下该物质的溶解度。 [例7] 某物质溶解度曲线如图所示。现有该物质的A、B两种不同浓度的不饱和溶液,当A冷却至10℃时有晶体析出,B在60℃时成为饱和溶液。若取10℃时A的100g饱和溶液,取60℃时B的50g饱和溶液混合得C溶液,则需降温到多少时能析出5g无水晶体? [例8]某固体混合物中含有硝酸钾和不溶性杂质、把它们加入一定量的水中充分溶解,其结果如下表: KNO 3的溶解度见下表: 求:1.所加水的质量。 2.该固体混合物中KNO3的质量。 [例9]在加热情况下,300 g水中溶解了231.9 g氯化铵,如果把这种溶液冷却到10℃,会有多少克氯化铵析出?如果把析出的氯化铵在10℃又配成饱和溶液,需加水多少克(10℃时氯化铵溶解度为33.3 g) [例10] 在20℃时,将氯化钠与一种不溶物组成的固体混合物30 g,投入40 g水中,搅拌、溶解、过滤后,尚余15.6 g固体,将这15.6 g固体再加入40 g水中,搅拌、溶解、过滤,还剩余5 g固体,求原混合物中氯化钠的质量及其20℃时的氯化钠的溶解度。
【精品】常用试剂的溶解性
常用试剂的溶解性 1 . 二甲胺:有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂, 强烈刺激性。 2 . 石油醚:不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇 混溶,与低级烷相似。 3 . 乙醚:微溶于水,易溶与盐酸,与醇、醚、石油醚、苯、氯仿等多数有机溶 剂混溶。麻醉性 4 . 戊烷:与乙醇、乙醚等多数有机溶剂混溶,低毒性。 5 .二氯甲烷:与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶。低毒性,麻醉 性强 7 . 二硫化碳:微溶与水,与多种有机溶剂混溶。麻醉性,强刺激性 8 .丙酮:与水、醇、醚、烃混溶。低毒,类乙醇,但较大 9 . 1,1-二氯乙烷:与醇、醚等大多数有机溶剂混溶。低毒、局部刺激性 10 . 氯仿:与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶。中 等毒性,强麻醉性 11 . 甲醇:与水、乙醚、醇、酯、卤代烃、苯、酮混溶。中等毒性,麻醉性 12 . 四氢呋喃:优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃。吸入微毒,经口低毒。 13 . 己烷:与甲醇部分溶解,与比乙醇高的醇、醚、丙酮、氯仿混溶。低毒, 麻醉性,刺激性 14 . 三氟代乙酸:与水、乙醇、乙醚、丙酮、苯、四氯化碳、己烷混溶,溶解 多种脂肪族、芳香族化合物。 15 . 1,1,1-三氯乙烷:与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶。低毒类溶剂 16 . 四氯化碳:与醇、醚、石油醚、冰醋酸、二硫化碳、氯代烃混溶。氯代甲 烷中毒性最强。 17 . 乙酸乙酯:与醇、醚、氯仿、丙酮、苯等大多数有机溶剂互溶,能溶解某
些金属盐。低毒,麻醉性 18 . 乙醇:与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶。微毒类,麻 醉性 19 . 丁酮:与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶。低毒,毒性强 于丙酮 20 . 苯:难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶。强烈毒性 21 . 乙睛:与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、 氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶。中等毒性,大量吸入蒸气, 引起急性中毒 22 . 异丙醇:与乙醇、乙醚、氯仿、水混溶。微毒,类似乙醇 23 . 甲苯:不溶于水,与甲醇、乙醇、氯仿、丙酮、乙醚、冰醋酸、苯等有机 溶剂混溶。低毒类,麻醉作用。 24 .乙二胺:溶于水、乙醇、苯和乙醚,微溶于庚烷。刺激皮肤、眼睛 25 . 丁醇:与醇、醚、苯混溶。低毒,大于乙醇3倍。 26 . 乙酸:与水、乙醇、乙醚、四氯化碳混溶,不溶于二硫化碳及C12以上高级脂肪烃。低毒,浓溶液毒性强 27 .吡啶:与水、醇、醚、石油醚、苯、油类混溶。能溶多种有机物和无机物。 低毒,皮肤黏膜刺激性 28 . 乙酸丁酯:优良有机溶剂,广泛应用于医药行业,还可以用做萃取剂。一 般条件毒性不大 29 . N,N-二甲基甲酰胺:与水、醇、醚、酮、不饱和烃、芳香烃烃等混溶, 溶解能力强。低毒。 30 . N,N-二甲基乙酰胺:溶解不饱和脂肪烃,与水、醚、酯、酮、芳香族化 合物混溶。微毒类 31 . 二甲亚砜:与水、甲醇、乙醇、乙二醇、甘油、乙醛、丙酮乙酸乙酯吡啶、 芳烃混溶。微毒,对眼有刺激性 32 . 甲酰胺:与水、醇、乙二醇、丙酮、乙酸、二氧六环、甘油、苯酚混溶, 几乎不溶于脂肪烃、芳香烃、醚、卤代烃、氯苯、硝基苯等。皮肤、黏膜刺激性、
有关溶解度计算题讲解
初三有关溶解度计算专题 溶解度计算公式:溶质质量/溶剂质量=溶解度(S) /100g (理解记忆) 溶解度(S)=溶质质量/溶剂质量* 100g 推论:溶质质量1 /溶剂质量仁溶质质量2 /溶剂质量2 溶质质量1 /溶液质量仁溶质质量2 /溶液质量2 溶剂质量1 /溶液质量仁溶剂质量2/溶液质量2 【典型例题精讲】 1、20C时,把50克的硝酸钾饱和溶液蒸干,得到12克硝酸钾。求20C时硝酸钾的溶解度。(31.6 g) 2、20 C时,把53.6克氯化钾饱和溶液蒸干,得到13.6克氯化钾。求20 C时氯化钾的溶解度(34g) 3、20 C时,把4克氯化钠固体放入11克水中,恰好形成饱和溶液。求20C时氯化钠的溶解度(36.4g) 探4、把100克20 C时硝酸钾的饱和溶液蒸干,得到24克硝酸钾。则: (1)若配制350克20C的硝酸钾的饱和溶液,需硝酸钾和水各多少克(84g , 266g) (2)若将78克硝酸钾配成20C时的饱和溶液,需水多少克(247g) 探5、已知氯化铵在30C时的溶解度为45.8克。30C时将68.7克氯化铵配制成400克的溶液,通过计算: (1)溶液是否饱和(不饱和溶液) (2 )若不饱和,为了使其饱和,可用下面的方法: ①蒸发溶剂法:需蒸发多少克水才能成为饱和溶液() ②加溶质法:需再加入多少克氯化铵,溶液才能成为饱和溶液() 6、tC时,NaNQ的溶解度是25g,现向盛有200g 10%NaNO s溶液的烧杯中,加入30g NaN03固体,则此时烧杯中(D ) A.溶液质量是230g B.溶质质量是50g
C.溶剂质量是170g D.溶质质量是45g 解析:此时NaNQ 饱和溶液中m (NaN03)=45g, m (H2O) = 180g, m (溶液)=225g
各种金属盐类溶解度表
銨溶解度單位為g/100ml 物質化學式0°C 10°C 20°C 30°C 40°C 50°C 60°C 70°C 80°C 90°C 100°C 氨NH388.5 70 56 44.5 34 26.5 20 15 11 8 7 碳酸氫銨NH4HCO311.9 16.1 21.7 28.4 36.6 59.2 109 170 354 溴化銨NH4Br 60.6 68.1 76.4 83.2 91.2 108 125 135 145 碳酸銨(NH4)2CO3100 氯酸銨NH4ClO328.7 氯化銨NH4Cl 29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3 鉻酸銨(NH4)2CrO425 29.2 34 39.3 45.3 59 76.1 重鉻酸銨(NH4)2Cr2O718.2 25.5 35.6 46.5 58.5 86 115 156 磷酸二氫銨NH4H2PO422.7 39.5 37.4 46.4 56.7 82.5 118 173 甲酸銨NH4HCO2102 143 204 311 533
磷酸一氫銨(NH4)2HPO442.9 62.9 68.9 75.1 81.8 97.2 碘化銨NH4I 155 163 172 182 191 209 229 250 硝酸銨NH4NO3118 150 192 242 297 421 580 740 871 高氯酸銨NH4ClO412 16.4 21.7 37.7 34.6 49.9 68.9 磷酸銨(NH4)3PO426.1 硒酸銨(NH4)2SeO496 105 115 126 143 192 硫酸銨(NH4)2SO470.6 73 75.4 78 81 88 95 103 亞硫酸銨(NH4)2SO347.9 54 60.8 68.8 78.4 104 144 150 153 酒石酸銨(NH4)2C4H4O645 55 63 70.5 76.5 86.9 硫氰酸銨NH4SCN 120 144 170 208 234 346 硫代硫酸銨(NH4)2S2O3 2.15
关于溶解度的计算
关于<<溶解度的计算>>读后感 通过研读<<溶解度的计算>>一文,现将有关溶解度计算的常见类型归纳如下: 溶解度的计算,关键在于正确理解溶解度的概念。 一定温度下,一定量的溶剂中所溶解物质的质量是一定的,反之,任意量的饱和溶液里溶质质量与溶剂质量或溶质质量与溶液的质量比是一定的,如果把一定温度下溶剂的量规定为100g,此时所溶解溶质形成饱和溶液时的质量称为溶解度。由此可得以下关系: 溶解度——100g溶剂——100+溶解度 (溶质质量) (溶剂质量) (饱和溶液质量) 可得出以下正比例关系: 式中W溶质、W溶剂、W饱和溶液分别表示饱和溶液中溶质、溶剂和溶液的质量,S表示某温度时该溶质的溶解度。 在以上的比例式中,100是常量,其它3个量中只要知道其中2个量就可求出另外一个量。由此,不仅明确了溶解度的解题的基本思路就是比例关系,从而避免质量混淆的现象,而且也使学生明确溶解度计算的一题多种解法,并从中找出最佳解法。 现将有关溶解度计算的常见类型归纳如下: 一、已知一定温度下某物质饱和溶液里的溶质和溶剂的质量,求溶解度 例1 在一定温度下,ng某物质恰好溶于一定量的水中形成mg饱和溶液,求该物质在此温度下的溶解度。 解;由题意可知,W溶液=W溶质+W溶剂,因此mg该物质的饱和溶液中含水的质量为:(m-n)g,此题可代入分式(1): 设某温度下该物质的溶解度为Sg 也可代入分式(2) 二、已知一定温度下某物质的溶解度,求此温度下一定量的饱和溶液中含溶质和溶剂的质量 例2 已知在20℃时KNO3的溶解度为31.6g。现要在20℃时配制20gKNO3饱和溶液,需KNO3和H2O各几克? 解:设配制20℃20g硝酸钾饱和溶液需硝酸钾的质量为xg。 此题若代入公式(1),列式为:若代入公式(2),列式为: 需水的质量为20-4.8=15.2g 答:配制20℃时20gKNO3的饱和溶液需KNO34.8g和水15.2g。
几种常见无机盐的缺乏症及食物来源见下表
几种常见无机盐的缺乏症及食物来源见下表 The final revision was on November 23, 2020
几种常见无机盐的缺乏症及食物来源见下表: 几种常见维生素的功能、缺乏症及食物来源见下表:
糖类 (1)食物来源:谷类、豆类和根茎类等食物中含有较多的糖类。 (2)功能:糖类是人体主要的供能物质,人体的一切活动,包括走路、学习、呼吸等都要消耗能量,这衅能量大部分是由糖类提供的。 (3)缺乏时的症状:瘦弱、乏力、低血糖。 脂肪 (1)食物来源:猪油、奶油、蛋黄、花生油、芝麻、豆类和硬果类等食物中含有较多的脂肪。 (2)功能:脂肪也是人体能量来源的重要物质,但是脂肪一般是储存在体内作为备用能源 (3)缺乏时的症状:瘦弱。 蛋白质 (1)食物来源:奶、蛋、鱼,瘦肉、豆类制品等。 (2)功能: ①组成细胞的主要有机物,如蛋白质是构成细胞膜、染色体的主要成分。 ②能源物质,蛋白质能分解释放能量,为人体的牛命活动提供能量。 ③人的生长发育以及受损细胞的修复和更新都离不开蛋白质。(3)缺乏时的症状:长期供应不足可导致营养不良,发生贫血。
水 (1)来源:食物和饮料。 (2)作用: ①人体细胞的主要成分之一,占体重的60%~70%。 ②人体各种生命活动离不开水,人体内的细胞生活在液体环境中。 ③人体内的营养物质和废物都必须溶解在水中才能进行运输。 无机盐 无机盐在人体内的含量不多,约占体重的4%,是构成人体的重要原料,如钙和磷是构成牙齿和骨骼的重要成分。无机盐还参与人体的各种代谢活动,是人体生长发育等生命活动正常进行的重要保证。 维生素 维生素不是构成细胞的主要原料,不为人体提供能量,人体每日对它们的需要鼙也很小。但是,维生素对人体的重要作用是其他营养物质所不能代替的。人体一旦缺乏维生素,就会影响正常的隹长发育,甚至患病。 很多妈妈都问过小孩皮肤粗糙怎么办这个问题,小孩的皮肤相对而言比较薄嫩,到了秋冬干燥的季节就容易粗糙,同时也有很少的宝宝是天生的皮肤粗糙,那么小孩皮肤粗糙怎么办呢我们来听听专家是怎么说的吧。 海军总医院皮肤专家指出,宝宝皮肤粗糙问题的产生是因为皮肤缺少所致,一般婴儿体内水分占体重的70%~75%,较成人(60%~65%)高,因其生长发育旺盛,故需水量也多,由于供水不足很有可能会产生宝宝皮肤粗糙问题。水分的需要量与年龄、体重、食物的质与量,代谢高低、体温与肾浓缩功能等因素有关,年龄越小相对需水量越大,因而要解决宝宝皮肤粗糙怎么办的问题,就要做好以下这些事项: 1、多喝温开水改善宝宝皮肤粗糙,这是最有效的滋润方法。 2、不要经常的洗澡,特别是不要用较烫的水洗,一般一周2-3次即可,禁止用香皂等化学品,应该选用柔和的婴儿沐浴液。 3、改善宝宝皮肤粗糙要用温水洗脸,洗后涂抹润肤油,同样不追求美白、抗衰老
常见盐的溶解度
下列物质不同温度(℃)时每100克水中的最大溶解克数 温度 0 10 20 25 30 40 50 60 70 80 90 100 物质 硫酸钾 7.4 10.2 11.1 13.0 14.8 16.6 18.2 19.8 21.4 22.4 24.1 硫酸钠 4.5 9.6 19.527.9 40.8 48.4 46.7 45.3 44.1 43.7 42.9 42.3 硫酸铵 70.1 72.7 75.4 76.9 78.1 81.2 84.3 87.4 90.7594.1 98.05102.0硫酸氢钠 5.028.6 100.0硫酸钡 0.12 0.2 0.24 0.29 0.31 0.42 0.46 0.43 0.4 0.4 0.41 硫酸钙 0.18 0.19 0.21 0.21 0.2 0.2 0.16 氢氧化钙 0.18 0.17 0.16 0.15 0.14 0.11 0.09 0.07 氯化钠 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8 氯化钾 28.0 31.2 34.4 37.4 40.3 42.8 45.8 48.1 51.1 54.0 56.0 氯化铵 29.4 33.3 37.2 41.4 45.8 50.4 55.2 60.2 65.6 71.3 77.3 碳酸钠 7.0 12.2 21.8 29.4 39.7 48.8 47.3 46.4 46.2 45.8 45.7 45.5 碳酸钾 107.0 109.0111.0114.0117.0126.0139.0156.0碳酸铵 100.0 碳酸氢钾 22.5 27.4 33.7 39.9 47.5 65.6 碳酸氢铵 11.9 16.1 21.7 24.8 28.4 36.6 59.2 109.0 碳酸氢钠 6.9 8.15 9.6 10.3511.1 12.7 14.45 16.4 20.2 24.3 碳酸氢钙 0.16 0.17 0.17 0.18 0.18 0.18 碳酸钙 8.1 7.0 6.5 5.2 4.4 3.8 碳酸钡 1.7 2.3 2.4 6.5 甘氨酸14.1818.0422.5227.5933.1639.145.2651.3957.2762.6267.17 IDA 2.6 3.3 4.04 6.089.7312.9616.5823.8132.2152.0
初中化学中溶解度的计算
初中化学中溶解度的计算 一定温度下,一定量的溶剂中所溶解物质的质量是一定的,反之,任意量的饱和溶液里溶质质量与溶剂质量或溶质质量与溶液的质量比是一定的,如果把一定温度下溶剂的量规定为100g,此时所溶解溶质形成饱和溶液时的质量称为溶解度。由此可得以下关系: 溶解度————100g溶剂————100+溶解度 (溶质质量) (溶剂质量) (饱和溶液质量) 可得出以下正比例关系: 式中W溶质、W溶剂、W饱和溶液分别表示饱和溶液中溶质、溶剂和溶液的质量,S表示某温度时该溶质的溶解度。 在以上的比例式中,100是常量,其它3个量中只要知道其中2个量就可求出另外一个量。由此,不仅明确了溶解度的解题的基本思路就是比例关系,从而避免质量混淆的现象,而且也使学生明确溶解度计算的一题多种解法,并从中找出最佳解法。 一、已知一定温度下某物质饱和溶液里的溶质和溶剂的质量,求溶解度 例1 在一定温度下,ng某物质恰好溶于一定量的水中形成mg饱和溶液,求该物质在此温度下的溶解度。解;由题意可知,W溶液=W溶质+W溶剂,因此mg该物质的饱和溶液中含水的质量为:(m-n)g,此题可代入分式(1): 设某温度下该物质的溶解度为Sg 也可代入分式(2) 二、已知一定温度下某物质的溶解度,求此温度下一定量的饱和溶液中含溶质和溶剂的质量 例2 已知在20℃时KNO3的溶解度为31.6g。现要在20℃时配制20gKNO3饱和溶液,需KNO3和H2O各几克? 解:设配制20℃20g硝酸钾饱和溶液需硝酸钾的质量为xg。 此题若代入公式(1),列式为: 若代入公式(2),列式为:
需水的质量为20-4.8=15.2g 答:配制20℃时20gKNO3的饱和溶液需KNO34.8g和水15.2g。 三、已知一定温度下某物质的溶解度,求一定量溶质配制成饱和溶液时,所需溶剂的质量 例3 已知氯化钠在20℃的溶解度是36g,在20℃时要把40g氯化钠配制成饱和溶液,需要水多少克?解:从题意可知,在20℃时36g氯化钠溶于l00g水中恰好配制成氯化钠的饱和溶液。 设20℃时40g氯化钠配制成氯化钠饱和溶液需要水为xg 答:在20℃时,40g氯化钠配制成饱和溶液需要水111g。 四、计算不饱和溶液恒温变成饱和溶溶需要蒸发溶剂或加入溶质的质量 例4 已知硝酸钾在20℃的溶解度为31.6g,现有150g20%的硝酸钾溶液,欲想使其恰好饱和,应加入几克硝酸钾或蒸发几克水? 解:先计算150g20%的KNO3溶液里含KNO3的量为150×20%=30g,含水为150-30=120g,则欲使之饱和,所要加进溶质或蒸发溶剂后的量之比与饱和溶液中溶质和溶剂之比相等进行列式。 设要使20℃150克20%KNO3溶液变为饱和溶液需加入x克KNO3或蒸发yg水,依题意列式: 答:要使20℃150g20%的KNO3溶液变为饱和溶液需加入KNO37.92g,或蒸发25.1g水。 五、计算温度升高时变成饱和溶液需加入溶质或蒸发溶剂的质量 例5 将20℃时263.2g硝酸钾饱和溶液温度升至60℃需加入几克硝酸钾或蒸发几克水才能变为饱和溶液?(20℃硝酸钾溶解度为31.6g,60℃为110g) 设将20℃时263.2gKNO3饱和溶液升至60℃时需加入xgKNO3或蒸发yg水后才能变成饱和溶液。 先计算20℃此饱和溶液中含溶质和溶剂的量,设含溶质为ag
作业——溶解度的相关计算
作业—溶解度的相关计算 2020.3.20【学而时习之,不亦说乎!】(都要写计算过程哦!) 1.用溶质质量分数为15%的氯化钠溶液来配制500g溶质质量分数为6%的氯化钠溶液,需要15%的氯化钠溶液g. 2.已知20℃,S(NaCl)=36g,则室温下,68 kg饱和食盐水中溶质的质量为。3.取一定质量某温度下的氯化钾饱和溶液,将其恒温蒸发10 g水,析出4g氯化钾固体,剩余溶液中还含16 g氯化钾,则所取溶液的质量为( ) A.40g B.50g C.56g D.70g 4.某温度下饱和氯化钠溶液的溶质质量分数为26%,试列式计算该温度下氯化钠的溶解度S (计算结果保留小数点后一位). 5.若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便 ...方法是继续向其中添加氯化钠。那么,需要再加入多少千克氯化钠呢?(已知:20℃时氯化钠的溶解度为36g。) 6.若用10.0%的氢氧化钠溶液16. 0g滴加到20. 0g盐酸中(含2滴酚酞试液),混合液刚好由无色变为粉红色时,可认为恰好完全反应。 ①原盐酸中溶质的质量分数为。 ②试列式计算说明将该反应后的溶液转化为20℃时饱和溶液的一种简单方法(计算结 果精确到0.1g)。已知:20℃时氯化钠的溶解度为36.0g。
7.用胶头滴管向盛有20.0g稀硝酸的烧杯中滴加2滴酚酞试液,再向其中缓缓加入20.0g5.6%的氢氧化钾溶液;边滴加边用玻璃棒搅拌,待滴入最后1滴碱液时,混合液刚好由无色变为粉红色,且30s内颜色不变,即可认为恰好完全反应。 (1)请列式计算反应后溶液中溶质的质量分数。 (2)将反应后的溶液冷却到室温,若要配制室温时的饱和溶液,还需向其中加入10.0 g 硝酸钾固体。按规范操作,用托盘天平称取10.0g硝酸钾时,若指针略向左偏转,要使指针居中的恰当操作是:。 (3)根据上述情境,列式计算此时硝酸钾的溶解度(计算结果保留小数点后一位)。 【保持好奇心,下定决心,坚定信心!】
常用试剂的溶解性和毒性
常用试剂的溶解性和毒性 剂名称沸点(101.3kPa)溶解性毒性 液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性员?婷疋0? 二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强 二硫化碳46.23 微溶与水,与多种有机溶剂混溶麻醉性,强刺激性 溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大 丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性 氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性 甲醇64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性 四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。麻醉性,刺激性 三氟代乙酸71.78 与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷74.0 与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性 乙醇78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性 丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性 乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒 异丙醇82.40 与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇 1,2-二氯乙烷83.48 与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌 乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。能溶解各种树脂,还是二氧化硫、氯代甲烷、乙烯等气体的优良溶剂吸入和经口低毒 三氯乙烯87.19 不溶于水,与乙醇.乙醚、丙酮、苯、乙酸乙酯、脂肪族氯代烃、汽油混溶有机有毒品_ 三乙胺89.6 水:18.7以下混溶,以上微溶。易溶于氯仿、丙酮,溶于乙醇、乙醚易爆,皮肤黏膜刺激性强 丙睛97.35 溶解醇、醚、DMF、乙二胺等有机物,与多种金属盐形成加成有机物高度性,与氢氰酸相似 庚烷98.4 与己烷类似低毒,刺激性、麻醉性 水100 略略 硝基甲烷101.2 与醇、醚、四氯化碳、DMF、等混溶麻醉性,刺激性 1,4-二氧六环101.32 能与水及多数有机溶剂混溶,仍溶解能力很强微毒,强于乙醚2~3倍 不溶于乙醚、氯仿、二硫化碳、苯、四氯化碳、石油醚食用对人体无毒 甲苯110.63 不溶于水,与甲醇、乙醇、氯仿、丙酮、乙醚、冰醋酸、苯等有机溶剂混溶低
常用试剂的溶解性
常用试剂的溶解性 1.二甲胺:有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂,强烈刺激性。 2.石油醚:不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶,与低级烷相似。 3.乙醚:微溶于水,易溶与盐酸,与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶。麻醉性 4.戊烷:与乙醇、乙醚等多数有机溶剂混溶,低毒性。 5.二氯甲烷:与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶。低毒性,麻醉性强 7.二硫化碳:微溶与水,与多种有机溶剂混溶。麻醉性,强刺激性 8.丙酮:与水、醇、醚、烃混溶。低毒,类乙醇,但较大 9.1,1-二氯乙烷:与醇、醚等大多数有机溶剂混溶。低毒、局部刺激性 10.氯仿:与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶。中等毒性,强麻醉性 11.甲醇:与水、乙醚、醇、酯、卤代烃、苯、酮混溶。中等毒性,麻醉性 12.四氢呋喃:优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃。吸入微毒,经口低毒。 13.己烷:与甲醇部分溶解,与比乙醇高的醇、醚、丙酮、氯仿混溶。低毒,麻醉性,刺激性 14.三氟代乙酸:与水、乙醇、乙醚、丙酮、苯、四氯化碳、己烷混溶,溶解多种脂肪族、芳香族化合物。 15.1,1,1-三氯乙烷:与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶。低毒类溶剂 16.四氯化碳:与醇、醚、石油醚、冰醋酸、二硫化碳、氯代烃混溶。氯代甲烷中毒性最强。 17.乙酸乙酯:与醇、醚、氯仿、丙酮、苯等大多数有机溶剂互溶,能溶解某些金属盐。低毒,麻醉性 18.乙醇:与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶。微毒类,麻醉性 19.丁酮:与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶。低毒,毒性强于丙酮 20.苯:难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶。强烈毒性 21.乙睛:与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶。中等毒性,大量吸入蒸气,引起急性中毒 22.异丙醇:与乙醇、乙醚、氯仿、水混溶。微毒,类似乙醇 23.甲苯:不溶于水,与甲醇、乙醇、氯仿、丙酮、乙醚、冰醋酸、苯等有机溶剂混溶。低毒类,麻醉作用。 24.乙二胺:溶于水、乙醇、苯和乙醚,微溶于庚烷。刺激皮肤、眼睛 25.丁醇:与醇、醚、苯混溶。低毒,大于乙醇3倍。 26.乙酸:与水、乙醇、乙醚、四氯化碳混溶,不溶于二硫化碳及C12以上高级脂肪烃。低毒,浓溶液毒性强 27.吡啶:与水、醇、醚、石油醚、苯、油类混溶。能溶多种有机物和无机物。低毒,皮肤黏膜刺激性 28.乙酸丁酯:优良有机溶剂,广泛应用于医药行业,还可以用做萃取剂。一般条件毒性不大
最标准酸碱盐的溶解性表
酸碱盐的溶解性表 OH(-1)NO3(-1)Cl(-1) SO4(-2)CO3(-2) PO4(-3) H(+1)溶、挥溶、挥溶溶、挥溶 K(+1)溶溶溶溶溶溶 Na(+1)溶溶溶溶溶溶 NH4(+1)溶、挥溶溶溶溶溶 Ba(+2)溶溶溶不不不 Ca(+2)微溶溶微不不 Mg(+2)不溶溶溶微不 Al(+3)不溶溶溶--- 不 Zn(+2)不溶溶溶不不 Fe(+2)不溶溶溶不不 Fe(+3)不溶溶溶不不 Cu(+2)不溶溶溶--- 不 Ag(+1)--- 溶不微不不说明:此为20℃时的情况。“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“---”表示那种物质不存在或遇到水就分解了 背诵口诀 1.钾钠铵盐都可溶,氯化物不溶氯化银 硫酸盐钙银微溶钡不溶 硝酸盐遇水影无踪 碳酸盐除钾钠铵都不溶 钾钠钡钙碱可溶 红褐铁,蓝絮铜 其它沉淀白色呈 注:1.初中用够了,红褐铁,代表铁盐沉淀为红褐色【fe(oh)2氢氧化亚铁除外】,蓝絮铜代表,铜盐为蓝色絮状沉淀。2.氯化银【不溶酸】,碳酸钙,碳酸钡,硫酸钡【不溶酸】,氢氧化铝,氢氧化镁,为白色沉淀。氢氧化铁(红褐色)氢氧化铜(蓝色) 说明【】内为前一物质的特点 2.钾钠铵盐全都溶 碳酸除镁是微溶 其他全都不能溶 AgCl、BaSO4酸也不溶 磷酸盐,更不溶
一、氧气的性质: (1)单质与氧气的反应:(化合反应) 1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO 2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4 3. 铜在空气中受热:2Cu + O2 加热 2CuO 4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O3 5. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O 6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 点燃 2P2O5 7. 硫粉在空气中燃烧: S + O2 点燃 SO2 8. 碳在氧气中充分燃烧:C + O2 点燃 CO2 9. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO (2)化合物与氧气的反应: 10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO2 11. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O 12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O (3)氧气的来源: 13.玻义耳研究空气的成分实验 2HgO 加热 Hg+ O2 ↑ 14.加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑(实验室 制氧气原理1) 15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2 ↑(实验室制氧气原理2) 二、自然界中的水: 16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+ O2 ↑ 17.生石灰溶于水:CaO + H2O == Ca(OH)2 18.二氧化碳可溶于水: H2O + CO2==H2CO3 三、质量守恒定律: 19.镁在空气中燃烧:2Mg + O2 点燃 2MgO 20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu 21.氢气还原氧化铜:H2 + CuO 加热 Cu + H2O 22. 镁还原氧化铜:Mg + CuO 加热 Cu + MgO 四、碳和碳的氧化物: (1)碳的化学性质 23. 碳在氧气中充分燃烧:C + O2 点燃 CO2 24.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑ 25.焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑ (2)煤炉中发生的三个反应:(几个化合反应) 26.煤炉的底层:C + O2 点燃 CO2 27.煤炉的中层:CO2 + C 高温 2CO 28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2 (3)二氧化碳的制法与性质: 29.大理石与稀盐酸反应(实验室制二氧化碳): CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 30.碳酸不稳定而分解:H2CO3 == H2O + CO2↑ 31.二氧化碳可溶于水: H2O + CO2== H2CO3 32.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温 CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳): Ca(OH)2 + CO2 === CaCO3 ↓+ H2O
有关溶解度计算题
溶解度 (一)关于溶解度的计算的类型 1. 已知一定温度下,饱和溶液中溶质的质量和溶剂的质量。求该温度下的溶解度。 例如:把50克20C时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。求20C时硝酸钾的溶解度。 解析:溶液的质量为溶质质量和溶剂质量之和,因此50克硝酸钾饱和溶液中含水的 质量疋:50克—12克=38克 设: 20 C时100克水里溶解硝酸钾达到饱和状态时所溶解的质量为x 溶质溶剂溶液 12g38g50g x100g(x+100) g 12g38g x100g解得x=31.6g 答: 20 C时硝酸钾的溶解度为31.6 克 (1 )把20C时53.6克氯化钾饱和溶液蒸干,得到13.6克氯化钾。求20C时,氯化 钾的溶解度? 设:20C时氯化钾的溶解度为x 溶质溶剂溶液 13.6g40g53.6g x100g(x+100) g 13.6g40g x100g解得x=34g 答:20C时氯化钾的溶解度为34克 (2) 20C时,把4克氯化钠固体放入11克水中,恰好形成饱和溶液。求20C时,氯化钠的溶解度? 设:20 C时氯化钠的溶解度为x 溶质溶剂溶液 4g 11g 15g x 100g (x+100) g 4g 11g x 100g解得x=36.4g 答:20C时氯化钠的溶解度为36.4克 2. 已知某温度时物质的溶解度,求此温度下饱和溶液中的溶质或溶剂的质量。 例如:把100克20C时硝酸钾的饱和溶液蒸干,得到24克硝酸钾。则: (1)若配制350克20C的硝酸钾的饱和溶液,需硝酸钾和水各多少克? (2)若将78克硝酸钾配成20C时的饱和溶液,需水多少克? 解析:设配制350克20C的硝酸钾的饱和溶液,需硝酸钾和水的质量分别为x和y。将78
溶解度及有关计算1
溶解度及有关计算 教学目标 知识技能:了解饱和溶液、不饱和溶液的概念。理解溶解度概念。理解温度对溶解度的影响及溶解度曲线。掌握有关溶解度的计算。 能力培养:结合溶解度计算,培养学生学会用比例法和守恒法解决溶解度有关计算的能力。 科学思想:结合饱和溶液、不饱和溶液和溶解度曲线的复习,使学生进一步树立平衡是相对的、有条件的、动态的辩证思想。 科学方法:结合溶解度计算的复习,进一步掌握守恒法、比例法解决问题的方法。 重点、难点有关溶解度的计算。 教学过程设计 教师活动 【引言】上一讲我们复习了溶液浓度计算,溶液有饱和溶液和不饱和溶液之分。而且在一定温度下,固体不能无限溶于水中,因此存在溶解度的问题。本节我们将复习饱和溶液、不饱和溶液和溶解度的概念,同时要重点复习溶解度的有关计算。 【板书】一、饱和溶液和不饱和溶液 【投影】问题:1.什么是饱和溶液,什么是不饱和溶液? 2.溶液处于饱和状态时,有什么特点? 学生活动 倾听、回忆。 回答:
1.在一定温度下,当溶质溶解的速率和溶质从溶液中析出的速率相等,此时溶液达到溶解平衡状态,所得的溶液为饱和溶液,反之为不饱和溶液。 2.在一定条件下,溶液达到饱和时,溶液处于溶解平衡状态,它与化学平衡状态相似,具有“等”、“定”、“动”、“变”等特点。即在一定条件下,当溶液达饱和时,溶质溶解和结晶的速率相等,溶液处于动态平衡,溶液的浓度保持不变,当条件改变时,例如:改变温度,可使溶液由饱和变成不饱和。 【评价】同学们回答得很好。这里还应明确两点: 1.当溶液溶解一种溶质达饱和时,溶液中仍可溶解其他溶质。 倾听、思考。 2.化学平衡移动原理适用于溶解平衡,条件改变时,溶液可由饱和溶液转化成不饱和溶液。 倾听、思考。 【投影】练习题:氯气在下列液体中溶解度最小的是 [ ] A.水 B.饱和食盐水C.氢氧化钠溶液 D.饱和石灰水 分析并回答: 氯气溶于水中发生如下反应: Cl2+H2O H++Cl-+HClO 当氯气溶于氢氧化钠溶液或饱和石灰水时,由于生成的盐酸和次氯酸与碱反应,可加速氯气在溶液中的溶解,并生成金属氯化物和次氯酸盐。 而在饱和食盐水中,由于存在下列溶解平衡: NaCl Na++Cl- 溶液中氯离子浓度已达饱和,抑制了氯气在溶液中的溶解。因此氯气在饱和食盐水中溶解度最小,应选B。 【小结】由于饱和食盐水中溶解平衡的存在,溶液中氯离子浓度已达饱和,对氯气在溶液中的溶解起抑制作用,和化学平衡中增大生成物浓度使平衡向逆方向移动的道理相同。 【板书】二、溶解度(S)
