乙醇-水溶液平衡数据及沸点(常压)
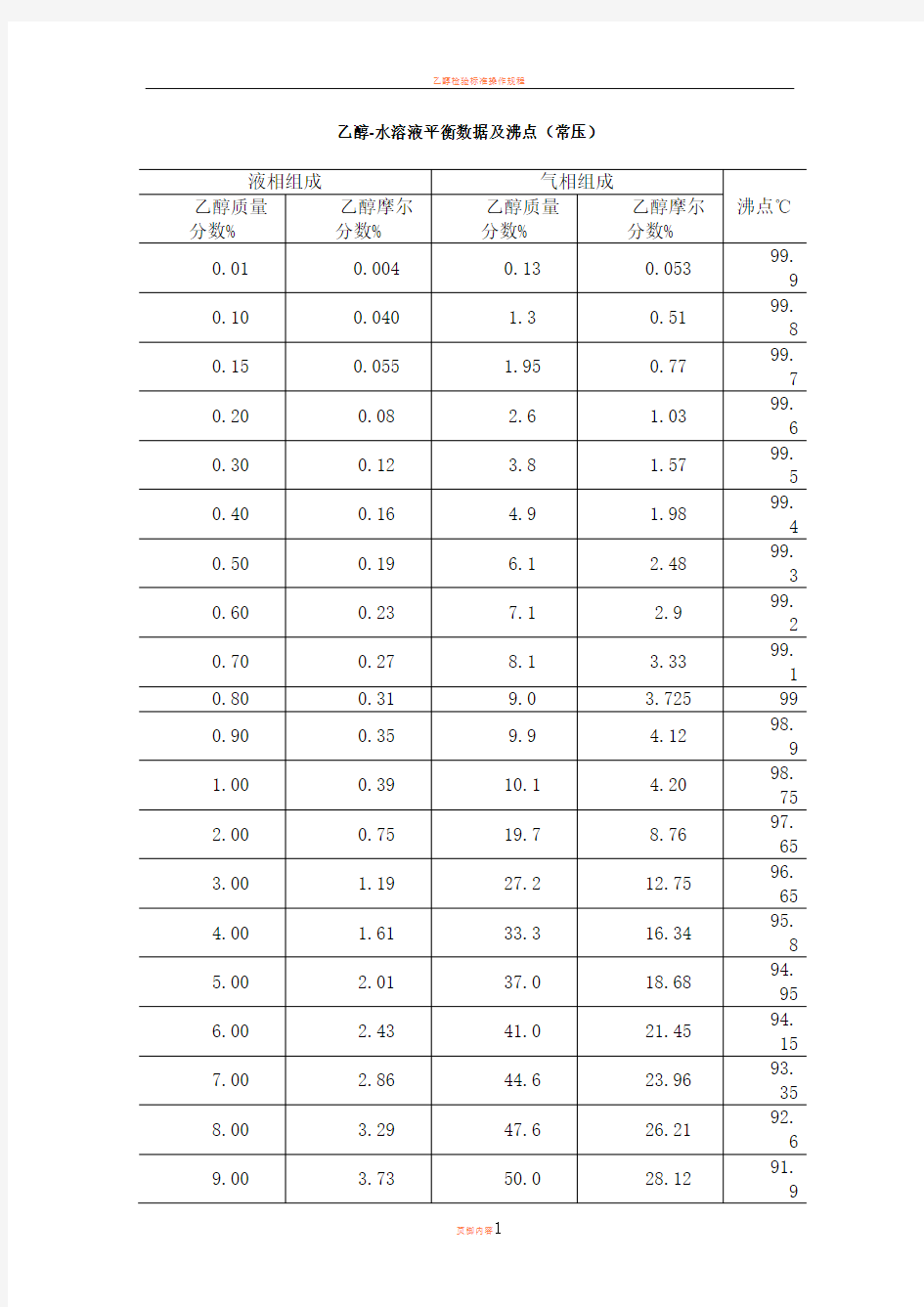

乙醇-水溶液平衡数据及沸点(常压)
气液平衡
汽液平衡数据的测定 汽液平衡数据是最常用的化工基础数据。许多化工过程如精馏的设计、操作及过程控制等都离不开汽液平衡数据。有热力学研究方面,新的热力学模型的开发,各种热力学模型的比较筛选等也离不开大量精确的汽液平衡实测数据。现在,各类化工杂志每年都有大量的汽液平衡数据及汽液平衡测定研究的文章发表。所以汽液平衡数据的测定及研究深受化工界人士的重视 一、实验目的: 通过测定常压下乙醇—水二元系统汽液平衡数据的实验,使同学们了解、掌握汽液平衡数据测定的方法和技能,熟悉有关仪器的使用方法,将课本上学到的热力学理论知识与实际运用有机地联系在一起。从而既加深对理论知识的理解和掌握,又提高了动手的能力。 二、汽液平衡测定和种类: 由于汽液平衡体系的复杂性及汽液平衡测定技术的不断发展,汽液平衡测定也形成了特点各异的不同种类。 按压力分,有常减压汽液平衡和高压所液平衡测定。高压汽液平衡测定的技术相对比较复杂,难度较大。常减压汽液平衡测定则相对较易。 按形态分,有静态法和动态法。静态法技术相对要简单一些,而动态法测定的技术要复杂一些但测定较快较准。 在动态法里又有单循环法和双循环法。双循环法就是让汽相和液相都循环,而单循环只让其中一相(一般是汽相)循环。在一般情况下,常减压汽液平衡都采用双循环,而在高压所液平衡中,只让汽相强制循环。循环的好处是易于平衡、易于取样分析。 根据对温度及压力的控制情况,有等温法与等压法之分。一般,静态法采用等温测定,动态法的高压汽液平等多采用等温法。 总之汽液平衡系统特点各异,而测定的方法亦丰富多彩。 本实验采用的是常压下(等压)双循环法测定乙醇—水的汽液平衡数据。 三、实验原理: 以循环法测定汽液平衡数据的平衡釜有多种形式,但基本原理是一样的。如图书馆所示,当体系达到平衡时,A 和B 两容器中组成不随时间布景为化,这时从A 和B 两容器中取样分析可以得到一组汽液平衡实验数据。 根据下平衡原理,当所液两相达到相平衡时,汽液两相温度压力相等,同时任一组分在各相中的逸度相等,即: v L i i f f =)) 这里 v v i i i f y P =Φ)) 0 L i i i i f r x f =)) 对低压汽液平衡,其汽相可以视为理想气体混合物,即1v i Φ=) ,忽略压力对液体 逸度的影响,即0 i i f P =),从而得出低压下汽液平衡关系式: i i i i Py r x P = 式中 P ——体系压力(总压) i P ——纯组分i 在平衡温度下的饱合蒸汽压。
乙醇-水溶液偏摩尔体积的测定
乙醇-水溶液偏摩尔体积的测定 一、实验目的 1、掌握用比重瓶测定溶液密度的方法。 2、加深理解偏摩尔量的物理意义 。 3、测定乙醇—水溶液中各组分的偏摩尔体积。 二、实验原理 在多组分体系中,某组分i 的偏摩尔体积定义为 j n p r i n V V ,,m i,???? ????= (1) 若是二组分体系,则有 2,,1m 1,n p r n V V ???? ????= (2) 1 ,,2m 2,n p r n V V ???? ????= (3) 体系总体积 m m total V n V n V ,22,11+= (4) 将(4)式两边同除以溶液质量W W V M W W V M W W V m m ,222,111?+?= (5) 令 2 ,21,1, , ααα===W V W V W V m m (6) 式中α是溶液的比容;α1,α2分别为组分1、2的偏质量体积。
将(6)式代入(5)式可得: α=W1%α1+W2%α2=(1-W2%)α1+W2%α2 (7) 将(7)式对W2%微分: 2 12% α αα +-=??W (8) 将(8)代回(7),整理得 % % 121W W ??-=ααα (9) 和 % % 212W W ??+=ααα (10) 图1 比容-质量百分比浓度关系 所以,实验求出不同浓度溶液的比容α,作α—W2%关系图,得曲线CC′(见图1)。欲求M浓度溶液中各组分的偏摩尔体积,可在M点作切线,此切线在两边的截距AB和A′B′即为α1和α2,再由关系式(6)就可求出V1,m 和V2,m 。 三、仪器与试剂 仪器:分析天平(公用);比重瓶(5mL)2个; 工业天平(公用);磨口三角瓶(50mL)4个。
乙醇溶液密度表
乙醇溶液密度(g/cm3)(20℃)-每g含有乙醇重量(%)-浓度(体积比%)=度(1度=1%体积) 0.998-0.15-0.2 0.996-1.20-1.5 0.994-2.30-3.0 0.992-3.50-4.4 0.990-4.70-5.9 0.988-5.90-7.4 0.985-7.90-9.9 0.982-10.0-12.5 0.980-11.5-14.2 0.978-13.0-16.0 0.975-15.3-18.9 0.972-17.6-21.7 0.970-19.1-23.5 0.968-20.6-25.3 0.965-22.8-27.8 0.962-24.8-30.3 0.960-26.2-31.8 0.957-28.1-34.0 0.954-29.9-36.1 0.950-32.2-38.8 0.945-35.0-41.3 0.940-37.6-44.8 0.935-40.1-47.5 0.930-42.6-50.2 0.925-44.9-52.7 0.920-47.3-55.1 0.915-49.5-57.4 0.910-51.8-59.7 0.905-53.9-61.9 0.900-56.2-64.0 0.895-58.3-66.2 0.890-60.5-68.2 0.885-62.7-70.2 0.880-64.8-72.2 0.875-66.9-74.2 0.870-69.0-76.1 0.865-71.1-77.9 0.860-73.2-79.7 0.855-75.3-81.5 0.850-77.3-83.3 0.845-79.4-85.0 0.840-81.4-86.6
乙醇量测定法(含乙醇相对密度表)
中国药典2000版一部附录 乙醇量测定法 附录Ⅸ M. 乙醇量测定法 一、气相色谱法 本法系用气相色谱法[附录Ⅵ E3.项下,照高效液相色谱法3.(1)测定各种制剂中 在20℃时乙醇(C2H5OH)的含量(%)(ml/ml)。除另有规定外,按下列方法测定。 色谱条件与系统适用性试验用直径为0.25~0.18mm的二乙烯苯-乙基乙烯苯型高 分子多孔小球作为载体,柱温为120~150℃;另精密量取无水乙醇4ml、5ml、6ml,分别 精密加入正丙醇(作为内标物质)5ml,加水稀释成100ml,混匀(必要时可进一步稀释),照气相色谱法(附录Ⅵ E)测定,应符合下列要求: (1)用正丙醇峰计算的理论板数应大于700; (2)乙醇和正丙醇两峰的分离度应大于2; (3)上述3份溶液各注样5次,所得15个校正因子的相对标准偏差不得大于2.0%。 标准溶液的制备精密量取恒温至20℃的无水乙醇和正丙醇各5ml,加水稀释成100 ml,混匀,即得。 供试溶液的制备精密量取恒温至20℃的供试品适量(相当于乙醇约 5ml)和正丙 醇5ml,加水稀释成100ml,混匀,即得。 上述两溶液必要时可进一步稀释。 测定法取标准溶液和供试品溶液适量,分别连续注样3次,并计算出校正因子和供 试品的乙醇含量,取3次计算的平均值作为结果。 【附注】 (1) 在不含内标物质的供试品溶液的色谱图中,与内标物质峰相应的位 置处不得出现杂质峰。 (2)标准溶液和供试品溶液各连续3次注样所得各次校正因子和乙醇含量与其相应的 平均值的相对偏差,均不得大于1.5%,否则应重新测定。 (3) 选用其他载体时,系统适用性试验必须符合本法规定。 二、蒸馏法 本法系用蒸馏后测定相对密度的方法测定各种制剂中在20℃时乙醇(C2H5OH)的含量(%)(ml/ml)。按照制剂的性质不同,分为下列三法。 第一法本法系供测定多数流浸膏、酊剂及甘油制剂中的乙醇含量。根据制剂中含 乙醇量的不同,又可分为两种情况。 1.含乙醇量低于30%者 取供试品,调节温度至20℃,精密量取25ml,置150~200ml蒸馏瓶中,加水约25ml,加玻璃珠数粒或沸石等物质,连接冷凝管,直火加热,缓缓蒸馏,速度以馏出液一滴接一 滴为准。馏出液导入25ml量瓶中,俟馏出液约达23ml时,停止蒸馏。将馏出液温度调节至20℃,加20℃的水至刻度,摇匀,在20℃时按相对密度测定(附录Ⅶ A)项下的方法测定 相对密度。在乙醇相对密度表内查出乙醇的含量(%)(ml/ml),即为供试品中的乙醇含量(%)(ml/ml)。 2.含乙醇量高于30%者 取供试品,调节温度至20℃,精密量取25ml,置150~200ml蒸馏瓶中,加水约50ml,加玻璃珠数粒,如上法蒸馏。馏出液导入50ml量瓶中,俟馏出液约达48ml时,停止蒸馏。调节馏出液温度至20℃,加20℃的水至刻度,摇匀,在20℃时照上法测定相对密度。将查得所含乙醇的含量(%)(ml/ml)与2相乘,即得。
乙醇密度
无水酒精温度密度如下:温度密度 0 0.80625 1 0.80541 2 0.80457 3 0.80374 4 0.80290 5 0.80207 6 0.80123 7 0.80039 8 0.79856 9 0.79872 10 0.79788 11 0.79704 12 0.79620 13 0.79535 14 0.79451 15 0.79367 16 0.79283 17 0.79198 18 0.79114 19 0.79029 20 0.78945 21 0.78860 22 0.78775 23 0.78691 24 0.78606 25 0.78522 26 0.78437 27 0.78352 28 0.78267 29 0.78182 30 0.78097 31 0.78012 32 0.77927 33 0.77841 34 0.77756 35 0.77671 36 0.77585 37 0.77500 38 0.77414 39 0.77329 11 |评论(2)
其他答案共2条 2008-12-29 16:03 不知道抑或知道|八级 乙醇相对密度表—————┬————┬——————┬————┬——————┬————┬——————┬————— 相对密度│ 浓度│相对密度│浓度│相对密度│ 浓度│相对密度│浓度(20℃/20℃)│%(ml/ml)│(20℃/20℃) │%(ml/ml)│(20℃/20℃) │%(ml/ml)│(20℃/20℃) │%(ml/ml —————┼————┼——————┼————┼——————┼————┼——————┼————— 0.9992 │ 0.5 │ 0.9922 │ 5.5 │ 0.9865 │ 10.0 │ 0.9807 │ 15.0 85 │ 1.0 │ 15 │ 6.0 │ 59 │ 10.5 │ 02 │ 15.5 78 │ 1.5 │ 08 │ 6.5 │ 53 │ 11.0 │ │ 70 │ 2.0 │ 02 │ 7.0 │ 47 │ 11.5 │ 0.9796 │ 16.0 68 │ 2.5 │ │ │ 41 │ 12.0 │ 90 │ 16.5 56 │ 3.0 │ 0.9896 │ 7.5 │ 35 │ 12.5 │ 85 │ 17.0 49 │ 3.5 │ 89 │ 8.0 │ 30 │ 13.0 │ 80 │ 17.5 42 │ 4.0 │ 83 │ 8.5 │ 24 │ 13.5 │ 74 │ 18.0 35 │ 4.5 │ 77 │ 9.0 │ 18 │ 14.0 │ 69 │ 18.5 28 │ 5.0 │ 71│ 9.5 │ 13 │ 14.5 │ 64 │ 19.0 0.9758 │ 19.5 │ 0.9670 │ 27.5 │ 0.9566 │ 35.5 │ 0.9439 │ 43.5 53 │ 20.0 │ 64 │ 28.0 │ 58 │ 36.0 │ 30 │ 44.0 48 │ 20.5 │ 58 │ 28.5 │ 51 │ 36.5 │ 21 │ 44.5 43 │ 21.0 │ 52 │ 29.0 │ 44 │ 37.0 │ 12 │ 45.0 37 │ 21.5 │ 46 │ 29.5 │ 36 │ 37.5 │ 03 │ 45.5 32 │ 22.0 │ 40 │ 30.0 │ 29 │ 38.0 │ │ 26 │ 22.5 │ 33 │ 30.5 │ 21 │ 38.5 │ 0.9394 │ 46.0 21 │ 23.0 │ 27 │ 31.0 │ 13 │ 39.0 │ 85 │ 46.5 15 │ 23.5 │ 21 │ 31.5 │ 05 │ 39.5 │ 76 │ 47.0
乙醇含醇量与密度、温度对照表
乙醇密度表 乙醇溶液密度(g/cm³)(20℃) 每(g/cm³)含有乙醇质量(%)g 浓度(体积比%)=度(1度=1%体积) 0.998 0.15 0.2 0.996 1.20 1.5 0.994 2.30 3.0 0.992 3.50 4.4 0.990 4.70 5.9 0.988 5.90 7.4 0.985 7.90 9.9 0.982 10.0 12.5 0.980 11.5 14.2 0.978 13.0 16.0 0.975 15.3 18.9 0.972 17.6 21.7 0.970 19.1 23.5 0.968 20.6 25.3 0.965 22.8 27.8 0.962 24.8 30.3 0.960 26.2 31.8 0.957 28.1 34.0 0.954 29.9 36.1 0.950 32.2 38.8
0.945 35.0 41.3 0.940 37.6 44.8 0.935 40.1 47.5 0.930 42.6 50.2 0.925 44.9 52.7 0.920 47.3 55.1 0.915 49.5 57.4 0.910 51.8 59.7 0.905 53.9 61.9 0.900 56.2 64.0 0.895 58.3 66.2 0.890 60.5 68.2 0.885 62.7 70.2 0.880 64.8 72.2 0.875 66.9 74.2 0.870 69.0 76.1 0.865 71.1 77.9 0.860 73.2 79.7 0.855 75.3 81.5 0.850 77.3 83.3 0.845 79.4 85.0 0.840 81.4 86.6 0.835 83.4 88.2 0.830 85.4 89.8 0.825 87.3 91.2
乙醇密度表
乙醇密度表 乙醇溶液密度 (g/cm³)(20℃) 每(g/cm³)含有乙醇质量 (%)g 浓度(体积比%)=度(1度=1%体 积) 0.998 0.15 0.2 0.996 1.20 1.5 0.994 2.30 3.0 0.992 3.50 4.4 0.990 4.70 5.9 0.988 5.90 7.4 0.985 7.90 9.9 0.982 10.0 12.5 0.980 11.5 14.2 0.978 13.0 16.0 0.975 15.3 18.9 0.972 17.6 21.7 0.970 19.1 23.5 0.968 20.6 25.3 0.965 22.8 27.8 0.962 24.8 30.3 0.960 26.2 31.8 0.957 28.1 34.0 0.954 29.9 36.1 0.950 32.2 38.8 0.945 35.0 41.3 0.940 37.6 44.8 0.935 40.1 47.5 0.930 42.6 50.2 0.925 44.9 52.7 0.920 47.3 55.1 0.915 49.5 57.4 0.910 51.8 59.7 0.905 53.9 61.9 0.900 56.2 64.0 0.895 58.3 66.2 0.890 60.5 68.2 0.885 62.7 70.2
0.880 64.8 72.2 0.875 66.9 74.2 0.870 69.0 76.1 0.865 71.1 77.9 0.860 73.2 79.7 0.855 75.3 81.5 0.850 77.3 83.3 0.845 79.4 85.0 0.840 81.4 86.6 0.835 83.4 88.2 0.830 85.4 89.8 0.825 87.3 91.2 0.820 89.2 92.7 0.815 91.1 94.1 0.810 93.0 95.4 0.805 94.4 96.6 乙醇溶液密度 (g/cm³)(20℃) 每(g/cm³)含有乙醇质量 (%)g 浓度(体积比%)=度(1度=1%体 积) 0.800 96.5 97.7 0.795 98.2 98.9 0.791 99.5 99.7 从中可以计算出:每(g/cm3)含有乙醇重量(%)g 浓度(体积比%)=度(1度=1%体积) 例如:密度为0.791g/cm3 每(g/cm3)含有乙醇重量:0.791×99.5%=0.787045g 浓度:99.7%=99.7度
乙醇-水系统设计举例 挺详细(仅供参考)
目 录 1 概述 (3) 1.1设计依据与原理.................................................................................3 1.2技术来源..........................................................................................3 1.3设计任务.............................................................................................3 2 塔的工艺计算 (4) 2.1最小回流比及操作回流比的确定...............................................................4 2.2塔顶产品产量、釜残液量的计算..................................................................6 2.3理论塔板层数的确定 (6) 2.4实际塔板数P N 及全塔效率的估算...............................................................6 3 塔主要尺寸的设计计算 (8) 3.1精馏段与提馏段的体积流量.....................................................................8 3.2塔径 (10) 3.3塔板尺寸的确定....................................................................................11 3.4塔板结构 (12) 3.4.1堰高..........................................................................................12 3.4.2降液管底隙高度h 0........................................................................11 3.4.3进口堰高和受液盘.....................................................................13 3.4.4浮阀数目及排列........................................................................13 4 流体力学验算及操作性能负荷图 (15) 4.1气体通过浮阀塔板的压力降(单板压降)p h (15) 4.1.1干板阻力c h .................................................................................15 4.1.2由表面张力引起的阻力1h ...............................................................15 4.1.3板上充气液层阻力h .....................................................................15 4.2漏液验算.............................................................................................15 4.3液泛验算.............................................................................................16 4.4雾沫夹带验算.......................................................................................16 4.5操作性能负荷图 (17) 4.5.1雾沫夹带上限线 (17) 4.5.2液泛线……………………………………………………………………………17 4.5.3液体负荷上限线…………………………………………………………………17 4.5.4漏液线……………………………………………………………………………18 4.5.5液相负荷下限线…………………………………………………………………18 4.5.6 操作性能负荷图 (18) 5 辅助设备的计算及选型..............................................................................19 5.1进料管................................................................................................19 5.2釜残液出料管 (19)
乙醇-环己烷气液平衡相图的绘制实验报告
环己烷-乙醇双液系气液平衡相图的绘制 姓名: 学号: 班级: 同组: 成绩 一、实验目的 1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。 2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。 3.掌握阿贝折射仪的使用方法。 二、实验原理 恒定压力下,真实的完全互溶双液系的气-液平衡相图(T -x ),根据体系对拉乌尔定律的偏差情况,可分为3类: (1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。 (2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸—水体系,如图2.7(b)所示。 (3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合 物存在着最低沸点如图2.7(c))所示。 图1 二组分真实液态混合物气—液平衡相图(T-x 图) 本实验以环己烷-乙醇为体系,该体系属于上述第三种类型,在沸点仪(如图2.8)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T -x 相图。 本实验中两相的成分分析均采用折光率法测定。 t A t A t A t B t B t B t / o C t / o t / o C x B x B x B A B A A B B (a) (b) (c) x ' x '
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。溶液的浓度不同、组成不同,折光率也不同。因此可先配制一系列已知组成的溶液,在恒定温度下测其折光率,作出折光率-组成工作曲线,便可通过测折光率的大小在工作曲线上找出未知溶液的组成。 三、仪器与试剂 沸点仪,阿贝折射仪,调压变压器,超级恒温水浴,温度测定仪,长短取样管。环己烷物质的量分数x环己烷为0、0.2、0.4、0.6、0.8、1.0的环己烷-乙醇标准溶液,已知101.325kPa下,纯环己烷的沸点为80.7℃,乙醇的沸点为78.4℃。25℃时,纯环己烷的折光率为1.4264,乙醇的折光率为1.3593。 四、实验步骤 1.环己烷-乙醇溶液折光率与组成工作曲线的测定(略) 2. 无水乙醇沸点的测定 将干燥的沸点仪安装好。从侧管加入约20mL无水乙醇于蒸馏瓶内,并使温度计浸入液体内。冷凝管接通冷凝水。将液体加热至缓慢沸腾。液体沸腾后,待测温温度计的读数稳定后应再维持3~5min以使体系达到平衡。在这过程中,不时将小球中凝聚的液体倾入烧瓶。记下温度计的读数,即为无水乙醇的沸点,同时记录大气压力。 3. 环己烷沸点的测定(略) 4. 测定系列浓度待测溶液的沸点和折光率 同2步操作,从侧管加入约20mL预先配制好的1号环己烷-乙醇溶液于蒸馏瓶内,将液体加热至缓慢沸腾。因最初在冷凝管下端内的液体不能代表平衡气相的组成,为加速达到平衡,须连同支架一起倾斜蒸馏瓶,使槽中气相冷凝液倾回蒸馏瓶内,重复三次(注意:加热时间不宜太长,以免物质挥发),待温度稳定后,记下温度计的读数,即为溶液的沸点。 切断电源,停止加热,分别用吸管从小槽中取出气相冷凝液、从侧管处吸出少许液相混液,迅速测定各自的折光率。剩余溶液倒入回收瓶。 按1号溶液的操作,依次测定2、3、4、5、6、7、8号溶液的沸点和气-液平衡时的气,液相折光率。 五、数据处理
乙醇--水相平衡数据(共115组数据)
n=115 dim x(n),y(n) “乙醇—水相平衡数据如下:” “(x1,x2,x3 ......x115 ) 注意单位是 % 数据必须从小到大排列”data 0.000,.0040,.0117,.0157,.0196,.0235,.0274,.0313,.0352 data .04,.055,.08,.12,.16,.19,.23,.27,.31 data .35,.39,.79,1.19,1.61,2.01,2.43,2.86,3.29,3.73,4.16 data 4.61,5.07,5.51,5.98,6.46,6.86,7.41,7.95,8.41,8.92 data 9.42,9.93,10.48,11.00,11.53,12.08,12.64,13.19,13.77 data 14.35,14.95,15.55,16.15,16.77,17.41,18.03,18.68,19.34 data 20.00,20.68,21.38,22.07,22.79,23.51,24.25,25.00,25.75 data 26.53,27.32,28.12,28.93,29.80,30.61,31.47,32.34,33.24 data 34.16,35.09,36.02,36.93,37.91,38.95,40.00,41.02,42.00 data 43.17,44.27,45.41,46.55,47.72,48.92,50.16,51.39,52.68 data 54.00,55.34,56.71,58.71,59.55,61.02,62.52,64.05,65.64 data 67.27,68.92,70.62,72.36,74.15,75.99,77.88 data 79.82,81.82,83.87,85.97,88.15,89.41 “(y1,y2,y3 ......y115 ) 注意单位是 % 数据必须从小到大排列”data 0.000,.053,.153,.209,.255,.307,.358,.410,.461,.510 data .77,1.03,1.57,1.98,2.48,2.90,3.33,3.725,4.12 data 4.51,8.76,12.75,16.34,18.68,21.45,23.96,26.21,28.12 data 29.92,31.56,33.06,34.57,35.83,36.98,38.06,39.16,40.18 data 41.27,42.09,42.94,43.82,44.61,45.41,46.08,46.90,47.49 data 48.08,48.68,49.30,49.77,50.27,50.78,51.27,51.67,52.04 data 52.43,52.68,53.09,53.46,53.76,54.12,54.54,54.80,55.22 data 55.48,55.74,56.03,56.44,56.71,57.12,57.41,57.70,58.11 data 58.39,58.78,59.10,59.55,59.84,60.29,60.58,61.02,61.44 data 61.76,62.22,62.52,62.99,63.43,63.91,64.21,64.70,65.34 data 65.81,66.28,66.93,67.42,68.07,68.76,69.59,70.29,71.14 data 71.86,72.71,73.61,74.69,75.81,76.93,78.00,79.26,80.42 data 81.83,83.25,84.91,86.40,88.25,89.41 1
乙醇-环己烷气液平衡相图的绘制实验报告
环己烷-乙醇双液系气液平衡相图的绘制 : 学号: 班级: 同组: 成绩 一、实验目的 1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图。 2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理。 3.掌握阿贝折射仪的使用方法。 二、实验原理 恒定压力下,真实的完全互溶双液系的气-液平衡相图(T -x ),根据体系对拉乌尔定律的偏差情况,可分为3类: (1)一般偏差:混合物的沸点介于两种纯组分之间,如甲苯-苯体系,如图1(a)所示。 (2)最大负偏差:存在一个最小蒸汽压值,比两个纯液体的蒸汽压都小,混合物存在着最高沸点,如盐酸—水体系,如图2.7(b)所示。 (3)最大正偏差:存在一个最大蒸汽压值,比两个纯液体的蒸汽压都大,混合 物存在着最低沸点如图2.7(c))所示。 图1 二组分真实液态混合物气—液平衡相图(T-x 图) 本实验以环己烷-乙醇为体系,该体系属于上述第三种类型,在沸点仪(如图2.8)中蒸馏不同组成的混合物,测定其沸点及相应的气、液二相的组成,即可作出T -x 相图。 本实验中两相的成分分析均采用折光率法测定。 t A t A t A t B t B t B t / o C t / o t / o x B x B x B A B A A B B (a) (b) (c) x ' x '
折光率是物质的一个特征数值,它与物质的浓度及温度有关,因此在测量物质的折光率时要求温度恒定。溶液的浓度不同、组成不同,折光率也不同。因此可先配制一系列已知组成的溶液,在恒定温度下测其折光率,作出折光率-组成工作曲线,便可通过测折光率的大小在工作曲线上找出未知溶液的组成。 三、仪器与试剂 沸点仪,阿贝折射仪,调压变压器,超级恒温水浴,温度测定仪,长短取样管。环己烷物质的量分数x环己烷为0、0.2、0.4、0.6、0.8、1.0的环己烷-乙醇标准溶液,已知101.325kPa下,纯环己烷的沸点为80.7℃,乙醇的沸点为78.4℃。25℃时,纯环己烷的折光率为1.4264,乙醇的折光率为1.3593。 四、实验步骤 1.环己烷-乙醇溶液折光率与组成工作曲线的测定(略) 2. 无水乙醇沸点的测定 将干燥的沸点仪安装好。从侧管加入约20mL无水乙醇于蒸馏瓶,并使温度计浸入液体。冷凝管接通冷凝水。将液体加热至缓慢沸腾。液体沸腾后,待测温温度计的读数稳定后应再维持3~5min以使体系达到平衡。在这过程中,不时将小球中凝聚的液体倾入烧瓶。记下温度计的读数,即为无水乙醇的沸点,同时记录大气压力。 3. 环己烷沸点的测定(略) 4. 测定系列浓度待测溶液的沸点和折光率 同2步操作,从侧管加入约20mL预先配制好的1号环己烷-乙醇溶液于蒸馏瓶,将液体加热至缓慢沸腾。因最初在冷凝管下端的液体不能代表平衡气相的组成,为加速达到平衡,须连同支架一起倾斜蒸馏瓶,使槽中气相冷凝液倾回蒸馏瓶,重复三次(注意:加热时间不宜太长,以免物质挥发),待温度稳定后,记下温度计的读数,即为溶液的沸点。 切断电源,停止加热,分别用吸管从小槽中取出气相冷凝液、从侧管处吸出少许液相混液,迅速测定各自的折光率。剩余溶液倒入回收瓶。 按1号溶液的操作,依次测定2、3、4、5、6、7、8号溶液的沸点和气-液平衡时的气,液相折光率。 五、数据处理
汽液平衡数据的测定
百度文库 - 让每个人平等地提升自我 实验报告 课程名称: 化工专业实验 指导教师: 李勇 成绩:_________ 实验名称: 气液平衡数据的测定 同组学生姓名: 一、实验目的和内容 二、实验原理及数据处理依据 三、实验装置与试剂 四、操作方法和实验步骤 五、数据记录及处理 六、实验结论及误差分析 七、分析和讨论 汽液平衡数据是最常用的化工基础数据。许多化工过程如精馏的设计、操作及过程控制等都离不开汽液平衡数据。在热力学研究方面,新的热力学模型的开发,各种热力学模型的比较筛选等也离不开大量精确的汽液平衡实测数据。现在,各类化工杂志每年都有大量的汽液平衡数据及汽液平衡测定研究的文章发表。所以,汽液平衡数据的测定及研究深受化工界人士的重视。 一、实验目的和内容 通过测定常压下乙醇—水二元系统汽液平衡数据的实验,使同学们了解、掌握汽液平衡数据测定的方法和技能,熟悉有关仪器的使用方法,将课本上学到的热力学理论知识与实际运用有机地联系在一起。从而既加深对理论知识的理解和掌握,又提高了动手的能力。 气液平衡测定的种类: 由于汽液平衡体系的复杂性及汽液平衡测定技术的不断发展,汽液平衡测定也形成了特点各异的不同种类。按压力分,有常减压汽液平衡和高压汽液平衡。高压汽液平衡测定的技术相对比较复杂,难度较大。常减压汽液平衡测定则相对较易。按形态分,有静态法和动态法。静态法技术相对要简单一些,而动态法测定的技术要复杂一些但测定较快较准。在动态法里又有单循环法和双循环法。双循环法就是让汽相和液相都循环,而单循环只让其中一相(一般是汽相)循环。在一般情况下,常减压汽液平衡都采用双循环,而在高压汽液平衡中,只让汽相强制循环。循环的好处是易于平衡、易于取样分析。 根据对温度及压力的控制情况,有等温法与等压法之分。一般,静态法采用等温测定,动态法的高压汽液平衡测定多采用等温法。 总之,汽液平衡系统特点各异,而测定的方法亦丰富多彩。 本实验采用的是常压下(等压)双循环法测定乙醇—水的汽液平衡数据。 二、实验原理及数据处理依据 以循环法测定汽液平衡数据的平衡器类型很多,但基本原理一致,如图1所示,当体系达到平衡时,a 、b 容器中的组成不随时间而变化,这时从a 和b 两容器中取样分析,可得到一组汽液平衡实验数据。 当达到平衡时,除了两相的压力和温度分别相等外,每一组分的化学 位也相等,即逸度相等,其热力学基本关系为: V i L i f f = (1) i i i i i x f py ογφ= 装 订 线 专业: 姓名: 学号: 日期: 2015 地点:
