不合格药品

附:铬超标企业及药品(国标限值2mg/kg)
生产企业药品名称胶囊铬含量
青海省格拉丹东药业有限公司脑康泰胶囊 39.064mg/kg
青海省格拉丹东药业有限公司愈伤灵胶囊3.46mg/kg
长春海外制药集团有限公司盆炎净胶囊 15.22mg/kg
长春海外制药集团有限公司苍耳子鼻炎胶囊 17.65mg/kg
长春海外制药集团有限公司通便灵胶囊 37.26mg/kg
丹东市通远药业有限公司人工牛黄甲硝唑胶囊 10.48mg/kg
吉林省辉南天宇药业股份有限公司抗病毒胶囊 3.54mg/kg
四川蜀中制药股份有限公司阿莫西林胶囊 2.69mg/kg
四川蜀中制药股份有限公司诺氟沙星胶囊 3.58mg/kg
修正药业集团股份有限公司羚羊感冒胶囊 4.44mg/kg
通化金马(000766,股吧)药业集团股份有限公司清热通淋胶囊 87.57mg/kg
通化盛和药业股份有限公司胃康灵胶囊 51.45mg/kg
通化颐生药业股份有限公司炎立消胶囊 181.54mg/kg
湖北通报不合格药品涉及亚宝药业、金石粉针剂
公司等企
https://www.360docs.net/doc/416871692.html, 2010年02月05日丽水特快
湖北省食品药品监督管理局发布2009年第三季度《湖北省药品质量公告》。
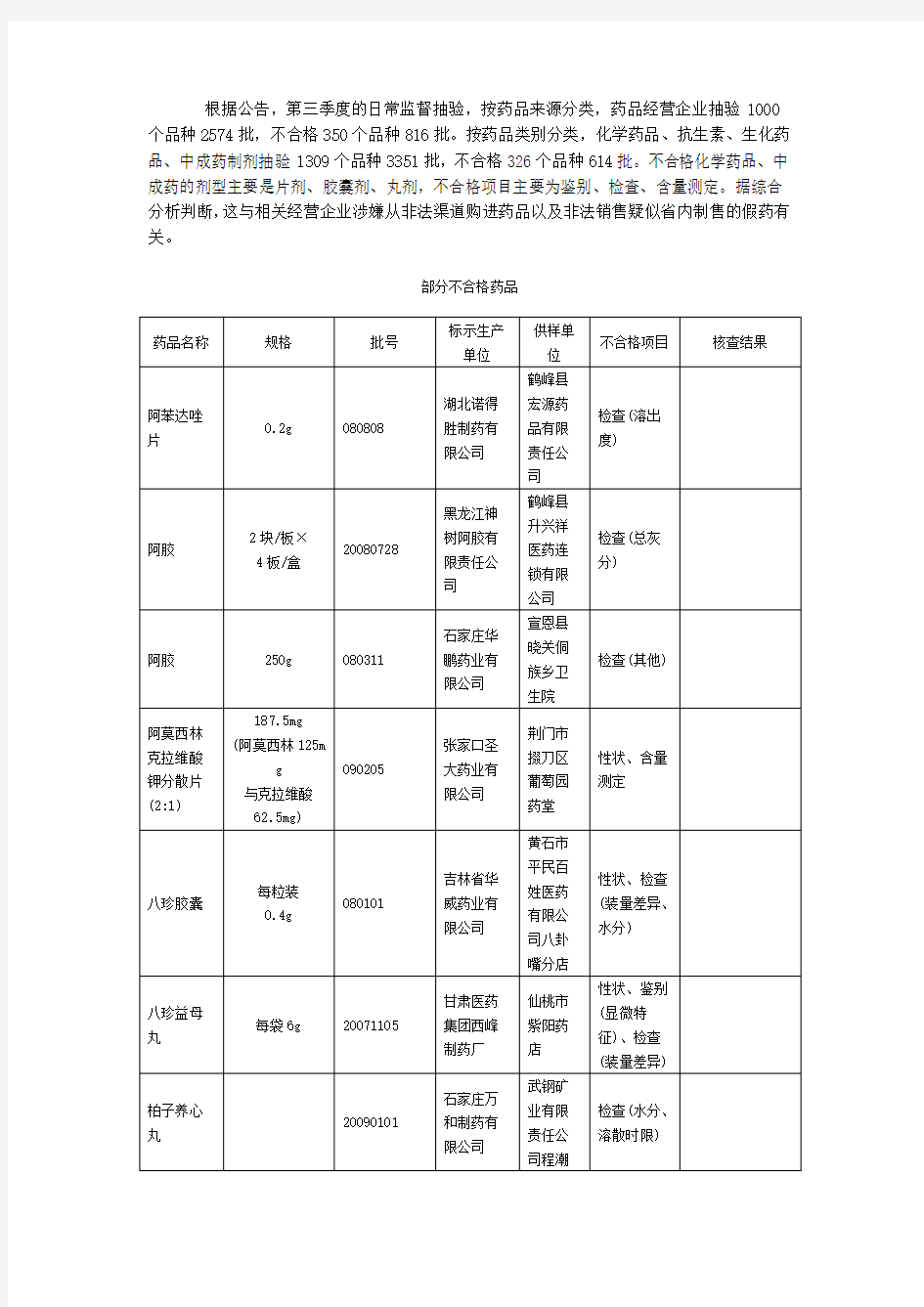
根据公告,第三季度的日常监督抽验,按药品来源分类,药品经营企业抽验1000个品种2574批,不合格350个品种816批。按药品类别分类,化学药品、抗生素、生化药品、中成药制剂抽验1309个品种3351批,不合格326个品种614批。不合格化学药品、中成药的剂型主要是片剂、胶囊剂、丸剂,不合格项目主要为鉴别、检查、含量测定。据综合分析判断,这与相关经营企业涉嫌从非法渠道购进药品以及非法销售疑似省内制售的假药有关。
部分不合格药品
不合格药品管理规定
不合格药品管理规定 This model paper was revised by the Standardization Office on December 10, 2020
不合格药品管理制度 1、不合格药品是指:药品的包装不合格、外观质量不合格、内在质量不合格。 2、不合格药品的确认: (1)国家或省、市各级药品监督管理部门发布的通知或质量公报中的不合格药品。 (2)质量验收、保管养护和销售过程中发现的外观、包装、标识不符, 包装污染、破碎及超过有效期的药品,并报质量管理员确认为不合格的.(3)各级药品监督管理部门抽查检验不合格的药品。 (4)符合药品管理法中有关假、劣药品定义的。 (5)生产厂商、供货单位来函通知的不合格药品。 3、不合格药品一旦确认,即不能再销售,将不合格药品移入不合格区,并做好“不合格药品台帐”记录. 4、入库验收发现不合格药品,验收员填写“药品拒收报告单”交质量管理员,由质量管理员确认后,提出处理意见进行处理。 5、在储存、养护或出库时发现质量有疑问药品,应立即挂黄牌暂停销
售,填写“药品质量复查通知单”交质量管理员复验。复验合格,摘除黄牌;不合格,将不合格品移入不合格品区,填写“药品质量处理通知单”进行处理。 6、在门诊陈列、检查、销售过程中发现不合格药品应停止销售,立即下柜。 7、凡药监局公告或发文通知不合格的药品,以及抽查检验发现的不合格药品,应立即清查,集中存放于不合格区内,按要求上报。 8、各环节发现的不合格药品,均应及时报质量管理员,质量管理员每季度对不合格药品进行汇总和分析,分清质量责任,制定处理和预防措施. 9、对于包装破损或者包装不符合规定的不合格药品,可由采购员根据协议及时联系退货处理;对过期失效药品、超过供货商负责期的有质量问题药品、属假劣药品范围的不合格药品应报废,并在药品监督管理部门的监督下进行销毁处理。 10、不合格药品的确认、报告、报损、销毁应有完善的手续和记录。
保健食品安全管理制度 不合格产品处理制度示范文本
保健食品安全管理制度不合格产品处理制度示范 文本 In The Actual Work Production Management, In Order To Ensure The Smooth Progress Of The Process, And Consider The Relationship Between Each Link, The Specific Requirements Of Each Link To Achieve Risk Control And Planning 某某管理中心 XX年XX月
保健食品安全管理制度不合格产品处 理制度示范文本 使用指引:此管理制度资料应用在实际工作生产管理中为了保障过程顺利推进,同时考虑各个环节之间的关系,每个环节实现的具体要求而进行的风险控制与规划,并将危害降低到最小,文档经过下载可进行自定义修改,请根据实际需求进行调整与使用。 为有效控制不合格保健食品的管理,保证所经营保健 食品的质量符合规定要求,特制定本制度。 1、质量管理部是负责对不合格保健食品实行有效控制 管理的机构。 2、质量不合格保健食品不得采购、入库和销售。 3、不合格保健食品须存放在不合格品区,挂有红牌标 志,不合格品库设专人、专帐管理。 4、保健食品安全管理人员在检查保健食品的过程中发 现不合格保健食品,应开具停售通知单,及时通知仓储 部、业务部门立即停止出库和销售,追回售出保健食品, 不合格保健食品及时移入不合格品区。发现假、劣产品,
要报告食品药品监督管理局,不得擅自退货。 5、食品药品监督管理局抽查、检验判定为不合格保健食品时,或食品药品监督管理局公告、发文、通知查处发现的不合格保健食品时,应立即停止销售,并追回售出的不合格保健食品,将不合格保健食品移入不合品区。 6、在库过期失效、破损保健食品由保管员填写《报损审批表》,经保健食品安全管理负责人签字确认后移入不合格品库,销毁时仓储部应填写《销毁清单》,报保健食品安全管理负责人审核后,由总经理批准。 7、销后退回、配送退回的质量可疑保健食品,验收员及时报保健食品安全管理员确认不合格后,移不合格品库。 8、不合格保健食品的报损和销毁应有记录,保存二年。 9、保健食品安全管理人员会同业务部每半年对不合格
不合格药品处理程序
不合格药品的确认与处理质量控制程序 1.目的:根据《药品管理法》、《药品流通监督管理办法》、GSP及实施细则,对不合格品进行控制性管理,确保不合格药品不入库或出库,保证人民用药安全。2.范围:本程序规定了企业不合格药品控制性管理的内容、方法和要求,明确了相关部门或人员的职责,适用于对药品进货验收、在库储存养护、出库复核、销后退回全过程,发现不合格药品的报告、确认与处理控制。 3.职责: 1、质管部负责对不合格药品的确认,上报药监局,监督、销毁,并作记录。 2、仓库不合格品区由专人专帐保管,其保管负责不合格品报损。 3、质管部会同业务部向供方进行质量查询。 4、程序和内容: 4.1不合格药品的范围界定: 4.1.1、依据《药品管理法》中假、劣药定义划定不合格药品; 4.1.2、质量验收、保管养护、出库验发时发现的外观质量及包装质量不符合法定质量标准的药品; 4.1.3、国家或各级药品监督管理部门发文通知禁止销售的品种,或质量公报中的不合格药品。 4.1.4、法定的药品检验机构的报告书所示的不合格品。 4.2不合格药品的报告与确认 4.2.1、入库验收环节发现不合格药品的报告与确认 4.2.1.1验收员对购进药品及销售退回药品在入库验收时发现的内在不合格情况,应立即填写《药品拒收通知单》向质量管理部进行报告。
4.2.1.2质量管理部接到不合格情况报告后,应在12小时内对所报告的药品进行质量确认,必要时送药品检验机构检验,依据检验结果处理整批货。如为假劣药品由质管部封存于不合格品区并立即上报药监部门。 4.2.2、在库储存、养护检查过程发现不合格药品的报告与确认 4.2.2.1在库药品储存、养护检查过程发现的不合格情况应立即填写《药品质量复查通知单》向质量部进行报告。 4.2.2.2质量管理部接到药品养护员的不合格情况报告后,应在12小时内开始对不合格情况进行复查,必要时送药品检验所进行检验,依据检验结果进行处理。 4.2.3药品销售环节发现不合格药品的报告与确认。 4.2.3.1对于销售过程及已销售出药品发现的不合格情况,包括质量投诉情况,业务部在得知相关信息后,应立即填写《信息传递反馈单》向质量管理部进行报告; 4.2.3.2质量管理部接到销售过程发现的不合格情况报告后,质管部应在12小时内对售出药品的不合格情况进行复查,必要时送药品检验所进行检验,依据检验结果进行处理。 4.3不合格的标识与处理 4.3.1、入库验收环节发现不合格药品的标识与处理 4.3.1.1进货药品在入库验收环节发现并经确认的内在质量不合格药品,应存放于不合格区,悬挂红色不合格品标志牌,注明不合格项目等有关内容。属外观质量不合格的药品应拒收,由质管部、业务部向供方查询,联系进行处理。 4.3.1.2销后退回药品在入库验收环节发现并经确认的外在质量不合格药品,应存放于不合格品区,悬挂红色不合格品标志牌,注明不合格项目等有关内容;如未超过规定效期或供方负责期,由业务部与供方交涉,符合退货条件的,按《购进退出药品管理程序》执行,如内在质量不合格,应执行第(四)程序。 4.3.2、在库储存、养护检查过程发现不合格药品的标识与处理 养护检查过程已确认的不合格药品,应立即挂红色不合格标志牌,移入不合格品区,并进行质量分析,查明原因,分清责任,制定预防措施。
不合格药品、药品销毁管理制度
惠康药房质量管理制度文件名称:不合格药品、药品销毁管理制度编号:SZHKQM0142013 起草人:审阅人:批准人:起草日期:2013.7.31 批准日期:2013.10.02 执行日期:2012.10.03 版本号:04 变更记录:变更日期:发至部门:购进、营业、养护、质管。目的:严格不合格药品的控制管理,严防不合格药品购进、陈列、售出,确保消费者用药安全。依据:《药品经营质量管理规范》及其实施细则。一、质量管理员负责对不合格药品实行有效管理。二、质量不合格药品不得采购、陈列和销售。凡与法定质量标准及有关规定不符的药品,均属不合格药品,包括:1、药品的内在质量不符合国家法定质量标准及有关规定的;2、药品的外观质量不符合国家法定质量标准及有关规定的;3、药品包装、标签、说明书,批号,有效期等不符合国家有关规定的;4、质量证明文件不合格的药品5、来源不符合规定的药品。6、药监部门发文要求停止使用的药品7、对药品的内在质量有怀疑而不能确定其质量状况时,应抽样送市药品检验所检验。三、在药品购进验收时发现不合格药品,验收员应在验收记录中说明,填写《药品拒收报告单》,
同时药品移入不合格药品区,并报质量管理人员进行复核;经质量管理人员确认为不合格的药品,视合同是否允许退货情况按相应手续进行。1、在养护检查中,发现质量可疑药品,养护员应将药品移入待验区或挂上黄色的“质量可疑”标志,填写《不合格(可疑)药品确认、报告表》,并向质量管理员报告,经复核确认为不合格的药品,应将其存放在红色标志的不合格品区,并通知将该批号药品撤离柜台,不得继续销售;如复核确认不属于不合格药品,应将药品移回合格区或去除“质量可疑”标志。2、已确认的不合格药品如购销合同规定可以退货的情形(假劣药品不得退货),将药品移入退货区,按退货手续办理,不能退货的品种进入按报损程序处理。3、在调配过程中由于操作失误(如将药品掉落地面造成药品污染等情况)产生不合格药 - 28 - 品,可简化程序,将药品移入不合格药品区,填写《不合格 药品报损审批表》,报质量负责人处理。4、售后使用过程中出 现质量问题的药品,由质量管理人员依据顾客意见及具体情况 协商处理。四、质量管理员在检查中发现不合格药品,应出具 不合格药品通知单,及时通知营业员立即停止销售,同时将不 合格药品存入于不合格区,挂红色标识。五、上级药品监督管 理部门检查、抽验发现不合格品,应立即停止销售,同时将不
药品不合格品处理流程以及客户投诉
药品不合格品处理流程以及客户投诉 1、目的: 建立用户投诉处理的管理制度。 2、范围: 所有的用户投诉。 3、责任: 质量部及销售部负责人。 4、内容: 4.1、用户投诉处理人须由质管部或企业相关部门授权人担任,具有丰富的专业知识和工作经验,能对用户意见进行评价,负责用户意见处理过程的全部管理工作。 4.2、所有用户意见需及时转到用户投诉处理人手中,其他人不得擅自处理。 4.3、收到用户投诉后填写用户投诉处理单,用户投诉处理人须立即查明投诉原因,并对此进行评价,确定问题的性质和类别,按规定的工作程序及时处理,并及时填写用户投诉处理单。 4.4、用户投诉的分类 A类:一般的质量问题,如改换包装后的误解、外包装轻微破损。 B类:可能引起麻烦或导致销售用户的使用的问题,如误贴标签、稳定性下降等。 4.5、用户投诉类别不同,其处理方法不同,但在调查处理结束后,均应以书面形式报质量部。 4.5.1 A类处理程序: 4.5.1.1收到以用户投诉后,只需提出文字或口头答复就能满足用户用户要求的,处理负责人必须立即或3日内答复,必要时可给予样品:
4.5.1.2需调查后答复的,应立即向有关部门调查了解产生的原因,做好记录,一周内向用户须向用户做出答复,如不属于企业产品质量问题,也要向用户解释清楚; 4.5.1.3建立用户投诉记录,内容包括:品名、规格、批号、数量,投诉单位(个人)、投诉日期,用户主要意见、调查结果、处理方法、答复日期、处理负责人签名等。 4.5.1.4用户意见资料的归档:所有用户意见均应建立记录,并编号,保存至产品有效期 4.5.2 B类处理程序: 4.5.2.1接到用户投诉后,处理负责人填写用户投诉记录,内容同A类,同时向总经理报告; 4.5.2.2公司内部自查: a、检查批生产记录:投料是否正确,时间控制是否符合处方要求,物料平衡是否符合限度,生产过程重要物理参数记录是否异常,记录是否完整、正确; b、批包装记录:包装材料检查配套情况,标签领发和销毁记录,物料平衡情况等; c、批现场监控记录:主配方审核,原料外观抽查情况,过程监控异常情况,清场检查,包装检查,半成品化验情况,各种物料放行流转情况; d、批化验记录:原料检验记录是否正确,是否为定点采购厂家,检验数据符合规定限度,检测项目齐全,半成品化验、取样正确,检验方法使用正确。 4.5.2.3检查产品留样的质量情况,确认问题产生的原因。
不合格药品管理制度(新编版)
( 安全管理 ) 单位:_________________________ 姓名:_________________________ 日期:_________________________ 精品文档 / Word文档 / 文字可改 不合格药品管理制度(新编版) Safety management is an important part of production management. Safety and production are in the implementation process
不合格药品管理制度(新编版) 1、不合格药品是指:药品的包装不合格、外观质量不合格、内在质量不合格。 2、不合格药品的确认: (1)国家或省、市各级药品监督管理部门发布的通知或质量公报中的不合格药品。 (2)质量验收、保管养护和销售过程中发现的外观、包装、标识不符,包装污染、破碎及超过有效期的药品,并报质量管理员确认为不合格的. (3)各级药品监督管理部门抽查检验不合格的药品。 (4)符合药品管理法中有关假、劣药品定义的。 (5)生产厂商、供货单位来函通知的不合格药品。 3、不合格药品一旦确认,即不能再销售,将不合格药品移入不合格区,并做好“不合格药品台帐”记录.
4、入库验收发现不合格药品,验收员填写“药品拒收报告单”交质量管理员,由质量管理员确认后,提出处理意见进行处理。 5、在储存、养护或出库时发现质量有疑问药品,应立即挂黄牌暂停销售,填写“药品质量复查通知单”交质量管理员复验。复验合格,摘除黄牌;不合格,将不合格品移入不合格品区,填写“药品质量处理通知单”进行处理。 6、在门诊陈列、检查、销售过程中发现不合格药品应停止销售,立即下柜。 7、凡药监局公告或发文通知不合格的药品,以及抽查检验发现的不合格药品,应立即清查,集中存放于不合格区内,按要求上报。 8、各环节发现的不合格药品,均应及时报质量管理员,质量管理员每季度对不合格药品进行汇总和分析,分清质量责任,制定处理和预防措施. 9、对于包装破损或者包装不符合规定的不合格药品,可由采购员根据协议及时联系退货处理;对过期失效药品、超过供货商负责期的有质量问题药品、属假劣药品范围的不合格药品应报废,并在
不合格药品的确认和处理程序
1/2 1.目的:规范不合格药品管理,保证经营药品质量。 2.范围:适用于不合格药品处理的全过程。 3.责任:质量管理部负责对不合格药品的确认、报告、报损、销毁全过程实施控制性管理。 4.内容: 4.1 在药品入库验收和退货药品验收过程中,验收员发现不合格品时(包括包装质量不符合要求,内在质量不符合 要求,超过有效期等情况的品种)应: 4.1.1不属于内在质量问题的应拒收,不得入库; 4.1.2 属于内在质量问题的不能退货,应填写“不合格药品报告确认表”; 4.1.3确认为不合格品的药品应存放于不合格品库,挂红牌标志; 4.1.4发现假劣药,及时通知供货方,并报告当地药品监督管理局,不得擅自退货。 4.2在检查、养护库存药品或出库复核过程中发现不合格品时应: 4.2.1立即停止发货和出库,通知质量管理员电脑调成“停售”状态,并填写“不合格药品报告确认表”报告 质量管理部,并通知储运部、销售部停止销售和使用,并追回售出药品,不合格药品应及时移入不合格品库。 4.2.2质量管理部应及时进行质量查询,分清质量责任,与供货单位协商处理,挽回损失。并追回已销出的不 合格药品,将不合格药品移放于不合格药品库。 4.3上级药监部门抽查、检验判定为不合格品,或上级药监、药检部门公告、发文、通知查处不合格品时应: 4.3.1立即停止销售,并按销售记录追回已售出的不合格品; 4.3.2 将不合格药品移入不合格品库。 4.4不合格品的报损、销毁,应按以下规定进行: 4.4.1不合格品的报损由仓储运输部填写“药品报损审批表”,经部门经理审核批准后报损;同时报质量管理部 确认,业务部、财务部审核、并报企业负责人批准。 4.4.2不合格药品报损后需作销毁处理时,应在质量管理部和其他有关部门的监督下进行并填写“不合格药品销 毁记录”。 4.4.3对质量不合格的药品,应查明原因,分清责任,及时制定并采取纠正和预防措施。 4.5不合格品的上报 4.5.1储运部应及时做好药品报损登记,并按季送质量管理部统计汇总,重大不合格药品事件应随时上报; 4.5.2公司质量管理部对公司不合格品情况上报企业负责人。 4.6及时做好不合格药品处理记录,记录应保存三年。 4.7不合格药品的确认和处理流程图
不合格药品处理程序
不合格药品处理程序 1.目的: 通过制定实施本程序,使不合格药品的确认和处理规范化,以保证不合格药品得到及时、有效的控制和处理,不再流入经营渠道。 2.范围: 适用于不合格药品处理的全过程。 3.职责: 采购部、营销部、物流事业部、质管部对本程序的实施负责。 4.程序: 4.1入库验收和销售退货发现不合格品应按以下程序处理: 4.1.1药品到货时,收货人员应当核实运输方式是否符合要求,并对照随货同行单(票)和采购记录核对药品,做到票、账、货相符,不符合要求拒收。 4.1.2冷藏、冷冻药品到货时,应当对其运输方式及运输过程的温度记录、运输时间等质量控制状况进行重点检查并记录。对温度不符合要求的应当拒收,保存采集到的温度数据,将药品隔离存放于符合规定要求的温度环境中,并报质量管理部门处理;对销后退回的药品,要严格检查温度控制状况,售出时间较长的,要求退货方提供温度控制说明文件及售出期间相关温度控制数据,不能提供相关文件及数据的,不得收货。 4.1.3对未按规定加印或者加贴中国药品电子监管码,或者监管码的印刷不符合规定要求的,验收员应当拒收。监管码信息与药品包装信息不符的,应当及时向供货单位查询,未得到确认之前不得入库,必要时向当地药品监督管理部门报告。 4.1.4 对验收不合格的药品(包装破损的除外),应填写《药品质量处理通知单》,报质管部确认。 4.1.5质管部对药品进行确认,怀疑为假药的,及时报告药品监督管理部门。确认为不合格药品的,验收员填写《拒收报告单》,注明不合格事项及处置措施,交采购部联系退换货事宜,同事通知财务部对该批药品拒付货款。如为销售退货,验收员应在《销售退回验收记录》上注明“质量不合格”的结论。 4.1.6确认为不合格品的应存放于不合格品区,挂红牌标志;并记入不合格药品台账。 4.2在检查库存药品(盘存、养护等)或出库复核过程中发现不合格品的处理:4.2.1由保管员、养护员在可疑质量问题的药品上挂“暂停发货牌”并有效隔离,不得销售,立即通知质量管理部门处理,质管部立即在计算机系统中填写《药品
供应商不合格品处理办法
” ” 一、目的: 为了有效督促零部件供应商积极开展质量改进工作,确保不合格品对外索赔工作的顺利开展。 二、范围: 适用于来料检验、制程发现及客户退回的不合格品(即市场三包件)的管理。 三、权责单位: 1. 品质部:负责组织不合格品的最终判定,并督促责任部门或供应商采取纠正预防措施。 2. 售后部:负责客户退回不合格品的初步判定。 3. PMC 部:负责与供应商联络和通传,并督促供应商采取纠正预防措施。 4. 财务部:负责对不合格品的财务核算。 四、作业流程:附件一 五、作业说明: 1.对于来料检验中发现的不合格品,经评审后需特采处理时,应由品质部按照附件二规定在“特 采申请单”上注明特采降价比率,对供应商进行索赔处理。 1.1 对于来料检验中发现的不合格品,经评审后不能特采时,由仓库将不合格品退回供应商。 2. 对于制程中发现的不合格品,由发现单位填写 “不合格品处理通告单”交品质部处理。 2.1 经判定为不合格品由品质部贴“制程不合格品”黄色标签;按附件二规定签发“质量索赔通知 单”对供应商进行索赔处理。 3. 对于客户退回的不合格品,先由售后服务部进行初步判定统计并填写“奔马公司配件接收 明细表”随附带“故障实物卡”交品质部作最终判定,必要时对不合格品填写“质量整改及处理 单。 3.1 对于经品质部判定不属三包范围或非本厂的不合格品由售后服务部退回销售商。 3.2 经判定为索赔的不合格品应由品质部贴 “市场不合格品”红色标签;按照附件二规定签发“质 量索赔通知单,对供应商进行索赔处理。 4. PMC 部根据“特采申请单”、“不合格品处理通知单、“质量索赔通知单”的处理结论及时通传供
医药公司不合格药品管理规定
医药公司不合格药品管理规定1.目的:为规范不合格品的管理、加强对经营过程中发现的不合格品的控制管理,防止不合格药品销售出库,特制定本管理规定。 2.范围:适用于本企业药品经营过程中发现的不合格品的控制管理。 3.定义: 3.1 不合格品:本规定所称不合格品是指凡不符合国家有关法律、法规、行政规章相关规定的药品和不符合法定质量标准的药品。 4.内容: 4.1 不合格药品的范围 4.1.1符合《药品管理法》规定的假药、劣药定义或假药、劣药范畴的药品。 4.1.2国家或省、市各级药品监督管理部门发布的通知或质量公报中的不合格品。 4.1.3经国家或省、市各级药品监督管理部门抽检发现的不合格品。 4.1.4包装出现破损污染、受潮污染、封口不牢、封条损坏等异常情况的药品。 4.1.5包装或标签上所示内容与实物不符、模糊不清或脱落等情况的药品。 4.1.6外观质量发生变化,已不符合质量标准的药品。 4.1.7由质量管理部门依据国家或企业有关规定,确认为不符合规定的药品。 4.2 不合格品的确认 4.2.1本企业经营的药品发现不合格,由质量管理部门进行确认。被确认为不合格的药品,应立即停止购进和销售,需要召回的应立即召回。 4.2.2在购进药品到货验收、销后退回药品到货验收、库存药品养护、药品出库复核、运输配送等环节中发现不合格品或疑似不合格品的确认程序,按公司《不合格品确认与处理程序》执行。 4.3 不合格药品的存放与标志 4.3.1经确认的不合格药品,实物应存放在不合格品库区并做好《不合格药品台帐》记录,不合格品库区应有明显的红色标志。 4.3.2对库存中发现并确认的不合格药品,应在计算机管理信息系统中进行库位转移实施控制,仓库保管员按移库单的库位指令将不合格药品存放在不合格品库区。 4.3.3对销后退回的不合格药品,应在计算机管理信息系统中直接退入不合格品库位,保管员按流转单的库位指令将不合格药品存放在不合格库区。
不合格药品处理操作规程
一、目的:通过制定实施不合格药品质量管理操作规程,有效控制不合格药品的处理过程,以保证经营药品的质量符合规定的要求。二、职责:质量管理部、业务部负责对不合格药品的确认、报告、报损、销毁全过程实施控制性管理。 三、范围:适用于不合格药品处理的全过程。 四、主要内容: 1.不合格药品的定义: 凡不符合国家有关法律、法规,不符合药品质量标准,包装不符合规定以及药监部门明文规定禁止销售的药品均属不合格药品。有以下情形的,按不合格品处理: 1.1《药品管理法》规定的假药、劣药。 1.2质量证明文件不合格的药品。 1.3包装、标签、说明书内容不符合规定的药品。 1.4包装破损、被污染,影响销售和使用的药品。 1.5批号、有效期不符合规定的药品。 1.6各级药品监督管理部门公告的抽检不合格的。 1.7各级药品监督管理部门发文通知禁止销售的。 1.8质量管理部抽样送检确认不合格的。 2.不合格药品的处理: 2.1购进验收时发现不合格药品的:
2.1.1验收员进行验收时,填写《药品采购入库质量验收记录单》后,根据拒收数量自动生成《药品拒收报告单》报质量管理部。质量管理人员依据《药品拒收报告单》所反映的情况,依据国家有关法规及企业内部有关规定,对验收过程中质量有疑问的药品进行复核,确认为不合格药品的予以审核,通知采购员填写《到货拒收单》,及时通知供货方,并按购销合同或质量保证协议的有关规定进行处理,并通知保管员将货物放到退货区,同时若确认为不合格品的药品应存放于不合格品库(区); 2.1.2验收员进行验收时,填写《药品采购入库质量验收记录单》后,如填写了不合格品数量,则通知质量管理人员进行处理判定,质量管理员根据实际情况,并依据判定标准,做出相应的处理意见,在系统内参照生成《不合格品处理审批单》,并经过质管部负责人、质量负责人二级审批后,将确认为不合格品的药品存放于不合格品库(区),做好标识,等待处理,处理意见一般分为三种,直接报损,入库报损,先暂存后退货。 2.1.3处理意见为直接报损:质管员填制《不合格品记录单》,之后保管员填制《不合格品报损审批表》,经业务部经理、质量管理部经理、财务部经理、质量负责人签署审批通过后,质量管理部出具《不合格药品报废销毁审批表》,指导相关人员按法律法规要求将不合格药品进行处理,并及时在系统中维护《不合格药品报废销毁记录》,登记《药品销毁记录》,系统自动生成《不合格药品台账》。 2.1.4处理意见为入库报损:业务部根据《不合格品处理审批单》的结果,办理入库业务,后按照2.1.3的处理规程执行 2.1.5处理意见为先暂存后退货:业务部根据《不合格品处理审批单》的结果,办理入库业务,后按照《销售退回操作规程》执行。 2.1.6在销后退回验收时有发现可疑或不合格药品的,应按照2.1所规定的处理规程处理。 2.2在库内检查、养护过程、出库复核时发现不合格药品的: 2.2.1保管员、养护员或复核员在工作发现药品质量可疑或不合格药
药品不合格品处理-
1、目的:建立不合格产品的处理程序,防止不合格产品混淆、误用或出厂。 2、范围:本公司所有不合格的产品。 3、责任者:质保部、生产部、仓储部、中心化验室、生产车间 4、程序: 4.1 不合格品分类 4.1.1 不合格成品:成品检验不合格的、经审查不同意放行的、超出有效期的、退回及召回的不合格成品以及产品储存期内发生质量变化导致不合格的产品。 4.1.2 不合格半成品(中间体):生产过程中产生的不符合半成品质量标准的。 4.2 处理流程 4.2.1 不合格成品 4.2.1.1 成品检验不合格的:中心化验室出具不合格检验报告单,注明不合格项,交质保部及仓储部各一份,仓储部将产品放至不合格品区,并作相应的标识。中心化验室按《偏差处理》规定及时上报偏差。相关部门按偏差处理措施进行相应的处理。 4.2.1.2 经审核不同意放行的:仓储部接到不同意放行的成品放行单后,将产品移至不合格品区,并作相应的标识。 4.2.1.3 产品超出有效期的:应及时将产品移入不合格品区,并作相应的标识。 4.2.1.4 不合格品标识:应在每件不合格产品包装上粘贴醒目的红色不合格牌。 4.2.1.5 退回及召回的产品分别按《产品退货及处理和《产品召回及处理》程序进行。 4.2.1.6产品在储存期内发生质量变化导致不合格的产品,发现部门应及时按《偏差处理》规定及时上报偏差。相关部门按偏差处理措施进行相应的处理。 4.2.1.7 库存不合格产品处理,应由仓储部填写《不合格品处理申请单》(附件1),经质保部审核并签署处理意见,质量管理负责人批准后,相关部门应按处理意见进行处理。 4.2.1.7.1 处理意见涉及产品销毁的,由仓储部安排销毁,销毁过程中由质保部负责监销。 4.2.1.7.2处理意见涉及返工的,应将处理意见及时发放给生产部、生产车间、仓储部及中心化验室。由生产部根据生产计划,安排车间进行返工,仓储部与生产车间做好产品的交接;原料药若因内在质量需返工的,中心化验室对返工后批次进行长期稳定性考察。
不合格药品管理制度
不合格药品管理制度 1、药品是用于防病治病的特殊商品,其质量与人体的健康密切相关。为严格不合格药品的控制管理,严防不合格药品进入或流出本企业,确保消费者用药安全,特制定本制度。 2、质量管理部是企业负责对不合格药品实行有效控制管理的机构。 3、质量不合格药品不得采购、入库和销售。凡与法定质量标准及有关规定不符的药品,均属不合格药品: (1)定量检测(即含量测定)结果不符合法定质量标准及有关规定的药品;(2)定性检测(即理化鉴别)结果不符合法定质量标准及有关规定的药品;(3)细菌检测(即微生物测定)结果不符合国家有关规定的药品; 4、在药品入库验收过程中发现不合格药品,应存放于药品库(区),挂红牌标志。报质量管理部门同时填写有关单据,通知财务部门拒付货款,并及时通知供货方,确定退货或报废销毁等处理办法。 5、质量管理部在检查药品的过程中发现不合格药品,应出具药品质量报告书或不合格药品通知单,及时通知仓储部门、配货部门和各零售连锁门店立即停止出库、配送和销售。同时,按配送记录追回已发到各连锁门店的不合格品,集中存放于配送中心不合格药品库,挂红牌标志。 6、在药品养护过程或出库、复核过程中发现不合格药品,应立即停止配送和发运。同时,按配送记录追回已发出的不合格药品。并将不合格药品移放于不合格药品库(区),挂红牌标志。 7、上级药监部门抽查、检验判定为不合格品时,或上级药监、药检部门公告、发文、通知查出发现的不合格品,企业应立即通知各部门及连锁门店停止配送和销售。同时,按配送记录追回发出的不合格品。并将不合格品移入不合格药品库(区),挂红牌标志,等待处理。 8、不合格药品应按规定进行报废和销毁。 (1)不合格药品的报损、销毁由配送中心统一管理,各连锁门店不得擅自销毁不合格药品; (2)不合格药品的报损、销毁由仓储部门提出申请,填报不合格药品报损有关单据;
不合格药品管理制度
不合格药品管理制度 1、不合格药品是指:药品的包装不合格、外观质量不合格、内在质量不合格。 2、不合格药品的确认: (1)国家或省、市各级药品监督管理部门发布的通知或质量公报中的不合格药品。 (2)质量验收、保管养护和销售过程中发现的外观、包装、标识不符, 包装污染、破碎及超过有效期的药品,并报质量管理员确认为不合格的.(3)各级药品监督管理部门抽查检验不合格的药品。 (4)符合药品管理法中有关假、劣药品定义的。 (5)生产厂商、供货单位来函通知的不合格药品。 3、不合格药品一旦确认,即不能再销售,将不合格药品移入不合格区,并做好“不合格药品台帐”记录. 4、入库验收发现不合格药品,验收员填写“药品拒收报告单”交质量管理员,由质量管理员确认后,提出处理意见进行处理。 5、在储存、养护或出库时发现质量有疑问药品,应立即挂黄牌暂停销售,填写“药品质量复查通知单”交质量管理员复验。复验合格,摘除黄牌;不合格,将不合格品移入不合格品区,填写“药品质量处理通知单” 进行处理。 6、在门诊陈列、检查、销售过程中发现不合格药品应停止销售,立即下柜。 7、凡药监局公告或发文通知不合格的药品,以及抽查检验发现的不合格药品,应立即清查,集中存放于不合格区内,按要求上报。 8、各环节发现的不合格药品,均应及时报质量管理员,质量管理员每季度对不合格药品进行汇总和分析,分清质量责任,制定处理和预防措施. 9、对于包装破损或者包装不符合规定的不合格药品,可由采购员根据协议及时联系退货处理;对过期失效药品、超过供货商负责期的有质量问 题药品、属假劣药品范围的不合格药品应报废,并在药品监督管理部门的 监督下进行销毁处理。 10、不合格药品的确认、报告、报损、销毁应有完善的手续和记录。
不合格药品管理制度
不合格药品管理制度 药品是用于防病治病的特殊商品,其质量与人体的健康密切相关。为严格不合格药品的控制管理,严防不合格药品发放,确保消费者用药安全,特制定本制度。 1、质量不合格药品不得采购、入库、销售和使用。凡与法定质量标准及有关规定不符的药品,均属不合格药品,包括: ①药品的内在质量不符合国家法定质量标准及有关规定的药品; ②药品的外观质量不符合国家法定质量标准及有关规定的药品; ③药品包装、标签及说明书不符合国家有关规定的药品; ④法定药检所的检验报告中确定的为假药、劣药的药品; ⑤食品药品监管部门下达的有关药品质量问题的文件、通知及质量通报等的药品。 2、在药品验收、储存、养护、上柜、销售、使用过程中发现不合格药品,应放于不合格药品库(区),及时进行处理。 3、在检查过程中发现不合格药品,应及时通知仓储、使用等岗位立即停止出库和使用,同时将不合格品集中存放于不合格药品库,及时处理。
4、上级食品药品监管部门监督检查、抽验发现不合格品,应立即停止销售、使用。同时,将不合格品移入不合格药品库(区),做好记录,等待处理。 5、不合格药品应按规定进行报损和销毁 ①不合格药品的报损、销毁由质量管理小组统一负责,其他各岗位不得擅自处理、销毁不合格药品; ②不合格药品的报损、销毁由仓库及药房有关人员提出申请,填报不合格药品报损有关单据; ③不合格药品销毁时,应填写“报损药品销毁记录”。销毁特殊管理药品时,应在食品药品监督管理部门监督下进行。 6、对质量不合格的药品,应查明原因,分清责任,及时制定与采取纠正、预防措施。 7、明确为不合格药品仍继续发货、使用的,应按经营责任制、质量责任制的有关规定予以处理,造成严重后果的,依法予以处罚。 8、应认真、及时、规范地做好不合格药品的处理、报损和销毁记录,记录应妥善保存至少五年。 XXXX医院 XXXX年XX月XX日
不合格药品管理制度范文3篇 不合格药品管理制度
不合格药品管理制度范文3篇:不合格药品管理制度 为了对不合格药品实行控制性管理,防止购进不合格药品和将不合格药品销售给顾客,需要制定并实施相应的管理制度。X为你带来了不合格药品管理制度范文,一起来看看吧。 不合格药品管理制度范文篇一 1、不合格药品是指:药品的包装不合格、外观质量不合格、内在质量不合格。 2、不合格药品的确认: (1)国家或省、市各级药品监督管理部门发布的通知或质量公报中的不合格药品。 (2)质量验收、保管养护和销售过程中发现的外观、包装、标识不符,包装污染、破碎及超过有效期的药品,并报质量管理员确认为不合格的。 (3)各级药品监督管理部门抽查检验不合格的药品。 (4)符合药品管理法中有关假、劣药品定义的。 (5)生产厂商、供货单位来函通知的不合格药品。 3、不合格药品一旦确认,即不能再销售,将不合格药品移入不合格区,并做好“不合格药品台帐”记录。 4、入库验收发现不合格药品,验收员填写“药品拒收
报告单”交质量管理员,由质量管理员确认后,提出处理意见进行处理。 5、在储存、养护或出库时发现质量有疑问药品,应立即挂黄牌暂停销售,填写“药品质量复查通知单”交质量管理员复验。复验合格,摘除黄牌;不合格,将不合格品移入不合格品区,填写“药品质量处理通知单”进行处理。 6、在门诊陈列、检查、销售过程中发现不合格药品应停止销售,立即下柜。 7、凡药监局公告或发文通知不合格的药品,以及抽查检验发现的不合格药品,应立即清查,集中存放于不合格区内,按要求上报。 8、各环节发现的不合格药品,均应及时报质量管理员,质量管理员每季度对不合格药品进行汇总和分析,分清质量责任,制定处理和预防措施。 9、对于包装破损或者包装不符合规定的不合格药品,可由采购员根据协议及时联系退货处理;对过期失效药品、超过供货商负责期的有质量问题药品、属假劣药品范围的不合格药品应报废,并在药品监督管理部门的监督下进行销毁处理。 10、不合格药品的确认、报告、报损、销毁应有完善的手续和记录。 不合格药品管理制度范文篇二
不合格药品处理程序
不合格药品处理程序内部编号:(YUUT-TBBY-MMUT-URRUY-UOOY-DBUYI-0128)
大泽山镇卫生院 药品购进、验收、储存、养护 不合格药品处理程序 目的:根据《药品管理法》、《药品流通监督管理办法》、GSP及实施细则,对不合格品进行控制性管理,确保不合格药品不入库或出库,保证人民用药安全。 范围:本程序规定了医院不合格药品控制性管理的内容、方法和要求,明确了相关部门或人员的职责,适用于对药品进货验收、在库储存养护、出库复核、销后退回全过程,发现不合格药品的报告、确认与处理控制。 职责: 1、质量管理负责人对不合格药品负责确认,上报药监局,监督、销毁,并作记录。 2、药房不合格品区由专人专帐保管,其保管负责不合格品报损。 3、质量管理负责人负责向供方进行质量查询。 程序和内容: 1、不合格药品的范围界定: 、依据《药品管理法》中假、劣药定义划定不合格药品; 、质量验收、保管养护、出库验发时发现的外观质量及包装质量不符合法定质量标准的药品; 、国家或各级药品监督管理部门发文通知禁止销售的品种,或质量公报中的不合格药品。 、法定的药品检验机构的报告书所示的不合格品。 2、不合格药品的报告与确认 、入库验收环节发现不合格药品的报告与确认
2.1.1验收员对购进药品及销售退回药品在入库验收时发现的内在不合格情况。质量管理负责人接到不合格情况报告后,应在12小时内对所报告的药品进行质量确认,必要时送药品检验机构检验,依据检验结果处理整批货。如为假劣药品由质管部封存于不合格品区并立即上报药监部门。 、在库储存、养护检查过程发现不合格药品的报告与确认 2.2.1在库药品储存、养护检查过程发现的不合格情况应立即向质量管理责任人进行报告。 2.2.2质量管理责任人接到药品养护员的不合格情况报告后,应在12小时内开始对不合格情况进行复查,必要时送药品检验所进行检验,依据检验结果进行处理。 3不合格的标识与处理 、入库验收环节发现不合格药品的标识与处理 3.1.1进货药品在入库验收环节发现并经确认的内在质量不合格药品,应存放于不合格区,悬挂红色不合格品标志牌,注明不合格项目等有关内容。属外观质量不合格的药品应拒收,由质量管理负责人向供方查询,联系并进行处理。 3.1.2销后退回药品在入库验收环节发现并经确认的外在质量不合格药品,应存放于不合格品区,悬挂红色不合格品标志牌,注明不合格项目等有关内容;如未超过规定效期或供方负责期,由业务人员与供方交涉,符合退货条件的,按《购进退出药品管理程序》执行。 、在库储存、养护检查过程发现不合格药品的标识与处理 养护检查过程已确认的不合格药品,应立即挂红色不合格标志牌,移入不合格品区,并进行质量分析,查明原因,分清责任,制定预防措施。 4.不合格品的报损销毁
不合格药品处理程序
不合格药品处理程序 1.目的:加强对不合格药品的管理,防止不合格药品销售给客户。2.2.范围:不合格药品。 3.3.责任人:验收员、仓管员、养护员、药店经理。 4.4.内容: 4.1 对购进药品进行验收时发现不合格药品的处理。 4.1.1 验收员在对购进药品验收时发现不合格药品,予以拒收并填写《药品拒收报告单》。 4.1.2 验收员在购进药品验收中发现假、劣药品,立即就地封存假、劣药品,填写《药品质量问题报告表》报质管员。质管员接到报告后,及时调查取证,了解药品来源等详细情况,并在24小时内将所了解的情况以书面形式报药品监督管理局,等候处理。 4.2药品储存、养护过程中发现或怀疑不合格药品的处理. 4.2.1 过期或包装破损的不合格药品,经养护员确认后,撤离货架,由仓管员将药品转入不合格药品区。 4.2.2 其他情形的不合格品药品,由养护员通知仓管员暂停发货,并悬挂【待处理】标牌。 4.2.3 养护员填写《药品质量问题报告表》与药品一起交质管员确认。 4.2.4 质管员确认为不合格药品的,在《药品质量问题报告表》上填写确认结果与处理意见,仓管员接到质管部的确认报告后,将药品转入不合格品区。4.2.5 质管员确认为合格药品的,在《药品质量问题报告表》上填写确认结果,通知仓管员恢复发货。 4.2.6 质管员无法确认的,送当地药检所检验,并根据检验结果作相应的处理。 4.3 陈列销售过程中发现或怀疑不合格药品的处理。 4.3.1 发现不合格药品,报质管员确认后,撤离货架,放置在不合格品区。 4.3.2 质管员确认为不合格药品的,在《药品质量问题报告表》上填写确认结果与处理意见。 4.3.3 质管员确认为合格药品的,在《药品质量问题报告表》上填写确认结果,通知门店恢复销售。 4.3.4 质管部不能确认的,送当地药检所检验,并根据检验结果作相应的处理。
不合格药品处理程序
文件名称不合格药品操作规程页数 3 文件编号ZX-CX-18-2018 版本号03 起草人:审核人:批准人: 日期:年月日日期:年月日日期:年月日 分发部门:质量管理部、信息部、综合业务部、财务部、办公室 变更记录时间:变更原因:质量管理体系内审 一、目的:通过制定实施不合格药品质量管理操作规程,有效控制不合格药品的处理过程,以保证经营药品的质量符合规定的要求。 二、依据:根据[食药总局28号令]《药品经营质量管理规范》《药品经营质量管理规范现场检查指导原则》等法律法规制定本制度。 三、范围:本程序适用于公司不合格药品处理全管理。 四、职责:本公司质量管理部门、质量机构负责人负责对不合格药品的确认、报告、报损、销毁全过程实施控制性管理。 五、内容: 1、定义: 1.不合格药品的定义: 凡不符合国家有关法律、法规,不符合药品质量标准,包装不符合规定以及药监部门明文规定禁止销售的药品均属不合格药品。有以下情形的,按不合格品处理: 1.1《药品管理法》规定的假药、劣药。 1.2质量证明文件不合格的药品。 1.3包装、标签、说明书内容不符合规定的药品。 1.4包装破损、被污染,影响销售和使用的药品。 1.5批号、有效期不符合规定的药品。 1.6各级药品监督管理部门公告的抽检不合格的。 1.7各级药品监督管理部门发文通知禁止销售的。 1.8质量管理部抽样送检确认不合格的。 2.不合格药品的处理: 2.1【药品停售通知单】 --由仓管员或养护员制单并锁定库存,停售通知单保存后会生成【药品质量复检通知单】,并上报质管部,通知质管员到仓库复检;按下图顺序填写 责任人:仓库保管员养护员 软件中的菜单:【GSP管理】-【GSP历程】-【储存与养护】-【药品停售通知单】
不合格产品处理流程
不合格产品处理流程(草稿、试行) 1.目的 为建立正常的生产经营秩序,保证对不合格的原器件、辅料、工序过程产品和最终产品的有效控制。防止不合格品的非预期使用,确保不合格品不进入下道工序,不合格最终产品不得出厂。用户反映有问题的产品能及时得到回应和处理。 2.适用范围 本程序适用于本公司进货检验;生产过程中检出的不合格品;最终产品检验中发现的不合格品以及产品出厂后用户反馈信息待定的产品处理。 3.职责 3.1总经理负责对负有严重影响的不合格品项目评审结果进行审批。 3.2总工程师负责组织对负有严重影响的不合格品项目评审和过程处理。 3.3质检部负责不合格品控制的归档处理,对不合格品进行确认和报告,协助总工程师组织对不合格品的评审、纠正和预防,并对发现的不合格品的标识隔离和处理情况进行检查和监督,并做好记录。
3.4技术研发部参与不合格品的评审过程,根据评审过程结果及时对不合格品进行处理,必要时进行验证和再确认,并提供整改和纠正的有关信息。 3.5生产部参与不合格品的评审,根据评审结果和处理意见及时对不合格品进行处理。生产车间应按《产品标识和可追溯性控制程序》的要求对不合格品进行标识和隔离,并做好记录。 3.6采购人员应根据有关部门对进货检验中不合格品确认结果,负责与供应商沟通,确保进货产品满足规定的要求,仓库保管员应对进货中确认的不合格品进行隔离、标识,等待处理。防止误用。 3.7市场部因客户投诉或者反馈认为产品存在缺陷不能满足合同要求的产品,应及时的向质检部提出重检和再确认的申请,同意后也应及时通知客户将反映有缺陷的产品寄回本公司进行处理,待再确认后,应将处理结果及时通知客户。 4.不合格品的分类 不合格品一般分为两类: a.轻微的不合格品:一指超出本公司进货验收标准,但可代用不影响产品检测,验收准则的进货物料;二指是本公司生产过程中的产品和最终产品,个别指标与验收标准略有差别,但不是主要技术指标。
