抗生素效价计算过程
USP Cylinder-plate assay 美国药典 管碟法---(标准曲线法)
1、美国药典规定的管碟法抗生素效价方法简述:
首先制备5个标准溶液浓度(U/ml ),分别为S1、S2、S3、S4和S5,其中S3为中间浓度。除S3外的每个浓度准备3个碟子,每个碟子放置6个牛津杯,其中不相连的三个分别加入Si (i 为1、2、4或5),另外三个不相连的加入S3。待检样品(Unknown )加样方式如Si ,具体放置方法如下图1:
图1:标准及样品管碟放置方式图例
2、在以上方法的基础上以具体数据进行计算举例: 下表2为按以上方法进行抗生素效价检测的一组测量结果:
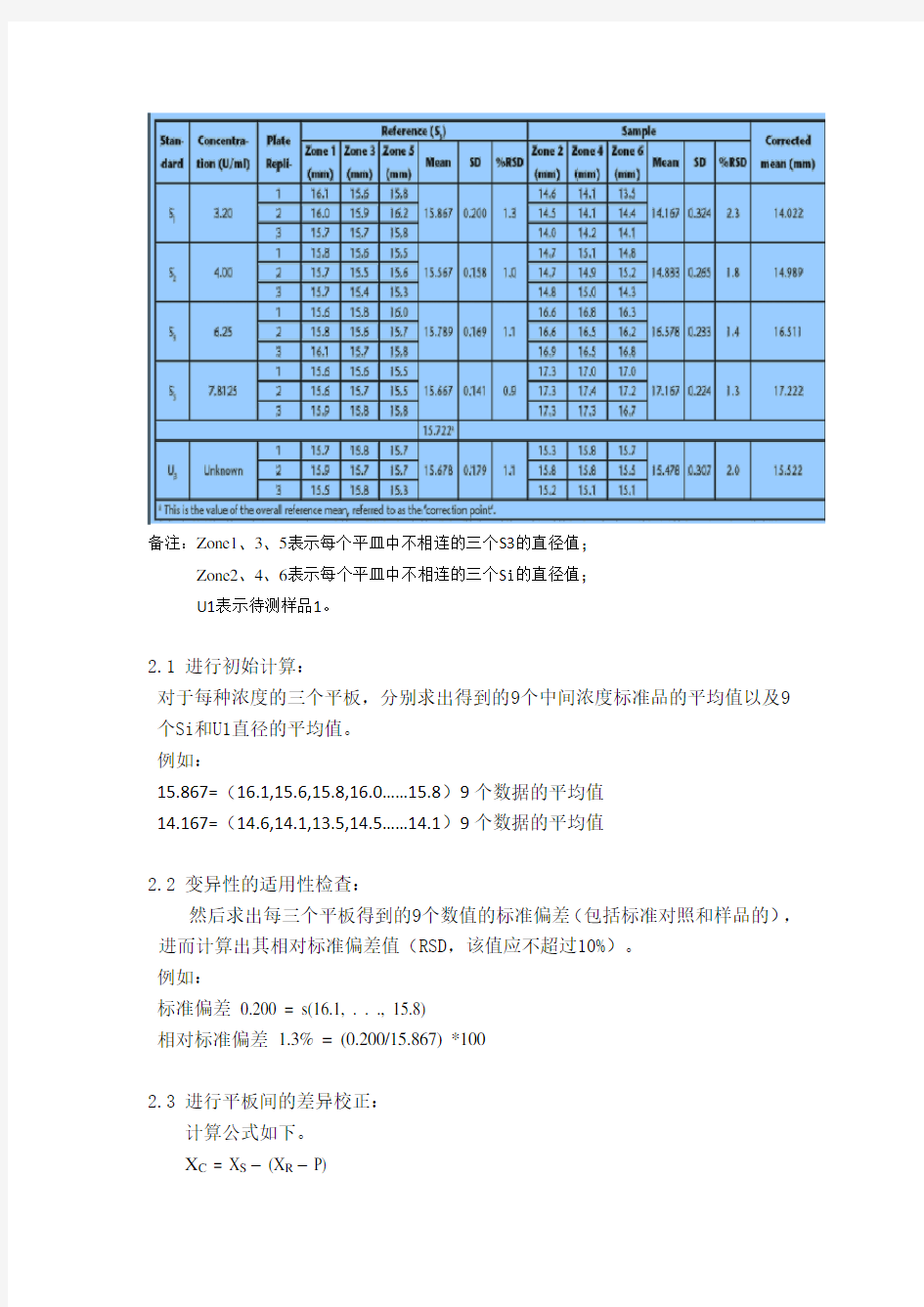
表2:抗生素效价检测测量结果表
Replicate1
Replicate2
Replicate3
Set S1 Set S2 Set S4 Set S5 Sample U1
备注:Zone1、3、5表示每个平皿中不相连的三个S3的直径值;
Zone2、4、6表示每个平皿中不相连的三个S i的直径值;
U1表示待测样品1。
2.1 进行初始计算:
对于每种浓度的三个平板,分别求出得到的9个中间浓度标准品的平均值以及9 个Si和U1直径的平均值。
例如:
15.867=(16.1,15.6,15.8,16.0……15.8)9个数据的平均值
14.167=(14.6,14.1,13.5,14.5……14.1)9个数据的平均值
2.2 变异性的适用性检查:
然后求出每三个平板得到的9个数值的标准偏差(包括标准对照和样品的),进而计算出其相对标准偏差值(RSD,该值应不超过10%)。
例如:
标准偏差0.200 = s(16.1, . . ., 15.8)
相对标准偏差1.3% = (0.200/15.867) *100
2.3 进行平板间的差异校正:
计算公式如下。
X C = X S– (X R– P)
X C = 标准品平均值的校正值
X S = 原始的标准品的平均值
X R = 对照值的平均值
P = 校正值
例如:
14.022 = 14.167 – (15.867 – 15.722) = 14.167 – 0.145
2.4 建立标准曲线:
标准曲线由2.3计算的标准品平均值的校正值Xc和标准品浓度值的对数值构成。(使用适宜的计算软件或手动计算)(注意----可以使用自然对数或底数为10的对数建立标准曲线中以确定回归方程,这样可以得到同样的结果)
例如:下表3是针对下列计算中会用到的数据从表2中截出的部分。
表3:标准曲线数据表
图4:线形回归结果
标准曲线:Z = [3.5502* ln(C)] + 9.9794
Z=校正抑菌圈大小
C=浓度
R2 = 0.9968
2.5 待测样品效价:
估算一个待测样品的效价,计算对照抑菌圈和样品抑菌圈的平均值(三个平板的)。用上面介绍的标准品平均值的校正值Xc以计算待测样品的浓度平均值。
的对数值[注意---另一个可以接受的用校正值的方式为,根据标准品中间浓度S
3
在估计效价的回归线中进行校正]。在标准曲线中使用公式用校正平均值计算样品的含量对数值L U。
L U = (Z – a)/b
a = 回归线的截距
b =回归线的斜率
要得知待测样品的效价,取L U的反对数值乘以适当的稀释因子,该值也可描述为参考值浓度的百分比。
例如:
待测样品校正值(表 2中) = 15.522
待测样品效价的ln值:L U = (15.522 – 9.978) / 3.5502= 1.562
待测样品效价值:C U = e1.562 = 4.765
待测样品效价与对照中间浓度的百分比为:(4.765/5.000) *100% = 95.3%
抗生素效价测定操作规程
QCA/QC-SOP-006 1.主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2.引用标准 《中国药典》2010年版二部。 3.术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生 素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4.操作技术(仪器与用具) 4.1操作室:光线明亮,操作间分a.一般操作间b半无菌操作间。室温控制20-25℃。注 意抗生素的污染。 4.2双蝶:内径90mm高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁液 中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4钢管:内径6.0±0.1mm高7.8±0.1mm或8.0±0.1mm,10.0±0.1mm.重量差异不超±0.05g. 用后置1:1000苯扎溴铵溶液内浸泡2h以上,再灭菌洗涤,先用水洗,超声波30min或 用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW冲洗3次150-160℃干热灭菌2小时 备用. 4.5钢管放置器 4.6恒温培养箱:隔水式为宜35-37℃ 4.7灭菌刻度吸管:用于吸取菌液及培养基(5ml、20ml),用后立即置5%石碳酸或1:1000 苯扎溴铵溶液中消毒后再常规洗涤.150-160℃干热灭菌2小时备用. 4.8玻璃容器:滴定管、移液管、刻度吸管、容量瓶.符合一等品规定用前用清洁液浸泡, 水 洗、PW冲3次
管碟法测定抗生素效价中的影响因素分析及对策.
管碟法测定抗生素效价中的影响因素分析及对策 关键字: 管碟法;抗生素;效价;抑菌圈 摘要: 目的提高管碟法测定抗生素效价的准确性。方法按操作步骤逐步分析,并提出合理的解决方案。结果减少外界因素与人为因素给试验带来的误差。结论可以提高测定结果的准确性。 Abstract: OBJECTIVE To improve the veracity of antibiotics titer evaluation by cylinder- plate method. METHOD According to the process of test, ana lyze the test and offer a proper measure to avoid influenci ng factors. RESULTS Reduce the errors caused by environment al and artificial factors. CONCLUSION This can improve the veracity of test results. Key words: cylinder- plate method; antibiotics; titer; bacterial inhibition ring 管碟法是国内外常用的抗生素微生物检定法[1],利用管碟法测定抗生素效价,具有准确、直观、重复性好等优点,因而被广泛采用。但是整个试验过程中影响结果的因素很多,任何一个环节操作不当或者忽略就会造成很大误差,导致整组试验失败。根据实际操作中的积累经验,对管碟法中影响试验结果的因素进行如下分析及提出解决的方法。 1. 实验器材的准备 1.1 实验器材的选择 试验应该选择底面平整的玻璃双碟,避免底面的凹凸影响琼脂层的厚度。可将双碟放置在水平台上,下垫一层白纸,加入3mL水,再滴加蓝墨水,根据蓝色是否深浅一致来判断双碟底面平整程度。小钢管则应该选择加工精细的同一批产品,这样才能保证管壁厚薄与重量均匀一致,使得小钢管在培养基中下陷相同的深度,抗生素溶液扩散均匀有可比性。如果小钢管两端不够平,就应予剔除,否则会使抗生素溶液漏出,破坏均匀扩散现象。 1.2 实验器材的清洗 抗生素试验中,玻璃双碟、小钢管往往会连续使用。由于清洗方面的原因,它们还是容易残留上次试验中的抗生素(庆大霉素、争光霉素、链霉素等)或者被清洗用的杀菌剂(如新洁而灭、洗洁精、去污粉等)污染,以至于在下次试验中造成抑菌圈不正常的现象。因此,在清洗时要尤为注意多用流水冲洗。160℃干热灭菌2h后备用。 2. 配制试验所需的样品、标准品、缓冲液与培养基
管碟法测定抗生素效价中的影响因素分析及对策讲解
管碟法测定抗生素效价中的影响因素分析及对策摘要: 目的提高管碟法测定抗生素效价的准确性。方法按操作步骤逐步分析,并提出合理的解决方案。结果减少外界因素与人为因素给试验带来的误差。结论可以提高测定结果的准确性。 Abstract: OBJECTIVE To improve the veracity of antibiotics titer evaluation by cylinder-plate method. METHOD According to the process of test, analyze the test and offer a proper measure to avoid influencing factors. RESULTS Reduce the errors caused by environmental and artificial factors. CONCLUSION This can improve the veracity of test results. Key words: cylinder-plate method; antibiotics; titer; bacterial inhibition ring 管碟法是国内外常用的抗生素微生物检定法[1],利用管碟法测定抗生素效价,具有准确、直观、重复性好等优点,因而被广泛采用。但是整个试验过程中影响结果的因素很多,任何一个环节操作不当或者忽略就会造成很大误差,导致整组试验失败。根据实际操作中的积累经验,对管碟法中影响试验结果的因素进行如下分析及提出解决的方法。 1. 实验器材的准备 1.1 实验器材的选择 试验应该选择底面平整的玻璃双碟,避免底面的凹凸影响琼脂层的厚度。可将双碟放置在水平台上,下垫一层白纸,加入3mL水,再滴加蓝墨水,根据蓝色是否深浅一致来判断双碟底面平整程度。小钢管则应该选择加工精细的同一批产品,这样才能保证管壁厚薄与重量均匀一致,使得小钢管在培养基中下陷相同的深度,抗生素溶液扩散均匀有可比性。如果小钢管两端不够平,就应予剔除,否则会使抗生素溶液漏出,破坏均匀扩散现象。 1.2 实验器材的清洗
抗生素效价计算过程
USP Cylinder-plate assay 美国药典 管碟法---(标准曲线法) 1、 美国药典规定的管碟法抗生素效价方法简述: 首先制备5个标准溶液浓度(U/ml ),分别为S1、S2、S3、S4和S5,其中S3为中间浓度。除S3外的每个浓度准备3个碟子,每个碟子放置6个牛津杯,其中不相连的三个分别加入Si (i 为1、2、4或5),另外三个不相连的加入S3。待检样品(Unknown )加样方式如Si ,具体放置方法如下图1: 图1:标准及样品管碟放置方式图例 2、在以上方法的基础上以具体数据进行计算举例: 下表2为按以上方法进行抗生素效价检测的一组测量结果: 表2:抗生素效价检测测量结果表 Replicate1 Replicate2 Replicate3 Set S1 Set S2 Set S4 Set S5 Sample U1
备注:Zone1、3、5表示每个平皿中不相连的三个S3的直径值; Zone2、4、6表示每个平皿中不相连的三个Si的直径值; U1表示待测样品1。 2.1 进行初始计算: 对于每种浓度的三个平板,分别求出得到的9个中间浓度标准品的平均值以及9 个Si和U1直径的平均值。 例如: 15.867=(16.1,15.6,15.8,16.0……15.8)9个数据的平均值 14.167=(14.6,14.1,13.5,14.5……14.1)9个数据的平均值 2.2 变异性的适用性检查: 然后求出每三个平板得到的9个数值的标准偏差(包括标准对照和样品的),进而计算出其相对标准偏差值(RSD,该值应不超过10%)。 例如: 标准偏差0.200 = s(16.1, . . ., 15.8) 相对标准偏差1.3% = (0.200/15.867) *100 2.3 进行平板间的差异校正: 计算公式如下。 X C = X S– (X R– P)
抗生素的生物效价测定法(管碟法)
抗生素的生物效价测定法 测定抗生素效价的方法比较多,一般可以分为物理学方法、化学方法、生物学方法、和两种方法配合等四大类,可根据具体情况选择使用。 生物学方法以抗生素的杀菌力作为衡量效价的标准,其原理恰好和临床应用于的要求一致这是它的优点;又其灵敏度较高,需用检品的量较小,也是其它方法所不及的。 抗生素的生物效价测定法,常用的有稀释法、比浊法和扩散法(或称渗透法)。 稀释法这一方法是用培养基将检品抗生素稀释到各种浓度,并依次分装到一系列的容器内,再加入等量“试验菌种”菌种菌液,并放在37 ℃保温箱内培养一定时间,观察何种稀释度适能抑制细菌的生长,该稀释度即为测定终点(或以细菌生长所引起的PH改变及溶血现象等生化反应作为测定终点),再与同样处理的标准抗生素的终点作比较,即可求得检品的效价。这种方法可以使用液体培养基,也可以使用固体培养基。所用的材料及培养基都必须严格无菌,并要注意无菌操作。由于测定终点是以有无细菌生长来判断的,因此所得结果公是一个范围。 比浊法原理及操作大致与稀释法相同。比浊法也是将不同量的检品及标准品分别加入培养基中,观察其对“试验菌种”的效应——即细菌生长所引起的混浊。这一方法和稀释法的区别有二:a.比浊法的稀释间隔的密度比较近,准确度高一些;b.比浊法不以细菌有无生长的区分为终点,而是将标准品浓度和细菌生长所引起的混浊度求得一定的比例,再由检品的细菌生长混浊度推算检品的效价。这一方法易受杂质的影响,并且不适用于有色或混浊的检品。 扩散法使用固体培养基,在培养基凝固以前将“试验菌种”混合进去,在这样备妥的培养表面,可以用种种设计使检品液或含有抗生素的物质与有菌种的培养基接触。经过培育后,由于抗生素向培养基中扩散,凡抑菌浓度所能达到之下细菌不能生长因而形成透明的抑菌范围,此种范围一般都呈圆形,称为“抑菌圈”。扩散法有几种,或中一种叫管碟扩散法(筒称管碟法)为国际上常用的方法,在我国也作为法定的抗生素检定法。 下面我们将详细地讨论管碟法的原理和实验方法。 一、管碟法测定的设计原理及计算方法 管碟法所用的管子系用瓷、铝或玻璃制成,较好的用不锈钢制成,它是内径为6+0.1毫米、外径为8+0.1毫米、高10+0.1毫米的圆筒形管子,管子的重量尽可能相等。 摊布固体培养基的容器可用双碟,亦可用平底下班盘。管子放在混有菌种的固体培养基上时,可用人工放臵,也可用特定的管子放臵器放臵。
抗生素效价测定操作规程
抗生素效价测定操作规 程
1. 主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2. 引用标准 《中国药典》2010年版二部。 3. 术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4. 操作技术(仪器与用具) 4.1 操作室:光线明亮,操作间分 a.一般操作间b 半无菌操作间。室温控制20-25℃。注意抗生素的污染。 4.2 双蝶:内径90mm 高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁 液中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3 陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4 钢管:内径 6.0±0.1mm 高7.8±0.1mm 或8.0±0.1mm,10.0±0.1mm.重量差异不超 ±0.05g.用后置1:1000苯扎溴铵溶液内浸泡2h 以上,再灭菌洗涤,先用水洗,超声波30min 或用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW 冲洗3次150-160℃干热灭菌2小时备用. 4.5 钢管放置器 4.6 恒温培养箱:隔水式为宜35-37℃ 4.7 灭菌刻度吸管:用于吸取菌液及培养基(5ml 、20ml ),用后立即置5%石碳酸或 QCA/QC-SOP-006 山东良福制药有限公司 起草人 日 期 抗生素效价测定操作规程 审核人 日 期 批准人 日 期 第五版 实施日期 总页数 共5页
临床常用抗生素分类及化学名
临床常用抗生素分类及化学名、商品名 一、β-内酰胺类(β-lactams)抗生素:包括青霉素类、头孢菌素类和非典型类。 非典型β-内酰胺类:包括头霉素类如头孢西丁、头孢美唑等;氧头孢烯类如拉氧头孢、氟氧头孢等;碳青霉烯类如亚胺培南、美罗培南、帕尼培南等;单环类如氨曲南、卡芦莫南等。 (一)青霉素类 1.阿莫西林(Amoxicillin):即羟氨苄青霉素,商品名:“阿莫仙”、“阿莫灵”、“弗莱莫星”。 2.哌拉西林(Piperacillin):氧哌嗪青霉素。 3.替卡西林(Ticarcillin):羧噻吩青霉素钠,是羧苄青霉素的替代药。 4.阿洛西林(Azlocillin):苯咪唑类广谱半合成青霉素新品,商品名:“阿乐欣”。 5.美洛西林(Mezlocillin):商品名:天林。 6.β-内酰胺酶抑制剂:克拉维酸(Clavulanic acid)——棒酸;舒巴坦(Sulbactam)——青霉烷砜;三唑巴坦(Tazobactam)——他唑巴坦。 7.奥格门汀(Augmentin):阿莫西林/克拉维酸,商品名:“安灭菌”、“力百汀”、“安奇”。 8.泰门汀(Timentin):替卡西林/克拉维酸,商品名:“特美汀”。 9.优立新(Unasyn):氨苄西林/舒巴坦。 10.克菌(Copliscan):阿莫西林/双氯西林,同类产品:新灭菌(Biflocin)。 11.他唑西林(Tazocillin):哌拉西林/三唑巴坦,商品名:“特治星”、“海他欣”。 (二)头孢菌素类 一代头孢 1.头孢唑啉(Cefazolin):先锋Ⅴ。 2.头孢拉定(Cephradine):先锋Ⅵ,商品名:“泛捷复”(Velosef)。 3.头孢噻吩(Cefinase): 二代头孢 1.头孢呋辛(Cefuroxime):又名头孢呋肟,商品名:“西力欣”(Zinacef)、“力复乐”。
实验三 抗生素效价的测定
实验三抗生素效价的生物测定 一、实验目的 1.熟悉抗生素效价测定的原理 2.掌握培养基的配制、灭菌 3、掌握接种技术 二、实验原理 抗生素的医疗价值决定于它的抗菌特性,因此利用它们各自的抗菌活性来测定其效价有着特殊的意义。效价的测定法有:液体稀释法,比浊法和扩散法等。本实验采用国际上最为常用的杯碟扩散法来定量测定洁霉素的效价。测定时,将规格完全一致的不锈钢小管(即牛津小杯)置于含敏感菌的琼脂平板上,并在牛津小杯中加入己知浓度的标准青霉素溶液和未知浓度的青霉素发酵液。于是,抗生素就自牛津小杯处向平板四周扩散,在抑菌浓度所达范围内敏感菌的生长被抑制而出现抑菌圈。在一定的范围内,抗生素浓度的对数值与抑菌圈直径呈线性关系。因此,只要将被测样品与标准样品抑菌圈直径进行比较,就可在标准曲线上查得未知样品的抗生素效价。 三、材料和器皿 1 菌种:大肠杆菌(E.coli)。 2培养基:牛肉膏蛋白胨琼脂培养基(作生物测定用时,平板应分上下两层,上层须另加25%葡萄糖)。 牛肉膏蛋白胨琼脂培养基配方: 牛肉膏3g 蛋白胨10g Nacl 5g 琼脂15-20g 1000ml 水pH 7.4-7.6 3试剂 (1)l%pH6磷酸缓冲液:K2HPO4 0.2g(或K2HPO4·3H20 0.253g)KH2P040.8g,蒸馏水100ml。 (2)25% 葡萄糖溶液100ml。 (3)苄青霉素钠盐:1667U/mg(1U即1国际单位,等于0.6ug)。 4其他:牛津小杯(不锈钢小管,内径6土0.lmm,外径8土0.lmm,高10土0.1mm),培养皿(直径90mm,深20mm;大小一致,皿底平坦),试管、滴管、移液管(5ml)、移液枪(1ml)、枪头、镊子、涂布棒等。 四、方法和步骤 1标准曲线的测绘 (1)倒底层培养基:取无菌培养皿5套,每皿移入20ml牛肉膏蛋白陈底层琼脂培养基,置水平待凝,备用。
2019抗菌药物临床应用指导原则【最新整理】
《抗菌药物临床应用指导原则》测试题 1. 治疗产超广谱β内酰胺酶(ESBLs)菌感染首选第三代头孢菌素(T,F) 2. 应用头孢菌素前应进行皮内试验(T,F) 3. 肾功能不全时禁用氨基糖苷类抗菌药(T,F) 4. 所有β内酰胺类抗生素均不宜用于甲氧西林耐药葡萄球菌感染,即使体外药敏结果显示敏感(T,F) 5. 两性霉素B静滴容易发生发热、高钾血症、肾功能不全等不良事件(T,F) 6. 头孢唑啉可用于治疗MSSA、溶血性链球菌、肠球菌属所致感染(T,F) 7. 氟喹诺酮类药物不宜用于未成年人(T,F) 8. 肾功能不全患者禁用万古霉素(T,F) 9. 应用碳青霉烯类药物无需合并抗厌氧菌药物(T,F) 10. 治疗不典型病原体感染可选用大环内酯类、氟喹诺酮类或碳青霉烯类(T, F) 11. 两性霉素B静滴时较少发生肝肾功能损害等不良事件(T,F) 12. 氟喹诺酮类药物适用于各年龄段感染性腹泻患者的治疗(T, F) 13. 某些头孢菌素如头孢哌酮较大剂量使用时可有出血倾向(T,F) 14. SMZ-TMP适用于治疗卡氏肺孢菌肺炎(T, F) 答案
1. F, 2. F, 3. F 4. T, 5 F 6 F 7. T 8. F 9. T 10. F 11. F 12. F 13. T 14. T 抗菌药物合理使用与管理测试题——题型来源于:宁夏远程网__国家级继续教育学分 1、链球菌引起的化脓性扁桃体炎,因为耐药尽量不选择哪种抗菌药物()? A:大环内酯类药;B:头孢菌素类;C:青霉素;D:喹诺酮类药 2、以下不属于大环内酯类药物的是(): A:红霉素;B:庆大霉素;C:阿奇霉素;D:克拉霉素 3、抗菌药物不合理使用最突出的原因是()
抗生素效价测定操作规程
QCA/QC-SOP-??? 1.主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2.引用标准 《中国药典》2010年版二部。 3.术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生 素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4.操作技术(仪器与用具) 4.1操作室:光线明亮,操作间分a.一般操作间b半无菌操作间。室温控制20-25℃。注 意抗生素的污染。 4.2双蝶:内径90mm高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁液 中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4钢管:内径6.0±0.1mm高7.8±0.1mm或8.0±0.1mm,10.0±0.1mm.重量差异不超±0.05g. 用后置1:1000苯扎溴铵溶液内浸泡2h以上,再灭菌洗涤,先用水洗,超声波30min或 用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW冲洗3次150-160℃干热灭菌2小时备用. 4.5钢管放置器 4.6恒温培养箱:隔水式为宜35-37℃ 4.7灭菌刻度吸管:用于吸取菌液及培养基(5ml、20ml),用后立即置5%石碳酸或1:1000 苯扎溴铵溶液中消毒后再常规洗涤.150-160℃干热灭菌2小时备用. 4.8玻璃容器:滴定管、移液管、刻度吸管、容量瓶.符合一等品规定用前用清洁液浸泡, 水 洗、PW冲3次
临床抗菌药物的选择
临床抗菌药物的选择 抗菌药的选择 随着抗菌药物的广泛应用,使多种细菌性感染得到有效的治疗和控制,但不合理使用和滥用则导致了不良反应增多和细菌耐药等问题,例如耐甲氧西林葡萄球菌、耐万古霉素肠球菌、耐药革兰阴性杆菌和多重耐药结核分枝肝菌等,其中有些耐药菌感染目前尚无有效治疗药物。所以,合理使用抗菌药物可最大程度发挥抗菌药物的疗效并使不良反应降到最低程度。 抗菌药物通常仅对细菌性感染有用,对病毒感染无效。并非所有的发热均由感染所致,而且并非所有的感染均由细菌引起,抗菌药物不能治疗病毒感染。下列情况不宜或应限制使用抗菌药物:病毒性感染;原因不明的发热,又无细菌感染迹象提示者;无症状或轻型胃肠炎型的沙门菌感染,因使用抗菌药物可抑制正常肠道细菌,有利于沙门菌生长繁殖,延长带菌期,并易产生耐药;抗菌药物的预防性应用不应列为常规,应严格控制;抗菌药物的局部应用应予限制,因局部应用后易产生过敏反应,也易导致耐药菌株的产生。 2004年10月国家卫生部颁布《抗菌药物临床应用指导原则》,该规范要求合理应用抗菌药:联合应用抗菌药物指征确定是否联合用药,最好按药敏试验结果用药;1种抗菌药物可以治疗时不联合应用多种药物,一般不联用3 种以上抗菌药;一旦联合应用,用药剂量要足,不宜采取少量长时间应用或频繁更换;还需注意配伍禁忌,联合应用抗生素应达到协同或相加的治疗效果,必须有严格的指征,如重症混合感染患儿免疫功能低下、白细胞低的患儿,以及耐药菌感染和难治的细菌感染等,防止拮抗作用和毒性作用的产生和增强。 药物用于临床抗感染治疗中一直发挥着重要的作用,但是如果药物的选择不当,不但产生不了抗菌治疗效果,还可能给病人带来一系列不良后果,诸如不良反应增多,致病菌的变迁现象增多,促使细菌产生耐药性,,增加合并症,延长病程,增加患者的经济负担等等。因此,在使用抗菌药物时必须严格掌握适应症,应从以下几个方面考虑。 1 细菌学诊断和体外药敏试验 抗菌药物的选择,首先取决于病原微生物的种类和性质,多数抗菌药物仅选择地作用于有限范围的致病菌,因此,正确选择抗菌药物必须建立在对致病菌的正确诊断之上,有条件者应进行细菌分类与药敏试验。 2 患者情况 有药物过敏疾病及具有过敏性家族史者,对易发生过敏反应的抗菌药物应禁用;机体防御机能低下者,应采用杀菌剂来治疗。肾脏是大部分抗生素排泄的主要途径。肾功能不全时,应用主要经肾脏排泄的药物,宜减量或延长给药时间,
抗生素效价测定操作规程
1.主题内容和适用范围 本规程规定了公司外购原料药品及生产成品中抗生素的效价测定方法及要求。 本规程适用于公司外购原料药品及生产成品中抗生素的效价测定。 2.引用标准 《中国药典》2015年版四部。 3.术语 抗生素微生物检定法:在适宜的条件下,根据量反应平行原理设计,通过检测抗生素对微生物的抑制作用,计算抗生素活性(效价)方法。 抗生素微生物检定包括两种方法,即管碟法和浊度法。本法采用的是管碟法。 4.操作技术(仪器与用具) 4.1操作室:光线明亮,操作间分a.一般操作间b半无菌操作间。室温控制20-25℃。注 意抗生素的污染。 4.2双蝶:内径90mm高16-17mm.用后经高压灭菌倒出培养基后,置专用洗液或清洁液 中浸泡过夜,冲洗,沥干150-160℃干热灭菌2小时或高压灭菌121℃30min,备用。 4.3陶瓦盖:内径103mm,外经108mm,吸水性强,定期清洗、干燥或干热灭菌。 4.4钢管:内径6.0±0.1mm高7.8±0.1mm或8.0±0.1mm,10.0±0.1mm.重量差异不超±0.05g. 用后置1:1000苯扎溴铵溶液内浸泡2h以上,再灭菌洗涤,先用水洗,超声波30min或用去污粉的沙布条串擦内外壁,水冲洗,淋干,PW冲洗3次150-160℃干热灭菌2小时备用. 4.5钢管放置器 4.6恒温培养箱:隔水式为宜35-37℃ 4.7灭菌刻度吸管:用于吸取菌液及培养基(5ml、20ml),用后立即置5%石碳酸或1:1000 苯扎溴铵溶液中消毒后再常规洗涤.150-160℃干热灭菌2小时备用. 4.8玻璃容器:滴定管、移液管、刻度吸管、容量瓶.符合一等品规定用前用清洁液浸泡, 水 洗、PW冲3次
管碟法测定抗生素效价中的影响因素分析及对策解析
管碟法测定抗生素效价中的影响因素分析及对策(1) 关键字: 管碟法;抗生素;效价;抑菌圈 摘要: 目的提高管碟法测定抗生素效价的准确性。方法按操作步骤逐步分析,并提出合理的解决方案。结果减少外界因素与人为因素给试验带来的误差。结论可以提高测定结果的准确性。 Abstract: OBJECTIVE To improve the veracity of antibiotics titer evaluation by cylinder-plate method. METHOD According to the process of test, analyze the test and offer a proper measure to avoid influencing factors. RESULTS Reduce the errors caused by environmental and artificial factors. CONCLUSION This can improve the veracity of test results. Key words: cylinder-plate method; antibiotics; titer; bacterial inhibition ring 管碟法是国内外常用的抗生素微生物检定法[1],利用管碟法测定抗生素效价,具有准确、直观、重复性好等优点,因而被广泛采用。但是整个试验过程中影响结果的因素很多,任何一个环节操作不当或者忽略就会造成很大误差,导致整组试验失败。根据实际操作中的积累经验,对管碟法中影响试验结果的因素进行如下分析及提出解决的方法。 1. 实验器材的准备 1.1 实验器材的选择 试验应该选择底面平整的玻璃双碟,避免底面的凹凸影响琼脂层的厚度。可将双碟放置在水平台上,下垫一层白纸,加入3mL水,再滴加蓝墨水,根据蓝色是否深浅一致来判断双碟底面平整程度。小钢管则应该选择加工精细的同一批产品,这样才能保证管壁厚薄与重量均匀一致,使得小钢管在培养基中下陷相同的深度,抗生素溶液扩散均匀有可比性。如果小钢管两端不够平,就应予剔除,否则会使抗生素溶液漏出,破坏均匀扩散现象。 1.2 实验器材的清洗
临床常用抗生素的分类及特点
临床常用抗生素的分类及特点 临床常用的抗生素包括β-内酰胺类、氨基糖苷类、大环内酯类、林可霉素类、多肽类、喹诺酮类、磺胺类、抗结核药、抗真菌药及其他抗生素。 β-内酰胺类 此类属于繁殖期杀菌剂。其特点是:血药浓度高、抗菌谱广和毒性低。包括青霉素类、头孢菌素类、新型β-内酰胺类及β-内酰胺类与β-内酰胺酶抑制剂组成的复合制剂。 (1)青霉素类 青霉素G:临床上主要用于肺炎球菌、溶血性链球菌及厌氧菌感染,金黄色葡萄球菌和流感杆菌多数对其耐药。普鲁卡因青霉素G半衰期较青霉素长。青霉素V 钾片耐酸,可口服,使用方便。 双氯青霉素:对产酸耐青霉素G的金黄色葡萄球菌抗菌活性最强,对其它G 球菌较青霉素G差,对耐甲氧西林的金黄色葡萄球菌(MRSA)无效。 阿莫西林:抗菌谱与氨苄青霉素相似,肺炎球菌、溶血性链球菌、肠球菌和流感杆菌对本药敏感,抗菌作用优于氨苄青霉素,但对假单胞菌无效。 广谱抗假单胞菌类:对G 球菌的抗菌作用与青霉素G相似,对G-杆菌(如大肠杆菌、变形杆菌、流感杆菌等)及假单胞菌有很强的抗菌作用,尤其哌拉西林、阿洛西林、美洛西林抗菌活性更强。 (2)头孢菌素类 此类属广谱抗菌药物,分四代。第一、二代对绿脓杆菌无效,第三代中部分品种及第四代对绿脓杆菌有效,该类药物对支原体和军团菌无效。 第一代头孢菌素:包括头孢噻吩/氨苄/唑林/拉定。对产酸金黄色葡萄球菌、肺炎球菌、溶血性链球菌等G 球菌抗菌活性较第二、三代为强,对G-杆菌的作用远不如第二、三代,仅对少数肠道杆菌有作用。对β-内酰胺酶稳定性差,对肾有一定毒性。对绿脓杆菌、变形杆菌、不动杆菌等无效。其中头孢唑林/拉定较常用。
管碟法抗生素效价测量实验
管碟法抗生素效价测量实验 抗生素的生物检定是以抗生素对微生物的抗菌效力作为效价的衡量标准,具有与应用原理相一致、用量少和灵敏度高等优点。管碟法是琼脂扩散法中的一种,已被各国药典广泛采用,作为法定的抗生素生物检定方法。 当抗生素在菌层培养基中扩散时,会形成抗生素浓度由高到低的自然梯度,即扩散中心浓度高而边缘浓度低。因此,当抗生素浓度达到或高于mic(最低抑制浓度)时,试验菌就被抑制而不能繁殖,从而呈现透明的抑菌圈。根据扩散定律的推导,抗生素总量的对数值与抑菌圈直径的平方成线性关系。 实验简介 在管碟法抗生素效价测量实验中需要注意的影响因素分析及对策如下: 管碟法是国内外常用的抗生素微生物检定法[1],利用管碟法测定抗生素效价,具有准确、直观、重复性好等优点,因而被广泛采用。但是整个试验过程中影响结果的因素很多,任何一个环节操作不当或者忽略就会造成很大误差,导致整组试验失败。根据实际操作中的积累经验,对管碟法中影响试验结果的因素进行如下分析及提出解决的方法。 实验器材的准备 1.1 实验器材的选择 试验应该选择底面平整的玻璃双碟,避免底面的凹凸影响琼脂层的厚度。可将双碟放置在水平台上,下垫一层白纸,加入3mL水,再滴加蓝墨水,根据蓝色是否深浅一致来判断双碟底面平整程度。小钢管则应该选择加工精细的同一批产品,这样才能保证管壁厚薄与重量均匀一致,使得小钢管在培养基中下陷相同的深度,抗生素溶液扩散均匀有可比性。如果小钢管两端不够平,就应予剔除,否则会使抗生素溶液漏出,破坏均匀扩散现象。
1.2 实验器材的清洗 抗生素试验中,玻璃双碟、小钢管往往会连续使用。由于清洗方面的原因,它们还是容易残留上次试验中的抗生素(庆大霉素、争光霉素、链霉素等)或者被清洗用的杀菌剂(如新洁而灭、洗洁精、去污粉等)污染,以至于在下次试验中造成抑菌圈不正常的现象。因此,在清洗时要尤为注意多用流水冲洗。160℃干热灭菌2h后备用。 配制试验所需的样品及药品 2.1 样品与标准品溶液的配制 标准品与样品从冰箱取出后,使与室温平衡。供试品应放于干燥器内至少 30min方可称取。称量最好为一次取样称量,动作迅速,不得反复称取,取样后立即将称量瓶瓶盖盖好,以免吸水。标准品的称量最好用1/100,000克的分析天平,样品称量不得低于1/10,000克的分析天平。天平中的干燥剂应保持经常注意更换。称量结束后,加入超声波处理后的磷酸缓冲液,定容至刻度,过滤并稀释。稀释时,都应采用容量瓶,每一步稀释取样量不得少于2mL。用刻度吸管吸取溶液前,要用待稀释液冲洗吸管2,3次,吸取溶液后,要用滤纸把刻度吸管外壁多余液体擦去,再从起始刻度开始放溶液。把稀释后的抗生素溶液分装至干燥灭菌试管待用。在称量抗生素样品过程中,操作者的工作服上有可能会沾染抗生素粉末,在配培养基、加底层培养基、加菌层培养基或滴加抗生素溶液时,会随衣袖的抖动落入培养基,造成破圈或者无抑菌圈。所以配制抗生素溶液应单独使用一套工作服。 2.2 培养基与缓冲液的配制 配制培养基与缓冲液时要按照文献的配比用量,配制后调节其pH值。因为在pH值、盐浓度的影响下,即使琼脂培养基上的两个相邻的小管距离足够,还是可能会出现卵圆形抑菌圈。例如四环素易受pH值影响,链霉素易受盐浓度影响[2]。
抗生素效价测定
项目2青霉素效价测定 一、知识连接 (一)抗生素效价表示方法 效价就是评价抗生素效能得标准,也就是衡量抗生素活性成分含量得尺度。效价一般指得就是生物活性得大小或者高低,生物活性得大小与高低就是与效价成正比得。实际应用中,合理使用抗生素得剂量十分重要。抗生素应用时剂量小,因此除重量外,常用特定得效价单位(unit)表示,效价单位也称抗菌活性单位。 最初,由于抗生素无法制得纯品,用其生物活性得大小来表示其剂量、 一个青霉素得效价单位(U):能在50mL肉汤培养基中完全抑制金黄色葡萄球菌标准菌株得发育得最小青霉素剂量。 一个链霉素效价单位(U):能在1mL肉汤培养基中完全抑制大肠杆菌(ATCC9637)发育得最小剂量。 重量单位(μg):以抗生素得有效成分(生理活性成分)得重量作为抗生素得基准单位(大多数使用)。 (二)抗生素效价测定 抗生素微生物检定法可分为稀释法、比浊法与琼脂扩散法(管碟法与打孔法)。各国药典通常采用后两种方法测定抗生素得效价。 管碟法就是利用抗生素在琼脂培养基得扩散渗透作用,在含有高度敏感性试验菌得琼脂平板上放置小钢管(内径6、0±0。l mm,外径8、0±0。l mm,高10±0.lmm),管内放入标准品与检品得溶液,经16~18小时恒温培养,当抗生素在菌层培养基中扩散时,会形成抗生素浓度由高到低得自然梯度,即扩散中心浓度高而边缘浓度低。因此,当抗生素浓度达到或高于MIC(最低抑制浓度)时,试验菌就被抑制而不能繁殖,从而呈现透明得无菌生长得区域,常呈圆形,称为抑菌圈。抑菌圈得大小代表药剂抗菌力得高低。在一定得药剂浓度范围内,药剂得浓度越高则抑菌圈得直径越大。目前最常用得就是游标卡尺与直尺直接测量抑菌圈直径、根据扩散定律得推导,抗生素总量得对数值与抑菌圈直径得平方成线性关系,即通过检测抗生素对微生物得抑制作用,比较标准品与供试品产生抑菌圈得大小,计算出供试品得效价。 管碟法得基本操作与设计适用于各种抗生素,试验结果较稳定;样品用量少,灵敏度高;适合于大批样品得测定。然而凡具有抗菌活性得物质都会干扰测定结果;试验过程长,得出结果慢;操作手工化,需熟练人员才能得到较正确得结果;受扩散因素得影响,如培养基原材料得质量,一般琼脂中得杂质可能影响扩散速度及效价强度。尽管如此,由于它有上述得独特优点而被世界各国所公认,成为国际通用得方法被列入各国药典法规内、 二、制订方案 根据情境导入中得问题,制订抗生素生物效价得测定方案表,如表5—2-1所示。
抗生素生物效价测定
实验一抗生素生物效价测定 【实验目的】 1. 掌握抗生素生物效价测定的原理和方法; 2. 掌握管碟法测定抗生素生物效价相关的操作方法。 【实验原理】 抗生素的效价常采用微生物学方法测定,它是利用抗生素对特定的微生物具有抗菌活性 的原理来测定抗生素效价的方法,如管碟法。管碟法是目前抗生素效价测定的国际通用方法, 我国药典也采用此法。管碟法是根据抗生素在琼脂平板培养基中的扩散渗透作用,比较标准品和检品两者对试验菌的抑菌圈大小来测定供试品的效价。管碟法的基本原理是在含有高度 敏感性试验菌的琼脂平板上放置小钢管(内径6.0 ±).1 mm外径8.0 ±).1 mm高10 ±). Imm), 管内放人标准品和检品的溶液,经16~18小时恒温培养,当抗生素在菌层培养基中扩散时______ 会形成抗生素浓度由高到低的自然梯度,___ 即扩散中心浓度高而边缘浓度低。_因此,当抗生素 圈直径的平方成线性关系,—比较抗生素标准品与检品的抑菌圈大小,可计算出抗生素的效价。 常用的管碟法有:一剂量法、二剂量法、三剂量法。后二法已经列入药典。二剂量法系将抗生素标准品和供试品各稀释成一定浓度比例( 2:1或4:1 )的两种溶液,在同一平板上 比较其抗药活性,再根据抗生素浓度对数和抑菌圈直径成直线关系的原理来计算供试品效价。取含菌层的双层平板培养基,每个平板表面放置4个小钢管,管内分别放入供试品高、 低剂量和标准品高、低剂量溶液。先测量出四点的抑菌圈直径,按下列公式计算出检品的效价。 (1)求出W和V:W=( SH+UH -( SL+UL ( V= (UH+UL - (SH+SL ( 式中:UH供试品高剂量之抑菌圈直径; UL:供试品低剂量之抑菌圈直径; SH标准品高剂量之抑菌圈直径; SL:标准品低剂量之抑菌圈直径; (2)求出0:匸Dantilog (IV/W) ( 式中:0供试品和标准品的效价比;式 2.10-1) 式 2.10-2) 式 2.10-3)
抗生素效价测定
项目2青霉素效价测定 一、知识连接 (一)抗生素效价表示方法 效价是评价抗生素效能的标准,也是衡量抗生素活性成分含量的尺度。效价一般指的是生物活性的大小或者高低,生物活性的大小和高低是和效价成正比的。实际应用中,合理使用抗生素的剂量十分重要。抗生素应用时剂量小,因此除重量外,常用特定的效价单位(unit)表示,效价单位也称抗菌活性单位。 最初,由于抗生素无法制得纯品,用其生物活性的大小来表示其剂量。 一个青霉素的效价单位(U):能在50mL肉汤培养基中完全抑制金黄色葡萄球菌标准菌株的发育的最小青霉素剂量。 一个链霉素效价单位(U):能在1mL肉汤培养基中完全抑制大肠杆菌(ATCC9637)发育的最小剂量。 重量单位(μg):以抗生素的有效成分(生理活性成分)的重量作为抗生素的基准单位(大多数使用)。 (二)抗生素效价测定 抗生素微生物检定法可分为稀释法、比浊法和琼脂扩散法(管碟法和打孔法)。各国药典通常采用后两种方法测定抗生素的效价。 管碟法是利用抗生素在琼脂培养基的扩散渗透作用,在含有高度敏感性试验菌的琼脂平板上放置小钢管(内径6.0±0.l mm,外径8.0±0.l mm,高10±0.lmm),管内放入标准品和检品的溶液,经16~18小时恒温培养,当抗生素在菌层培养基中扩散时,会形成抗生素浓度由高到低的自然梯度,即扩散中心浓度高而边缘浓度低。因此,当抗生素浓度达到或高于MIC(最低抑制浓度)时,试验菌就被抑制而不能繁殖,从而呈现透明的无菌生长的区域,常呈圆形,称为抑菌圈。抑菌圈的大小代表药剂抗菌力的高低。在一定的药剂浓度范围内,药剂的浓度越高则抑菌圈的直径越大。目前最常用的是游标卡尺和直尺直接测量抑菌圈直径。根据扩散定律的推导,抗生素总量的对数值与抑菌圈直径的平方成线性关系,即通过检测抗生素对微生物的抑制作用,比较标准品与供试品产生抑菌圈的大小,计算出供试品的效价。 管碟法的基本操作和设计适用于各种抗生素,试验结果较稳定;样品用量少,灵敏度高;适合于大批样品的测定。然而凡具有抗菌活性的物质都会干扰测定结果;试验过程长,得出结果慢;操作手工化,需熟练人员才能得到较正确的结果;受扩散因素的影响,如培养基原材料的质量,一般琼脂中的杂质可能影响扩散速度及效价强度。尽管如此,由于它有上述的独特优点而被世界各国所公认,成为国际通用的方法被列入各国药典法规内。 二、制订方案
抗生素效价培训大全
抗生素效价培训内容 一、需要干热灭菌的器皿: C 二、以检磷酸泰乐菌素为例配置培养基和缓冲液的准备如下: ㈠①磷酸泰乐菌素原料含量测定标准:精密称取本品适量,加灭菌水定量制成每1ml中约 含1000单位的溶液,照抗生素微生物检定法测定。1000泰乐菌素单位相当于1mg的泰 乐菌素。 成品含量测定标准:精密称取本品适量,置100ml量瓶中,加灭菌磷酸盐缓冲液(pH6.0)40ml,加甲醇40ml,超声15分钟,摇匀,放冷,加灭菌磷酸盐缓冲液(pH6.0)稀释至 刻度,使成每1ml中约含1000单位的溶液,取上清液,照磷酸泰乐菌素项下的方法测定,即得。 ②查《中国兽药典》2005年版附录103页抗生素微生物检定法,可知: 泰乐菌素试验菌——藤黄微球菌(28001);培养基——Ⅱ,pH值为6.5~6.6或7.8~8.0; 灭菌缓冲液pH值——6.0;抗生素浓度范围2.5~10.0;温度——35~37; 时间——16~18 培养基Ⅱ制备方法: 胨6g;酵母浸出粉6g;琼脂15~20g;牛肉浸出粉 1.5g;葡萄糖1g;水1000ml 磷酸盐缓冲液(6.0)——取磷酸氢二钾2g与磷酸二氢钾8g,加水使成1000ml。 ③缓冲液及培养基配置完成后进行高压121℃湿热灭菌,时间为15~20min。 ㈡①标准品、原料、成品取样量的计算方法: 标准品效价:1034u/mg 原料效价:800u/mg 成品效价:880×104/100g 原料800u/mg×x=1000u×10ml x=0.0125g 成品 100g: 880×104=x:100ml×1000u x=1.13636g 标准品 1034u/mg×x=1000u×10ml x=0.00967g 注意事项:a.称量量必须大于应取的量,多余的量要另加溶液使溶液浓度达到标准;如 标准品取0.00992g,多加溶液量为x, 1034u/mg×9.92mg=1000u×x,x=10.26ml,则 另加溶液0.26ml。另外也要考虑容量瓶的体积,以免称量量过多使之盛不下。b.标准品 应从冰箱拿出后放置室温再进行称量。 ②稀释步骤: 取5ml 1000u/ml 50u/ml 缓冲液6.0定容至100ml 取5ml 50u/ml 5u/ml 缓冲液6.0定容至50ml 取5ml
抗生素生物效价测定
实验一抗生素生物效价测定 【实验目的】 1. 掌握抗生素生物效价测定的原理和方法; 2. 掌握管碟法测定抗生素生物效价相关的操作方法。 【实验原理】 抗生素的效价常采用微生物学方法测定,它是利用抗生素对特定的微生物具有抗菌活性 的原理来测定抗生素效价的方法,如管碟法。管碟法是目前抗生素效价测定的国际通用方法, 我国药典也采用此法。管碟法是根据抗生素在琼脂平板培养基中的扩散渗透作用,比较标准品和检品两者对试验菌的抑菌圈大小来测定供试品的效价。管碟法的基本原理是在含有高度 敏感性试验菌的琼脂平板上放置小钢管(内径6.0 ±.l mm,外径8.0 ±.l mm,高10±0. lmm),管内放人标准品和检品的溶液,经16~18小时恒温培养,当抗生素在菌层培养基中扩散时, 圈直径的平方成线性关系,比较抗生素标准品与检品的抑菌圈大小, 可计算出抗生素的效价。 常用的管碟法有:一剂量法、二剂量法、三剂量法。后二法已经列入药典。二剂量法系 将抗生素标准品和供试品各稀释成一定浓度比例(2:1或4:1)的两种溶液,在同一平板上比 较其抗药活性,再根据抗生素浓度对数和抑菌圈直径成直线关系的原理来计算供试品效价。 取含菌层的双层平板培养基,每个平板表面放置4个小钢管,管内分别放入供试品高、低剂量和标准品高、低剂量溶液。先测量出四点的抑菌圈直径,按下列公式计算出检品的效价。 (1)求出W 和V : W=(SH+UH)-(SL+UL)(式2.10-1) V= (UH+UL)-(SH+SL)(式2.10-2)式中:UH :供试品高剂量之抑菌圈直径; UL :供试品低剂量之抑菌圈直径; SH :标准品高剂量之抑菌圈直径; SL :标准品低剂量之抑菌圈直径; (2)求出0: 0 =D- antilo(IV/W )(式2.10-3)
临床抗生素的使用原则
1.治疗性应用的基本原则 (1)只能用于治疗感染性疾病所有抗生素仅用于治疗细菌、支原体、衣原体、真菌等所致的感染性疾病,非上述感染原则上不用抗生素。虽然近十年来,许多学者报导了大量的大环内酯类非抗菌作用,如用于治疗:慢性支气管哮喘、胃肠道神经源性运动障碍、胆囊结石等,但由于其易诱导细菌耐药性的产生,因此应十分谨慎地对待这些新用途,原则上不予利用。 (2)尽早确立病原菌诊断病原菌检查对感染性疾病的诊治有着极其重要的作用。虽然临床上许多感染性疾病可以通过经验性治疗治愈,但在不同的时间、不同的感染、不同的医疗单位,致病菌种类、构成、药物敏感性有着很大的差别。因此,为了找到敏感的抗生素,及时地控制感染,就应当及早确立感染性疾病的病原诊断,力争在使用抗生素治疗前,正确采集标本,及时送病原学检查及药敏试验,以期获得用药的科学依据。一旦获得培养结果,则应参考试验结果、临床用药效果等调整用药方案,进行目标治疗。 (3)针对性经验治疗在未获得准确的病原学诊断前或病情不允许耽误的情况下,应尽快判断感染性质,可进行针对性的经验治疗。对轻型的社区获得性感染,或初治患者可选用一般抗生素;对医院感染或严重感染、难治性感染应根据临床表现及感染部位,推断可能的致病菌及耐药情况,选用覆盖面广、抗菌活性强及安全性好的杀菌剂,可以联合用药。对导致脏器功能不全、危及生命的感染所应用的抗生素应覆盖革兰氏阳性球菌、革兰氏阴性杆菌、厌氧菌、真菌。 (4)结合临床评价细菌培养与药敏结果的意义应根据临床用药效果,尽快判断经验性治疗方案的有效性,以便参照“培养+药敏”的结果有针对性地选用作用强的敏感抗生素。无感染表现的阳性结果多无意义,应排除污染菌、正常菌群和寄殖菌的可能。 (5)选用作用强,在感染部位浓度高的抗生素应综合考虑以下因素: ①患者的疾病状况基础疾病种类、病情严重程度、病理、生理、免疫功能状况等。 ②药物的有效性包括抗生素的抗菌谱,抗菌活性、药代动力学特点(吸收、分布、代谢与排泄,如半衰期、血药浓度、组织浓度、细胞内浓度等),药效学特点及不良反应等。 ③本地区、医疗机构、病区细菌耐药状况选用致病菌敏感的抗生素。 ④给药途径应根据感染的严重程度及药代动力学特点决定给药途径,轻症感染尽量选用生物利用度高的口服制剂。 ⑤有多种药物可供选用时,应以窄谱、不良反应少、价廉者优先。 ⑥其它药物的相互作用、供应等。 (6)要注意及时更换抗生素要根据临床疗效或(和)微生物检查结果来决定是否需要更换所用的抗生素一般感染患者用药72小时(重症感染48小时)后,就可根据临床疗效来判断所用抗生素的有效性。 (7)要有合理的治疗终点或疗程一般感染待症状、体征及实验室检查明显好转或恢复正常后再继续用药2~3天,就可终止抗感染治疗;特殊感染按特定疗程执行,如结核病等。 (8)要重视必要的综合治疗在应用抗生素治疗细菌感染的过程中,必须充分认识到人体免疫力的重要性,过分依赖抗生素的功效而忽视人体内在因素常是抗生素治疗失败的重要原因之一。因此,在应用抗生素的同时,必须尽最大努力使人体全身状况有所改善,各种综合性措施如纠正水、电解质和酸碱平衡失调,改善微循环,补充血容量,输血、血浆、白蛋白或氨基酸,处理原发病和局部病灶等,均不可忽视。 (9)要尽量避免皮肤粘膜局部用药如果局部感染较轻,或感染较重但全身用药在局部感染病灶难以达到有效浓度时,可考虑局部选用如下外用制剂:呋喃西林、新霉素、杆菌肽、磺胺嘧啶银、莫匹罗星、磺胺醋酰钠等。不允许擅自将全身用制剂在局部使用,以防对临床常用药物耐药的菌株产生。(10)指征明确才能联合使用抗生素只有那些病因未明的严重感染、多种细菌引起的混合感染需长期用药、细菌有可能产生耐药才能联合使用抗生素。
