大学网络教育学院-药物化学2试题及答案

药物化学模拟卷2
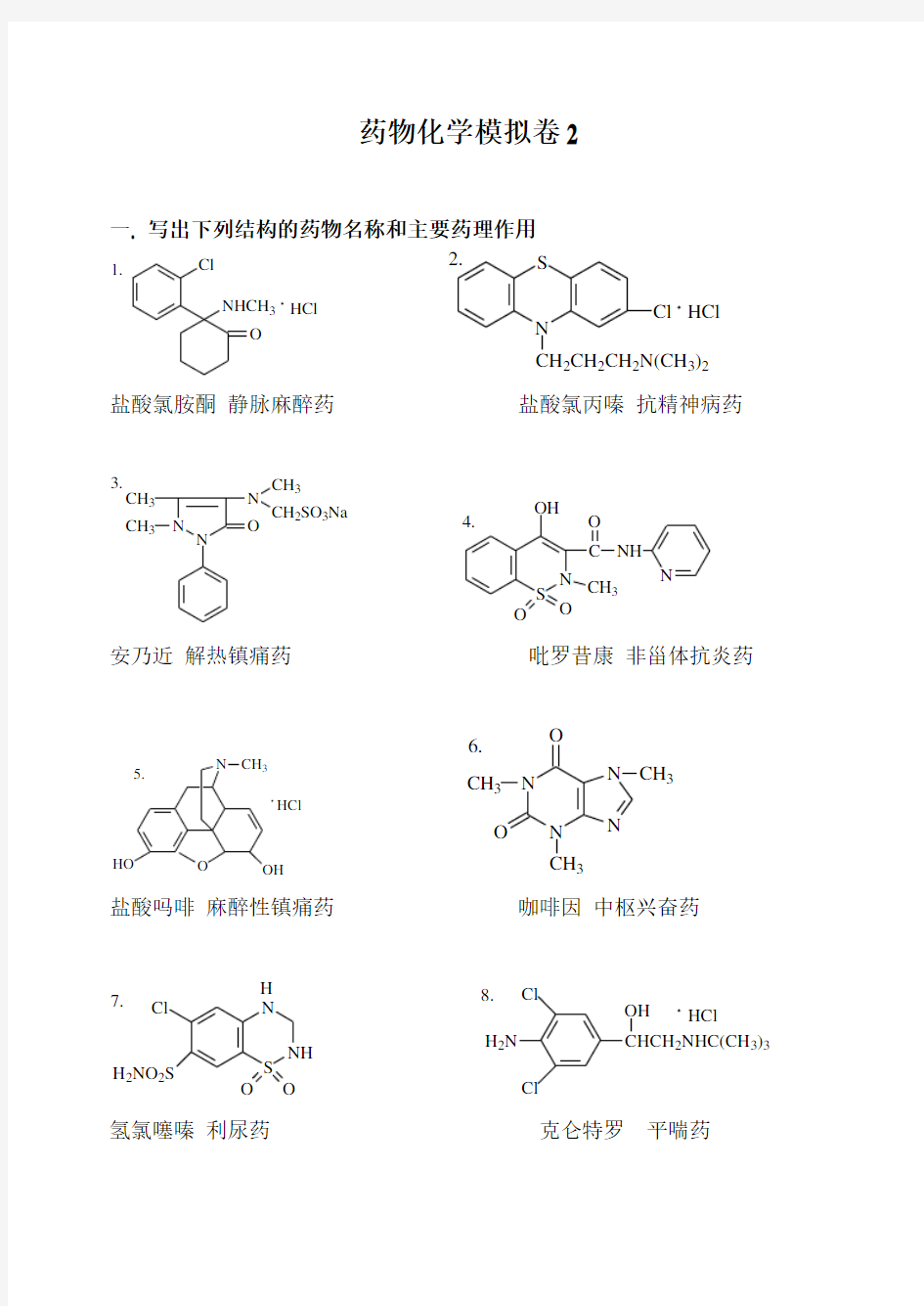
一. 写出下列结构的药物名称和主要药理作用
O
NHCH 3Cl
HCl
1.
N
S 2CH 2CH 2N(CH 3)
2
Cl HCl
2.
盐酸氯胺酮 静脉麻醉药 盐酸氯丙嗪 抗精神病药
N N
O N CH 3CH 2SO 3Na
CH 3CH 3
3.
S
N O
O
OH
C O NH
N
CH
3
4.
安乃近 解热镇痛药
吡罗昔康 非甾体抗炎药
HCl
N N N
N O O
CH 3
CH 3
CH 36.
盐酸吗啡 麻醉性镇痛药 咖啡因 中枢兴奋药
S NH N Cl
H 2NO 2S
O
O
H 7.
Cl
H 2N
Cl
CHCH 2NHC(CH 3)3
OH
HCl
8.
氢氯噻嗪 利尿药 克仑特罗 平喘药
HS
CH 2CH CH 3C O N
COOH
9.
CH 3
卡托普利 抗高血压药 青蒿素 抗疟药
二. 写出下列药物的化学结构和主要药理作用 1.盐酸丁卡因 2.苯巴比妥
N
C 4H 9
H
COOCH 2CH 2N(CH 3)2
HCl
NH
O
O
O CH 3CH 2
局麻药 镇静催眠药或抗癫痫药
3.地西泮
4.乙酰水杨酸
N
N CH 3O
Cl
COOH
OCOCH 3
镇静催眠药或抗癫痫药 解热镇痛药
5.布洛芬
6.盐酸哌替啶
COOH
N
CH 3
COOC 2H 5
HCl
非甾体抗炎药 镇痛药
7.螺内酯 8.硫酸阿托品
O
O SCOCH 3
O
CH 2OH
2
H 2SO 4
利尿药 解痉药
三.回答下列问题
1、如何改善丙戊酸钠的吸湿性?
制备片剂时,环境湿度小于41%;加入少量有机酸如硬脂酸,枸橼酸等,生成丙戊酸-丙戊酸钠复合物。
2、比较咖啡因、可可豆碱和茶碱的中枢作用的强弱,并说明原因。
咖啡因> 茶碱>可可豆碱,取代基的多少与位置有关
3、肾上腺素、去甲肾上腺素、异丙肾上腺素和沙丁胺醇各作用于什么受体?
肾上腺素:αβ受体;去甲肾上腺素:α受体;异丙肾上腺素:β受体; 沙丁胺醇:β2>>>β1受体
4、说明利多卡因较普鲁卡因化学稳定性好的原因。
利多卡因以其结构中的酰胺键区别于普鲁卡因的酯键。酰胺键较酯键稳定,另外利多卡因酰胺键的两个邻位均有甲基,有空间位阻,使利多卡因的酸或碱性溶液均不易水解,体内酶解的速度也比较慢。因此利多卡因较普鲁卡因作用强,稳定性好。
5、说明耐酸青霉素的结构特点。
耐酸青霉素酰胺侧链的α-碳原子上都具有吸电子基,由于吸电子基的诱导效应,阻碍了青霉素在酸性条件下电子转移不能生成青霉二酸,故对酸稳定。
6、吩噻嗪类药物N 10与侧链N 之间间隔2,3个碳原子,各有什么样的药理作用?
吩噻嗪母核与侧链上碱性氨基之间相隔3个碳原子是本类药物的基本结构。碳链延长或缩短则活性减弱或消失,若相隔2个碳原子则抗精神病作用减弱而抗组胺作用增强。
7、如何增加咖啡因在水中的溶解度?
为了增加溶解度,制成注射液使用,可用有机酸或其碱金属盐,如苯甲酸钠,水杨酸钠等形成复盐。
8、说明鸦片受体的结构特点。
a 、一个平坦的结构,可以和药物的苯环通过范德华力连接;
b 、一个阴离子部位能和药物的正电中心以静电结合;
c 、一个方向合适的空穴与哌啶环相适应。
四.写出下列药物的一种主要代谢产物的化学结构
N
Cl
CH 3O
1
CO N
C N
CO C 2H 5
O
H H
2
CH 3
CH 3
NHCOCH 2N(C 2H 5)23
N
CONHNH 2
4
N N O
O
C 4H 9
5
答案:
N
Cl
CH 3O
1
N
Cl
CH 3O OH
N
Cl
H
O OH
或
CO N
C N
CO C 2H 5
O
H H
2
CO N
C N
CO C 2H 5
O
HO
H H
CH 3
CH 3
NHCOCH 2N(C 2H 5)23
CH 3
CH 3
NHCOCH 2NH 2
N CONHNH 2
4
N
CONHNHCOCH 3
N
N O
O
C 4H 9
5
N
N O
O
C 4H 9
OH
大学普通化学综合练习题1
普通化学练习题 一、选择题(将唯一正确答案的序号填入括号内, 每题2分,共15题,计30分。) 1.下面对功和热的描述正确的是A A.都是途径函数,无确定的变化途径就无确定的数值 B.都是途径函数,对应于某一状态有一确定值 C.都是状态函数,变化量与途径无关 D.都是状态函数,始终态确定,其值也确定 2.已知在等温等压条件下进行的某反应A(g)+B(g)=C(g)+D(l)的H0、S0,则该反应A A.低于某温度时正向自发 B.高于某温度时正向自发 C.任意温度时正向均自发 D.任意温度时正向均非自发 3.下列说法正确的是D A.H>0的反应都是自发反应。 B.某反应的G(298K)=10KJ·mol-1, 表明该反应在298K温度下不可能自发进行。C.已知(Fe3+/Fe2+(Cu2+Cu),则反应Fe3+(aq)+Cu(s) = Cu2+(aq)+Fe 2+(aq)向左进行。 D.对于AB2型难溶电解质来讲,k sp越大,则其溶解度越大。 4.下列说法错误的是D A.Ag+与Cl-混合,不一定有沉淀生成。 B.反应A(g)+B(g)=C(g),H0; 达到平衡后,若升高温度,则平 衡常数K减小。 C.电极电势越小,则其对应的还原态物质的还原性越强。 D.在H2S(g)的饱和溶液中,C eq(H+)是C eq(S2-)的2倍。
5.下列溶液的浓度均为mol·dm-3,渗透压最大的是D A.C6H12O6+(葡萄糖) B.HAc C.NaCl D.Na2SO4 6.已知(Cu2+/Cu)>(Zn2+/Zn),其中最强的还原剂是D A.Cu2+ B.Cu C.Zn2+ D.Zn 7.下列电极电势与C(H+)无关的是A A.(Fe3+/Fe2+) B.( H+/H2) C.(O2/OH-) 8.在标准条件下,f H m、S m、f G m均为零是C A.H2O(l) B.H2(g) C.H+(aq) D.H2O2 (l) 9.某温度时,下列反应已达到平衡CO(g)+H2O(g)=CO2 (g)+H2 (g),H<0,为要提高 CO的转化率,可采取方法D A.增加总压力 B.减少总压力 C.升高温度 D.降低温度
中大药物化学考试复习答案..
(一)名词解释 1.药物:凡具有治疗、预防、缓解和诊断疾病或调节机体生理功能、符合药品质量标准并经政府有关部门批准的特殊化学品。(PPT 13-1, P1) 2.药物化学:是关于药物的发现、发展和确证,并在分子水平上研究药物作用方式的一门学科。(PPT 13-1,P1) 3.血脑屏障:血脑屏障是指脑毛细血管阻止某些物质(多半是有害的)由血液进入脑组织的结构。(百度百科) 4.拟胆碱药:是一类具有与乙酰胆碱相似作用的药物。(P85) 5.乙酰胆碱酯酶抑制剂:又称为抗胆碱酯酶药,通过对乙酰胆碱酯酶的可逆性抑制,达到使乙酰胆碱 (ACh)在突触处的积累,延长并且增加了乙酰胆碱的作用。(百度百科) 6.抗胆碱药:主要是阻断乙酰胆碱与胆碱受体相互作用的药物。(百度百科) 7.拟肾上腺素药:是一类通过兴奋交感神经而发挥作用的药物,亦称为拟交感神经药(P107) 8.局部麻醉药:是指当局部使用时能够可逆性阻断周围神经冲动从局部向大脑传递的药物(P131) 9. 钙通道阻滞剂:是在细胞膜生物通道水平上选择性地阻滞Ca2+经细胞膜上的钙离子通道进入细胞内,减少细 胞内Ca2+浓度的药物(P149) 10. NO供体药物:在体内释放出外源性NO分子的药物。(P175) 11. 血管紧张素转化酶抑制剂:指抑制血管紧张素转化酶活性的化合物。它通过抑制血管紧张素Ⅱ的生物合成 而控制高血压。(百度百科) 12. 羟甲戊二酰辅酶A(HMG–CoA)还原酶抑制剂:或称他汀,是一类新型抗高血脂药物。这类药物能有效的 阻止内源性胆固醇的合成,显著降低血中胆固醇的水平。(百度百科) 13. 质子泵抑制剂:即H+/K+-ATP酶抑制剂,通过抑制H+与K+的交换,组织胃酸的形成。(P209) 14. 前列腺素:是一类含20个碳原子,具有五元酯环,带有两个侧链的一元脂肪酸。(P409) (二)名词解释: 15.非甾类抗炎药:是一类具有解热、镇痛,多数还有抗炎、抗风湿作用的药物。由于其化学结构和抗炎机制与糖皮质激素甾体抗炎药(SAIDS)不同,故又称为非甾体类抗炎药(NSAIDS)(百度百科查取) 16.生物烷化剂:也称烷化剂,属于细胞毒类药物,是抗肿瘤药物中使用得最早、也很重要的一类药物(书本P258) 17.抗代谢药物:是指能与体内代谢物发生特异性结合,从而影响或拮抗代谢功能的药物,通常它们的化学结构与体内的核酸或蛋白质代谢物相似。(百度百科查取、书本P270) 18.抗生素:是微生物的次级代谢产物或合成的类似物,能在小剂量的情况下对各种病原菌微生物有抑制或杀灭作用,而对宿主不会产生严重的毒副作用(P294)。 19.β-内酰胺酶抑制剂:β-内酰胺酶抑制剂也属于非经典β-内酰胺类抗生素,是针对细菌对β-内酰胺类抗生素产生耐药机制而研究发现的一类药物。它们对β-内酰胺酶有很强的抑制作用,本身又具有抗菌活性。(P316)20.核苷类逆转录酶抑制剂:是合成HIV的DNA逆转录酶底物脱氧核苷酸的类似物,在体内转化成活性的三磷酸核苷衍生物,与天然的三磷酸脱氧核苷竞争性与HIV逆转录酶(RT)结合,抑制RT的作用,阻碍前病毒的合成。(P370) 21.利尿药:利尿药(diuretics)是一类能够增加尿液生成率的化合物。其主要作用于肾脏来增加尿液的流速,
[实用参考]大学化学普通化学习课后题答案.doc
普通化学马家举 第一章物质结构基础习题 4假定有下列电子的各套量子数,指出哪几套不可能存在,并说明原因。 (1)3,2,2,1/2;(2)3,0,-1,1/2;(3)2,2,2,2; (2)当角量子数l 取0时,磁量子数m 不能取-1。 (3)当主量字数取2时,角量子数不能取2;自旋量子数不能取2,只能取+1/2或-1/2。 5写出原子序数为47的银原子的电子分布式,并用四个量子数表示最外层电子的运动状态。 Ag :1s 22s 22p 63s 23p 63d 104s 24p 64d 105s 15,0,0,+1/2。 试用杂化轨道理论解释: (1) H 2S 分子的键角为920,而PCl 3的键角为1020。 (2) NF 3分子为三角锥形构型,而BF 3分子为平面三角形构型。 (1) H 2S 分子与H 2O 分子一样,中心原子采取sp 3不等性杂化,在两个孤电子对的作用下,两个H-S 键键角减小。之所以键角小于H 2O 分子中两个H-O 键的键角104045’,是因为H-S 键的成键电子对更靠近H 原子,两个H-S 键之间的斥力小,被压缩的程度更大。PCl 3分子与NH 3分子一样,也是中心原子采取sp 3不等性杂化,同理Cl-P 键的成键电子对更靠近Cl 原子,所以两个P-Cl 键的键角小于NH 3分子中两个N-H 键的键角。 (2) NF3分子与NH 3分子一样中心原子采取sp 3不等性杂化,使分子产生三角锥形构型;BF 3分子中心 原子B 采用sp 2 等性杂化,使分子产生平面三角形构型。 7为什么(1)室温下CH 4为气体,CCl 4为液体,而CI 4为其固体?(2)水的沸点高于H 2S ,而CH 4的沸点低于SiH 4? (1) 从CH 4→CCl 4→CI 4分子量增加,分子间色散力增大,而色散力在范德华力中占较大比例,即分子 间力是增大的,而分子间力越大,熔沸点越高。 (2) H 2O 分子与H 2S 分子相比,水中H 2O 分子之间存在氢键,虽然H 2O 分子间的色散力较小,氢键的存 在却使沸点更高一些。CH 4分子之间没有氢键,只能比较色散力大小,故分子量小的CH 4的沸点低于分子量大的SiH 4的沸点。 第二章热力学基础习题 6计算下列反应的(298.15)r m H K θ ?和(298.15)r m S K θ ? (1)32224NH (g)+3O (g)==2N (g)+6H O(l) (2)22224C H (g)+H (g)==C H (g) (1) 2232111 (298.15)2(N ,g)6(H O,l)4(NH ,g)3(O ,g) 206(285.83kJ mol )4(46.11kJ mol )301530.54kJ mol r m f m f m f m f m H K H H H H θθθθθ ---?=?+?-?-?=?+?-?-?-?-?=-? 22321111111111 (298.15)2(N ,g)6(H O,l)4(NH ,g)3(O ,g) 2191.6J mol K 669.91J mol K 4192.4J mol K 3205.14J mol K 582.36J mol K r m m m m m S K S S S S θθθθθ----------?=+--=???+???-???-???=-?? (2) 24242111 (298.15)(C H ,g)(C H ,g)(H ,g) (52.26kJ mol )(226.7kJ mol )0174.44kJ mol r m f m f m f m H K H H H θθθθ---?=?-?-?=?-?-=-? 2424211111111 (298.15)(C H ,g)(C H ,g)(H ,g) (219.6J mol K )(200.9J mol K )(130.68J mol K )111.98J mol K r m m m m S K S S S θθθθ--------?=--=??-??-??=-?? 7利用下列反应的(298.15)r m G K θ ?值,计算Fe3O4(s )在和298.15K 时的标准摩尔生成吉布斯函数。 (1)1223r 2Fe(s)+3/2O (g)==Fe O (s), (298.15)742.2kJ mol m G K θ -?=-? (2)12334r 4Fe O (s)+Fe(s)==3Fe O (s) (298.15) 77.7kJ mol m G K θ -?=-? 1 1 1 (298.15)(4/3)(1)(1/3)(2) (4/3)(742.2kJ mol )(1/3)(77.7kJ mol )1015.5kJ mol r m r m r m G K G G θθθ---?=?+?=?-?+?-?=-? 8估算反应222CO (g)+H (g)==CO(g)+H O(g)在873K 时的标准摩尔吉布斯函数变和标准平衡常数。
生物化学中山大学本科生笔记整理知识点汇编各章名词解释
生物化学知识点汇编 知识点: 1、各类糖分子的结构和功能;
2、脂类中与生物膜有关的物质结构与功能; 3、核酸的基本结构、相互关系与功能; 4、各类氨基酸的基本结构、特征以及蛋白的构象与功能的关系; 5、酶的分类、作用机制、抑制类型、动力学过程与调节; 6、代谢中的生物氧化过程特别是光合磷酸化过程的机理及意义; 7、代谢中的糖代谢过程; 8、核酸的生物合成、复制、转录及基因表达; 9、各种代谢过程的调控及相互关系; 10、现代生物学的方法和实验手段特别是分离、纯化、活性册顶的基本方法等; 11、生物化学研究进展; ◎●将两种旋光不同的葡萄糖分别溶与水后,其旋光率均逐渐变为+52.7°。,称为变旋现象。 ◎●羟甲基在糖环平面的上方的为D-型,在平面的下方的为L-型。在D-型中,半缩醛羟基在平面的下方的为α-型,在平面的上方的为β-型。 ◎●一切糖类都有不对称碳原子,都具旋光性。 ◎●区分酮糖、醛糖用Seliwanoff反应。 ◎●天然糖苷多为β-型。 ◎●糖醛酸是肝脏内的一种解毒剂。 ◎●自然界存在的糖胺都是己糖胺。 ◎●麦芽糖为[α-D-葡萄糖-α(1→4)-α-D-葡萄糖苷],异麦芽糖为[α-D-葡萄糖-α(1→6)-α-D-葡萄糖苷],蔗糖为[α-D-葡萄糖-α,β(1→4)-果糖苷],乳糖为[半乳糖-β(1→4)-α-D-葡萄糖苷],纤维二糖为[α-D-葡萄糖-β(1→4)α-D-葡萄糖苷]。 ◎●直链淀粉成螺旋状复合物,遇碘显紫蓝色,碘位于其中心腔内,在620——580nm有最大光吸收。支链淀粉分支平均有24——30个葡萄糖,遇碘显紫红色,在530——555nm有最大光吸收。糖原遇碘显棕红色,在430——5490nm有最大光吸收。◎●与糖蛋白相比,蛋白聚糖的糖是一种长而不分支的多糖链,即糖胺聚糖。其一定的部位上与若干肽链连接,糖含量超过95%,多糖是系列重复双糖结构。 ◎●糖蛋白是病毒、植物凝集素、血型物质的基本组成部分,Fe2+、Cu2+、血红蛋白和甲状腺素转运蛋白是糖蛋白,它们分别叫转铁蛋白、铜蓝蛋白、触珠蛋白、甲状腺素结合蛋白。参与凝血过程的糖蛋白有:凝血酶原、纤维蛋白酶原。 ◎●血型物质含75%的糖,它们是:岩藻糖、半乳糖、葡萄糖、半乳糖胺。 ◎●木糖-Ser连接为结缔组织蛋白聚糖所特有。 ◎●动植物体的不饱和脂肪酸为顺式,细菌中含脂肪酸种类少,大多为饱和脂肪酸,有的有分支。 ◎●分析脂肪酸混合物的分离用气液柱层析,即气液色谱技术。 ◎●甘油三酯、甘油单酯形成小颗粒微团,叫micelles。 ◎●烷基醚脂酰甘油含有2个脂肪酸分子和一个长的烷基或烯基链分别与甘油分子以酯键、醚键相连。 ◎●糖基脂酰甘油中,糖基与甘油分子第三个羟基以糖苷键相连。 ◎●磷脂根据所含醇类可分为甘油磷脂类和鞘氨醇磷脂类。 ◎●不饱和脂肪酸常与甘油分子的第二个碳原子羟基相连。 ◎●肝脏、心肌中的甘油磷脂多为磷脂酰肌醇,脑中的甘油磷脂多为磷脂酰肌醇磷酸、磷脂酰肌醇二磷酸。 ◎●缩醛磷脂中一个碳氢键以醚键与甘油C1羟基相连。 ◎●除了11-顺-视黄醛外,多数直链萜类的双键均为反式。 ◎●柠檬油的主要成分是柠檬苦素,薄荷油的主要成分是薄荷醇,樟脑油的主要成分是樟脑。 ◎●胆石几乎全是由胆固醇组成,它易与毛地黄核苷结合沉淀。 ◎●脊椎动物体内,胆酸能与甘氨酸、牛黄氨酸结合成甘氨胆酸、牛黄胆酸。 ◎●蟾毒不以糖苷而以酯的形式存在。 ◎●前列腺素是花生四烯酸及其他不饱和脂肪酸的衍生物。分为PGA、PGB、PGD、PGE、PGF、PGG、PGH、PGI 等八类,其功能有:平滑肌收缩、血液供应、神经传递、发炎反应的发生、水潴留、电解质去钠、血液凝结。◎●在tay-sachs病中,神经节苷脂在脑中积累。 ◎●按生理功能,蛋白质可分为酶、运输蛋白、营养和贮存蛋白、收缩蛋白运动蛋白、结构蛋白质和防御蛋白质。◎●胱氨酸、酪氨酸不溶于水。脯氨酸、羟还能溶于乙醇或乙醚中。
大学普通化学习题资料#(精选.)
一、判断题(对的在括号内填“√”,错的填“×”) (1)已知下列过程的热化学方程式为UF 6(l) = UF 6(g);11.30-?=?mol kJ H m r θ,则此温度时蒸发1mol UF 6(l),会放出热30.1 kJ 。( ) (2)在定温定压条件下,下列两个生成液态水的化学方程式所表达的反应放出的热量是一 相同的值。( ))1()(2 1(g)H 222O H g O =+ )1(2)()(H 2222O H g O g =+ (3)功和热是在系统和环境之间的两种能量传递方式,在系统内部不讨论功和热。( ) 4)对反应系统 )()()()(C 22g H g CO g O H s +=+,11 ,3.131)15.298(-?=?mol kJ K H m r θ。由于化学方程式两边物质的化学计量数的总和相等,所以增加总压力对平衡无影响。 ( ) (5)反应的级数取决于反应方程式中反应物的化学计量数。( ) (6)催化剂能改变反应历程,降低反应的活化能,但不能改变反应的θ m r G ?。( ) (7)两种分子酸HX 溶液和HY 溶液有同样的pH ,则这两种酸的浓度)3-?dm mol (相同。( ) (8)2PbI 和3CaCO 吨的溶度积均近似为-910,从而可知在它们的饱和溶液中。 的者的+2Pb 浓度与后者的+2Ca 浓度近似相等。( ) (9)3MgCO 的溶度积61082.6-?=s K 这意味着所有含有团体3MgCO 的溶液中, )()(232-+=CO c Mg c ,而且62321082.6)()(--+?=?CO c Mg c 。 ( ) (10)当主量子数n =2时,角量子数l 只能取1。 ( ) (11)多电子原子轨道的能级只与主量子数n 有关。 ( ) (12)就主族元素单质的熔点来说,大致有这样的趋势:中部熔点较高,而左右两边的熔点 较低。 ( ) (13)活泼金属元素的氧化物都是离子晶体,熔点较高;非金属元素的氧化物都是分子晶体, 熔点较低。 ( ) (14)同族元素的氧化物2CO 与2SiO ,具有相似的物理性质和化学性质。 ( ) (15)对于放热反应,正反应的活化能应小于逆反应的活化能。 ( ) (16)s 电子绕核起动的轨道为一圆圈,而p 电子走的8字形轨道。 ( ) (17)螯合物的稳定性大于一般配合物。 ( ) (18) 往HAc 稀溶液中加入水,HAc 的解离度增大,所以)c(H + 也增大。 ( ) (19)[AgCl 2]?和[Co(NH 3)6]2+的θ稳K 值十分相近, 所以只要溶液中中心离子Ag +和Co 2+的浓度相同,则配体Cl ?和NH 3的浓度也相同,溶液中的两种配离子的浓度也一定相近。( ) (20)恒温定压条件下进行的一个化学反应,ΔH=ΔU+pΔV ,所以ΔH 一定大于ΔU 。 ( ) (21)任何单质、化合物或水合离子,298.15K 时的标准熵均大于零。 ( )
中山大学生命科学院生物化学试题答案与评分标准(2006秋季,A卷)
生物化学I(2006年秋季学期, A卷) I.简答题(共25小题,超过60分以60分计入总分) 1.哪些标准氨基酸含两个手性碳原子?写出它们的Fisher投影式。 2.为什么SDS变性电泳可以估算蛋白质的分子量? 3.Mass spectroscopy在生物大分子研究中有什么应用? 4.-Keratin、Collagen、Silk fibroin的二级结构和氨基酸组成有何特点?5.根据二级结构的组成和排列可将蛋白质结构分为哪些类型? 6.蛋白质in vivo条件下的折叠有哪些辅助因子? 7.蛋白质在与其他分子的相互作用中发挥作用,这种相互作用有何特点? 8.哪些因素可以导致Hemoglobin与O 2 的亲和力增加? 9.图示抗体的一般结构(包括结构域及可能的二硫键)。 10.构成肌肉粗丝和细丝的蛋白分子有哪些,各有什么功能? 11.写出蛋白质氨基酸测序的基本步骤。 12.什么是酶催化的过渡态理论?列出你所知道的支持证据? 13.酶的可逆抑制剂有几类?它们的抑制动力学各有何特点? 14.酶在体内的活性是如何受到调控的? 15.淀粉与纤维素的结构有何区别? 16.细胞膜表面的Glycoprotein和Glycolipid有哪些生物学功能? 17.细胞内的DNA可能会出现哪些异常结构,他们有什么生物学意义? 18.膜脂的分类及其结构特点 19.生物膜的功能有哪些? 20.膜蛋白以哪些方式参与生物膜的构成? 21.图示secondary active transport,uniport,symport,antiport. 22.Acetylcholine receptor通道是如何控制开关的? 23.K+离子通道是如何对通过的离子进行选择的? 24.膜电位是怎样控制Na+通道开关的(可图示并说明)? 25.Ca2+泵和Na+-K+泵的异同点。 II. You have a crude lysate sample containing a mixture of six proteins (1, 2, 3, 4, 5, and β-galactosidase). Some characteristics of these proteins are shown in the table below. Give an available procedure of purifying β-galactosidase. Protein Concentration of ammonium sulfate required for precipitation Molecular Weight (kDa) Isoelectric point (pI)
(中山大学必备)人卫版药理学第七版笔记及总结
人卫版药理学第七版笔记及总结 写在前面:此总结综合了前届所留资料以及个人总结,凡出现页码均为新版教材(《药理学第七版》人卫版殷明主编)和新版教材配套习题集,如有谬误,还请指正哈! 使用说明:建议将书看一遍或者结合书来看,这样效果会好一些! 第一篇总论 第一章 1. 药效学pharmacodynamics:研究药物对机体作用及其作用机制,以阐明药物防治疾病的规律。 2. 药动学pharmacokinetics:研究机体对药物处置的动态变化。包括药物在机体内的吸收、分布、代谢(生物转化)及排泄过程,特别是血药浓度随时间变化规律。 3. 临床前药理研究:药效学研究、一般药理学研究、药动学研究、新药毒理学研究。 4. 药物理化性质:脂溶性、解离度、分子量 第二章药动学 1.药物转运体: 2.首过效应:(first past effect) P14 :某些药物经口服后首次通过肠壁或肝脏时被其中的酶代谢使进入人体循环有效药量减少的现象(其属于吸收过程) 3.半衰期(half-life,t1/2):血浆药物浓度降一半所需的时间 4.表观分布容积:(Vd apparent volume of distribution)体内药物总量按血药浓度推算时所需的体液总体积 5.血药浓度-时间曲线下面积 (AUC area under the concentration-time curve ):血药浓度对时间作图,所得曲线下的面积,是计算生物利用度的基础数值 6.生物利用度(bioavailability,F)bioavailability F ):药物活性成分从制剂释放进入血液循环的程度和速度,程度用AUC表示,速度用达峰时间表示 7.总体清除率(total body clearance,CLtot):体内诸多消除器官单位时间内清除药物的血浆体积,即单位时间内有多少毫升血浆中所含药量被清除。又称血浆清除率(plasma clearance,CLp) 8.稳态血药浓度(steady-state plasma concentration,Css),又称坪值(plateau):Css steady-state plasma concentration :随着给药次数增加,体内总药量的蓄积率逐渐下降,直至在给药间隔内消除的药量等于给药量,从而达到平衡,此时的血药浓度称为稳态血药浓度Css ,达到Css的时间仅取决于半衰期。 9.药物代谢:I相反应(氧化、还原、水解); II相反应(结合) 10. 肝药酶的诱导剂:苯巴比妥、苯妥英钠、利福平、水合氯醛、卡马西平 肝药酶的抑制剂:氯霉素、异烟肼、别嘌醇、磺胺苯吡唑、西咪替丁 ※肝药酶特点、定义及临床意义P19 11. 一级动力学过程(first-order kinetic process) 概念:指药物在某房室或某部位的转运速率(dC/dt)与该房室或该部位的药量D或浓度C的一次方成正比。 特点: (1)药物转运呈指数衰减,每单位时间内转运的百分比不变,即等比转运,但单位时间内药物的转运量随时间而下降。
中山大学-药化笔记 by丽纯师姐
1、抗菌药 ①细菌前提:能被革兰氏试剂(结晶紫和碘)染为蓝色的称为革兰氏阳性菌G+);相反不能染色或呈粉红色的称为革兰氏阴性菌(G-) ②对抗菌药物的要求: 具有较高的抗菌选择性 细菌不易对药物产生抗药性 具有良好的吸收和代谢性质 ③抗菌药物的作用机制 1) 干扰细胞壁的合成 2) 损伤细胞膜: 3) 抑制细菌蛋白质的合成 4) 抑制和干扰核酸的合成 2、磺胺药作用:抑菌繁殖但不能灭菌,对大多数革兰氏阳性和许多革兰氏阴性细菌有效。但个别菌种的菌株可能对其耐药。磺胺类药物通过竞争性抑制叶酸代谢循环中的对氨基苯甲酸而抑制细菌性增殖。细菌对1种磺胺类耐药意味着对所有的磺胺药耐药。
3、喹诺酮类药作用机制:选择性地抑制原核生物DNA TOPⅡ,从而导致这种酶对DNA 不能发挥正常的功能,最后导致DNA降解及菌体死亡。耐药性:细菌降低细胞壁的通透性,或激活细胞膜上的药物外排泵;DNA拓扑异构酶发生突变使药物酶DNA复合物的稳定性降低,导致细菌能够耐受高浓度的药物。
4、噁唑烷酮类抗菌药物:与细菌核糖体50S亚基作用,阻止蛋白质合成的开始。与四环素、氯霉素,林可霉素等现有抑制细菌蛋白质合成的药物作用机制和位点不同,因此不产生交叉耐药性。
5、①抗结核药物作用机制:干扰NADH正常氧化还原;阻断去饱和酶作用,抑霉菌酸生成。喹诺酮类抗结核药物:莫西、环丙、氧氟、司帕沙星。②抗结核抗生素通过抑制分枝杆菌的DNA依赖性的RNA聚合酶, 阻止细菌合成RNA。利福平一般与其他抗结核药物联合使用,单独使用易产生耐药性。抗生素:环丝氨酸、卷曲霉素、紫霉素。
6、抗真菌药①作用于麦角甾醇的药物作用机制:两性霉素等多烯类抗生素与真菌细胞膜上的麦角甾醇结合,损伤膜的通透性,细菌细胞内K+、核苷酸、氨基酸等外漏,破坏正常代谢而起抑菌作用。②P450脱甲基酶抑制剂作用机制:通过抑制真菌细胞色素P-450脱甲基酶,阻断真菌细胞内羊毛甾醇转化为麦角甾醇,损坏真菌细胞膜的完整性。 7、抗病毒药物 ? 阻止病毒吸附的药物(如丙种球蛋白) ? 抑制病毒核酸复制的药物(如碘苷) ? 阻止病毒穿入细胞的药物(如金刚烷胺) ? 影响核糖体翻译的药物(如美替沙腙) ? 流感病毒神经氨酸酶抑制剂(如达菲) ? HIV逆转录酶抑制剂(AZT) ? HIV蛋白酶抑制剂(如利托那韦) 一、镇静催眠药 1、苯二氮卓类——地西泮 A、结构特点 地西泮
贵州大学大学普通化学期末试题及答案
贵州大学2009-2010学年第二学期考试试卷 《大学化学(1)》A 卷 参考答案 注意事项: 1. 请考生按要求在试卷装订线内填写姓名、学号和年级专业。 2. 请仔细阅读各种题目的回答要求,在规定的位置填写答案。 3. 不要在试卷上乱写乱画,不要在装订线内填写无关的内容。 4. 满分100分,考试时间为120分钟。 一、选择题(本大题共10个小题,每个2分,共20分, 将1个或2个正确答案的代码填入括号内,选错或未选均 无分) 1. 已知:A + B → M + N (θ m r H ?)1 = 35 kJ·mol -1 2M + 2N → 2D (θ m r H ?)2 = - 80 kJ·mol -1 则A + B → D 的 (θ m r H ?)3 是( C )。 (A)-10 kJ·mol -1 (B)-45 kJ·mol -1 (C)-5 kJ·mol -1 (D)25 kJ·mol -1 2. 下列说法正确的是( C )。 (A) 热的物体比冷的物体含有更多的热量; (B) 同一种状态可能有多个热力学能值; (C) 热是一种传递中的能量; (D) 物体温度越高,则所含热量越高。 3.在平衡系统中 PCl 5(g) PCl 3(g) + Cl 2(g) ΔrH θ m >0 欲增大生成物Cl 2平衡时的浓度,需采取下列哪些措施( B D )。 (A)加大压力 (B)加大PCl 5浓度 (C)降低温度 (D)升高温度 4. 如果一个反应的吉布斯自由能变为零,则反应 ( D )。
(A) 能自发进行 (B) 是吸热反应 (C) 是放热反应 (D) 处于平衡状态 5.下列物质中含有氢键的是( B D )。 (A)HBr (B) HF (C) CCl 4 (D) H 2SO 4 6.在标准条件下,下列反应均为正方向进行: Cr 2O 72-+6Fe 2++14H +=2Cr 3++6Fe 3++7H 2O 2Fe 3++Sn 2+=2Fe 2++Sn 4+ 它们中间最强的氧化剂和最强的还原剂是( B )。 (A) Sn 2+和Fe 3+ (B) Cr 2O 72-和Sn 2+ (C)Cr 3+和Sn 4+ (D) Cr 2O 72-和Fe 3+ 7.下列各物质只需克服色散力就能沸腾的是( B )。 (A)H 2O (B)Br 2(l ) (C)NH 3(l ) (D)C 2H 5OH 8.下列各离子变形性最强的是( B )。 (A)O 2- (B)S 2- (C)F - (D)Na + 9. 已知H 3PO 4的电离常数:K 1 = 7.5 ? 10-3,K 2= 6.23 ? 10-8,K 3 = 3.6 ? 10-13,则0.10 mol·dm -3 H 3PO 4溶液中氢离子浓度(mol·dm -3)为 ( B ) (A) 0.1 (B) 2.7 ? 10-2 (C) 2.4 ? 10-2 (D) 7.5 ? 10-3 10. 下列物质中熔点最高的是( C ) (A)SnCl 2 (B) AlCl 3 (C) SiC (D)KCl 二、填空题(本大题共30个空格,每空1分,共30分, 填错或未填均无分) 1. 在298.15K 和100kPa 下,H 2O(l)→H 2O(s)过程中△H θ < 0,△S θ < 0 △G θ > 0(填 > 、< 或 =) 2. 将Ni + 2Ag + = 2Ag + Ni 2+ 氧化还原反应设计为一个原电池。则原电池符号为 (-)N i ︱Ni 2+(c 1)‖Ag +(c 2)︱Ag (+) 。 ()()为则原电池的电动势,已知Θ+Θ+Θ=-=E V Ag A V Ni N ,80.0/g 25.0/i 2?? 1.05V ,为Θ ?m r G -202.618kJ ·mol -1 ,该氧化还原反应的平 衡常数为 3.16×1035 。(F= 96485 C mol -1)
中国农业大学《普通化学》试卷
中国农业大学《普通化学》试卷 生物学院、生命科学实验班用 班级_____________ 学号_____________ 姓名_____________ 成绩___________ 一、选择题 1、证实电子具有波动性的实验依据就是: A、电子衍射实验; B、光电效应; C、α粒子散射实验; D、氢原子光谱实验。 2、下列物质的性质,可以用轨道杂化理论来解释的就是: A、NaF的熔点(993℃)比NaCl的熔点(801℃)高; B、O2分子中有单电子,具有顺磁性; C、H2O分子中H-O键夹角为104o45ˊ,呈“V”字形结构; D、邻位与对位硝基苯酚在水中的溶解度之比为0、39:1,而在苯中溶解度之比为1、93:1。 3、化学科学与生命科学交叉的一个活跃领域就是: A、生物无机化学; B、环境化学; C、核化学与放射化学; D、食品化学。 4、指示剂甲基橙就是弱一元碱, p K b为10、6,其酸型体呈红色,碱型体呈黄色。向纯水中滴加甲基橙后,水溶液呈: A、红色; B、黄色; C、橙色; D、无色。 5、欲测定某蛋白质的摩尔质量,可选用的实验测定方法就是: A、测定一定浓度的该蛋白质水溶液的pH值; B、测定一定浓度的该蛋白质水溶液的渗透压; C、测定它的等电点; D、测定它在水中的溶解度。 6、在元素周期表中,从ⅣB族开始,同一副族第三过渡系列元素的第一电离能比第二过渡系列元素的第一电离能大,原因就是: A、镧系收缩; B、钻穿效应; C、保利不相容原理; D、测不准原理。 7、下列说法正确的就是: A、离子键有方向性与饱与性; B、共价键有方向性与饱与性; C、色散力有方向性与饱与性; D、诱导力与分子变形性无关。 8、已知CuCl、CuBr、CuI的溶度积顺序减小。下列电极的标准电极电势最高的为: A、Cu2+/Cu+ ; B、Cu2+/CuCl; C、Cu2+/CuBr; D、Cu2+/CuI。 9、水溶液中能大量共存的一对物质为: A、Cr2O72-与Cr(OH)4- ; B、MnO4-与Mn2+ ; C、Fe3+与Sn2+ ; D、Ag+与Cr2O72-。 10,K sp (AgCl) = 1、8?10-10, K f {Ag(NH3)2+} = 1、1?107, K b (NH3) = 1、8?10-5。反应Ag(NH3)2+ + Cl- + 2H+ = AgCl + 2NH4+ 的标准平衡常数等于: A, 1、6?1021; B, 6、1?10-22; C, 9、1?1011; D, 1、6?10-16。
中山大学《细胞生物学》中山大学生物化学考试试题(B卷)
中山大学生物化学考试试题(B卷) 2003-2004年度第一学期 主考老师:邓庆丽苏菁 一、填空题:(每题一分,共15分) 1.在酶的广义酸碱催化机制中,特别重要的一个氨基酸残基是__his_____,因为其侧链PK值接近生物体内的PH条件。 2.紫外分光光度法测定蛋白质的原理在于__trp__ ,Tyr,Phe这三个氨基酸残基侧链基团在280nm处有吸光性。 3.糖类除了作为能源和生物大分子碳骨架的供体之外,它还与生物大分子间的__信号____识别有关。 4.The most two common secondary structures of proteins are α螺旋and β折叠。5.Monosaccharides containing an aldehyde group are called 醛糖aldoses 。6.Both Western blotting and ELISA are used to detect proteins with 抗体antibody 。 7. NMR spectroscopy and X-Ray 衍射are both used to reveal the three dimensional structure of proteins。 8.Anomers produces an equilibrium mixture of α - and β -forms in both furanose and pyranose ring structures。 9.神经节苷脂是一类含有唾液酸的鞘糖脂。 10.DNA变性后,紫外吸收能力增强,沉降速度升高,粘度降低。11.磷脂酶A的水解产物是脂肪酸和溶血磷脂。 12.开链己糖有16 种异构体。 13.胶原蛋白的氨基酸序列是很有特征的。常见的三个氨基酸重复单位是gly-x-y 。
普通化学试卷A卷
电子科技大学2012-2013学年第2学期期末考试A 卷 课程名称:_普通化学__ 考试形式:闭卷考试日期:2013年5 月日考试时长:_120_分钟课程成绩构成:平时30 %,期中%,实验%,期末70 % 本试卷试题由__三__部分构成,共_6__页。 一、选择题(共20分,共20题,每题1 分) 1、理想气体是指:( ) A、分子间距离很大,分子有体积; B、分子间引力可忽略,分子体积可不计; C、分子无体积,但分子间有引力; D、分子既有体积,也有分子间作用力。 2、在总压力为100KPa的混合气中,具有相同质量的H2、He、N2、CO2,其分压最小的是()。 A、H2 B、He C、N2 D、CO2 3、在工业上常用减压蒸馏,以增大蒸馏速度并避免物质分解。减压蒸馏所依据的原理是()。 A、液相的沸点降低B、液相的蒸汽压增大 C、液相的温度升高D、气相的温度降低 4、已知乙醇和水的正常沸点分别为78℃和100℃,下列说法错误的是( )。 A、相同温度时乙醇的蒸气压大于水的蒸汽压 B、乙醇分子间作用力小于水分子间作用力 C、乙醇受外压小于水所受外压 D、78℃时乙醇的蒸汽压等于101.325KPa 5、将0.45g某非电解质溶于30.0g水中,使溶液凝固点降为—0.150℃。已知水的K f为 1.86℃·kg·mol -1,则该电解质相对分子质量为() A、100 B、83.2 C、204 D、186 6、关于稀溶液依数性的下列叙述中,错误的是( )。 A、稀溶液的依数性是指溶液的蒸气压下降、沸点升高、凝固点下降和渗透压 B、稀溶液的依数性与溶质的本性有关 C、稀溶液的依数性与溶液中溶质的微粒有关 D、稀溶液定律只适用于难挥发非电解质稀溶液 7、已知下3个反应的标准焓变:
中山大学生化资料中山大学生命科学院生物化学试题答案与评分标准.doc
生物化学I (2006年秋季学期,A卷) 1.简答题(共25小题,超过60分以60分计入总分) 1 .哪些标准氨基酸含两个手性碳原子?写出它们的Fisher投影式。 2.为什么SDS变性电泳可以估算蛋白质的分子量? 3.Mass spectroscopy在生物大分子研究中有什么应用? 4.-Keratin、Collagen、Silk fibroin的二级结构和氨基酸组成有何特点? 5.根据二级结构的组成和排列可将蛋白质结构分为哪些类型? 6.蛋白质in条件下的折叠有哪些辅助因了? 7.蛋白质在与其他分子的相互作用中发挥作用,这种相互作用有何特点? 8.哪些因素可以导致Hemoglobin与O2的亲和力增加? 9.图示抗体的一般结构(包括结构域及可能的二硫键)。 10.构成肌肉粗丝和细丝的蛋白分子有哪些,各有什么功能? 11.写出蛋白质氨基酸测序的基本步骤。 12.什么是酶催化的过渡态理论?列出你所知道的支持证据? 13.酶的可逆抑制剂有几类?它们的抑制动力学各有何特点? 14.酶在体内的活性是如何受到调控的? 15.淀粉与纤维素的结构有何区别? 16.细胞膜表面的Glycoprotein和Glycolipid有哪些生物学功能? 17.细胞内的DNA可能会出现哪些异常结构,他们有什么生物学意义? 18 .膜脂的分类及其结构特点 19.生物膜的功能有哪些? 20.膜蛋白以哪些方式参与生物膜的构成? 21.图示 secondary active transport, uniport, symport, anti port. 22.Acetylcholine receptor通道是如何控制开关的? 23.K+离子通道是如何对通过的离子进行选择的? 24.膜电位是怎样控制Na*通道开关的(可图示并说明)? 25.Ca新泵和NaF泵的异同点。 IT. You have a crude lysate sample containing a mixture of six proteins (1, 2, 3, 4, 5, and P -galactosidase). Some characteristics of these proteins are shown in the table below. Give an available procedure of purifying B -galactosidase.
2010年中山大学药学院考研的一些经验和看法
近来不少07级的童鞋向我问起中山大学药学院的考研情况,所以就决定写个帖子介绍下情况,造福一下后面的学弟学妹们。言语比较啰嗦,叙述的东西可能也是比较主观,其中应该有不少不对不确切的地方,希望各位同学和前辈能指正。 今年共有5名药大06级学生进入中大药学院复试,最终基本都录上了理想的导师和拿到了奖助名额,其中两位男生是药理,两位女生药剂,一位女生药化结构生物学实验室。06级是药大人比较大规模地登陆中大药学院的一年,我们也希望以后也能有更多的学弟学妹能报考那。 我,06级,来自药大以“3+3年制”直研而闻名的专业。从大二结束的暑假起起开始酝酿考外事宜,大三一年通过电邮联系了不少复旦、浙大药学院、中大的在读硕士学长学姐打探情况,后来大三下确定想报考的方向是临床药理后,基于专业方向需要强势医科和附属医院的依托以及导师招生情况、报考风险等指标确定下报考中大药学院,并最终考上了所预想的导师门下。 中大药学院大楼位于中山大学东校区,广州大学城里。这里是珠江中的一个岛,10个大学环岛而建,地铁穿岛而过,环境不错,宿舍和校区都很新,体育馆和图书馆都很大,生活设施也很齐全,中大约有2万学生在东校区。药学院的本科生生源质量比较好,据说一半是高考时被中山医学院临床医学刷下的高分考生。比较喜欢药大的学生,招生时将药大来的和本院考生一视同仁,院里的老师里面也有很多在药大求学过。 1 中大药学院的优缺点: 缺点:2003年才成立的药学院,历史和传统比中国五大药学院差很多,江湖地位不高,还处于迈向中国一流药学院的成长路上,院内学科发展也不均衡。 优点:引自过来人24号传奇人物苦瓜木鱼蛤蟆学长“软件硬件条件一流;数据库很多,仪器设备很新很贵,科研经费充足,用不完就乱买东西;实验条件很好,大小实验室都有空调;硕士不分公费自费每月都有500左右的生活补助,各种国际交流很多。” 另外觉得,因为中山医科较为强势的传统,所以中大比较重视这个年轻的药学院的发展。广东省投巨资打造的华南新药创制中心(项目负责人是中大副校长医学院药理学教授颜光美)就将与药学院“构筑合作大平台,在经费支持、实验设备共享、科学研究队伍共建、国家重点实验室建设以及知识产权等领域全面联姻。“ 2 导师和学科 下面将介绍中大药学院比较强势的学科和比较推荐报考的导师。 药理:药理学科是药学院最有历史和传统的学科,导师基本在药学院成立前来自于中山医学院国家重点学科药理学,也是现在中大药学院整体发展最好的学科。 药理主要分为两个PI(课题组)——中大临床药理所和药理毒理PI 黄民教授:黄民PI负责人,院长,中大临床药理所所长,主要作临床药理,实验室的主要研究方向是遗传药理与药物基因组学,药物临床前药物代谢与动力学研究,Ⅰ期临床(人体耐受性试验、人体药代动力学试验)研究等。 课题组在东校区药学院和北校区医学院分别有实验室,其中医学院实验室部分的学生经
大学普通化学期末卷子
一、选择题(以下每题均为单选题,多选不得分。每题2分,共30分) 1.根据定义,下列物质中标准摩尔生成吉布斯函数△r G mθ为零的物质是:( D ) (A) 压力为100kPa、温度298.15K下的金刚石;(B)温度为298.15K、200kPa的氢气;(C) 温度为298.15K、压力为100kPa的水蒸气;(D)温度为298.15K、压力为100kPa的氧气2.升高温度可增加反应速率,最主要的原因是因为: ( B ) (A) 增加了反应分子总数; (B) 增大了活化分子的百分数; (C) 降低了反应的活化能; (D) 促进平衡正向移动 3.等温等压条件下任何温度都可自发进行的化学反应,其条件是: ( A ) (A) ΔH< 0、ΔS >0; (B) ΔS< 0、ΔH>0; (C) △r G mθ< 0; (D) ΔS< 0、ΔH< 0 4.下面一组量子数中, 准确描述原子轨道的是: ( A ) (A) (3, 2, -2); (B) (3, 3, 1); (C) (3, 2, -3); (D) (3, 2, 0, 1); (E) (3, 2, 1, -1/2); (F) (3, 2, -1, 0); (G) (3, 3, 2, +1/2) 5.上述量子数中, 准确描述电子运动状态的是: ( E ) 6.根据“酸碱质子理论”,属于HPO42-的共轭酸是: ( B ) (A) PO43-; (B) H2PO4-; (C) H3PO4; (D) H4PO4+ 7.已知Kθsp(Ag2CrO4)=1.2?10-12,0.1mol·dm-3CrO42-溶液中滴加AgNO3,开始产生沉淀时Ag+的浓度为 ( D ) (A) 1.2?10-11mol·dm-3; (B) 6.5?10-5mol·dm-3; (C) 0.1mol·dm-3; (D) 3.46?10-6mol·dm-3 8.室温下,0.20mol.dm-3HCOOH溶液电离度为3.2%,HCOOH的电离常数为: ( A ) (A) 2.0×10-4; (B) 1.3×10-3; (C) 6.4×10-3; (D) 6.4×10-4 9.可以用作缓冲溶液的系统是: ( C ) (A) 0.10 mol·dm-3NaAc+0.10 mol·dm-3HCl溶液;(B) 0.10 mol·dm-3HAc+0.20 mol·dm-3NaOH 溶液;(C) 0.20 mol·dm-3HAc+0.10 mol·dm-3NaOH溶液; (D) 0.20 mol·dm-3醋酸+0.10 mol·dm-3HCl溶液 10.原电池 (-) Pt?SO32-,SO42-??H+,Mn2+,MnO4-?Pt (+) 的电池反应: ( A ) (A) 2 MnO4- + 5 SO32- + 6H+ =2 Mn2+ + 5SO42- +3H2O; (B) 2 MnO4- + 8H+ + 5e=2 Mn2+ + 4H2O; (C) SO32- + H2O = SO42- +2H+ + 2e; (D) MnO4- + SO32- + 6H+ + 3e = Mn2+ + SO42- +3H2O 11.22T原子核外电子分布式正确的是: ( B ) (A) 1s22s22p63s23p64s24p2 (B) 1s22s22p63s23p63d24s2 (c) 1s22s22p63s23p64s23d2 (C) 1s22s22p63s23p63d4 12.已知反应 A(g) = 2B(g) + C(g),T、V一定,开始时P(A) = 20kPa,达到平衡时总压为40kPa,该反应的转化率为 ( B ) (A) 30%; (B) 50%; (C) 10%; (D) 100%; 13.根据酸碱质子理论,下列各组物质中都可以作为酸的有 ( B ) (A) HCl, S2-, CO32-; (B) NH4+, HSO4-, H2O; (C) HS-, HPO4-, CO32-; (D) NH3, H2S, H2O 14.在21.8℃时,反应NH4HS(s) = NH3(g) + H2S(g)的标准平衡常Kθ = 0.070,4molNH4HS 分解达到平衡是混合气体的总压力是: ( C ) (A) 7.0 kPa; (B) 26 kPa; (C) 53 kPa; (D) 0.26 kPa 15.一个化学反应达到平衡时,下列说法正确的是: ( A ) (A) 各物质的浓度或分压不随时间变化;(B) △r G mθ = 0; (C) 正、逆反应的速率常数相等; (D) △r H mθ = 0 二、填空题 (25分,每空1分)
