四种晶体比较(1)
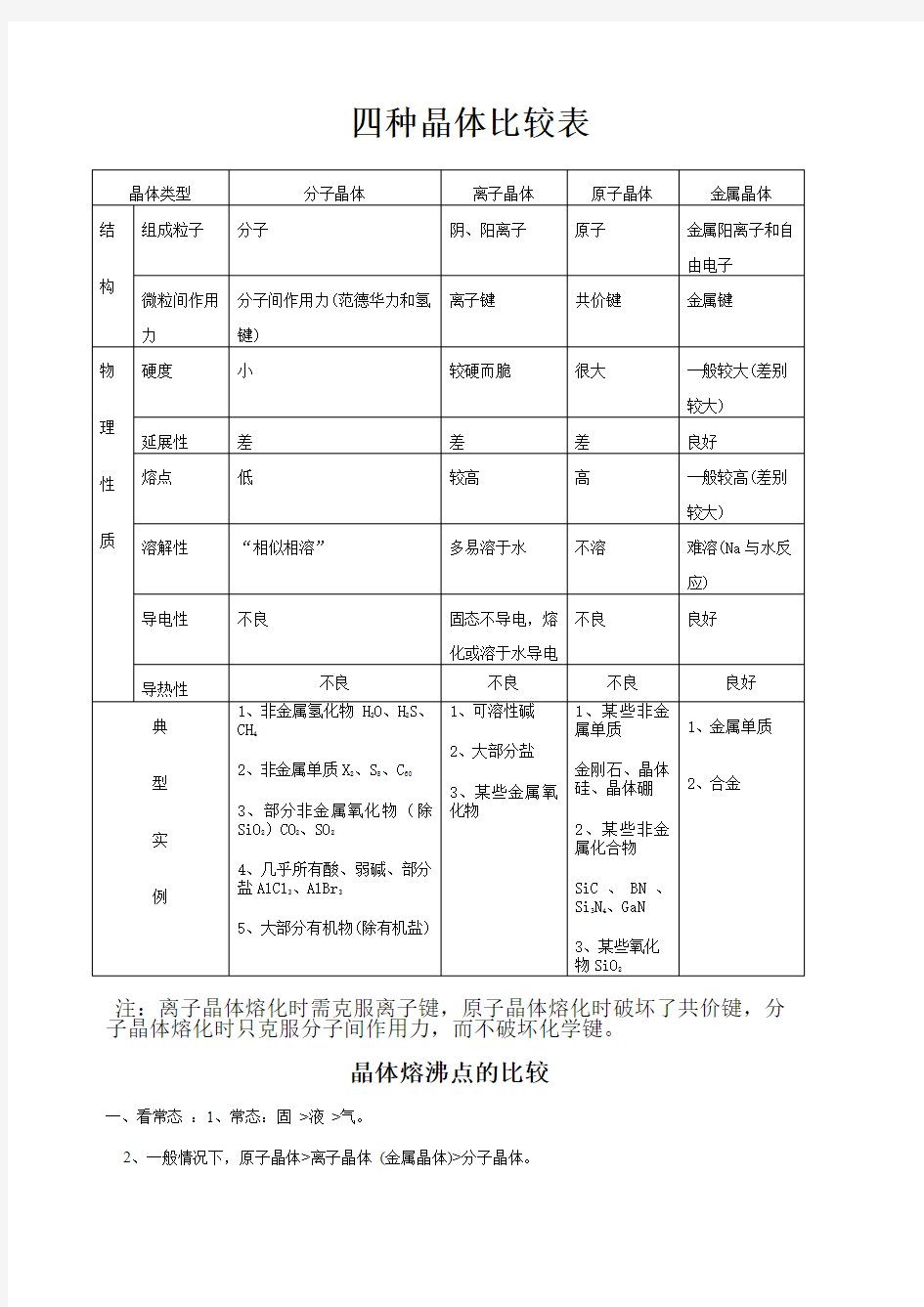

四种晶体比较表
注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。
晶体熔沸点的比较
一、看常态:1、常态:固>液>气。
2、一般情况下,原子晶体>离子晶体(金属晶体)>分子晶体。
3、原子晶体:共价键(取决于原子半径)。
4、离子晶体:离子键(取决于离子半径和离子电荷)
5、金属晶体:金属键(取决于金属原子半径和价电子数)
6、分子晶体:①结构相似,分子量越大,熔沸点越高。
②分子量相等,正>异>新。③氢键反常
二、看类型
三、分类比较
18.请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。
(2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于晶体。
(3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是(填化学式)。
19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布
式。
(2)根据等电子原理,写出CO分子结构式。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子中
碳原子轨道的杂化类型为。
②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目
为。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为。
(完整word版)四种晶体类型的比较
物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
B 、离子晶体:熔、沸点的高低,取决于离子键的强弱。一般来说,离子半径越小,离子所带电荷越多,离子键就越强,熔、沸点就越高,反之越低。 例如:MgO>CaO ,NaF>NaCl>NaBr>NaI 。 KF >KCl >KBr >KI ,CaO >KCl 。 C 、金属晶体:金属晶体中金属阳离子所带电荷越多,半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。如:Na <Mg <Al ,Li>Na>K 。 合金的熔沸点一般说比它各组份纯金属的熔沸点低。如铝硅合金<纯铝(或纯硅)。 D 、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。分子晶体分子间作用力越大物质的熔沸点越高,反之越低。(具有氢键的分子晶体,熔沸点反常地高) 如:H 2O >H 2Te >H 2Se >H 2S ,C 2H 5OH >CH 3—O —CH 3。 (1)组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,物质的熔沸点越高。如:CH 4<SiH 4<GeH 4<SnH 4。 (2)组成和结构不相似的物质(相对分子质量相近),分子极性越大,其熔沸点就越高。如熔沸点 CO >N 2,CH 3OH >CH 3—CH 3。 (3)在高级脂肪酸形成的油脂中,不饱和程度越大,熔沸点越低。 如:C 17H 35COOH >C 17H 33COOH ;硬脂酸 > 油酸 (4)烃、卤代烃、醇、醛、羧酸等有机物一般随着分子里碳原子数增加,熔沸 点升高,如C 2H 6>CH 4, C 2H 5Cl >CH 3Cl ,CH 3COOH >HCOOH 。 (5)同分异构体:链烃及其衍生物的同分异构体随着支链增多,熔沸点降低。如: CH 3(CH 2)3CH 3 (正)>CH 3CH 2CH(CH 3)2(异)>(CH 3)4C(新)。 芳香烃的异构体有两个取代基时,熔点按对、邻、间位降低沸点按邻、间、对位降低) 针对性训练 一、选择题 1.下列性质中,可以证明某化合物内一定存在离子键的是( ) (A )溶于水 (B )有较高的熔点 (C )水溶液能导电 (D )熔融状态能导电 2.下列物质中,含有极性键的离子化合是( ) (A )CaCl 2 (B )Na 2O 2 (C )NaOH (D )K 2S 3.Cs 是IA 族元素,F 是VIIA 族元素,估计Cs 和F 形成的化合物可能是( ) (A )离子化合物 (B )化学式为CsF 2 (C )室温为固体 (D )室温为气体 4.某物质的晶体中含A 、B 、C 三种元素,其排列方式如图所示(其中前后两面心上的B 原子未能画出),晶体中A 、B 、C 的中原子个数之比依次为( ) (A )1:3:1 (B )2:3:1 (C )2:2:1 (D )1:3:3 6.在NaCl 晶体中与每个Na +距离等同且最近的几个Cl -所围成的空间几何构型为( ) (A )正四面体 (B )正六面体 (C )正八面体 (D )正十二面体 7.如图是氯化铯晶体的晶胞(晶体中最小的重复单元),已知晶体中2个最近的Cs +离子核间距为a cm ,氯化铯的式量为M ,NA 为阿伏加德罗常数,则氯化铯晶体的密度为( ) (A )3 8a N m A ?g·cm -3 (B )A N Ma 83 g·cm -3 (C )3 a N M A ?g·cm -3 (D )A N Ma 3 g·cm -3
四种晶体类型的比较
四种晶体类型的比较 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价
键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C —C
高中化学四种晶体类型的比较
四种晶体类型的比较
物质熔沸点高低的比较方法 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr (固)>Br2>HBr(气)。 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,原子半径越小,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
四种晶体类型的比较
四种晶体类型的比较 GE GROUP system office room 【GEIHUA16H-GEIHUA GEIHUA8Q8-
四种晶体类型的比较
物质熔沸点高低的比较方法 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体> >HBr(气)。 液体>气体。例如:NaBr(固)>Br 2 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
例如:MgO>CaO ,NaF>NaCl>NaBr>NaI 。 KF >KCl >KBr >KI ,CaO >KCl 。 C 、金属晶体:金属晶体中金属阳离子所带电荷越多,半径越小,金属阳离子与自由电子静电作用越强,金属键越强,熔沸点越高,反之越低。如:Na <Mg <Al ,Li>Na>K 。 合金的熔沸点一般说比它各组份纯金属的熔沸点低。如铝硅合金<纯铝(或纯硅)。 D 、分子晶体:熔、沸点的高低,取决于分子间作用力的大小。分子晶体分子间作用力越大物质的熔沸点越高,反之越低。(具有氢键的分子晶体,熔沸点反常地高) 如:H 2O >H 2Te >H 2Se >H 2S ,C 2H 5OH >CH 3—O —CH 3。 (1)组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,物质的熔沸点越高。如:CH 4<SiH 4<GeH 4<SnH 4。 (2)组成和结构不相似的物质(相对分子质量相近),分子极性越大,其熔沸点就越高。如熔沸点 CO >N 2,CH 3OH >CH 3—CH 3。 (3)在高级脂肪酸形成的油脂中,不饱和程度越大,熔沸点越低。 如:C 17H 35COOH >C 17H 33COOH ;硬脂酸 > 油酸
四种晶体比较
四种晶体比较 内部编号:(YUUT-TBBY-MMUT-URRUY-UOOY-DBUYI-0128)
四种晶体比较表 注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。
晶体熔沸点的比较 一、看常态:1、常态:固 >液 >气。 2、一般情况下,原子晶体>离子晶体 (金属晶体)>分子晶体。 3、原子晶体:共价键 (取决于原子半径)。 4、离子晶体:离子键 (取决于离子半径和离子电荷) 5、金属晶体:金属键 (取决于金属原子半径和价电子数) 6、分子晶体:①结构相似,分子量越大,熔沸点越高。 ②分子量相等,正>异>新。③氢键反常 二、看类型 三、分类比较 18.请完成下列各题: (1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。 (2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式 为。在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于晶体。 (3)在极性分子NCl 3 中,N原子的化合物为―3,Cl原子的化合价为+ 1,请推测NCl 3 水解的主要产物是(填化学式)。 19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、 CO 2、H 2 等)与H 2 混合,催化合成甲醇是生物质能利用的方法之一。 (1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式。
(2)根据等电子原理,写出CO分子结构式。 的碱性溶液反应生(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH) 2 O沉淀。 成Cu 2 ①甲醇的沸点比甲醛的高,其主要原因 是;甲醛分子中碳原子轨道的杂化类型 为。 ②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目为。 ③在1个Cu O晶胞中(结构如图所示),所包含的Cu原子数目 2 为。
四种晶体性质比较
四种晶体性质比较 1.晶体 ⑴晶体与非晶体 ⑵得到晶体的途径 ①熔融态物质凝固。 ②气态物质冷却不经液态直接___________________ 。 ③溶质从溶液中析出。 ⑶晶胞 ①概念 描述晶体结构的基本单元。 ②晶体中晶胞的排列一一无隙并置 a. _______________________________ 无隙:相邻晶胞之间没有。 b?并置:所有晶胞________ 卡列、取向相同。 ⑷晶格能 ①定义:气态离子形成1摩离子晶体释放的能量,通常取正值,单位: __________________ 。 ②影响因素 a.离子所带电荷数:离子所带电荷数越多,晶格能越大。一 b. ____________________________ 离子的半径:离子的半径晶格能越大。 ③与离子晶体性质的关系
晶格能越大,形成的离子晶体越稳定,且熔点越高,硬度_________________ 。
2.四种晶体类型的比较 3?晶体熔沸点的比较 ⑴不同类型晶体熔、沸点的比较 ①不同类型晶体的熔、沸点高低的一般规律:______________________________ >离子晶体〉_____________________________________ 0 ②金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。 ⑵同种晶体类型熔、沸点的比较 ①原子晶体:
原子半径越小」—>1键长越短②离子晶体: a?—般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强, 其离子晶体的熔、沸点就越高,如熔点:MgO ____ MgCI 2 ______ N aCl _____ CsCI。 b.衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越大。 ③分子晶体: a.分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常地高。女口H20> H2Te> H2Se> H2S。 b.组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,女口Sn H4> GeH4 > SiH4> CH4。 c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点 ___________ 如 C0>N2,CH3OH>CH3CH3。 d.同分异构体,支链越多,熔、沸点越低。 ④金属晶体: 金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,如熔、沸点:Na v Mg v Al。 2 .在下列物质中:NaCl、NaOH、Na2S、H2O2、Na2S2、(NH4)2S、CO2、CCI4、 C2H2、SiO2、SiC、晶体硅、金刚石。 ⑴其中只含有离子键的离子晶体是___________ ; (2)其中既含有离子键又含有极性共价键的离子晶体是_____________ ; (3)其中既含有离子键,又含有极性共价键和配位键的离子晶体是______________ ; ⑷其中既含有离子键又含有非极性共价键的离子晶体是______________ ; (5)其中含有极性共价键的非极性分子是____________ ; (6)其中含有极性共价键和非极性共价键的非极性分子是_____________ ; (7)其中含有极性共价键和非极性共价键的极性分子是 (8)其中含有极性共价键的原子晶体是 _______ 。
四种晶体比较表
四种晶体比较表 注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。 晶体熔沸点的比较 一、看常态:1、常态:固>液>气。
2、一般情况下,原子晶体>离子晶体(金属晶体)>分子晶体。 3、原子晶体:共价键(取决于原子半径)。 4、离子晶体:离子键(取决于离子半径和离子电荷) 5、金属晶体:金属键(取决于金属原子半径和价电子数) 6、分子晶体:①结构相似,分子量越大,熔沸点越高。 ②分子量相等,正>异>新。③氢键反常 二、看类型 三、分类比较 18.请完成下列各题: (1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。 (2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于晶体。 (3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是(填化学式)。 19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。 (1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式。 (2)根据等电子原理,写出CO分子结构式。 (3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。 ①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子 中碳原子轨道的杂化类型为。 ②甲醛分子的空间构型是;1mol甲醛分子中σ键的数 目为。 ③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为。
四种晶体类型的比较
创作编号: GB8878185555334563BT9125XW 创作者:凤呜大王* 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体>液体>气体。例如:NaBr(固)>Br2>HBr(气)。
2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
四种晶体比较
四种晶体比较 Document serial number【KKGB-LBS98YT-BS8CB-BSUT-BST108】
四种晶体比较表 注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。 晶体熔沸点的比较 一、看常态:1、常态:固 >液 >气。
2、一般情况下,原子晶体>离子晶体 (金属晶体)>分子晶体。 3、原子晶体:共价键 (取决于原子半径)。 4、离子晶体:离子键 (取决于离子半径和离子电荷) 5、金属晶体:金属键 (取决于金属原子半径和价电子数) 6、分子晶体:①结构相似,分子量越大,熔沸点越高。 ②分子量相等,正>异>新。③氢键反常 二、看类型 三、分类比较 18.请完成下列各题: (1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。 (2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。 在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于 晶体。 (3)在极性分子NCl 3 中,N原子的化合物为―3,Cl原子的化合价为+1,请 推测NCl 3 水解的主要产物是(填化学式)。 19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO 2、H 2 等)与H 2 混合,催化合成甲醇是生物质能利用的方法之一。 (1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式。 (2)根据等电子原理,写出CO分子结构式。 (3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH) 2的碱性溶液反应生成Cu 2 O 沉淀。 ①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子中碳原子轨道的杂化类型为。 ②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目为。
四种晶体比较
四种晶体比较 This model paper was revised by the Standardization Office on December 10, 2020
四种晶体比较表 注:离子晶体熔化时需克服离子键,原子晶体熔化时破坏了共价键,分子晶体熔化时只克服分子间作用力,而不破坏化学键。 晶体熔沸点的比较 一、看常态:1、常态:固 >液 >气。
2、一般情况下,原子晶体>离子晶体 (金属晶体)>分子晶体。 3、原子晶体:共价键 (取决于原子半径)。 4、离子晶体:离子键 (取决于离子半径和离子电荷) 5、金属晶体:金属键 (取决于金属原子半径和价电子数) 6、分子晶体:①结构相似,分子量越大,熔沸点越高。 ②分子量相等,正>异>新。③氢键反常 二、看类型 三、分类比较 18.请完成下列各题: (1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有种。 (2)第ⅢA、ⅤA原元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为。 在GaN晶体中,每个Ga原子与个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为。在四大晶体类型中,GaN属于 晶体。 (3)在极性分子NCl 3 中,N原子的化合物为―3,Cl原子的化合价为+1,请 推测NCl 3 水解的主要产物是(填化学式)。 19.生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO 2、H 2 等)与H 2 混合,催化合成甲醇是生物质能利用的方法之一。 (1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式。 (2)根据等电子原理,写出CO分子结构式。 (3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH) 2的碱性溶液反应生成Cu 2 O 沉淀。 ①甲醇的沸点比甲醛的高,其主要原因是;甲醛分子中碳原子轨道的杂化类型为。 ②甲醛分子的空间构型是;1mol甲醛分子中σ键的数目为。
四种晶体类型的比较完整版
四种晶体类型的比较 HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】
四种晶体类型的比较 物质熔沸点高低的比较方法 物质的熔沸点的高低与构成该物质的晶体类型及晶体内部粒子间的作用力有关,其规律如下: 1、在相同条件下,不同状态的物质的熔、沸点的高低是不同的,一般有:固体> >HBr(气)。 液体>气体。例如:NaBr(固)>Br 2 2、不同类型晶体的比较规律 一般来说,不同类型晶体的熔沸点的高低顺序为:原子晶体>离子晶体>分子晶体,而金属晶体的熔沸点有高有低。这是由于不同类型晶体的微粒间作用不同,其熔、沸点也不相同。原子晶体间靠共价键结合,一般熔、沸点最高;离子晶体阴、阳离子间靠离子键结合,一般熔、沸点较高;分子晶体分子间靠范德华力结合,一
般熔、沸点较低;金属晶体中金属键的键能有大有小,因而金属晶体熔、沸点有高(如W)有低(如Hg)。例如:金刚石>食盐>干冰 3、同种类型晶体的比较规律 A、原子晶体:熔、沸点的高低,取决于共价键的键长和键能,键长越短,键能越大共价键越稳定,物质熔沸点越高,反之越低。如:晶体硅、金刚石和碳化硅三种晶体中,因键长C—C
晶体类型的判断与比较怎样比较熔点的高低
晶体类型的判断与比较,晶体结构的计算,怎样比较熔点的高低, 8晶体类型的判断与比较 1、判断晶体类型的方法 (1)依据物质的分类判断 金属氧化物(如K2O、Na2O2等),强碱(如NaCl、KOH等)和绝大多数的盐类是离子晶体。大多数非金属单质(除金刚石、石墨、晶体硅、晶体硼外)、气态氢化物、非金属氧化物(除SiO2外)、酸、绝大多数有机物(除有机盐外)是分子晶体。常见的原子晶体单质有金刚石、石墨、晶体硅、晶体硼等;常见的原子晶体化合物有碳化硅、二氧化硅等。金属单质(除汞外)与合金都是金属晶体。 (2)依据物质的性质判断 离子晶体的熔点较高,常在数百至1000余度;原子晶体熔点高,常在100 0度至几千度;分子晶体熔点低,常在数百度以下至很低温度;金属晶体多数熔点高,但也有相当低的。 离子晶体水溶液及熔化时能导电,晶体不导电;原子晶体一般为非导体,但石墨等导电;分子晶体为非导体,而分子晶体中的电解质(主要是酸和非金属氢化物)溶于水,使分子内的化学键断裂形成自由移动的离子也能导电,但熔化不导电,金属晶体是良导体。 2、晶体中的几个不一定 (1)离子晶体除含离子键外不一定不含其他化学键。如氨盐中除含离子键,还含极性键和配位键;Na2O2中除含离子键还含非极性键。
(2)离子晶体不一定肯定含金属阳离子,如NH4Cl中含的阳离子是NH4+(凡是氨盐、肯定同时含离子键、极性键和配位键)。 (3)离子晶体的熔点不一定肯定低于原子晶体,如MgO的熔点高于SiO2。(4)含有阳离子的晶体不一定是离子晶体,如金属晶体中就含有金属阳离子。 (5)金属和非金属形成的晶体不一定都是离子晶体,如AlCl3就是含共价键的分子晶体 (6)具有金属光泽且能导电的单质不一定就是金属,如石墨具有金属光泽且能导电,却是非金属。 3、四类晶体的比较:
四种晶体性质比较
四种晶体性质比较1.晶体 (1)晶体与非晶体 (2)得到晶体的途径 ①熔融态物质凝固。 ②气态物质冷却不经液态直接_______________。 ③溶质从溶液中析出。 (3)晶胞 ①概念 描述晶体结构的基本单元。
②晶体中晶胞的排列——无隙并置 a.无隙:相邻晶胞之间没有____________。 b.并置:所有晶胞______排列、取向相同。 (4)晶格能 ①定义:气态离子形成1摩离子晶体释放的能量,通常取正值,单位:_________________。 ②影响因素 a.离子所带电荷数:离子所带电荷数越多,晶格能越大。 b.离子的半径:离子的半径________,晶格能越大。 ③与离子晶体性质的关系 晶格能越大,形成的离子晶体越稳定,且熔点越高,硬度___________。2.四种晶体类型的比较
3.晶体熔沸点的比较 (1)不同类型晶体熔、沸点的比较 ①不同类型晶体的熔、沸点高低的一般规律:________________>离子晶体>____________。 ②金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。 (2)同种晶体类型熔、沸点的比较
①原子晶体: 原子半径越小―→键长越短―→键能越大―→ ②离子晶体: a .一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,其离子晶体的熔、沸点就越高,如熔点:MgO____MgCl 2______NaCl______CsCl 。 b .衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越大。 ③分子晶体: a .分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸点反常地高。如H 2O >H 2Te >H 2Se >H 2S 。 b .组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如SnH 4>GeH 4>SiH 4>CH 4。 c .组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其熔、沸点____________,如CO >N 2,CH 3OH >CH 3CH 3。 d .同分异构体,支链越多,熔、沸点越低。 ④金属晶体: 金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,如熔、沸点:Na <Mg <Al 。 2.在下列物质中:NaCl 、NaOH 、Na 2S 、H 2O 2、Na 2S 2、(NH 4)2S 、CO 2、CCl 4、C 2H 2、SiO 2、SiC 、晶体硅、金刚石。 (1)其中只含有离子键的离子晶体是________;
四种晶体性质比较
四种晶体性质比较 This model paper was revised by the Standardization Office on December 10, 2020
四种晶体性质比较 1.晶体 (1)晶体与非晶体 (2)得到晶体的途径 ①熔融态物质凝固。 ②气态物质冷却不经液态直接_______________。 ③溶质从溶液中析出。 (3)晶胞 ①概念 描述晶体结构的基本单元。 ②晶体中晶胞的排列——无隙并置 a.无隙:相邻晶胞之间没有____________。 b.并置:所有晶胞______排列、取向相同。 (4)晶格能 ①定义:气态离子形成1摩离子晶体释放的能量,通常取正值,单位:_________________。 ②影响因素 a.离子所带电荷数:离子所带电荷数越多,晶格能越大。 b.离子的半径:离子的半径________,晶格能越大。 ③与离子晶体性质的关系
晶格能越大,形成的离子晶体越稳定,且熔点越高,硬度___________。2.四种晶体类型的比较 3.晶体熔沸点的比较 (1)不同类型晶体熔、沸点的比较 ①不同类型晶体的熔、沸点高低的一般规律:________________>离子晶体>____________。
②金属晶体的熔、沸点差别很大,如钨、铂等熔、沸点很高,汞、铯等熔、沸点很低。 (2)同种晶体类型熔、沸点的比较 ①原子晶体: 原子半径越小―→键长越短―→键能越大―→ ②离子晶体: a.一般地说,阴、阳离子的电荷数越多,离子半径越小,则离子间的作用力就越强,其离子晶体的熔、沸点就越高,如熔点: MgO____MgCl 2______ NaCl______CsCl。 b.衡量离子晶体稳定性的物理量是晶格能。晶格能越大,形成的离子晶体越稳定,熔点越高,硬度越大。 ③分子晶体: a.分子间作用力越大,物质的熔、沸点越高;具有氢键的分子晶体熔、沸 点反常地高。如H 2O>H 2 Te>H 2 Se>H 2 S。 b.组成和结构相似的分子晶体,相对分子质量越大,熔、沸点越高,如 SnH 4>GeH 4 >SiH 4 >CH 4 。 c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,其 熔、沸点____________,如CO>N 2,CH 3 OH>CH 3 CH 3 。 d.同分异构体,支链越多,熔、沸点越低。 ④金属晶体: 金属离子半径越小,离子电荷数越多,其金属键越强,金属熔、沸点就越高,如熔、沸点:Na<Mg<Al。 2.在下列物质中:NaCl、NaOH、Na 2S、H 2 O 2 、Na 2 S 2 、(NH 4 ) 2 S、CO 2 、CCl 4 、 C 2H 2 、SiO 2 、SiC、晶体硅、金刚石。 (1)其中只含有离子键的离子晶体是________; (2)其中既含有离子键又含有极性共价键的离子晶体是________; (3)其中既含有离子键,又含有极性共价键和配位键的离子晶体是________; (4)其中既含有离子键又含有非极性共价键的离子晶体是________;
晶体结构与性质知识总结(完善)
3-1、晶体的常识 一、晶体和非晶体 1、概述——自然界中绝大多数物质是固体,固体分为和两大类。 2、对比——
* 自范性——晶体能自发地呈现多面体外形的性质。本质上,晶体的自范性是晶体中粒子在微观空间里呈现周期性有序排列的宏观表象。 * 晶体不因颗粒大小而改变,许多固体粉末用肉眼看不到规则的晶体外形,但在显微镜下仍可看到。 * 晶体呈现自范性的条件之一是晶体生长的速率适当,熔融态物质凝固速率过
快常得到粉末或没有规则外形的块状物。 * 各向异性——晶体的许多物理性质如强度、热导性和光导性等存在各向异性即在各个方向上的性质是不同的 二、晶胞 1、定义——描述晶体结构的基本单元。 2、特征—— (1)习惯采用的晶胞都是体,同种晶体所有的晶胞大小形状及内部的原子种类、个数和几何排列完全相同。 (2)整个晶体可以看作是数量巨大的晶胞“无隙并置”而成。 <1> 所谓“无隙”是指相邻晶胞之间没有任何间隙; <2> 所谓“并置”是指所有晶胞都是平行排列的,取向相同。 3、确定晶胞所含粒子数和晶体的化学式——均摊法分析晶胞与粒子数值的关系 (1)处于内部的粒子,属于晶胞,有几个算几个均属于某一晶胞。 (2)处于面上的粒子,同时为个晶胞共有,每个粒子有属于晶胞。 (3)处于90度棱上的粒子,同时为个晶胞共有,每个粒子有属于晶胞。
(4)处于90度顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于60度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞;处于120度垂面顶点的粒子,同时为个晶胞共有,每个粒子有属于晶胞。 4、例举 三、分类 晶体根据组成粒子和粒子之间的作用分为分子晶体、原子晶体、金属晶体和离子晶体四种类型。 3-2、分子晶体和原子晶体 一、分子晶体 1、定义——只含分子的晶体。 2、组成粒子——。 3、存在作用——组成粒子间的作用为(),多原子分子内部原子间的作用为。 * 分子晶体中定含有分子间作用力,定含有共价键。 * 分子间作用力于化学键。 4、物理性质 (1)熔沸点与硬度——融化和变形只需要克服,所以熔沸点、
