过剩载流子及其基本理论

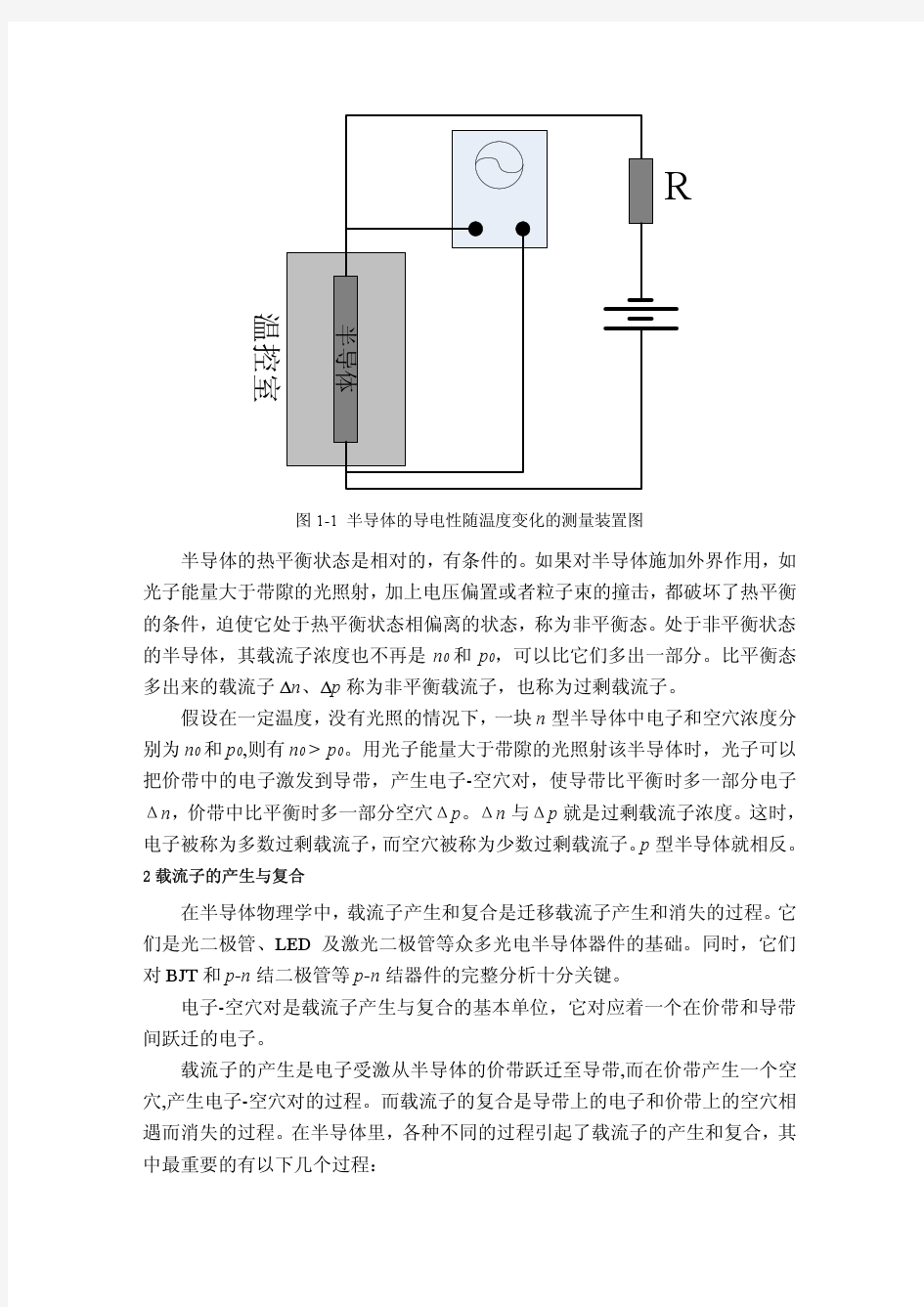
非平衡半导体中载流子的运动规律
第四章习题 1. 试计算本征Si 在室温时的电导率,设电子和空穴迁移率分别为1350cm 2/V·s 和 500cm 2/V·s 。当掺入百万分之一的As 后,设杂质全部电离,试计算其电导率比本征Si 的电导率增大了多少倍? 2. 电阻率为10Ω·m 的p 型Si 样品,试计算室温时多数载流子和少数载流子浓度。 3. 试从图 4.14求杂质浓度为1016cm -3、和1018 cm -3的Si ,当温度分别为-50℃ 和+150℃时的电子和空穴迁移率。 1) 电子的平均动能为(3/2)kT ,若有效质量为0.2m 0。求电子热运动的均方根速度。 2) 求迁移率为1000cm 2/V·s 的载流子在103V/cm 的电场下的漂移速度。 3) 比较两者的大小。 4. 说明电离杂质散射和声学波散射的基本特点,两者τ、μ的温度关系,起主要作用的温度范围,在μ-T 、σ-1/T 曲线中的表现。 5. 设r a ετ=,讨论r 为正和负时,高能量的载流子荷载电流作用的相对大小。 6. 假定在掺杂浓度不均匀(掺杂浓度为N(x))的N 型半导体中,在室温时杂质完全电离。求出热平衡状态时半导体内的电势、电场分布的表达式,并定性画出其平衡能带图、电势和电场分布图。设在x=0处电势为0(电势参考点),载流子浓度分别为为n 和p ,在x=x0处的电势为V ,求x=x0出的载流子浓度表达式。 7. 一维过剩载流子的扩散分布p L x e p x p -?=?0)()(,说明相应梯度的绝对值随x 减小,因而扩散电流随x 减小,并从物理上说明产生这种现象的原因。证明在x>0的范围内,单位时间内复合掉的载流子数量等于x=0处扩散流的大小。 8. 设室温下,Si 中过剩载流子寿命为1μs 。 1)若多子浓度为1015/cm 3,少子浓度为零,求室温下,电子-空穴对的产生速率。2)在无外场一维稳定扩散分布的讨论中,为何只考虑少子的扩散运动?多子又如何? 9. 画出p 型半导体在光照(小注入)前后的能带图,标出原来的费米能级和光照时的准费米能级。 10. 由于光的照射在半导体中产生了非平衡载流子12310n p cm -?=?=,分别计算施主掺杂浓度N D =1016cm -3的n 型硅和本征硅,这种情况下准费米能级的位置,并和原来的费米能级作比较。画出相应的能带图。 11. 设空穴浓度是线性分布,在3m μ内浓度差为1015cm -3,s V cm p ?=/4002 μ。试计算空穴扩散电流密度。 12. 从子系化学势的角度,讨论以下几种情形下是否有载流子的净复合或净产生。n, p>n i ; 2) n 载流子寿命 半导体中的非平衡载流子寿命是半导体的一个基本特性参数,它的长短将直接影响到依靠少数载流子来工作的半导体器件的性能,这种器件有双极型器件和p-n结光电子器件等。但是,对于在结构上包含有p-n结的单极型器件(例如MOSFET)也会受到载流子寿命的影响。 非平衡载流子寿命主要是指非平衡少数载流子的寿命。影响少子寿命的主要因素是半导体能带结构和非平衡载流子的复合机理;对于Si、Ge、GaP等间接禁带半导体,一般决定寿命的主要因素是半导体中的杂质和缺陷。 对于少子寿命有明显依赖关系的电子器件特性,主要有双极型器件的开关特性、导通特性和阻断特性;对于光电池、光电探测器等之类光电子器件,与少子寿命直接有关的特性主要有光生电流、光生电动势等。 (1)少子寿命对半导体器件性能的影响: ①双极型器件的开关特性与少子寿命的关系: 双极型器件的开关特性在本质上可归结为p-n结的开关性能。 p-n结的开关时间主要是关断时间,而关断时间基本上就是导通时注入到扩散区中的少子电荷消失的过程时间(包括有存储时间和下降时间两个过程)。少子寿命越短,开关速度就越快。因此,为了提高器件的开关速度,就应该减短少子寿命。 ②器件的阻断特性与少子寿命的关系: 半导体器件在截止状态时的特性——阻断特性,实际上也就是p-n结在反向电压下反向漏电流大小的一种反映。因此,这里器件的阻断特性不单指双极型器件,而且也包括场效应器件在内。 p-n结的反向漏电流含有两个分量:一是两边扩散区的少子扩散电流,二是势垒区中复合中心的产生电流;这些电流都与少子寿命有关,载流子寿命越长,反向漏电流就越小,则器件的阻断特性也就越好。当载流子寿命减短到一定程度时,反向电流即大幅度地上升,就会产生反向电流不饱和的“软”的阻断特性。 一般,硅p-n结的反向漏电流主要是势垒区复合中心的产生电流,因此载流子的产生寿命将严重地影响到器件的阻断特性。所以注意工艺控制,减小杂质和缺陷的不良影响,对于提高器件的阻断特性至关重要。 总之,为了获得良好的器件阻断特性,要求器件应该具有较长的少数载流子寿命。为此, PH与氢离子的浓度换算表 ph [H+]mol/L ph [H+]mol/L ph [H+]mol/L ph [H+]mol/L n.00 1.00*10-n n.26 5.5*10-(n+1)n.51 3.09*10-(n+1)n.76 1.74*10-(n+1) n.01 9.77*10-(n+1)n.27 5.37*10-(n+1)n.52 3.02*10-(n+1)n.77 1.7*10-(n+1) n.02 9.55*10-(n+1)n.28 5.25*10-(n+1)n.53 2.95*10-(n+1)n.78 1.66*10-(n+1) n.03 9.33*10-(n+1)n.29 5.13*10-(n+1)n.54 2.88*10-(n+1)n.79 1.62*10-(n+1) n.04 9.12*10-(n+1)n.30 5.01*10-(n+1)n.55 2.82*10-(n+1)n.80 1.59*10-(n+1) n.05 8.91*10-(n+1)n.31 4.9*10-(n+1)n.56 2.76*10-(n+1)n.81 1.55*10-(n+1) n.06 8.71*10-(n+1)n.32 4.79*10-(n+1)n.57 2.69*10-(n+1)n.82 1.51*10-(n+1) n.07 8.51*10-(n+1)n.33 4.68*10-(n+1)n.58 2.63*10-(n+1)n.83 1.48*10-(n+1) n.08 8.32*10-(n+1)n.34 4.57*10-(n+1)n.59 2.57*10-(n+1)n.84 1.45*10-(n+1) n.09 8.13*10-(n+1)n.35 4.47*10-(n+1)n.60 2.51*10-(n+1)n.85 1.41*10-(n+1) n.10 7.94*10-(n+1)n.36 4.37*10-(n+1)n.61 2.46*10-(n+1)n.86 1.38*10-(n+1) n.11 7.76*10-(n+1)n.37 4.27*10-(n+1)n.62 2.4*10-(n+1)n.87 1.35*10-(n+1) n.12 7.58*10-(n+1)n.38 4.17*10-(n+1)n.63 2.35*10-(n+1)n.88 1.32*10-(n+1) n.13 7.41*10-(n+1)n.39 4.07*10-(n+1)n.64 2.29*10-(n+1)n.89 1.29*10-(n+1) n.14 7.25*10-(n+1)n.40 3.98*10-(n+1)n.65 2.24*10-(n+1)n.90 1.26*10-(n+1) n.15 7.08*10-(n+1)n.41 3.89*10-(n+1)n.66 2.19*10-(n+1)n.91 1.23*10-(n+1) n.16 6.92*10-(n+1)n.42 3.8*10-(n+1)n.67 2.14*10-(n+1)n.92 1.2*10-(n+1) n.17 6.76*10-(n+1)n.43 3.72*10-(n+1)n.68 2.09*10-(n+1)n.93 1.18*10-(n+1) n.18 6.61*10-(n+1)n.44 3.63*10-(n+1)n.69 2.04*10-(n+1)n.94 1.15*10-(n+1) n.19 6.46*10-(n+1)n.45 3.55*10-(n+1)n.70 2*10-(n+1)n.95 1.12*10-(n+1) n.20 6.31*10-(n+1)n.46 3.47*10-(n+1)n.71 1.95*10-(n+1)n.96 1.1*10-(n+1) n.21 6.17*10-(n+1)n.47 3.39*10-(n+1)n.72 1.91*10-(n+1)n.97 1.07*10-(n+1) n.22 6.03*10-(n+1)n.48 3.31*10-(n+1)n.73 1.86*10-(n+1)n.98 1.05*10-(n+1) n.23 5.89*10-(n+1)n.49 3.24*10-(n+1)n.74 1.82*10-(n+1)n.99 1.02*10-(n+1) n.24 5.76*10-(n+1)n.50 3.16*10-(n+1)n.75 1.78*10-(n+1)(n+1).00 1.00*10-(n+1) 例: PH=2.23 由PH=-lg[H+] [H+]=10-2.23=5.89*10-3mol/L 查表得: [H+]=5.89*10-(2+1)=5.89*10-3mol/L 第三章:少数载流子寿命测试 少数载流子寿命是半导体材料的一个重要参数,它在半导体发展之初就已经存在了。早在20世纪50年代,Shockley 和Hall等人就已经报道过有关少数载流子的复合理论[1-4],之后虽然陆续有人研究半导体中少数载流子的寿命,但由于当时测试设备简陋,样品制备困难,尤其对于测试结果无法进行系统地分析。因此对于少数载流子寿命的研究并没有引起广泛关注。直到商业需求的增加,少数载流子寿命的测试才重新引起人们的注意。晶体生产厂家和IC集成电路公司纷纷采用载流子寿命测试来监控生产过程,如半导体硅单晶生产者用载流子寿命来表征直拉硅单晶的质量,并用于研究可能造成质量下降的缺陷。IC集成电路公司也用载流子寿命来表征工艺过程的洁净度,并用于研究造成器件性能下降的原因。此时就要求相应的测试设备是无破坏,无接触,无污染的,而且样品的制备不能十分复杂,由此推动了测试设备的发展。 然而对载流子寿命测试起重要推动作用的,是铁硼对形成和分解的发现[5,6],起初这只是被当作一种有趣的现象,并没有被应用到半导体测试中来。直到Zoth 和Bergholz发现,在掺B半导体中,只要分别测试铁硼对分解前后的少子寿命,就可以知道样品中铁的浓度[7]。由于在现今的晶体生长工艺中,铁作为不锈钢的组成元素,是一种重要的金属沾污,对微电子器件和太阳能电池的危害很严重。通过少数载流子寿命测试,就可以得到半导体中铁沾污的浓度,这无疑是一次重大突破,也是半导体材料参数测试与器件性能表征的完美结合。之后载流子寿命测试设备迅速发展。 目前,少数载流子寿命作为半导体材料的一个重要参数,已作为表征器件性能,太阳能电池效率的重要参考依据。然而由于不同测试设备在光注入量,测试频率,温度等参数上存在差别,测试值往往相差很大,误差范围可能在100%,甚至以上,因此在寿命值的比较中要特别注意。 概括来说,少数载流子寿命的测试及应用经历了一个漫长的发展阶段,理论上,从简单的载流子复合机制到考虑测试结果的影响因素。应用上,从单纯地用少子寿命值作为半导体材料的一个参数,到把测试结果与半导体生产工艺结合起来考虑。测试设备上,从简陋,操作复杂到精密,操作简单,而且对样品无接触, 少子寿命是半导体材料和器件的重要参数。它直接反映了材料的质量和器件特性。能够准确的得到这个参数,对于半导体器件制造具有重要意义。 少子,即少数载流子,是半导体物理的概念。它相对于多子而言。 半导体材料中有电子和空穴两种载流子。如果在半导体材料中某种载流子占少数,导电中起到次要作用,则称它为少子。如,在 N型半导体中,空穴是少数载流子,电子是多数载流子;在P型半导体中,空穴是多数载流子,电子是少数载流子。 多子和少子的形成:五价元素的原子有五个价电子,当它顶替晶格中的四价硅原子时,每个五价元素原子中的四个价电子与周围四个硅原子以共价键形式相结合,而余下的一个就不受共价键束缚,它在室温时所获得的热能足以便它挣脱原子核的吸引而变成自由电子。出于该电子不是共价键中的价电子,因而不会同时产生空穴。而对于每个五价元素原子,尽管它释放出一个自由电子后变成带一个电子电荷量的正离子,但它束缚在晶格中,不能象载流子那样起导电作用。这样,与本征激发浓度相比,N型半导体中自由电子浓度大大增加了,而空穴因与自由电子相遇而复合的机会增大,其浓度反而更小了。 少子浓度主要由本征激发决定,所以受温度影响较大。 香港永先单晶少子寿命测试仪 >> 单晶少子寿命测试仪 编辑本段产品名称 LT-2单晶少子寿命测试仪 编辑本段产品简介 少数载流子寿命(简称少子寿命)是半导体材料的一项重要参数,它对半导体器件的性能、太阳能电池的效率都有重要的影响.我们采用微波反射光电导衰减法研制了一台半导体材料少子寿命测试仪,本文将对测试仪的实验装置、测试原理及程序计算进行了较详细的介绍,并与国外同类产品的测试进行比较,结果表明本测试仪测试结果准确、重复性高,适合少子寿命的实验室研究和工业在线测试. 技术参数: 测试单晶电阻率范围 >2Ω.cm 少子寿命测试范围 10μS~5000μS 配备光源类型 波长:1.09μm;余辉<1 μS; 闪光频率为:20~30次/秒; 闪光频率为:20~30次/秒; 高频振荡源 用石英谐振器,振荡频率:30MHz 前置放大器 放大倍数约25,频宽2 Hz-1 MHz 仪器测量重复误差 <±20% 第六章酸碱滴定第三节酸碱溶液中氢离子浓度的计算 教学目的:1.学生了解酸碱溶液pH计算公式的一般推导过程 2. 学生掌握各类酸碱溶液pH的计算 所需课时:2学时 本次课重点:强酸碱、一元弱酸碱及多元酸碱溶液pH的计算 本次课难点:一元弱酸碱及多元酸碱溶液pH计算 授课方式:讲授与学生练习相结合,PPt与板书结合 授课安排: 一、(3分钟)复习PBE的书写 HAc, H3PO4, NaHCO3 二、(2分钟)酸碱溶液中氢离子浓度计算的重要性(本次课内容是同学们认为最难最麻烦的部分,对其重要性的分析对有利于提高学生学习积极性): 1、氢离子浓度决定溶液中各存在型体的分布分数 2、酸碱滴定过程中溶液pH不断发生改变,通过pH计算画出滴定曲线,分析滴定过程,选择合适指示剂,确定滴定方法。 三、(3分钟)酸碱溶液的分类及氢离子浓度计算过程的一般处理方法 1、分类:一元强酸碱、一元弱酸碱、二元及多元酸碱、两性物质、混合溶液。 2、一般处理方法:写出PBE,根据平衡关系进行代换得到精确式,误差要求范围内适当简化得到近似式(画框图,板书)。 3、溶液氢离子浓度计算方法:先对溶液进行分类,根据判据利用相应的公式进行计算。 四、(5~10分钟)一元强酸(碱)氢离子浓度的计算 设问1:0.1 mol/L HCl和NaOH溶液的pH是多少? 引出:一般情况下强酸(碱)溶液中[H+]= c ([OH-]= c) 设问2:c= 10-7mol ?L -1的HCl 呢? 答:此时不能忽略水的解离所产生的氢离子对溶液pH 的影响,一般式显然不能 使用,否则引入误差过大。 对c= 10-7mol ?L -1的HCl 的pH 进行计算(推导过程板书) PBE :[H +] = c (HCl) + [OH -] 精确式:[]H + =(板书至此) 练习题:c= 10-7mol ?L -1的NaOH 的pH 是多少? 2分钟时间,由同学们自己在练习本上推导。提问同学宣读自己的结果。 再给出正确的推导过程及结果(播放PPt ,不板书),与同学自己的结果对照。 五、(20~30分钟)一元弱酸(碱)氢离子浓度的计算 1、以c mol·L -1的一元弱酸HA 为例,过程由教师一步步讲解推导(板书,可以 留给学生思考的时间) PBE :[H +]=[A -]+[OH -] 平衡关系式:+a w [HA][H ][H ][H ] K K ++=+ 精确表达式:[]H += 提问:利用+a +a [H ][HA][H ]c K =+代入上式即可达到结果,每次解三次方程,有必要吗? 提出简化公式的条件:①水的解离是否可以忽略,②酸解离度小,解离部分对 其浓度的影响是否可以忽略。针对精确式就这两个方面进行讨论。 得到计算公式: ①最简式:+20,H [] 400,a w a cK K c H K ++>=>水的解离产生的对溶液酸度的影响可忽略, 则 若同时 酸解离对酸分子溶液浓度的影响可忽略,则 [H 溶液中H +浓度的计算公式总结: 一、强酸(强碱)溶液 1. c a ≥10-6 mol/L 时,[H +] =c a ; 2. c a ≤10-8 mol/L 时,[H +] = [OH -]=10-7; 3. 10-8<c a <10-6 mol/L 时,求解一元二次方程0][][2=--++w a K H c H ,即得 24][2 w a a K c c H ++=+ 二、一元弱酸(碱)溶液 由PBE 可得:w a K HA K H +=+][][,整理得到一元三次方程。 1. c a ?K a ≥10K w 时,水的离解忽略不计: (1) c a /K a ≥100 (5-9) (2) c a /K a <100似式1 (5-8),整理得到一元二次方程0][][2=-+++a a a K c H K H ,求解方程可得 a a a a K c K K H ++-=+ 42][2 2. c a ?K a <10K w 时, 水的离解不能忽略: (1) c a /K a ≥100 2 (5-10) (2) c a /K a <100时,弱酸离解部分不能忽略不计:整理得到一元三次方程 0])[(][][23=-+-++++w a w a a a K K H K K c H K H ——精确式(5-6) 三、多元弱酸(碱)溶液 以二元弱酸为例,由PBE 可得)] [21]([][221++++=H K A H K K H a a w ,整理得到一元四次方程,难以求解,见课本精确式(5-12),故要采取近似处理。 H 2A 的第二级解离忽略不计,按一元弱酸处理。上述计算一元弱酸溶液中氢离子浓度的计算公式以及相关的近似条件都适用,只是要用二元弱酸的K a1代替一元弱酸的K a 。 *推广到所有碱溶液pH 的计算,先求算溶液中OH -浓度:(1) [OH -]代替[H +]; (2) K b 代替K a ;(3) c b 代替c a ;则pOH= -lg[OH -],pH=14- pOH 。 (注1:涉及到计算多元碱溶液中的OH -浓度,则注意要用相应的碱的各级离解常数代替酸的相应的各级离解常数(如用k b1代替k a1,用k b2代替k a2))。 (注2:c a 代表酸的浓度,c b 代表碱的浓度) 四、混合溶液 1. 弱酸(弱碱)的混合溶液 由PBE 可得:w HB HA K HB K HA K H ++=+][][][ 由于溶液为弱酸性,可忽略水的离解;两酸互相抑制,离解较弱,可以分析浓度代替平衡浓度,因而HB HB HA HA c K c K H +=+][——(5-17) 若K HA c HA >>K HB c HB ,则HA HA c K H =+][——(5-18) 2. 弱酸与弱碱的混合溶液 由PBE 可得,B HA HB HA c c K K H /][=+——(5-20) 五、两性物质溶液 包括弱酸的酸式盐、弱酸弱碱盐和氨基酸类: (一)以弱酸的酸式盐为例:--?→??? ←2K 22b2B HB B H a K ,由PBE 可得] [)][(][121--+++=HA K K HA K K H a w a a ,由于HA -的酸式离解和碱式离解相互抑制,离解出的部分忽略不计,则[HA -]≈c ,c K K c K K H a w a a ++=+121)(][ 实验二光电导衰退测量少数载流子的寿命 实验项目性质:综合实验 所涉及课程:半导体物理、半导体材料 计划学时:2学时 一、实验目的 1.理解非平衡载流子的注入与复合过程; 2.了解非平衡载流子寿命的测量方法; 2.学会光电导衰退测量少子寿命的实验方法。 二、实验原理 半导体中少数载流子的寿命对双极型器件的电流增益、正向压降和开关速度等起着决定性作用。半导体太阳能电池的换能效率、半导体探测器的探测率和发光二极管的发光效率也和载流子的寿命有关。因此,半导体中少数载流子寿命的测量一直受到广泛的重视。 处于热平衡状态的半导体,在一定的温度下,载流子浓度是一定的,但这种热平衡状态是相对的,有条件的。如果对半导体施加外界作用,破坏了热平衡的条件,这就迫使它处于与热平衡状态相偏离的状态,称为非平衡状态。处于非平衡状态的半导体,其载流子浓度也不再是n0和p0,可以比它们多出一部分。比平衡状态多出来的这部分载流子称为非平衡载流子,有时也称为过剩载流子。要破坏半导体的平衡态,对它施加的外部作用可以是光,也可以是电或是其它的能量传递方式。常用到的方式是电注入,最典型的例子就是PN结。用光照使得半导体内部产生非平衡载流子的方法,称为非平衡载流子的光注入,光注入时,非平衡载流子浓度Δn=Δp。 当外部的光注入撤除以后,注入的非平衡载流子并不能一直存在下去,它们要逐渐消失,也是原来激发到导带的电子又回到价带,电了和空穴又成对的消失了。最后,载流子浓度恢复到平衡时的值,半导体又回到平衡态,过剩载流子逐渐消失,这一过程称为非平衡载流子的复合。实验表明,光照停止后,Δp随时间按指数规律减少。这说明非平衡载流子不是立刻全部消失,而是有一个过程, 第5章非平衡载流子 1. 一个n型半导体样品的额外空穴密度为1013cm-3,已知空穴寿命为100μs,计 算空穴的复合率。 2. 用强光照射n型样品,假定光被均匀吸收,产生额外载流子,产生率为g p, 空穴寿命为τ,请 ①写出光照开始阶段额外载流子密度随时间变化所满足的方程; ②求出光照下达到稳定状态时的额外载流子密度。 3. 有一块n型硅样品,额外载流子寿命是1μs,无光照时的电阻率是10Ω?cm。 今用光照射该样品,光被半导体均匀吸收,电子-空穴对的产生率是1022/cm3?s,试计算光照下样品的电阻率,并求电导中少数载流子的贡献占多大比例?4.一块半导体样品的额外载流子寿命τ=10μs,今用光照在其中产生非平衡载流子,问光照突然停止后的20μs时刻其额外载流子密度衰减到原来的百分之几? 5. 光照在掺杂浓度为1016cm-3的n型硅中产生的额外载流子密度为?n=?p= 1016cm-3。计算无光照和有光照时的电导率。 6.画出p型半导体在光照(小注入)前后的能带图,标出原来的费米能级和光照 时的准费米能级。 7. 光照在施主浓度N D=1015cm-3的n型硅中产生额外载流子?n=?p=1014cm-3。试 计算这种情况下准费米能级的位置,并和原来的费米能级作比较。 8. 在一块p型半导体中,有一种复合-产生中心,小注入时,被这些中心俘获 的电子发射回导带的过程和它与空穴复合的过程具有相同的几率。试求这种复合-产生中心的能级位置,并说明它能否成为有效的复合中心? 9.一块n型硅内掺有1016cm-3的金原子,试求它在小注入时的寿命。若一块p型硅内也掺有1016cm-3的金原子,它在小注入时的寿命又是多少? 10.在下述条件下,是否有载流子的净复合或者净产生: ①载流子完全耗尽(即n,p都大大小于n i)的半导体区域。 ②在只有少数载流子被耗尽(例如p n< >n i。 11、对掺杂浓度N D =1016cm-3、少数载流子寿命τp=10μs的n型硅,求少数载流子 全部被外界清除时电子-空穴对的产生率。(设E T=E i) 实验一光电导衰退测量少数载流子的寿命 一、实验目的 1.理解非平衡载流子的注入和复合过程; 2.了解非平衡载流子寿命的测量方法; 3.学会光电导衰退测量少子寿命的实验方法。 二、实验原理 半导体中少数载流子的寿命对双极型器件的电流增益、正向压降和开关速度等起着决定性作用。半导体太阳能电池的换能效率、半导体探测器的探测率和发光二极管的发光效率也和载流子的寿命有关。因此,半导体中少数载流子寿命的测量一直受到广泛的重视。 处于热平衡状态的半导体,在一定的温度下,载流子浓度是一定的,但这种热平衡状态是相对的,有条件的。如果对半导体施加外界作用,破坏了热平衡的条件,这就迫使它处于与热平衡状态相偏离的状态,称为非平衡状态。处于非平衡状态的半导体,其载流子浓度也不再是 n0 和 p0,可以比它们多出一部分。比平衡状态多出来的这部分载流子称为非平衡载流子,有时也称为过剩载流子。要破坏半导体的平衡态,对它施加的外部作用可以是光,也可以是电或是其它的能量传递方式。常用到的方式是电注入,最典型的例子就是 PN 结。用光照使得半导体内部产生非平衡载流子的方法,称为非平衡载流子的光注入,光注入时,非平衡载流子浓度Δn=Δp。 当外部的光注入撤除以后,注入的非平衡载流子并不能一直存在下去,它们要逐渐消失,也是原来激发到导带的电子又回到价带,电了和空穴又成对的消失了。最后,载流子浓度恢复到平衡时的值,半导体又回到平衡态,过剩载流子逐渐消失,这一过程称为非平衡载流子的复合。实验表明,光照停止后,Δp 随时间按指数规律减少。这说明非平衡载流子不是立刻全部消失,而是有一个过程,即它们在导带和价带中有一定的生存时间,有的长些,有的短些。非平衡载流子的平均生存时间称为非平衡载流子的寿命,用t 表示。由于相对于非平衡多数载流子,非平衡少数载流子的影响处于主导的、决定的地位,因而非平衡载流子的寿命通常称为少数载流子寿命。显然 1/t 就表示单位时间内非平衡载流子的复合概率。通常把单位时间单位体积内净复合消失的电子-空穴对数称为非平衡载流子的复合率。很明显,Δp/t 就代表复合率。 以光子能量略大于半导体禁带宽度的光照射样品,在样品中激发产生非平衡电子和空穴。若样品中没有明显的陷阱效应,那么非平衡电子和空穴浓度相等,他们的寿命也就相同。如果所采用的光在半导体中的吸收系数比较小,而且非平衡载流子在样品表面复合掉的部分可以忽略,那么光激发的非平衡载流子在样品内可以看成是均匀分布。假定一束光在一块n型半导体内部均匀的产生非平衡载流子Δn和Δp。在t=0时刻,光照突然停止,Δp 随时间而变化,单位时间内非平衡载流子浓度的减少应为-dΔp(t)/dt,它由复合引起,因此应当等于非平衡载流子的复合率,即 多数载流子与少数载流子的特性比较 2009-11-02 20:09:52| 分类:微电子物理| 标签:|字号大中小订阅 作者:Xie M. X. (UESTC,成都市) l 载流子浓度: 对于n型半导体,如果掺杂浓度为ND,则在杂质全电离情况下,其中多数载流子浓度为:n0 ≈ ND,即多数载流子浓度基本上决定于掺杂浓度。假若杂质未全电离,则多数载流子浓度决定于杂质的电离程度,随着杂质的不断电离,多数载流子浓度也不断增大(与温度有指数函数关系)。 而少数载流子浓度,在杂质全电离情况下,可根据热平衡关系n0 p0 = ni2,得到为p0 = ni2 / n0 ≈ ni2 / ND。这就是说,少数载流子浓度基本上决定于本征激发过程,并且与掺杂浓度有关。掺杂浓度越高,少数载流子浓度就越低;掺杂浓度越低,少数载流子浓度就越高。 总之,对于Si器件,在室温附近,一般杂质是全电离的,这时多数载流子浓度基本上与温度无关,可近似等于掺杂浓度;而少数载流子浓度则与温度有指数函数的关系(决定于本征激发)。这种不同的多数载流子浓度与少数载流子浓度的温度关系,也就决定了多数载流子器件(场效应器件)与少数载流子器件(双极型器件)在性能上的不同温度关系。 l 载流子的运动: 载流子的运动形式基本上有两种,即漂移运动和扩散运动。这两种运动所产生的电流大小分别决定于不同的因素:漂移电流主要决定于多数载流子浓度和电场的大小;扩散电流主要决定于载流子的浓度梯度,而与浓度本身的大小无关。 半导体与金属一样,其内部都需要保持电中性(表面不需要保持电中性,可以带有电荷)。对于多数载流子而言,由于电中性的要求,在半导体中很难形成明显的浓度梯度,所以扩散电流往往可以忽略;但是少数载流子则恰恰相反,能够在出现很大浓度梯度的情况下保持电中性,所以数量很少的少数载流子可以产生很大的扩散电流。 总之,多数载流子电流主要以漂移电流为主,少数载流子电流则主要以扩散电流为主。 l 载流子的注入和抽出: 在外界作用下,半导体即偏离平衡状态,成为了一个非平衡体系。偏离平衡的程度即由多数载流子的准Fermi能级与少数载流子的准Fermi能级的分开大小来衡量(如果外加电压为V,则两条准Fermi能级的分开大小=qV)。 在非平衡半导体中,载流子浓度将比平衡载流子浓度增多了(即注入了非平衡载流子)或者减少了(即抽出了非平衡载流子)。由于要满足电中性的要求,则一般只能注入或抽出少数载流子,而不能注入或抽出多数载流子。也正因为如此,多数载流子在半导体中较难以积累或减小而产生浓度梯度;相反,少数载流子则可在半导体中的局部区域积累、或把局部区域的少数载流子抽掉,而可在局部区域形成较大的浓度梯度。 l 载流子的寿命: 在非平衡半导体,其中的载流子浓度将偏离于平衡载流子浓度(在注入情况下是多出了载流子,在抽取情况下是缺少了载流子)。 当去掉外加在非平衡半导体上的作用后,半导体体系将要恢复到平衡状态,即其中多出的载流子将要复合掉,缺少的载流子将要产生出来。这种载流子的复合或者产生,都需要时间,这就是所谓复合寿命或者产生寿命。对于Si、Ge半导体,由于载流子的复合与产生主要是通过复合中心或者产生中心来实现的,所以载流子的复合寿命或者产生寿命的长短也主要决定于复合中心或者产生中心的性质和数量。 由于注入或抽出的载流子一般是少数载流子,所以载流子的复合寿命或者产生寿命通常 光电导衰退测量少数载流子的寿命 一、 目的 本实验的目的是学会用高频光电导衰退法测量硅单晶中少数载流子的寿命。 半导体中少数载流子的寿命对双极型器件的电流增益、正向压降和开关速度等起着决定性作用。半导体太阳能电池的换能效率、半导体探测器的探测率和发光二极管的发光效率也和载流子的寿命有关。因此,半导体中少数载流子寿命的测量一直受到广泛的重视。 测量少数载流子寿命的方法很多,分别属于瞬态法和和稳态法两大类。瞬态法是由测量半导体样品从非平衡态向平衡态过渡过程的快慢来确定载流子寿命。例如:对均匀半导体材料有光电导衰退法,双脉冲法,相移法;对P-N 结二极管有反向恢复时间法,开路电压衰退法。稳态法是由测量半导体处在稳定的非平衡时的某些物理量来求得载流子的寿命。例如:扩散长度法,稳态光电导法,光磁效应法,表面光电压法等。近年来,许多文章介绍扫描电镜测量半导体的少数载流子扩散长度。在硅单晶的检验和器件工艺监测中应用最广泛的是光电导衰退法和表面光电压法,这两种测试方法已经被列入美国材料测试学会(ASTM)的标准方法。 光电导衰退法有直流光电导衰退法、高频光电导衰退法和微波光电导衰退法。其差别主要在于用直流、高频电流还是微波来提供检测样品中非平衡载流子的衰退过程的手段。直流法是标准方法,高频法在硅单晶质量检验中使用十分方便,而微波法则可以用于器件工艺线上测试晶片的工艺质量。 二、 原理 以光子能量略大于半导体禁带宽度的光照射样品,在样品中激发产生非平衡电子和空穴。若样品中没有明显的陷阱效应,那么非平衡电子和空穴浓度相等,他们的寿命也就相同。如果所采用的光在半导体中的吸收系数比较小,而且非平衡载流子在样品表面复合掉的部分可以忽略,那么光激发的非平衡载流子在样品内可以看成是均匀分布。设t=0时停止照射,非平衡的电子和空穴将不断复合而逐渐减少。对于n 型半导体中任意一点,非平衡载流子流过体内复合中心消失的复合率是dt p d ??,它和非平衡载流子的浓度?p 成正比。即: p dt p d ?=??β (1) 在非平衡少数载流子浓度?p 比平衡载流子浓度n 0小得多时,(1)式中的β是一个常数。设t=0时,?p=?p(0),由式(1)可得: )exp()0(t p p β??=? (2) 非平衡少数载流子的平均存在时间就是少数载流子寿命 ∫∫∞ ∞ ??=00p d p td p τ (3) 将(2)式代入(3)式中,得:βτ1 =p (4) 第五章 非平衡载流子 1、在一个n 型锗样品中,过剩空穴浓度为1013cm -3 ,空穴的寿命为100μm ,计算空穴的复合率。 解:133 1131010/()100U cm cm s s p τμμ-===? 4、一块半导体材料的寿命10s τμ=,光照在材料中会产生非平衡载流子,试求光照突然停止20s μ后,其中非平衡载流子将衰减到原来的百分之几? 解:20100 002 0()()13.5%(()())t s s p p e p p e e p t μμτ --=== = 6、画出p 型半导体在光照(小注入)前后的能带图,标出原来的费米能级和光照时的准费米能级。 7、掺施主浓度15310D N cm -=的n 型硅,由于光的照射产生了非平衡载流子143 10n p cm -== 。试计算这种情况下准费米能级的位置,并和原来的费米能级作比较。 解:光照前,室温下,半导体处于过渡区,杂质全部电离,本征激发还未开始(可忽略), 15 3 010D n N cm -==,2 00i n p n =过渡区00103 ln()0.026ln()0.2891.510F i i i i n E E k T E ev E ev n cm -=+=+?=+? 光照,小注入后: 153143 0103 53143 0103 1010ln 0.026ln()0.2911.5102.251010ln 0.026ln()0.2291.510n F i i i i p F i i i i n p F F F F n cm cm E E k T E ev E ev n cm p cm cm E E k T E ev E ev n cm E E E E ------+=+=+?=+??+=+=+?=+?即在原费米能级上面0.002ev 处,在原费米能级下面0.06ev 处。 10、一块n 型硅内有1016cm -3 的金原子,试求它在小注入时的寿命。若一块p 型硅内也掺有1016cm -3 的金原子,它在小注入时的寿命又是多少?(室温下) 迁移率是指载流子(电子和空穴)在单位电场作用下的平均漂移速度,即载流子在电场作用下运动速度的快慢的量度,运动得越快,迁移率越大;运动得慢,迁移率小。同一种半导体材料中,载流子类型不同,迁移率不同,一般是电子的迁移率高于空穴。如室温下,轻参杂硅材料中,电子的迁移率为1350cm^2/(V S),而空穴的迁移率仅为480cm^2/(VS)。 迁移率主要影响到晶体管的两个性能: 一是载流子浓度一起决定半导体材料的电导率(电阻率的倒数)的大小。迁移率越大,电阻率越小,通过相同电流时,功耗越小,电流承载能力越大。由于电子的迁移率一般高于空穴的迁移率,因此,功率型MOSFET通常总是采用电子作为载流子的n沟道结构,而不采用空穴作为载流子的p沟道结构。 二是影响器件的工作频率。双极晶体管频率响应特性最主要的限制是少数载流子渡越基区的时间。迁移率越大,需要的渡越时间越短,晶体管的截止频率与基区材料的载流子迁移率成正比,因此提高载流子迁移率,可以降低功耗,提高器件的电流承载能力,同时,提高晶体管的开关形影速度。 什么是本征激发内部载流子运动有何特点什么叫复合 答:一般来说,共价键中的价电子不完全像绝缘体中价电子 所受束缚那样强,如果能从外界获得一定的能量(如光照、温升、电 磁场激发等),一些价电子就可能挣脱共价键的束缚而成为自由电 子,这就是本征激发。 理论和实验表明:在常温(T=300K)下,硅共价键中的价电子 只要获得大于电离能Ec(=的能量便可激发成为自由电子。本征锗的 电离能更小,只有。 半导体中,当共价键中的一个价电子受激发挣脱原子核的束 缚成为自由电子的同时,在共价键中便留下了一个空位,称为“空 穴”。当空穴出现时,相邻原子的价电子比较容易离开它所在的共 价键而填补到这个空穴中来,使该价电子原来所在共价键中出现一 1,那么此溶液的摩尔浓 14-(-lg(0.1%))=14+lg0.001=14-3=11 PH 值等于氢离子摩尔浓度的负对数。因为此溶液的浓度较低故把密度近似为 度为 0.1/40/0.1=0.025 mol/L 又因 NaOH 是强碱[0H-]=0.025 mol/L POH=-log[OH-]=-log(0.025)=1.6 ??? PH+POH=14 ??? PH=14-1.6=12.4 0.1%的NaOH (重量)的PH 值应怎么算? 质量为100克的溶液,合0.1升,含NaOH 0.1克,合0.1/40=0.0025mol 则氢氧化钠的摩尔浓度为 0.0025/0.仁0.025 mol/L 那么 P[OH]=-logC[OH]=-log(0.025)=1.6 所以 PH=14-1.6=12.4 pH 的概念 如果某溶液所含氢离子的浓度为 每升0.00001摩尔(mol/L ),它的氢离子浓度指数就是 5, 计算方法为-lg[浓度值]。 与其相反,如果某溶液的氢离子浓度指数为 5,他的氢离子浓度为 0.00001摩尔每升(mol/L), 计算方法为10A (-浓度指数) 氢离子浓度指数一般在 0-14之间,当它为7时溶液呈中性,小于 7时呈酸性,值越小,酸 性越强;大于7时呈碱性,值越大,碱性越强。 pH 是1909年由丹麦生物化学家 Soren Peter Lauritz Sorensen 提出。p 来自德语 Potenz(means potency, power) ,意思是浓度、力量, H ( hydrogen ion )代表氢离子(H+) ; 有 时候pH 也被写为拉丁文形式的 Pondus hydrogenii (Pondus=压强、压力,hydrogenii= 氢)。 pH 是溶液中氢离子活度的一种标度,也就是通常意义上溶液酸碱程度的衡量标准。 pH 值越 趋向于0表示溶液酸性越强,反之,越趋向于 14表示溶液碱性越强,在常温下, pH=7的溶液为 中性溶液。 由于实际中的溶液不是理想溶液,所以仅仅用 H+浓度是不可以准确测量的,因此也无法准 确计算得到溶液的 pH 。故而应当采用 H+活度,即pH=-lg aH+=- lg 丫?cH+。这样从理论上讲只 要知道氢离子的活度 aH+就可以得到溶液的准确 pH 。 水的电离和水的离子积常数 为了便于理解和说明 pH,首先阐述一下水的电离和水的离子积常数。 水的电离 水是一种极弱的 电解质,可以发生微弱的 电离,其电离方程式 为:H2O+H2OH3O+ + OH-,简写为H2SH+ + OH-,是一个吸热过程。水的电离受温度影响,加酸加碱都能抑制水 的电离。水的电离是水分子与水分子之间的相互作用而引起的,因此极难发生。实验测得, 25 r 时1L 纯水中只有1X 10A( -7)mol 的水分子发生电离。由水分子电离出的 H+和OH 数目在任何情 况下总相等。25r 时,纯水中 [H+]=[OH- ]=1 X 10A( -7)mol/L. 水的离子积常数 [H+] ? [OH -]=K(W),其中K(W)称作水的离子积常数,简称水的离子积;[H+] 和[OH-]是分别是指整个溶液中氢离子和氢氧根离子的总 物质的量浓度.K(W)只随温度变化而变 化,是温度常数.如 25E ,[H+]=[OH -]=1 X 10A( -7)mol/L,K(W)=1 X 10八(-14);100 r 时,[H+]=[OH- ]=1 X 10A( -6)mol/L,K(W)=1 X 10八(-12). 编辑本段溶液的酸碱性和 pH 掌握溶液中氢离子浓度的计算方法 教学目标:让学生掌握溶液中氢离子浓度的计算方法,并让学生通过能够完成相关习题的训练,提高学生综合考虑和分清主次的能力。 教学重点:混合溶液和两性物质溶液的PH 值的计算。 教学难点:弱酸和弱减的混合溶液和两性物质溶液的PH 值的计算。 教学方法:讲授法和练习法 课时安排:三个课时 第一课时: 教学目标:掌握强酸或强碱溶液的酸度计算,弱酸或弱碱溶液的酸度计算 教学重点:强酸或强碱溶液的酸度计算,弱酸或弱碱溶液的酸度计算 教学难点:弱酸中酸度的计算 课时安排:40分钟 教学内容: PH 的计算 常用PH 计测量的方法确定溶液的PH 。如果已知某酸的浓度及其pKa ,还可以用计算的方法求得PH 。酸的种类繁多,如强酸、弱酸、一元酸、多元酸、混合酸、两性物质等。下面简要介绍常见的PH 计算方法。 一. 强酸或强碱溶液的酸度计算: 强酸强碱溶液在溶液中全部解离,故在一般情况下,酸度的计算比较简单。但他们的浓度很稀的时候,溶液的酸度的计算就需要考虑酸或碱本身解离出来的氢离子浓度或氢氧根离子浓度之外,还要考虑水解离出来的氢离子和氢氧根离子浓度。 二.弱酸和弱碱溶液的酸度计算: 1. 一元弱酸或弱碱 一元弱酸溶液中存在的酸碱组分有H ,OH ,HO ,A 和HA ,以HA 和HO 为参考水准,设 浓度为a mol/L 的 HCl 溶液 PBE a +=-+][OH ][H a a =≥+][H mol/L 101-6时,)(] OH [][H mol/L 102-8-+=≤时,)(a a K a a w +=+=<<+-+] [H ]OH [][H mol/L 101036-8-时,)(整理得 0 ][H ][H 2=--++w K a 若允许误差不>5%,有: 用同样的思路可处理强碱体系。 1. 强酸(强碱)溶液载流子寿命
PH与氢离子的浓度换算表
少数载流子寿命测试
少子寿命概念
酸碱滴定酸碱溶液中氢离子浓度的计算
溶液中氢离子浓度的计算公式总结-final
实验二 光电导衰退测量少数载流子的寿命
第5章-非平衡载流子-习题讲解
实验一 光电导衰退测量少数载流子的寿命
多数载流子与少数载流子的特性比较
光电导衰退测量少数载流子的寿命
第五章 非平衡载流子 布置作业解答
载流子
PH值与氢离子浓度的关系
掌握溶液中氢离子浓度的计算方法
