关于药用胶囊、胶囊剂药品生产企业所用明胶、药用胶囊
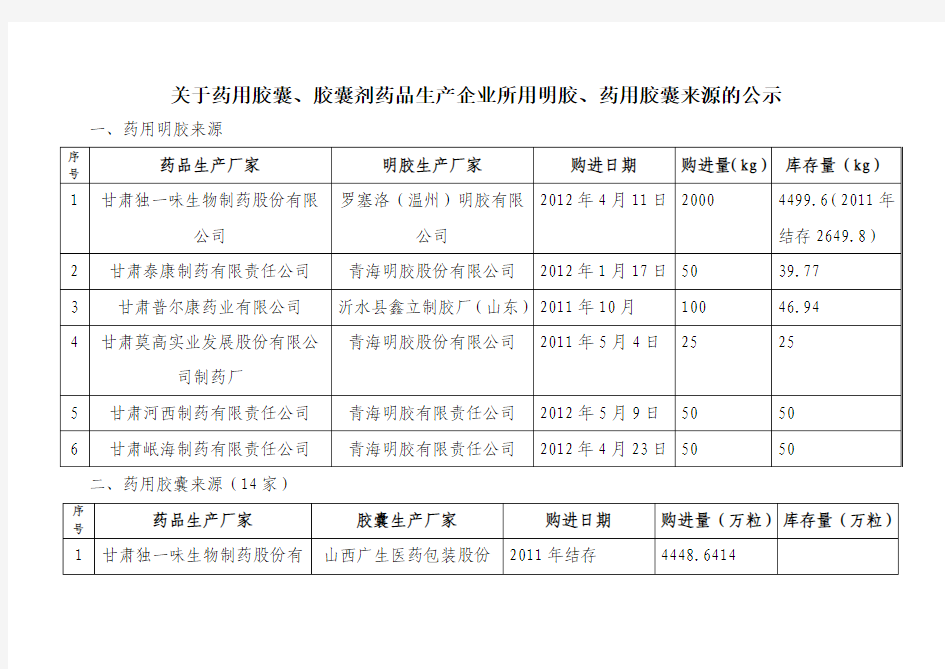

关于药用胶囊、胶囊剂药品生产企业所用明胶、药用胶囊来源的公示一、药用明胶来源
二、药用胶囊来源(14家)
未使用明胶和胶囊的企业(6家):
甘肃天森药业有限公司、甘肃祁连山药业有限公司、兰州伟慈制药有限责任公司、甘南佛阁藏药有限公司、甘肃众友药业制药有限公司、太水岐黄药业有限责任公司。
药用辅料生产企业换发《药品生产许可证》现场检查报告
附1-3 换发《药品生产许可证》现场检查报告企业名称****药业有限公司 生产范围药用辅料[聚****树脂**胶液(肠溶型)、聚甲基****树脂**胶液E30(胃崩型)、聚****树脂**胶液包衣预混剂、甲基 ****-****乙酯共聚物水分散体、药用薄膜包衣预混剂(胃溶型)] 检查依据药品管理法、药品生产监督管理办法、药用 辅料生产质量管理规范 检查日期2018年11月3日检查结论建议整改一、综合评价 按照****省局《关于印发2018年****省药品生产许可证换发工作方案和医疗机构制剂许可证换发工作方案的通知》(*药监药生[**]**号),2018年11月3日,市局与****区市场监督管理局对其进行了现场检查: 1、厂房设施概况: ****药业有限公司成立于2007年5月,生产范围为药用辅料,生产品种有:聚****树脂**胶液、甲基****-****乙酯共聚物水分散体等,综合生产能力为****公斤。公司占地面积10000㎡,建筑面积5000 ㎡,其中洁净区面积570㎡,质检室面积120㎡,仓库面积760㎡。 车间建有以下生产线:一条水分散体(聚****树脂**胶液,甲基****-****乙酯共聚物水分散体,聚甲基****树脂**胶液E30(胃崩型))生产线,一条预混剂(药用薄膜包衣剂(胃溶型),聚****树脂**胶液包衣预混剂)生产线,所有生产车间内主要设备进行了验证及清洁验证。 车间净化空调系统采用集中式空调,空气在组合式空调器内经
初、中、高效**过滤,由风管送至室内,风管末端设置高效过滤器,气流组织为顶送侧回。车间空气消毒采用臭氧消毒法,臭氧发生设于组合空调机组送风段内;洁净室与室外大气的静压差大于10pa,产尘量大的的房间与其余房间的静压差大于10pa。 在净化区结构布置上,所有墙壁与墙壁、墙壁与地面、墙壁与顶板的夹角均由内外圆弧铝过度,所有圆弧铝的缝隙处均有密封胶密封,净化区内部的照明全部采用净化灯具,所有净化区均有不锈钢洁净地漏,并用消毒剂进行液封。 生产设备按照药品申报工艺进行配备,生产设备的选型、安装符合生产要求。与物料直接接触部分为药用不锈钢材质。 纯化水系统采用二级反渗透方式,纯化水管路采用不锈钢管道,系统采用紫外消毒后输送到用水点,定期监控。 2、车间相应设备: 车间主要生产设备有不锈钢反应罐、槽型混合机、摇摆制粒机、真空泵、振动筛、三维混合机、粉碎机。 3、该公司具有较完善的组织机构和质量保证体系,人员配备符合要求并已进行了培训。 4、该公司建有文件体系并运行,生产管理及质量管理基本符合要求。 5、厂房、生产设备和公用工程等基本能够满足药用辅料的生产工艺要求。 6、该公司检测设备和仪器基本能够满足检验需要。 经现场检查,检查组认为该公司已具备药用辅料的生产和质量检验条件,但生产质量管理、检验人员的培训等方面仍需加强管理,建议企业整改。同时,请****区药品监督管理部门加强对该公司的日常监督检查。
(医疗药品)一开办药品生产企业必须具备以下条件
药品管理法 一、开办药品生产企业,必须具备以下条件: (一)具有依法经过资格认定的药学技术人员、工程技术人员及相应的技术工人。 (二)具有与其药品生产相适应的厂房、设施和卫生环境; (三)具有能对所生产药品进行质量管理和质量检验的机构、人员以及必要的仪器设备; (四)具有保证药品质量的规章制度。 二、药品经营企业购销药品,必须有真实完整的购销记录。购销记录必须注明药品的通用名称、剂型、规格、批号、有效期、生产厂商、购(销)货单位、购(销)货数量、购销价格、购(销)货日期及国务院药品监督管理部门规定的其他内容。 有下列情形之一的,为假药: (一)药品所含成份与国家药品标准规定的成份不符的; (二)以非药品冒充药品或者以他种药品冒充此种药品的。 有下列情形之一的药品,按假药论处; (一)国务院药品监督管理部门规定禁止使用的; (二)依照本法必须批准而未经批准生产、进口,或者依照本法必须检验而未经检验即销售的。 (三)变质的; (四)被污染的; (五)使用依照本法必须取得批准文号而未取得批准文号的原料药生产
的; (六)所标明的适应症或者功能主治超出规定范围的。 三、有下列情形之一的药品,按劣药论处: (一)未标明有效期或者更改有效期的; (二)不注明或者更改生产批号的; (三)超过有效期的; (四)直接接触药品的包装材料和容器未经批准的; (五)擅自添加着色剂、防腐剂、香料、矫味剂及辅料的; (六)其他不符合药品标准规定的。 四、新开办药品批发企业和药品零售企业,应当自取得《药品经营许可证》之日起30日内,向发给其《药品经营许可证》的药品监督管理部门或者药品监督管理机构申请《药品经营质量管理规范》认证。 五、药品抽样必须由两名以上药品监督检查人员实施,并按照国务院药品监督管理部门的规定进行抽样;被抽检方应当提供抽检样品,不得拒绝,药品被抽检单位没有正当理由,国务院药品监督管理部门和被抽检单位所在地省、自治区、直辖市人民政府药品监督管理部门可以宣布停止该单位拒绝抽检的药品上市销售和使用。 六、药品生产企业、药品经营企业有下列情形之一的,由药品监督管理部门依照《药品管理法》第七十九条的规定给予处罚: (一)开办药品生产企业、药品生产企业新建药品生产车间、新增生产剂型,在国务院药品监督管理部门规定的时间内未通过《药品生产质量管理规范》认证,仍进行药品生产的;
2014年药品生产企业名录(北京市)267家
2014年北京市药品生产企业名录267家
8北京御生堂制药有限 公司 李玉文 李玉 文 其他有限责任 公司 北京市房山区良乡工业 开发区金光南街3号 片剂、颗粒剂、硬胶囊剂、凝胶剂、膏药、橡 胶膏剂、丸剂(浓缩丸、微丸)、中药提取、 中药饮片(净制、切制、炒制、炙制、蒸制、 煮制、煅制)。 京20100007 HbZ bY 2011/8/24 2015/12/17 9北京市永康药业有限 公司 陈平 李艳 明 有限责任公司 北京市丰台区科学城中 核路8号(园区) 小容量注射剂、片剂、硬胶囊剂、颗粒剂。京20100008 Hb 2010/12/18 2015/12/17 10北京三联制药有限公 司 张海涛 卜绿 萍 其他有限责任 公司 北京市丰台区丰台路口 139号2幢617室(园区) 片剂、颗粒剂、丸剂(浓缩丸)、硬胶囊剂、 散剂;中药提取。 京20100009 HbZ b 2014/1/13 2015/12/17 11扬子江药业集团北京 海燕药业有限公司 徐镜人 徐镜 人 有限责任公司 北京市昌平区生命园路 16号 片剂、硬胶囊剂。京20100115 HbZ b 2011/2/24 2015/12/18 12北京太洋树康中药饮 片厂 崔国静 崔国 静 集体所有制 (股份合作) 北京市大兴区长子营镇 企融路1号 中药饮片(含直接服用、净制、切制、炒制、 炙制、蒸制、煅制、煮制)。 京20100122 Y 2010/12/19 2015/12/18 13北京康而福药业有限 责任公司 宋明选 王爱 荣 有限责任公司 北京市昌平区科技园区 中兴路10号二层 片剂、硬胶囊剂、软胶囊剂、颗粒剂、口服液、 滴丸剂、中药提取。 京20100124 Zb 2012/6/11 2015/12/19 14北京仟草中药饮片有 限公司 杨如意 杨如 意 有限责任公司 北京市大兴区西红门镇 大生庄工业区二条三号 中药饮片(含直接服用、净制、切制、炒制、煅 制、蒸制、煮制、燀制、炙制、煨制)。 京20100129 Y 2010/12/20 2015/12/19 15北京华邈中药工程技 术开发中心 商国懋 商国 懋 全民所有制 北京市顺义区顺通路西 侧 中药饮片(含毒性饮片、净制、切制、煮制、 蒸制、炒制、炙制、煅制)。 京20100037 Y 2010/12/18 2015/12/17 16北京市恒通制药有限 公司 袁社民 袁社 民 其他有限责任 公司 北京市通州区张家湾镇 柳营村 合剂、片剂、硬胶囊剂、颗粒剂、中药提取、 糖浆剂。 京20100039 Zb 2010/12/18 2015/12/17 17北京宏济药业有限公 司 苗洁苗洁 有限责任公司 (自然人投资 或控股) 北京市通州区于家务渠 头村北 中药饮片(含净制、切制、炒制、炙制、蒸制)。京20100046 Y 2010/12/18 2015/12/17 18北京赛而生物药业有 限公司 马骉马骉 其他有限责任 公司 北京市大兴工业开发区 科苑路35号 片剂(含头孢菌素类),胶囊剂(含头孢菌素类), 散剂,颗粒剂,中药前处理及提取,原料药(肝 素钠、盐酸精氨酸、胰酶、胃膜素、胃蛋白酶、 盐酸林可霉素、土霉素、四环素、麦白霉素、 乙酰螺旋霉素、猴头菌粉、二溴甘露醇、天麻 密环菌粉、单唾液酸四己糖神经节苷脂钠、帕 米膦酸 京20100048 Hab Zb 2014/1/24 2015/12/22
药品销售管理制度培训试题【最新版】
药品销售管理制度培训试题 姓名:部门:岗位:成绩: 一、填空题:(每空2分、共50分) 1.公司在药品销售过程中,严禁销售和。 2.企业应当严格审核购货单位的、,确保将药品销售给具有合法资格的药品生产、经营企业或医疗机构。 3.企业应当将药品销售给的购货单位,并对购货单位的证明文件、及提货人员的进行核实,保证药品销售流向、合法。 4.药品批发企业不得将药品直接销售给,不得参与或其他违法药品推销活动。 5. 销售药品应开具,做到票、、、款一致。 6.做好销售记录,记录应包括药品的、剂型、规格、、、生产企业、、销售数量、单价、金额、销售日期等内容等内容。销售记录应保存不得少于年。
7.销售人员应以国家药品监督管理部门批准的为依据介绍药品,不得和误导用户。 8.销售进口药品必须向购货单位出具《进口药品检验报告书》和 复印件,并加盖企业质量管理机构。 9.企业应开展用户访问、查询、服务工作,及时向质量管理部反馈质量查询或,并落实相关质量改进措施。 10.注意所售出药品的不良反应情况,出现药品不良反应情况时,应严格执行本公司。 二、简答题:(每题25分、共50分) 1.公司建立合法客户档案,具体内容包括哪些? 2.供货单位是药品生产企业时,应索要企业的哪些资质和文件? 一、1.假劣药品、质量不合格药品
2.法定资格、经营(生产)或诊疗范围 3.合法、采购人员、身份证明、真实 4.患者、非法药品市场 5.发票、货、帐 6.通用名称、批号、有效期、供货单位、5 7.药品说明书、虚假夸大 8.《进口药品注册证》、原印章 9.售后、投诉 10.《药品不良反应报告制度》 二、1.(1)客户单位的合法证照复印件(包括《营业执照》、《药品经营(生产) 许可证》或《医疗机构执业许可证》或其他有效资质证明),加
中国药品生产企业排名前一百的名单
中国药品生产企业排名前一百的名单 1 哈药集团有限公司 2 石家庄制药集团有限公司 3 上海医药集团有限公司 4 广州医药集团有限公司 5 天津医药集团有限公司 6 扬子江药业集团有限公司 7 华北制药集团有限责任公司 8 吉林修正药业集团股份有限公司 9 中国同仁堂(集团)有限责任公司10 北京医药集团有限责任公司11 西安杨森制药有限公司12 东北制药集团有限责任公司13 太极集团有限公司14 杭州华东医药集团有限公司15 拜耳先灵医药有限公司16 浙江海正药业股份有限公司17 步长制药集团18 珠海联邦制药股份有限公司19 齐鲁制药有限公司20 汇仁(集团)有限公司21 中国生物技术集团22 四川科伦实业集团有限公司(医药制造业部份)23 上海罗氏制药有限公司24 江西济民可信集团有限公司25 浙江医药股份有限公司26 诺和诺得(中国)制药有限公司27 山东新华医药集团有限责任公司28 阿斯利康制药有限公司29 北京诺华制药有限公司30 三九医药股份有限公司31 江苏恒瑞医药股份有限公司32 天津天士力集团有限公司(医药制造业部份)33 山东鲁抗医药集团有限公司34 辉瑞制药有限公司(中国·大连)35 丽珠医药集团股份有限公司36 上海复星医药(集团)股份有限公司(医药制造业部份)37 鲁南制药集团股份有限公司38 浙江新和成股份有限公司39 上海实业医药投资股份有限公司(医药制造业部份)40 先声药业有限公司41 利君制药42 中美上海施贵宝制药有限公司43 金陵药业股份有限公司44 康恩贝集团有限公司45 云南白药集团股份有限公司46 杭州赛诺菲安万特民生制药有限公司47 江苏康缘集团有限责任公司(医药制造业部份)48 辅仁药业集团有限公司49 河南省宛西制药股份有限公司50 菏泽睿鹰制药集团有限公司51 寿光富康制药有限公司52 广东康美药业股份有限公司53 黑龙江省珍宝岛制药有限公司54 中美天津史克制药有限公司55 成都地奥制药集团有限公司56 中国(杭州)青春宝集团有限公司57 福建省福抗
胶囊制剂生产工艺规程
胶囊制剂生产工艺规程 目的:编制规范化、标准化的工艺规程作为全面指导生产和控制质量的基准性技术文件。 范围:川贝末胶囊 责任:生产科长、质量总监、固体制剂车间主任、前处理提取车间主任。 内容: 一、产品名称:川贝末胶囊 二、产品概述: 1、产品性状和特点:本品为胶囊剂,内容物为类白色的粉末。 2、规格:每粒重0.5g。 3、功能与主治:清热润肺,化痰止咳。用于肺热燥咳,干咳少痰,阴虚劳嗽、咳痰带血。 4、用法与用量:口服,一次2,4粒,一日3次。 5、注意:不宜与乌头类药材同用。 6、贮藏:密封。 7、处方来源和依据:《卫生部药品标准》第五册。三、主配方: 原辅料名称 每万粒用量(g) 原辅料名称 每万粒用量(g) 川贝母 5000 最大限量: 36万粒/批 四、工艺流程
净制 胶囊填充 干燥 粉碎 过筛 外包装 总混合 内包装 五、操作过程与工艺条件: 1、净选: 生产前检查:操作间有清场合格证及准许生产证。设备、容器有“完好证”及“已清洁”状态标记,物料有物料卡及流转证,计量器具有周检合格证。 生产操作:拣选时要认真仔细的把混入药材中的杂质除去,将拣选好的药材置洁净的容器内, 并有QA监控员监控、填写记录。 2、清洗 生产前检查:操作间有清场合格证及准许生产证。设备、容器有“完好证”及“已清洁”状态 标记,物料有物料卡及流转证,计量器具有周检合格证。生产操作:将净选后的药材,按工艺要求置适宜的容器内,用足量的水清洗,并由QA监控员监控。 3、干燥 生产前检查:操作间有清场合格证及准许生产证。设备、容器有“完好证”及“已清洁”状态标记,物料有物料卡及流转证,计量器具有周检合格证。
论药用辅料的发展现状与未来
论药用辅料的发展现状与未来 2009-05-29 13:42:09| 分类:默认分类| 标签:|字号大中小订阅 概要:本文分析了我国药用辅料的现状、目前国家相关政策以及药用辅料发展趋势,提出了药用辅料使用时注意几点问题。 主题词药用辅料,发展趋势,注意的问题 引言:药用辅料系指生产药品和调配处方时使用的赋形剂和附加剂,随着 现代科技的发展以及医疗事业的发展的需求,有关制剂带来的有关药用辅料的开发越来越多,至今国内外制剂研究和生产中实际使用的辅料已有1000多种,因此对于辅料的研制与发展将是一个重要的研究话题. 正文:现代药剂学领域中药物传递系统的出现,是科学技术进步的结晶; 新型药物剂型及制剂的问世是药剂学领域中突破性的进展。而这些成就的取得,离不开药用辅料的发展。药用辅料是生产药品和调配处方时所用的赋形剂或附加剂,对药品质量起着至关重要的作用。与欧美国家相比,我国的药用辅料起步较晚,产品的品种、规格较少,质量比较粗糙。近年来随着药品质量要求的提高,国外辅料的进入,市场竞争的加剧以及国家的鼓励政策,我国药用辅料在品种和质量上都有了很大的增加和提高,但目前我国药用辅料还存在许多问题,不利于药业发展。并且我国对药用辅料重要性的认识、相应的管理措施、跟进的技术及其运用的深度研究还没有达到应有的程度;因此我国药用辅料产业仍然存在巨大的发展缺陷和扬伸空间,除少数药用辅料企业生产的产品能生产系列化产品外,绝大多数企业生产的药用辅料质量仍然比较单一。 首先在我国,目前,药品生产企业普遍使用具有国家药品标准和批准文号的药用辅料,但是关于制剂对药用辅料有何特别要求,却缺乏一定的认识。 以《中国药典》收载的吐温80为例,标准“类别”项下仅描述为“药用辅料”,而没有说明可以用于何种给药途径、不同给药途径的最大安全剂量是多少、和哪些药物存在配伍禁忌、应该使用什么包装材料等。由于当前的辅料标准对制剂质量、安全性、疗效关联性缺乏评价,因此使得辅料在制剂中的作用没有得到应有的体现。而在得不到市场回应的情况下,往往不能有效激发企业科学使用药用辅料的积极性,使得改进产品质量的动力不足,从而难以促进药用辅料生产企业进行技术革新。此外,药品低价政策也在一定程度上制约了药用辅料的发展与运用。 但是如今,国家有关部门和一些研究机构、药品生产企业已经认识到以上问题,开始着手具有行业意义的研究工作。相信未来会哦变的更好.
最新药用辅料申报资料要求(试行)资料
附件2 药用辅料申报资料要求(试行) 品种名称:XXXXX 申请人:XXXXX 应用情况:□境内外上市制剂中未使用过的药用辅料 □境外上市制剂中已使用而在境内上市制剂中未使用过的 药用辅料 □境内上市制剂中已使用,未获得批准证明文件或核准编 号的药用辅料 □已获得批准证明文件或核准编号的药用辅料改变给药途 径或提高使用限量 □国家食品药品监督管理总局规定的其他药用辅料拟用制剂给药途径:□注射□吸入□眼用□局部及舌下□透皮□口服□其他 来源:□动物或人□矿物□植物□化学合成□其他 注册申请人名称:盖章 法定代表人:签名
一、申报资料项目 1 企业基本信息 1.1 企业名称、注册地址、生产地址1.2 企业证明性文件 1.3 研究资料保存地址 2 辅料基本信息 2.1 名称 2.2 结构与组成 2.3 理化性质及基本特性 2.4 境内外批准信息及用途 2.5 国内外药典收载情况 3 生产信息 3.1 生产工艺和过程控制 3.2 物料控制 3.3 关键步骤和中间体的控制 3.4 工艺验证和评价 3.5 生产工艺的开发 4 特性鉴定 4.1 结构和理化性质研究 4.2 杂质研究 4.3 功能特性 5 质量控制
5.1 质量标准 5.2 分析方法的验证 5.3 质量标准制定依据 6 批检验报告 7 稳定性研究 7.1 稳定性总结 7.2 稳定性数据 7.3 辅料的包装 8 药理毒理研究 二、申报资料正文及撰写要求 1 企业基本信息 1.1 企业名称、注册地址、生产地址 提供企业的名称、注册地址、生产厂、生产地址。 生产地址应精确至生产车间、生产线。 1.2 企业证明性文件 境内药用辅料生产企业需提交以下证明文件: (1)企业营业执照复印件。如企业同时持有其他类型许可证,也应同时提供其复印件,如《药品生产许可证》《食品添加剂生产许可证》及相关认证文件等。 (2)对于申请药用明胶空心胶囊、胶囊用明胶和药用明胶的国内生产企业,需另提供:①申请药用空心胶囊的,应提供明胶的合法来源证明文件,包括药用明胶的批准证明文件、标准、
药品生产企业或科工贸一体化的集团型企业设立的仅销售本企
药品生产企业或科工贸一体化的集团型企业设立的仅销售本企业(集团)药品的全资或控股商业公司(全国仅限1家商业公司)名称 序号生产企业(集团)名称经营企业名称 备 注 1 珠海联邦制药股份有限公司珠海市万邦药业有限公司 2 重庆莱美药业股份有限公司重庆市莱美医药有限公司 3 牡丹江友博药业有限责任公 司 牡丹江博博医药有限责任公司 4 长春海悦药业股份有限公司安徽同仁药业有限公司 5 江西普正制药有限公司普正药业股份有限公司 6 浙江仙琚制药股份有限公司浙江仙居制药销售有限公司 7 江西药都樟树制药有限公司江西正方医药有限公司 8 安徽环球药业股份有限公司安徽环球医药贸易有限公司 9 沈阳双鼎制药有限公司沈阳双鼎医药有限公司 10 修正药业集团股份有限公司修正药业集团营销有限公司 11 修正药业集团股份有限公司安徽忠诚医药销售有限公司 12 甘肃扶正药业科技股份有限 公司 兰州扶正医药营销有限责任公司 13 浙江华海药业股份有限公司浙江华海医药销售有限公司 14 山西仟源医药集团股份有限 公司 西藏仟源药业有限公司 15 江苏万邦生化医药股份有限 公司 江苏万邦医药营销有限公司 16 成都地奥九泓制药厂四川天麒医药有限公司 17 安庆乘风制药有限公司回音必集团芜湖医药有限公司 18 扬子江药业集团江苏制药股 份有限公司 扬子江药业集团江苏扬子江医药 经营有限公司 19 山东新华制药股份有限公司山东新华医药贸易有限公司
20 辽宁海思科制药有限公司海思科医药集团股份有限公司 21 鲁南制药集团股份有限公司鲁南新时代医药有限公司 22 海南灵康制药有限公司灵康药业集团股份有限公司 23 江苏德源药业股份有限公司连云港德源医药商业有限公司 24 西藏诺迪康药业股份有限公 司 西藏诺迪康医药有限公司 25 平光制药股份有限公司合肥平光医药有限公司 26 天津金耀药业有限公司天津天药医药科技有限公司 27 齐鲁制药有限公司合肥永吉医药有限公司 28 齐鲁制药有限公司合肥永吉医药有限公司 29 瑞阳制药有限公司瑞阳医药销售有限公司 30 北京诺华制药有限公司中美天津史克制药有限公司 31 辽宁上药好护士药业(集团) 有限公司 辽宁好护士集团医药有限公司 32 山东绿叶制药有限公司(北京 北大维信生物科技有限公司、 南京绿叶制药有限公司、四川 绿叶制药股份有限公司) 烟台绿叶药品贸易有限公司 33 内蒙古双奇药业股份有限公 司 深圳市新万泽医药有限公司34 辽宁诺维诺制药股份有限公 司 辽宁圣康医药有限公司 35 上海绿谷制药有限公司绿谷(上海)医药产业投资有限公司 36 先声药业集团(先声药业有限 公司、芜湖先声中人药业有限 公司、南京先声东元制药有限 公司、山东先声麦得津生物制 药有限公司) 江苏先声药业有限公司 37 华润赛科药业有限责任公司北京赛科昌盛医药有限责任公司 38 湖北东信药业有限公司湖北东信医药有限公司 39 深圳奥萨制药有限公司深圳市奥萨药业有限公司 40 华润双鹤药业股份有限公司 (山西晋新双鹤药业有限责 任公司、北京万辉双鹤药业有 限责任公司) 北京双鹤药业经营有限责任公司41 天津红日药业股份有限公司、天津红日康仁堂药品销售有限公
最新药品销售岗前培训资料
销售员岗前培训试卷 姓名分数 一、填空题(每题8分) 1.企业应当将药品销售给()的购货单位,并对购货单位的证明文件、()及提货人员的()进行核实,保证药品销售流向()、合法。 2.企业应当严格审核购货单位的()、经营范围或者诊疗范围,并()的范围销售药品。 3.企业销售药品,应当如实开具(),做到票、()、货、()一致。 4.企业应当做好药品()。销售记录应当包括药品的()、规格、剂型、()、有效期、生产厂商()、销售数量、单价、()、销售日期等内容。 5.销售特殊管理的药品以及国家有专门管理要求的药品,应当严格按照()执行。 6.购货单位是药品生产企业时,应查验该企业()和《营业执照》、()加盖有该企业()的复印件。 7.购货单位是药品经营企业时,应查验该企业()和
《营业执照》、()加盖有该企业()的复印件。 8.购货单位审验合格后,按其提供的购货计划开具合法的票据,销售票据按规定保存()年。 9.销售人员应以国家药品监督管理部门批准的()为依据介绍药品,不得()和误导用户。 10.销售进口药品必须向购货单位出具()和《进口药品注册证》复印件,并加盖企业质量管理机构()。对已售出的药品如发现质量问题,应及时向当地药品监督管理部门报告,并及时追回所售药品,做好()。 二、简答。 1、药品销售人员任职资格?(5分)
2、对药品批发企业、连锁企业、零售单体药店,销售人员应当收取对方哪些材料?(15分) 销售员培训试卷
1.合法、采购人员、身份证明、真实 2. 生产范围、按照相应 3. 发票、账、款 4、销售记录、通用名称、批号、购货单位、金额 5. 国家有关规定 6、《药品生产许可证》、《GMP》、原印章 7、《药品经营许可证》、《GSP》、原印章 8. 5 9. 药品说明书、虚假夸大 10、《进口药品检验报告书》、原印章、《销出药品追回记录表》
软胶囊生产工艺技术及设备
软胶囊生产工艺技术及设备 一、概述 软胶囊是继片、针剂后发展起来的一种新剂型,系将油状药物、药物溶液或药物混悬液、糊状物甚至药物粉末定量压注并包封于胶膜内,形成大小、形状各异的密封胶囊,可用滴制法或压制法制备。软胶囊囊材是用明胶、甘油、增塑剂、防腐剂、遮光剂、色素和其它适宜的药用材料制成。其大小与形态有多种,有球形(0.15~0.3ml)、椭圆形(0.10~0.5ml)、长方形(0.3~0.8ml)及筒形(0.4~4.5ml)等,可根据临床需要制成内服或外用的不同品种,胶囊壳的弹性大,故又称弹性胶囊剂或称胶丸剂。 软胶囊的主要特点: 1、整洁美观、容易吞服、可掩盖药物的不适恶臭气味。 2、装量均匀准确,溶液装量精度可达±1%,尤适合装药效强、过量后副作用大的药物,如甾体激素口服避孕药等。 3、软胶囊完全密封,其厚度可防氧进入,故对挥发性药物或遇空气容易变质的药物可以提高其稳定性,并使药物具有更长的存储期。
4、适合难以压片或贮存中会变形的低熔点固体药物。 5、可提高药物的生物利用度。 6、可做成肠溶性软胶囊及缓释制剂。 7、若是油状药物,还可省去吸收、固化等技术处理,可有效避免油状药物从吸收辅料中渗出,故软胶囊是油性药物最适宜的剂型。 8、此外,低熔点药物、生物利用度差的疏水性药物、不良苦味及臭味的药物、微量活性药物及遇光、湿、热不稳定及易氧化的药物也适合制成软胶囊。 二、软胶囊的制法 1、配料 (1)药物本身是油类的,只需加入适量抑菌剂,或再添加一定数量的玉米油(或PEG400),混匀即得。(2)药物若是固态,首先将其粉碎过100~200目筛,再与玉米油混合,经胶体磨研匀,或用低速搅拌加玻璃砂研匀,使药物以极细腻的质点形式均匀的悬浮于玉米油中。 (3)软胶囊大多填充药物的非水溶液,若要添加与水相混溶的液体如聚乙二醇、吐温-80等时,因注意其吸水性,因胶囊壳水分会迅速向内容物转移,而使
含特殊药品复方制剂管理规定
转发关于切实加强部分含特殊药品复方制剂销售管理的通知 各市食品药品监督管理局(药品监督管理局): 现将国家食品药品监督管理局《关于切实加强部分含特殊药品复方制剂销售管理的通知》(国食药监安〔2009〕503号)(以下简称503号文)转发给你们,结合我省实际提出以下贯彻意见,请及时通知辖区内有关企业一并遵照执行: 一、根据国家食品药品监督管理局《关于进一步加强含麻黄碱类复方制剂管理的通知》(国食药监办〔2008〕613号)的要求,具有蛋白同化制剂、肽类激素经营资质的药品经营企业,方可从事含麻黄碱类复方制剂的批发业务。现根据503号文精神,具有《药品经营许可证》的企业均可经营含特殊药品复方制剂。仅经营含麻黄碱类复方制剂且取得“蛋白同化制剂、肽类激素”经营资质的药品经营企业如决定今后不经营蛋白同化制剂、肽类激素,在换发《药品经营许可证》申请的同时递交核减“蛋白同化制剂、肽类激素”经营范围的报告并交回《蛋白同化制剂、肽类激素经营资格批件》原件,对已完成第二轮GSP认证且取得GSP证书的药品经营企业,无需开展现场验收检查。在换发的《药品经营许可证》上将自动核减“蛋白同化制剂、肽类激素”经营范围。 已换发《药品经营许可证》的药品经营企业,可按《药品经营许可证(批发)、药品GSP(批发)证书变更审批》程序向省食品药品监督管理局提出核减“蛋白同化制剂、肽类激素”经营范围申请,同时交回《蛋白同化制剂、肽类激素经营资格批件》原件。 二、药品生产、批发企业销售含特殊药品复方制剂时,销售、采购、验收入库等工作必须指定专人负责,必须确保药品送达购买方《药品经营许可证》所载明的仓库地址、药品零售企业注册地址,或者医疗机构的药库。如托运含特殊药品复方制剂必须选择当地有资质、信誉好且较大型的物流公司作为相对固定的承运单位,在签托运合同前必须对承运单位的有关资质、承运能力、运输安全等情况进行详细的考察,将考察材料与合同存档备查。承运单位必须将承运的含特殊药品复方制剂直接送至收货单位《药品经营许可证》登记的仓库地址。药品送达后,购买方应查验货物,无误后由入库员在随货同行单上签字。随货同行单原件留存,复印件加盖购买方公章或验收专用章后及时返回销售方存档。 三、各市药品监管部门应加强对含特殊药品复方制剂销售行为的监督检查。一是加强对药品生产企业的日常检查,严格审查复方制剂生产所需特殊药品原料药的购入、贮存、使用情况,跟踪核实含特殊药品复方制剂的销售流向;二是加强对药品经营企业购销含特殊药品复方制剂的跟踪检查,重点核查含特殊药品复方制剂的购进、进货验收、销售流向、资金流向等情况。如发现药品生产企业违规生产、销售含特殊药品复方制剂,应及时通报当地公安机关和省局。
各药品生产经营企业
公告 各药品生产经营企业: 根据《云南省曲靖市第十次暨第七届电子商务药品集中竞价招标采购〈招标文件〉》,经2007年10月30日上午曲靖市药品医疗设备招标采购中心会议研究决定,现将云南省曲靖市第十次暨第七届电子商务药品招标采购的中标药品配送中标企业及相关事项公告如下: 一、本次中标药品配送中标企业名单: 参加此次药品招标采购中标药品数前15家企业拟为本次中标药品配送中标企业。具体名单如下: 1、云南省医药有限公司 2、云南靖兴药业有限公司 3、昆明健宇医药有限公司 4、云南药品有限公司 5、云南医药工业股份有限公司 6、曲靖市康桥医药有限责任公司 7、昆明东盛医药有限公司 8、曲靖俊伟药业有限公司 9、曲靖市云康药业有限公司 10、云南双鹤医药有限公司 11、云南云珊医药有限公司
12、云南一诚医药有限公司 13、云南省久泰药业有限公司 14、云南昊邦医药销售有限公司 15、云南吉鸿麟医药器械有限公司 二、相关事项: (一)以上15家中标药品配送中标企业,请于2007年10月31日上午11:30点前将书面申请及书面承诺送曲靖市药品医疗设备招标采购中心,书面申请及书面承诺分别提供,并盖具单位公章。过时未交者,视为自动放弃。 (二)15家中标药品配送中标企业,请于2007年10月31日下午3:00点到曲靖市卫生局六楼会议室开会,研究有关事宜。 (三)15家中标药品配送中标企业书面承诺应包括的主要内容: 1、保证严格遵守《中华人民共和国招标投标法》及国家有关法律、法规。 2、保证按购销合同规定,按时、按质、按量对市、县(市区)、乡(镇)医疗机构进行药品配送。急救药品4—8小时内送到;一般药品12—36小时内送到,节假日照常配送。不论医疗机构采购药品规模大小如何、不论医疗机构远近均保证配送。 3、配送的药品的剩余有效期必须占药品有效期的一半以上。 4、保证接受转配送,并负责对所有转配送药品在全市区域内进行配送。
胶囊剂的制备
胶囊剂的制备 一、实验目的和要求 1.掌握硬胶囊剂的制备过程及手工填充硬胶囊的方法。 2.能进行硬胶囊剂的装量差异检查。 二.实验原理 胶囊剂系指药物或加有辅料充填于空心胶囊或密封于软质囊材中制成的固体制剂。主要供口服用,也可用于直肠、阴道等。空胶囊的主要材料为明胶,也可用甲基纤维素、海藻酸盐类、聚乙烯醇、变性明胶及其他高分子化合物,以改变胶囊的溶解性或达到肠溶的目的。根据胶囊剂的硬度与溶解和释放特性,胶囊剂可分为硬胶囊与软胶囊、肠溶胶囊和缓释胶囊。硬胶囊剂的一般制备工艺流程为: 空胶囊与内容物准备→充填空胶囊→质量检查→包装 1.空胶囊与内容物准备 空胶囊分上下两节,分别称为囊帽与囊体。空胶囊根据有无颜色,分为无色透明、有色透明与不透明三种类型;根据锁扣类型,分为普通型与锁口型两类;根据大小,分为000、00、0、1、2、3、4、5号八种规格,其中000号最大,5号最小。 内容物可根据药物性质和临床需要制备成不同形式的内容物,主要有粉末、颗粒和微丸三种形式。 2.充填空胶囊 大量生产可用全自动胶囊充填机充填药物,填充好的药物使用胶囊抛光机清除吸附在胶囊外壁上的细粉,使胶囊光洁。 小量试制可用胶囊充填板或手工充填药物,充填好的胶囊用洁净的纱布包起,轻轻搓滚,使胶囊光亮。 3.质量检查 充填的胶囊进行含量测定、崩解时限、装量差异、水分、微生物限度等项目的检查。 胶囊剂的装量差异检查方法:取供试品20粒,分别精密称定重量后,倾出内容物,硬胶囊用小刷或其他适宜的用具拭净;再分别精密称定囊壳重量,求出每粒内容物的装量(M1)与平均装量(M2),装量差异=M1-M2/M2。按规定,超出装量差异限度的不得多于2粒,并不得有1粒超出限度1倍。 胶囊剂装量差异限度
2014版四川省药品生产企业名录469家
2014版四川省药品生产企业名录469家
34四川凯京制药有 限公司 刘楚 言 陈中 燕 有限责任公司 (台港澳与境 内合资) 四川省眉山市彭 山县城南经济开 发区 片剂、颗粒剂、硬胶囊剂、丸剂(糊丸、大蜜丸、浓缩 丸、水丸)(含中药前处理提取)、原料药(柠檬烯)、 中药饮片(净制、切制、炒制、煅制、蒸制、烫制、煮 制、燀制、酒制、醋制、盐制、姜汁炙、油炙、蜜炙) *片剂、颗粒剂、硬胶囊剂(含中药前处理提取)* 川 20100152 HabZ bY 2014/1/21 2015/12/31 35成都金江制药有 限公司 付常 清 付常 清 自然人出资有 限责任公司 成都市双流县黄 水镇杨公村 原料药(葛根素、胆酸钠、黄芩苷、猪去氧胆酸、胆酸) * 川 20100371 Ha 2011/1/1 2015/12/31 36四川辰龙制药有 限公司 张红 波 冷钊 莹 其他有限责任 公司 眉山市东坡区大 石桥 原料药(盐酸洛非西定)、片剂、硬胶囊剂、颗粒剂、 栓剂、散剂、酊剂、合剂、丸剂* 川 20100372 HabZ b 2012/1/4 2015/12/31 37四川子仁制药有 限公司 李昌 华 高传 敬 有限责任公司 广汉市深圳路西 三段 颗粒剂、片剂、丸剂、硬胶囊剂(含中药前处理提取)、 原料药(谷氨酸诺氟沙星、兰索拉唑、炎琥宁、埃索美 拉唑钠、盐酸度洛西丁、埃索美拉唑钠、盐酸度洛西丁) * 川 20100373 HabZ b 2011/1/1 2015/12/31 38四川省迪威药业 有限责任公司 张德 超 张德 超 有限责任公司 (自然人投资 或控股) 四川省资中县重 龙镇迪威路1号 酊剂(外用)(含中药前处理提取)、片剂、硬胶囊剂、 颗粒剂、糖浆剂、合剂、软膏剂、栓剂、搽剂* 川 20100255 Zb 2013/12/30 2015/12/31 39四川省营山县景 弘中药饮片厂 全春 平 全春 平 私有 营山县三星工业 经济区北干道南 侧 中药饮片 (净制、切制、炒制、烫制、煅制、制炭、蒸 制、煮制、炖制、燀制、酒制、醋制、盐制、姜汁炙、 蜜炙、煨制、油炙)* 川 20100036 Y 2011/1/1 2015/12/31 40四川康定金珠制 药有限责任公司 张燕 李永 光 有限责任公司康定县姑咱镇片剂、丸剂、煎膏剂(膏滋)* 川 20100037 Zb 2013/7/30 2015/12/31 41四川御鼎堂中药 饮片有限公司 王颖 群 王颖 群 有限责任(公 司) 四川省汉源县甘 溪坝工业园区 中药饮片(净制、切制、炒制、烫制、煅制、制炭、蒸 制、煮制、炖制、燀制、酒制、醋制、盐制、姜汁炙、 蜜炙、油炙、制霜、水飞、煨制)、毒性饮片(净制、 切制、炒制、烫制、蒸制、煮制、醋制、姜汁炙)* 川 20120424 Y 2012/2/23 2015/12/31 42四川峨边荣成气 体有限公司 杨荣 成 杨荣 成 有限责任公司 峨边县沙坪镇核 桃坪工业区 医用气体(液态氧)* 川 20110422 Q 2011/12/28 2015/12/31 43四川绵阳万利兴 企业有限公司 任伟 陈文 开 有限责任公司 (自然人投资 或控股) 绵阳市高新开发 区永兴工业区 中药饮片(净制、切制、蒸制)* 川 20100395 Y 2011/1/1 2015/12/31 44成都康弘生物科 技有限公司 柯尊 洪 陈粟 有限责任公司 (法人独资) 成都市金牛区蜀 西路36号 生物工程产品(重组人血管内皮生长因子受体-抗体融 合蛋白注射液、康柏西普眼用注射液)* 川 20110400 S 2014/3/12 2015/12/31
车间工艺课程设计说明书,胶囊剂工厂设计,制药工程课程设计说明书
中南大学 CENTRAL SOUTH UNIVERSITY 制药工程设计 题目年产2.5亿粒胶囊生产车间工艺设计学生姓名 学号 指导教师 学院 专业班级 2010年12月
制药工程设计任务书 专业班级学号姓名 设计题目:年产2.5亿粒胶囊(硬胶囊)生产车间工艺设计 设计时间:2010.11.22-2010.12.10 指导老师: 设计内容和要求: 1.确定工艺流程及净化区域划分; 2.物料衡算、设备选型(按单班考虑、片重按0.5g计;要求有湿法制粒 铝塑包装)。 3.按GMP规范要求设计车间工艺平面图; 4.编写设计说明书。 设计成果: 1.设计说明书一份。包括工艺概述、工艺流程及净化区域划分说明、物料衡算、工艺设备选型说明、工艺主要设备一览表、车间工艺平面布置说明、车间技术要求; 2.工艺平面布置图一套(1#图纸); 3.工艺管道流程图
目录 第1章硬胶囊剂生产工艺概述..................................................................... 错误!未定义书签。 1.1 项目概述............................................................................................ 错误!未定义书签。 1.2 设计依据............................................................................................ 错误!未定义书签。 1.3 设计内容............................................................................................ 错误!未定义书签。 1.4 设计指导思想和设计原则................................................................ 错误!未定义书签。第2章生产方法及工艺流程......................................................................... 错误!未定义书签。 2.1生产制度、规模及包装方式............................................................. 错误!未定义书签。 2.1.1 生产制度、规模................................................................... 错误!未定义书签。 2.1.2 包装形式............................................................................... 错误!未定义书签。 2.1.3工艺流程制定的原则............................................................ 错误!未定义书签。 2.2 生产工序............................................................................................ 错误!未定义书签。 2.3 工艺流程............................................................................................ 错误!未定义书签。第3章物料衡算............................................................................................. 错误!未定义书签。第4章生产设备选型..................................................................................... 错误!未定义书签。 4.1 生产设备选型的步骤........................................................................ 错误!未定义书签。 4.1.1 生产设备选型依据............................................................... 错误!未定义书签。 4.1.2 制药设备GMP设计通则的具体内容................................... 错误!未定义书签。 4.1.3生产设备选型说明................................................................ 错误!未定义书签。 4.2 主要生产设备选型............................................................................ 错误!未定义书签。第5章车间(设备)布置............................................................................. 错误!未定义书签。 5.1 车间设计原则.................................................................................... 错误!未定义书签。 5.2车间平面布置.................................................................................... 错误!未定义书签。 5.2.1车间布置平面图.................................................................... 错误!未定义书签。 5.2.2车间产尘的处理.................................................................... 错误!未定义书签。 5.2.3车间排热、排湿及臭味的处理............................................ 错误!未定义书签。 5.2.4参观走廊的设置.................................................................... 错误!未定义书签。 5.2.5 安全门的设置....................................................................... 错误!未定义书签。 5.3设备的安装........................................................................................ 错误!未定义书签。第6章采暖通风与空调公用工程................................................................. 错误!未定义书签。 6.1 设计要求........................................................................................... 错误!未定义书签。 6.2 设计参数........................................................................................... 错误!未定义书签。 6.3洁净室换气次数................................................................................ 错误!未定义书签。 6.4 洁净室压力........................................................................................ 错误!未定义书签。 6.5正压风量的计算................................................................................ 错误!未定义书签。 6.6 噪声................................................................................................... 错误!未定义书签。 6.7 通风量............................................................................................... 错误!未定义书签。第7章结束语................................................................................................. 错误!未定义书签。第8章参考文献............................................................................................. 错误!未定义书签。
