零部件检验单
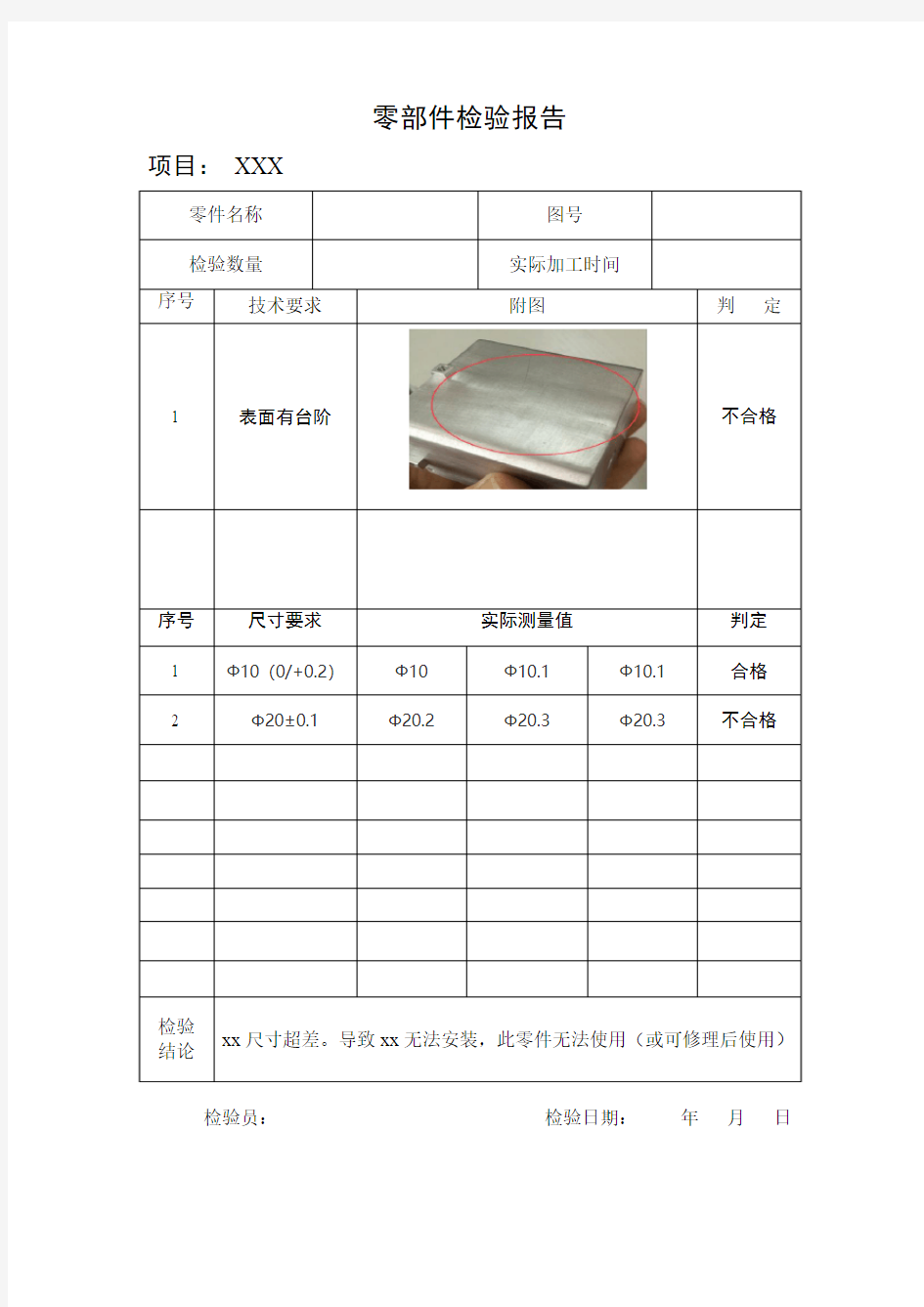
零部件检验报告
项目:XXX
检验员:检验日期:年月日
材料零部件控制程序
1.目的 根据《特种设备制造、安装、改造、维修质量保证体系基本要求》、公司《压力管道安装、改造、维修质量保证手册》的要求,建立材料、零部件质量控制系统,通过对材料、零部件的采购、验收、标识、存放与保管、领用和使用、材料代用等环节的管理和控制,以确压力管道安装、改造、维修用的材料、零部件的质量和正确使用。 2.适用范围 适用于公司压力管道安装、改造、维修工程所用材料、零部件的全过程控制。 3. 职责 3.1 工程技术部 a).工程室 ①.物资采购组:负责收集合格分供方的评审的输入资料和材料、零部件的采购。 ②.库房:负责材料、零部件的标识、保管、发放和回收。 b).技术室:负责编制订货技术条件和参与合格分供方评审,并对分供方的技术能力提 出合理意见。 c).项目组:负责材料、零部件的使用和参与合格分供方评审,并对分供方的综合服务 能力提出合理意见。 3.2 质量安全部 a).质量室:参与合格分供方评审,并对分供方的质量保证能力提出合理意见。
b).检验试验组:负责材料、零部件的验收。 3.3 运营管理部 财务室:参与合格分供方评审,并对分供方的经济保证能力提出合理意见。 4. 程序 4.1 合格分供方评价 4.1.1 评价范围 为公司压力管道安装、改造、维修工程提供设备、材料、零部件的所有制造商、生产商、贸易商和外协加工商。 4.1.2评价类型 合格分供方评价分为准入评价和重新评价两种类型。 4.1.3 准入评价 4.1.3.1准入评价时机 a).材料、零部件分供方拟为公司供货前。 b).拟在合格分供方名录外分供方采购时。 4.1.3.2 准入评价内容 a).分供方合法性评价 ①.分供方必须是依法成立的企业、个体工商户或其他组织。
原材料零部件进厂检验制度
原材料、零部件入库检验办法 为加强原材料、外协件、外购件、零部件的入库验收管理,不断完善原有的入库验收制度,现对我公司作如下规定,望公司相关部门严格遵照执行:1.抽样方法 对于原材料、外协件的入库验收不进行抽样检验,均进行全数验收;对于外购件、零部件则进行随机抽样检验 2.抽样数量 对于原材料、外协件的入库验收不进行抽样检验,均进行全数验收;外购件、零部件的抽样数量为入库量的30%,另外,入库量在10以内(包括10)则进行全数验收,当入库量超过10,但是按30%算出的抽样量不达到10的,则按10的抽样量进行抽样验收 3.检查项目 (1)传感器入库验收检查项目包括:外观、包装、产品完整性、合格证书、输入电阻及输出电阻共六项,在入库验收单上应注明进库时间、供货单位、品种、规格、产地、入库数量、抽检数量及编号、存放地、验收人、验收时间 (2)仪表入库验收检查项目包括:外观、包装、产品完整性、合格证书、通电是否正常共五项,在入库验收单上应注明进库时间、供货单位、品种、规格、产地、入库数量、抽检数量及编号、存放地、验收人、验收时间(3)接线盒入库验收检查项目包括:外观、包装、产品完整性、合格证书共四项,在入库验收单上应注明进库时间、供货单位、品种、规格、产地、
入库数量、抽检数量及编号、存放地、验收人、验收时间 (4)钢材入库验收检查项目包括:材料的规格(包括厚度、长度、宽度)、种类、产地、数量、是否有材质报告共五项,在入库验收单上应注明进库时间、供货单位、运输单位、品种、规格、产地、入库数量、抽检数量、存放地、验收人、验收时间 4.检查方法及检查条件 原材料、外协件、外购件、零部件入库验收的检查条件(即前提)是供货商所出具的供货清单上所列物品与我公司的订货清单所列物品一致;具体的检查方法是:按照订货清单所列物品名称、规格型号检查物品是否相符,再检查物品的出厂合格证所列规格型号与实物是否一致,最后按照物品的出厂合格证或说明书上所列的技术数据进行相关检验 5.检验设备/仪器 原材料、外协件、外购件、零部件入库验收的检验设备/仪器主要有:卷尺、模拟器、万用表 6.检验报告的样式 检验报告的样式详见《传感器进库验收单》、《仪表进库验收单》、《接线盒进库验收单》、《钢材进库验收单》,进库验收单的格式及检验项目可根据实际需要而稍作改动 7.合格判断原则 供货清单与订货清单所列项目一致;产品包装与实物一致;合格证所标的名称、型号、规格及相关的技术数据与实物一致,则为合格,只要有一项不一致均为不合格
关键零部件和材料检验及定期确认控制程序
关键零部件和材料检验及定期确认控 制程序 1 目的 通过对关键零部件和材料的检验和验证控制管理,确保产品质量的一致性和稳定性。 2 范围 适用于所有认证产品的关键零部件和材料。 3 职责 所有认证产品的关键零部件和材料检验由质检部门门负责。 4 程序内容 4.1检验或验证的确定 4.1.1关键零部件和材料进厂时,由仓库通知质检部门门检验。 4.1.2质检部门门应及时安排检验人员对关键零部件和材料要按零部件和材料“检验规范”进行检验或验证。 4.1.3经使用质量稳定及本厂暂无能力进行检查的关键零部件,每次进货时应验证并保留其产品的出厂合格证。每季度要求其提供1份符合其制造标准要求的检验报告。 4.1.4质检部门门应确认在强制性认证范围内的关键零部件的型号、规格、主要参数、品牌、外包装使用是否与要采购相符,不得随意替换。 4.2 正常检验和验证 仓管员核实进料的采购单上的名称、数量、型号规格等无误后将进料放在待检验区域,交质检部门门指定的质检员签收。
质检员确认进料是否与订单、物料清单之规格是否相符。检验和试验完毕,检验员将检验和试验的具体内容(外观、计测、试验等)填写于相应之《关键原材料和零部件进厂检验记录表》表中,并对检验和试验结果进行合格与不合格判定,交主管审核。 4.3 定期确认检验 4.3.1检测项目 参见相关支持性文件的检测项目规定。 4.3.2定期确认的频次 每年进行了一次定期确认。 4.3.3定期确认的方法 要求具有3C认证、出口许可证或质量安全认证的安全件的供应商提供每年通过的复查报告或其产品确认检验报告,对非获得认证的关键件要求供应商按相关产品国家标准检测并提供确认检验报告。 4.3.4定期确认结果评定 由本厂质检部门进行确认,符合产品各项指标的,继续保持《合格供应商管理名录》。不符合指标的,取消其供应商资格,重新选择供应商。 4.3.5对供应商的确认报告或工厂复查报告要归档保存(至少两年)。 5 表格记录 《关键原材料和零部件进厂检验记录表》 《关键原材料和零部件定期确认检验记录表》
材料及建筑成品检验检测规定(送检)
材料及建筑成品检验检测规定 序号项目名称证明文件送检规定送检数量 1 水泥1、产品合格证 2、出厂物理性能抽 检报告 3、建筑材料放射性 指标检验报告 4、物理性能进场后 检验报告 (水泥进场要收集的 前面3种文件) 取样批量:同一水泥生 产厂、同期出厂、同一出厂编号 及同强度的水泥: (1)散装水泥:≤批 /500t; (2)袋装水泥:≤批 /200t; (3)当对水泥质量有怀疑或 存放期超过三个月(快硬硅酸盐 水泥超过一个月)必须复检。 做到先检验后使用,严禁先施工 后检验 (备注:28天有检测结果,有施 工可否使用,但此资料不能存 档,28天的才能存档) 20个以上不同部位取 等量样品不小于 12kg。 2 1、钢筋 2、预应钢 筋 3、钢绞线 4、钢丝 1、产品合格证 2、出厂抽检报告 3、力学及工艺性能 检验报告 (钢筋只有一份产品 质量证明书) (圆钢即直径是6.5、 8、10,其送检不能 是 加工后的,是刚入场 时,是圆形时就要剪 下来送检了) 同一生产厂、同一炉罐号、同一 规格、级别、同一交货状态及同 一进场时间的钢筋: (a)热轧带肋、光圆钢筋、低 碳钢热轧圆盘条及余热钢筋:≤ 60t/批。(工地用得最多的) (b)冷轧带肋钢筋:≤50t/ 批。 (c)钢筋焊接网应成批验收, 每批应由同一厂家生产的、受力 主筋为同一直径的焊接网组成, 重量不应大于20t/批 做到先检验后使用,严禁先施工 后检验 (备注:送检时,盘形条的钢筋 不能是加工后的直筋,应是弯 筋,即是圆钢筋,即是板筋、箍 筋,未加工过的,即未拉直就要 送检了) 拉伸L=200mm+10d (2支/组)(d是直径) 弯曲L=140mm+6.2d (2支/组)(d是直径) (备注:拉伸的要长弯 曲的钢筋长一些, 如: 拉伸: 弯曲: ) (例:直径12厘) 拉伸: L=200mm+10*12 =200+120 =320mm 弯曲: L=140mm+6.2*12 =140+74.4 =214.4mm
医疗器械检查记录表精选范文
附件2 医疗器械生产企业日常监督检查表 企业名称: 条款检查内容及要求检查方式检查情况备注 生产企业许可证有效性1.生产企业许可证有效性 查看生产现场,核对企业工商营业执照与生产企业 许可证内企业名称、注册地址、生产地址一致性。 2.所生产产品是否与许可证核发 的产品范围相符合 查看企业生产现场,成品库房、销售台帐、与企业 许可证核定范围进行核对。 3.企业生产、质量管理人员有无 变化 查看企业人员名单,核对企业工商营业执照和生产 企业许可证内法人代表与负责人姓名的一致性。 4.企业管理层人员是否经过医疗 器械法规的培训 查看培训证书(各级食品药品监督管理部门或企业 内部培训)。 5.三类医疗器械生产企业是否有 内审员 查看证书。 生产条件的符合性检查1.生产、组装能力是否具备,设 备能否正常工作,维护保养是否 在有效期内 查看生产现场,看是否配备完成该工艺的生产设 备,核对企业工艺要求及设备维护保养记录。2.生产现场是否管理有序 查看现场及企业是否按产品注册标准的要求进行 生产,并查看是否制定了生产过程控制和管理文 件。 3.生产场地环境、照明是否与其 生产的产品及规模相适应 查看生产现场环境与照明情况,并查看环境监测记 录,查看生产面积是否拥挤。注:一次性无菌医疗 器械生产现场应符合《无菌医疗器具生产管理规
范》(YY0033)的要求。 医疗器械生产企业日常监督检查表 条款检查内容及要求检查方式检查情况备注 4.《生产实施细则》执行情况;有专项要求的,是否符合相应的《生产实施细则》的要求查看生产现场与生产记录是否符合相应的实施细则。尤其是生产输液器、注射器等一次性使用无菌医疗器械是否符合《一次性使用无菌医疗器械产品(注、输器具)生产实施细则》;生产外科植入物的是否符合《外科植入物的生产实施细则》。 5.原材料、外协件和外购件等采购产品是否符合规定要求检查企业供方的评审记录。原材料、外协件和外购件的采购检验记录,采购合同/技术协议是否符合该产品的质量要求,检查物资供应方的资质证明,尤其是原材料必须是有医疗器械注册证的(如义齿等),要注意检查相关资质证明。 6.生产过程的控制,在产品形成过程中,是否有清晰的状态标识和可追溯标识检查企业生产工艺的验证报告(或记录)。检查生产过程的记录,按生产批号能否追溯到产品原材料的批号、每批产品关键工序及特殊过程的控制情况、每批产品生产过程中有关设备、人员情况和质量记录。 出厂检验记录1.检验设备的配置是否能够覆盖 标准中所规定的出厂检验项目。检 验人员是否经过培训持证上岗 查看检验现场,检验设备清单,查验出厂检验报告 (与注册产品标准的要求核对)查看检验人员的上 岗证及相关的证明培训记录。 2.企业是否对检验设备(含计量器 具)的管理建立制度 查检验设备管理制度,应包括采购、入库、首次检 定、使用保养、周期检定及停用报废等内容。 3.检验设备的精度是否符合检验 要求,检验记录是否真实有效,出 查看(技术监督局)检定合格证是否在有效期内, 查看检验设备上的检定标签是否在有效期内,查看
汽车零部件和材料进货检验、验证及定期确认管理程序
零部件和材料进货检验、验证及定期确认管理程序 1范围 本程序规定了本公司对所采购的零部件和材料的检验或验证,以及关键零部件的定期确认的工作程序,明确了在零部件和材料管理中各职能部门的工作职责和权限; 本程序适用于本公司生产中所需所有连续批供货的零部件和原材料的检验或验证。 2 职责 2.1.采购中心供应商质量管理部负责本程序的归口管理与组织实施; 2.2.1供应商质量管理部负责编制《外购(件)检验指导表》; 2.2.2供应商质量管理部负责连续批供货的国内零部件和原材料的检验或验证; 2.2.3 供应商质量管理部负责关键零部件的定期确认。 2.2 物管部负责零部件和材料的到货确认。 2.3 物管部负责根据供应商质量管理部的检验单办理零部件入库手续。 2.4 物管部负责外购(协)零部件和材料的送检工作。 4 程序内容 4.1供应商质量管理部依据产品图纸、标准、检查基准书、样件、《采购物资分类一览表》、《安全性零部件清单》、《关键零部件清单》等分类编制《外购(件)检验指导表》。 4.2检验员资格 按质量控制点设立专职检验员,专职检验员必须通过有关程序要求的技术培训并取得资格证书。 4.3 零部件、原材料在开发阶段的检验与验证按QG/GACCF 01.130-2007《供应商准入管理程序》中的有关规定实施。 4.4 送检 4.4.1 外购(协)件进货后,由物管部门负责分类分批存放在待检或指定地点,做好标识。 4.4.2同一批进货、同一规格的外购(协)件为一个检查批次送检。 4.4.3外购(协)件进货后,物管部门应先对其进行初步验收,内容包括:
a) 清点数量,查看包装有无明显破损; b) 查证供方是否按要求提供了符合要求的《出厂检验报告》。 4.4.4 通过初步验收的外购(协)件,由物管部门填写《外购(协)件送检单》(书面或电子表格),向供应商质量管理部送检,同时应提交供方提供的《出厂检验报告》; 4.5检验或验证 4.5.1 供应商质量管理部检验员接到《外购(协)件送检单》后,如无特殊情况(须进行性能试验确认),应于2个工作日内完成产品检验或验证; 4.5.2进口KD件的检验或验证 a) 进口KD件由物管部门进行验证,在包装未破损,规格、型号、数量、批次号与送检单相符, 具有合格证或产品出厂检验报告的情况下即认为验证合格; b) 对于进口KD件中属于《低污染排放小汽车生产一致性保证计划》所规定的外购(协)件范畴的 零部件、属于“3C”认证范畴的关键零部件以及召回管理中的安全性零部件,由物资管理部向供应商质量管理部送检,供应商质量管理部检验员应按检验文件的规定实施检验、试验或验证。 4.5.3 国产零部件的检验或验证。 4.5.3.1检查阶段划分 a) 初期检查阶段指零部件刚开始正式批量供货但尚未转入定期检查前的阶段,或者零部件 出现问题,经整改后重新批量供货但尚未转入定期检查前的阶段。 b) 定期检查阶段指的是零部件开始正式批量供货或经整改后重新批量供货,在连续批质 量稳定的情况下,本公司认为可以放宽检查的阶段。 4.5.3.2转移规则 a) 零部件在连续10批质量稳定的情况下,可由供应商质量管理部部品检验科填写《国产 零部件定期检查申请单》,经供应商质量管理部部长审核批准后转入定期检查阶段; b) 处于定期检查阶段的零部件,若在检验或验证过程中有一批产品判为不合格,则从下 批供货起自动转入初期检查阶段; 4.5.3.3 检验或验证 a) 对原材料、各种辅料进行包装、规格、型号、数量、批次号、合格证、产品出厂检验报告的验 证; b) 检验员应根据零部件所处的检查阶段,按照外购(协)检验指导表中所列的样本大小和检验要 求随机抽样进行检验、试验或验证; c) 所有未特殊注明的检验项目统一实行零缺陷判定,若发现缺陷,检验员应立即将情况上 报供应商质量管理部。 4.6检验记录与标识 4.6.1 产品批检验完成后,由库房检验员填写《入库检验单》,上报供应商质量管理部审核; 4.6.2检验员对已检产品的状态进行标识; 4.6.3所有检验记录由检验员应按关键零部件、安全性零部件进行分类整理、汇总、保存至当年年底,每年一月15日前将上一年度的检验记录报品保部部品科归档,其保存期按QG/GACCF 01.106-2007《体系运行记录管理程序》中之规定执行; 4.6.4部品检验科每月应组织一次对检验记录的完整性和规范性检查。 4.7入库手续 4.7.1 物管部门根据供应商质量管理部审核后的《入库检验单》上实际合格数量办理入库手续。 4.7.2对于让步或紧急放行的零部件,按《采购过程管理程序》中有关条款的要求处理后,可以办理入库手续。 4.8 不合格品处置 零部件检验或验证、以及生产线使用过程中发现的不合格品,按照QG/GACCF 01.156 —2007《不合格品控制程序》中的有关条款进行处置。
成品检验管理表格
盐城永胜蛋白饲料有限公司 成品检验管理表格 一、产品质量报告表 名称规格设计号业务号数量客户不合 格原 因检 查 车间主任不 合 格 内 容 说 明 不合格项目规格检验结果 不合 格原 因分 析及 改进 对策技术科长 车间主任厂长 批示 质 量 管 理 主 任 主管组长 二、产品质量检验表
第四十章 成品检验管理表格 387 制造 号码 产品 名称 生产数量 生产日程 月 日 至 月 日 工程名称 检验项目 上限 下 限 抽 查 记 录 次 时间 1 2 3 4 5 次 时间 1 2 3 4 5 次 时 间 1 2 3 4 5 三、产品质量抽查记录表 机器名称: 班别: 抽查时间 抽查项目 1 2 3 4 5 6 7 8 9 10 平均 标准 时分 时分 时分 时分 时分 时分 时分 时分 时分 时分 备 注 主管: 抽查员: 四、产品质量改进记录表 编号:
产品名称规格 管理项目原质量 标准 更改后 标准 变动 原因 交办 日期 完成 日期 变动因素 改进结果 制程设备材料操作技术 五、质量改进因素记录表 产品名称:产品规格:编号: 质量改进事项日期改进 结果 改进结果 比较 变动因素统计 项目细 目 编 号 内 容 交 办 完 成 结 果 改 进 费 用 改 进 前 改 进 后 差 异 制 造 条 件 操 作 标 准 控 制 基 准 原 料 改 进 设 备 改 进 技 术 性 作 业 水 平 填表:填表日期: 六、产品质量改进分析表 编号: 388
第四十章 成品检验管理表格 389 产品名称 规格 检验产品 目前水准 目标水准 产品质量分析图 原因分析 目前水准 拟变更 现状检查 改进对策 经办单位 主管批示 分析者 七、产品质量改进通知单 改进单位 改进项目 生产 过程 改变 项目 现况 改进方法 重点 批示 拟办 预定日程 月 方始 处理 结果 年 月 日以前 经办 完成 日期 经办 主管 批示 主管 批示 八、产品质量异常通知单 通知单位: 年 月 日
