血清总蛋白测定的基质效应评价

血清白蛋白和球蛋白的分析测定-盐析法
血清白蛋白和球蛋白的分析测定-盐析法 [目的与原理] 掌握血清白蛋白和球蛋白测定的原理和方法,并用盐析法测定水产动物血清中白蛋白和球蛋白 的含量。 血清中含有多种不同成分的蛋白质,主要为白蛋白和球蛋白。用盐析法沉淀血清中球蛋白,用 双缩脲法测定上清液中白蛋白,同时测定血清总蛋白。血清球蛋白的量从两者的差值求得。[试剂与器材] 试剂: 1、球蛋白沉淀剂:称取硫酸钠(Na2SO4)208g,及亚硫酸钠(Na2SO3)70g,加入蒸馏水约900ml,并加入浓硫酸2ml,使蒸馏水酸化。不停搅拌,待完全溶解后将溶液移入1L容量瓶内,用蒸馏水稀释至1L刻度。保存于25℃以上的温度中。 2、双缩脲试剂:溶解1.50g硫酸铜(CuSO4.5H2O)和 6.0g酒石酸钾钠(NaKC4H4O6.4H2O)于500ml蒸馏水中,在搅拌下加入300ml 10%氢氧化钠溶液,用水稀释到1000ml,贮存在内壁涂以石蜡的瓶中,此试剂可长期保存。 3、标准血清:将待测样品用0.05mol/L氢氧化钠配制成适当浓度的溶液(使测定值在标准曲线范围内),学生实验中可用酪蛋白配制或用血清样品稀释10 倍,冰箱存放待用。。 4、乙醚 器材: 可见分光光度计,离心机,试管若干及试管架,旋涡混合器,塑料试剂瓶,1L容量瓶,烧杯2个,吸管若干支,滤纸,擦镜纸。 [实验步骤] 1、准确吸取血清样本0.2ml,置于10×100mm试管内。以5ml刻度吸管加入球蛋白沉淀剂 3.8ml,塞住管口,反复倒转混和10次(不宜过多)。以1ml 刻度吸管吸取悬液1ml (相当于血清0.05ml),置于另一试管内,作为“总蛋白测定管”。剩余的混悬液另加乙醚约2ml,揿住管口,在约20 秒钟内颠倒混和40 次,然后经每分钟2500 转的速度离心沉淀 5 分钟。此时试管内分成三层:上层为乙醚,中层为球蛋白,下层为澄清的白蛋白溶液。将试管斜置在桌面片刻或轻击试管,待蛋白块自管壁分离后,将1ml吸管插入白蛋白溶液中并吸取此溶液1ml(小心,准确,且不可触及球蛋白块片)。取出吸管,用滤纸拭去管尖可能附着的球蛋白沉淀,将白蛋白溶液加入另一试管内,作为“白蛋白 测定管”。在另一试管内加入标准血清0.2ml及球蛋白沉淀剂 3.8ml,混和后准确吸取混悬液1ml,加入一试管中作为“标准管”。再取一试管加球蛋白沉淀1ml,作为“空白管” 2、每管中各加入双缩脲试剂4毫升,充分混和后置室温暗处30分钟,用540nm或绿色滤光片进行比色,以空白管校正光密度到0点,读取各管光密度读数。 3、计算 将所测得的光密度读数按下列公式计算出白、球蛋白含量及其比值: (1)总蛋白测定管光密度/ 标准管光密度×标准血清蛋白浓度(g/100ml)=血清总蛋白g/100ml (2)白蛋白测定管光密度/标准管光密度×标准血清蛋白浓度(g/100ml)=血清白蛋白g/100ml (3)血清总蛋白—血清白蛋白=血清球蛋白g/100ml (4)血清白蛋白÷血清球蛋白=血清白蛋白、球蛋白比值(A/G) 4、标准曲线绘制:同血清(浆)总蛋白测定双缩脲法见《血清(浆)总蛋白测定》。
EP14基质效应的评价
基质效应的评价 1.基质效应的初步认识 基质效应是指检测系统检测样品中的分析物时,处于分析物周围的所有非分析物质对分析物参与反应的影响。产生基质效应的原因与以下四个主要因素的相互作用密切相关:仪器的设计、试剂的组成成分、测试方法的原理、质控材料的组成及处理技术等。通过回收实验可以评估分析方法是否受基质效应的影响,而EP14A文件介绍的方法则是评估经过物理或化学方法处理过的样本在分析过程中是否存在基质效应。 2.基质效应评价的实验步骤 2.1 材料选择 本实验需要如下材料:①待评估检测系统:包括待评估方法的试剂、校准品及仪器系统等。②对比检测系统:包括对比方法的试剂、校准品及仪器系统等。用理想的对比方法检测处理过的校准品或控制品时,其基质效应应尽可能的小,因此可以选择如下方法作为对比方法:国际参考系统(National Reference System,NRSCL)的决定性方法,如胆固醇的同位素稀释质谱法;NRSCL的参考方法,如胆固醇的Abell-Kendall法;NRSCL认可设计的对比方法等。但是在实际实验过程中,选择上述方法作为对比方法并不是绝对要求,选择常用方法作为对比方法即可。③处理过的样本(processed samples):如待评估的控制品等。④20份新鲜的患者样本:其内含分析物浓度或活性的分布范围应覆盖处理过样本的分析物浓度或活性,但是这些样本不应包含已知含有某些干扰物的样本。此外,如果样本冷冻不影响待评估方法、对比方法的测定,则实验过程中也可以使用冷冻样本。 2.2 实验步骤 按如下步骤进行实验:①按产品说明书的步骤准备处理过的样本。②将处理过的样本随机排列在20份新鲜的患者样本之中,用待评估方法对患者样本、处理过的样本进行检测。再将上述过程重复2次,每个样本共得到3个结果。实验过程中最好将3批次的重复检测连续完成,因为这样可以减少结果漂移等对实验结论的影响。此外,每批检测前都应重新定标。 ③用对比方法对20份新鲜的患者样本、处理过的样本进行检测,步骤同上。④将20份患者样本和处理过的样本冷冻保存(最好是-70℃)以便进行后续研究,如果在数据分析中和分析后出现任何问题,则可用其他对比方法如NRSCL的决定性方法或参考方法检测这些样本。但是应该注意的是,冷冻可能导致粘蛋白、酶结构发生改变而引入基质效应。
体液免疫球蛋白测定
体液免疫球蛋白测定 第一节血清IgG、IgA、IgM测定 血清免疫球蛋白IgG、IgA、IgM定量测定方法一般有单向环状免疫扩散法、火箭免疫电泳法、ELlSA、免疫比浊法、放射免疫分析法等。临床常用单向环状免疫扩散法和免疫比浊法来测定血清免疫球蛋白含量。 一、血清IgG、IgA、lgM测定 (一)单向环状免疫扩散法 该法的原理是将抗血清均匀地分散于琼脂或琼脂糖凝胶内,胶板上打孔,孔内注入抗原或待测血清,抗原在含有抗血清的胶内呈放射状(环状)扩散,在抗原抗体达到一定比例时形成可见的沉淀环。在一定条件下,抗原含量越高,沉淀环越大。 (二)免疫比浊法 该法具有检测范围宽、测定结果准确、精密度高、检测时间短(一般在几分钟内即可完成测试)、敏感度高、稳定性好等优点。 二、血清IgG、IgA、IgM测定的临床意义 (一)年龄 新生儿可由母体获得通过胎盘转移来的IgG,故血液中含量较高,接近成人水平。 (二)免疫球蛋白IgG、IgA、IgM均升高 慢性肝脏疾病如慢性活动性肝炎、原发性胆汁性肝硬化、隐匿性肝硬化患者血清中可见3种Ig均升高。慢性细菌感染如慢性支气管炎、肺结核,血IgG可升高。宫内感染时脐血或出生后的新生儿血清中IgM含量可增高。SLE患者以IgG、IgA升高较多见。类风湿关节炎患者以IgM增高为主。 (三)单一免疫球蛋白升高 主要是指患者血清中某一类免疫球蛋白含量显著增多,大多在30g/L以上,这种异常增多的免疫球蛋白其理化性质十分一致,称为单克隆蛋白(MP)即M蛋白。此类异常增多的免疫球蛋白多无免疫活性,故又称副蛋白。由它所致的疾病称为免疫增殖病如多发性骨髓瘤、巨球蛋白血症、恶性淋巴瘤、重链病、轻链病等。 (四)免疫球蛋白降低 先天性低Ig血症,主要见于体液免疫缺陷病和联合免疫缺陷病。IgA缺乏患者,易发生反复呼吸道感染。IgG缺乏患者,易发生化脓性感染。IgM缺乏患者,易发生革兰阴性细菌败血症。 第二节血清IgD和IgE测定 正常人血清中IgD含量很低,仅占血清免疫球蛋白总量的0.2%。膜结合型IgD(mIgD)构成BCR,是B 细胞分化发育成熟的标志。未成熟的B细胞仅表达mIgM,成熟B细胞可同时表达mIgM和mIgD。活化的B 细胞或记忆B细胞其表面的mIgD逐渐消失。 IgE是正常人血清中含量最少的免疫球蛋白,要由黏膜下淋巴组织中的浆细胞分泌。其重要特征为糖含量高达12%。IgE为亲细胞抗体,可引起Ⅰ型超敏反应。IgE可能与机体抗寄生虫免疫有关。 第1页
血清总蛋白测定方法及临床意义
血清总蛋白测定方法及临床意义 1.测定方法血清总蛋白测定一般采用双缩脲比色法,它是目前首先推荐的蛋白质定量方法。此法的原理是蛋白质分子中的肽键在碱性条件下与二价铜离子(Cu2+)作用生成蓝紫色的化合物,这种颜色反应强度在一定浓度范围内与蛋白质含量成正比,经与同样处理的蛋白标准液比较,即可求得蛋白质含量。此反应的优点是清、球蛋的反应性相近,操作简单,重复性好,干扰物质少,为首选的常规方法,其缺点是灵敏度较低。 2.临床意义血清总蛋白生理性波动。直立体位由于体液分布原因,血液相对浓缩,而长久卧床者血液较直立体位稀。因此长久卧床者血清总蛋白比直立活动时约低3~ 5g/L。新生儿血清总蛋白可比成人低5~8g/L。60岁以上的老年人约比成人低2g/L。血清总蛋白增高:(1)血液浓缩,导致总蛋白浓度相对增高:严重腹泻、呕吐、高热时急剧失水,血清总蛋白浓度可明显升高。休克时,由于毛细血管通透性增加,血液中水分渗出血管。血液可发生浓缩,慢性肾上腺皮质功能减退的患者,由于丢失钠的同时伴随水的丢失,血浆也可出现浓缩现象。(2)血浆蛋白质合成增加:主要见于球蛋白合成增加,多发性骨髓瘤患者。血清总蛋白降低:(3)血液稀释,导致总蛋白浓度相对降低:如静脉注射过多低渗溶液或因各种原因引起的钠、水潴留。(4)摄人不足和消耗增加:食物中长期缺乏蛋白质或慢性胃肠道疾病所引起的消化吸收不良,因患消耗性疾病,如严重结核病,甲状腺功能亢进,恶性肿瘤等,均可造成血清蛋白浓度降低。(5)蛋白质丢失:严重烧伤时大量血浆渗出,大量失血,肾病综合征时大量蛋白尿,溃疡性结肠炎时肠道长期丢失一定量的蛋白质,这些病理改变均可使血清总蛋白浓度降低。
血清白蛋白ALB溴甲酚绿BCG法测定
血清白蛋白ALB溴甲酚绿BCG法测定 1.实验原理 在pH值4.2时,白蛋白和溴甲酚绿染料结合产生蓝绿色复合物,在630nm处比色,颜色的深度与白蛋白浓度成正比。 pH4.2 白蛋白+溴甲酚绿--------------绿色化合物 2. 标本采集 2.1 病人准备:无特殊要求。最好用禁食的标本以减少乳糜血的干扰。 2.2 类型:血清、肝素或EDTA血浆。 3. 标本存放留取标本后请尽快分离血清/血浆。在室温条件下(15~25℃)可以稳定一周,在冰箱保存的条件下(2~8℃)稳定一个月,-20℃保存至少可以稳定3个月。 4. 标本运输室温条件下运输 5. 标本拒收标准:细菌污染的不能做测定。
6. 实验材料: 6.1 上海奥林巴斯白蛋白测定试剂盒 6.1.1 试剂准备:试剂为即用式。 6.1.2 试剂稳定性与贮存:试剂避光保存于2~25℃,若无污染,可稳定至失效期。试剂有效期为24个月。试剂不可冰冻。开盖后应避免污染。 6.1.3 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。 6.1.4 注意事项:避免试剂与皮肤及粘膜接触。 6.2 校准品:参见生化检验校准品和质控品.SOP文件 6.3 质控品:参见生化检验校准品和质控品.SOP文件 7. 仪器:奥林巴斯AU2700生化分析仪 8. 操作步骤 8.1 项目基本参数:参见生化检验奥林巴斯AU2700生化分析仪项目测定参数.SOP文件 8.2仪器操作步骤:参见生化检验奥林巴斯AU2700生化分析仪操作规程.SOP文件 9. 检验结果的判断与分析
10. 质量控制:在每一批标本中都应把非定值血清水平I 与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。质控规则参见生化室室内质控操作规程.SOP文件。 11. 计算方法:以TruCal U复合校准品白蛋白校准值或标准品标准值校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果。手工测定计算方法为: Au 白蛋白(g/L)= ×校准液浓度 As 12. 参考值范围 成人35~52g/L 参考值因性别、年龄、饮食和地域的不同而有所差别。根据好的实验室经验,每个实验室应建立自己的参考值。 13. 临床意义:白蛋白是血浆中多种物质重要的结合与运输蛋白,并是维持血浆渗透压的主要组分。血清白蛋白可用于众多疾病的诊断。血清白蛋白升高通常见于脱
血清总蛋白和白蛋白测定实验方案
血清中总蛋白和白蛋白测定的实验方案 血清总蛋白的测定: 实验原理 血清(浆)中蛋白质的肽键(-CO-NH-)在碱性溶液中能与2价铜离子作用生成稳定的紫红色络合物。此反应和2个尿素分子缩合后生成的双缩脲(H2N-OC-NH- CO-NH2)在碱性溶液中与铜离子作用形成紫红色的反应相似,故称之为双缩脲反应。这种紫红色络合物在540nm处有明显吸收峰,吸光度在一定范围内与血清蛋白含量呈正比关系,经与同样处理的蛋白质标准液比较,即可求得蛋白质含量。实验器材分光光度计 实验试剂 1.6mol/L NaOH溶液称取NaOH 240g,溶于新鲜制备的蒸馏水约800ml中,定容至1L,贮于有盖塑料瓶中。 2.双缩脲试剂称取硫酸铜结晶(CuSO4·5H2O)3g溶于新鲜制备的蒸馏水500ml 中,加入酒石酸钾钠(NaKC4H406·4H2O),用以结合Cu2+,防止CuO在碱性条件下沉淀)9g和KI(防止碱性酒石酸铜自动还原并防止Cu2O的离析)5g。待完全溶解后,在搅拌下加入6mol/L NaOH溶液100ml,并用蒸馏水定容至1L,置塑料瓶中盖紧保存。此试剂室温下可稳定半年,若贮存瓶中有黑色沉淀出现,则需要重新配制。 3.60~70g/L蛋白质标准液可用定值参考血清或标准白蛋白作标准。 实验操作 取试管3支,混匀,置25℃30min或37℃10min,在波长540mm处比色,用空白管调零,测各管吸光度。 参考范围 60~80g/L。 注意事项 1.黄疸血清,严重溶血,葡萄糖,酚酞及溴磺酞钠对本法有明显干扰,故用标本空白管来消除。但如标本空白管吸光度太高,可影响测定的准确度。
2.高脂血症混浊血清会干扰比色,可采用下述方法消除:取2支带塞试管或离心管,各加待测血清0.1ml,再加蒸馏水0.5ml和丙酮10ml,塞紧并颠倒混匀10次后离心,倾去上清液,将试管倒立于滤纸上吸去残余液体。向沉淀中分别加入双缩脲试剂及双缩脲空白试剂,再进行与上述相同的其他操作和计算。 方法评价 1.双缩脲显色反应仅和蛋白质中肽键数成正比关系,与蛋白质的种类、分子量及氨基酸的组成无明显关系,各种蛋白质的显色程度基本相同。 2.本法重复性好,RCV为4%,CCV为 3.9%;线性范围为0~140g/L;本法干扰少,并且大多可以避免;使用单一的稳定试剂,操作简便、快速,既适于手工操作,也便于自动化分析,已被推荐为 测定血清总蛋白的参考方法。 3.唯一的缺点是灵敏度较低,比酚试剂法低约100倍。但本法的检出限为0.2~1.7g/L,这相当于70g/L的血清3~24μl,已能满足临床生化检验的需要。 4.本法是临床测定血清总蛋白质首选最方便、最实用的常规方法。 5.临床上常见的血清蛋白定量法主要有双缩脲法、临床折射计法、染料结合法、BCA法和免疫比浊法。 临床意义 血清总蛋白浓度受到血容量变化的影响,脱水时蛋白浓度相对增加,水潴留时则降低。在生理情况下,体位、运动等也可使血蛋白浓度发生轻微变化。 1.血清总蛋白浓度升高 (1)各种原因失水所致的血液浓缩:如呕吐、腹泻、烧伤、糖尿病酮症酸中毒、急性传染病、急腹症等。 (2)网状内皮系统疾病:如多发性骨髓瘤、原发性巨球蛋白血症、单核细胞性白血病等; (3)风湿性疾病:如系统性红斑狼疮、多发性硬化。 (4)慢性传染病:如结核、梅毒等 2.血清总蛋白浓度降低 (1)各种原因引起的血清蛋白丢失或摄入不足:如肾病综合征、营养不良、消耗增加;
蛋白质含量测定方法汇总
实验七蛋白质含量测定 测定蛋白质的定量方法有很多,目前常用的有染料法,双缩脲(Biuret)法,酚试剂法(Lowry)法及紫外吸收法。 [目的要求] 1.掌握测定蛋白质的含量基本方法。 2.了解染料法、双缩脲法、Lowry法和紫外吸收法测定原理。 一、染料法 [实验原理] 在酸性溶液中染料考马斯亮蓝G-250与蛋白质结合,此时考马斯亮蓝G-250颜色从红色变为蓝色,吸收高峰从460nm移至595nm。利用这个原理可以测定蛋白质含量。 该法近年在某些方面有取代经典的Lowry法趋势,因为它操作简单,反应时间短,染料-蛋白质颜色稳定,抗干扰性强。本法的缺点是:对于那些与标准蛋白氨基酸组成有较大差异的蛋白质,有一定误差,因为不同的蛋白质与染料的结合是不同的,故该法适合测定与标准蛋白质氨基酸组成相近的蛋白质。 [器材] 吸量管;试管;721型分光光度计 [试剂] 1.标准牛血清白蛋白溶液:配成0.1mg/ml的溶液。 2.待测蛋白质溶液。 3.染料溶液:称取考马斯亮蓝G-250 0.1g溶于95%的酒精50ml,再加入85%的浓磷酸100ml,用水稀释至1000ml,混匀备用。
[操作步骤] 1.标准曲线的绘制: 按上表分别向各支试管内加入各种试剂,充分混匀,5min后在595nm波长处以0号管调零,测定各管吸光度值(A)。以吸光度值为纵坐标,蛋白质浓度为横坐标绘制标准曲线。 2.样品测定: 取1ml样品溶液(约含25~250微克蛋白质),加入染料溶液5ml混匀,5min后测定其595nm吸光度值,对照标准曲线求得蛋白质浓度。 二、双缩脲(Biuret)法测定蛋白质含量 [实验原理] 在碱性溶液中,双缩脲(H2N-CO-NH-CO-NH2)与二价铜离子作用形成紫红色的络合物,这一反应称双缩脲反应。凡分子中含二个或二个以上酰胺基(—CO-NH2),或与此相似的基团[如—CH2-NH2,—CS-NH2,—C(NH)NH2]的任何化合物,无论这类基团直接相连还是通过一个碳或氮原子间接相连,均可发生上述反应。蛋白质分子含有众多肽键(—CO-NH—),可发生双缩脲反应,且呈色强度在一定浓度范围内与肽键数量即与蛋白质含量
血清免疫球蛋白测定.docx
血清免疫球蛋白测定 B-淋巴细胞受抗原刺激后,引起一系列细胞形态与生化特性变化,转化为淋巴母细胞并增生繁殖,最后演化为浆细胞,合成免疫球蛋白。免疫球蛋白普遍存在于生物体的血液、体液、外分泌液及某些细胞(如淋巴细胞)的细胞膜上。免疫球蛋白是一组具有抗体特性的球蛋白,其分子量很大,含有1000个以上的氨基酸分子,均由其共同抗原的两个相同的轻链(L链)和具有特异性抗原的两个不同的重链(H链)组成。 1分类 根据重链的氨基酸组成不同,免疫球蛋白可分为分五类:免疫球蛋白G(IgG)、免疫球蛋白A(IgA)、免疫球蛋白M(IgM)、免疫球蛋白D(IgD)和免疫球蛋白E(IgE)。 1.1IgG IgG是人体的主要免疫球蛋白,也是唯一能通达胎盘的免疫球蛋白。根据IgG的重链氨基酸顺序的差别,可分为IgG1,IgG2,IgG3,IgG4各亚类。IgG是主要抗感染抗体,对各种细菌、病DU有抗体活性,并有激活补体的作用。 1.2IgA IgA是分泌液中主要抗体,可分为IgA1和IgA2两个亚类。存在于血清中的称血清型IgA,存在于泪液、乳汁、胃肠道、呼吸道和泌尿生殖道分泌液中的称分泌型IgA,对局部粘膜有抗菌和抗病DU作用。
1.3IgM IgM可分为IgM1和IgM2两个亚类。是抗原刺激最先产生的免疫球蛋白,有较强的固定补体、溶解细菌及细胞的能力。IgM是抗革兰氏阴性菌和异体红细胞的主要抗体,也是存在于B淋巴细胞表面的主要免疫球蛋白。 1.4IgD 其作用与过敏反应有关。据报道,IgD可对某些抗原起反应,如青霉素、胰岛素、核抗原、甲状腺抗原等。它存在于B淋巴细胞表面,构成早期的膜受体,具有识别抗原,制动B淋巴细胞的分化作用。 1.5IgE 与I型变态反应有关,具有亲细胞特性。IgE通过Fc段与肥大细胞、嗜碱粒细胞上的Fc受体结合,故属亲同种细胞性抗体。当机体再次接触同种抗原后,过敏原即与结合在细胞表面的IgE作用,使细胞释放介质,引起平滑肌痉挛,血管通透性增加等过敏反应,还具有抗寄生虫感染作用。 2正常参考值 IgG:8~16g/L,IgA:1~4g/L,IgM:0.5~1.9g/L,IgD:0.01~0.4g/L,IgE:0.001~0.009g/L。 3临床意义 3.1血清免疫球蛋白降低 血清免疫球蛋白水平取决于免疫球蛋白合成和分解代谢的速率以及由体内丢失的程度。血清免疫球蛋白降低可由于合成不足,丢失
人血白蛋白多聚体测定法
人血白蛋白多聚体测定法 本法系用分子排阻色谱法测定人血白蛋白多聚体含量。 照分子排阻色谱法(附录ⅢD)测定。 色谱条件与系统适用性试验用亲水硅胶高效体积排阻色谱柱(SEC,排阻极限300kD,粒度10μm),柱直径7.5mm,长60cm;以含1%异丙醇的pH7.0 0.2mol/L磷酸盐缓冲液[取0.5mol/L磷酸二氢钠200ml、0.5mol/L磷酸氢二钠420ml、异丙醇15.5ml及水914.5ml,混匀]为流动相;检测波长为280nm ;流速为每分钟0.6ml。取每1ml含蛋白质为12mg 的人血白蛋白溶液20μl,注入色谱柱,记录色谱图,人血白蛋白单体峰与二聚体峰间的分离度应大于1.5,拖尾因子按人血白蛋白单体峰计算应为0.95~1.40。 测定法取供试品适量,用流动相稀释成每1ml约含蛋白质12mg的溶液,取20μl,注入色谱柱,记录色谱图30分钟(色谱柱长30cm)或60分钟(色谱柱长60cm)。 按面积归一法计算,色谱图中未保留(全排阻)峰的含量(%)除以2,即为人血白蛋白多聚体含量。 人血白蛋白 Renxue Baidanbai Human Albumin 本品系由健康人血浆,经低温乙醇蛋白分离法或经批准的其他分离法分离纯化,并经60℃ 10小时加温灭活病毒后制成。含适宜稳定剂,不含防腐剂和抗生素。 1 基本要求 生产和检定用设施、原料及辅料、水、器具、动物等应符合“凡例”的有关要求。 2 制造 2.1 原料血浆 2.1.1 血浆的采集和质量应符合“血液制品生产用人血浆”的规定。 2.1.2 低温冰冻的血浆保存期应不超过3年。 2.1.2 组分Ⅳ沉淀为原料时,应符合本品种附录“组分Ⅳ沉淀原料质量标准”。 2.1.3 组分Ⅳ沉淀应冻存于-30℃以下,运输温度不得超过-15℃。低温冰冻保存期不得超过1年。 2.1.4 组分Ⅴ沉淀应冻存于-30℃以下,并规定其有效期。 2.2 原液 2.2.1 采用低温乙醇蛋白分离法或经批准的其他分离法制备。生产过程中不得加入防腐剂或抗生素。组分Ⅳ沉淀为原料时也可用低温乙醇结合柱色谱法。 2.2.2 经纯化、超滤、除菌过滤后即为白蛋白原液。 2.2.3 原液检定 1
免疫球蛋白IgA测定
免疫球蛋白IgA测定 1检验目的 指导本室工作人员规范操作本检测项目,确保检测结果的准确。 2原理 免疫透射比浊法 抗免疫球蛋白A抗体和样本中的抗原形成抗原抗体复合物,出现凝集,进行透射比浊检测。通过加入PEG可促使反应迅速达到终点,可增加灵敏度,降低样本中抗原过剩导致假阴性的风险。 3标本要求 3.1使用新鲜血清,不使用血浆. 3.2在采集血液后2h分离血清. 3.38h内不能及时测定血清可存放于2-80C冰箱保存,3天后测定的血清置-150C―-200C 冰冻保存,但冰冻血清只能复融一次. 3.4严重溶血或脂血的标本不能作测定.
4试剂 4.1 试剂:上海罗氏诊断产品有限公司IgA试剂盒,国械注进20142405056 YZB/GER 5724-2014) 4.1.1 试剂组成 R1:TRIS 缓冲液:20 mmol/l,pH 8.0;氯化钠:200 mmol/L;PEG:3.6%;防腐剂和稳定剂。 R2:抗人免疫球蛋白A抗体(羊):取决于滴度;TRIS缓冲液:20 mmol/l;氯化钠:150 mmol/L;防腐剂。 4.1.2 试剂准备:试剂为即用式。 4.1.3 试剂稳定性与贮存:2-8°C下保存期限:见试剂标签上的有效期。机上稳定期:90天。 4.1.4变质指示:当试剂有浊度时,表明有细菌污染则试剂不能使用。 4.2 校准品:使用罗氏多项生化校准品提供的IgA校准品对自动分析仪进行校准。 4.3 质控品:使用正常值、病理值复合控制品。 5 仪器
AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪 6 操作步骤 6.1 样品的准备:将标好号的样品离心后放到仪器规定的位置。 6.2 试剂的检测:仪器开机后,检查各种试剂的位置,体积等确认无误后方可进行测定。 6.3 项目基本参数:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪项目测定参数。 6.4仪器操作步骤:参见生化检验AU2700生化分析仪,罗氏P800生化分析仪, 西门子ADVIA-2400生化分析仪,东芝TBA-120生化分析仪操作规程。 7 质量控制 在每一批标本中都应把非定值血清水平I与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
血清总蛋白测定的基质效应评价
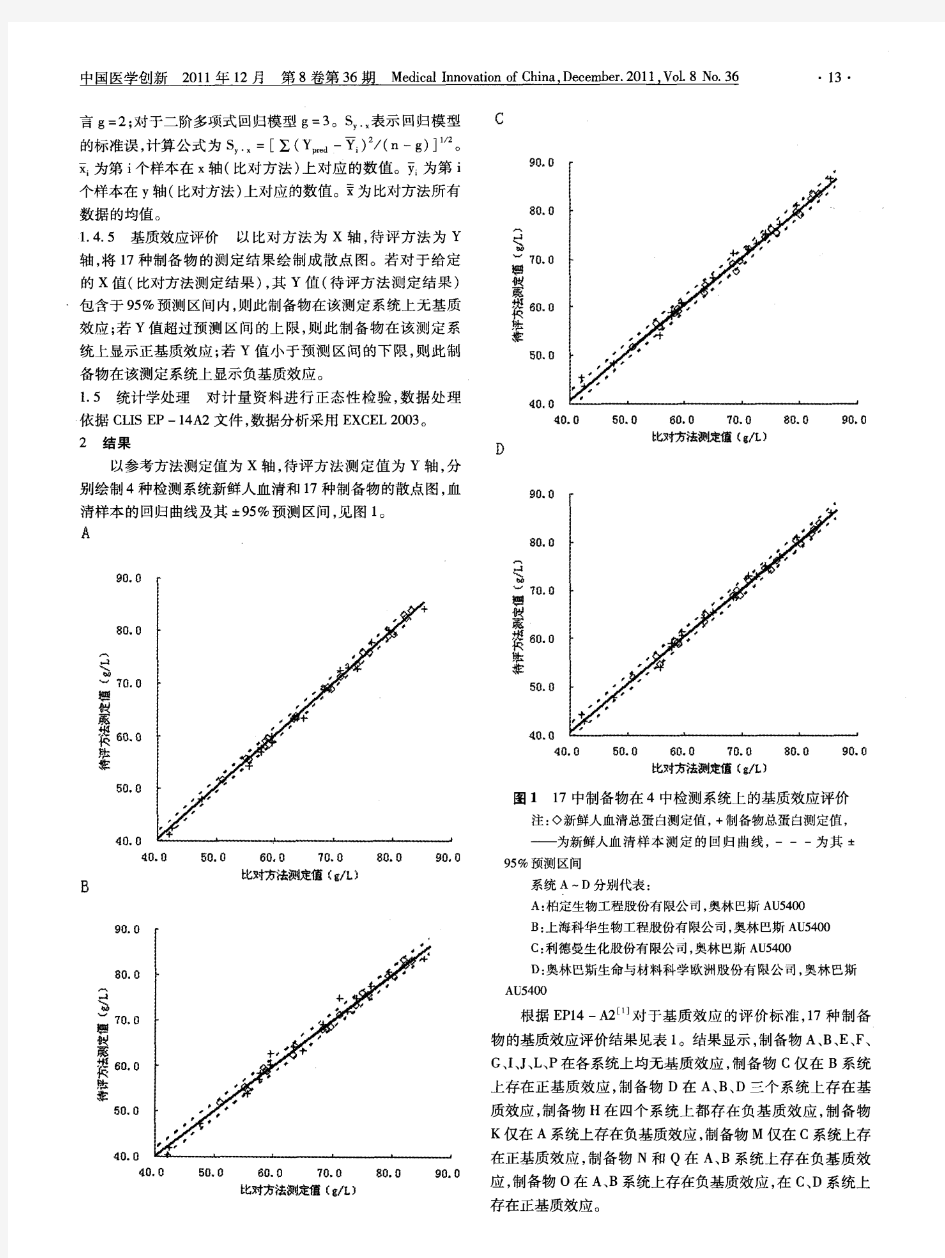
血清总蛋白测定的基质效应评价 目的评价14种室间质量评价(EQA)材料和3种市售材料在4个检测系统上测定血清总蛋白的基质效应。方法参照美国临床实验室标准化协会(CLSI)EP14-A2指南,以美国临床化学协会(AACC)推荐血清总蛋白双缩脲为参考方法,以4个检测系统为待评方法,评价制备物的基质效应。结果9种制备物对各系统均无基质效应,1种制备物对所有系统均存在基质效应,其余样本对不同检测系统存在不同程度的基质效应。结论制备物样本的基质效应可影响血清总蛋白测定的准确性和可比性,在临床检测中应重视其对检验结果量值溯源的影 响。 标签:血清总蛋白;双缩脲反应;参考方法;基质效应 Evaluation of matrix effect for serum total protein HE Mei-lin*, ZHAI Jing*, ZHANG Jie.*The Space Center Hospital of Beijing, Beijing 100049, China 【Abstract】Objective To evaluate the matrix effects of measurement for total protein in serum using 14 materials of external quality assessment(EQA) and 3 commercial reference materials in 4 measurement systems.Methods The matrix effects of 17 processed samples were evaluated by EP14-A2. The biuret method for serum total protein, recommended by the American Association for Clinical Chemistry(AACC), was reproduced as reference method. 4 measurement systems were evaluated as compared method.Results Evaluation of matrix effect: nine processed samples showed no matrix effect at all measurement systems. One processed sample showed matrix effect at all systems. Others showed different matrix effects at different systems.Conclusion The accuracy and comparability for serum total protein measurement is affected by the matrix effects of processed samples. 【Key words】Serum total protein; Biuret reaction; Reference method; Matrix effect
血清白蛋白测定标准操作规程
血清白蛋白测定标准操作规程 1 检验申请 单独检验项目申请:血清白蛋白测定(缩写ALB);组合项目申请:血生化中肝功能测定项目组合。临床医生根据需要提出检验申请。 2 标本采集与处理 2、1标本采集 2、1、1常规静脉采血约2ml,不抗凝,置普通试管中。或采用含分离胶得真空采血管. 2、1、2检验申请单与血标本试管标上统一且唯一得标识符。 2、1、3急诊标本采集后,在检验申请单上填写标本采集时间。 2、1、4标本采集后与检验申请单一起及时运送至检验科。专人负责标本得接收并记录标本得状态,对不合格标本予以拒收。 2、1、5下列标本为不合格标本 2、1、5、1标本量不足:少于0、3ml得全血标本,或少于0、1ml得血清或血浆。 2、1、5、2对反应吸光度有干扰得标本,包括严重溶血、严重浑浊得标本。 2、1、5、3无法确认标本与申请单对应关系得。 2、1、5、4其她如标识涂改、标本试管破裂等。 2、2标本保存 2、2、1接收标本后在30min内将标本离心分离出血清。 2、2、2标本保存时间:室温(15~25℃)下可稳定一周,普通冰箱中(2~8℃)稳定一个月。为避免标本中水分挥发使血清浓缩,对保存时间超过1天得标本均加塞密闭或覆盖湿巾。 2、2、3已完成测试得标本保持完整得识别号,置4~8℃冰箱内保存7天。 2、3标本采集得注意事项 2、3、1采血前使受检者保持平静、松弛与空腹状态。
2、3、2不建议采集抗凝血标本,如果必须使用血浆,推荐得抗凝剂就是肝素。 3 方法原理 血清中得白蛋白与溴甲酚绿在PH=4、2得条件下结合生成绿色复合物,溶液由黄色变为绿色,其颜色深浅与白蛋白浓度成正比,通过在630nm处测定其吸光度可得出白蛋白得含量。 PH=4、2 白蛋白 + 溴甲酚绿-—---——-------- 绿色复合物 4试剂及其她用品 4、1试剂:溴甲酚绿法测定白蛋白试剂盒,由北京利德曼生化技术有限公司出品. 4、2试剂盒保存:保存于2~8℃,不开盖情况下至标签得失效期.开盖后放于仪器得冰箱中至少稳定14天。开盖后避免污染。变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。 4、3试剂盒准备:液态单试剂型,即开即用,无特殊准备 4、4试剂盒主要成分:缓冲液(pH 4、2)50 mmol/L,溴甲酚绿0、25 mmol/L,其中含有稳定剂与保护剂〈0、1%. 5 校准品与校准模式 5、1校准品: Beckman—Coulter SYNCHRON LX MULTI 校准液(P/N 442600),其白蛋白浓度值可溯源至美国国家标准技术研究所(NIST)标准参考材料。 5、2校准类型与校准点数目:线性模式,1个校准点。 5、3校准周期:校准间隔时间不限。但在:①更换试剂批号或出现质控漂移时;②仪器进行全面保养后;③仪器得重要零件更换后;均须进行一次校准。 5、4校准液重建方法:Beckman-Coulter SYNCHRON LX MULTI 校准液即开即用,无需特殊准备. 6 质控品与室内质控规则
临床检验方法学评价
临床检验方法学评价 目前,临床实验室中所使用的检验方法,多为常规分析方法,一般使用商品试剂,基本上可以满足临床检验的要求。由于作为常规分析方法的商品试剂种类繁多,其检验结果的质量也不相同,因此,临床实验室在建立新的检验方法时,应对该方法的基本性能进行评价,以掌握方法的特征,判断其能否满足使用要求。在选择方法并对其进行评价时,可主要考虑以下几个方面: 检验结果的可溯源性 检验结果的准确性,是临床医生对疾病进行诊断和治疗的重要依据。在临床实验室中如何确保检验结果的准确,是每个检验人员必须关心的问题。通常,在检验过程中使用可溯源性校准品是保证检验结果准确性的前提,而参加室间质评价活动,可以发现实验室结果准确性的偏倚。 检验方法学分类包括:决定性方法(definitive method ):经详尽研究尚未发现不准确度或不确定性原因的方法;参考方法(reference method ):经详尽研究证实其不准确度与不精密度可以忽略的方法;常规方法(routine method ):可满足临床或其他目的需要的日常使用的方法。 标准物质又称参考物质(reference material ),是一类充分均匀,并具有一个(或多个)确定的特性值的材料或物质,用以校准仪器设备、
评价测量方法,或给其它物质赋值。标准物质的定值结果一般表示为:标准值±总不确定度。“标准物质证书“是介绍标准物质的技术文件,是研制单位向用户提出的质量保证书和使用说明。附有证书的标准物质称为有证标准物质(certified reference material, CRM ),其特性值由建立了溯源性的程序确定,使可溯源至准确复现的表示该特性值的计量单位,且每个标准值都附有给定置信水平的不确定度。 一级标准物质(primary reference material ):稳定、均一,采用高度准确、可靠的若干方法定值,可用于校准决定性方法及为二级标准物质定值。在我国,一级标准物质是测量准确度达到国内最高水平的有证标准物质,由国家技术监督局批准、颁布并授权生产。如:人血清无机成分分析标准物质(GBW09135 )和血清胆固醇标准物质(GBW 09138 )。 二级标准物质(secondary reference material ):用一级标准物质校准,参考方法定值。如:红细胞微粒标准物质—GBW (E )090001 、胆红素标准物质—GBW ( E )090002 、氰化高铁血红蛋白溶液标准物质—GBW (E )090004 和纯化血红蛋白标准物质—GBW (E )090011 。 校准物(calipator ):用二级标准物质校准,常规方法定值。用于对常规方法和仪器的校准。 质控物(control material ):具有与检测过程相适应的特性,其成份与检测样本的基质相同或相似。应使用充分均一和稳定的质控物,其瓶间变异必须小于监测系统预期的变异,其常规检测应有助于确
蛋白含量测定方法
四种紫外吸收法: 1. 280nm的光吸收法 用标准曲线法进行测定。标准蛋白质溶液配制的浓度为1.0 mg/mL。常用的标准蛋白质为牛血清清蛋白(BSA)。 标准曲线的测定: 取6支试管,按下表编号并加入BSA(1.0 mg/mL)0、1.0、2.0、3.0、4.0、5.0 mL,用蒸馏水补体积至5.0 mL;测定A280 :用第1管为空白对照,各管溶液混匀后在紫外分光光度计上测定吸光度A280,以A280为纵坐标,各管的蛋白质浓度或蛋白质量(mg)为横坐标作图,标准曲线应为直线。 利用此标准曲线,根据测出的未知样品的A280值,即可查出未知样品的蛋白质含量。 2. 280 nm和260 nm的吸收差法 核酸对紫外光有很强的吸收,在280 nm处的吸收比蛋白质强10倍(每克),但核酸在260 nm 处的吸收更强,其吸收高峰在260 nm附近。核酸260 nm处的消光系数是280 nm处的2倍;而蛋白质则相反,其280 nm的紫外吸收值大于260 nm的吸收值。通常: 纯蛋白质的光吸收比值:A280/A260 =1.8 纯核酸的光吸收比值:A280/A260=0.5 含有核酸的蛋白质溶液,可分别测定其A280和A260,由此吸收差值,用下面的经验公式,即可算出蛋白质的浓度。 蛋白质浓度=1.45×A280 -0.74×A260 (mg/mL) 3. 215 nm与225 nm的吸收差法 蛋白质的稀溶液由于含量低而不能使用280 nm的光吸收测定时,可用215nm与225 nm 吸收值之差,通过标准曲线法来测定蛋白质稀溶液的浓度。 用已知浓度的标准蛋白质,配制成20~100 mg/mL的一系列5.0 mL的蛋白质溶液,分别测定215 nm和225 nm的吸光度值,并计算出吸收差: 吸收差D= A215 -A225 以吸收差D为纵坐标,蛋白质浓度为横坐标,绘出标准曲线。再测出未知样品的吸收差,即可由标准曲线上查出未知样品的蛋白质浓度。 4. 肽键测定法 蛋白质溶液在238 nm处的光吸收的强弱,与肽键的多少成正比。因此可以用标准蛋白质溶液配制一系列50~500 mg/mL已知浓度的5.0 mL蛋白质溶液,测定238 nm的光吸收值A238,以A238为纵坐标,蛋白质含量为横坐标,绘制出标准曲线。未知样品的浓度即可由标准曲线求得。
实验一 双缩脲法测定蛋白质含量
创作编号: GB8878185555334563BT9125XW 创作者:凤呜大王* 实验一:双缩脲法测定蛋白质含量 一目的掌握双缩脲法测定蛋白质含量的原理及方法。 二原理 双缩脲( )是两分子尿素经180℃左右加热,放出一分子氨( NH3)后得到的产物。在强碱溶液中,双缩脲与CUSO4形成紫色络合物,称为双缩脲反应。其原因是含有两个及以上肽键或类似肽键有化合物都具有类似双缩脲反应。蛋白质含有多个肽键,在碱性溶液中能与CU2+络合成紫红色的络合物。其颜色的深浅与被测样品中蛋白质浓度呈正比,而与蛋白质分子量和氨基酸成分无关,故可用来测定蛋白质含量。该法对样品中蛋白质含量要求相对较高,一般在1—10mg/L蛋白质。tris(三甲羟基氨基甲烷)、一些氨基酸、EDTA(乙二胺四乙酸)、草二酰胺、多肽等会于扰该测定。 在一定浓度范围内,反应后颜色与被测样品蛋白质含量呈线性关系,即蛋白质浓度越高,体系的颜色越深。反应产物在540nm处有最大吸收峰(吸光度)。 将未知浓度的样品溶液与一系列已知浓度的标准蛋白质溶液同时与双缩脲试剂反应,并在540nm处比色,可通过标准浓度蛋白质绘制的标准曲线,求得未知样品中的蛋白质含量(浓度)。 由于本法操作简便、迅速、蛋白质浓度与光密度的线性关系好,故对蛋白质快速而不需要十分精确的测定可用此法。 三仪器与器材 可见光分光光度计、水浴锅、分析天平、振荡机(器)、漏斗、试管架、具塞三角瓶(100ml) 容量瓶(250 ml、500 ml、1000 ml)、刻度吸管(1.0 ml 2.0 ml 5.0 ml)试管(1.5cmX15cm)。 四试剂 1、双缩脲试剂称取硫酸铜(CUSO4·5H2O)1.5g,酒石酸钾钠()6.0g,分别用250 ml蒸馏水溶解后,一并转入1000 m l容量瓶中,在搅拌下(可用旋涡混合器或摇动)加入30 ml10%(质量分数)NaOH溶液,然后用蒸馏水稀释至刻度(1000ml)。将该试剂贮存于塑料瓶或内壁涂以石蜡的瓶内。此试剂可长期保存(须无红色或黑色沉淀出现),长期使用。 2、0.05 ml/L的NaOH(需标定)。 3、标准酪蛋白溶液准确称取0.5 g酪蛋白(干酪素)溶于0.05 ml/L的NaOH 溶液中,并定容于100ml,即为5mg/L的标准溶液。 4、未知蛋白质溶液浓度应在1—10mg/L范围内。可根据条件选用小麦粉或家畜血清,后者需用水稀释10倍,置于冰箱保存备用。
室间质量评价结果分析及整改
室间质量评价结果分析及整改 一、临床化学:1 、方法监测项目为钾、钠、氯、钙、磷、血糖、尿素、尿酸、肌酐、总蛋白、白蛋白、胆固醇、甘油三酯、总胆红素、丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、碱性磷酸酶、淀粉酶、肌酸激酶及胆固醇,共20个项目。 2 结果我院使用临床化学标本批号为,我院开展并提供的六项数据血糖3、56为(预期检测结果为3、65),白蛋白为 26、3(预期检测结果为 23、2),胆固醇为2、3(预期检测结果为2、2),甘油三酯为0、84(预期检测结果为0、71),丙氨酸氨基转移酶为38(预期检测结果为36),天门冬氨酸氨基转移酶为32(预期检测结果为 31、8)。3不合格原因分析能力比对检验(PT)不合格数最多的项目白蛋白(Alb),原因为质控物的基质效应和测定方法的固有特征所导致的;其他项目不合格的原因是由于这些项目都是使用电极法测定,由于电极法检测原理特性而导致的。 2、临床尿液质评:1 、方法监测项目为PH值、比重、蛋白、葡萄糖、隐血、酮体、胆红素、亚硝酸盐、尿胆原、白细胞、维生素C,共11个项目。2 结果我院使用临床尿液标本批号为,我院提供的数据为PH值5、0(预期检测结果为5、6)、比重1、010(预期检测结果为1、021)、蛋白阴性(预期检测结果
为+)、葡萄糖阴性(预期检测结果为++)、隐血阴性(预期检测结果为+++)、酮体+(预期检测结果为+++)、胆红素+++(预期检测结果为++)、亚硝酸盐阴性(预期检测结果为+)、尿胆原阴性(预期检测结果为++)、白细胞阴性(预期检测结果为阴性)、维生素C为0(预期检测结果为++)。3不合格原因分析经推断认为,我院尿液分析仪存在设备老化,误差较大的情况。临床化学检验及临床尿液室间质量评价情况整改报告根据济宁市临床检验中心反馈的《xx年度检验医学室间评价第一次质评结果》,我院认真查找不合格原因,依据查找出的原因,做出了以下几点改进措施: 1、加强对医护人员的培训,要求检验科室的工作人员均熟练掌握相关知识,使工作人员能够提高对标本质量影响因素的防范意识。 2、要求医护人员在进行标本采集前,向患者传达医嘱,详细介绍标本采集的各项要求,如:标本的量、采集的方法,提醒患者采样前切忌服用任何会对检验结果有影响的药物或食物,要求患者务必要使用检验科提供的容器采集标本,并使用正确的方法进行采样,尽可能降低标本被污染的几率。女性患者在进行尿液采样时,医护人员应确定患者不处于经期,可在条件允许的情况下,要求患者清洗外阴后,再进行尿液标本的采集。 3、建立健全的样本送检制度。建立健全的样本采集、送检管理制度并严格执行。要求检验科工作人员务必遵守相关制度,
血清免疫球蛋白测定(一)
血清免疫球蛋白测定(一) B-淋巴细胞受抗原刺激后,引起一系列细胞形态与生化特性变化,转化为淋巴母细胞并增生繁殖,最后演化为浆细胞,合成免疫球蛋白。免疫球蛋白普遍存在于生物体的血液、体液、外分泌液及某些细胞(如淋巴细胞)的细胞膜上。免疫球蛋白是一组具有抗体特性的球蛋白,其分子量很大,含有1000个以上的氨基酸分子,均由其共同抗原的两个相同的轻链(L链)和具有特异性抗原的两个不同的重链(H链)组成。 1分类 根据重链的氨基酸组成不同,免疫球蛋白可分为分五类:免疫球蛋白G(IgG)、免疫球蛋白A(IgA)、免疫球蛋白M(IgM)、免疫球蛋白D(IgD)和免疫球蛋白E(IgE)。 1.1IgG IgG是人体的主要免疫球蛋白,也是唯一能通达胎盘的免疫球蛋白。根据IgG的重链氨基酸顺序的差别,可分为IgG1,IgG2,IgG3,IgG4各亚类。IgG是主要抗感染抗体,对各种细菌、病毒有抗体活性,并有激活补体的作用。 1.2IgA IgA是分泌液中主要抗体,可分为IgA1和IgA2两个亚类。存在于血清中的称血清型IgA,存在于泪液、乳汁、胃肠道、呼吸道和泌尿生殖道分泌液中的称分泌型IgA,对局部粘膜有抗菌和抗病毒作用。 1.3IgM IgM可分为IgM1和IgM2两个亚类。是抗原刺激最先产生的免疫球蛋白,有较强的固定补体、溶解细菌及细胞的能力。IgM是抗革兰氏阴性菌和异体红细胞的主要抗体,也是存在于B淋巴细胞表面的主要免疫球蛋白。 1.4IgD 其作用与过敏反应有关。据报道,IgD可对某些抗原起反应,如青霉素、胰岛素、核抗原、甲状腺抗原等。它存在于B淋巴细胞表面,构成早期的膜受体,具有识别抗原,制动B淋巴细胞的分化作用。 1.5IgE 与I型变态反应有关,具有亲细胞特性。IgE通过Fc段与肥大细胞、嗜碱粒细胞上的Fc受体结合,故属亲同种细胞性抗体。当机体再次接触同种抗原后,过敏原即与结合在细胞表面的IgE作用,使细胞释放介质,引起平滑肌痉挛,血管通透性增加等过敏反应,还具有抗寄生虫感染作用。 2正常参考值 IgG:8~16g/L,IgA:1~4g/L,IgM:0.5~1.9g/L,IgD:0.01~0.4g/L,IgE:0.001~0.009g/L。3临床意义 3.1血清免疫球蛋白降低 血清免疫球蛋白水平取决于免疫球蛋白合成和分解代谢的速率以及由体内丢失的程度。血清免疫球蛋白降低可由于合成不足,丢失增多和分解加快引起。合成不足:血清免疫球蛋白降低可由于原发性或继发性合成缺陷所致。原发性免疫缺陷病有性联先天性丙种球蛋白缺乏症、婴儿暂时性丙种球蛋白低下症、伴IgM升高的性联低丙种球蛋白血症、选择性IgA缺乏症、选择性IgM缺乏症、选择性IgG亚类缺乏症等。继发性免疫缺陷病有慢性淋巴细胞性白血病、多发性骨髓瘤、巨球蛋白血症和恶性肿瘤等。丢失增多:从胃肠道丢失的见于溃疡性结肠炎、消化道癌肿、吸收不良综合征、淋巴瘤、肠淋巴管扩张症。从皮肤丢失的有急性灼伤、特异反应性皮炎。从浆膜腔丢失的有胸膜炎、腹膜炎、反复抽胸腹水。从肾脏丢失的有肾小球肾炎(微小病变型、膜性、增殖性)、肾静脉血栓形成、SLE和淋巴瘤。主要是由于蛋白从尿中丢失或毒素抑制免疫球蛋白合成,后者首先影响IgM,其次影响IgA,然后再影响IgG。分
