药物研发过程全解

史上最全药物研发过程全解
我们身边常用的药物多少岁了?
青霉素:1941年,76岁;病毒灵:1960年,57岁,而最常备的感冒药阿司匹林于1898年上市,至今已有119年的历史了。这些老牌药物在科技发展如此迅速的今天,为何依然活跃于每个人的生活中?
药物研发之路有多难,看一看就知道了。(此处,小编回想到无数个泡在实验室的日日夜夜,已经哭晕在厕所)
一、结构筛选
结构筛选是新药研发过程中至关重要的一项,决定着项目的生死存亡。
1.药物靶点的确认
这个是所有工作的开始。只有确定了靶点,后续所有的工作才有展开的依据。确定靶标和靶标分析需要基于治疗的疾病,做大量的文献调研和生物信息分析,从基因序列到晶体结构,从基因组学到蛋白质组学。这一阶段整理的信息特别重要,将直接影响和指导新药研发的全流程。陶素生化可提供涵盖大部分已知通路和靶点的筛选工具库,助力药物靶点的确认,最受客户欢迎的工具筛选库包括激酶库,GPCR库等,通过这些工具小分子的对靶点活性和功能筛选,鉴定,可以大大加快靶点确认工作的进程。
当科学家发现某个家族或某类蛋白中的一个/几个蛋白对其感兴趣的生物现象的发生起了非常重要的作用,他们会用各类相关的小分子抑制剂,逐个打断其中的蛋白,观察是哪个蛋白的打断对该生物现象的
发生有明显的影响,从而确认其所感兴趣的哪个/些蛋白。
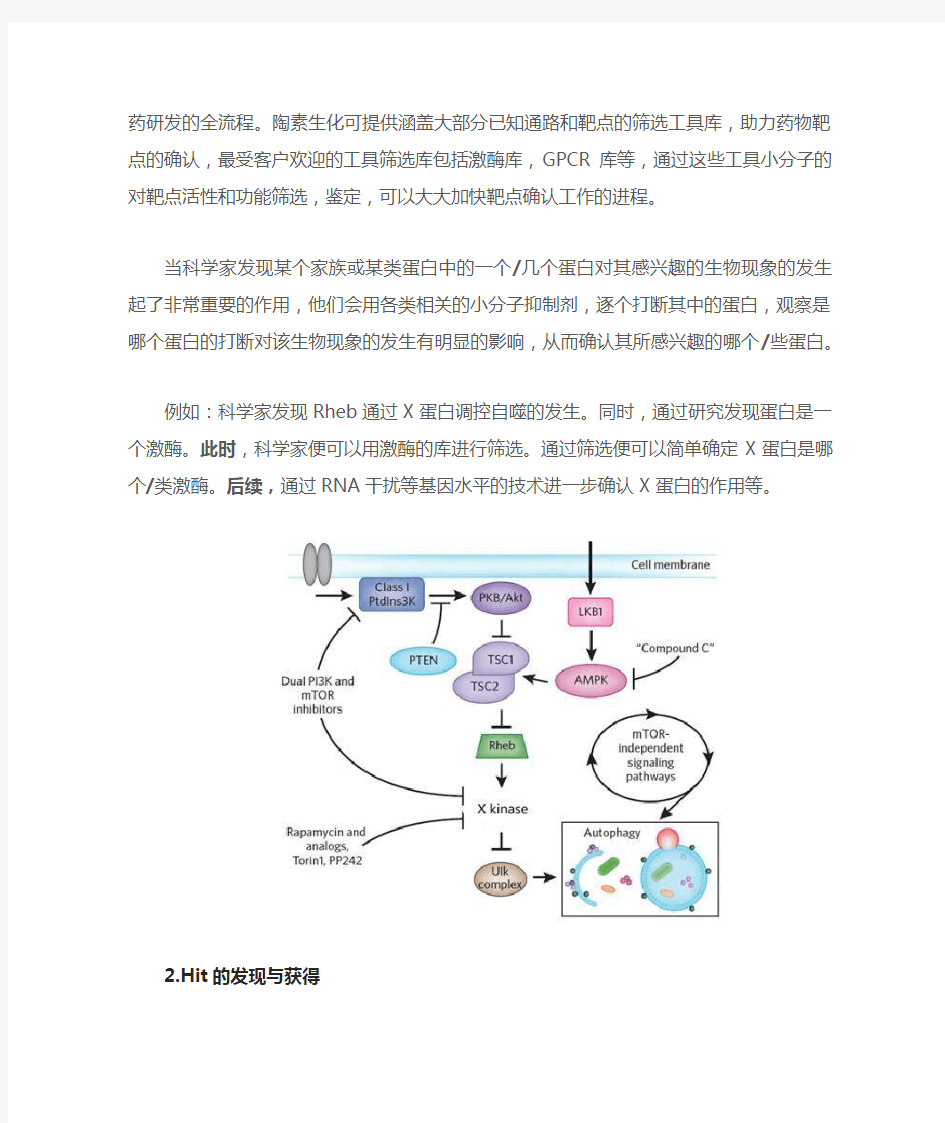
例如:科学家发现Rheb通过X蛋白调控自噬的发生。同时,通过研究发现蛋白是一个激酶。此时,科学家便可以用激酶的库进行筛选。通过筛选便可以简单确定X蛋白是哪个/类激酶。后续,通过RNA 干扰等基因水平的技术进一步确认X蛋白的作用等。
2.Hit的发现与获得
发现苗头化合物(hit),hit是指对待特定靶标或作用环节具有初步活性的化合物。发现hit的主要途径包括随机筛选的方法和理性设计的方法,理性设计的方法主要基于受体或配体结构和机制的分子设计。人工进行分子设计是一项复杂艰难,费时又烧钱的庞大工程。药物研发工作者很多时候采用虚拟筛选的方式获得hit。
进行计算机虚拟筛选,有两种方式可以选择。
第一种,基于受体的虚拟筛选从靶蛋白的三维结构出发,研究靶蛋白结合位点的特征性质以及它与小分子化合物之间的相互作用模式,根据与结合能相关的亲合性打分函数对蛋白和小分子化合物的结合能力进行评价,最终从大量的化合物分子中挑选出结合模式比较合理的、预测得分较高的化合物,用于后续的生物活性测试。
第二种,基于配体的虚拟筛选一般是利用已知活性的小分子化合物,根据化合物的形状相似性或药效团模型在化合物数据库中搜索能够与它匹配的化学分子结构。最后对这些挑选出来的化合物进行实验筛选研究。
陶素生物科技有限公司可以提供含有高达500万个小分子化合物集合的高通量筛选库。其庞大的数
量,创造了无限的可能,科研工作者通过邮件(info@https://www.360docs.net/doc/957325117.html,)等形式联系到陶素,免费获得量级百万的靶点库进行虚拟筛选。陶素生化协助众多机构用很好的性价比,高效的研发效率,精准、快
速的发现优质苗头化合物(hit)。陶素提供的500万小分子可以有效地帮助科学家寻找hit。陶素提供的500万个小分子,都有库存,都拥有极好的耐药性,科学家随时都可以购买,避免后期筛选出来目标小分子后缺货或者供应不及时的情况出现。
下图,为陶素计算机筛选的两大方向,一类是基于分子结构的筛选,陶素可以使用计算机筛选帮助其客户从500万个化合物中筛选出目标分子,另一类是使用基于配体的方式进行筛选。
对于不从事计算机虚拟筛选的实验室,陶素生化也精选了骨架化合物库,最大限度的降低筛选工作的成本和精度,从500万个类药小分子中去除了99%以上的相似结构的化合物,仅通过4131个极具代表性的化合物就可以筛选到最全的母核结构,最大程度上保证了化合物库的多样性。在先导化合物的发现和优化过程中,起到了极为重要的作用,保证实验的高效性与准确性,作为Hit 发现的筛选库具有独一无二的优势:
◆多样性好,千里挑一
4131多样性骨架库,每个骨架只对应一个化合物;
◆纯度高
具有较高的纯度(不低于90%),随货附带HNMR/LCMS谱图符合药物筛选的纯度要求,利于后期优化;
◆产品新颖度高
产品新颖度高,在筛选中先人一步,同样的筛选模型,筛出不一样的分子
◆类药性
小分子在分子量、亲疏水常数等方面符合药物的类似性,适合于在高通量筛选平台建立初期的基础化合物库购置,为后期在多靶点、多通路上的类药筛选和前沿研究奠定化合物基础。
同样,作为最专业的药物筛选平台,陶素也支持不同骨架小分子的定制库,如果陶素的客户有感兴趣的骨架,陶素就能为其提供全球范围内最全的相关骨架小分子。
3.候选药物的获得
在hit的基础上,我们通过ADMET预测分析,类药五原则,结合靶标分析阶段的文献调研和生物信息学分析所获得的信息以及生物活性验证等等,除掉大部分研发风险高的hit,获得先导化合物(lead)。先导化合物,意为通过各种途径和手段得到的具有某种生物活性和化学结构的化合物,用于进一步的结构改造和修饰,是现代新药研究的出发点。
从先导化合物到候选药物,我们需要对先导化合物的各种缺陷通过分子对接、生物电子等排原理、前药原理等技术方法进行结构改造和修饰。
陶素生化提供涵盖候选药物研发全过程的科研支持,除已被众多科研用户熟悉并高度认可的高通量筛选外,还可提供针对先导化合物的定制,合成,修饰服务,打造一站式药物研发平台。
例:
总之,候选药物的研发阶段包含了创制药物的四大要素:靶标分析、检测模型、先导化合物的发现和先导化合物的优化。基于多学科交叉的药物分子设计是目前实现新药创制的主要途径和手段。
二、临床实验的申请及审批
候选药物经过临床前优化制备工艺、检验方法、质量指标、稳定性、药理、毒理和药代动力学等研究,方可进入临床实验的申请和审批。
药物临床试验的准备条件概括如下:
1、获得CFDA审批的药品临床试验批件
2、符合规范的药检报告
3、内容齐备的研究者手册
4、具有资格的药物临床研究机构
5、合格的研究人员
6、规范化设计的新药临床试验方案
7、制定可操作的标准操作规程(简称SOP)。
三、临床试验
1. 临床一期试验---评价药物的安全性和剂量,需要20~100例健康志愿者。
初步的临床药理学及人体安全性评价试验,为新药人体试验的起始期,又称为早期人体试验。I期临床试验包括耐受性试验和药代动力学研究,一般在健康受试者中进行。其目的是研究人体对药物的耐受程度,并通过药物代谢动力学研究,了解药物在人体内的吸收、分布、消除的规律,为制定给药方案提供依据,以便进一步进行治疗试验。
人体耐受性试验(clinical tolerance test) 是在经过详细的动物实验研究的基础上,观察人体对该药的耐受程度,找出人体对新药的最大耐受剂量及其产生的不良反应,是人体的安全性试验,为确定II期临床试验用药剂量提供重要的科学依据。
人体药代动力学研究( clinical pharmacokinetics) 是通过研究药物在人体内的吸收、分布、生物转化及排泄过程的规律,为II 期临床试验给药方案的制订提供科学的依据。人体药代动力学观察的是药物及其代谢物在人体内的含量随时间变化的动态过程,这一过程主要通过数学模型和统计学方法进行定量描述。药代动力学的基本假设是药物的药效或毒性与其所达到的浓度(如血液中的浓度)有关。
2. 临床二期试验---评价药物的疗效,需要多于100例病患志愿者。
II期临床试验为治疗作用初步评价阶段。其目的是初步评价药物对目标适应症患者的治疗作用和安全性,也包括为III期临床试验研究设计和给药剂量方案的确定提供依据。此阶段的研究设计可以根据具体的研究目的,采用多种形式,包括随机盲法对照临床试验。
3. 临床三期试验---对药物疗效及安全性作进一步的评价,需要多于300例病患志愿者。
治疗作用确证阶段。其目的是进一步验证药物对目标适应症患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据。试验一般应为具有足够样本量的随机盲法对照试验。
本期试验的样本量要远大于比前两期试验,更多样本量有助于获取更丰富的药物安全性和疗效方面的资料,对药物的益处/风险进行评估,为产品获批上市提供支撑。
该期试验一般为具有足够样本量的随机化盲法对照试验(random control trial, RCT)。临床试验将对试验药物与安慰剂(不含活性物质)或已上市药品的有关参数进行比较。试验结果应当具有可重复性。
小编感叹即便在临床期夭折的药物也经历了如此多的筛选和考验,是极具研究价值和研究基础的先
导化合物范本。对临床期药物感兴趣的客户可以直接联系陶素生化(info@https://www.360docs.net/doc/957325117.html,)了解相关化合物库,获得相关化合物库的详细信息。
客户可根据自己的兴趣定制不同研究领域或临床期的分子库,陶素生化是业内第一家推出按临床期分类的临床药物库的筛选平台。拥有全部由进入临床期的药物分子组成的临床分子库,每个化合物都包含了药理活性、来源、参考文献等信息。
陶素的临床分子库:
◆ 514个临床期化合物集合,可用于高通量筛选和高内涵筛选;
◆所有化合物均已被批准进入临床期,包括临床一期、二期、三期;
◆是新药研发和新药筛选的有效工具;
◆配有详细的说明书,化合物结构、靶点信息、IC50值、活性描述等;
◆结构多样,药效显著,可渗透细胞;
◆NMR和HPLC技术保证产品高纯度;
◆所有化合物现货供应。
陶素临床库信息一览
四、上市申请及审批
中外新药上市都要过两道关卡,新药临床试验审批(IND)和新药生产上市审批(NDA)。另外,对于那些“治疗严重危及生命疾病的药品”中美都有“绿色通道”。
陶素生化提供业内知名的上市药物库,收录了包括FDA,CFDA,EMA,PMDA等全球最主要最权威药物的机构批准上市的产品,以高度全面的信息做依托,陶素为客户提供高度定制服务,大量科研人员仅通过基数极小的筛选定制库就获得了进行药物重定位的目标分子!
四、上市后进一步研究
药物上市后仍然需要进行进一步的研究,在广泛使用条件下考察其疗效和不良反应。上市后的研究在国际上多数国家称为“ IV期临床试验”。以及用生物利用度研究的方法,以药代动力学参数为指标,比较同一种药物的相同或者不同剂型的制剂,在相同的试验条件下,其活性成份吸收程度和速度有无统计学差异的人体试验。
药物研发是一个高投入高风险同时伴随高回报的行业,一旦药物成功上市,那么回报也是惊人的。业界有个词叫“重磅炸弹”,指的是年销售10亿美元以上的药物。一个极端的例子是辉瑞已经过了专利保护的降血脂药物立普妥(Lipitor),2010年的全球销售额是101.33亿美元。
药物研发,痛并快乐着。冬天来了,少做点事,养点肥膘才是正事。陶素在整个药物研发过程中,可以替我们干的活儿,小编都给大家写出来了。
你们懂得......
药物研发到上市过程
In drug research and development, the patient is the focus. The mission for nova is to help the patient overcome a disease and improve their quality of life. The drug development process is designed to ensure that innovative new medicines are effective ,safe and available for patients in the shortest possible time. Chapter 1 Target Discovery The first step in drug development is to discover the best targets for treating or prevent a disease. Targets are usually proteins in the patient’s body which are associated with the disease or proteins in microorganisms causing a disease. The challenge is to identify which proteins are relevant and more importantly confirm their role in a disease. Increasingly, nova focuses on understanding cellular networks of proteins or pathways. A single protein may transmit messages to several other proteins, sometimes in multiple pathways affecting their function. Knowing how these pathways work and interact helps to identify the most appropriate target for a drug. The pathway approach allows nova to better understand the mechanisms of a disease. This knowledge together with the desire to address unmet medical needs determines the primaries in target discovery. Chapter 2 Drug Discovery In drug discovery, several methods like high-throughput screening and computer-based design are used to find chemical compounds or biologics that bind to the identified target. If a compound modulates the target in a way that is expected to alter the disease. This so-called hit will be refined to improve its safety and effectiveness, eventually becoming a drug candidate. Discovering and bringing one new drug to the market typically takes an average of fourteen years of research and clinical development efforts and cost around two billion us dollars. Of 10,000 or more hits tested in early drug discovery only one may eventually lead to a drug that reaches the market. Chapter 3 Safety and Drug Metabolism In the late preclinical stage, further experiments are conducted on the drug candidate to ensure it is safe for patients and has the required pharmacokinetic properties like appropriate absorption and metabolism by the human body. These experiments are executed with extraordinary diligence to minimize any risks to human test subjects. Animals play a critical role in the drug discovery processes as well. Although much research and development can be done using various experiments or using computers, complex disease mechanisms can often only be understood though the use of animal studies. Also, governments and regulatory authorities require that medicines be tested in animals before they are tested in humans. Nova keeps this research as limited as possible had always ensures that animal research is scientifically acceptable according to current standards and regulations. For these reasons, nova continues to use animals in its quest to find innovative safe and life-saving medicines for patients. At the same time, nova is committed to refining, reducing and replacing the use of animals in research and upholding the highest standards in animal welfare.
新药研发流程
新药研发流程 集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)
新药研发及上市项目流程 总的来说新药的研发分为两个阶段:研究和开发。这两个阶段是相继发生有互相联系的。区分两个阶段的标志是候选药物的确定,即在确定候选药物之前为研究阶段,确定之后的工作为开发阶段。 研究阶段包括四个重要环节,即靶标的确定,模型的建立,先导化合物的发现,先导化合物的优化: 1、靶标的确定:确定治疗的疾病目标和作用的环节和靶标,是创制新药的出发点,也是以后施行的各种操作的依据。 2、模型的建立:靶标选定以后,要建立生物学模型,以筛选和评价化合物的活性。 3、先导化合物的发现:所谓先导化合物,也称新化学实体,是指通过各种途径和方法得到的具有某种生物活性或药理活性的化合物。 4、先导化合物的优化:由于发现的先导化合物可能具有作用强度或特异性不高、药代动力性质不适宜、毒副作用较强或是化学或代谢上不稳定等缺陷,先导化合物一般不能直接成为药物。因此有必要对先导化合物进行优化以确定候选药物,这是新药研究的最后一步。 新药开发阶段包括四个重要环节,即临床前试验,研发中新药申请,新药申请,批准: 1、临床前试验:由制药公司进行的实验室和动物研究,以观察化合物针对目标疾病的生物活性,同时对化合物进行安全性评估。这些试验大概需要3.5年的时间。
2、研发中新药申请:在临床前试验完成后,公司要向FDA提请一份IND,之后才能开始进行药物的人体试验。 3、新药申请:通过三个阶段的临床试验,公司将分析所有的试验数据。如果数据能够成功证明药物的安全性和有效性,公司将向FDA提出新药申请。 4、批准:一旦FDA批准了一份新药申请,此种新药就可以被医师用于处方。公司必须继续向FDA提交阶段性报告,包括所有的不良反应报告和一些质量控制记录。
新药开发中药物分析流程
新药开发中药物分析一般程序 1.原料药质量标准的确定 原料药的质量标准确定一般程序,这里将它分为三大阶段:合成工艺待确定期,合成工艺确定期,稳定性试验考察期。 1.1 合成工艺待确定期 一个原料药首先由药物合成部进行合成工艺的确定,在其进行工艺确定期间,就已经与药分部门有了密切的联系。 协助合成部门的工作:帮助确定反应步骤的终点控制、反应产物的纯度监控,所能提供的分析方法可能有薄层色谱、液相色谱或熔点等。 做好自己的准备工作:通过各种途径搜集查阅有关该药品的各方面信息,比如该药的理化性质(性状、溶解度、熔点、旋光性质、紫外光谱、鉴别方法等)、检查项(一般杂质检查、有关物质检查)、含量测定方法和该药物的稳定性等等。 1.2 合成工艺确定期 合成工艺路线打通后,合成部门将会提供试制的三批样品(已确定该药物结构)供分析部门质量研究及稳定性试验用,一般来说,所提供三批样品应该是成熟的工艺条件,以一定规模制备得到样品,此时我们的质量研究工作正式开始。 1.2.1 质量研究工作 理化常数:性状(外观、臭、味)、溶解度、熔点、比旋度、紫外吸收系数鉴别:化学法、色谱法、光谱法 检查:酸碱度、溶液澄清度与颜色、干燥失重或水分、炽灼残渣、重金属、无机盐、无菌、热原或细菌内毒素、有机溶剂残留、有关物质 含量测定:容量法、光谱法、色谱法 1.2.2 质量研究试验顺序安排 1.3 稳定性试验考察期 按照中国药典稳定性研究指导原则规定,我们的稳定性研究包括三大部分—影响因素试验、加速试验和长期留样试验。 考察项目:样品性状、有关物质和含量这三项必须考察(对于某些特殊药物可能无法考察有关物质),另外诸如:熔点(若质量标准中规定了熔点检查,或能测出准确熔点且熔点低于250℃的样品,稳定性研究中必须对其检查)、溶液颜色与澄清度(若为供注射用原料,稳定性研究中必须对其检查)、pH值(若 为供注射用原料,稳定性研究中必须对其检查)等项目则根据各药物的性质而具体制定。 上面将原料药分析工作分三大块做了简单讨论,文中所讲的多是实际试验的简单思路和一些注意事项,但对于新药研究这样一个很严肃的工作有很多法定性的规定内容在文中并未详细说明,在《中国药典2000年版二部》和《新药质量研究与质量标准指导原则》中有详细的说明。 2.药物溶解度试验 1.试验溶剂的选择可参考有关文献制定,若无文献一般选择常用的水相溶剂(水、酸、碱溶液)和有机溶剂(甲醇、乙醇、乙腈、乙醚、丙酮、氯仿、冰醋酸、DMF、DMSO)。 2.若按照中国药典要求的做法将用去大量的原料和溶剂一般我们都按倍数 减量试验,但在做极易溶解或易溶时因溶剂量较小可适当放大原料量试验。
药物研发流程
通常,从药物研发到普通药品上中须经过以下几个过程 ①研发筛选(R&D Screening),包括市场凋查(Market Survey)与专利调查(Patent Survey);②临床前研究(Preclincal Studies); ③临床阶段(Clinical Phases); ④新药批准上市(New Drug Approval); 整个研究是一个循环往复的过程,其中缺一不可。在药物研究过程中,更多的是依赖精心加上处理过的专业信息。我们应该选择针对性强、质量高、覆盖面大、有权威性的检索工具。另外,信息源的可靠性、获取数据的方便性、检索的效率都是是我们要考虑的首要因素。DIALOG系统具有600多个数据库,其中和制药相关的数据达200个,这些数据库在为制药企业提供各个环节数据和信息的同时,还利用其功能庞大的指令检索系统为企业提供了优秀的信息和情报的解决方案。 1 研发筛选阶段 药物的研究开发途径主要包括:合理药物设计,组合化学技术,从天然产物中寻找新药,仿制安全、有效、市场需要的国外新药,开发新制剂、新剂型、新药用辅料等。在此阶段可选择下列数据库。 1.1 Current Contents (科研近期报道) 该数据库主要提供临床医学,生命科学,工程学,技术与应用科学,农业,生物学与环境科学,物理学,化学与地球科学,社会与行为科学,以及艺术与人类学等方面信息。 1.2 Chemical Abstracts (美国化学文摘) 该数据库主要收载生物化学、有机化学、大分子化学、应用化学、化学工程、物理化学、分析化学、理论化学、环境化学、农业化学、化合物和化学物质性质与反应,技术与操作规程,材料,仪器设备,理论与应用等信息。 1.3 Beilstein (贝尔斯坦文摘) 该数据库提供了900多万个有机化合物的结构资料和一千多万个化学反应资料以及两千万有机物性质和相关文献,包含可供检索的化学结构和化学反应、相关的化学和物理性质,以及详细的药理学和生态学数据在内的最全面的信息资源。收录的资料有分子的结构,物理化学性质,制备方法,生物活性,化学反应和参考文献来源,最早的文献可回溯到1771年。其中收录的性质数值资料达3000万条,化学反应超过500万种。 1.4 Biosis Previews (美国生物文摘数据库) 该数据库收录了1969年以来的《生物学文摘》(BA)和《生物学文摘综述、技术报告、会议文献》(BA/RRM)以及BA/RRM 1980年创刊时的前身检索刊物《生物研究索引》(Biobesearch Index)。内容涉及细胞学、动物学、基因学、植物学、微生物学以及相关学科:包括生物化学、生物工程、农业、生态学、食品科学与研究、医学、生物技术、环境研究及药理学等。 1.5 Incidence &- Prevalence (发病率与患病率) 该数据库提供流行病学、发病率、患病率、死亡率、疾病趋势、花费、风险因素、以及疾病分类等信息。 在药物筛选阶段,还应该进行市场调查(Market Survey)和专利调查(Patent Survey)。在市场调查阶段,使用Dialog Newsroom和Dialog Profoud数据库可以获得全球超过10,000种新闻期刊和来自130多个市场研究机构超过20万份市场调研报告。我们也可选择以下数据库资源:①Pharmaco-economics(药物经济学);②SCRIP(World PharmaceuticalNews世界制药新闻)等期刊。③FREEDONIA(Freedonia Market Research)
新药研发基本流程
新药研发基本流程
新药研发基本流程 概述近年来,由于国家政策的支持,我国的生物医药产业正在成为发展最活跃的产业,医药研发进展可谓日新月异。鉴于药监局的监管政策在不断更新,从事医药研发的企业和人员越来越多。考虑到从事医药研发的新人的增加,有必要将新药研发的基本流程做一个简单梳理。现代药物的概念除了我们传统意义上的小分子化合物(如阿司匹林,青蒿素),还包括多肽、蛋白质和抗体,(寡)核苷酸,小分子—抗体复合物,还有疫苗。下面以传统的小分子化合物药为例,就新药(主要以1.1类创新药为例)研发从无到有,到最后上市的基本流程做一个概述。 新药的发现(Drug Discovery) 1.药物作用靶点(target)以及生物标记(biomarker)的选择与确认 早期人们对药物作用靶标认识有限,往往只知道有效,但不知如何起效。比如,百年来,人们知道阿司匹林(aspirin)具有解热、消炎、止痛、抗血栓,甚至抗癌作用。直到1971年,英国人John R. Vane 在《Nature》期刊发文才阐明了Aspirin作用机理为抑制前列腺素合成,并于1982荣获Nobel生理和医学奖。现代生物医学
的研究进展,以及人类基因图谱的建立,让人类对疾病的机理了解更加准确,为新药开发提供了明确的方向、具体的靶标。 2.先导化合物(lead compound)的确定 一旦选定了药物作用的靶标,药物化学家(medicinal chemist)首先要找到一个对该靶标有作用的化合物。这个化合物可以来自天然产物(动物、植物、海洋生物);也可以是根据靶标的空间结构,计算机模拟设计、合成的化合物;还可以根据文献报道或以前其它项目的研究发现。比如,某一类化合物具有作用于该靶标的药理活性或副反应等等。治疗勃起障碍的药物Viagra就是由其副作用开发而成。目前我们常用的方法是跟踪国外研发机构对某一靶标的药物开发,以他们的化合物作为先导,希望设计出更优秀的化合物。3.构效关系的研究与活性化合物的筛选 围绕先导化合物,设计并合成大量新化合物,通过对所合成化合物活性数据与化合物结构的构效关系分析,进一步有效的指导后续的化合物结构优化和修饰,以期得到活性更好的化合物。 4.候选药物(candidate)的选定 通过构效关系研究,几轮优化所有筛选出来的满足基本生物活性的最优化合物,一般就选作为候选药物,进入开发。此时,从事新药发现的药物化学家工作暂告结束。
新药研发基本流程
新药研发基本流程 概述近年来,由于国家政策的支持,我国的生物医药产业正在成为发展最活跃的产业,医药研发进展可谓日新月异。鉴于药监局的监管政策在不断更新,从事医药研发的企业和人员越来越多。考虑到从事医药研发的新人的增加,有必要将新药研发的基本流程做一个简单梳理。现代药物的概念除了我们传统意义上的小分子化合物(如阿司匹林,青蒿素),还包括多肽、蛋白质和抗体,(寡)核苷酸,小分子—抗体复合物,还有疫苗。下面以传统的小分子化合物药为例,就新药(主要以1.1类创新药为例)研发从无到有,到最后上市的基本流程做一个概述。 新药的发现(Drug Discovery) 1.药物作用靶点(target)以及生物标记(biomarker)的选择与确认 早期人们对药物作用靶标认识有限,往往只知道有效,但不知如何起效。比如,百年来,人们知道阿司匹林(aspirin)具有解热、消炎、止痛、抗血栓,甚至抗癌作用。直到1971年,英国人John R. Vane 在
《Nature》期刊发文才阐明了Aspirin作用机理为抑制前列腺素合成,并于1982荣获Nobel生理和医学奖。现代生物医学的研究进展,以及人类基因图谱的建立,让人类对疾病的机理了解更加准确,为新药开发提供了明确的方向、具体的靶标。 2.先导化合物(lead compound)的确定 一旦选定了药物作用的靶标,药物化学家(medicinal chemist)首先要找到一个对该靶标有作用的化合物。这个化合物可以来自天然产物(动物、植物、海洋生物);也可以是根据靶标的空间结构,计算机模拟设计、合成的化合物;还可以根据文献报道或以前其它项目的研究发现。比如,某一类化合物具有作用于该靶标的药理活性或副反应等等。治疗勃起障碍的药物Viagra就是由其副作用开发而成。目前我们常用的方法是跟踪国外研发机构对某一靶标的药物开发,以他们的化合物作为先导,希望设计出更优秀的化合物。 3.构效关系的研究与活性化合物的筛选 围绕先导化合物,设计并合成大量新化合物,通过对所合成化合物活性数据与化合物结构的构效关系分析,进一步有效的指导后续的化合物结构优化和修饰,以期得到活性更好的化合物。 4.候选药物(candidate)的选定 通过构效关系研究,几轮优化所有筛选出来的满足基本生物活性的最优化合物,一般就选作为候选药物,进入开发。此时,从事新药发现的药物化学家工作暂告结束。
仿制药研发流程-经典
仿制药研发具体流程 一、综述 根据药品注册管理办法附件二的规定,仿制药即是已有国家药品标准的原料药或者制剂,该类药物国内已批准生产或上市销售,经过国内外广泛使用,其安全性、有效性已经得到较充分证实。 如今的新法规对仿制药提出了新的要求,主要是以下几点: 1、规范对被仿制药品的选择原则,即参比制剂的选择问题。 2、增加批准前生产现场的检查。 3、按照CTD格式要求提供申报资料,使申报规范,统一。 4、强调了对比研究,是判断两者质量是否一致的重要方法之一。 5、强化了工艺验证,目的是确保大生产时能始终如一地按照申报工艺生产出质量恒定的产品。 6、提出了晶型的要求,晶型的不同,溶解度和稳定性不同。 分析上述新要求和参考指导原则,从而得出结论: 仿制药研发的目的是做到规模化生产,强调本地化,以实现“替代性”。要求是做到“同”。方法为对比研究。 1.安全性“同”: 对于安全性,口服固体制剂控制的主要为有关物质,而液体制剂除控制有关物质外,还需对防腐剂、氧化剂等对人体有影响的物质进行控制。因此,必须要将防腐剂含量测定定入质量标准。 研究的内容:静态上应包括杂质谱的对比,单个杂质的对比,杂质总量的对比。动态上的对比为影响因素试验、加速试验的对比,即稳定性对比研究。 2.有效性“同”: 对于口服固体制剂,口服混悬剂(包括干混悬剂),溶出曲线是主要的控制指标[1];对于口服溶液剂,防腐剂、矫味剂、氧化剂、增溶剂及稳定剂的选用非常重要,控制点为口感、渗透压、PH及有无絮凝现象;对于局部用制剂(如鼻喷雾剂),粒度分布、渗透压及黏度是主要控制指标。 研究的内容:分别进行溶出曲线对比;粒度分布对比;渗透压及黏度对比。 3.晶型: 晶型的不同,药物的溶解度及稳定性有可能不相同,从而导致生物利用度不尽相同。而某个药物的晶型,文献资料很少;制剂中原料的晶型测定有一定的难度;在做成制剂的过程中,又不能保证晶型不产生变化。 但是,鉴于仿制药研究的特点,溶解度方面可通过溶出曲线对比来说明;稳定性方面可通过影响因素试验和加速试验的对比来说明。 二、仿制药研发项目汇总(从立项到申报,时间为10—12个月)
新药研发流程
螆药物从最初的实验室研究到最终摆放到药柜销售平均需要花费12年的时间。进行临床前试验的5000种化合物中只有5种能进入到后续的临床试验,而仅其中的1种化合物可以得到最终的上市批准。 蒄总的来说新药的研发分为两个阶段:研究和开发。这两个阶段是相继发生有互相联系的。区分两个阶段的标志是候选药物的确定,即在确定候选药物之前为研究阶段,确定之后的工作为开发阶段。所谓候选药物是指拟进行系统的临床前试验并进入临床研究的活性化合物。 莁研究阶段包括四个重要环节,即靶标的确定,模型的建立,先导化合物的发现,先导化合物的优化。 肇一、靶标的确立确定治疗的疾病目标和作用的环节和靶标,是创制新药的出发点,也是以后施行的各种操作的依据。药物的靶标包括酶、受体、离子通道等。作用于不同的靶标的药物在全部药物中所占的比重是不同的。以2000年为例,在全世界药物的销售总额中,酶抑制剂占32.4%,转运蛋白抑制剂占16.0%,受体激动剂占9.1%,受体拮抗剂占10.7%,作用于离子通道的药物占9.1%等等。目前,较
为新兴的确认靶标的技术主要有两个。一是利用基因重组技术建立转基因动物模型或进行基因敲除以验证与特定代谢途径相关或表型的靶标。这种技术的缺陷在于,不能完全消除由敲除所带来的其他效应(例如因代偿机制的启动而导致的表型的改变等)。二是利用反义寡核苷酸技术通过抑制特定的信使RNA对蛋白质的翻译来确认新的靶标。例如嵌入小核核糖核酸(snRNA)控制基因的表达,对确证靶标有重要作用。 膆二、模型的确立靶标选定以后,要建立生物学模型,以筛选和评价化合物的活性。通常要制订出筛选标准,如果化合物符合这些标准,则研究项目继续进行;若未能满足标准,则应尽早结束研究。一般试验模型标准大致上有:化合物体外实验的活性强度;动物模型是否能反映人体相应的疾病状态;药物的剂量(浓度)——效应关系,等等。可定量重复的体外模型是评价化合物活性的前提。近几年来,为了规避药物开发的后期风险,一般同时进行药物的药代动力模型评价(ADME评价)、药物稳定性试验等。 羁三、先导化合物的发现新药研制的第三步是先导化合物的发现。所谓先导化合物(leading compound),也称新化学实体(new chemical entity,NCE),是指通过各种途径和方法得到的具有某种生物活性或药理活性的化合物。因为目前的知识还不足以渊博到以足够的受体机制指导药物设计以使药物的合成不必使用预先已知的模型,所以,先导化合物的发现,一方面有赖于以上两步所确定的受体
药物研发过程全解
史上最全药物研发过程全解 我们身边常用的药物多少岁了? 青霉素:1941年,76岁;病毒灵:1960年,57岁,而最常备的感冒药阿司匹林于1898年上市,至今已有119年的历史了。这些老牌药物在科技发展如此迅速的今天,为何依然活跃于每个人的生活中? 药物研发之路有多难,看一看就知道了。(此处,小编回想到无数个泡在实验室的日日夜夜,已经哭晕在厕所) 一、结构筛选 结构筛选是新药研发过程中至关重要的一项,决定着项目的生死存亡。 1.药物靶点的确认 这个是所有工作的开始。只有确定了靶点,后续所有的工作才有展开的依据。确定靶标和靶标分析需要基于治疗的疾病,做大量的文献调研和生物信息分析,从基因序列到晶体结构,从基因组学到蛋白质组学。这一阶段整理的信息特别重要,将直接影响和指导新药研发的全流程。陶素生化可提供涵盖大部分已知通路和靶点的筛选工具库,助力药物靶点的确认,最受客户欢迎的工具筛选库包括激酶库,GPCR库等,通过这些工具小分子的对靶点活性和功能筛选,鉴定,可以大大加快靶点确认工作的进程。 当科学家发现某个家族或某类蛋白中的一个/几个蛋白对其感兴趣的生物现象的发生起了非常重要的作用,他们会用各类相关的小分子抑制剂,逐个打断其中的蛋白,观察是哪个蛋白的打断对该生物现象的 发生有明显的影响,从而确认其所感兴趣的哪个/些蛋白。 例如:科学家发现Rheb通过X蛋白调控自噬的发生。同时,通过研究发现蛋白是一个激酶。此时,科学家便可以用激酶的库进行筛选。通过筛选便可以简单确定X蛋白是哪个/类激酶。后续,通过RNA 干扰等基因水平的技术进一步确认X蛋白的作用等。
2.Hit的发现与获得 发现苗头化合物(hit),hit是指对待特定靶标或作用环节具有初步活性的化合物。发现hit的主要途径包括随机筛选的方法和理性设计的方法,理性设计的方法主要基于受体或配体结构和机制的分子设计。人工进行分子设计是一项复杂艰难,费时又烧钱的庞大工程。药物研发工作者很多时候采用虚拟筛选的方式获得hit。
中药新药研发申报流程及相关材料说明
中药新药研发申报流程及相关申报材料说明 一、中药新药的注册分类及说明 1.1注册分类 中药新药注册按审批管理的要求分以下几类: 1. 未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂。 2. 新发现的药材及其制剂。 3. 新的中药材代用品。 4. 药材新的药用部位及其制剂。 5. 未在国内上市销售的从植物、动物、矿物等物质中提取的有效部位及其制剂。 6. 未在国内上市销售的中药、天然药物复方制剂。 7. 改变国内已上市销售中药、天然药物给药途径的制剂。 8. 改变国内已上市销售中药、天然药物剂型的制剂。 9. 仿制药。 1.2说明 注册分类1-6的品种为新药,注册分类7、8按新药申请程序申报,注册分类9的品种为已有国家标准的药品。 二、中药新药的研发及申报流程 中药新药的研发申报一般按以下程序进行: 选题立项一一临床前研究一一临床研究一一申报审批一一正式生产,其中,新药临床前及临床研究的主要 内容及注意事项分别列举如下: 2.1新药的临床前研究 (一)主要内容: 新药的临床前研究主要包括制备工艺(中药制剂包括原药材的来源、加工及炮制)、理化性质、纯度、检验方法、处方筛选、剂型、稳定性、质量标准、药理、毒理、动物药代动力学等研究。新发现中药材还应包括来源、生态环境、栽培(养殖)技术、米收处理、加工炮制等研究。 (二)注意事项: 从事新药安全性研究的实验室应符合国家药品监督管理局《药品非临床研究质量管理规范》(GLP)的相应要求,实验动物应符合国家药品监督管理局的有关要求,以保证各项实验的科学性和实验结果的可靠性。 2.2新药的临床研究 (一)主要内容:
新药研发的定义及过程
.2 新药研发的定义及过程从新化合物的发现到新药成功上市的过程通常被称为新药研发。新药研发是一项系统的技术创新工程,其通过试验不断改进药物性能,并证明该药物的有效性和安全性,同时经过严格的科学审查,最后取得发给的允许上市的证明文件。从完整意义上说,新药的研发过程需要历经“药物发现” 、“药物临床前研究”及“药物临床研究”三个阶段。通常,“药物临床前研究”及“药物临床研究”这两个研究阶段又被统称为“开发阶段” ,这三个阶段的工作相互关联并且各有侧重点。 “药物发现”环节是药物研发活动的开始,具有浓厚的科研探索性质,旨在找到并确定针对某一疾病具有活性的先导化合物。此阶段工作内容包括作用机理的研究、大量化合物的合成、活性研究等以寻找先导化合物为目的的研究工作,涉及到分子生物学、微生物学、生物化学、有机化学甚至基因组学等学科。药物发现处于新药研发早期,是一项创新程度及偶然性极高的科研活动,失败率极高,不但需要极高的科研水平,且投入巨大,所以往往由高校或者科研院所在从事基础研究中完成,研发经费来源主要依靠政府资助学校科研经费拨款,各级政府科研计划资助等,以及部分制药公司的资金投入。 “药物临床前研究” 是药物研发过程中最为复杂的环节,是承上启下的关键阶段,的是针对己经确定的先导化合物进行一系列非人体试验的研究,这一阶段的工作完成后需要向政府监管部门提出临床试验申请并接受技术审评,审评通过后方可进入下一研究阶段。此阶段工作内容包括药学研究,安全性评价、药代动力学评价等成药性研究内容参见图一,涉及到药物化学、药剂学、药物分析学、药理学、药物代谢动力学、药理毒理学等 其主要目学科。
