陶瓷材料介绍

陶瓷材料
陶瓷可以大致定义为金属元素与非金属元素的化合物。这里“陶瓷”一词来自英语“Ceramic”,大致相当于我国的“无机非金属材料”。因此,陶瓷所包括的范围远不止金属与非金属的化合物。除了以上定义所覆盖的材料外,以二氧化硅为主体的玻璃,碳化硅等无机非金属化合物都被归入陶瓷的范畴。碳材料也被算作陶瓷家族的一员。但上述定义为陶瓷材料的分类提供了方便,可以按照化合物中的非金属元素分成氧化物、氮化物、碳化物、氢化物、卤化物等。卤化物一般不用作材料,只以溶液形式作试剂使用。但在光学透镜和分析样品载体方面,卤化物还是有一定应用的。
Ceramic一词的远祖是希腊文“keramos”,意为“灼烧过的泥土”。人类使用陶器与瓷器的年代甚至要早于使用金属。直到现代,一提起陶瓷,人们不免想起饭碗、茶杯等用具,很难想到日常接触的砖头、水泥、混凝土也是陶瓷,更难想像近年来出现的高科技陶瓷了。
大约在60年代,人们开始开发新一代的陶瓷材料。被开发的陶瓷材料有的是传统材料的新利用,如氧化铝、碳化硅、氮化硅等,有的则是人工合成的新材料如碳化钨、碳化铌等。半稳定的氧化锆更是高科技的产物。人们给新一代陶瓷材料冠以各种各样的名称:高科技陶瓷、高性能陶瓷、精细陶瓷、新型陶瓷、高增值陶瓷、工程陶瓷及先进陶瓷等。在本书中我们倾向于使用“先进陶瓷”一词。
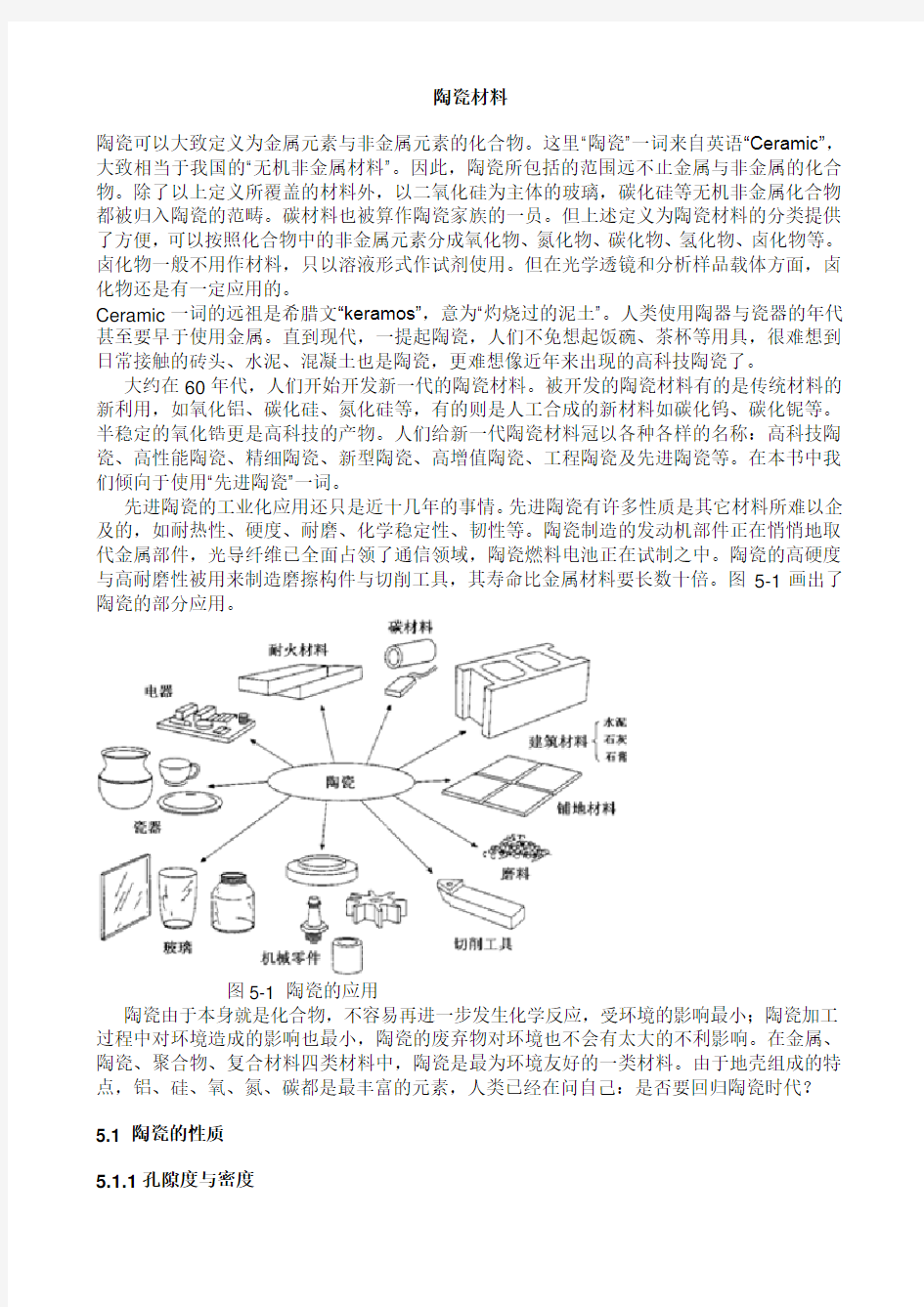
先进陶瓷的工业化应用还只是近十几年的事情。先进陶瓷有许多性质是其它材料所难以企及的,如耐热性、硬度、耐磨、化学稳定性、韧性等。陶瓷制造的发动机部件正在悄悄地取代金属部件,光导纤维已全面占领了通信领域,陶瓷燃料电池正在试制之中。陶瓷的高硬度与高耐磨性被用来制造磨擦构件与切削工具,其寿命比金属材料要长数十倍。图5-1画出了陶瓷的部分应用。
图5-1 陶瓷的应用
陶瓷由于本身就是化合物,不容易再进一步发生化学反应,受环境的影响最小;陶瓷加工过程中对环境造成的影响也最小,陶瓷的废弃物对环境也不会有太大的不利影响。在金属、陶瓷、聚合物、复合材料四类材料中,陶瓷是最为环境友好的一类材料。由于地壳组成的特点,铝、硅、氧、氮、碳都是最丰富的元素,人类已经在问自己:是否要回归陶瓷时代?
5.1 陶瓷的性质
5.1.1孔隙度与密度
陶瓷的密度具有特殊的含义。如果我们说铁的密度是7.8g/cm3,聚丙烯的密度是0.89 g/cm3,高密度聚乙烯的密度是0.94 g/cm3,意义是很清楚的。但当我们描述陶瓷的密度时,就必须说明是什么密度。因为陶瓷一般是由微小的颗粒烧结而成的,颗粒之间必然存在孔隙,于是就有了表观体积与真实体积之别,显然,表观体积为真实体积与材料内孔隙体积之和(这里“孔隙”的概念不是指晶格中原子排列的空隙,而是由于球形颗粒堆积时必然留下的孔隙,尺寸在微米或纳米级)。陶瓷的重量除以表观体积就得到表观密度,除以真实体积就得到真实密度。但所谓“真实”密度并不等于理论密度(r),理论密度是计算得到的晶格密度,而真实密度是用某种测定方法得到的不含孔隙的密度。孔隙体积占表观体积的百分数称为孔隙度。如果我们说某一陶瓷的孔隙度为20%,那么其表面密度就应是理论密度的80%。在实际情况中,陶瓷的密度一般低于理论密度的60%。要想提高陶瓷的密度,可采取很多措施。如使用宽分布的颗粒,让小颗粒嵌入大颗粒的缝隙中;或采用机械振动,拍打等手段。即使如此,也很难使陶瓷的表观密度达到理论密度的80%以上。要想进一步提高密度,就不能使用颗粒烧结的方法,必须采用新技术。气相渗滤法、定向氧化法就可以大大降低孔隙度,使表观密度达到95%以上。陶瓷中的孔隙分为开孔和闭孔。开孔指孔隙与外部相通,可以注入液体。闭孔则是完全被陶瓷基体包围的孔隙。闭孔只有通过理论计算,从表观密度与理论密度的差别来判断其存在,得到真实孔隙率。开孔可以采用ASTM C373的标准进行测定。这一标准的依据是阿基米德定律:一个物体在液体中所受浮力为该物体所排开液体的重量。阿基米德定律的另一种表述则更为有用:物体在液体中的重量等于该物体的干重量减去所受的浮力。只须称三个重量:干燥重量W D,孔隙中充满液体后的重量W S以及在液体中且充满液体后的重量W L,就能够计算陶瓷的表观密度与表观孔隙率。
表观体积: (5-1)
真实体积: (5-2)
表观密度: (5-3)
真实密度:(5-4)
表观孔隙率: (5-5)
真实孔隙率:(5-6)
如果用水作测量液,上述公式中的d L=1,计算就能进一步简化。
例5-1:碳化硅的理论密度r=3.2g/cm3。有一碳化硅制品干重量为360g,浸饱水的重量为385g,水中重量为224g,求其表观密度,表观孔隙率,真实孔隙率及闭孔的体积分数。解:W D=360,W L=385,W S=224,d L=1。
表观密度
表观孔隙率
真实孔隙率
闭孔的所占百分数应为真实孔隙率减去表观孔隙率:30-15.5=14.5。闭孔在孔体积中的分数为14.5/30=0.483
陶瓷的孔隙从两个方面影响其强度。第一,它会形成应力集中。从第二章我们知道,圆形孔边缘上的应力为平均应力的3倍。如果孔隙不是圆形,应力集中的情况更严重。第二,孔隙的存在减小了实际截面积,材料所承受的负荷高于表观上的应力。因此,孔隙度越高,陶瓷的强度和模量也就越低。
5.1.2磨损阻力
磨损的定义是表面物质的减少。磨损是机械故障或坏损的主要原因之一。我国每年因磨损而造成的损失在几十亿元以上。而使用陶瓷材料则是降低这项庞大开支的有效办法。造成磨损的机理很多。两个表面的粘结会使一部分表面物质被带走;表面粗糙则会使凸出部分被磨掉;如果两个表面硬度相差悬殊会产生切割;含硬颗粒的流体冲击或冲刷表面会造成磨蚀,等等。
测定材料的抗磨损性能有许多方法。最新的一种方法是用一种长方体样(100×25×6mm)。将样品装在一根轴上,轴带动样品在一个装满磨料的容器中转动。测定磨擦前和磨擦后样品的重量差,可以得出样品的抗磨损性能。据说这种方法最能代表实际使用情况。还可以用磨擦寿命因子来表征抗磨损性能。因子值越高,寿命越长。
Alanx公司最新开发出CG系列抗磨损金属陶瓷。其中CG896是碳化硅颗粒在氧化铝和某种合金中的复合材料。碳化硅和氧化铝都是耐磨的,合金则是作为两种陶瓷的粘结材料。图5-2比较了CG896和其它材料的磨擦寿命,可以看出这种材料在耐磨方面是极为优越的。
图5-2 各种材料耐磨性的的比较
5.1.3断裂韧性
陶瓷是典型的脆性材料。陶瓷不仅脆,而且对裂缝非常敏感。我们都看见过用玻璃刀划玻璃。只要玻璃上有一道划痕,就可以从这道划痕开始使玻璃断成两半。即使是从表面上看不出裂纹,内部细小的裂纹也足以使陶瓷制品断裂。而金属与聚合物材料就不同。既使是很脆的聚合物材料如聚苯乙烯,对裂缝或裂纹也不是敏感到这个程度。图5-3是典型金属与陶瓷材料的应力-应变曲线的对比。金属能够发生较大的塑性形变,而陶瓷只有很小的弹性形变,看不
到屈服点。缺乏韧性是限制陶瓷应用的最大障碍,所以陶瓷的韧性受到了较多的关注。
图5-3金属与陶瓷的典型应力-应变曲线
同其它材料一样,陶瓷韧性的度量也是用临界应力强度因子K1C。K1C有时也称作断裂韧性。1的含义指外力作用于x轴,产生正应力。如果外力作用的结果是产生剪应力,断裂韧性就应是K2C。测定陶瓷断裂韧性的方法如图5-4所示,使用的样品有两种:单缺口试样和Chevron试样。二者的区别仅在于开缺口的方式不同。单缺口试样是平缺口,如图5-4(b)所示。Chevron试样开的是Chevron缺口,如图5-4(a)所示。Chevron缺口的好处是裂缝在扩展过程中的扩展速率越来越慢,因为阻力越来越大。两种样品都能够直接测定断裂韧性。单缺口样品的计算公式为:
% (5-6)
其中:P = 外力
a - 裂缝长度
S1、S2 - 上、下辊的间距,如图5-4所示
B - 样品厚度
W - 样品高度
Y - 无量纲校正因子
断裂韧性的量纲为Mpa.m1/2。一旦受力条件超过临界应力强度因子,材料就会断裂。外力越大,裂缝长度越长,材料就越容易断裂。无损探伤所能探测的裂缝下限为50μm,而导致陶瓷断裂的裂缝往往小于50μm。所以陶瓷的脆性成为先进陶瓷开发应用的瓶颈。在本章中我们将会看到,在陶瓷的增韧方面已经取得很大进展,韧化陶瓷的断裂韧性已经达到与金属同数量级的水平,见图5-5。
图5-4 断裂韧性的测定图5-5 金属与陶瓷的挠曲强度与裂缝尺寸关系
(a)单缺口试样(b) Chevron试样
5.1.4抗热冲击性
热冲击指材料经历温度突变。例如发动机的转子要在2s内在340°C与1230°C之间变化一周。目前设计的汽车发动机转子要求在2s内在室温与1200°C之间变化一周。这种骤冷骤热会导致材料的机械破坏,尤其是陶瓷材料。金属没有热冲击的问题。因为金属有大量自由电子,可以很快将热量分布均匀,且金属较容易发生弹性形变和塑性形变,不会因为骤冷骤热积蓄很大的内应力。由于陶瓷传热系数很低,局部受热会引起较大的应力。加之陶瓷的脆性,很容易造成开裂。如果一种材料具有同素异构性且在温度变化过程中会发生相转变,热冲击就会直接转化为机械冲击。因为相转变必须伴随着体积的变化,这一变化往往比热膨胀要大。例如二氧化锆在1000°C以上为正交晶系,在1000°C时转变为单斜晶系,并伴随剧烈的体积膨胀。这一膨胀往往会使材料崩裂。考虑材料的抗热冲击性能时,必须同时考虑弹性模量(E)、线膨胀系数(a)、导热系数(k)、拉伸强度(s)与断裂韧性(K1C)。例如,硅酸锂铝(LAS)就具有极低的热胀系数(2.0×10-6/K),尽管其导热性很低,强度与模量都很低,韧性也差,却是理想的抗热冲击材料。此外,陶瓷的孔隙率、颗粒尺寸等都是值得考虑的因素。如上所述,陶瓷中的孔隙是造成应力集中的隐患,对抗热冲击性能的影响最大。
陶瓷材料也并非抗热冲击性能都差。结构比较简单的陶瓷如碳化硅,由于碳与硅的原子尺寸差不多,具有较高的导热系数,基本不受热冲击的影响。
为定量评价材料的抗热冲击性,可以用一种抗热冲击指数(T SI)来衡量:
T SI = (5-7)
式中 s -拉伸强度
k -导热系数
a -线性热胀系数
E -弹性模量(杨氏模量)
从式(5-7)可以看出,对抗热冲击性质而言,导热系数越大越好,而热胀系数越小越好。表
5-1是一些材料的抗热冲击性:
表5-1 一些材料的抗热冲击性质
5.1.5辐射系数
当一个表面受到照射时,它会吸收部分或全部辐射(能量),也会反射部分或全部辐射。被吸收的能量分数称为辐射系数(e)。黑体(理想吸收体)的辐射系数为1,理想反射体的辐射系数为零。于是我们看到,这个名称语意正相反,按照定义应该称为吸收系数。但我们仍保留其原来的字面。
辐射系数也是陶瓷的一个重要性质,尤其是在高温下工作的陶瓷。内燃机涡轮金属零件上的陶瓷涂层就必须具有低导热系数与低辐射系数。这样就能对金属零件既起到化学保护作用,又起到热保护作用。更贴近生活的一个例子是节能玻璃。也具有很低的辐射系数,在夏季能够反射更多的阳光。反过来,用于太阳能发电或取暖的设备需要吸收更多的太阳能。
5.2陶瓷材料的加工
陶瓷的加工过程一般可分为两个阶段:冷阶段与热阶段。冷阶段是将陶瓷粉体预制成型坯。制备过程可能要使用粘合剂和压力。有时只用水就能制成型坯。热阶段是将型坯加热到很高温度,一方面脱除型坯中的所有液体,一方面使粉体粒子粘结在一起,形成一个整体。这一过程称为烧结。部分(不是全部)陶瓷在冷阶段之前有一个粉体制取的过程。这个过程的起点可能是采矿,将矿物转化为所需的化学物质,再加工成所需的粒度尺寸与尺寸分布。在这些加工过程中,不免带入物理缺陷和化学缺陷。物理缺陷包括粒子上的微孔和缺口,化学缺陷则指混入不需要的元素或杂质。这些缺陷对普通的陶瓷生产没有什么影响,但对先进陶瓷尤其是功能陶瓷影响很大。所以我们必须了解从粉体制取开始的每一环节,因为第一环节造成的结构因素都要带到最后制品之中。
5.2.1粉体的制取
制取粉体是陶瓷制备的第一步,是陶瓷材料环的第一节。绝大多数陶瓷制品是通过粉体的烧结制备的。制取方法因材料而异,下面对一些重要陶瓷材料作简单介绍。
氧化铝在自然界中以刚玉的晶体结构存在。将铝矾土粉用苛性钠洗涤,可产生氢氧化铝沉淀。氢氧化铝经热处理就转化为氧化铝。大部分氧化铝粉体被用于电解生产金属铝。少部分用于生产陶瓷,包括翻砂模具、高温水泥、摩擦部件、耐火材料等。
氧化镁从海水中的MgCO3制取。先从海水中取得氢氧化镁,再加热转化为氧化镁MgO。同氧化铝一样,大量的氧化镁用于生产金属镁,但少量的氧化镁用于制备高温绝缘与耐火材料。
碳化硅(SiC)用Acheson法生产。将电流通过SiO2与焦炭的混合物,使之达到2200°C。在高温下焦炭与二氧化硅作用生成碳化硅与CO气体。碳化硅也能用其它的碳源生产,例如稻糠。碳化硅是最有希望制造内燃机的陶瓷材料。
氮化硅可以用硅的金属化合物与氮气在1250°到1400°C下作用合成。生成的是a体与b
体的混合物。粉碎后即可使用。高纯度的氮化硅可以用SiO2与氮气作用产生,也可以用SiCl4与氨作用生成。
氧化锆通过四丁氧基锆在乙醇中水解得到。在氧化锆中混入少量氧化钇可以起到显著的增韧作用,这种增韧作用是人们广泛关注的热点。氧化锆可用于加工铜棒的挤出模具以及作为内燃机零件的等离子喷涂保护膜。
二氧化钛大量用作涂料、塑料及纸张的增白,也有一部分用作陶瓷。它在自然界中以钛铁矿和金红石矿的形式存在。金红石中二氧化钛的含量高达97%。当然,要加工成我们常用的钛白粉还要经过一系列复杂的化学过程。
以上只列举了几种陶瓷粉体的制取过程,它们代表的仅是传统的粉体制备工艺。更先进的工艺有金属有机聚合物的热解,碳热还原法、等离子体合成、激光合成等。
5.2.2冷压与烧结
这一步是将粉体制成型坯。首先要与粘合剂、润滑剂等混合。粘合剂都是有机物质,可以在稍后的加热过程中除去。混合时总要加入一定量的水分。如果水分量在0~4%,就称为干压;如果水分在10%~15%,就称为湿压。粘土类陶瓷制作时就必须使用湿压。简单制品、小型制品都只使用单向压机,而形状复杂或较大型的制品就必须使用均匀压力装置,以达到较高的密度。均匀压制的方法也分为干法与湿法。但不是根据型坯中的水分,而是根据传递压力的介质分。湿法见图5-6(b)。粉体被密封在不透液体的柔性模具中,四周都是液体。压力施加到液体上,通过柔性模具传递到型坯上。干法均匀压制见图5-6(a)。它也是使用弹性体制造的柔性模具,也是通过液体加压。与湿法不同的是,液体不是直接将压力传递到模具上,而是先传递到外层弹性体上,再通过这层弹性体再传递到内层的模具上。有了外层弹性体,就使操作方便得多了。不仅提高了工作效率,还提高了尺寸控制精度。
图5-6 陶瓷型坯的均匀压制(a)干法(b)湿法
型坯压制完成后,需要在高温下烧结,即使颗粒发生充分的流动,互相粘结在一起。烧结过程可大大增加型坯的密度,达到90%~95%。烧结过程中密度增加,粒度也会增加。粒度的增大必须加以控制。因为大粒子伴随着大间隙,对制品的强度不利。当然,间隙有利于隔热,作为绝缘材料是求之不得。但作其它材料是非常不利的。不同陶瓷制品对烧结有不同的要求。例如Si3N4必须在封闭体系中在有压力的氮气下烧结,否则就会发生分解。具有高介电损耗
的陶瓷可以用微波加热,如Al2O3、ZrO2等。利用介质加热是对陶瓷粒子表面加热,在粒子内形成温度梯度。而使用微波加热是使整个粒子均匀受热,可降低烧结温度,限制大粒子的形成,能够提高制品的强度。某些材料的烧结是通过低熔点相的粘结,尤其是硅酸盐类陶瓷。低熔点组分首先熔融并发生流动,充满粒子间的缝隙。不仅将粒子粘结在一起,而且可使制品的密度接近100%。这一技术称为液相烧结法,低熔点相则称为烧结助剂。
5.2.3热压
在陶瓷粉体转变为制品的过程中,有时可以分成清楚的冷压与热压两个阶段,有时则二者相结合,一次成型。一种单向热压装置见图5-7。在压力条件下烧结,促进粒子间的接触,使之结合更加紧密,可使密度高于98%。热压温度一般为0.5Tm(K)。热压温度决定了设备的类型。如果压制温度在2000°C以上,就要使用石墨及碳化硅等耐热部件。热压压力一般在6.9~34.5MPa的范围。表5-2对比了热压与冷压烧结的Si3N4的不同性能。
表5-2 热压与冷压烧结Si3N4的性能比较
图5-7 陶瓷热压装置
和冷压技术一样,均匀热压能够提供高密度、高尺寸精度的制品。但均匀热压不能使用液体来传递压力,只能用惰性气体氦气或氩气。但惰性气体在高温下会被离子化,形成的等离子体会与型坯作用。为防止这一点,型坯必须被完全密封。对热压模具的材料要求也非常严格,既要耐高温,又要耐高压(242MPa)。温度较低时可采用玻璃或钢模具,温度较高时就要使用石墨或钼等耐高温材料。均匀热压设备昂贵,技术复杂,只用来制造磁记录头及内燃机关键部件等高值产品。
5.2.4化学加工方法
5.2.4.1 溶胶-凝胶法
溶胶-凝胶法是通过烷氧化物的水解合成氧化物的化学加工方法。溶胶是指直径小于0.1mm 的胶体粒子在液体中的稳定悬浮液,或者说是胶体粒子与液体的混合物,胶体粒子可以在液体中长时间悬浮而不会沉淀。或因胶体粒子之间发生化学反应,或因胶体粒子间发生物理凝聚,可使体系粘度增大而失去流动性(见图5-8)。溶胶失去流动性即称为凝胶。由粒子间作用形成凝胶的过程称为粉末过程。虽然这种方法的名称是溶胶-凝胶法,反应的起点也可以是溶液,例如烷氧化物通过水解直接形成凝胶。起点为溶液的过程称非粉末过程。溶胶-凝胶法可以制备陶瓷、玻璃与玻璃陶瓷。最后产物为晶态或非晶态取决于所用的原料与加工工艺。
图5-8 胶体粒子间的凝聚
溶胶-凝胶法可以分为单组分过程与多组分过程。单组分过程可以用硅陶瓷的制备来说明。制备的起点配方为43%(体积分数)四氧乙基硅,43%乙醇,14%水。四氧乙基硅水解生成硅醇与乙醇,硅醇之间再通过缩聚连接成为体型的硅陶瓷(图5-9)。在多组分过程中是由多种烷氧化物形成溶胶或溶液。典型体系由表5-3所示。多组分过程中会发生的问题是不同的烷氧化物的水解速率不同,造成体系的不均匀性。解决这一问题的途径之一是先对活性低的组分如四氧乙基硅进行水解,然后再加入活性高的组分如三丙氧基钛和铝等。反应起点的溶液或溶胶粘度很低,随着反应的进行,粘度逐渐增大。到了某一点,溶液或溶胶转变为凝胶。可以想像,当最后形成无限大网络的最后一个化学键生成的那一刻,就是溶胶-凝胶转变点。溶液或溶胶向凝胶转变的不同在于,溶液-凝胶转变是不可逆的,而溶胶-凝胶转变是可逆的。溶液-凝胶转变没有体积变化,而溶胶-凝胶转变涉及粒子的凝聚,发生体积收缩。
表5-3 单组分与多组分烷氧化物溶液配方
图5-9 硅凝胶的形成过程
凝胶化转变之后,体系由两相组成:氧化物的骨架与溶剂。要制成陶瓷制品,必须将溶剂脱除,即将凝胶干燥。
溶胶-凝胶法最广泛的应用是制造薄膜与涂层。制膜或涂层的主要方法是浸渍。使基材在溶液中通过,基材表面就会留下一层膜。膜的厚度取决于溶液粘度、表面张力、基材牵引速度和溶液中氧化物的浓度。设法将膜与基材相分离,就制得陶瓷薄膜。如果需要单面涂覆,就要使用流延法:使基材固定,将溶液均匀涂在基材表面。不管用什么方法,一次涂覆的厚度在50~500nm之间。更厚的涂层就需要多次浸渍或涂覆。
溶胶-凝胶法的另一应用是制造纤维。如果使用溶液,可以控制溶液的粘度,在最合适的粘度将溶液拉成纤维;如果使用溶胶,可以在溶胶中添加粘合剂,采用挤出的方法制造纤维。最新探索的方法是将溶胶或溶液涂覆在有机纤维的表面上。除掉芯层的有机纤维,外面的壳层就能坍缩为陶瓷纤维。用这一方法还有可能制造出中空纤维。
陶瓷粉体的溶胶或凝胶也可以通过浇铸制成所需形状。将溶胶注入模具,并使粒子在模具内发生反应生成凝胶。待凝胶的形状固定之后便可脱除模具。使凝胶干燥,再进行烧结,就可以得到具有尺寸精度的制品。用这种方法可以制造陶瓷制品,也可以制造陶瓷复合材料。溶胶-凝胶法的优点是高纯度、高均匀性和低温操作。由于组分间的结合是在溶液中完成的,结合的尺寸是纳米级的,所以热压密化温度只需熔融温度的1/2到2/3。缺点是对原料要求高,提高了大件制品的成本。但在薄膜或纤维制造等特殊领域,本身就要求材料的高纯度,溶胶-凝胶法就成为首选方法。
5.2.4.2 气相加工法
气相加工法的过程是,加热一个固体使之转变为蒸汽。当这一蒸汽与冷的基体表面接触时,会迅速凝结为固体,粘附在基体表面上。用此类方法可在材料表面涂上一层牢固的薄膜,达到表面改性、表面保护或表面装饰等作用。化学气相沉积(CVD)与物理气相沉积法(PVD)是两种蒸汽加工方法(详见第八章)。用这种技术可以在任何金属和陶瓷材料表面涂密实的陶瓷或金属膜,膜的厚度可任意控制,并可使陶瓷与金属紧密结合。这些优点是传统陶瓷加工所不能比拟或无法做到的。
化学蒸汽渗透法(CVI)是CVD技术在制备复合材料中的应用。它是将气体、液体或溶胶渗透沉积到型坯的缝隙中,通过化学反应生成复合材料的基体,原来的型坯就成为增强材料。与CVD不同的是,CVD是将气相反应得到的材料沉积到表面,而CVI是沉积到纤维型坯中的纤维表面或纤维之间,形成复合材料的基体。通过化学蒸汽渗透法可生成多种基体,如硼化物、碳化物、氮化物、氧化物等。这种方法最大的优点是制备温度低,可以避免损害增强纤维;也不需要使用高压。可用于生产碳碳复合材料或陶瓷-陶瓷复合材料。例如制备碳化硅纤维在三氧化二铝中的复合材料。碳化硅纤维直径只有10mm,经受不住传统加工方法中的应力与压力。而化学蒸汽渗透法使用低压力与气体原料,渗透纤维的每一个缝隙,将基体材料包复在纤维上,最后使之成为一个整体。图5-10是一个CVI炉的示意图。
在纤维预制件中预置一个温度梯度,同时还施加一个反方向的气体压力梯度,迫使反应气体
强行通过型坯低温区。由于温度低而不发生反应。当反应气体到达温度较高的区域后发生分解并沉积。在纤维上与纤维间形成基体。在此过程中,温度界面不断由型坯顶部的高温区向底部的低温区推移。由于温度梯度与压力的存在,避免了沉积物将孔隙过早的封闭,提高了沉积速率。
图5-10 化学蒸汽渗透装置
由于CVI是个分子过程,基体材料一分子一分子地沉积在缝隙中,经济性较差。反应熔体渗透法可以弥补这一不足。CVI需要几天的过程,反应熔体渗透法只需几分钟,花费的成本也仅有CVI的一半。例如制备碳化硅/碳化硅复合材料,先将碳化硅纤维与碳纤维制成型坯。用熔融硅进行渗透,硅与碳反应再生成碳化硅,包复在原有的碳化硅纤维上。这种方法也能制造复杂形状的制品,尺寸精度高,制品密度接近100%。
5.2.4.3 反应烧结法
反应烧结有别于传统的固相烧结与液相烧结。图5-11演示了二者的不同。图5-11(a)是物理融合过程,融合的同时伴随着体积收缩。图5-11(b)是化学融合过程,材料体积可保持不变。物理融合依赖的是颗粒的熔融,需要2000°C以上的高温,而化学融合是通过粒子间的化学反应,只需1400°C。反应融合碳化硅就是用这种方法加工的。将碳化硅与碳的粉末混合物制成所需形状,然后在高温下与硅的蒸汽或硅的熔体作用。碳与硅反应生成碳化硅,将原有的碳化硅颗粒融合起来。过剩的硅渗透到颗粒的每一个缝隙,最后形成无孔隙的复合材料(SiC/Si)。这种复合材料还有一种制法,就是将碳纤维的编织布浸到熔融的硅中,碳纤维逐步转变为碳化硅纤维分散在硅基体中。控制原料与反应条件,可以获得各种所需性能的材料。
图5-11 (a)物理融合(b)化学融合
反应烧结氮化硅的加工方法与此类似。先用硅制成型坯,置于氮气、氮/氦或氮/氢混合气
体中。先将温度升至1250°C,氮气开始渗入型坯与硅作用生成Si3N4,逐步将温度升至略低于硅的熔点附近以加快反应。这种反应要持续约一个星期,可以得到具有良好尺寸稳定性、抗热冲击性、良好导热性的陶瓷材料。唯一的缺点是材料仍具有通孔,耐氧化性略显不足。如果在充分的氧气下,会与氮化硅作用在表面生成二氧化硅(SiO2)。这层二氧化硅会起到保护膜的作用,使氧气不能进到材料内部。这种氧化称为钝性氧化。如果氧气不足,就会生成气体一氧化硅(SiO)。此类氧化会连续不断地进行下去,称为活性氧化。在氧气不足的外层空间,最容易发生这种反应。因此氮化硅制品都预先氧化生成一层二氧化硅,就能对内部材料起到保护作用。
5.2.4.4 金属定向氧化法
金属定向氧化法(Dimox法)是由熔融的金属与氧气作用生成陶瓷基复合材料,由Lanxide 公司于1983年开始研制,1989年生产第一批产品。用这种方法制备的零件用于汽轮发动机、活塞发动机、火箭发动机、高温熔炉等。图5-12是这种方法的演示。先将增强填料制成型坯,其尺寸与最后制品完全一致。型坯可以用任何方法制备,不管是冷压、均匀热压、浇铸、还是注射成型。型坯外壳是一层阻隔材料,保证基体严格按照设计的形状和尺寸充满型坯。将型坯放在基体金属锭上面,置于氧气气氛下,加热到足以使金属熔融的温度。熔融的金属与氧气迅速作用生成氧化物,氧化物向型坯扩散并最终充满型坯,成为复合材料的基体。金属的氧化会生成固体陶瓷层,阻隔了金属的进一步氧化。此时可加入助剂镁或硅,可帮助熔融金属对陶瓷的润湿并降低陶瓷粒子的颗粒稳定性,从而保证了金属不断被氧化。这一方法的奇特之处在于仿佛金属是被自己的氧化物吸着走,一直向材料内部深入,而且在运动过程中不断被氧化,直到金属被耗尽或型坯被充满。金属氧化物在充满型坯的过程中几乎不发生尺寸变化,保证了最后制品的尺寸精度和密度。陶瓷加工过程中难以克服的问题是产生孔隙和尺寸收缩,而用金属定向氧化法可以完全避免这两个问题。
这种方法的一个示例是SiC纤维增强的Al2O3。SiC的形式是迭层纤维织物。用金属铝定向氧化形成氧化铝基体。其主要力学性能见表5-4。抗热冲击性能也非常优异,可以加热到1200°C迅速冷却到室温而只有轻微的损伤(强度降低16%);而单独的碳化硅或氧化铝从200°-400°C淬火就会完全损坏。Al2O3基体也可以用SiC颗粒增强。产品具有优异的耐磨性能,广泛用作耐磨部件和衬里。
表5-4定向氧化法材料的力学性能
金属定向氧化法的一个变例是硼化锆(ZrB2)碎屑增强的碳化锆(ZrC)。为形成这种复合材料,金属锆在1850-2000°C下的熔体定向地与石墨模具中的B4C粉末作用,同时生成两个陶瓷相ZrB2与ZrC,ZrB2以六方晶片的形式分散于ZrC 连续相之中,也有少量金属锆存在于连续相中。金属锆的含量对材料韧性有很大影响。低金属含量时的韧性为10-12 MPa·m1/2,高金属含量时可提高到15 MPa·m1/2。此类复合材料可以短时间在2700°C的高温下工作,被用在火箭发动机中,但不能在高温下长期工作。利用此类复合材料强度、韧性、耐磨性与生物相容性的综合性能,可以用于制造假肢。
图5-12定向氧化法
用金属定向氧化法可以很容易地进行外形复制,如图5-13所示。将被复制金属件嵌入型坯,型坯中含有增强的碳化硅粒子。这个被复制的金属件同时又充当了定向氧化的金属原料。当温度升到金属熔点以上时,液体金属一面向型坯渗透,一面被氧化,最后以氧化物的形式完全充满型坯。金属耗尽留下的空间恰恰就是要复制的形状。
图5-13外形复制
5.2.4.5 聚合物前驱体法
一种独特的加工技术可以聚合物为起点加工出陶瓷制品。这种方法不能生产氧化物,却可以生产出碳化硅、氮化硅、氮化铝、氮化硼与氮化钛。广泛应用的制品形式包括纤维、涂层、非迁移性粘合剂与陶瓷基复合材料。制造陶瓷所用的聚合物都是硅树脂,如聚硅苯乙烯、乙烯基聚硅烷、聚硅氨烷、聚羰基硅烷等。从聚合物制造陶瓷,第一步是将聚合物制造成所需的形状,或为纤维,或为各种形状的制品。第二步是将聚合物转化为陶瓷,可以在惰性气体气氛下加热到1000°C以上,使体系中只剩下SiC或Si-N-C结构。也可以在常温下对聚合物进行氨解,得到Si2N2O、Si3N4的粉末或纤维。热解的结果使材料重量损失,体积收缩,密度增加。按重量计的得率在60%-90%,而按体积计的得率只有25%-35%。体积收缩对纤维制品影响不大,对涂层就会有较大影响。聚合物前驱体在陶瓷中的用途有四方面:纤维、复合材料、涂层和非挥发性粘合剂。图5-14是这些材料的加工工艺路线。
图5-14 聚合物前驱体法制备陶瓷工艺路线
有两种聚合物前驱体的陶瓷纤维已经工业化,商品名分别为Nicalon和Tyranno。两种纤维的直径都可以小于15mm,都可以进行纺织。
用聚合物前驱体制造陶瓷基复合材料,前阶段的工艺路线与聚合物基复合材料相似。首先是纤维的预浸及型坯的制备。可以是纤维预浸后纺织成织物,也可以是纤维纺织成织物后再进行预浸。预浸料可通过压制、树脂转移模塑、纤维缠绕等方法制成型坯。预成型之后,聚合物前驱体就被固化和热解。热解过程中聚合物会收缩,产生孔隙与裂缝。要得到密实的材料,需要进行多次浸渍与固化、热解的循环过程。根据纤维的用量与热解后的产率,循环次数可为4~10次。
有一种复合材料是用Nicalon纤维的织物增强的,基体材料为聚硅氧烷。聚合物在1200°C 热解后的产率为80%,化学组成为Si:35% ,C:45%,O:20%。在6次浸渍/热解循环后,达到2.15g/cm3的密度。
聚合物前驱体制备的涂层可以赋予碳材料与金属材料抗氧化性与耐磨性。一种制法是将硼氧烷与聚羰基硅氧烷溶于一种有机溶剂,喷涂或刷涂在基底上。加热到200-250°C以脱除所有的溶剂,并保证涂层具有10-250nm的厚度。涂层在600-900°C的温度下热解。涂层厚度可以超过250nm,但必须分层进行涂复和热解。由于使用聚合物作原料,涂复工艺非常简单,成本也远远低于CVD等过程。
用聚合物前驱体作为陶瓷粉末的粘合剂,可以提高型坯的强度,降低烧结时的收缩。由于聚合物的密度低于陶瓷,而型坯的密度主要取决于陶瓷颗粒的堆积。聚合物对烧结后制品的密度贡献取决于聚合物的产率。如果产率为50%,就相当于为最后制品贡献了9%的密度。在一项工作中,采用聚硅烷、聚硅氨烷与Si3N4混合,同时加入Al2O3与Y2O3烧结助剂。型坯在900°C、氮气氛下热解,再在1700-1900°C,高压氮气下烧结。所得制品密度为2.94~3.30g/cm3。
以聚合物为前驱体为陶瓷的加工开辟了一条新路。不仅操作简便,且能得到独特的结构与性质。目前所用的前驱体都是含硅聚合物,将来会有更多的聚合物成为陶瓷材料的前驱体。
5.3工程陶瓷材料
5.3.1 氧化物
氧化物是最大的一族陶瓷材料。氧可以与几乎所有金属形成化合物,也可以与许多非金属元素化合。氧化物可分为单氧化物与复氧化物两大类。单氧化物是氧与另一种元素形成的二元化合物,而复氧化物是氧与两种以上元素形成的化合物。单氧化物是按氧原子数与另一种原子数的比例分类的。以字母A代表另一种元素,单氧化物可以有A2O,AO,A3O4,A2O3,AO2,AO3等类型。AO型中比较重要的有氧化镁(MgO)、氧化锌(ZnO)和氧化镍(NiO);AO2型中较重要的有二氧化硅(SiO2)、二氧化钛(TiO2)和二氧化锆(ZrO2);A2O3型中最重要的是三氧化二铝(Al2O3)。氧化物体系由图5-15所示。
图5-15氧化物的分类
二氧化钛(TiO2)有三种晶形:低温下稳定的锐钛(anatase)、板钛(brookite)与高温下稳定的金红石(rutile)。锐钛与板钛在400~1000°C的温度范围内会不可逆地转化为金红石。
氧化铝(Al2O3)是在铝钒土(Al2O3·2H2O)的加热过程中制得的。在不断升温的过程中,会产生一系列不同结构的氧化铝,这些结构都是不稳定的,最终都会不可逆地转化为a- Al2O3。a- Al2O3具有六方的刚玉结构,是1200°C以上唯一可用作结构材料与电子材料的稳定形式。另一个稳定结构是g- Al2O3,但只能在催化方面应用。故在本书中Al2O3特指a- Al2O3。由于O-Al键的键能高达400kcal/mol,Al2O3具有突出的物理性质,硬度是氧化物中最高的,而熔点高达2050°C。
硅酸盐是地壳中最丰富的矿物,有正式名称的硅酸盐就有几千种。大多数硅酸盐都不是人工合成的,而是直接取自矿物,用于耐火材料、砖瓦、瓷器和陶器。一般说来,硅酸盐的力学性能低于氧化铝、氧化锆等单氧化物,但在民用领域,各种硅酸盐得到了广泛的应用,也有少数作为工程陶瓷应用。我们只以堇青石和叶蜡石作为此类工程陶瓷的代表加以介绍。
堇青石(Cordierite, 2MgO·2Al2O3·5SiO2)的热胀系数极低,所以有很高的抗热冲击性能。其力学性能也不低,所以被用在发动机过滤器、火花塞、汽轮机换热器的叶轮等热敏感部位。堇青石有两种结构形式,天然存在的形式是四方晶形,人工合成的形式是六方晶形。为保证纯度与加工重复性,工程应用中都使用六方晶形的合成堇青石。
叶蜡石(Pyrophyllite)是一种层状结构的硅酸盐,化学组成为Al2(Si2O5)2(OH)2。它的用途非常广泛。由于价廉易得,不仅可以烧制成各种陶瓷,还可以机械加工,在西方被称为“魔石”。层间作用力主要是范德华力,因此材料较软,易于机械加工。热处理时,在800°C发生脱羟基反应,在1100°C时发生相转变,产生白硅石(SiO2)和铝红柱石(3Al2O3·2SiO2)的双相结构。在脱羟基和相转变过程中尺寸变化仅有2%。
铝红柱石在自然界非常罕见,主要矿藏发现于英国Mull岛,故称为Mullite。其热胀系数低于Al2O3,故具有更好的抗热冲击性,尤其是在1000°C以上的温度。工程上应用的铝红柱石都是人工合成的。最初的合成方法是将Al2O3与SiO2在1600°C下烧结,但强度与韧性都不高。采用新技术合成的新一代铝红柱石,具备了高强度和高韧性,强度达到500MPa,断裂韧性可达到2-4MPa·m1/2。铝红柱石的传统用途是熔炉中的耐火材料。工程化的铝红柱石
的用途大大加宽,包括电子元件的基板、保护性涂料、发动机部件和红外透射窗等。
表5-5氧化物陶瓷的性质
5.3.2 碳化物
一般意义上的碳化物可以分为三类:(1)离子碳化物,即碳与I,II,III族金属或镧系金属形成的化合物;(2)共价碳化物,只包括两种:碳化硅(SiC)与碳化硼(B4C);(3)间隙碳化物,包括许多与过渡元素形成的化合物,如IV族的钛、锆,V族的铌、钽,VI族的铬、钼、钨,以及VIII族的铁、钴、镍等。从工程的角度看,离子碳化物可以不必考虑。因为它们在空气中极不稳定,还容易与潮分作用分解为烃类。间隙碳化物虽然数量众多,但目前有工程价值只有碳化钨与碳化钛两种。主要碳化物的性能见表5-6。
5.3.2.1 碳化硼
在工业上碳化硼不单独使用,而是以与石墨的复合材料的形式使用。碳化硼是通过氧化硼与碳在熔炉中作用生成。这种共价的陶瓷很难制成100%密度的制品,所以常用石墨粉与碳化硼混合使用,形成两者的复合材料。石墨的加入降低了碳化硼的使用性能,但目前还找不到更好的助剂。工业上的碳化硼制品一般用热压法成型,少数制品先进行烧结,再进行均匀热压。热压条件为2100°C,35MPa,30min。典型的烧结条件为2200-2250°C,30min,压力只需10MPa左右。烧结后的均匀热压条件为2000°C,20MPa和120min。热压只能加工简单形状的制品,如管、板、轴向对称的喷管等。复杂形状的制品必须先经过烧结。碳化硼能够捕捉热中子,同时释放出低能粒子。5B10原子吸收中子后的蜕变并不放出高能射线:5B10 + 0n1 ? 3Li7 + 2He4
故其主要用途是中子吸收剂和屏蔽材料。
5.3.2.2 碳化硅
碳化硅有上百种结构,最简单的一种具有金刚石结构,每隔一个碳原子被硅取代一个。这种立方结构被称为b体,其它的六方和菱形结构合称为a体。碳化硅粉末用Acheson法生产。将电流通过SiO2与焦炭的混合物。当混合物温度升到2200°C左右时,焦炭会与SiO2作用生成SiC与CO。根据反应时间与温度的不同,还原产物可能是细粉末,也可能是团块。结团的产物则必须粉碎后使用,较细的级分可以用来烧结,较粗的级分直接用作磨料。
根据不同的用途,碳化硅可用三种方法加工。(1)将碳化硅粉末与第二相材料如树脂、金属、氮化硅、粘土等混合,然后根据第二相材料进行处理,将碳化硅粘结起来。(2)将碳化硅粉末与纯碳粉或纯硅粉混合,制成型坯。让碳与硅蒸汽反应形成碳化硅,新形成的碳化硅会将原有的碳化硅融合起来,这一过程称为自融合。如果让硅粉与氮气作用生成氮化硅,也可将
碳化硅融合起来。这两种加工技术都称为反应融合。(3)用碳化硼作助剂,烧结碳化硅制品。这种方法可得到高密度的制品。以上三种方法各有优缺点。第二相融合法多用于烧蚀与耐火材料。第二材料的性质限制了材料的应用。自融合碳化硅中常含有残留的硅粉,在温度高于1400°C时会熔融流出。用火焰或真空处理可除去这些游离硅。自融合时如果使用过量的碳就会避免硅的残留。自融合碳化硅比烧结产物抗氧化能力强。烧结碳化硅只能在非氧化场合使用。由于产物中含硼与游离碳,抗氧化能力较差。
碳化硅的膜、涂层与渗透加工产物不是用碳化硅粉末制造的,而是用化学气相沉积(CVD)或化学气相渗透(CVI)法制造的。
表5-6 碳化物的性能
5.3.3 氮化物
与金属相比,氮化物陶瓷的主要优势是耐高温性能,在1000°C以上仍能保持高强度;以及抗氧化与抗腐蚀性能。
氮化物家族中最主要的成员是氮化硅。氮化硅的粉末通过硅粉与氮气在1250-1400°C的温度下反应制得。氮化硅在陶瓷材料中的优势是抗热冲击性能,其导热系数几乎为Al2O3·TiC 的两倍,热胀系数却只有Al2O3的一半,是制造陶瓷发动机的有力竞争材料。使用氮化硅的主要问题是烧结比较困难。纯氮化硅在高温下不能发生有效的体积扩散,即粒子之间很难互相粘合在一起。欲得到密实的氮化硅材料,必须使用烧结助剂。氮化硅的性能,尤其是高温性能,主要取决于烧结助剂。氮化硅最有效的烧结助剂是Al2O3、氮化铝(AlN)与二氧化硅。氮化硅材料基本上都是氮化硅与其它材料的合金,而不用纯粹的氮化硅。氮化硅材料可以用许多不同的方法加工,根据加工方法的不同分为以下几类:反应融合氮化硅、热压氮化硅、烧结(无压)氮化硅、烧结反应融合氮化硅、均匀热压氮化硅等。不同加工方法的氮化硅性能不同,见表5-7。
表5-7不同方法加工的氮化硅的性能
由于在氮化硅的烧结过程中要加入Al2O3、AlN或SiO2等助剂,铝原子可能取代部分硅原子的位置,氧原子可能取代部分氮原子的位置,这样的结合体就形成了一类特殊的陶瓷—硅铝氧氮陶瓷。这种陶瓷具有Si6-zAl z O z N8-z的通式,晶格与b-Si6N8相似。这种氮化物的烧结要容易得多,但烧结过程中会有部分玻璃相形成。玻璃相限制了高温下的使用,但在较低温度下的优异性能仍使此类陶瓷有广泛的应用。
氧氮化硅从氮化硅和二氧化硅的混合物中合成。在Al2O3存在的情况下,具有一定的固体溶解性。可以用无压或压力烧结加工。氧氮化硅的性能略低于氮化硅,但由于其杨氏模量较低,热胀系数较高,在热机械方面有应用的潜力。
氮化铝具有较高的导热系数,在微电子工业中用作绝缘基板。用氮化铝粉末与密化助剂和CaO或Y2O3在1650-1800°C下在氮气氛中烧结而成。用Y2O3作烧结助剂时,会有钇铝化合物在颗粒边界形成。氮化铝的导热系数随Y2O3的含量迅速增加。这是由于当Y2O3含量很低时(<0.8wt%),钇铝化合物会在氮化铝颗粒外形成一层连续的外壳,阻止了氮化铝(导热系数50-90W/m·K)颗粒间的热传导。当钇的含量增加时,钇铝全结成较大的瘤(可达15mm),氮化铝颗粒之间能够直接接触。钇含量达到 4.2wt%时,导热系数可达160W/m·K。氮化铝的机械性能不高,且在800°C以上发生氧化,所以不能作为结构材料使用。
氮化硼的电子结构与碳相似,晶体有两种变体,一种类似于石墨(六方),一种类似于金刚石(立方)。六方氮化硼较软,具有片层结构,可以热压成型。材料具有各向异性,因为层片垂直于压力方向取向,不同方向上的导热系数与导电率大不相同。可以用化学沉积法制造坩埚一类薄壁制品。立方氮化硼的密度和硬度要高得多,用六方氮化硼在高温高压下制得,类似人造金刚石的制法。可用作磨料或切削刀具。
氮化硅基体的复合材料主要用碳化硅晶须和碎片增强,目的是提高韧性和高温强度。由于碳化硅晶须的存在,阻碍了氮化硅基体的收缩,使无压烧结更为困难。因此,氮化硅复合材料只能用热压法才能得到致密的产品。在从烧结温度冷却时,由于基体与晶须的热胀系数不匹配,材料内会产生应力。碳化硅为4.4×10-6/K,而氮化硅为3.2×10-6/K。这样,纤维会处于张力状态而基体处于压缩状态。因此使基体开裂的应力就应更高。在径向上,晶须会收缩而减弱与基体的结合,这样会使裂缝偏移并会使晶须容易拔出,也造成增韧。虽然碳化硅晶须的加入使强度略有降低,但有显著的增韧作用,报道的最高断裂韧性为10MPa·m1/2。上述各类氮化物的性能见表5-8。
表5-8氮化物陶瓷的性能
5.3.5金属陶瓷
顾名思义,金属陶瓷是金属与陶瓷的结合体,实际上是一种复合材料。其分散相是陶瓷颗粒,多为碳化物,如碳化钛、碳化钨等。基体是一种金属或几种金属的混合物,如镍、钴、铬、
钼等。实际上金属仅起到粘合剂的作用,将坚硬的陶瓷粒子粘合在一起。金属陶瓷家族中最著名的成员是钴粘合的碳化钨。
图5-16金属陶瓷的制备过程
碳化钨/钴的起点原料是钨的粉末,通过碳化将钨粉转化为碳化钨。然后将碳化钨粉末与钴一起球磨,一方面减小碳化钨的粒度,一方面将钴涂到陶瓷表面。涂饰好的粉末按粒度分级,取所需粒度压成型坯。型坯在真空下或氢气氛中烧结成型。所谓烧结不过是将金属熔融,把陶瓷粒子彻底“焊”在一起。图5-16是金属陶瓷的一般制备流程。
陶瓷金属比任何工具钢都硬,耐磨性能极佳。可作切削工具,可作任何软、硬表面的磨擦件。如果单纯使用陶瓷,因为其脆性,不能用作切削工具、模具或振动强烈的机器部件。而金属陶瓷中的金属提供了韧性,陶瓷提供了硬度与强度,这种复合产生了性能上的协同效应。
金属陶瓷有下列共同的特点:
?模量比钢高(413-620GPa)。
智慧树知到《材料学概论》章节测试答案
智慧树知到《材料学概论》章节测试答案 绪论 1、材料让我们成为人,而我们用语言赋予材料生命,这句话对吗? A:对 B:错 答案:对 2、材料与人类发展:“材料-时代”对吗? A:对 B:错 答案:对 3、“物质-有用的物品就是材料“这句话对吗? A:对 B:错 答案:对 4、材料学的基本思想是? A:尺度之上 B:应用为王 C:物质 答案:尺度之上,应用为王 5、“材料是一种物质,但并不是所有的物质都是材料”这句话对吗? A:对 B:错
答案:对 第一章 1、珠光体的含碳量是 A:0.77% B:2.11% C:6.69% 答案:0.77% 2、亚共析钢加热成奥氏体后冷却转变成 A:珠光体+铁素体 B:珠光体 C:铁素体 答案:珠光体+铁素体 3、将铁碳合金加热成奥氏体后在空气中冷却的热处理方式,称为 A:回火 B:退火 C:淬火 答案:退火 4、生铁、熟铁、钢的主要化学成分均为Fe,但他们之间的性能差别显著,主要原因是其中()不同 A:珠光体含量 B:硬度 C:含碳量 答案:含碳量
5、金属中原子的排列方式 A:面心立方 B:体心立方 C:秘排六方 答案:面心立方,体心立方,秘排六方 第二章 1、生产普通陶瓷的主要矿物原料是 A::石英、粘土、长石 B:高岭土、碳酸盐 C:粘土、石英、烧碱 答案::石英、粘土、长石 2、陶瓷坯料采用可塑成型的方法手工成型时,需要控制其含水量在()范围之内,以保证坯体良好的塑形效果。 A:15~25% B:28~35% C:7~15% 答案:15~25% 3、构成敏感陶瓷的主要物质属于()类。 A:导体 B:绝缘体 C:半导体 答案:半导体
常见金属材料的介绍
常用金属材料 1、钢的分类 钢的分类方法很多,常用的分类方法有以下几种: 1)按化学成分碳素钢可以分为:低碳钢(含碳量<0.25%)、中碳钢(含碳量0.25%?0.6%)、高碳钢(含碳量>0.6%);合金钢可以分为:低合金钢(合金元素总含量<5% )、中合金钢(合金元素总含量5%?10%)、高合金钢(合金元素总含量>10%); 2)按用途分结构钢(主要用于制造各种机械零件和工程构件)、工具钢(主要用于制造各种刀具、量具和模具等)、特殊性能钢(具有特殊的物理、化学性能的钢,可分为不锈钢、耐热钢、耐磨钢等) 3)按品质分普通碳素钢(P W 0.045% S<0.05% )、优质碳素钢(P W 0.035% S <0.035% )、高级优质碳素钢(P W 0.025% S <0.025%) 2、碳素钢的牌号、性能及用途 常见碳素结构钢的牌号用“Q+数字”表示,其中“Q”为屈服点的“屈”字的汉语拼音字首, 数字表示屈服强度的数值。若牌号后标注字母,则表示钢材质量等级不同。 优质碳素结构钢的牌号用两位数字表示钢的平均含碳量的质量分数的万分数,例如,20钢 的平均碳质量分数为0.2%。 表1 —1常见碳素结构钢的牌号、机械性能及其用途 3、合金钢的牌号、性能及用途 为了提高钢的性能,在碳素钢基础上特意加入合金元素所获得的钢种称为合金钢。
合金结构钢的牌号用“两位数(平均碳质量分数的万分之几) +元素符号+数字(该合金元 素质量分数,小于 1.5%不标出;1.5%?2.5%标2; 2.5%?3.5%标3,依次类推)”表示。 对合金工具钢的牌号而言,当碳的质量分数小于 1%,用“一位数(表示碳质量分数的千分 之几)+元素符号+数字”表示;当碳的质量分数大于1%时,用“元素符号+数字”表示。(注: 高速钢碳的质量分数小于 1%,其含碳量也不标出) 表1 — 2常见合金钢的牌号、机械性能及其用途 4、铸钢的牌号、性能及用途 铸钢主要用于制造形状复杂,具有一定强度、塑性和韧性的零件。碳是影响铸钢性能的主要 元素,随着碳质量分数的增加, 屈服强度和抗拉强度均增加, 而且抗拉强度比屈服强度增加 得更快,但当碳的质量分数大于 0.45%时,屈服强度很少增加,而塑性、韧性却显著下降。 所以,在生产中使用最多的是 ZG230-450、ZG270-500、ZG310-570三种。 表1 — 35、铸铁的牌号、性能及用途 铸铁是碳质量分数大于 2.11%,并含有较多Si 、Mn 、S 、P 等元素的铁碳合金。铸铁的生产 工艺和生产设备简单,价格便宜,具有许多优良的使用性能和工艺性能, 所以应用非常广泛, 是工程上最常用的金属材料之一。 铸铁按照碳存在的形式可以分为:白口铸铁、 灰口铸铁、麻口铸铁;按铸铁中石墨的形态可 以分为:灰铸铁、可锻铸铁、球墨铸铁、蠕墨铸铁。
金属陶瓷材料
[长春工业大学] 金属陶瓷材料读书笔记 090201 20090516 胡冰 2013/3/14 摘要:介绍了Ti(C,N)基金属陶瓷的基本组成和结构,其组织性能及其影响因素,综述了Ti(C,N)基金属陶瓷的研究现状,指出了未来的发展方向和应用。
Ti(C,N)基金属陶瓷的基础研究与进展 前言 TiC—Ni金属陶瓷最早出现在1929年,作为WC—Co合金的替代材料,主要用于切削加工[1]。Ti(C,N)基金属陶瓷是1931年发明的[2]。1956年,美国福特汽车公司Humenik发现在TiC—Ni基金属陶瓷中加入Mo后,可以改善Ni对TiC的润湿性,大大提高合金强度[3]。1971年Kiefer发现在TiC —Ni基金属陶瓷中引入N,并同时加入Mo2C和Mo粉,可使其获得更高的硬度、耐磨性、抗弯强度,较好的切削性能和抗氧化能力。此后,Ti(C,N)基金属陶瓷的研究越来越多。因此国内外对Ti(C,N)基金属陶瓷非常重视,进行深入系统的研究。自2O世纪8O年代以来,Ti(C,N)基金属陶瓷获得了迅速的发展,世界各国硬质合金厂先后推出了系列的Ti(C,N)基金属陶瓷刀具[4]。 3O多年来,随着粉末冶金技术的发展,成分的演化趋于稳定,烧结技术的不断更新,粉末粒径的不断细化,Ti(C,N)基金属陶瓷的机械性能不断提高,Ti(C,N)基金属陶瓷发展到一个比较成熟的阶段。在日本,Ti(C,N)基金属陶瓷刀具材料已占可转位刀片的30%。我国在“八五”期间也研制成功多种牌号的Ti(C,N)基金属陶瓷刀具,并批量上市,但性能不稳定[5]。 Ti(C,N)基金属陶瓷作为一种新型的工具材料,具有密度低、室温硬度和高温硬度都优于WC基硬质合金,化学稳定性和抗氧化性好,耐磨性好等优点。其应用填补了WC硬质合金和陶瓷刀具之间高速精加工和半精加工的空白,既适用于高速精加工,又适用于半精加工和间断切削加
常用金属材料
2.1 铸铁 2.1.1灰口铸铁 2.1.2可锻铸铁 2.1.3球墨铸铁 2.2 碳素钢 2.2.1.碳素钢的分类 2.2.2普通碳素钢 2.2.3优质碳素钢 2.2.4高级优质碳素钢 2.3 合金钢 2.3.1合金钢分类 2.3.2常用合金钢 2.4 常用金属材料技术条件标准 2常用金属材料 介绍压力管道中常用的金属材料的分类、特点、用途和表示方法 金属材料:黑色金属:通常指铁和铁的合金 有色金属:指铁及铁合金以外的金属及其合金。 黑色金属根据它的元素组成和性能特点分为三大类,即铸铁、碳素钢及合金钢。 2.1铸铁 铸铁:含碳量大于2.06%的铁碳合金。 ◆真正有工业应用价值的铸铁其含碳量一般为2.5%~6.67%。 ◆铸铁的主要成分除铁之外,碳和硅的含量也比较高。由于铸铁中的含碳量较高,使得其中的
大部分碳元素已不再以Fe3C化合物存在,而是以游离的石墨存在。 性能特点:是可焊性、塑性、韧性和强度均比较差,一般不能锻,但它却具有优良的铸造性、减摩性、切削加工性能,价格便宜。 用途:常用作泵机座、低压阀体等材料;地下低压管网的管子和管件。 根据铸铁中石墨的形状不同将铸铁分为灰口铸铁、可锻铸铁和球墨铸铁。 2.1.1灰口铸铁:石墨以片状形式存在于组织中的铸铁称之为灰口铸铁。 ◆灰口铸铁浇铸后缓冷得到的组织为铁素体和游离石墨共存,断口呈灰色,灰口铸铁也因此而得名。灰口铸铁的各项机械性能均较差,工程上很少使用。 2.1.2可锻铸铁:经过长时间石墨化退火,使石墨以团絮状存在于铸铁组织中,此类铸铁称为可锻铸铁。 性能特点:强度、塑性、韧性均优于灰口铸铁,其延伸率可达12%;但可锻铸铁制造工艺复杂,价格比较高。 ◆由于可锻铸铁具有一定的塑性,故"可锻"的名称也由此而出,其实它仍为不可锻。 用途:可锻铸铁在工程上常用作阀门手轮以及低压阀门阀体等。 根据断面颜色或组织的不同,可锻铸铁又分为黑心可锻铸铁、白心可锻铸铁和珠光体可锻铸铁三种。常用的是黑心可锻铸铁。 2.1.3球墨铸铁:是通过在浇注前向铁水中加入一定量的球化剂进行球化处理,并加入少量的孕育剂以促进石墨化,在浇注后直接获得具有球状石墨结晶的铸铁。 性能特点:球墨铸铁的各项性能指标均优于可锻铸铁,比可锻铸铁价格便宜。 用途:可代替可锻铸铁用在较苛刻条件下。用途更广泛。 铸铁命名:根据GB9439的规定铸铁的牌号表示方法:
金属陶瓷材料
金属陶瓷材料
[长春工业大学] 金属陶瓷材料读书笔记 090201 20090516 胡冰 2013/3/14 摘要:介绍了Ti(C,N)基金属陶瓷的基本组成和结构,其组织性能及其影响因素,综述了Ti(C,N)基金属陶瓷的研究现状,指出了未来的发展方向和应用。
Ti(C,N)基金属陶瓷的基础研究与进展 前言 TiC—Ni金属陶瓷最早出现在1929年,作为WC—Co合金的替代材料,主要用于切削加工[1]。Ti(C,N)基金属陶瓷是1931年发明的[2]。1956年,美国福特汽车公司Humenik发现在TiC—Ni基金属陶瓷中加入Mo后,可以改善Ni对TiC的润湿性,大大提高合金强度[3]。1971年Kiefer发现在TiC —Ni基金属陶瓷中引入N,并同时加入Mo2C和Mo粉,可使其获得更高的硬度、耐磨性、抗弯强度,较好的切削性能和抗氧化能力。此后,Ti(C,N)基金属陶瓷的研究越来越多。因此国内外对Ti(C,N)基金属陶瓷非常重视,进行深入系统的研究。自2O世纪8O年代以来,Ti(C,N)基金属陶瓷获得了迅速的发展,世界各国硬质合金厂先后推出了系列的Ti(C,N)基金属陶瓷刀具[4]。 3O多年来,随着粉末冶金技术的发展,成分的演化趋于稳定,烧结技术的不断更新,粉末粒径的不断细化,Ti(C,N)基金属陶瓷的机械性能不断提高,Ti(C,N)基金属陶瓷发展到一个比较成熟的阶段。在日本,Ti(C,N)基金属陶瓷刀具材料已占可转位刀片的30%。我国在“八五”期间也研制成功多种牌号的Ti(C,N)基金属陶瓷刀具,并批量上市,但性能不稳定[5]。 Ti(C,N)基金属陶瓷作为一种新型的工具材料,具有密度低、室温硬度和高温硬度都优于WC基硬质合金,化学稳定性和抗氧化性好,耐磨性好等优点。其应用填补了WC硬质合金和陶瓷刀具之间高速精加工和半精加工的空白,既适用于高速精加工,又适用于半精加工和间断切削加
罗杰-材料学概论parper(纳米陶瓷)
纳米陶瓷材料的初步了解 罗杰无机1001 摘要:本文主要介绍了纳米陶瓷材料的制备方法、特性、一些当前的应用和前景 前言 随着纳米技术的广泛应用,纳米陶瓷随之产生,希望以此来克服 陶瓷材料的脆性,使陶瓷具有像金属似柔韧性和可加工性。英国材料学家Cahn指出,纳米陶瓷是解决陶瓷脆性的战略途径。纳米耐高温陶瓷粉涂层材料是一种通过化学反应而形成耐高温陶瓷涂层的材料。作为一名无机专业的学生,我认为纳米陶瓷将会是本专业的一个极有前景的发展方向,也可能是将来我们自己所要研究的方向,因此我把自己的short parper 的主题放在了这。 纳米陶瓷的制备 纳米陶瓷的制备工艺主要包括纳米粉体的制备、成型和烧结。目前世界上对纳米陶瓷粉体的制备方法多种多样,其中主要分为两类:物理方法和化学方法。其中物理方法有:惰性气体冷凝法、电子蒸发法、激光剥离法等等;化学方法有:化学气相沉积法、沉淀法、溶胶一凝胶法等等。但应用较广且方法较成熟的主要有气相合成和凝聚相合成2种。 1、气相合成:主要有气相高温裂解法、喷雾转化法和化学气相合成法,这些方法较具实用性。化学气相合成法可以认为是惰性气体凝聚法的一种变型,它既可制备纳米非氧化物粉体,也可制备纳米氧化物粉体。这种合成法增强了低温下的可烧结性,并且有相对高的纯净性和高的表面及晶粒边界纯度。原料的坩埚中经加热直接蒸发成气态,以产生悬浮微粒和或烟雾状原子团。原子团的平均粒径可通过改变蒸发速率以及蒸发室内的惰性气体的压强来控制,粒径可小至3~4nm,是制备纳米陶瓷最有希望的途径之一。 2、凝聚相合成(溶胶一凝胶法):是指在水溶液中加入有机配体与金属离子形成配合物,通过控制PH值、反应温度等条件让其水解、聚合,经
高级金属屋面常用材料介绍
铝镁锰铝镁锰 铝镁锰合金介绍: 铝金属通过电解作用从自然界中提炼出来,再通过熔炼分别配以定量的铜、锰、镁、硅、锌等元素形成多种多样的合金,可获得能满足各种不同需要的机械和物理性能。目前规定了从1000到9000共九个系列的变形铝合金,分别应用于消费品、航空航天、建筑、包装、交通运输、电气设备等各个方面。 符合DIN1725标准所规定的3004合金,其具有质轻、结构强度适中、耐候、耐渍,易于加工和焊接,正常气候环境(空气污染严重除外)下使用寿命可达50年,其再欧美等国建建筑上早已广泛应用,在近几年在国内建筑的使用中得到了认可和肯定,为现代建筑向舒适、耐久、轻型、经济、环保等方向发挥了重要的作用。 铝镁锰合金的性能铝镁锰合金的性能:: 屋面和墙面所用铝镁锰合金板常用厚度有0.7mm、0.8mm、0.9mm、1.0mm1.2mmmm 等规格,密度为2.73g/cm 3,抗拉强度≥225Mpa,屈服强度≥190Mpa,延伸率>3%,基材膨胀系数23×10-6。 铝镁锰合金的特点铝镁锰合金的特点:: 1、重量轻,密度为2.73g/cm 3,只有刚的1/3. 2、抗拉强度是普通铝的2.5倍,铝合金中含有一定的镁和锰,使其具有一定的强度和刚度。
3、耐腐蚀;与大气形成氧化铝薄膜,防止被进一步腐蚀。 4、外观表面处理多样、美观:可进行锤纹、阳极氧化、电泳、化学处理、抛光、涂漆处理。 5、可塑性好,易加工,适合各种建筑金属屋面和金属幕墙。 6、良好的导电性:厚度一般为0.7~0.9mm 的铝镁锰,可直接作防雷接闪器(国家规范《建筑防雷设计规范》GB 50057),但应避免在屋面穿孔。 7、优越的电磁波屏蔽性能,使人体大脑不受到伤害。 8、不释放有害毒素,是理想的环保材料。 9、回收利用价值很高,长期使用成本较经济,节约自然资源。 9、利于消防:熔点低(660摄氏度),发生火灾时,屋面易被烧穿,使火势向外蔓延,而不向内横向蔓延,有助于消防人员从顶部灌水灭火,到A 1级防火标准。 10、综合性价比较高。 锌铜钛锌铜钛((俗称钛锌板俗称钛锌板)) 锌铜钛合金介绍锌铜钛合金介绍 锌铜钛合金(俗称钛锌)是上世纪10年代研制出的一种高强度、抗蠕变合金,其机械性能可以与铜合金、铝合金相媲美。60年代后在欧美逐步获得了工业生产和应用,开辟了结构材料的新领域。 钛锌板是以符合欧洲质量标准的E N179的高纯度金属锌(99.995)与少量的钛和铜熔炼而成。钛的含量是0.06~0.2%,可以改善合金的
现代陶瓷材料发展及应用.
现代陶瓷材料发展及应用 摘要:本文简述了现代技术陶瓷最新研究、发展动态以及在实际中的应用,其中包括结构陶瓷、陶瓷基复合材料和功能陶瓷三个部分。还介绍了绿色陶瓷的发展及前景,科 学家试图使陶瓷生产与环境和谐完美的结合,开发出新型的绿色陶瓷材料。 关键词:陶瓷材料绿色陶瓷碳化硅晶须切削刀具氧化铝非氧化物陶瓷功能陶瓷结构陶瓷陶瓷基复合材料发展应用环境和谐 参考文献:《陶瓷材料概述》《现代技术陶瓷展与应用》《绿色陶瓷的发展前景》《陶瓷生产与环境和谐》 我国是一个具有悠久历史的陶瓷古国,在世界长期享有盛誉。当今陶瓷可以说已然成为了对我们生活产生重大影响的一门重要学科。近半个多世纪以来,随着先进陶瓷材料的研究和开发,在与人类生活息息相关的各个领域,如电子、通讯、能源、交通、宇宙探索和国家安全等,都能找到陶瓷的身影。可以说现代人的生活离不开陶瓷,陶瓷的进步给人类带来的是生活方式的日新月异。 陶瓷材料一般分为传统陶瓷和现代技术陶瓷两大类。传统陶瓷是指用天然硅酸盐粉末(如黏土、高岭土等为原料生产的产品。因为原料的成分混杂和产品的性能波动大,仅用于餐具、日用容器、工艺品以及普通建筑材料(如地砖、水泥等,而不适用于工业用途。现代技术陶瓷是根据所要求的产品性能,通过严格的成份和生产工艺控制而制造出来的高性能材料,主要用于高温和腐蚀介质环境,是现代材料科学发展最活跃的领域之一。 现代陶瓷材料主要有三大领域:结构陶瓷、陶瓷基复合材料和功能陶瓷。 一、结构陶瓷 同金属材料相比,陶瓷的最大优点是优异的高温机械性能、耐化学腐蚀、耐高温氧化、耐磨损、比重小(约为金属的1/3,因而在许多场合逐渐取代昂贵的超高合
陶瓷简介
陶瓷 陶瓷是陶器和瓷器的总称。人早在约公元前8000年前的新石器时代就发明了陶器。陶瓷材料大多是氧化物、氮化物、硼化物和碳化物等。常见的陶瓷材料有粘土、氧化铝、高岭土等。陶瓷材料一般硬度较高,但可塑性较差。除了在食器、装饰的使用上,在科学、技术的发展中亦扮演重要角色。陶瓷原料是地球原有的大量资源黏土经过淬取而成。而粘土的性质具韧性,常温遇水可塑,微干可雕,全干可磨;烧至700度可成陶器能装水;烧至1230度则瓷化,可几乎完全不吸水且耐高温耐腐蚀。其用法之弹性,在今日文化科技中有各种创意的应用。 陶瓷英文Ceramic(或者China);陶瓷拼音Táocí;陶瓷是以天然粘土以及各种天然矿物为主要原料经过粉碎混炼、成型和煅烧制得的材料的各种制品。以前人们把用陶土制作成的在专门的窑炉中高温烧制的物品称作陶瓷,陶瓷是陶器和瓷器的总称。陶瓷的传统概念是指所有以粘土等无机非金属矿物为原料的人工工业产品。它包括由粘土或含有粘土的混合物经混炼,成形,煅烧而制成的各种制品。由最粗糙的土器到最精细的精陶和瓷器都属于它的范围。对于它的主要原料是取之于自然界的硅酸盐矿物(如粘土、石英等),因此与玻璃、水泥、搪瓷、耐火材料等工业,同属于“硅酸盐工业”的范畴。陶瓷的主要产区为景德镇、醴陵、高安、丰城、萍乡、黎川、佛山、潮州、德化、淄博、北流等地。 早在欧洲掌握制瓷技术之前一千多年,中国已能制造出相当精美的瓷器。从我国陶瓷发展史来看,一般是把“陶瓷”这个名词一分为二,为陶和瓷两大类。中国传统陶瓷的发展,经历过一个相当漫长的历史时期,种类繁杂,工艺特殊,所以,对中国传统陶瓷的分类除考虑技术上的硬性指标外,还需要综合考虑历来传统的习惯分类方法,结合古今科技认识上的变化,才能更为有效地得出归类结论。 作为汉族传统文化之一的陶瓷文化,在民族母体中孕育、成长与发展,它以活生生的凝聚着创作者情感、带着泥土的芬芳、留存着创作者心手相应的意气的艺术形象,表现着汉族文化,叙述着一个个动听的故事,展现着广阔的社会生活画卷,记录着芸芸众生的悲欢离合,描述着民族的心理、精神和性格的发展与变化,伴随着民族的喜与悲而前行。 新石器时期彩陶中的陶塑作品,记录着先民生存的愿望。那陶塑的猪、牛、狗,模仿着打猎而来或者豢养而食的动物形象,演示着与大自然搏斗的酷烈,表达着文明的演化与发展。摩娑这些与实物逼真无二的作品,想象着先民的困惑、喜悦和奋争,那在洪荒、野蛮中奔突与呼叫的景象,撼人心魄。
功能陶瓷材料概述
功能陶瓷材料概述 功能陶瓷由于其在电、磁、声、光、热、力等方面优异的性能,广泛应用于电子电力、汽车、计算机、通讯等领域,在科学技术发展和实际生产生活中发挥着越来越重要的作用。主要阐述了功能陶瓷电学、光学、磁学、声学、力学等基本性质,并介绍了功能陶瓷的种类和应用以及未来发展趋势。 标签: 功能陶瓷;性质;应用 1 前言 功能陶瓷是具有电、磁、声、光、热、力、化学或生物功能等的介质材料。它有别于我们所熟知的日用陶瓷、艺术陶瓷、建筑陶瓷等,而是指在电子、微电子、光电子信息和自动化技术以及能源、环保和生物医学领域中所使用的陶瓷材料。功能陶瓷以其独特的声、光、热、电、磁等物理特性和生物、化学以及适当的力学等特性,在相应的工程和技术中发挥着关键作用,如制造电子线路中电容器用的电介质瓷,制造集成电路基片和管壳用的高频绝缘瓷等。 2 功能陶瓷基本性质 功能陶瓷是利用其对电、光、磁、声、热等物理性质所具有的特殊功能而制造出的陶瓷材料。其电学、光学、磁学、声学、热学、力学等性质是研究和运用的重点。功能陶瓷的这些性质与其组成、结构和工艺等有着密切关系。 功能陶瓷电学性质可以用电导率、介电常数、击穿电场强度和介质损耗来表示,是功能陶瓷材料很重要的基本性质之一。光学性质指其在可见光、红外光、紫外光及各种射线作用时表现出的一些性质。表征磁学性质的参数有磁导率、磁化率、磁化强度、磁感应强度等。材料在外力作用下都会发生相应的形变甚至破坏,有必要研究材料的力学性能,功能陶瓷材料也具有弹性模量、机械强度、断裂韧度等表征力学性能的参数。 3 功能陶瓷种类及其应用 功能陶瓷的发展始于20世纪30年代,经历从电介质陶瓷→压电铁电陶瓷→半导体陶瓷→快离子导体陶瓷→高温超导陶瓷的发展过程,目前已发展成为性能多样、品种繁多、使用广泛、市场占有份额很高的一大类先进陶瓷材料。目前已经研究比较深入并大量使用的功能陶瓷有绝缘陶瓷、介电陶瓷、压电陶瓷、半导体陶瓷、敏感陶瓷、磁性陶瓷、生物陶瓷和结构陶瓷等,下面将介绍几种主要的功能陶瓷及其应用。 3.1 绝缘陶瓷
材料学导论陶瓷材料
材料学导论陶瓷材料 《材料科学导论》课程学习报告 —关于陶瓷材料学习的体会 1. 陶瓷材料概论 说到陶瓷,在许多人的印象中,是一种坚硬易碎的物体,缺乏韧性,缺乏塑性。许多陶瓷学家把陶瓷看成是用无机非金属化合物粉体,经高温烧结而成,以多晶聚集体为主的固态物。这一定义虽然同时指出了材料的制备特征和结构特征,但却把玻璃、搪瓷、金属陶瓷等摒除在外。所以,陶瓷材料是用天然或合成化合物经过成形和高温烧结制成的一类无机非金属材料。它具有高熔点、高硬度、高耐磨性、耐氧化等优点。可用作结构材料、刀具材料,由于陶瓷还具有某些特殊的性能,又可作为功能材料。 2. 陶瓷材料的发展 陶瓷是人类最早利用自然界提供的原料制造而成的材料。旧石器时代,人们就发现经火煅烧过的粘土,其硬度和强度都大大提高,而且不再被水瓦解。于是,就有了利用粘土的可塑性,将其加工成所需的形状,然后用火烧制成的陶器。随着金属冶炼术的发展,人类掌握了通过鼓风机提高燃烧温度的技术,并且发现,有一些经高温烧制的陶器,由于局部熔化变得更加致密坚硬,完全改变了陶器多孔,透水的缺点。经过长期的摸索和经验积累,以粘土,石英,长石等矿物原料配制而成的瓷器出现了。 从陶器发展到瓷器,是陶瓷发展过程中的一次重大飞跃。这种传统的瓷器,从结构上来看,是由玻璃相结合在一起的、由许多微小的晶 粒构成的物体。 随着科学技术的高速发展,人们迫切需要大量强度很高,绝缘性能良好的陶瓷材料。此时,人们发现,尽管陶瓷中的玻璃相使陶瓷变得坚硬、致密,然而它却妨碍了
陶瓷强度的提高。同时,玻璃相也是陶瓷绝缘性能,特别是高频绝缘性能不好的根源。于是,玻璃相含量比传统陶瓷低的一些强度高,性能好的材料不断涌现。现在,许多科学与技术方面使用的高性能陶瓷(High performance Ceramics)都是几乎不含有玻璃相的结晶态陶瓷。为了有别于传统陶瓷,称之为先进陶瓷(Advanced Ceramics)或高技术陶瓷(High Tech Ceramics);有时也称为精细陶瓷(Fine Ceramics)或工程陶瓷(Engineering Ceramics)。 3. 陶瓷材料的定义 陶瓷的传统定义:陶器和瓷器的总称,包括玻璃,搪瓷,耐火材料,砖瓦,水泥,石膏等。 陶瓷的狭义定义:以粘土为主要原料,经高温烧制而成的制品。 陶瓷的广义定义:经高温烧制而成的无机非金属材料的总称。 陶瓷的精确定义:用天然原料或人工合成的粉状化合物,经过成型和高温烧结制成的,由无机化合物构成的多相固体材料。 4. 陶瓷材料的分类陶瓷材料按照性能可大致分为普通陶瓷和特种陶瓷。 1. 普通陶瓷:原料: 粘土、石英和长石。 特点:坚硬而脆性较大、绝缘性和耐腐蚀性极好;制造工艺简单,成本低廉,各种陶瓷中用量极大。 分类:普通陶瓷又分为普通日用陶瓷和普通工业陶瓷。 (1) 普通日用陶瓷:特点:作日用器皿和瓷器,具有良好的光泽度、透明度,热稳定性和机械强度较高。分类:长石质瓷(国内外常用的日用瓷,作一般工业瓷制品)、绢云母质瓷(我国的传统日用瓷)、骨质瓷(近些年得到广泛应用,主要作为高级日用瓷制品)和滑石质瓷(我国发展的综合性能好的新型高质瓷)。 (2) 普通工业陶瓷:特点:普通工业陶瓷有炻器和精陶。炻器是陶器和瓷器之间的一种瓷。分类:工业陶瓷按用途分为:建筑卫生瓷(用于装饰板,卫生间装置和器
(1)--常见的金属材料
(1)--常见的金属材料
九年级化学辅导《讲义一》学生姓名:__________ 课题常见的金属材料 【优秀的学习品质】专心听讲、勤于思考的习惯 【是真的吗?】市场上有人卖假黄金欺骗消费者,谋取暴利,是真的吗? 在室内放一盆水可以为防止煤气中毒,是真的吗? 【问题一】金属的物理性质有哪些? (一)金属的物理性质 1. 大部分金属具有银白色金属光泽,而铜呈紫红色,金呈黄色。 2. 常温下,大多数金属都是固体,而汞(水银)是液体。 3. 金属有导电性、导热性、延展性,密度大、熔点高,硬度大等物理性质。(参见课本表54页) (二)认识几种重要的金属 1. 铁 (1)纯铁具有银白色的金属光泽,质软,有良好的延展性,密度为7.86g/cm3,熔点1535℃,沸点2750℃,铁是电和热的导体。铁能被磁体吸引。 (2)铁是最常见的金属,是人类生活和生产中非常重要的材料。 2. 铝 (1)铝是分布较广的元素,在地壳中含量仅次于氧和硅,是金属元素中含量最高的。 (2)纯铝具有银白色金属光泽,较软,熔点较低660℃,密度较低,为2.7g/cm3,导电性很好(仅次于Cu),在电力工业上它可以代替部分铜作导线和电缆。铝有很大的延展性,能够抽成细丝,也能压成薄片成为铝箔。有良好的耐腐蚀性。铝粉跟某些油料混合,可以制成银白色防锈油漆。 (3)铝是最常见的金属之一,虽然利用比铜、铁晚,但现在世界上铝的年产量已超过了铜,位于铁之后,居第二位。 3. 铜 (1)纯铜呈紫红色,故又称紫铜。密度较大,10.5g/cm3,熔点1083℃,有极好的导热、导电性,其导电性仅次于银。 (2)铜具有优良的化学稳定性和耐蚀性,具有优良的导电性。 【反馈练习一】 1、菜刀、锤子用铁制而不用铅制的原因是() A. 铁硬度大,铅硬度小 B. 铁熔点高,铅熔点低 C. 铁密度小,铅密度大 D. 铁导电性好,铅导电性较差 2、下列金属不用于制作装饰品的是() A. 金 B. 银 C. 铂 D. 铁 3、下列各项比较中不正确的是() A. 地壳中元素含量:Al>Fe B. 含铁量:Fe2O3>Fe3O4 C. 延展性:铁>金 D. 导电性:银>铜 【问题二】合金是纯净物还是混合物? 1. 合金的定义: 在一种金属中加热熔合其它金属或非金属而形成的具有________的物质叫合
金属与陶瓷的润湿性概述
龙源期刊网 https://www.360docs.net/doc/9a18239910.html, 金属与陶瓷的润湿性概述 作者:刘娟娟苟小斌 来源:《城市建设理论研究》2013年第24期 摘要:研究金属对陶瓷的润湿性对开发新型金属—陶瓷体系,探寻和发展材料的制备技术,制备高性能金属—陶瓷复合材料有着重要的现实意义。本文阐述了润湿性的分类、界面化学反应对金属—陶瓷润湿性和陶瓷材料性能的影响,并介绍了润湿性研究的实验研究方法,探讨改善润湿性的途径。 关键词:金属—陶瓷;接触角;化学反应;润湿性 中图分类号:TL25 文献标志码:A 文章编号: 1 引言 金属—陶瓷复合材料作为一种以一种或多种陶瓷相为基体,以金属或合金为粘结相的复合材料[1],如何发挥其中陶瓷相基体的优良性能一直是科研人员研究的重点方向。其中陶瓷与 金属润湿性的好坏很大程度上决定了金属—陶瓷复合材料综合性能的发挥,因此金属—陶瓷复合材料研究的热点在于开发新型金属—陶瓷体系、改善金属—陶瓷界面结合状况以提高材料综合性能,这一切都是建立在金属对陶瓷具有良好的润湿性的基础之上。研究金属对陶瓷的润湿性对制备高性能金属—陶瓷复合材料有着重要的现实意义。金属陶瓷复合材料的研究还处于初期阶段。研究较多的有金刚石、石墨、SiC、Al2O3、ZrO2、TiC等陶瓷相和金属合金所组成 的体系。由于陶瓷和金属的晶体类型及物理化学特性的差异,两者的相容性很差,绝大部分液态金属都不能润湿陶瓷,因此如何改善金属与陶瓷的润湿性,从而改善材料的综合性能性能成为当前材料制备中的一个重要问题。 2 润湿性的分类 根据陶瓷—金属的界面结合情况,金属对陶瓷的润湿过程可分为非反应性润湿和反应性润湿。 非反应性润湿是指界面润湿过程中不发生化学反应,润湿过程的驱动力仅仅是扩散力及范德华力。其中液态金属的表面张力是决定液态金属是否能在固相陶瓷表面润湿的主要热力学参数。一般此类润湿过程进行得很快,在很短的时间内就能达到平衡;且温度和保温时间对润湿性影响不大。非反应性润湿体现出对体系成分的不敏感性。添加合金元素对改善金属—陶瓷润湿性有较大的影响,其机制为合金元素在液态金属表面及固—液界面的吸附和富集,降低了液态金属表面张力及固—液界面张力。如在Cu中添加Cr不但降低液态金属表面张力,且Cr在金属—陶瓷界面偏聚造成界面张力降低,从而有效地降低Cu对ZrO2的接触角。
陶瓷材料学教学大纲
《陶瓷材料学》教学大纲 英文名称:Science of Ceramic Material 课程编码:0933043 课程性质:限选课 学时:30 周学时:2 学分:1.5 适用专业:材料物理学专业 授课学期:2015-2016学年第二学期 【课程性质、目的和要求】 通过考试考查学生对《陶瓷材料学》课程理论教学和实践教学环节的掌握程度,促使学生系统掌握关于陶瓷材料合成的基本理论和基本工艺方法,掌握有关工艺设计和科研的基本知识和方法,了解陶瓷材料的性质和特点,对陶瓷材料的应用尤其是现代陶瓷材料在各方面的应用深入了解,使学生在学完课程之后,能够胜任陶瓷材料生产技术工作,并且能从事开发、研究和设计工作。 主要依据教学大纲的内容和要求考核。通过闭卷考试方式考查学生对该课程的基本概念、基本理论和基本技能掌握牢固程度,以及综合分析的能力,着重考查学生运用所学知识解决问题的能力。主要以教材内容为主,少量内容考查学生对参考书、文献等了解情况。 【教学内容、要点和课时安排】 绪论(2课时) 教学目的:了解本课程的性质和任务,了解陶瓷材料的发展史,掌握陶瓷材料的概念及其内涵,了解陶瓷材料的分类方特,对不同种类陶瓷材料的性质特点熟悉掌握。 教学重点和难点: 1、陶瓷材料概念 2、陶瓷材料分类 3、陶瓷材料特点 第一节陶瓷材料发展历史及其概念的内涵 第二节陶瓷材料的分类 第三节陶瓷材料的特点 思考题: 1、陶瓷材料的分类? 2、陶瓷材料具有哪些特点? 第一章陶瓷的晶体结构(2课时)
教学目的:了解化学键的形成和分子间的相互作用力,了解陶瓷材料的基本结构有哪些,掌握代表性晶体结构的特点,熟练掌握硅酸盐结构特性,区分离子型晶体和共价型晶体的结构和性质。 教学重点和难点: 1、陶瓷的晶体结构 2、代表性晶体结构 3、硅酸盐结构 4、离子型晶体与共价型晶体的区别 第一节原子间的结合力 第二节陶瓷的晶体结构 第三节代表性晶体结构 第四节硅酸盐晶体结构 第五节离子型晶体的结构与性质 第六节共价型晶体的结构与性质 思考题: 1、陶瓷的晶体结构有哪些? 2、离子型晶体与共价型晶体在结构和性质上的区别? 第二章非晶态与玻璃结构(2课时) 教学目的:了解晶体的形态,认识晶体与非晶态的区别,掌握玻璃结构的特点,了解非晶的晶化过程,对无机玻璃的种类有一定的认识。 教学重点和难点: 1、非晶态的形成 2、玻璃结构的特点 3、非晶的晶化过程 第一节非晶态 第二节玻璃结构 第三节非晶的晶化 第四节无机玻璃的种类 思考题: 1、玻璃结构的特点? 2、非晶的晶化过程? 第三章晶体缺陷(2课时) 教学目的:了解陶瓷材料中晶体的缺陷有哪些,对点缺陷、线缺陷和位错的概念深入了解,掌握不定比化合物的特点,掌握晶界概念。。 教学重点和难点: 1、点缺陷和位错概念理解 2、不定比化合物 第一节点缺陷 第二节不定比化合物
陶瓷材料
简介 陶瓷材料是用天然或合成化合物经过成形和高温烧结制成的一类无机非金属材料。它具有高熔点、高硬度、高耐磨性、耐氧化等优点。可用作结构材料、刀具材料,由于陶瓷还具有某些特殊的性能,又可作为功能材料。 编辑本段分类 陶瓷材料分为普通陶瓷(传统陶瓷)材料和特种陶瓷(现代陶瓷)材料两大类。 普通陶瓷材料 采用天然原料如长石、粘土和石英等烧结而成,是典型的硅酸盐材料,主要组成元素是硅、铝、氧,这三种元素占地壳元素总量的90%,普通陶瓷来源丰富、成本低、工艺成熟。这类陶瓷按性能特征和用途又可分为日用陶瓷、建筑陶瓷、电绝缘陶瓷、化工陶瓷等。 特种陶瓷材料 采用高纯度人工合成的原料,利用精密控制工艺成形烧结制成,一般具有某些特殊性能,以适应各种需要。根据其主要成分,有氧化物陶瓷、氮化物陶瓷、碳化物陶瓷、金属陶瓷等;特种陶瓷具有特殊的力学、光、声、电、磁、热等性能。本节主要介绍特种陶瓷。 编辑本段性能特点 力学性能 陶瓷材料是工程材料中刚度最好、硬度最高的材料,其硬度大多在1500HV以上。陶瓷的抗压强度较高,但抗拉强度较低,塑性和韧性很差。 热性能 陶瓷材料一般具有高的熔点(大多在2000℃以上),且在高温下具有极好的化学稳定性;陶瓷的导热性低于金属材料,陶瓷还是良好的隔热材料。同时陶瓷的线膨胀系数比金属低,当温度发生变化时,陶瓷具有良好的尺寸稳定性。 电性能 大多数陶瓷具有良好的电绝缘性,因此大量用于制作各种电压(1kV~110kV)的绝缘器件。铁电陶瓷(钛酸钡BaTiO3)具有较高的介电常数,可用于制作电容器,铁电陶瓷在外电场的作用下,还能改变形状,将电能转换为机械能(具有压电材料的特性),可用作扩音机、电唱机、超声波仪、声纳、医疗用声谱仪等。少数陶瓷还具有半导体的特性,可作整流器。 化学性能 陶瓷材料在高温下不易氧化,并对酸、碱、盐具有良好的抗腐蚀能力。 光学性能 陶瓷材料还有独特的光学性能,可用作固体激光器材料、光导纤维材料、光储存器等,透明陶瓷可用于高压钠灯管等。磁性陶瓷(铁氧体如:MgFe2O4、CuFe2O4、Fe3O4)在录音磁带、唱片、变压器铁芯、大型计算机记忆元件方面的应用有着广泛的前途。 编辑本段常用特种陶瓷材料 根据用途不同,特种陶瓷材料可分为结构陶瓷、工具陶瓷、功能陶瓷。 1.结构陶瓷 氧化铝陶瓷主要组成物为Al2O3,一般含量大于45%。氧化铝陶瓷具有各种优良的性能。耐高温,一般可要1600℃长期使用,耐腐蚀,高强度,其强度为普通陶瓷的2~3倍,高者可达5~6倍。其缺点是脆性大,不能受受突然的环境温度变化。用途极为广泛,可用作坩埚、发动机火花塞、高温耐火材料、热电偶套管、密封环等,也可作刀具和模具。氮化硅陶瓷主要组成物是Si3N4,这是一种高温强度高、高硬度、耐磨、耐腐蚀并能自润滑的高温陶瓷,线膨胀系数在各种陶瓷中最小,使用温度高达1400℃,具有极好的耐腐蚀性,除氢氟酸外,能耐其它各种酸的腐蚀,并能耐碱、各种金属的腐蚀,并具有优良的电绝缘性和耐
陶瓷材料
陶瓷材料 【摘要】:陶瓷材料是我们日常生活中一种非常重要的材料,尤其是在我们中国,制作陶瓷自古以来就是我们的专长。到了现代陶瓷的概念和功能发生了一系列的变化,本文主要对陶瓷材料的性能,应用以及发展前景做一个简单的概述 【关键字】:陶瓷,材料 正文: 1,概述:传统的陶瓷材料是粘土、石英、长石等硅酸盐材料,而现代陶瓷材料是无机非金属材料的统称。 陶瓷材料是一种天然或人工合成的粉状化合物, 经过成型或高温烧结,由金属元素和非金属的无机化合物构成的多相固体材料。陶瓷材料具有耐高温、耐腐蚀、耐磨损、原料丰富、成本低廉等诸多优点而被人一直关注。现在,陶瓷材料、金属材料、高分子材料被称为三大主要固体材料。 2,性能: (1)力学性能:陶瓷材料具有极高的硬度和优良的耐磨性,弹性模量高,钢度大抗拉强度低抗压强度很高,陶瓷的塑性、韧性低,脆性大,在室温下几乎没有塑性。 (2)机械性能:大多数陶瓷的硬度都比金属高的多,特别好, 常用作耐磨零件(如轴承, 刀具).它具有高的弹性模量和高脆性,具有低的抗拉强度和高的抗压强度, 具有较强的耐热功能,具有耐高温的特性, 其熔点一般大于2000℃。此外, 陶瓷材料还具有热膨胀系数较小、导热性较低、热容量较小等机械特性。 (3)电学性能:大多数陶瓷材料有较高的电阻率、较小的介电常数和介电损耗, 因此它可以用作绝缘材料。少数的陶瓷材料可以用作半导体材料,而且已经成为无线电技术和高新技术领域不可或缺的材料。有的陶瓷材料还具有超导特性,,具有超导特性的陶瓷已经成为高温超导材料中的重要组成部分。 (4)化学性能:陶瓷材料具有抗高温氧化、抗腐蚀的能力。它不仅对酸、碱、盐具有良好的抵抗作用,而且还对熔融金属具有抗蚀作用。所以陶瓷材料常用作化学反应的发生器、用作离子交换膜。有的陶瓷材料还可以含载体对化学反应有催化作用。 (5)生物性能:陶瓷材料的生物功能主要表现在可以修复或替换人体的某些组织、器官或增强脏器功能的方面。比如人造腔膜、心脏起搏器用电池板、助听器用振动板等。另外, 有的陶瓷材料还具有人体感知功能。 (6)光学性能:某些陶瓷材料具有光吸收、光反射及光偏移的特性,还有的具有分光性、感光性及导光性。一些先进光学陶瓷材料还具有良好的透光性。利用陶瓷材料的这些光特性可以制造出许多光学产品, 例如制作特种灯具(比如Na灯) 的灯管材料、陶瓷感光计等等。 3,应用: (1),纳米陶瓷材料:纳米陶瓷是指在纳米技术的基础上研究开发的具有更高更多特性陶瓷材料。在陶瓷材料的显微结构中, 相粒尺寸、第二相分布、气孔尺寸等量纲均在纳米量级( 0.1nm至100nm) 的水平上, 因此使得材料的强度、韧性和超塑性大幅度提高。我们都知道普通陶瓷材料的显微组织主要由晶体相、玻璃相及气相组成, 各相的组成、结构、数量、形状与分布都对陶瓷材料的性能有直接的影响, 而玻璃相及气相的含量较大会使陶瓷的强度、硬度和抗热冲击等性能降低。纳米陶瓷材料的出现很好地克服了普通陶瓷材料这些缺点。并且对材料的力学、电学、化学、光 学、磁学等性能产生重要影响, 为替代普通陶瓷材料的应
材料科学概论复习题及答案
复习 特种陶瓷—材料的结构—.材料科学—无机非金属材料—失效—特种陶瓷— 硅酸盐水泥—热处理—纳米材料 判断题 1. 低碳钢的硬度及塑性均比高碳钢的高。错 2. 橡胶是在高弹态下使用的高分子材料。对 3. 玻璃是一种晶体材料,它具有透光性、抗压强度高、但脆性大的特点。错 4. 位错、空位、间隙原子都是实际晶体中的点缺陷。错 5. 什么是材料?如何进行分类? 材料是指人类社会可接受、能经济地制造有用器件或物品的固体物质。 6. 什么是材料的成分?什么是材料的组织?什么是材料的结构? 材料的成分是指组成材料的元素种类及其含量,通常用质量分数(w),也可以用粒子数分数表示。材料的组织是指在光学显微镜或电子显微镜下可观察到,能反应各组成相形态、尺寸和分布的图像。材料的结构主要是指材料中原子的排列方式。 7. 材料科学与工程的四大要素是什么? 材料成分,结构,工艺,性能。 8. 传统陶瓷坯料常见的成形方法及生产工艺? 9. 什么是高分子材料?高分子材料具有哪些性能特点? 高分子材料是由可称为单体的原料小分子通过聚合反应而合成的。力学性能:最大的特点是高弹性和黏弹性。电性能:绝大多数高分子材料为绝缘体。热性能:绝热性。 10. 什么叫复合材料?按基体材料分为哪几类? 复合材料指由两种或更多种物理性能、化学性能、力学性能和加工性能不同的物质,经人工组合而成的多相固体材料。复合材料可分为基体相和增强相。按基体分为树脂基、金属基陶瓷基。
11. 陶瓷由哪些基本相组成?它们对陶瓷的性能有什么影响? 晶体相、玻璃相、气相。 12. 简述提高陶瓷材料强度及减轻脆性的途径? 13. 按照用途可将合金钢分为哪几类?机器零部件用钢主要有哪些? 可分为结构钢,工具钢,特殊钢和许多小类。 轴,齿轮,连接件。 14. 材料典型的热处理工艺有哪些?什么叫回火? 退火、正火、淬火、回火。 钢件淬火后,为了消除内应力并获得所要求的性能,将其加热Ac1以下的某一温度,保温一定时间,然后冷却到室温的热处理工艺叫做回火。 15. 什么是特种陶瓷?阐述其与传统陶瓷的区别 特种陶瓷是以高纯化工原料和合成矿物为原料,沿用传统陶瓷的工艺流程制备的陶瓷,是一些具有各种特殊力学、物理或化学性能的陶瓷。 16 .谈谈你对材料的认识,材料的未来发展趋势
功能陶瓷的简介
功能陶瓷的简单介绍 功能陶瓷是具有电、磁、声、光、热、化学及生物体特性,具有相互转化功能的陶瓷。它主要是利用纳米技术使陶瓷的性能发生改变的。 热学功能陶瓷、生物功能陶瓷、化学功能陶瓷、电磁功能陶瓷、光学功能陶瓷,还是在涂层/薄膜和复合材料死当今比较主要的几种功能陶瓷。 生物功能陶瓷 在生物功能陶瓷方面: 利用纳米技术生产的纳米抗菌材料有三类:一类Ag+系抗菌材料(当高价银离子与细菌接触时使细菌体内的蛋白质变性。);第二类是是ZnO,Tio2:等光触媒型纳米抗菌材料(通过催化反应,将细菌的尸体分解得一干二净,一般还有除臭,自洁,防霉,防锈,高效防老化,全能净化空气,自造“负离子雨林”气候等功能);第三类是C-18A纳米蒙脱土等无机材料。将前两类加人陶瓷中可制成对病菌、细菌有强的杀菌和抑菌作用的陶瓷产品。北京陶瓷厂和日本东陶机器株式会社合资生产的高档卫生洁具“TOTO”产品,即是应用这一技术生产的具有抗菌性能的卫生洁具。生物陶瓷材料亦可作为作为无机生物医学材料,且没有毒副作用,与生物组织有良好的生物相容性、耐腐蚀性等优点,已越来越爱人们的重视。 主要有以下几种活性材料; (1)羟基磷灰石生物活性材料。人工听小骨羟基磷灰石听小骨临床应用效果优于其它各种听小,具有优良的声学性质,平均提高病人的听力20-30db。在特定语言频率范围提高45-60db。微晶与人体及生物关系密切,在生物和医学中已有成功应用,利用ha 微晶能使细胞内部结构发生变化,抑制癌细胞生长和增殖,可望成为治疗癌症的“新药”。(2)磷酸钙生物活性材料。磷酸钙又称生物无机骨水泥,是一种广泛用于骨修补和固定关节的新型材料。有望部分取代传统的pm-ma有机骨水泥。国内研究抗压强度已达到60mpa以上;磷酸钙陶瓷纤维:磷酸钙陶瓷纤维具有一定机械强度和生物活性,可用于无机骨水泥的补强及制务有机与无机复合型植入材料。 (3)磁性材料。生物磁性陶瓷材料主要为治疗癌症用磁性材料,植入肿瘤灶内,在外部交变磁场的作用下,产生磁滞热效应,导致磁性材料区域内局部温度升高,借以杀死肿瘤细胞,抑制肿瘤的发展。
陶瓷概述
陶瓷概述 学号:姓名: [摘要]:陶瓷是陶器和瓷器的总称。人们早在约8000年前的新石器时代就发明了陶器。除了使用于食器、装饰上外,陶瓷在科学、技术的发展中亦扮演着重要角色。陶瓷原料是地球原有的大量资源黏土经过淬取而成。在今日文化科技中有各种创意的应用。陶瓷材料大多是氧化物、氮化物、硼化物和碳化物等。如今,陶瓷工艺真正飞速发展。 [关键词]:陶瓷历史;陶瓷材料;新品种陶瓷;新品种陶瓷特点 1.陶瓷的概念及发展历史 1.1什么是陶瓷 陶瓷是以粘土为主要原料以及各种天然矿物经过粉碎混炼、成型和煅烧制得的材料以及各种制品。陶器和瓷器的总称。陶瓷的传统概念是指所有以粘土等无机非金属矿物为原料的人工工业产品。它包括由粘土或含有粘土的混合物经混炼,成形,煅烧而制成的各种制品。由最粗糙的土器到最精细的精陶和瓷器都属于它的范围。对于它的主要原料是取之于自然界的硅酸盐矿物(如粘土、石英等),因此与玻璃、水泥、搪瓷、耐火材料等工业,同属于“硅酸盐工业”的范畴。 1.2陶瓷的发展历史 陶瓷的发展史是中华文明史的一个重要的组成部分,中国作为四大文明古国之一,为人类社会的进步和发展做出了卓越的贡献,其中陶瓷的发明和发展更具有独特的意义,中国历史上各朝各代有着不同艺术风格和不同技术特点。中国是世界上最早应用陶器的国家之一,而中国瓷器因其极高的实用性和艺术性而备受世人的推崇. 在中国,制陶技艺的产生可追溯到纪元前4500年至前2500年的时代,汉族劳动人民在科学技术上的成果以及对美的追求与塑造,在许多方面都是通过陶瓷制作来体现的,并形成各时代非常典型的技术与艺术特征。 夏朝以前发展的标志是彩陶。其中有较为典型的仰韶文化、以及在甘肃发现的稍晚的马家窑与齐家文化等等,解放后在西安半坡史前遗址出土了大量制作精美的彩陶器,令人叹为观止. 汉朝,陶器受到了更为确切的重视,在这一时期,烧造技艺有所发展,较为坚致的釉陶普遍出现,汉字中开始出现“瓷”字。同时,通过新疆、波斯至叙利亚的通商路线,中国与罗马帝国开始交往,促使东西方文化往来交流,从此一时期的陶瓷器物中也可以看出外来影响的端倪。 唐代,陶瓷的工艺技术改进巨大,许多精细瓷器品种大量出现,即使用当今的技术鉴测标准来衡量,它们也算得上是真正的优质瓷器。尤其以唐三彩最为出名。唐末五代十国出现了一个陶瓷新品种——柴窑瓷(萧窑),质地之优被广为传颂,但传世者极为罕见。
