医疗器械生产质量管理组织示范内审检查表-自检表
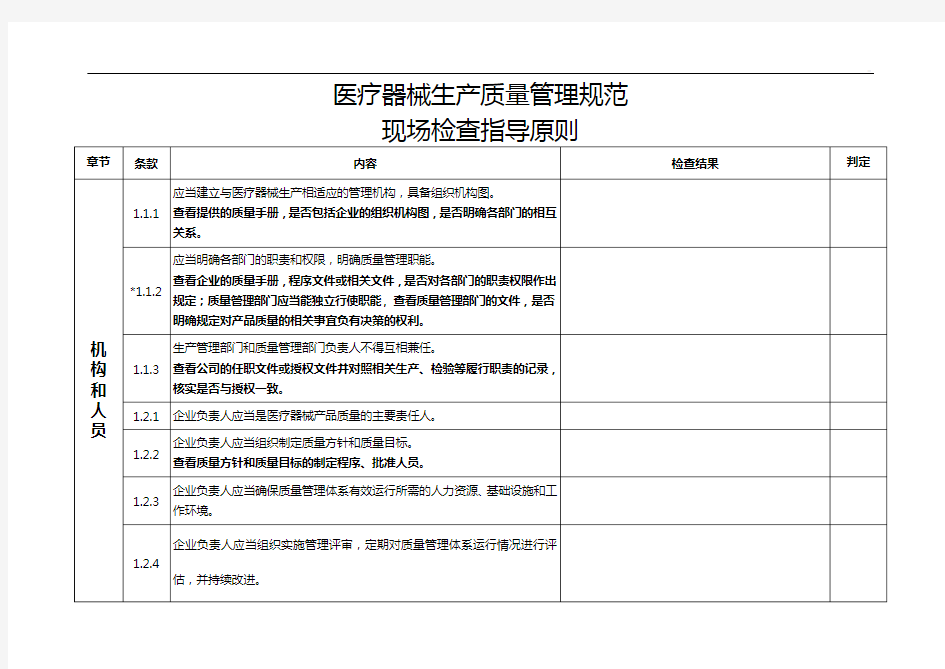
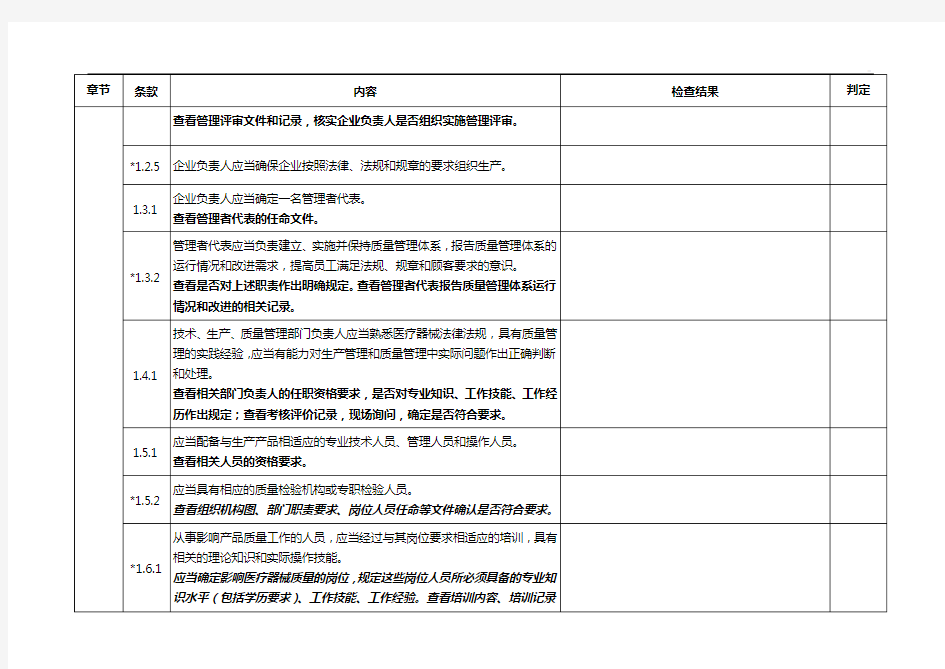
医疗器械生产质量管理规范
注解:
本指导原则条款编号的编排方式为:X1。X2。X3,其中X1为章节的顺序号,如1.1.1的第一位X1表示“机构与人员”章节,2.1.1的第一位X1表示“厂房与设施”章节;X2为同一章节内条款的顺序号,如1.1.1的第二位X2表示“机构与人员”章节第一条要求,1.2.1的第二位X2表示“机构与人员”
章节第二条要求;X3为同一条款内细化的检查指导的顺序号,如1.1.1的第三位X3表示“机构与人员”章节对第一条要求细化的第一个检查要点,1.1.2的第三位X3表示“机构与人员”章节对第一条要求细化的第二个检查要点。
其他章节编号规则相同。
安全生产检查表
企业(单位)安全生产检查表 企业(单位)名称:年月日项目主要内容检查细则检查结果说明 安全生产责任制落实企业法定代表人负责制 及主要负责人、分管负责 人、安全管理人员、各车 间岗位安全责任制的建 立及落实情况 是否制定安全生产责任书 检查 细则 中的 项目, 完成 的在 结果 栏打 √,没 完成 的打 ×。 是否层层签订责任书 责任书的奖惩是否兑现 安全生产管理机构建设 情况 是否成立专门的安全管理机构 是否配备专兼职安全管理员 安全生产投入情况 是否按规定提取和使用安全生产费用 是否为从业人员缴纳工伤保险 是否投保安全生产责任险或缴纳安全 生产风险抵押金 落实安全生产法律法规设备安全管理制度和岗 位安全作业规程建立、执 行情况 是否制定安全管理制度并严格执行 是否制定岗位操作规程并严格执行 作业现场的安全管理情 况 是否建立安全检查和管理记录台帐 作业现场是否有安全管理人员 作业现场安全管理制度和操作规定是 否上墙,并严格执行 新建、改建、扩建项目依 法履行安全设施“三同时” 制度情况 项目设计是否符合安全规范,并取得 相关审批手续 安全设施是否与主体工程同时设计、 同时施工、同时验收 外来施工(承包、承租) 方安全管理情况 是否与外来施工方签订安全生产合同 或在合同中明确安全生产条款 是否对外来施工方生产经营过程加强 安全监管 外来施工方是否具备资质 隐患排查 整改和重大危险源监控企业安全生产设施、设备 的日常维护、保养情况; 是否建立安全生产设施、设备管理检 查制度 是否按规定做好安全生产设施、设备 的维护、保养记录 附件2
检查组组长签字: 企业(单位)主要负责人签字: 危险性较大的特种设备和危险物品储存容器、运输工具的检验检测情况 是否建立特种设备管理台帐 检查细则中的项目,完成的在结果栏打√,没完成的打×。 是否对在用特种设备按规定进行检测、检验 对重点部位、重大危险源 的普查建档、风险辨识、 监控预警制度的建立及措施落实情况 是否建立重大危险源档案及监控台帐 是否落实专人或专业设备对危险源进 行24小时监控 应急管理 应急队伍建设情况 是否建立专(兼)职应急救援队伍或 与相关应急救援队伍签订救援协议 应急投入情况 是否配备应急救援物资、器材 应急制度建设及演练情况 是否建立安全生产应急值守制度 是否制定总体应急救援预案及岗位、车间单项预案 是否定期开展应急演练,并留存演练记录 对企业周边或作业过程中存在的易由自然灾害引发事故灾难的危险点排查、防范和治理情况 是否建立自然灾害隐患排查治理台帐 基础工作及安全宣传培训 安全生产教育培训情况 是否制定全年培训计划,并建立安全生产教育培训考核档案 企业主要负责人、安全管理人员、特种作业人员是否培训并持证上岗 是否进行全员安全培训,并形成书面记录 安全宣传情况 是否建立安全生产例会制度并严格执行 厂区、车间是否设置安全黑板报、标语口号、警示标志等 安全保障落实情况 是否按规定为从业人员无偿提供合格的劳动防护用品
药品生产管理和质量管理自检情况分析
药品生产管理和质量管理自检情况 一. 企业概况 内蒙古康丽药业有限公司位于赤峰市林西县工业园区内,始建于1974年,生产范围主要是片剂产品共二十个品种,现拥有固定资产1560万元,在册职工46人。各种专业技术人员23人,占职工总数的50%,年创产值1500万元,利税140万元,产品主要销内蒙、东北、华北等地区。 按《药品生产质量管理规范》的要求,我公司总投资1560万元的全厂GMP改造工程已经完成全部改造并投入使用,制剂车间使用面积2410 m2,净化面积920 m2,改造后的固体制剂车间在原有片剂剂型的基础上新增硬胶囊剂和颗粒剂两个剂型,年生产能力为片剂6亿片、硬胶囊剂2亿粒、颗粒剂2千万袋。在改造的同时,我们建立了完善了文件管理体系,同时实施了相关的验证工作。 二. 企业实施GMP情况及培训情况 药品的特殊属性赋予了药品生产、技术、质量、经营、使用、储运等环节管理上的特殊要求,决定了GMP是我们药品生产和质量管理的基本准则。为此,我公司逐步在企业内部树立了用GMP科学管理企业的思想,建立了各项管理规程、操作规程、技术标准,按GMP要求设立的生产管理系统和质量保证系统能够满足生产需要,做到了不合格物料不出厂,保证了产品质量稳定、安全、有效。为此我公司从2002年开始,成立了以总经理为组长的GMP认证领导小组,全面负责企业GMP改造和认证工作,并根据工程进度情况相继成立了员工培训领导小组和GMP自检领导小组,分别负责公司的GMP培训、员工培训和公司的GMP自检工作。
1.领导重视是开展实施GMP工作的关键。 公司领导重视GMP实施工作,把GMP管理纳入企业日常管理工作之中,多次召开GMP认证专题会议,贯彻GMP精神,成立了以总经理为组长的GMP领导小组。同时也非常重视对GMP的培训工作,总经理亲自参加培训,并多次讲课,强调实施GMP培训的重要性。把实施GMP工作作为企业加强和改善管理、保证产品质量、提高企业竞争力和生存能力的重要途径。 2. 确立质量否决权是开展实施GMP的前提。 我公司实行总经理负责制,由质量副经理负责质量管理,质量保证部下设质检中心及质监中心,质检中心及质监中心主任均为大专学历,从事药品生产及检验工作多年,有丰富的管理经验及实际操作技能。质监中心设有专职物料监控员及生产监控员2名,负责从物料采购开始到生产过程、主要控制点到成品出厂的质量监控,实施全过程质量跟踪管理。质检中心有专职质检员4名,检测仪器齐全,完全具备检测能力和条件,质量管理系统建立健全了各级质量职责,明确了各级人员质量职责,质量保证部对产品质量一票否决,真正实施了质量否决权。 三. GMP自查情况 技术改造结束后,由企业总经理担任组长,制订了自检管理规程及自检标准,对照GMP标准我们进行了自检,现将自检结果报告出下: 1.机构与人员 (1) 按着GMP的要求,我们建立健全了药品生产与质量管理机构,制订了生产与质量管理部门的工作职能,明确了各级质量人员的质量职
YYT0287-2017医疗器械生产企业内审检查表-生产部
XXXX医疗器械有限公司 内部审核检查表 FX/ JL8.2.2-03 №:201704060001审核日期2017.04.06 审核人员XXXX、XXXX、XXXX 受审部门生产部受审部门负责人XXXX 序号涉及条款检查内容检查方法检查结果 1 1.1.1应当建立与医疗器械生产相适应的管理机 构,具备组织机构图。 查看提供的质量手册,是否包括企业的组织 机构图,是否明确各部门的相互关系。 是。查《质量手册》中的FX/SC 2.0《组织 机构图》和FX/SC 3.0《职责分配表》。符合 要求 2 *1.1.2应当明确各部门的职责和权限,明确质量管 理职能。 查看企业的质量手册,程序文件或相关文 件,是否对各部门的职责权限作出了规定; 质量管理部门应当能独立行使职能, 查看质 量管理部门的文件,是否明确规定对产品质 量的相关事宜负有决策的权利。 是。查《质量手册》和《程序文件》FX/CX 5.5 《职责、权限与内部沟通程序》。符合要 求 3 1.1.3 生产管理部门和质量管理部门负责人不得 互相兼任。 查看公司的任职文件或授权文件并对照相 关生产、检验等履行职责的记录,核实是否 与授权一致。 是。查《任命书》,生产部负责人为XXXX, 质管部负责人为XXXX,未兼任。符合要求 4 1.4.1 技术、生产、质量管理部门负责人应当熟悉 医疗器械法律法规,具有质量管理的实践经 验,应当有能力对生产管理和质量管理中实 际问题作出正确判断和处理。 查看相关部门负责人的任职资格要求,是否 对专业知识、工作技能、工作经历作出了规 定;查看考核评价记录,现场询问,确定是 否符合要求。 是。查技术部门负责人XXXX、生产部门负 责人XXXX、质管部门负责人XXXX,有相 应资质;2016年度岗位人员考核、评价和再 评价确认满足要求。符合要求 5 1.5.1 应当配备与生产产品相适应的专业技术人 员、管理人员和操作人员。 查看相关人员的资格要求。是。查人员花名册。符合要求 6 *1.6.1 从事影响产品质量工作的人员,应当经过与 其岗位要求相适应的培训,具有相关的理论 知识和实际操作技能。 应当确定影响医疗器械质量的岗位,规定这 些岗位人员所必须具备的专业知识水平(包 括学历要求)、工作技能、工作经验。查看 培训内容、培训记录和考核记录,是否符合 要求。 是。查看花名册、人员档案和培训记录,从 事影响产品质量工作的人员有相应学历,具 备相关专业知识并进行了培训。符合要求
内审审核检查表生产车间
内部质量体系审核检查表 编号:HY/QR 8.02-03 审核员:NO:1 受审部门生产车间 审核时 间 质量标准条 款 审核内容及方法审核记录 5.5.1职责和权限 5.4.1质量目标 6.3基础设施 6.4 工作环1、生产车间在公司的质量 管理体系中,主要负责哪 些过程的控制? 2、生产车间的职责和权限 是什么? 3、生产车间建立的具体质 量目标是什么?如何在质 量方针的指引下从事本部 门的工作? 4、为实现产品,组织为本 部门提供了哪些设备和设 施? 5、设施和设备是否符合实 现产品的需求?是否得到 了维护? 6、查看设施、设备台帐, 设备维修记录及设备维护 规定,现场审核。 提供部门职责和岗位职责文件, 对生产车间的职责和权限作出了规 定, 部门提供了质量手册5.5.1章, 对职责作出了规定,按规定回答基 本完整 质量手册5.5.1章规定,主要负 责:7.2顾客有关的过程控制 7.5.4顾客财产 8.2.1顾客满意 度的调查,主要职责:生产过程贮存 保管服务 部门经理,准时交货率100%。 顾客满意度95%,在公司的质量目 标的指引下完善各方面的工作,力 争实现公司总目标。 设备名称抽查 生产过程设备:有螺旋焊管机组 (开卷机、铣边机、递送机、成型机)、 埋弧焊机、等离子切割机、空压机, 搬运工具:吊车等
境 5.5.3内部沟7、组织是否具备合适的工 作环境?是否得到管理? 8、现场检查工作环境有效 性? 9、生产车间与其他部门是 否经常沟通?采用什么方 式 查看相关记录,编写了设备保养 制度、生产过程设备都进行了维护 和保养。 生产过程要求,查看现场时,工 作环境较适宜。 环境保持较适宜。采用交流经常 沟通,向办公室提供库存情况及市 场信息。 内部质量体系审核检查表 编号:HY/QR 8.02-03 审核员:NO:2 受审部门生产车间 审核时 间 质量标准条 款 审核内容及方法审核记录 7.2与顾客有关的过程7.5.1生产10、是否在向顾客做出产 品承诺前对产品进行了评 审?评审内容有哪些是否 记录、查阅有关文件记 录? 11、产品要求变更后,文 件是否及时更改?是否将 变更后的信息传递给出有 关部门?到有关部门核实 是否收到合同订单更改通 知单? 12、与顾客进行沟通的方 通过与顾客签订书面合同,以合 同的形式确定顾客的要求。 按照国标/行标标准,对产品的 要求进行评审后,再与顾客签订书 面合同,合同在明确了顾客对产品 的各项要求。资源等方面,在产品 要求评审表中有详细的描述。 如有相关性问题通过电话等方 式进行沟通 公司提供了相关国标,公司工
GMP自检方案含自检日程安排(优质参考)
GMP自检方案 一、自检目的:对全厂执行《药品生产质量管理规范》(2010年修订)的情况进行检查和评价,并致力于缺陷改进,保证GMP体系的有效性、适宜性、符合性。 二、自检准则:《药品生产质量管理规范》(2010年修订) 三、自检类别: 层次类型范围频率执行人员检查日期Ⅰ现场检查生产、仓储、公用 Ⅱ例行检查各部门、区域有关GMP 程序执行情况 ⅢGMP自检整个GMP涉及部门、区 域、系统 四、自检日程安排 现场检查现场检查小组每周不定时对仓储设施、物料接收与放行、工艺用水的制备与质量控制、空调系统的使用和维护、质量控制实验室、生产厂房设施和设备情况、生产管理与质量控制验证与校验等进行一次现场检查。 例行检查时间第一组第二组第三组第四组第五组第六组14:00-- 17:00 大容量注 射剂车间 17:00-- 17:30 自检组会议,总结自检情况。 GMP自检日期时间第一、二、三组第四、五、六组 7月19日 8:30-- 8:50 首次会议 9:00-- 11:30 仓储设施、物料管理工艺用水系统、空调系统14:00-- 17:00 生产厂房设施、设备生产车间生产管理
7月20日9:00-- 11:30 机构与人员配备、培训情况质量控制实验室14:00-- 17:00 生产管理与质量管理文件验证或校验 17:00-- 17:30 自检组会议,总结自检情况。 自检重点检查内容1.物料的管理,原辅料和内包装材料的来源情况、原辅料和内包装材料的供应商审计情况、仓库 物料的管理情况,特殊药品的管理情况。 2.生产管理,处方和工艺的执行情况,对生产过程偏差的出来情况。 3.质量保证的管理,质量保证部门对生产过程的监控情况,对物料和成品的放行管理情况。 4.质量检验的管理,原辅料和成品的检验情况,委托检验的实施情况。 5.验证管理情况。 6.洁净厂房设施、设备的使用及维护情况。 7.空气净化系统、工艺用水系统的使用及维护情况。 8.人员培训组织、实施情况。 9.中药委托加工的生产和质量管理情况。 10.委托检验情况。 检查组成员1.现场检查小组组长:现场检查小组组员:2.审计小组组长: 第一组组员: 第二组组员: 第三组组员: 第四组组员: 第五组组员: 第六组组员: 制订人:日期:年月日批准人:日期:年月日备注
内审检查表完整各部门
受审部门 总经理 管理者代表 审核容 日期 标准条款 审核方法 记录 评价 符合 查看体系文件判别是否符合标准规定 。 1按要求建立文件化的质量管理体系。 查,符合标准规定 4.1质量管 2质量管理体系覆盖的产品围。 理体系总要 求 检查是否相符。 覆盖的产品围符合 查,文件齐全 符合 符合 符合 3质量管理体系各层次的文件。 检查是否齐全。 4质量管理体系的删减。 有没有删减部分,如有则记录 有删减合理 查文件目录判别各级文件是否齐全。 抽查三份文件是否相符 1公司应建立并保持的质量管理体系文件。 查,各级文件齐全 符合 符合 查目录,判别是否能满足生产经营的 需求 4.2.1文件 2保存的医疗器械的法律、法规。 要求总则 满足生产经营的需求 3对每一型号的医疗器械建立并保持一套技术文档 抽查一套技术文档,检查是否正确、 相关技术文件 符合 。 齐全、清晰,符合生产要求。 质量手册应包括以下容: 符合 符合 阐明企业质量管理体系 覆 盖 围 , 包 含 YY/T0287 专用要求 容,有描述过程及其相 互作用。 4.2.2质量 手册 检查质量手册,查有没有阐明企业质 量管理体系覆盖围,有无缺YY/T 0287专用要求容,有没有描述过程 及其相互作用。 1) 清楚的阐明企业质量管理体系覆盖的围。 2) 应形成文件的程序或对其引用。 符合 符合 3) 识别企业质量管理体系所需过程及过程之间 的相互作用的表述。 5.1 1总经理对其建立和改进质量管理体系的承诺。 通过查质量记录,作出判断的证据。 有质量方针 符合 符合 2总经理将满足顾客要求和法律、法规要求的重要 询问二个现场员工,作出判断 明白满足顾客要求和法 律、法规要求的重要性 管理承诺 性传达给组织的成员。 与领导层交谈,了解顾客要求和法律 了解顾客要求和法律、 、法规传达情况以及顾客要求得到满 法规传过情况以及顾客 符合 5.2 1确保顾客的需求得到确定并予以满足。 2应完全理解顾客和法律法规要求。 足的情况 要求得到满足。 以顾客为关 注焦点 完全理解顾客和法律法 规的要求 抽查二份合同的执行情况。 符合 符合 符合 1制定了质量方针,并已在相关层次中传达质量方 检查有无质量方针,在办公室、生 针。 产车间能否看到质量方针。 5.3 制定了质量方针 各层次人员对质量方针 的理解 质量方针 2各层次人员对质量方针的理解程度 询问二个员工。 1质量目标应与质量方针相一致,质量目标应是 查目标与方针是否一致,查相关职 可测量的,并应在相关职能和层次上展开。 能部门有无自己的质量目标。 5.4 查目标与方针一致 符合 各职能部门对质量目标 的完成情况达标 策划 2各职能部门对质量目标的完成情况。 抽查二个部门。 符合 符合 质量策划体现了质量管 理体系的持续改进 3质量策划体现了质量管理体系的持续改进。 查质量策划文件。 符合 符合 1最高管理者应确保企业的职责、权限得到规 查组织机构图和部门职责、权限。 最高管理者已规定企业 的职责、权限。 定。 5.5职责 、权限和2最高管理者应指定管理者代表并明确其职责和 查管理者代表的任命书和职责、权 最高管理者指定管理者 代表,明确其职责和权 符合 限 沟通 权限。 限。
企业安全生产自检全套材料
一、单位概况 二、单位其他情况 人员情况 安全管理人员 特种作业人员 伤亡事故 (二)安全工作日志 (三)安全评价 (四)单位周边环境 三、危险源种类 贮罐区 库区 危险性生产场所 危险建(构)筑物 压力管道 锅炉 压力容器 加油(气)站 危化品经营 剧毒品经营 危化品运输 剧毒品运输 危险品码头 放射源及射线装置 矿山 水库大坝 液化气换气站 建筑施工工程 变配电所 渡口(渡船) 铁路道口(专用线) 游乐场及游乐设施 电梯 自动扶梯 厂内机动车辆 起重机械 重点设备 其他危险源 危险源周边环境
单位名称 单位代码主管部门 行业代码行业类别 经济类型企业规模 法人代表法人手机 成立时间职工总数 固定资产总值 年销售收入(万元)年利税总额(万元)其中利润(万元)(万元) 占地面积(m2)邮政编码 单位电话单位传真 企业所在地 通讯地址 营业执照注册地 主要产品 备注 单位负责人签章:填报部门负责人签章填报人签章: 填报日期:联系电话:
安全许可证 单位名称: 安全许可证名称许可证编号 许可范围发证单位 发证日期有效期至 登记中心登记办公室 安全许可证名称许可证编号 许可范围发证单位 发证日期有效期至 登记中心登记办公室 安全许可证名称许可证编号 许可范围发证单位 发证日期有效期至 登记中心登记办公室 安全许可证名称许可证编号 许可范围发证单位 发证日期有效期至 登记中心登记办公室 安全许可证名称许可证编号 许可范围发证单位 发证日期有效期至 登记中心登记办公室 单位负责人签章:填报部门负责人签章填报人签章:填报日期:联系电话:
单位周边环境单位名称: 单位周边环境情况 可能灾害形式 最大危险区域面积 (m2) 周 边 地 区 情 况 单位类型数量单位名称人数与危险源最近距离(m)住宅区 生产单位 机关团体 公共场所 交通要道 其他 周边 环境 对单 位的 影响 类型数量简要说明 单位负责人签章:填报部门负责人签章填报人签章:填报日期:联系电话:
危险化学品生产企业安全生产日常管理检查表
危险化学品生产企业安全生产日常管理检查表 企业名称: 检查日期: 年月日 序 号 检查内容检查方式存在问题处理意见 一、生产、经营现场安全检查情况 1 作业人员是否持证上岗。抽查作业人员上岗证 2 作业人员是否按有关安全生产规章制度和安全 操作规程进行操作。 检查相关培训证书及培训记 录,抽查作业人员进行询问 3 作业人员是否熟悉本岗位化学品的基础知识,是否了解作业场所和工作岗位存在的危险因素及防范事故的应急措施。 4 作业人员是否佩戴和使用符合国家标准、行业 标准的劳动防护用品。 抽查作业场所劳动防护 用品配备情况 5 重大危险源(点)设备进行经常性维护、保养 和定期检测检验的情况。 查备案、查检修、保养记 录 6 重大危险源(点)已构成重大事故隐患的整改 情况。 查档案,查记录 7 重大危险源(点)监控情况。包括液位计、温 度计、压力表、安全阀、呼吸阀、湿度计、有 毒可燃气体检测仪等。 现场检查 8 现场安全警示标志的设置情况是否清晰、醒目, 是否有告知牌、特殊标识等。 现场检查 9 液体储存区是否有围堰,围堰是否有漏洞、破 损、防腐等情况,排水井是否有液封,围堰高 度是否符合标准。 现场检查 10 现场开展事故隐患排查及落实整改的情况检查生产场所整改档案、记录 11 安全评价报告中提出的事故隐患整改措施是否 全部落实。 对照安全评价报告抽查 整改措施落实情况 12 安全评价报告中描述的企业主要装置、设备、 设施、总平面布置是否改变并重新进行申请审 查。 对照安全评价报告检查 企业总平面布置 13 安全评价后企业的车间、仓库等建筑物是否改 变用途。 对照安全评价报告抽查 车间、仓库等建筑物的用 途 14 企业是否存在非法生产、储存危险化学品行为。抽查生产、储存环节 15 疏散用门是否按设计规范采用向疏散方向开启 的平开门。 现场检查 16 防雷、防潮、防晒、防冻、防腐、防渗漏等设 施是否完好。 现场检查 17 易燃易爆场所的电气、仪表是否安装防爆设施。现场检查 18 设备、管道压力、液位、温度、流量组分等检 测报警设施是否完好、指示是否正常。 现场检查 19 可燃、有毒气体厂房是否有检测仪器,是否定 期进行检测。 现场检查
企业档案管理系统自查报告材料
企业档案管理自查报告 导语:深入贯彻执行公司总部的文件精神,加强措施,加大力度,努力改进档案管理中存在的问题,完善档案管理制度,力争使档案管理工作更上一层楼。下面由小编为您整理出的企业档案管理自查报告内容,一起来看看吧。 篇一:企业档案管理自查报告20XX年以来,我司档案管理工作在公司总部的正确指导下,认真贯彻执行《中华人民共和国档案法》和《******公司档案管理办法(试行)》,以实现档案管理的规范化、标准化和科学化为目标,狠抓档案管理质量,不断加强档案整理水平。从行政公文的收集、整理、归档到保管利用过程,切实做到档案的完整和安全。现将我司档案管理自查情况报告如下: 一、加强组织领导,档案管理体制更加健全。 近年来,公司领导高度重视档案管理工作,始终将档案管理工作纳入日常工作日程。以职能建设为基础,以规范管理为核心,进一步完善了档案管理工作机制,先后建立健全了由公司领导任组长,各部室负责人为成员的档案管理工作小组,实现了档案目标管理工作的统一领导、统一规划、统一管理,形成了公司领导挂帅、各部门分管、档案管理员具体负责的管理网络,使我司的档案管理工作迈上新台阶。 二、强化制度管理,档案管理工作更加规范。 为做好档案管理工作,我司在原有的基础上,加强了对
档案保管、利用、保护、保密等规章制度的落实。在档案收集整理工作方面,我们从严要求,切实加强文件的收、发工作,严格登记、科学分类、组卷合理、编目规范,努力做好文件装订、排列、编号、编目、装盒等工作,保证归档文件材料的完整、准确、系统。在档案材料保密工作方面,我司定期做好法律法规、制度规定的宣传工作,加强档案管理人员的保密意识,增强对归档文件材料的保密力度,实行专人保管、专人查阅、集中归档,保证档案资料的安全和利用。在档案基础设施方面,我司根据资金的实际情况,配备了铁柜、空调、灾火器等办公设施,基本上满足了防潮、防霉、防鼠、防虫、防火、防尘、防光、防高温的八防要求,确保了档案的完整和安全。 通过一系列手段和措施,我司进一步提高了档案工作的管理水平,做到了规章制度上墙、工作意识进脑、管理理念入心,公司上下呈现出依法治档、规范管档、人人重档的良好局面。 三、明确工作目标,档案业务建设更加有序。 通过自检自查,我司的档案管理工作虽然取得了一定的成绩,但与总部领导的要求还有一定差距,主要表现在:一是各部室的档案责任意识方面有待加强;二是在开发利用方面有待深入探讨,跟踪利用效果反馈不够;三是由于实际客观因素限制,档案方面的专题培训还有待加强;四是档案管
企业自检管理规程 2017
企业自检管理规程 1.目的:建立一个企业自检管理规程,定期检查企业内部GMP执行情况,及时纠正不足,不断提高企业GMP水平。 2.范围:企业内部与产品质量有关的系统和部门。 3.职责:质量负责人、质量管理部部长、自检小组成员、被检部门负责人。 4.内容: 4.1 自检周期 4.1.1一般情况下,公司自检频次为一年一次。当发生下列情况之一时,应及时启动自检程序或增加自检频次: 4.1.2公司组织机构、产品剂型、生产工艺、生产设施和设备等发生重大变化时。 4.1.3有重大质量事故发生、出现严重的质量客户投诉或受到国家药品监督管理部门的警告时。 4.1.4公司的生产质量管理体系进行了重大修改时(例如新项目、新车间投入使用)。4.1.5重大法规环境发生变化时(例如新版GMP的实施)。 4.2 自检内容:公司各级人员及组织机构、厂房设施、设备、物料与产品、确认与验证、文件管理、生产管理、质量控制与质量保证、委托生产与委托检验、产品发运与召回、投诉与不良反应。 4.3自检标准:《GMP》2010版,GMP附录-中药饮片,企业现行的各项标准管理规程和标准操作规程。 4.4企业的自检工作由质量管理部负责。质量管理部于每年制订年度自检计划,报质量负责人审核、批准。 4.5成立自检小组,小组组长一般由质量负责人或质量管理部部长担任,由自检组长提出自检小组成员,参与人员应为经过公司自检培训的人员。自检小组成员可按不同的专
业或部门进行分工。 4.6自检小组通过查看现场和审核文件、记录,认真在《GMP自检检查记录表》中记录必要的检查信息, 对不符合项作出客观描述。 4.7自检完毕后,自检小组将缺陷项目汇总发至被检查部门。 4.8被检部门负责人应在一周内,就自检中发现的问题,及时完成整改。整改完成由自检小组进行验收。 4.9自检小组在整改检查完成后出具自检报告。自检报告应包括:自检日期、自检内容、自检区域、缺陷描述、整改措施、纠正和预防措施的建议、整改责任人、完成日期等。 4.10 自检小组组长应将自检报告报公司负责人、质量负责人、生产负责人审阅。报告原件由质量管理部存档。
安全生产管理安全检查表范文
安全生产管理安全检查表 依据中华人民共和国主席令第70号《中华人民共和国安全生产法》、国务院令第75号《企业职工伤亡事故报告和处理规定》(1991年2月22日)、劳动部劳部发[1995]30号《重大事故隐患管理规定》、天津市人大常委津政发[1987]15号《天津市安全生产责任制实施办法》、天津市人民政府津政办发[1996]65号转发市安委会《关于加强安全生产工作的意见》、原劳动部《企业职工劳动安全教育管理规定》(1995年11月8日颁布)等法规、标准编制安全检查表,检查项目内容及检查结果,见表5.9.3-1。 安全生产管理安全检查表表5.9.3-1
项目安全验收综合评价 项目评价组依据国家、地方、电子行业相关安全法规、规范及标准,运用安全系统工程的理论及方法,对项目建设内容及安全管理,全面进行了现场查验、查证及综合性安全评价,现将评价分析及整改建议的要点归纳如下。 主要危险危害因素和危险源点 1、燃爆中毒、灼伤-易燃液体、氯化剂、腐蚀品、有毒有害气体等化学危险品的贮存、输运、使用部位。 2、火灾爆炸-油罐,天然气调压、输送、用气装置(锅炉)。 3、物理爆炸-锅炉、压力容器(蒸发器、冷凝器、储气罐等)、气瓶。 4、触电危险-变配电设备设施、电气线路、用电设备设施。 5、静电危害-使用、输送、贮存易燃易爆物质的管路、设施,以及火灾爆炸危险环境中的设备设施。 6、高空坠落-2m以上各类高空作业点。 7、车辆伤害-厂内运输车辆。
8、机械伤害-空压站、冷冻站、水泵房、锅炉房的各类传动旋转部位。 9、灼伤-高温设备、管路及使用激光源,红外线光源的设备、机台。 10、噪声危害-空压设备、泵类、风机等设备。 供配电安全评价单元 1 单元概述 1、供电电源、电压 该公司由城市供电系统双港和吴庄220kV变电站各引来一路110kV专用架空线路至厂区内的总配变电站。每路架空线路传输容量为50MVA,厂区配电电压为10kV,冷冻机用电电压为3.3kV,低压用电设备电压为380/220V,频率为50Hz。 2、供配电系统 总配变电站110kV系统采用线路—变压器组方案,即每路110kV架空线路经由电动操作的SF6断路器后接至110/10kV、20MVA油浸式变压器,变压器10 kV出线引至站内的001#和007#配电站10 kV母线,10 kV系统采用单母线分段接线,通过母线分段断路器互为备用,并以放射式向各厂房10 kV配电站馈电,每座厂房10 kV配电站再以环形或放射式的形式向各终端(厂房内)变电站馈电,各终端变电站采用10/0.38 kV干式变压器,380/220V低压系统为单母线,设联络开关。终端变电装置将380/220V电压送至各厂房内的各电气室及用电部位的380V低压开关盘,再以低压开关引至各电动机控制中心MCCS和各层分配电盘;220V电源由位于各电气室和各层的380/220V的可移动式变压器提供。 应急电源由UPS及设置在C厂房内的三台1250 kW的柴油发电机组成。发电机并列运行,出口电压为3.3 kV,送至需要应急电源的厂房内的自动转换开关,再经变压器变压为380/220V馈电给各设备。当一处失电后发电机组自动启动并恢复供电。 在总配变电站中,110/10kV变压器到10kV开关柜采用架空母线馈电,由总配变电站10kV开关柜到各厂房10kV开关柜的馈电采用地下电缆排管。应急电源采用地下综合管道和桥架向各需要应急电源厂房馈电。
内审检查表(生产部(车间))
内审检查表 编号:KR-ZL-JL-12 审核员:朱显庆受审核部门:生产部(车间)审核日期:2008.8.1 标准条款审核要点与方法客观证据评定 5.5.1 5.4.1 6.3 6.4 本部门的质量职责是什么? 本部门的质量目标是什么?完成如何? 1、查看设备台帐并结合产品的工艺过程来评 价提供的设备是否能保证产品符合要求。 2、有无设备维护规定,是否按规定进行了设 备的维护保养,查看维护保养记录。 1、本公司对工作环境有什么要求? 2、本公司采取了哪些措施满足环境要求? 负责产品的生产,设备的管理以及现场环境的管理 共3项 1、查生产设备台帐,共有50台设备,包括2台车 床和1台铣床。 2、查设备点检记录,加工期间,对车床和铣床等 主要设备进行了保养,暂时没有设备维修。 1、要求卫生、地面整洁。 2、每天进行清扫,现场检查,车间地面干净。 √ √ √ √ 注:符合-√不符合—X 观察项—O NO.
内审检查表 编号:KR-ZL-JL-12 审核员:朱显庆受审核部门:生产部(车间)审核日期:2008.8.1 标准条款审核要点与方法客观证据评定 7.5.1 1、是否得到了过程控制所需的表述产品特性 信息的文件,包括产品标准、生产计划等。 2、没有作业指导书就不能保证质量的过程是 否制定了作业指导书? 3、生产设备有哪些? 4、生产过程中使用哪些监视和测量装置? 5、生产过程中实施了哪些监视和测量。 6、放行、交付和交付后活动的实施情况。1、有生产计划,规定了生产数量。有备货通知, 生产任务书,其中生产任务书中规定了产品测量的 范围,使用的填料等技术要求。 2、有设备安全操作规程。查阅了图纸,有面板图 纸。 3、有2台车床和1台铣床,每天进行保养。还配 备了各种安装工具。 4、压力表、秒表。 5、查生产流程卡,记录生产过程中安装和试漏等 情况等。查色谱柱装填记录,记录了装填填料材料, 长度等,但查色谱柱评价记录,不能提供评价结果。 6、有领料单、流程卡、出库单、发货单。 √ √ √ √ × √ 注:符合-√不符合—X 观察项—O NO.
安全生产管理制度与检查表
安全生产管理 一、安全生产检查制度和安全生产情况报告制度 由于各企业的生产性质和特点不同,以及检查的目的、要求不同,安全检查的具体内容差别较大,应根据企业的实际情况来制定。这里仅以车间、班组和安全管理部门的安全检查重点内容为例,说明安全检查的具体内容构成。 1.班组安全生产检查内容 (1)明确有安全员。 (2)班组的各项安全记录做到了准确、齐全、清晰、工整,记录本管理完好、整洁。(3)班组和每个岗位都有安全生产责任制和安全技术操作规程。 (4)新入厂、新调换工种的工人,离岗一个月后上岗前全部进行了班组安全教育及考核,教育考核有记录。 (5)特种工种持证上岗率达到100%。 (6)每周按规定的内容进行了安全活动,做到了人员、时间、内容三落实,活动有记录。 (7)全班人员都有自己的安全检查点,巡回检查路线及标准,并按点、路线、标准进行了检查,检查有记录。 (8)按时进行班前安全讲话及班后安全讲评,并有记录。 (9)连续生产的单位认真执行了交接班制度,并有记录。 (10)危险施工现场有安全监护人,严格执行监督检查,每次都应有记录。 (11)所使用的设备、设施、工具、用具、仪表、仪器、容器都有专人保管,有安全
检查责任牌,按时进行检查,检查有记录。 (12)所有设备、设施、工具、用具必须完好,安装前符合要求;部件、附件完好齐全,连接牢固;防护、保险、信号、仪表、报警完好齐全,准确灵活,作用有效,该检验的应有记录,符合规定标准;所有场地的油气水管线,闸门无跑、冒、滴、漏现象。(13)应装置安全标志的地方,按标准装置且标志完好清晰。 (14)生产场地平整、清洁、无危险建筑及设施;生产的成品、半成品,所用的材料、原料,使用的用品、工具堆、摆放符合安全要求;无生产中不需要的易燃易爆及危险物品,如需要应有使用规定及防护措施;光线、照明要符合国家标准,应装置安全防护的地方都按标准进行了安装。 (15)设备、设施等高处部位,无没有固定的工具及其它物件。 (16)电气、电路安装正确、完好,该使用防爆电气的地方,按要求使用,应装防静电装置的地方,正确装置了防静电装置。 (17)消防设施、器材、工具按要求配备,保管完好,定期进行了检验维修,实行了挂牌制。 (18)禁烟火的生产场所,无火源及烟蒂、火柴棒,动火作业按要求办理动火手续,并制定严格的防护措施。 (19)进行有毒、有害的作业,有安全防护措施。 (20)生产场所无生产中不需用的电炉、煤(汽、柴)油炉和液化气炉,经过批准使用的有安全规定,并按规定执行。 (21)应安避雷装置的地方,按要求正确地进行了安装。 (22)环保治理设施完好,运转正常,有运转记录。
物料系统GMP自检
物料管理系统GMP自检 检查依据药品生产质量管理规范(2010年修订) 第三十六条生产区、仓储区应当禁止吸烟和饮食,禁止存放食品、饮料、香烟和个人用药品等非生产用物品。 第四十四条应当采取适当措施,防止未经批准人员的进入。生产、贮存和质量控制区不应当作为非本区工作人员的直接通道。 第五十七条仓储区应当有足够的空间,确保有序存放待验、合格、不合格、退货或召回的原辅料、包装材料、中间产品、待包装产品和成品等各类物料和产品。 第五十八条仓储区的设计和建造应当确保良好的仓储条件,并有通风和照明设施。仓储区应当能够满足物料或产品的贮存条件(如温湿度、避光)和安全贮存的要求,并进行检查和监控。 第五十九条高活性的物料或产品以及印刷包装材料应当贮存于安全的区域。 第六十条接收、发放和发运区域应当能够保护物料、产品免受外界天气(如雨、雪)的影响。接收区的布局和设施应当能够确保到货物料在进入仓储区前可对外包装进行必要的清洁。第六十一条如采用单独的隔离区域贮存待验物料,待验区应当有醒目的标识,且只限于经批准的人员出入。 不合格、退货或召回的物料或产品应当隔离存放。 如果采用其他方法替代物理隔离,则该方法应当具有同等的安全性。 第六十二条通常应当有单独的物料取样区。取样区的空气洁净度级别应当与生产要求一致。如在其他区域或采用其他方式取样,应当能够防止污染或交叉污染。 第一百零九条使用计算机化仓储管理的,应当有相应的操作规程,防止因系统故障、停机等特殊情况而造成物料和产品的混淆和差错。 使用完全计算机化仓储管理系统进行识别的,物料、产品等相关信息可不必以书面可读的方式标出。 第二百四十一条应当建立操作规程,规定原辅料、包装材料、质量标准、检验方法、操作规程、厂房、设施、设备、仪器、生产工艺和计算机软件变更的申请、评估、审核、批准和实施。质量管理部门应当指定专人负责变更控制。
六大系统自检
“六大系统”自检 根据集团公司组织开展井下安全避险“六大系统”专项检查的通知。我矿认真开展井下安全避险自检工作,实现了矿井安全生产,进一步促使我矿井下安全管理工作向安全、可靠、保障有力的方向发展。为了做好井下安全避险工作,现对压风自救、供水施救、通讯联络系统进行自检结果如下: 一、成立领导组:********成立“六大系统”专项检查领导组 组长:*** 副组长:*** 常务副组长:*** 成员:*** *** *** *** ** 领导组下设办公室,办公室设在机电供应部 二:检查主题:井下安全避险“六大系统”专项检查。 三:检查内容: 1、压风系统 压风系统的压风管路已安装完成,压风机房正在施工。 2、供水施救系统 我矿现有水塔1座,容量为200m3,副井吃水井给水塔供水,由水塔到井下,供水管管径为4寸,每100米安装一个三通。
(1)系统应符合本标准的规定,符合《煤矿安全规程》、AQ 1020-2006等标准的有关规定,系统中的设备符合有关标准及各自企业产品标准的规定。 (2)自制件经检验合格、外协件、外购件具有合格证或经检验合格方可用于装配。 (3)装置的水管、三通及阀门及仪表等设备的材料符合GB.3836等相关规定。 (4)地面永久性水池每季度检查一次,根据情况及时清挖,安装过滤和净化设施,水质达到饮用水标准;还有防冻和防杂物掉入及中性化处理的措施。 (5)井下所有供水管路保持24小时供水。 (6)供水施救系统必须安设入井前、采区、工作面等多级水质过滤器,进入采掘工作面前的管路上装备高质量的水质过滤装置,过滤器有反水清杂装置并每月检查清理一次。 (7)采区及以上巷道中的供水施救系统安设内径不小于150mm的管路,其余所有巷道中的供水施救系统安设内径不小于100mm的管路,管路要吊挂平直、不拐死弯,接头阀门不花接不漏水(成线)。 (8)所有巷道内的供水管路每隔50m设一个三通阀门。 (9)所有供水管路三通阀门必须齐全、规格为6分、统一编号管理,手把灵活。 (10)采掘巷道管路安设距工作面距离不得大于50米。
生产车间内审检查表.docx
检查内容文件管理 记录管理 人力资源 内审检查表(生产用) 检查点检查结不合项说明1所有文件字迹是否清楚?□是□否 2所有文件标识是否明确?□是□否 3所有线上使用的文件是否受控□是□否 4文件发布前是否得到授权人的批准?□是□否 5所有文件是否均注明制定或修订日期?□是□否 6文件修改后是否重新批准?□是□否 7使用处是否都使用适应文件的有效版本?□是□否 是否对外来文件的收集、审查、批准、归档 8、发放、使用、评审、更新、补充、和作废□是□否 等作了规定? 9是否对保留的作废文件进行标识和管理,以□是□否 防止误用? 10各工序是否有按要求填写相关记录?□是□否 11记录是否填写完整?□是□否 12记录填写的数据是否正确?□是□否 13记录是否缺失?□是□否 14记录是否有规定保存期限?□是□否 15记录是否按规定期限保存□是□否 16过期记录是否按要求进行处置?□是□否 17是否有岗位职责、技能要求说明书□是□否 18是否有教育培训计划?□是□否 19是否按要求进行过培训、考核?□是□否 20是否有培训、考核记录?□是□否 21关键工位是否经过资格认证?□是□否 22是否有上岗证?上岗证是否在有效期范围□是□否 23 内? 作业员是否能按作业导书正确操作?□是□否 24临时工、培训工是否有区别标示?□是□否 25员工穿戴是否整齐清洁 , 是否衣衫不整?□是□否 26 员工是否按要求配戴防静装备 , 工衣 , 工帽, □是□否 工鞋 , 手套和厂牌? 27 员工是否有做与工作无关的事 , 是否聊天 , 打 □是□否 闹, 玩手机 , 打磕睡等?
作业控制 设备 ( 仪器、工装)控制 标识与追溯28每个工位是否有作业指导书或检验作业指导□是□否29 书? 作业指导书版本是否最新版本?□是□否30作业指导书字迹是否清楚?□是□否31作业指导书是否经过审核确认□是□否32作业指导书是否破损或有油污?□是□否33实际作业是否与作业指书一致?□是□否34使用的设备、工具、仪器是否符合作业指导□是□否书规定的要求? 35设备、工具、夹具所设定的参数是否符合作□是□否业指导书规定? 36关键工序是否有标识和定位□是□否 37是否有设备台账□是□否38台账所记录的内容与实际是否一致□是□否39是否有设备安全操作规范?□是□否40作业是否严格按照规范作业?□是□否41是否按要求进行日常点检、维护、保养?□是□否42是否有点检、维护、保养记录表?□是□否43对点检不合格项是否采取相应对策,并作了□是□否记录? 44是否有设备维修记录?□是□否45设备是否按周期进行了校准?□是□否46设备是否有校准和检验记录?□是□否47设备是否有易于识别的校准状态标示?□是□否48设备的使用是否在校准的有效期限内?□是□否49区域、物料、设备、工具等是否有标示?□是□否50标示是否能区分加工状态?物料,半成品,□是□否成品是否都有明确的状态标识 51是否有划分区域标示,区域化标示颜色是否□是□否符合程序文件规定? 52不合格品是否有隔离放置、是否有明确标□是□否53 识? 是否有机器运行状态标示?□是□否54防静电区域有无防静电标示?□是□否55标示与实物是否一致?□是□否56周转车、工具、成品、半成品及其他物品是□是□否否放置在规定的位置之内? 57是否对标示方法、方式进行标准化?□是□否58标示的大小、颜色、材料是否符合标准 ?□是□否59标示是否破损,脏污?□是□否
医疗器械生产质量管理规范内审检查表
医疗器械生产质量管理规范自查报告 章节条款内容检查结果判定 机构和人员1.1.1 应当建立与医疗器械生产相适应的管理机构,具备组 织机构图。 查看提供的质量手册,是否包括企业的组织机构图, 是否明确各部门的相互关系。 *1.1.2 应当明确各部门的职责和权限,明确质量管理职能。 查看企业的质量手册,程序文件或相关文件,是否对 各部门的职责权限作出规定;质量管理部门应当能独 立行使职能,查看质量管理部门的文件,是否明确规 定对产品质量的相关事宜负有决策的权利。 1.1.3 生产管理部门和质量管理部门负责人不得互相兼任。 查看公司的任职文件或授权文件并对照相关生产、检 验等履行职责的记录,核实是否与授权一致。 1.2.1企业负责人应当是医疗器械产品质量的主要责任人。 1.2.2 企业负责人应当组织制定质量方针和质量目标。 查看质量方针和质量目标的制定程序、批准人员。 1.2.3 企业负责人应当确保质量管理体系有效运行所需的人 力资源、基础设施和工作环境。 1.2.4 企业负责人应当组织实施管理评审,定期对质量管理 体系运行情况进行评估,并持续改进。 查看管理评审文件和记录,核实企业负责人是否组织 实施管理评审。 *1.2.5 企业负责人应当确保企业按照法律、法规和规章的要 求组织生产。 —4—
1.3.1企业负责人应当确定一名管理者代表。查看管理者代表的任命文件。 *1.3.2管理者代表应当负责建立、实施并保持质量管理体系,报告质量管理体系的运行情况和改进需求,提高员工满足法规、规章和顾客要求的意识。 查看是否对上述职责作出明确规定。查看管理者代表报告质量管理体系运行情况和改进的相关记录。 1.4.1技术、生产、质量管理部门负责人应当熟悉医疗器械法律法规,具有质量管理的实践经验,应当有能力对生产管理和质量管理中实际问题作出正确判断和处理。 查看相关部门负责人的任职资格要求,是否对专业知识、工作技能、工作经历作出规定;查看考核评价记录,现场询问,确定是否符合要求。 1.5.1应当配备与生产产品相适应的专业技术人员、管理人员和操作人员。 查看相关人员的资格要求。 *1.5.2应当具有相应的质量检验机构或专职检验人员。 查看组织机构图、部门职责要求、岗位人员任命等文件确认是否符合要求。 *1.6.1从事影响产品质量工作的人员,应当经过与其岗位要求相适应的培训,具有相关的理论知识和实际操作技能。 应当确定影响医疗器械质量的岗位,规定这些岗位人员所必须具备的专业知识水平(包括学历要求)、工作技能、工作经验。查看培训内容、培训记录和考核记录,是否符合要求。 1.7.1应当对从事与产品质量有影响人员的健康进行管理, 建立健康档案。 —5—
