初中化学元素符及化学式化合价化学方程式计算完整版

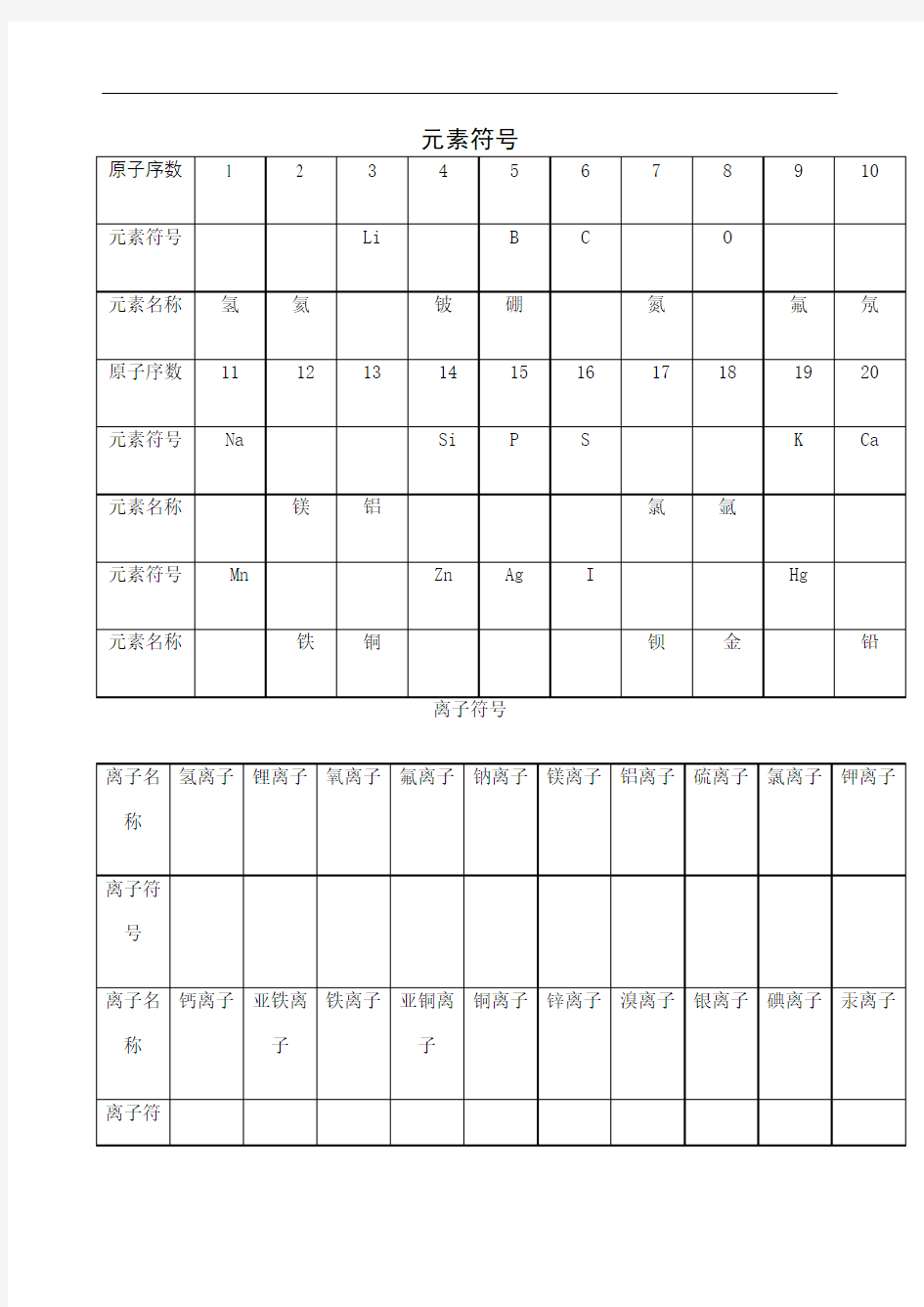
初中化学元素符及化学式化合价化学方程式计
算
标准化管理处编码[BBX968T-XBB8968-NNJ668-MM9N]
2
(SO
4
)
3(NO3)2
Cu2 (OH)
2
CO
3Cu SO45H2O
NH
4
H
CO
3KAl(SO4)224 H2O H2SO3H3PO4Na2SiO3 1:单质的化学式
2:化合物的化学式
中考类型题
1、下列物质中Cl元素化合价最高的是() A. HCl B. HClO C. HClO
3
D.
HClO
4
2、x、y、z三种元素的化合价分别是+1、+6、-2价,则此三种元素组成化合物的化学式
可能为()。
A. x
2
y z
3
B. x y z
C. x
2
y z
4
D. x
3
y z
4
3、重铬酸钾(K
2
Cr
2
O
7
)遇到酒中的乙醇分子由橙红色变为绿色的硫酸铬 [Cr
2
(SO
4
)
3
],由
此可用来检查司机是否酒后开车,K
2
Cr
2
O
7
和Cr
2
(SO
4
)
3
中铬元素的化合价依次为()。
A. +6 , +3
B. +5 ,+3
C. +3 , +3
D. +3 , +5
4、下列物质中,N 元素化合价由低到高排列的一组是( )。
A. N 2 , HNO 3 , N 2 O 3
B. N 2O, NO , HNO 3
C. NO , N 2 , N 2 O 5
D. N 2 O 5, N 2 O 3 , N 2
5、下列各组物质中同种元素的化合价完全相同的是( )
A. KMnO 4 与K 2MnO 4
B. SO 2与SO 3
C. HClO 3 与 KClO 3
D. Fe 2O 3和FeO
6、R 元素在化合物中只有一种化合价,请判断下列化学式中不正确的是( )
A. R 2O 3
B. R 2Cl 3
C. R 2(SO 4)3
D. R(NO 3)3
7、含磷洗涤剂因含Na 5P 3O 10能造成水生植物大量繁殖而污染环境。Na 5P 3O 10中P 元素的化合价为( )
A. +3价
B. +4价
C. +5价
D. +6价
8、按硫元素的化合价由低到高的顺序排列的物质:KHS 、S 、(X )、Na 2SO 4 , 其中括号内的X 物质可能是 ( )
A. H 2S
B. Na 2SO 3
C. MgSO 4
D. SO 3
9、下列元素(氧元素除外)化合价变化最大的是( )
A. ClO - → Cl -
B. MnO 4- →Mn 2+
C. C → CO 2
D. Fe 2O 3 → Fe
10、已知铵根(NH 4+)为+1价,硝酸根(NO 3-)的化合价为-1价。下列说法中正确的是( )。
A. 硝酸铵的化学式是NH 4(NO 3)2
B. 氮元素具有可变化合价。但在同一化合物中,氮
元素只有一种化合物。
C. 在硝酸铵中,求氮元素的化合价(x)的计算式:(+1)×4+(-2)×3+2 x =0
D. 在NH
4NO
3
中,氮元素既显-3价,又显+5价
11.有一种氮的氧化物,氮与氧的质量比为7:4,则该氧化物的化学式为( )
12.硫酸亚铁可用于治疗缺铁性贫血.某贫血患者每天需补充铁元素,服用的药物中含硫酸亚铁的质量至少为( ) 下列化合物中,铁元素质量分数最小的是( )
14.某气体单质和氧气的相对分子质量比为7:8,该气体可能是( )
15.氧化镁和另一种金属氧化物组成的混合物4g,含氧元素,另一种金属氧化物是( )
16.由Na
2SO
4
、Na
2
SO
3
和Na
2
S三种物质组成的混合物中,含氧元素的质量分数为22%,则其
中钠元素的质量分数为( ) % % D.无法确定
17.据报道,用于清洗龙虾的洗虾粉中含有柠檬酸钠,亚硫酸钠(Na
2SO
3
)等物质,可能对
人体产生危害。Na
2SO
3
中S元素的化合价为()
A.+6
B.+4
C.+2
18、我国的上海市建成了世界上第一条商业性磁悬浮铁路。磁悬浮的核心技术是利用超导
体的反磁性。高温超导物质(Y
2Ba
4
Cu
6
O
13
)是以YmOn、BaO、和CuO为原料,经研磨烧结而
成(此过程中所有元素的化合价均不变)。则高温超导物(Y
2Ba
4
Cu
6
O
13
)中元素Y显
价。
19:指出下列物质由几种元素组成,是单质还是化合物(物质分类)。
一、符号(化学式、元素符号、离子符号)前面的数字只表示粒子(分子、原子、离子)的个数。
①2H──2个氢原子;【元素符号前面的数字只表示原子的个数】
注意:千万别理解为两个氢元素。元素是宏观概念,只讲种类,不讲个数。
②2H
2
O──2个水分子;【化学式前面的数字只表示分子的个数】
③ 2Mg2+──2个镁离子;【离子符号前面的数字只表示离子的个数】
④2SO
4
2-──2个硫酸根离子;【离子符号(原子团) 前面的数字只表示离子的个数】
二、符号右下角的数字只表示一个(或每个)粒子中某元素原子的个数或原子团的个数。
──1个氢分子由2个氢原子构成;【化学式中元素右下角的数字只表示一个分
① H
2
子中所含原子的个数】
② 2H
O──每个水分子由2个氢原子和1个氧原子构成;前面的2只表示2个水分子
2
──1个硫酸根原子团中含有1个硫原子和4个氧原子;
③ SO
4
注意:原子团只是化合物的组成部分,不能把原子团符号当成化学式。
三、元素符号右上角的数字只表示离子所带的电荷。
① Mg2+──1个镁离子带2个单位的正电荷;
2-──每个硫酸根离子带2个单位的负电荷;(不要理解为两个硫酸根离子带
② SO
4
两个单位的负电荷)
四、元素符号正上方的数字只表示某物质中元素或原子团的化合价。
1:──氧化镁中,镁元素的化合价为+2
写出下列符号的意义
H
Fe
CO
2
1、化学式用元素符号和数字的组合表示物质组成的式子,叫做化学式。例如O
,
2
,HCl等都是化学式。
H
2
2、相对原子质量由于原子实际数值太小,书写和使用都不方便,所以采用相对原子质量。以一种碳原子质量的1/12为标准,其他原子的质量跟他相比较所得到的比,作为这种原子的相对原子质量。
3、相对原子质量与质子数、中子数之间的关系:相对原子质量≈质子数+中子数
4、纯净物中各元素质量比=纯净物中各元素原子的相对原子质量总和之比
5、质量分数=纯净物中某元素的质量分数=该元素原子的相对原子质量总和/相对分质量
×100%
6、原子个数比化学式中各元素原子个数比等于元素质量除以该元素的相对原子质量的商之比
1、计算相对分子质量
O
2KClO
3
2Ca(OH)
2
Fe
3
O
4
KMnO
4KClO
3
Na
2
CO
3
NH
4
HCO
3
CaCO
3
AgNO
3CH
3
COOH C
2
H
5
OH CO
2
CuSO
4
Fe
2O
3
H
2
SO
4
HCl MnO
2
NaCl:
神州七号载人航天飞船的火箭发射是以偏二甲肼(C
2H
8
N
2
)为燃料以N
2
O
4
为助燃物,C
2
H
8
N
2
是
由______ 元素组成,1个C
2H
8
N
2
分子共有____个原子,2 C
2
H
8
N
2
的相对分子质量等于___
1、据报道,月球上有大量3He存在,以下关于3He的说法正确的是
A.是4
He 的同分异构体 B.比4
He 多一个中子 C.是4
He 的同位素 D.比
4
He 少一个质子
2、某些建筑材料会产生放射性同位素氡222 86Rn,从而对人体产生伤害,该同位素原子的中
子数和质子数之差是
A .136
B .50
C .86
D .222
3.下列离子中,电子数大于质子数且质子数大于中子数的是
A .D 3O +
B .Li +
C .ODˉ
D .OHˉ
4.某元素的两种同位素,它们的原子具有不同的
A .质子数
B .质量数
C .原子序数
D .电子数
5. Se 是人体必需微量元素,下列关于78 34Se 和80 34Se 的说法正确的是
A 、7834Se 和8034Se 互为同素异形体
B 、7834Se 和8034Se 互为同位素
C 、 7834Se 和8034Se 分别含有44和46个质子
D 、7834Se 和8034Se 都含有34个中子
6.1996年2月9 日欧7 一科学小组,由Zn
6030
和
Pb
20882
两原子经核聚合,并放出一定数目
的中子而制得
X 227112
原子,则两原子在核聚合过程中放出的中子数目是( )。
A .41
B .115
C .142
D .162
7.以下有关原子结构的说法中,正确的是( )
A .原子核都是由质子和中子构成的
B .原子次外层电子数不一定都是8
C .稀有气体元素原子最外层电子数不一定都是8
D .原子最外层电子数一般不超过4
8.X 、Y 、Z 三种元素,已知X 和Y 原子核外电子层数相同,Y 和Z 原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
A .N 、P 、O
B .N 、
C 、Si C .B 、Mg 、Al
D .C 、N 、P
9.已知元素X 、Y 的核电荷数分别是a 和b,它们的离子X m+和Y n-的核外电子排布相同,则
下列关系式正确的是
A .a=b+m+n
B .a=b-m+n
C .a=b+m-n
D .a=b-m-n
10.下列离子化合物中,阴阳离子电子层结构相同的是( )
A .氯化钠
B .氧化镁
C .氯化钙
D .氧化钙
11.已知-2A 、-B 、+C 、+2D 、+3E 五种简单离子的核外电子数相等,则它们对应的核电荷数由大到小的顺序是( )
A .A >
B >
C >
D >
E B .B >A >C >D >E C .C >D >E >A >B D .E >D >C >B >A
12.下列微粒中,电子层结构完全相同的一组是( )。
A .-2S 、-Cl 、+K
B .-Cl 、-Br 、-I
C .+Na 、+2Mg 、-F
D .-2O 、
+2Mg 、-Cl
13.某原子中的电子由在K 层上运动变为在M 层上运动,将( )。
A .吸收能量
B .释放能量
C .能量不变
D .无法判断
14.已知元素X 、Y 的核电荷数分别是x 和y ,它们的离子+m X 和-n Y 的核外电子排布相同,则下列关系式中正确的是( )。
A .x -y =m -n
B .x -y =m +n
C .y -x =m -n
D .y -x = m +n
15.今有A 、B 两种原子,A 原子的M 层比B 原子的M 层少3个电子,B 原子的L 层电子数恰为A 原子L 层电子数的2倍。则A 、B 分别是( )。
A .He 和
B B .
C 和Cl C .Na 和Si
D .C 和Al
16.下列分子中有3个原子核和10个电子的是( )。
A .3NH
B .2SO
C .HF
D .O H 2
17.与氖原子核外电子数相同的双原子分子是________;与氖原子核外电子数相同的三原子分子是________;与氖原子核外电子数相同的四原子分子是________ ;与氖原子核外电子数相同的五原子分子是________。
18.结构示意图为的微粒,其x 值可能为________ 、________、________、
________、________、________,相应的微粒符号分别为________、________、________、________、________、________。
19.某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图为________ 。
20.A 和M 为两种主族元素,已知A 位于短周期,且A 2-与M +的电子数之差为8,则下列说法中正确的是( )
A.A和M的原子序数之差为8 B A和M原子的电子总数之和可能是11 C.A和M原子的最外层电子数之和为8 D.A和M原子的最外层电子数之差为7 3、原子个数比、元素质量比、质量分数
1、有关尿素[CO(NH
2)
2
]的说法正确的是 ( )
A.尿素的相对分子质量为:12+16+14+1×2×2=46 B.尿素是一种有机氮肥C.尿素中碳、氧、氮、氢四种元素的质量比为:12:16:14:1
D.尿素中氮元素质量分数的计算式为:(14/60)×l00%
2、某气体单质和氧气的相对分子质量比为7:8,则该气体可能是 ( )
A.CO B.CO
2 C.N
2
D.Cl
2
3、世界卫生组织(WHO)将某氧化物RO
2
列为A组高效安全灭菌消毒剂,它在食品保鲜、
饮用水消毒等方面有着广泛应用。实验测得该氧化物中R与O的质量比为71:64,R
2
O 的化学式为()
A.CO
2B.ClO
2
C.SO
2
D.NO
2
4、氮元素的一种氧化物中氮元素与氧元素质量之比为7:12,则该氧化物的化学式为
()
A.NO B.N
2O
3
C.NO
2
D.N
2
O
5
5、下列几种化合物,含铁元素的质量分数最高的是( )
A.Fe
3O
4
B.Fe
2
O
3
C.FeO D.FeS
6、在一氧化碳中,碳元素与氧元素的质量比是 ( )
A.1∶1 B.1∶2 C.3∶4 D.3∶8
7、3.2g某种铁的氧化物含有2.24g铁元素,则这种铁的氧化物的化学式为 ( )
A.FeO B.Fe
2O
3
C.Fe
3
O
4
D.Fe
3
O
2
8、当硝酸铵(NH
4NO
3
)和尿素[CO(NH
2
)
2
]中所含氮元素的质量相同时,它们的质量比为
( )
A.1︰1 B.2︰3 C.4︰3 D.8︰3
9、农村经常使用氮肥硝酸铵,化学式NH
4NO
3
,经过测定含氮量为37%,已知该化肥中只
含有一种杂质,则该化肥中可能混有下列物质中的哪种氮肥 ( )
A.氯化铵(NH
4Cl) B.硫酸铵[(NH
4
)
2
SO
4
] C.尿素[CO(NH
2
)
2
] D.碳铵
(NH
4HCO
3
)
10、已知某种NH
4NO
3
样品中混有不含氮元素的杂质,测得该NH
4
NO
3
样品中含氮的质量分数
为%,则样品中NH
4NO
3
的质量分数为 ( )
A.% B.49% C.70% D.80%
11、水中氢元素的质量分数为
A.% B.% C.% D.%
12、化学式为H
2R
2
O
3
的物质,其相对分子质量为114,则R的相对原子质量为 ( )
A.32g B.64g C.32 D.64
13、山茶油是一种绿色保健品,其主要成分是柠檬醛。现从山茶油中提取76g柠檬醛,将
其在氧气中完全燃烧,生成二氧化碳220g,水72g,则柠檬醛的组成中(相对原子质量:H-1 C-12 O-16)( )
A.只含有碳、氢元素 B.一定含有碳、氢、氧元素
C.一定含有碳、氢元素,可能含有氧元素 D.一定含有碳、氧元素,可能含有氢元素
14、今年春季以来,甲型H1N1流感疫情在一些国家持续蔓延,用于治疗流感的抗病毒药
物“达菲”可以有效地预防和治疗甲型H1N1流感。从烹调香料八角中提取到的莽草酸
(化学式为:C
7H
10
O
5
)是制取“达菲”的基本原料。下列有关莽草酸的说法正确的是
( )
A.莽草酸属于化合物 B.莽草酸中C、H、O三种元素的质量比为7∶10∶5
C.莽草酸的相对分子质量为174 D.该物质中含有22个原子
15、据报道,用750mL/L的乙醇处理5分钟,即可杀灭活甲型H1N1流感病毒。以下关于
乙醇(化学式:C
2H
6
O)说法错误的是 ( )
A.乙醇可用作消毒剂 B.乙醇中碳、氢、氧三种元素的质量比为2:6:1
C.乙醇由碳、氢、氧三种元素组成 D.乙醇是一种可再生能源
16、计算:
①氧化铁(Fe
2O
3
)的相对分子质量是;
②5000t含氧化铁84%的赤铁矿中,氧化铁的质量是多少
③上述赤铁矿理论上可炼得含铁98%的生铁多少
17、相同质量的CO
2和SO
2
中,含氧量之比为_________。若使CO
2
和SO
2
中含氧量相同,则
这两种物质的质量比为__________。
18、某新型胃药的一个分子中含有5个氮原子,氮元素的质量分数约为%,其相对分子质
量为________(计
算结果精确到)。
19、2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关。已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检
测值,俗称“蛋白精”,化学式为C
3H
6
N
6
。据此请计算:
(1)三聚氰胺中各元素的质量比;
(2)三聚氰胺中氮元素的质量分数。(写出具体的计算过程,结果精确到%)(3)某品牌合格奶粉蛋白质含量为18%,含氮量为%(假设奶粉中的含氮量全部来自蛋白质)。每100g奶粉中添加三聚氰胺,理论上能增加 g蛋白质。(写出具体的计算过程,结果精确到)
20、莽草酸(化学式:C
7H
10
O
5
)是制取抗“H1N1流感”药物“达菲”的原料。
请回答:
(1)莽草酸分子中C、H、O原子个数比为。
重点初中中考常见化合价口诀
精心整理化合价口诀(可以用到高中),找一个喜欢的版本 一家请驴脚拿银,(一价氢氯钾钠银)二家羊盖美背心.(二价氧钙镁钡锌)三铝四硅五价磷二三铁、二四碳一至五价都有氮铜汞二价最常见正一铜氢钾钠银正二铜镁钙钡锌三铝四硅四六硫二四五氮三五磷一五七氯二三铁二四六七锰为正碳有正四与正二再把负价牢记心负一溴碘与氟氯负二氧硫三氮磷 二钡钙镁锌铜氯正五七单质零正三铝 KNaHAg正一价CaMgZnBa正二价Cu为负二价Fe 氟氯溴碘银二氧汞铅铜,钡镁钙和锌三铝 ,二四碳,二四六硫都齐全铜 ,二四碳二四六硫都齐全铜汞二价最常见 编辑本段常见元素的主要化合价二 氟氯溴碘负一价;正一氢银和钾钠.氧的负二先记清;正二钡钙镁和锌.正三是铝正四硅;下面再把变价归.全部金属是正价;一二铜来二三铁.锰正二四与六七;碳的二四要牢记.非金属负主正不齐;氯的负一正一五七.氮磷负三与正五;不同磷三氮二四.二四六硫都齐全;边记边用就会熟.
一价氢氯钾钠银;二价氧钙钡镁锌,三铝四硅五价磷;二三铁,二四碳,二四六硫三五氮;铜汞二价最常见.一五七氯常常见,单质零价永不变. 氢钾钠银正一价;镁锌钡钙正二价铜有正一正二价;铁有正二正三价氧负二;铝正三;硅正四;负二正四正六硫;磷正五;氯在最后负一价负一硝酸氢氧根负二硫酸碳酸根负三记住磷酸根化合价口诀五一价氢氯钾钠银二价氧钙钡镁锌三铝四硅五价磷二三铁, 一价铵根硝酸根;氢氯酸根氢氧根. 酸根;氢硫酸根锰酸根. 常见元素化合价顺口溜(一): 钾钠氢银正一价, 正三,铁有正二和正三;碳有正二和正四, ,通常氧是负二价;铜一二铁二三, ,碳锡铅在二四寻,硫为负二正四六,,三价记住硼、铝、金.新增一价氢 ,二四碳一七氯,三五氮硫价常显二四六铜汞一二有都有 常见元素化合价顺口溜(四): 正一铜氢钾钠银正二铜镁钙钡锌三铝四硅四六硫二四五氮三五磷一五七氯二三铁碳有正二和正四再把负价牢记心负一溴碘与氟氯负二氧硫三氮磷(氮和磷都显正三价与负三价)
2020年中考化学复习专题-化学式与化合价
2 2 2 2 2 2 2 2 2 4 3 2 2 2020年中考化学复习专题-化学式与化合价 一、选择题 1. 下列化学符号中,表示 2 个氢分子的是( ) A .H B .2H C .2H D .2H + 2. 下列符号中,表示两个氢原子的是( ) A .2H B .2H C .H D .2H + 3. 下列化学符号书写正确的是( ) A .两个水分子﹣2H 2O B .氯化铝﹣AlCl C .两个氯原子﹣Cl D .正二价的铜元素﹣Cu 2+ 4.下列符号能表示阳离子的是( ) A .N B .H C .Na + D .Cl ﹣ 5.如图中能表示 2N 2 的是( ) A. B . C . D . 6.下列书写符合要求的是( ) A .氧离子:O ﹣2 B .2 个氢原子:H C .氢氧化镁的化学式:Mg (OH ) D .铁离子:Fe 2+ 7.下列符号表示两个氢原子的是( ) A .H + B .2H C .H D .2H 8.下列化学用语表达正确的是( ) A .三个镁离子:3Mg 2+ B .四氧化三铁:O Fe C .两个氢元素:2H D .氯化钙:CaCl 9.下列符号能表示 2 个氧分子的是( ) A .O B .2O C .2O D .2O 2﹣ 10. 下列化学用语书写正确的是( ) A.1 个铁离子:Fe 3+ B .3 个氧分子:3O C .氧化镁:MgO 2 D .2 个氮原子:N 2 二、填空题 2
3 11. 按要求填空: (1) 用化学符号表示:2 个亚铁离子 ,氨气 ; (2) 写出符号所表示的意义:2H , 2O 3 . 12.用化学用语或名称填空: (1) 磷元素 ; (2) 钠离子 ; (3) 两个氧分子 ; (4)NO 2 ; (5)AgCl ; (6)H 2CO 3 . 13. 用化学符号或名称填空. (1)碳元素 ; (2)H + ; (3)CO 2﹣ ; (4)氧化镁 ; (5)3 个氧分子 ; (6)NaCl . 14. 用适当的化学用语填空. (1)2 个氮原子 ; (2)保持水化学性质的最小粒子 ; (3)2 个铁离子 ; (4) 氧化铝中铝元素显+3 价 ; (5) 地壳中含量最多的元素 . 15.用化学用语填空: (1) 钾元素: ; (2) 镁离子: ; (3) 硝酸根离子: ; (4)2 个水分子: ; (5)碳酸: ;
(完整)初三化学化学式与化合价
初三化学化学式与化合价 一.选择题(共18小题)(注:第10和12题双选) 1.下列化学用语与意义相符的是() A.N2:表示2个氮原子B.Fe3O4:表示该物质中铁元素与氧元素的质量比为3:4 C.S2﹣:表示硫元素显﹣2价D.C2H3OH:表示该物质由三种元素组成,且1个分子中含7个原子2.血红蛋白的相对分子质量为68000,经测定其中铁的质量分数为0.335%,则每个血红蛋白分子中铁原子的个数为() A.1 B.2 C.3 D.4 3.人尿中含氮0.93%,如这些氮只存在于尿素中,则人尿中含尿素[CO(NH2)2]的质量分数为()A.0.20% B.1.00% C.1.99% D.0.02% 4.阿莫西林是一种常见的抗生素,其化学式为C16H19N3O5S,关于阿莫西林的说法正确的是()A.阿莫西林中含有16个碳原子B.阿莫西林是由五种元素组成的 C.一个阿莫西林分子中共含有43个原子D.阿莫西林中氢、氮元素质量比为19:3 5.X、Y两种元素,X原子的最外层有一个电子,元素Y为﹣2价,由X、Y两种元素形成的化合物的化学式可能是() A.X2Y B.XY C.X3Y2D.XY2 6.下列各个化学变化前后,同种元素的化合价数值变化最大的是() A.C→CO2B.KClO3→KCl C.KMnO4→K2MnO4D.NH3→NH4Cl 7.次氯酸(HClO)具有杀菌消毒的作用,HClO中氯元素的化合价表示正确的是()A.B.C.D. 8.酸根阴离子RO42﹣中R的化合价是() A.﹣2 B.0 C.+4 D.+6 9.下列有关化合价的说法中错误的是() A.在化合物中,有显正价的元素,也必有显负价的元素 B.在化合物中,金属元素显正价 C.同种元素在不同化合物中的化合价一定相同 D.离子所带电荷数与对应元素(或原子团)的化合价在数值上相等 10.下列关于化合价的说法正确的是() A.化合物中,氧元素通常显﹣2价B.化合物中,非金属元素一定显负价 C.氢气中氢元素的化合价为+1价D.化合物中正负化合价的代数和一定为零 11.C3N4是一种新型材料,它的硬度比金刚石还大,可做切割工具,在C3N4中,氮元素的化合价为﹣3,则碳元素的化合价是() A.+1 B.+3 C.+4 D.﹣4 12.某氮的氧化物中,氮、氧元素的质量比为7:16,该化合物的化学式是() A.NO B.NO2C.N2O3 D.N2O4 13.下列各组化合物中,所含原子团化合价不同的一组是() A.Ca(OH)2、KNO3 B.KNO3、KClO3 C.CaCO3、Na2SO4D.KMnO4、K2MnO4 14.下列说法正确的是() A.金属铁中铁元素有0、+2、+3价B.纯净物都是由同种元素组成的 C.离子在化学反应中不一定发生变化D.不同种元素组成的物质才是混合物 15.在下列化合物中,具有﹣1价原子团的是() A.Mg(OH)2 B.FeSO4C.KCl D.(NH4)2CO3
初三化学化学式与化合价
化学式与化合价 一、知识要点 知识要点一: 化学式 1.概念:用符号表示物质组成的式子。例: 2.化学式的意义: 宏观:表示物质及物质的组成. 微观:表示一个分子及该分子的原子构成。 化学式前面的数字表示的个数。 【随堂练习】指出下列符号的意义: H 2H H22H2 知识要点二:化合价 1.概念:表示原子之间相互的数目。 2.化合价的实质:元素在化合时,一个原子(或)电子的数目。规定:一个原子得到几个电子,该元素就显价,一个原子失去几个电子,该元素就显价。元素的化合价与原子的关系密切,是一种化学性质。 3.化合价的表示方法:在元素符号的正上方表上“+”或“-”号,然后标上数值。4.化合价有价和价之分。 5.单质中元素化合价为. 6.化合物中正负化合价的代数和为. 7.常见元素的化合价:氧-2 氢+1 口诀:8.原子团的化合价与原子团所带的电荷数一致。 知识要点三:根据化学式定化合价 原则:化合物中正负化合价的代数和为零。 【随堂练习】1. 标出下列物质中带“·”元素的化合价。 1. H2S. 2. H2S.O4 3. N.H4Cl 4. KN.O3 2.下列化学变化中,标“·”元素化合价变化最大的. A. KC.lO3—→KCl B. M.nO4—→K2MnO4 C. H.2O—→H2 D. C.O—→CO2 3.某化合物的化学式为H n RO3n+1,则R元素的化合价为。 4.试将R元素的化合价填入下表:
知识要点四:根据化合价写化学式 (一)单质化学式的写法 1. 单原子构成的单质:(1)稀有气体原子的最外层已达到相对稳定结构,其单质由单原子构成,化学式用元素符号表示。如:氦He、氖Ne等。(2)金属、某些固态非金属(如碳、磷、硫等)的化学式,也用元素符号表示。 2.多原子构成的单质:写多原子构成的单质的化学式时,它的分子是由几个同种原子构成的,就在元素符号的右下角写上数字几。如:氧分子由两个氧原子构成,其化学式是O2。气体单质多是双原子分子(稀有气体、臭氧等例外),液态溴(Br2)、固态碘(I2)等单质也是双原子分子。 (二)化合物化学式的写法:根据化合价书写化合物的化学式;1. 通常正价元素写在前,负价元素写在后。2. 把元素化合价的绝对值交叉写在元素符号的右下脚,再约分化成最简比。 【随堂练习】1. 写出下列物质的化学式: 氮气氦气锌氧化镁氧化铁 氧化亚铁氢氧化钠氢氧化钙硫酸铵硫酸铝 2.下列各组数字分别代表A、B两种元素的核电荷数,能组成AB2型化合物的是。 A. 11和7 B. 12和17 C. 13和17 D. 13和8 补充:1. 常见元素化合价表 K, Na, Ag+1H+1, -1 Ca, Mg, Ba, Zn+2F-1 Cu+1, +2Cl-1, +1, +5, +7 Fe+2, +3O-2, -1 Al+3S-2, +4, +6 Mn+2, +4, +6, +7Si+4 P-3, +3, +5B+3 As-3, +3, +5N-3, +1, +2, +3, +4, +5 补充2.常见原子团及离子符号: 硫酸根SO4硫酸根离子SO42-碳酸根CO3碳酸根离子CO32- 硝酸银NO3硝酸根离子NO3-磷酸根PO4磷酸根离子PO43- 氢氧根OH氢氧根离子OH-铵根NH4铵根离子NH4+ 锰酸银MnO4锰酸根离子MnO42-氯酸根ClO3氯酸根离子ClO3- 高锰酸根MnO4高锰酸根离子MnO4- 家长签字
2017年中考化学知识点大全:化学式和化合价
2017年中考化学知识点大全:化学式 和化合价 化学式和化合价 一、化学式 1、概念:用元素符号和数字表示物质组成的式子 2、含义(考点一):A表示某种物质;B表示某种物质的组成;C表示某种物质的一个分子;D表示某种物质的一个分子的构成。例如:H2O:A表示水这种物质;B表示水由氢元素和氧元素组成;C表示一个水分子;D表示一个水分子由一 个氧原子和二个氢原子构成。 3、分子个数的表示方法(考点二):在化学式前面加系数。若化学式前面有了系数后,这个符号就只能表示分子的个数。例如:表示3个二氧化碳分子:3CO2;4H2O:表示4个水分子。 4、化学式前面的数字的含义(考点三):表示分子的个数。例如:3H2O:3表示3个水分子。 5、元素符号右下角数字的含义(考点四):表示一个分子中所含该元素的原子个数。例如;H2O:2表示一个水分子中含有2个氢原子。 6、化学式的书写:(考点五) ⑴单质:A:氢气、氮气、氧气、氟气、氯气、溴、碘这七种单质:在元素符号右下角加2表示。例如:氢气:H2、氧气:O2 B:除上述七种以外的单质:通常用元素符号表示。例如:铁:Fe;红磷:P ⑵化合物(由两种元素组成或由两种原子团构成的):根据名称从右写到左。若已读出原子个数的就直接写;若未读出原子个数的需根据化合价来正确书写。例如:四氧化三铁: Fe3O4;氯化镁:Mg(+2) Cl(-1)2;硫酸钠: Na(+1)2SO4 7、化合物(由两种元素组成或由两种原子团构成的)的读法: 由两种元素组成的化合物:从右至左读作“某化某”;在氧化物中一般要读出原子个数 含有酸根(NO3、SO4、CO3、PO4)的化合物:从右至左读作“某酸某” 含有氢氧根(OH)的化合物:从右至左读作“氢氧化某” 例如:Fe3O4:四氧化三铁;MgCl2:氯化镁;Al(NO3)3:硝酸铝;Mg(OH)2:氢氧化镁。 二、化合价 1、化合价是用来表示元素在形成化合物时的原子个数比,是元素的一种化学性质。有正价与负价之分。
初中九年级化学上册《化学式与化合价》课后练习题附加答案
4.4化学与化合价 1.在1个H2SO4分子和1个H3PO4分子中,不正确的是( ) A.氧的质量分数一样 B.氧原子个数一样多 C.其相对分子质量一样 D.硫元素和磷元素的个数一样多 2.在100个C2H2和100个H2O2分子中,含量相同的是( ) A.氢元素 B.含氢的质量分数 C.氢原子 D.氢分子 3.下面叙述不正确的是( ) A.元素的化合价是元素的原子在形成化合物时才表现出来的性质 B.在氢气中氢元素的化合价为+1 C.在水中氧元素的化合价为-2 D.在NH3中氮元素的化合价为-3 4.X、Y两元素相对原子质量之比3∶4,在X,Y形成化合物的化学式中质量比为3∶8,则该化合物的化学式为( ) A.XY B.XY2 C.X2Y D.X2Y3 5.碳酸氢铵(NH4HCO3)是一种常用的氮肥,其中氮元素的化合价为( ) A.+5 B.+1 C.-1 D.-3 6.下列计算正确的是( ) A.2CO2的相对分子质量总和=2×12+16×2=56 B.Ca(OH)2的相对分子质量=40+16+1×2=58 C.(NH4)2SO4的相对分子质量=(14+1×4)×2+32+16×4=132 D.2H2O的相对分子质量总和=2×1×2+16=20
7.下列物质中,硫元素的化合价为+6的是( ) A.H2SO4 B.SO2 C.S D.H2SO3 8.下列含氮元素的化合物,氮元素化合价最高的是( ) A.NO B.NO2 C.N2O5 D.N2O 9.下列物质的化学式书写正确的是( ) A.五氧化二磷2PO5 B.氯化钾KCl C.氧化铝AlO D.高锰酸钾K2MnO4 10.在CuSO4中铜元素、硫元素、氧元素的质量比为( ) A.2∶1∶2 B.1∶1∶4 C.4∶2∶1 D.1∶2∶1 11.在二氧化硫中,硫元素的质量分数是( ) A.66.7% B.50% C.33.3% D.3.1% 12.某物质的化学式是R(OH)2,相对分子质量为58,则R的相对原子质量为( ) A.24 B.24g C.40 g D.40 13.某正三价金属元素A,它的氧化物中含氧元素的质量分数是30%,则A的相对原子质量是( ) A.56 B.27 C.32 D.16 14.1985年科学家发现一种新物质,化学式为C60,下列说法中正确的是( ) A.该物质是混合物 B.该物质为新型化合物 C.该物质的相对分子质量为120 D.该物质的一个分子中含有60个碳原子
初中化学九年级化学式与化合价习题精选.doc
初中化学九年级化学式与化合价习题精选 姓名:_____________ 年级:____________ 学号:______________ 一、选择题(共19题) 1.下列含硫物质中,硫元素的化合价为+4价的是() A.S B.H2S C.H2SO3 D.H2SO4 【答案】C 难度:容易知识点:化学式与化合价 2.下列四种物质①KClO3②Cl2③HCl④HClO,氯元素的化合价按由低到高顺序排列的是() A.①②④③ B.②③④① C.③②①④ D.③②④① 【答案】D 难度:容易知识点:化学式与化合价 3.某金属氧化物的组成为MO,如果在其氯化物中金属的化合价与该氧化物中的化合价相等,则该金属氯化 物的组成为() A.MCl B.MCl2 C.M2Cl D.M2Cl 【答案】B 难度:容易知识点:化学式与化合价 4.下列化学式正确的是() A.高锰酸钾(K2MnO4) B.氧化镁(MgO2) C.氯化钾(KClO3) D.氯化亚铁(FeCl2) 【答案】D 难度:容易知识点:化学式与化合价 5.某化合物化学式为HnMO2n已知在该化合物中M的化合价为+6,则n值为() A.1 B.2
C.3 D.6 【答案】B 难度:中等知识点:化学式与化合价 6.下列物质中氮元素的化合价由低到高的顺序排列一组是() A.N2O3、NH3、NO、N2 B.NH3N2NON2O3 C.NH3、NO、N2、N2O3 D.NON2N2O3NH3 【答案】B 难度:容易知识点:化学式与化合价 7.X、Y、Z三种元素的化合价分别为+1,+4,-2,则这三种元素所组成的化合物的化学式可能为()A.XYZ B.X4YZ3 C.X2YZ3 D.X3YZ2 【答案】C 难度:中等知识点:化学式与化合价 8.某元素R的氧化物分子中,R与O的原子个数比为2︰3,则R的化合价是() A.+2价 B.+3价 C.-2价 D.-3价 【答案】B 难度:中等知识点:化学式与化合价 9.某元素氧化物的化学式为M2O3(M化合价没有变化),则下列化学式中错误的是() A.MCl3 B.MSO4 C.M2(SO4)3 D.M(OH)3 【答案】B 难度:容易知识点:化学式与化合价 10.下列说法正确的是() A.元素的化合价数值等于一个原子得失电子的数目 B.铁的化合价为零 C.水中氢气的化合价为零 D.单质铜中铜元素化合价为零,化合物中铜元素化合价为+1或+2价 【答案】D 难度:中等知识点:化学式与化合价 11.下列化学式中正确的是()
最新初中化学化学式、化合价强化练习题
初中化学知识强化练习题 一、标出下列指定元素的化合价 N.2、N.H3、N.H4Cl、N.O、N.O2、N.2O4、HN.O3; H2S.、S.O2、S.O3、H2S.O4、BaS.O4; C.l2、NaC.l、HC.l、HC.lO、HC.lO4、HC.lO3、KC.lO3; C.H4、C.O、C.O2、H2C.O3、NaHC.O3、CaC.O3。 在下列化合物中根(原子团)下方划一短线,并标出根的化合价 ①KOH ②Na2CO3③BaSO4④NH4Cl ⑤AgNO3 ⑥KMnO4⑦NH4NO3⑧Cu2(OH)2CO3⑨KClO3⑩K2MnO4 (说明;同学们上述两个练习主要是为了复习初中阶段所学过的元素的化合价,有些常见元素化合价比较固定,例如化合物中氧为—2,氢为+1,我们初中是辅以口诀帮助大家记忆,一定要熟练的背诵并使用。另外呢,有些元素的化合价在不同的化合物中不同,我们称为变价,这种元素化合价的确定,往往是借助较固定元素的化合价,再根据化合物中各元素化合价之和等于零的原则加以计算,如练习一。要求同学们对化合价的复习,缘于高中阶段我们的第一章就要学习的:对氧化还原反应的判断中会使用。) 二、写出下列物质的化学式 硝酸根离子__ _ ___ 氢氧根离子__ _ ___ 硫酸根离子__ _ ___ 碳酸根离子__ _ ___ 铵根离子__ _ ___ 碳酸氢根离子__ _ ___ 碳酸__ _ ___、碳酸钠___ ___、碳酸氢钠______ ___、二氧化碳___________、 碳酸钙____ ____、碳酸氢钙_____________;氯化氢____ _____、氯气___ _____、 氯化钾___________、二氯化锰___________、氯酸钾_____ ______、 氢氧化钠___________、氢氧化钙___________、氢氧化铁___________、 氢氧化亚铁___________、氢氧化铝___________、氢氧化铜___________、 硝酸___________、硝酸钾____ _______、硝酸钡________ ___、硝酸铵______ ____、 硝酸铜______ _____、硝酸银___ ________;硫酸_______ ____、硫酸铵______ _____、硫酸钡______ _____、硫酸铝_______ ____、硫酸铁_______ ____、硫酸亚铁___________、
中考化学同步考点梳理:化学式与化合价(含答案)
2019-2020年中考化学同步考点梳理:化学式与化合价(含答案) 知识梳理 一、化学式 用元素符号和数字组合来表示物质组成的式子。 化学式的意义: 以H 2O 为例 对化学式的意义的几种错误说法 水由两个氢元素和一个氧元素组成;水由氢分子和氧分子构成 水由氢气和氧气组成; 水由氢分子和氧原子构成 水分子由氢分子和氧原子构成; 水由两个氢原子和一个氧原子构成 水分子由氢元素和氧元素组成 化学式的写法: 书写化合物的化学式时, 首先要弄清以下两点: ① 这种物质由哪种元素组成; ② 化合物中各元素的原子个数比是多少。 二、化合价:元素化合价是一个原子在化合时表现出来的性质。 在元素符号或原子团的上方标出化合价,“+”、“-”写在前,数字写在后。 化合价的一般规律: 金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价。氧元素通常显-2价,氢元素通常显+1价。 在化合物里正负化合价的代数和为0。 在单质中元素的化合价为0。 同一元素在不同物质里可显不同的化合价。在同一种物质里,同一元素也可显不同的化合价(如NH 4NO 3)。 三、化合价和化学式的关系: 根据化合价写化学式:“正价前,负价后,十字交叉右下处,化简才是原子数”。 根据化学式求化合价:根据记忆的其他元素的化合价,利用“化合物中正负化合价的代数和为0” 四、数字的意义: ① 元素符号前的数字表示几个某原子。如2H 中的“2”表示2个氢原子。 ② 化学式前的数字表示几个某分子。如2H 2O 中的“2”表示2个水分子。 ③ 元素符号右下角数字表示一个某分子或离子中有几个某原子。如CO 2中的“2”表示1个二氧化碳分子 -3 +5 水; 水由氢元素和氧元素组成; 一个水分子;
初三化学化学式与化合价练习题(含答案)
初三化学第四单元同步练习题:化学式与化合价 【模拟试题】(答题时间:35分钟) 一、选择题: 1. 下列物质的化学式书写正确的是 A. 氧化锌 OZn B.三氧化硫 03S C.氦气He2 D.氧化钙CaO 2. 已知二氧化碳的化学式为 C02,关于它的说法正确的是 A. 由一个碳元素和两个氧元素组成 ? B. 由一个碳原子和一个氧分子构成 ? C. 由碳元素和氧元素两种元素组成 ? D. 一个二氧化碳分子由一个碳原子和两个氧原子构成 3. 下列符号只具有微观意义的是 A. ::. B. 'I.'- 1 C. ..:< D. 4. 某工地发生多人食物中毒,经化验为误食工业用盐亚硝酸钠( 亠NaNO2)所致。亚硝酸 钠中氮元素的 化合价是 A. +1 B. +2 5. 航天飞船常用铝粉和高氯酸铵 化合价 是 D. +7 7. 化学用语是国际通用的化学语言,下列有关说法正确的是 2+ A. 2H 表示2个氢分子 B.镁离子的符号为 Mg C. O 2中氧元素的化合价为—2价 D. 一氧化碳的化学式是 Co 8. 下列微粒符号中,对“ 2”的含义理解正确的是 A. 2Cu 中的“ 2”表示2个铜元素 B. Fe 2+中的“ 2”表示每个亚铁离子带有 2个单位的正电荷 C. H 2S 中的“ 2”表示1个硫化氢分子中含有 2个硫原子 一2 ( )3 D. Al 2 S °4中化学式上方的“ 2”表示硫元素为一2价 9. 明矶[KAI (SO 4)m ]可用作净水剂,在该物质中 m 的值是 A. 1 B. 2 C. 3 D. 10 *10. H 2SO 3和H 2SO 4两种物质中,不同的是 A.物质的类别 B.所含元素种类 C.硫元素化合价 D.氧元素化合价 *11、元素A 与元素B 能形成AB 2型化合物,则A 、B 元素的核电荷数可能为 A. 13 和 17 B. 11 和 8 C. 6 和 8 D. 12 和 9 12.下列五种物质中均含有氮元素,它们是按氮元素的化合价由低到高的顺序排列的:① C.+3 D. +5 NH 4CIO 4)的混合物作为固体燃料,高氯酸铵中 CI 的 A.元素的化学性质、化合价 C.元素的核电荷数、原子的数目 B. 元素的种类、原子的质量 D.物质的状态、原子的稳定性 A. +1 B. +3 C.+5
九年级化学化学式与化合价教案 新课标 人教版
九年级化学化学式与化合价教案 根据化学式的计算1 教学目标: 1、知识与技能 (1)了解相对分子质量的涵义,并能利用相对原子质量和相对分子质量计算物质的组成。(2)能看懂某些商品标签或说明书上标示的物质成分和含量 2、过程与方法: 学习运用活动探究的方法,主动参与到学习中去获取知识。 3、情感态度与价值观 通过化学式的引入,对学生进行实事求是的科学态度的教育,充分培养学生的思维能力和计算能力。 重点、难点: 利用相对原子质量和相对分子质量计算物质的组成。 教法:讲练结合 教学过程: 复习练习: 1、一个水分子是由和构成。 2、硫的相对原子质量是32,表示的意义是() A .表示硫原子的相对原子质量是32g。 B.表示一个硫原子的质量为32g。 C.表示一个硫原子核内有32个质子。 D.表示一个硫原子质量是一个碳原子质量的1/12的32倍。 想一想: H的相对原子质量=1;O的相对原子质量=16,那么你们认为氢气(H2)分子、氧气(O2)分子、水(H2O)分子的相对分子质量是多少? H2的相对分子质量=2 O2的相对分子质量=32 你是怎样知道的? H2O的相对分子质量=? 18 是如何计算出来的? 相对分子质量(M r): (relative molecular mass) 化学式中各原子的 相对原子质量的总和。 (于书本P82画出关键词) (练习1) 下列关于相对分子质量的说法正确的是( ) A、物质的实际质量。 B、化学式中各原子的相对质量总和,是相对质量。 C、物质一个分子的实际质量。 D、化学式中各原子的数量的总和。
相对分子质量的单位是K g,这说法对吗? 三、有关相对分子质量的计算 1、计算相对分子质量 例1: 水(H2O)的相对分子质量 =1×2+16=18 (练习2) 下列物质的相对分子质量是多少呢? (1)氧气O2的相对分子质量= (2)二氧化碳CO2的相对分子质量= (3)氢氧化钙Ca(OH)2的相对分子质量= 计算相对分子质量的方法是怎样的?应注意些什么问题? 注意: 1)正确书写化学式. 2)元素符号之间用“+”号,元素符号与数字之间用“×”号。 3)化学式中的原子团作为一个整体, 如C a(OH)2 中的(OH),若含多个同种原子团时则把 (原子团的相对原子质量总和)×原子团个数。 讨论: 1个O2分子的相对分子质量大家都会算了,那么3个O2分子的总相对分子质量又如何计算? 2、计算多个分子的总相对分子质量 请算一算下列分子的总相对分子质量是多少? 1)3O2的总相对分子质量 =3×(16×2)=96 例2 1)3CO2的总相对分子质量 =3×(12+16×2)=3×44=132 2Ca(OH)2总的相对分子质量 =2×[40+(16+1)×2]=2×74=148 2)2H2O的总相对分子质量 =2×(1×2+16)=2×18=32 3)3Mg(OH)2的总相对分子质 =3×[24+(16+1)×2]= 174 注意: 4)计算多个分子的总相对分子质量时,化学式前的数字是表示分子的个数,计算时应把 个数×(一个分子的相对分子质量) 思考: 1、水是__________________由组成. 2、H2O的相对分子质量为18,则水中氢元素的质量占多少?氧元素的质量又占多少?那么水中氢元素质量与氧元素的质量比为多少? 例3:计算水中氢元素质量与氧元素的质量比 分析: 1、水由大量水分子构成。 2、水中氢元素质量是指所有水分子中H原子的质量总和。
2020年中考化学总复习考点素能检测:第8讲化学式与化合价-含答案
2020年中考化学总复习考点素能检测 第8讲 化学式与化合价 一、选择题 1.(2020-2021,泸州)下列物质的名称或俗称与化学式不相符的是(C) A.干冰——CO2 B.熟石灰——Ca(OH)2 C.小苏打——Na2CO2 D.氦气——He 2.(2020-2021,呼和浩特)地壳中含量最多的金属元素和含量最多的非金属元素所形成的化合物是(B) A.Fe3O4 B.Al2O3 C.SiO2 D.CuO 3.下列对于化学式“H2O”的各种表述不正确的是(B) A.表示水这种物质 B.表示水分子由氢元素和氧元素组成 C.表示1个水分子 D.表示1个水分子由2个氢原子和1个氧原子构成 4.(2020-2021,泰安)稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl3,则氧化铕的化学式为(B) A.EuO B.Eu2O3 C.Eu3O2 D.EuO3 5.学会分析寻找规律是学好化学的方法之一。分析NaCl、X、HClO、KClO3、KClO4的排列顺序,可知X代表的物质是(C) A.HCl B.Ca(ClO)2 C.Cl2 D.ClO2 6.(2020-2021,抚顺)氢氧化钠沾到皮肤上可用硼酸溶液处理。硼酸(H3BO3)中硼元素的化合价是(C) A.+1 B.+2 C.+3 D.+4 7.(2020-2021,泰安)掌握化学用语是学好化学的关键。下列化学用语与所表述的意义相符合的是(C) ①FeCl2—氯化亚铁 ②2Ca2+—2个钙离子 ③O2—2个氧原子 ④—钠离子 ⑤H2O—1个水分子 ⑥2H—2个氢元素 ⑦2—氮气中氮元素的化合价为零 A.①④⑤⑦ B.②③④⑥ C.①②⑤⑦ D.②⑤⑥⑦ 8.酸奶中含有的乳酸对健康是有益的。下列关于乳酸的叙述错误的是(B) A.乳酸属于有机化合物 B.乳酸分子中碳、氢、氧的原子个数比为1∶1∶2
初中化学式与化合价习题
化学式与化合价练习题 1.X、Y、Z三种元素的化合价分别为+1,+4,-2,则这三种元素所组成的化合物的化学式可能为() A.XYZ B.X 4YZ 3 C.X 2 YZ 3 D.X 3 YZ 2 2.下列离子符号书写正确的是() A.Na1+ B.OH-1 C.Al3+ D.SO 4 2- 3.下面是对“2”的含义的解释,其中错误的是() A.Fe2+:一个亚铁离子带2个单位正电荷 B.Ba(OH) 2 :氢氧化钡中,钡离子和氢氧根离子的个数比是1:2 C.Mg2+:带2个单位正电荷的镁离子 D.2 SO 4 2-:2个硫酸根离子,每个硫酸根离子带2个单位负电荷 4.下列化学式书写正确的是() A. MgO 2 B. K 2 Cl C. ZnCl 3 D. Ca(NO 3 ) 2 5.下列物质中硫元素化合价最低的是() A. S B. SO 2 C. H 2 SO 4 D. H 2 S 6.下列关于化合价的说法正确的是() A.化合物中,氧元素一定显-2价 B.化合物中,非金属元素一定显负价 C.氢气中氢元素的化合价为+1价 D.化合物中正负化合价的代数和一定为零7.下列物质的化学式,书写错误的是() A.氯化亚铁FeCl 2 B.氢氧化钠NaOH C.氧化镁MgO D.碳酸钠NaCO 3 8.有H、O、S、K四种元素,按指定化合价( H+1、O-2、S-2、K+1)组合,最多可以组成由两种元素组成的化合物的种数是 A.4种 B.5种 C.6种 D.7种 9.工业用盐亚硝酸钠(NaNO 2 )误作食盐,会使人中毒死亡。亚硝酸钠中氮元素的化合价是() A.+2 B.+3 C.+4 D.+5 10.在化合物KMnO 4和K 2 MnO 4 中不同的是() A.钾元素的化合价 B.氧元素的化合价 C.所含元素的种类 D.锰元素的化合价11.下列含碳的化合物中,碳元素的化合价相同的一组是() A. CO 2和Na 2 CO 3 B.CO和CO 2 C.CO和H 2 CO 3 D.CH 4 和CO 2 12.下列符号中只表微观意义的是( ) 既可用来表示一种物质,又可用来表示一种元素,还可用来表示一个原子的是 A.S B.O 2 C. 3C D.N 13在KMnO 4中锰元素的化合价为______,在NaNO 3 中氮元素的化合价为________。 14.标出下列物质中各元素的化合价:NH 3 N 2 K 2 SO 4
初中化学式与化合价习题
化学式与化合价练习题 1.X 、Y 、Z 三种元素的化合价分别为+1,+4,-2,则这三种元素所组成的化合物的化学式可能为( ) A .XYZ B .X 4YZ 3 C .X 2YZ 3 D .X 3YZ 2 2.下列离子符号书写正确的是 ( ) A.Na 1+ B.OH -1 C.Al 3+ D.SO 42- 3.下面是对“2”的含义的解释,其中错误的是( ) A.Fe 2+:一个亚铁离子带2个单位正电荷 B.Ba(OH)2:氢氧化钡中,钡离子和氢氧根离子的个数比是1:2 C.Mg 2+:带2个单位正电荷的镁离子 D.2 SO 42-:2个硫酸根离子,每个硫酸根离子带2个单位负电荷 4.下列化学式书写正确的是 ( ) A. MgO 2 B. K 2Cl C. ZnCl 3 D. Ca(NO 3)2 5.下列物质中硫元素化合价最低的是( ) A. S B. SO 2 C. H 2SO 4 D. H 2S 6.下列关于化合价的说法正确的是( ) A.化合物中,氧元素一定显-2价 B.化合物中,非金属元素一定显负价 C.氢气中氢元素的化合价为+1价 D.化合物中正负化合价的代数和一定为零 7.下列物质的化学式,书写错误的是( ) A .氯化亚铁FeCl 2 B .氢氧化钠NaOH C .氧化镁MgO D .碳酸钠NaCO 3 8.有H 、O 、S 、K 四种元素,按指定化合价( H +1、O -2、S -2、K +1 )组合,最多可以组成由两种元素组成的化合物的种数是 A .4种 B .5种 C .6种 D .7种 9.工业用盐亚硝酸钠(NaNO 2)误作食盐,会使人中毒死亡。亚硝酸钠中氮元素的化合价是( ) A.+2 B.+3 C.+4 D.+5 10.在化合物KMnO 4和K 2MnO 4中不同的是( ) A.钾元素的化合价 B.氧元素的化合价 C.所含元素的种类 D.锰元素的化合价 11.下列含碳的化合物中,碳元素的化合价相同的一组是( ) A. CO 2和Na 2CO 3 B.CO 和CO 2 C.CO 和H 2CO 3 D.CH 4和CO 2 12.下列符号中只表微观意义的是( ) 既可用来表示一种物质,又可用来表示一种元素,还可用来表示一个原子的是 A.S B.O 2 C. 3C D.N 13在KMnO 4中锰元素的化合价为______,在NaNO 3中氮元素的化合价为________。 14.标出下列物质中各元素的化合价:NH 3 N 2 K 2SO 4 15.用数字和化学符号表示:氦元素 ,3个硫酸根离子 ,4个亚铁离子 ,4个铁原子 ,铁元素的化合价为+3 ,3个二氧化硫分子 .3个水分子 ,2个硫原子______,钙离子_____,+5价的磷元素______ ,二氧化碳中氧元素的化合价为-2价 16.下列化学符号①2CO ②2Ag + ③Mg 2+ ④2 Mg ⑤H 2O 中的数字“2”表示(填序号)(1)离子个数的是 ;(2) 离子所带电荷数值的是 。(3)分子个数的是 ;(4)元素化合价数值的是 ;(5)表示1个分子中某原子个数的是 。 17.写出下列物质的化学式: 碳酸钙 氧化铁 硫酸铜 氯化钾 硫酸铝 氢氧化亚铁 氯化银 硝酸铜 碳酸钠 氯酸钾 高锰酸钾 二氧化锰 硫酸 18.下列含氯的化合物:①HClO ②Cl 2 ③NaCl ④KClO 3 ⑤HClO 4, 按氯元素的化合价由高到低的顺序排列为(填序号)________________。 19.为了履行国际社会的《关于消耗臭氧层物质的蒙特利尔议定书》,我国政府决定自2003年6月1日起在全国范围内禁止使用“CTC ”作为清洗剂。“CTC ”又称作四氯化碳,是常用的服装干洗剂,也是修正液(又称涂改液)中的一种溶剂,还是一种优良的灭火剂。根据以上信息回答: (1)“CTC ”的化学式为__________,其中碳元素的化合价为__________。 (2)推测“CTC ”的物理性质和化学性质各一种。 物理性质:____________________________________________; 化学性质:____________________________________________。 20.现有下列物质:氢气.二氧化硫.汞.水.氯化亚铁.红磷.二氧化碳.氧化铜.空气(除混合物之外均写化学式) (1)属于单质的是________________(2)属于化合物的是 ________________ (3)属于氧化物的是 (4)属于混合物的是
初中常用元素化合价表
钾 K +1 氯 Cl -1,+1,+5,+7 钠 Na +1 氧 O -2,-1 银 Ag +1 硫 S -2,+4,+6 钙 Ca +2 碳 C +2,+4 镁 Mg +2 硅 Si +4 钡 Ba +2 氮 N -3,+2,+3,+4,+5 锌 Zn +2 磷 P -3,+3,+5 铜 Cu +1,+2 硫酸根 SO4 -2 铁 Fe +2,+3,碳酸根 CO3 -2 铝 Al +3 硝酸根 NO3 -1 锰 Mn +2,+4,+6,+7 氢氧根 OH -1 氢 H +1 铵根 NH4 +1 氟 F -1 磷酸根 PO4 -3 氯酸根 ClO3 -1(Cl +5价) 关于化合价的口诀,方便大家记忆: 氢+1,氧-2, 银锂钠钾+l价, 锌镁钙钡+2价, 铝+3,硅+4. 只遇金属或是氢, 氮磷-3硫-2, 氟氯溴碘总-1. 可变价,不可怕, 具体判断"和为零". 单质为零要记清. "亚铜" +1"铜" +2, "亚铁" +2"铁" +3, 置换反应铁+2, 复分解时价不变. 关于化合价要准确记着金属元素化合价和原子团的化合价。一般非金属元素化合价是让你求的,所以只需要你了解非金属元素一般显负价,当含氧时显正价就可以了。具体是几不需要。
正一氢银和钠钾, 正二钙钡镁锌汞, 铜是一二,铁二三, 铝的价态是正三。原子团化合价口诀 OH氢氧根-1价, NO3硝酸根-1价 SO4硫酸根-2价 CO3碳酸根-2价 PO4磷酸根-3价 NH4铵根+1价 这种原子团化合价的记法便于掌握原子团的组成、名称、化合价。我们的学生一般都背这个。 一价钾钠氯(-1)氢银,二钾氧(-2)钙钡镁锌 三铝四硅五价磷 二三铁,二四炭,二四六硫都齐全 铜汞二价最常见 一价高锰、氯、硝酸根 二价锰、硫、碳酸根 三价磷酸根 元素化合价常用口诀表(金属显正价,非金属显负价) 一价钾钠氯氢银, 二价氧钙钡镁锌,
【最新整理】广东省中考化学第1部分物质构成的奥秘课时4化学式与化合价课时作业
课时4 化学式与化合价 基础巩固 1.下列化学式书写正确的是( ) A.氧化铝:AlO B.氯化亚铁:FeCl3 C.氢氧化镁:MgOH2D.氧化钠:Na2O 2.(2016·兰州)下列化学用语与意义对应不相符的是( ) A.O2:一个氧分子B.4Ne:4个氖原子 C.SiO2:二氧化硅D.2Mg2+:两个镁离子带两个单位的正电荷 3.(2016·潍坊)钛具有硬度大、密度小、熔点高、抗腐蚀性强等优良性能,被誉为“未来金属”。二氧化钛(TiO2)中氧元素为-2价,则钛元素的化合价为( ) A.+1 B.+2 C.+3 D.+4 4.(2016·滨州)2015年10月,诺贝尔生理学或医学奖被授予中国科学家屠呦呦,以表彰她所负责的研究团队发现了治疗疟疾的药物——青蒿素。下列关于青蒿素(C15H22O5)的说法错误的是( ) A.青蒿素是由碳、氢、氧三种元素组成的 B.青蒿素是由15个碳原子、22个氢原子、5个氧原子构成的 C.青蒿素的相对分子质量为282 D.青蒿素中氢、氧原子的个数比为22∶5 5.(2015·山西)(1)用化学用语填空:氮元素________;氧分子________;钠离子________;二氧化硫中硫元素的化合价________。 (2)闻名全国的“汾酒”是山西特产,其主要成分是乙醇,乙醇的化学式为C2H5OH。C2H5OH除表示乙醇外,还表示的意义有:①____________________________________;②C2H5OH中碳元素与氧元素的质量比为________。 能力提升 6.(2016·齐齐哈尔)清凉甘甜的汽水中常含柠檬酸,已知柠檬酸的化学式为C6H8O7,请回答: (1)柠檬酸中碳、氢、氧三种元素的原子个数是__________; (2)柠檬酸中碳元素的质量分数__________; (3)19.2 g柠檬酸含氢元素__________g。 7.(2016·郴州)焦亚硫酸钠有毒,不能直接用于食品加工,市场上有不法商贩将其溶液浸泡生姜,使生姜发黄发亮,食用此种生姜可能使人中毒,已知焦亚硫酸钠的化学式为Na2S2O x,相对分子质量是190,请计算: (1)x=__________; (2)焦亚硫酸钠中硫元素与氧元素的质量比是__________; (3)焦亚硫酸钠中钠元素的质量分数是__________(精确到0.1%)。 8.(2016·天津)尿素[CO(NH2)2]是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期施用没有不良影响。计算: 1
初三化学化学式与化合价练习题(含答案)
34 )SO ( 2 第四单元同步练习题:化学式与化合价 一、选择题: 1. 下列物质的化学式书写正确的是 A. 氧化锌OZn B. 三氧化硫O 3S C. 氦气He 2 D. 氧化钙CaO 2. 已知二氧化碳的化学式为CO 2,关于它的说法正确的是 A. 由一个碳元素和两个氧元素组成. B. 由一个碳原子和一个氧分子构成. C. 由碳元素和氧元素两种元素组成. D. 一个二氧化碳分子由一个碳原子和两个氧原子构成. 3. 下列符号只具有微观意义的是 A. B. C. D. 4. 某工地发生多人食物中毒,经化验为误食工业用盐亚硝酸钠(NaNO 2)所致。亚硝酸钠中氮元素的化合价是 A. +1 B. +2 C. +3 D. +5 5. 航天飞船常用铝粉和高氯酸铵(NH 4ClO 4)的混合物作为固体燃料,高氯酸铵中Cl 的化合价是 A. +1 B. +3 C. +5 D. +7 6. 与中数字“1”关系密切的是 A. 元素的化学性质、化合价 B. 元素的种类、原子的质量 C. 元素的核电荷数、原子的数目 D. 物质的状态、原子的稳定性 7. 化学用语是国际通用的化学语言,下列有关说法正确的是 A. 2H 表示2个氢分子 B. 镁离子的符号为Mg 2+ C. O 2中氧元素的化合价为-2价 D. 一氧化碳的化学式是Co 8. 下列微粒符号中,对“2”的含义理解正确的是 A. 2Cu 中的“2”表示2个铜元素 B. Fe 2+中的“2”表示每个亚铁离子带有2个单位的正电荷 C. H 2S 中的“2”表示1个硫化氢分子中含有2个硫原子 D. Al 2 中化学式上方的“2”表示硫元素为-2价 9. 明矾[KAl (SO 4)m ]可用作净水剂,在该物质中m 的值是 A. 1 B. 2 C. 3 D. 10 *10. H 2SO 3和H 2SO 4两种物质中,不同的是 A. 物质的类别 B. 所含元素种类 C. 硫元素化合价 D. 氧元素化合价 *11、元素A 与元素B 能形成AB 2型化合物,则A 、B 元素的核电荷数可能为 A. 13和17 B. 11和8 C. 6和8 D. 12和9 12. 下列五种物质中均含有氮元素,它们是按氮元素的化合价由低到高的顺序排列的:①NH 3;②N 2;③NO ;④X ;⑤N 2O 5。根据规律,X 不可能是 A. NO 2 B. NaNO 2 C. N 2O 3 D. N 2O *13. 蛋白质是构成细胞的基本物质,是由多种氨基酸构成的,是复杂的、相对分子质量
