化学物质分类混合物和纯净物
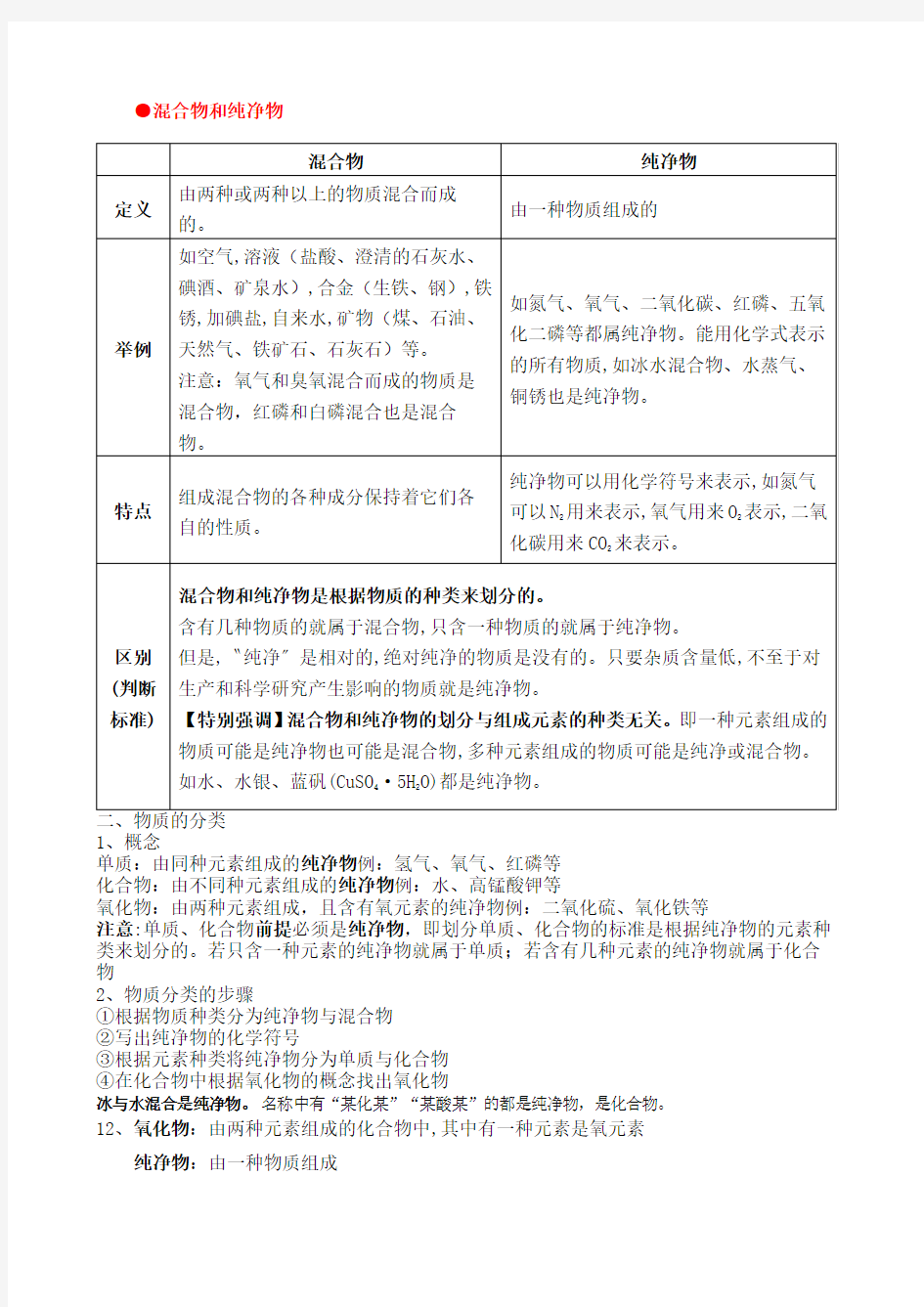

●混合物和纯净物
1、概念
单质:由同种元素组成的纯净物例:氢气、氧气、红磷等
化合物:由不同种元素组成的纯净物例:水、高锰酸钾等
氧化物:由两种元素组成,且含有氧元素的纯净物例:二氧化硫、氧化铁等
注意:单质、化合物前提必须是纯净物,即划分单质、化合物的标准是根据纯净物的元素种类来划分的。若只含一种元素的纯净物就属于单质;若含有几种元素的纯净物就属于化合物
2、物质分类的步骤
①根据物质种类分为纯净物与混合物
②写出纯净物的化学符号
③根据元素种类将纯净物分为单质与化合物
④在化合物中根据氧化物的概念找出氧化物
冰与水混合是纯净物。名称中有“某化某”“某酸某”的都是纯净物,是化合物。
12、氧化物:由两种元素组成的化合物中,其中有一种元素是氧元素
纯净物:由一种物质组成
混合物:由两种或两种以上纯净物组成,各物质都保持原来的性质
3.混合物:是由两种或两种以上的物质混合而成(或由不同种物质组成)例如,空气,溶液(盐酸、澄清的石灰水、碘酒、矿泉水),矿物(煤、石油、天然气、铁矿石、石灰石),合金(生铁、钢)
注意:氧气和臭氧混合而成的物质是混合物,红磷和白磷混合也是混合物。
纯净物、混合物与组成元素的种类无关。即一种元素组成的物质可能是纯净物也可能是混合物,多种元素组成的物质可能是纯净或混合物。
4.纯净物:由一种物质组成的。例如:水、水银、蓝矾(CuSO4·5H2O)都是纯净物
十三、物质的化学式
A单质:由同种(或一种)元素组成的纯净物。
1、金属单质(按金属活动性顺序由强至弱排列)
钡钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金
BaKCaNaMgAlZnFeSnPbCuHgAgPtAu
2、非金属单质
氢气H2氧气O2氮气N2氯气Cl2氟气(F2)溴(Br2)碘(I2)
碳C硅Si磷P硫S臭氧(O3)
3、稀有气体氦气He氖气Ne氩气Ar
B化合物:由不同种元素组成的纯净物。
(一)有机物:含碳元素的化合物(除CO、CO2和CO32-的化合物)
甲烷CH4乙醇C2H5OH甲醇CH3OH乙酸CH3COOH乙炔C2H2尿素CO(NH2)2
(二)氧化物:由两种元素组成,其中一种是氧元素的化合物。
1、非金属氧化物(大部分非金属氧化物通常是酸性氧化物,跟水化合成同价的含氧酸)
水一氧化碳二氧化碳二氧化硅五氧化二磷二氧化硫三氧化硫
H2OCOCO2SiO2P2O5SO2SO3
2、金属氧化物
氧化钡氧化钾氧化钙氧化钠氧化镁氧化铝氧化锌
BaOK2OCaONa2OMgOAl2O3ZnO
氧化铁氧化亚铁四氧化三铁氧化铜氧化亚铜氧化汞氧化银二氧化锰
Fe2O3FeOFe3O4CuOCu2OHgOAg2OMnO2
(三)酸:名称中最后一个字是“酸”,通常化学式的第一种元素是“H”
硫酸盐酸硝酸磷酸氢硫酸碳酸亚硫酸
H2SO4HClHNO3H3PO4H2S H2CO3H2SO3
(四)碱:由金属离子和氢氧根离子构成,碱的名称通常有“氢氧化某”化学式的最后面是“OH”
(五)盐:由金属离子和酸根离子构成
碱1、碳酸盐2、硫酸盐3、硝酸盐4.氯化物5.亚硫酸盐
氢氧化钾碳酸钾硫酸钾硝酸钾氯化钾亚硫酸钾
KOHK2CO3K2SO4KNO3KClK2SO3
氢氧化钠碳酸钠硫酸钠硝酸钠氯化钠亚硫酸钠
NaOHNa2CO3Na2SO4NaNO3NaClNa2SO3
氢氧化银碳酸银硫酸银硝酸银氯化银
AgOHAg2CO3Ag2SO4AgNO3AgCl
氨水碳酸铵硫酸铵硝酸铵氯化铵
NH3·H2O(NH4)2CO3(NH4)2SO4NH4NO3NH4Cl
氢氧化钙碳酸钙硫酸钙硝酸钙氯化钙亚硫酸钙
Ca(OH)2CaCO3CaSO4Ca(NO3)2CaCl2CaSO
3
氢氧化钡碳酸钡硫酸钡硝酸钡氯化钡
Ba(OH)2BaCO3BaSO4Ba(NO3)2BaCl2
氢氧化镁碳酸镁硫酸镁硝酸镁氯化镁
Mg(OH)2MgCO3MgSO4Mg(NO3)2MgCl2
氢氧化铜碳酸铜硫酸铜硝酸铜氯化铜
Cu(OH)2CuCO3CuSO4Cu(NO3)2CuCl2
氢氧化锌碳酸锌硫酸锌硝酸锌氯化锌
Zn(OH)2ZnCO3ZnSO4Zn(NO3)2ZnCl2
硝酸汞氯化亚铜
Hg(NO3)2 CuCl
氢氧化亚铁碳酸亚铁硫酸亚铁硝酸亚铁氯化亚铁
Fe(OH)2FeCO3FeSO4Fe(NO3)2FeCl2
氢氧化铁硫酸铁硝酸铁氯化铁
Fe(OH)3Fe2(SO4)
Fe(NO3)3FeCl3
3
氢氧化铝硫酸铝硝酸铝氯化铝
Al(OH)3Al2(SO4)3Al(NO3)3AlCl3
6、酸式盐(多元酸里的氢部分被金属取代,H夹在中间)
碳酸氢钠NaHCO3,碳酸氢钙Ca(HCO3)2
磷酸二氢钠NaH2PO4磷酸二氢钾KH2PO4硫酸氢钠NaHSO4,硫酸氢钾KHSO4
7、碱式盐(化学式的中间有“OH”):碱式碳酸铜Cu2(OH)2CO3
8、其他盐高锰酸钾KMnO4锰酸钾K2MnO4氯酸钾KClO3硫化钠Na2S
碘酸钾KIO3亚硝酸钠NaNO2硫化钾K2S
5.单质:由同种(或一种)元素组成的纯净物。例如:铁氧气(液氧)、氢气、水银。
6.化合物:由不同种(两种或两种以上)元素组成的纯净物。
名称中有“某化某”“某酸某”的是化合物。
7.有机物(有机化合物):含碳元素的化合物(除CO、CO2和含碳酸根化合物外)
无机物:不含碳元素的化合物以及CO、CO2和含碳酸根的化合物
8.氧化物:由两种元素组成,其中一种是氧元素的化合物。
a.酸性氧化物:跟碱反应生成盐和水的氧化物。CO2,SO2,SO3大部分非金属氧化物都是酸性氧化物,跟水反应生成同价的含氧酸。
CO2+H2O=H2CO3SO2+H2O=H2SO3SO3+H2O=H2SO4
b.碱性氧化物:跟酸反应生成盐和水的氧化物。CaONa2OMgOFe2O3CuO
大部分金属氧化物都是碱性氧化物,BaOK2OCaONa2O溶于水立即跟水反应
生成相应的碱,其他碱性氧化物不溶于水,跟水不反应。
CaO+H2O=Ca(OH)2BaO+H2O=Ca(OH)2Na2O+H2O=2NaOHK2O+H2O=2KOH
c.注意:CO和H2O既不是酸性氧化物也不是碱性氧化物,是不成盐氧化物。
9.酸:电离时生成的阳离子全部是氢离子的化合物。酸溶液的PH值小于7
酸的名称中最后一个字是“酸”,通常化学式的第一种元素是“H”,酸由氢和酸根离子组成紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色
根据酸的组成,通常有以下两种分类方法:酸的电离方程式:酸=nH++酸根离子n-
a.根据酸分子电离所能生成的氢离子的个数分为:一元酸(HCl、HNO3)、
二元酸(H2SO4、H2S、H2CO3)和三元酸(H3PO4)
b.根据酸分子里有无氧原子分为:
含氧酸(H2SO4,HNO3,H3PO4名称为:某酸)
无氧酸(HCl,H2S名称为:氢某酸)
鉴定酸(鉴定H+)的方法有:①加紫色石蕊试液变红色的是酸溶液;
②加活泼金属Mg、Fe、Zn等有氢气放出
10.碱:电离时生成的阴离子全部是氢氧根离子的化合物。碱通常由金属离子和氢氧根离子构成
溶碱有五种:钾钙钠钡氨(KOH,Ca(OH)2,NaOHBa(OH)2,氨水)它们的溶液无色。
有颜色的碱(不溶于水):红褐色的氢氧化铁(Fe(OH)3↓)、蓝色的氢氧化铜(Cu(OH)2↓)
其他固体碱是白色。碱的名称通常有“氢氧化某”,化学式的最后面是“OH”
可溶性碱的溶液PH值大于7,紫色石蕊试液遇溶碱变蓝色,无色酚酞试液遇溶碱变红色
鉴定可溶性碱溶液(鉴定OH-)方法一:加紫色石蕊试液变蓝色,加无色酚酞试液变红色是碱. 方法二:加铁盐溶液有红褐色沉淀生成;加铜盐溶液有蓝色沉淀的是碱。
11.盐:电离时生成金属离子和酸根离子的化合物。第一种分类方法:
a.正盐(酸碱完全中和的产物,没有可电离的氢离子或氢氧根离子),例如NaCl、Na2SKNO3
无氧酸正盐叫“某化某”Na2S_______MgCl2__________FeS__________
含氧酸盐叫“某酸某”KNO3_________BaSO4______________Na2CO3______
b.酸式盐(多元酸里的氢部分被金属取代,H夹在中间)
NaHCO3____________、Ca(HCO3)2_____________、NaH2PO4_____________
常见的酸式盐的酸根有:HCO3-、HSO4-、H2PO4-、HPO42-
c.碱式盐(化学式的中间有“OH”):Cu2(OH)2CO3
第二种分类方法
按盐中相同部分的离子称为某类盐:含碳酸根离子的盐称为碳酸盐、含硫酸根离子的盐称为硫酸盐、含硝酸根离子的盐称为硝酸盐、含铁离子的盐称为铁盐,等等。
12.酸碱指示剂(石蕊试液、无色酚酞)和PH值:
酸溶液的PH值小于7(如盐酸、稀硫酸、硝酸),酸性越强PH值越小,酸性越弱PH值越大。水、中性的硫酸盐、硝酸盐和盐酸盐溶液不能使指示剂变色,PH值等于7。不能使指示剂变色;可溶的碱溶液PH值大于7。碱性越强PH值越大,碱性越弱PH越小
13.酸碱盐溶解性口诀:
钾钠硝铵溶溶碱有五种钡钾钙钠氨
不溶氯化物AgCl不溶硫酸盐BaSO4碳酸盐只溶钾钠铵
口诀的含义:含有钾、钠、硝酸根、铵根的物质都溶于水
溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水
含Cl的化合物只有AgCl不溶于水,其他都溶于水;
含SO42-的化合物只有BaSO4不溶于水,其他都溶于水
含CO32-的物质只有含K+Na+NH4+溶于水,其他都不溶于水
14.沉淀物中AgCl和BaSO4不溶于稀硝酸,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀
其他沉淀是白色(包括Fe(OH)2)有以下常见的沉淀:Mg(OH)2Al(OH)3CaCO3BaCO3Ag2CO3
推断题中,往沉淀物加稀硝酸:若讲沉淀不溶解,则沉淀中一定有AgCl或BaSO4;若讲沉淀全部溶解,则沉淀中一定没有AgCl或BaSO4;若讲沉淀部分溶解,则沉淀中一定有AgCl或BaSO4中的一种,且还有另一种可溶于稀硝酸的沉淀。
高中化学《物质的分类》教案8新人教版必修
第二章第一课时“第一节物质的分类”教案 【教学目标】 1.体验进行分类的目的及意义。 2.学会根据物质的组成和性质对物质进行分类。 【教学重点】 分类法的意义及常见化学物质及其变化的分类方法 【教学方法】 讨论、讲授 【教学过程设计】 【情景引入】 若要到“万福”商场买一部复读机,你如何以最快的速度找到它? 【思考与交流】 请根据以往的生活经验和社会知识,列举一些应用分类法的例子。【师生交流】 分类法在日常生活中的应用是非常普遍的,我们应该善于发现和学会使用,以提高我们工作和学习的效率。 【学生活动】 组织学生对八支笔进行分类活动 分类并没有唯一性,它会根据分类的标准不同而不同。 【点评】当分类的标准确定之后,同类中的事物在某些方面的相似性可以帮助我们做到举一反三;对于不同类的事物的了解我们有可能做到由此及彼。所以分类的方法是一种非常简单易行的科学方法,分类法的应用也是非常普遍的。 【过渡】 其实分类方法不但在生活和工作中经常碰到,在化学学习过程中也普遍存在, 一、简单分类法及其应用 【学生活动】案例1、连线: 【师生交流】 通过这个活动,可以看出对于Na2CO3如果从阳离子来看,可以与Na2SO4一起分为硫酸盐。若从阴离子的角度来看可以与K2CO3一起分为碳酸盐。因此可以说, 【点评】 一种分类方法所依据的标准有一定局限,所能提供的信息少,人们在认识事物时往往需要采用多种分类方法来弥补单一分类方法的不足。1、交叉分类法 【学生活动】 案例2、对下列化学反应进行分类: (1)硫在氧气里燃烧 (2)红磷在氧气里燃烧 (3)铁丝在氧气里燃烧 (4)铝箔在氧气里燃烧
(5)蜡烛在氧气里燃烧 案例3、见课本P21,图2-32、树状分类法 【点评】:树状分类法可以让我们把同类事物进行再分 【实践活动】 按照物质的组成和性质,对纯净物进行分类,仿照P21图2-3作出树状分类图,然后选择下列合适的物质填在物质类别上。 O2, Cu,H2SO4, Ba(OH)2,KNO3, CO2,空气,含镁60%的MgO 【小结】 在学习了分类的方法以后,大家就要学会对以前和将要学的化学知识进行及时的归纳和整理,学会对物质及其变化进行分类,并通过对各类物质的代表物质的研究来了解这类物质的性质,从而提高我们化学学习的效率。 【练习】 【课后作业】 1、通过查找资料或与同学合作,为石油加工后的产物或用途制作一张树状分类图或交叉分类图。 2、某学校要举行田径运动会,有高一、高二、高三3个年级的男生、女生参加,请你画出以高一男子组、高一女子组……的方法分组的树状分类图。 3、填表: 【课后阅读材料】“白马非马”的故事 【原文】公孙龙是战国时期平原君的食客。一天,他牵一匹白马出关被阻,公孙龙便以白马非马的命题与之辩论,守关的人辩不过他,公孙龙就牵着马出关去了。(或说,他还是不得出关。)公孙龙说,白马为非马者,言白所以名色,言马所以名形也;色非形,形非色也。夫言色则形不当与,言形则色不宜从,今合以为物,非也。如求白马于厩中,无有,而有骊色之马,然不可以应有白马也。不可以应有白马,则所求之马亡矣;亡则白马竟非马。 【大致意思】公孙龙是战国时期平原君的食客。据说,公孙龙有一次骑马过关,把关的人对他说:“法令规定马不许过。”公孙龙回答说:“我骑的是白马,白马不是马,这可是两回事啊。”公孙龙的“白马”有没有过关,我们不得而知。从常人的观点来看,守关的兵士八成认为公孙龙是在诡辩。 【评论】 冯友兰(我国著名新理学家、哲学家)认为《公孙龙子》里的《白马论》对“白马非马”进行了三点论证: 一是强调“马”、“白”、“白马”的内涵不同。“马”的内涵是一种动物,“白”的内涵是一种颜色,“白马”的内涵是一种动物加一种颜色。三者内涵各不相同,所以白马非马。 二是强调“马”、“白马”的外延的不同。“马”的外延包括一切马,不管其颜色的区别;“白马”的外延只包括白马,有颜色区别。外延不同,所以白马非马。三是强调“马”这个共相与“白马”这个共相的不同。马的共相,是一切马的本质属性,它不包涵颜色,仅只是“马作为马”。共性不同,“马作为马”与“白马作为白马”不同。所以白马非马。
高中化学常见物质的分类
物质的分类 一、单质 按元素组成分为 1.金属单质 K钾、Ca钙、Na纳、Mg镁、Al铝、Zn锌、Fe铁、 Sn锡、Pb铅、Cu铜、Hg汞、Ag银、Pt铂、Au金 2.非金属单质 氢气H2、碳C、氮气N2、氧气O2、臭氧O3、氟气F2、硅Si、磷P、硫S、氯气Cl2、液溴Br2、碘I2、氦气He、氖气Ne、氩气Ar、 二、化合物 1.有机化合物 乙醇、甲烷、乙烷、乙烯、葡萄糖 2.无机化合物 三、氧化物 (1)按元素组成分为金属氧化物和非金属氧化物 1.金属氧化物 氧化钠Na2O、过氧化钠Na2O2、氧化钙CaO、氧化镁MgO、氧化铝Al2O3、氧化锌ZnO、氧化铁Fe2O3、氧化亚铁FeO、四氧化三铁Fe3O4、氧化铜CuO、氧化汞HgO、七氧化二锰Mn2O7 2.非金属氧化物 水H2O,过氧化氢H2O2、一氧化碳CO、二氧化碳CO2、一氧化氮NO、五氧化二氮N2O5、二氧化硅SiO2、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3 (2)按照性质分为 碱性氧化物 酸性氧化物 不成盐氧化物 两性氧化物 过氧化物 1.碱性氧化物 大部分的金属氧化物为碱性氧化物,但有特例:过氧化钠Na2O2为过氧化物、氧化铝Al2O3为两性氧化物、七氧化二锰Mn2O7为酸性氧化物、四氧化三铁Fe3O4、 碱性氧化物有:氧化钠Na2O、氧化钙CaO、氧化镁MgO、氧化锌ZnO、氧化铁Fe2O3、氧化亚铁FeO、氧化铜CuO、氧化汞HgO、 碱性氧化物一定为金属氧化物,金属氧化物不一定为碱性氧化物 2.酸性氧化物 大部分的非金属氧化物为,但有特例:水H2O,一氧化碳CO、一氧化氮NO不是酸性氧化物,七氧化二锰Mn2O7虽然为金属氧化物但属于酸性氧化物、 非金属氧化物不一定为酸性氧化物 3.不成盐氧化物:一氧化碳CO、一氧化氮NO 4.两性氧化物:氧化铝Al2O3 5.过氧化物:过氧化氢H2O2、过氧化钠Na2O2 四、酸 中学常见的酸: 盐酸HCl、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、磷酸H3PO4、次氯酸HClO、氯酸HClO3、高氯酸HClO4、亚硫酸H2SO3、硅酸H2SiO3、氢硫酸H2S、氢碘酸HI、氢溴酸HBr、氢氟酸HF、乙酸CH3COOH (1)依据组成分为含氧酸和无氧酸 1.含氧酸 硫酸H2SO4、硝酸HNO3、碳酸H2CO3、磷酸H3PO4、次氯酸HClO、氯酸HClO3、高氯酸HClO4、亚硫酸H2SO3、硅酸H2SiO3、乙酸CH3COOH 2.无氧酸
地区等级划分
4.2 地区等级划分 4.2.1、4.2.2 我国大型输气管道工程建设始于20世纪50年代。管道的安全保证基本上是沿用前苏联大型管线设计模式,埋地管道与居民点、工矿企业和独立建构筑物之间保持一定的安全距离。后来,根据我国情况制定了《埋地输气干线至各类建构筑物最小安全距离、防火距离》,但在执行过程中,遇到很多矛盾,有些问题,难以解决。20世纪70年代中期参照美国国家标准ASME B31.8,按不同的地区等级采用不同的设计系数,做出相应的管道设计。当时,地区等级不是按居民密度指数来划分,而是以建构筑物的安全防火类别为基础,相应地划分出四类地区等级,设计系数与美国国家标准ASME B31.8的规定一致,经实践,尚属可行。本标准在分析国外标准和总结国内经验的基础上,规定采用控制管道自身的安全性作为输气管道的设计原则。现分述如下: 第一,管道安全保证的两种指导思想。在输气管道建设中的安全保证有两种指导思想:一是控制管道自身的安全性,如美国国家标准ASMEB31.8。它的原则是严格控制管道及其构件的强度和严密性,并贯穿到从管道设计、设备材料选用、施工、生产、维护到更新改造的全过程。用控制管道的强度来确保管线系统的安全,从而对周围建构筑物提供安全保证。目前欧美各国多采用这种设防原则。二是控制安全距离,如前苏联“大型管线”设计标准。它虽对管道系统强度有一定的要求,但主要是控制管道与周围建构筑物的距离,以此对周围建构筑物提供安全保证。 四川地区30多年来输气管道设计、建设的实践表明,由于我国人口众多,地面建筑物稠密,按安全距离进行管道设计建设,不仅选线难度大,而且即使保证了安全距离未必就能保证周围建构筑物和居民的安全。例如,四川付纳输气管线(φ720×8)于1979年11月25日发生爆破,爆破时管道压力为2MPa,距管道150―200m远的农舍因室内余火未尽,引爆着火,烧毁民房8间,烧死牛1只、猪5头。1980年付纳线整改后,重新试压至5MPa时,管子爆破,管沟中 400mm×400mm×l000mm条石飞出100余米。又如,1965年4月美国路易斯安纳州发生一起美国有史以来最严重的输气管道爆破事故,当场炸死17人,钢管爆裂8m,炸出一条长8m、宽6m、深3m的大坑,把半吨多重的5块钢板炸到100余米远的地方。 第二,加强管道自身安全是对管道周围建筑物安全的重要保证。对于任何地区的管道仅就承受内压而言,应是安全可靠的。如果存在有可能造成管道损伤的不安全因素,就需采取一定的措施以保证管道的安全。欧美国家输气管道设计采取的主要的安全措施,是随着公共活动的增加而降低管道应力水平,即增加管道壁厚,以强度确保管道自身的安全,从而对管道周围建筑物提供安全保证。这种“公共活动”的定量方法就是确定地区等级,并使管道设计与相应的设计系数相结合。美国OPSR统计资料表明,处在三、四级地区的商业区、工业区、住宅区的管道外力事故是很低的。在这些地区主要采取降低管道应力的方法增加安全度。按不同的地区等级,采用不同的设计系数(F)来保证管道周围建构筑物的安全。显然这种做法比采取安全距离适应性强,线路选择比较灵活,也较经济合理。 第三,强度设计系数(F)。管道安全性的判断是许用应力值,使用条件不同其值亦异。即使在同样条件下,根据各国国情,其值亦有所不同。美国国家标准ASME B31.8按管道使用条件对许用应力值有详细的规定,该标准1992年以前规定的 许用应力值在0.4σ s ~0.72σ s 之间。其最大许用应力值(0.72σ s )与其他用途
人教版高中化学必修一物质的分类教案
必修《化学1》第二章化学物质及其变化第一节物质的分类 初中化学主要根据物质的组成介绍了物质的分类,如将元素分为金属元素和非金属元素,将化合物分为氧化物、酸、碱、盐等。在初中化学学习基础上,高中化学介绍了物质的简单分类法——树状分类法和交叉分类法,分类的标准侧重于根据物质的组成和性质,这样有利于学生认识化学物质及其性质,帮助学生树立分类思想,进一步形成分类观。 一、初高中衔接教学中的知识断点 初中化学中,有金属氧化物和非金属氧化物的概念及其跟酸或碱反应的性质,在本节有关氧化物的分类和以后有关元素及其化合物的教学中,需要酸性氧化物、碱性氧化物和两性氧化物等概念,对此,初高中教材均未涉及,需要补充。 关于几种常见的酸及其分类,初中只要求几种常见的酸,知道是强酸还是弱酸,不要求从电离的角度去认识酸,也不要求从离子的角度去认识酸的通性。而高中则要求从电离的角度去认识酸,从电离程度去理解强酸和弱酸,从H+去感受非氧化性酸,从硝酸、浓硫酸去感受氧化性酸。为此,教学中应补充酸的其它分类,如含氧酸和无氧酸、一元酸、二元酸和多元酸、强酸和弱酸、氧化性酸和氧化性酸等、应该让学生知道盐酸>醋酸>碳酸。 关于碱,初中只要求几种常见的强碱,如NaOH、KOH、Ca(OH)2等,不涉及弱碱,但简单介绍NH4+的检验。 关于盐,初中也只简单介绍了几种日常生活中常见的,可根据酸跟碱是否完全被中和分类但不作要求,没有正盐、酸式盐的概念,学生虽然初步认识了盐的组成,但是对盐的性质知之甚少。而高中则要求能根据物质的组成和性质对盐进行分类,从物质的组成认识盐可分为正盐、酸式盐、碱式盐和复盐,从物质的溶解性认识盐可分为可溶性盐和不溶性盐,在盐类的水解中,还可以从盐所对应的酸、碱的电离能力来分类等。学生很清楚盐分为可溶性盐和不溶性盐的依据,但对于哪些盐可溶、哪些盐不溶可就迷糊了。 在初中已学溶液、浊液的基础上,高中介绍了分散系及其分类,胶体及其性质。在分散系的认识基础上,高中要求重新认识溶液,了解溶液的组成。微粒大小是分散系分类的依据,也是影响性质的一个因素,微粒大小是这部分教学内容的初高中知识的衔接点。 二、初高中衔接教学中知识断点的突破 1.关于氧化物分类的教学 建议在课本P25实践活动1中,设计下列问题,实行渗透性衔接教学。 (1)带领学生回忆CO2和CaO的化学性质,并写出相应反应的化学方程式。 (2)从CO2和CaO分别与酸或碱的反应不同,引导学生分析得出酸性氧化物 和碱性氧化物的定义,并整合归纳酸性氧化物和碱性氧化物的通性, (3) SO2是酸性氧化物,请写出SO2与NaOH溶液反应的化学方程式。
九年级化学物质的组成结构和分类
中考化学专题练习:《物质的组成与分类》 【真题热身】 1.(2011.重庆)下列物质属于纯净物的是 ( ) A.寒冷的干冰 B.清澈的泉水C.清新的空气 D.坚硬的大理石2.(2011.衡阳)下列各种“水”中属于纯净物的是 ( ) A.蒸馏水 B.自来水C.海水 D.矿泉水 3.(2011.龙东)关于水的组成叙述正确的是 ( ) A.水是由氢分子和氧分子构成的 B.水是由氢气和氧气组成的 C.水分子是由一个氢分子和一个氧分子构成的 D.水是由氢元素和氧元素组成的4.(2011.永州)某井水中含有钙离子、镁离子和碳酸氢根离子等,该井水属于 ( ) A.纯净物 B.氧化物C.化合物 D.混合物 5.(2011.攀枝花)下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是( ) A.氯气(Cl2) B.氧化氯(ClO2) C.臭氧(O3) D.次氯酸钙[Ca(ClO)2] 6.(2011.泰安)掌握物质的分类是学好化学的基础,指出下列物质中属于碱的是 ( ) A.NaCl B.KOH C.MgO D.Cu 7.(2011.广州)下列物质中属于盐的是 ( ) A.NaOH B.Na2O C.Na2SO4D.Na 8.(2011.鸡西)“黑火药”是我国古代四大发明之一,它由硝酸钾、硫黄、木炭组成。“黑火药“属于 ( ) A.纯净物 B.化合物C.单质D.混合物 9.(2011.南通)从物质分类角度看,下列说法错误的是( ) A.石油属于混合物 B.氮气属于单质 C.甲烷属于化合物 D.干冰属于有机物10.(2011.赤峰)分别向两杯蒸馏水中加入冰块和蔗糖,得到冰水和糖水,从化学组成上分析,它们分别属于( ) A.单质和化合物 B.化合物和化合物 C.化合物和混合物 D.混合物和混合物11.(2011.德阳)当前,在食品生产经营中违法添加非食用物质和滥用食品添加剂已成为影响中国食品安全的突出问题。如一些不法生猪饲养户为使商品猪多长瘦肉,在饲料中非法添加“瘦肉精”(化学式为Cl2H18Cl2N2O).对消费者身体造成了极大危害。下列有关说法中
人教版化学必修1第二章第一节《物质的分类》【第一课时】说课稿
物质的分类(第1课时)说课 广西柳州铁一中学唐震 一、教材分析 本节教学内容位于新课标人教版高中化学必修1第二章《化学物质及其变化》第一节《物质的分类》。如果说第一章是从化学研究手段、化学实验方面展开化学的话,那么,本章则是从化 二、学情分析 教学对象是刚上高一的学生,处于初高中过渡时期,生活经验和知识基础还很少。在初中化学的学习中,学生只是简单掌握了一些化学物质和化学反应。其实,初中阶段纯净物、混合物及酸、碱、盐等的学习,就是物质分类方法的具体应用。但在思维上,学生正从直觉型经验思维向抽象型思维过渡,学生还没有把分类形成一种方法,没有形成化学学习的思想。本部分教学内容正好对初中化学中学习过的化学物质及反应进行总结和归纳,并进行适当的拓展和提高,帮助学生更好地认识化学物质,进而掌握分类方法,形成分类观。 三、教学目标及重难点的确定: 1.教学目标(三维目标的有机整合): 1.知识与技能 能根据物质的组成和性质对物质进行分类,知道分类的多样性,知道交叉分类法和树状分类法。 2.过程与方法 从日常生活中学生所遇见的一些常见的分类事例入手,通过合作学习的方式,将所学过的化学知识从自己熟悉的角度进行分类,将不同的知识通过某种关系联系起来,从而加深对知识的理解与迁移。并进一步通过探究活动,学习与他人合作交流,共同研究、探讨科学问题的方法。 3.情感态度与价值观 初步建立物质分类的思想,体会掌握科学方法能够有效提高学习效率和效果,体验活动探究的喜悦,感受化学世界的奇妙与和谐,增强学习化学、探究物质变化奥秘的兴趣。 2.教学重点难点: 本部分教学,知识性内容较为简单,故重难点落在了为学生建立起分类的思想上。 知识、能力、思想是体系的三个要素。常规的教学中我们往往重视知识、能力的培养,而忽视思想的培养。思想是的灵魂,分类思想是化 四、教学过程与方法: 教学主线
高中化学物质的分类及转化试题经典(1)
高中化学物质的分类及转化试题经典(1) 一、高中化学物质的分类及转化 1.X、Y、Z、W各代表一种物质,若X+Y=Z+W,则X和Y的反应不可能是( ) A.盐和盐的反应B.碱性氧化物和水的反应 C.酸与碱的反应D.酸性氧化物和碱的反应 【答案】B 【解析】 【详解】 A. 盐和盐反应能生成两种新盐,故A正确; B. 碱性氧化物和水的反应生成相应的碱,只生成一种物质,故B错误; C. 酸和碱反应生成盐和水,故C正确; D. 碱和酸性氧化物反应生成盐和水,故D正确; 故选:B. 【点睛】 根据题干提供的信息可以看出此反应为两种物质反应生成两种物质的反应,可以从具体的反应进行完成. 2.在给定条件下,下列选项所示的物质间转化均能实现的是() A.Fe(s) Fe2O3FeCl3(aq) B.CuO Cu(NO3)2(aq) Cu(NO3)2(s) C.SiO2(s) H2SiO3(s) Na2SiO3(aq) D.N2(g) NH3(g) NO(g) 【答案】D 【解析】 【分析】 【详解】 A.铁与水蒸汽反应生成四氧化三铁,故A不选; B.Cu(NO3)2(aq)加热要水解,产生氢氧化铜和硝酸,硝酸易挥发,水解平衡右移,得不到Cu(NO3)2(s),故B不选; C.二氧化硅不溶于水也不与水反应,故C不选; D.氮气与氢气合成氨气,氨气催化氧化生成NO,故D选; 故选D。 【点睛】 本题综合考查元素化合物知识,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,易错点C,二氧化硅不溶于水也不与水反应。 3.下列各项操作中不发生先沉淀后溶解现象的是()
①向饱和碳酸钠溶液中通入过量CO 2②向Fe(OH)3胶体中逐滴滴入过量的H 2SO 4 ③向Ba(NO 3)2溶液中通入过量SO 2④向石灰水中通入过量CO 2 ⑤向硅酸钠溶液中滴入过量的盐酸. A .①②③ B .①②⑤ C .①②③⑤ D .①③⑤ 【答案】D 【解析】 【分析】 【详解】 ①中发生的反应是Na 2CO 3+CO 2+H 2O=2NaHCO 3,NaHCO 3比Na 2CO 3溶解度小但质量大,且反应中中消耗H 2O ,所以有沉淀析出且不溶解,符合;②向Fe(OH)3胶体中加入H 2SO 4首先发生胶体的聚沉,出现Fe(OH)3沉淀,H 2SO 4过量,Fe(OH)3与H 2SO 4反应而溶解,不符合;③硝酸钡溶液中通入二氧化硫,二氧化硫溶于水生成亚硫酸,酸性溶液中硝酸根离子具有强氧化性,能氧化亚硫酸为硫酸,溶液中生成硫酸钡沉淀,现象是只生成沉淀,③符合;④向澄清石灰水中通入过量的CO 2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,反应现象是先沉淀后溶解,不符合;⑤向硅酸钠溶液中滴入过量的盐酸,发生反应Na 2SiO 3+2HCl=H 2SiO 3↓+2NaCl ,只生成白色沉淀,符合;答案选D 。 【点睛】 本题考查常见物质的的化学反应与现象。向溶液中加入某物质,先出现沉淀后沉淀溶解的总结如下: (1)向澄清石灰水中通入CO 2(SO 2)至过量。 (2)向Fe(OH)3胶体中加入硫酸至过量 (3)向可溶性铝盐中加入NaOH 溶液至过量 (4)向偏铝酸盐中加入盐酸至过量 4.下列说法正确的是( ) A .升高温度能提高活化分子的比例,从而加快反应速率 B .胶体和溶液的本质区别是有无丁达尔效应 C .将3FeCl 饱和溶液滴入NaOH 溶液中,可获得3Fe(OH)胶体 D .2CO 与2SiO 都属于酸性氧化物,都能与水反应生成相应的酸 【答案】A 【解析】 【分析】 【详解】 A .升高温度单位体积内活化分子总数增大,活化分子百分含量增大,发生有效碰撞的几率增大,反应速率加快,故A 正确; B .胶体和溶液的本质区别是分散质粒子的直径大小不同,胶体能产生丁达尔效应,溶液不能,可用丁达尔效应区分二者,但丁达尔效应不是本质区别,故B 错误; C .将3FeCl 饱和溶液滴入NaOH 溶液中,获得3Fe(OH)沉淀,制备3Fe(OH)胶体应将饱和
高中化学:物质的组成、性质和分类知识点
高中化学:物质的组成、性质和分类知识点 考点1 物质的组成 1.元素——宏观概念,说明物质的宏观组成。 元素是质子数相同的一类原子的统称。质子数相同的微粒不一定是同一种元素,因为微粒的含义要比原子广泛。 2.分子、原子、离子——微观概念,说明物质的微观构成。 (1)分子是保持物质化学性质的一种微粒。(单原子分子、双原子分子、多原子分子) (2)原子是化学变化中的最小微粒。(不是构成物质的最小微粒) (3)离子是带电的原子或原子团。(基:中性原子团) 3.核素——具有一定数目的质子和一定数目的中子的一种原子 同位素——具有相同质子数和不同中子数的原子互称为同位素 同素异形体——同种元素形成的结构不同的单质 特别提醒: 1.离子与基团: 2.同位素与同素异形体: [知识规律] 物质到底是由分子、原子还是离子构成?这与物质所属的晶体类型有关。如金刚石(C)、晶体Si都属原子晶体,其晶体中只有原子;NaCl、KClO3属离子晶体,其晶体中只有阴阳离子;单质S、P4属分子晶体,它们是由原子形成分子,进而构成晶体的。具体地: (1)由分子构成的物质(分子晶体): ①非金属单质:如H2、X2、O2、O3、N2、P4、S、C60、稀有气体等 ②非金属氢化物:如HX、H2O、NH3、H2S等 ③酸酐:如SO2、CO2、SO3、P2O5、N2O5 等 ④酸类:如HClO4、HClO、H2SO4、H3PO4、H2SiO3等 ⑤有机物:如烃类、烃的衍生物、糖类、氨基酸等 ⑥其它:如NO、N2O4、Al2Cl6等 (2)由原子直接构成的物质(原子晶体):稀有气体、金刚石、晶体硅、二氧化硅、碳化硅、石墨(混合型晶体)等; (3)由阴阳离子构成的物质(离子晶体):绝大多数盐、强碱、低价金属氧化物。 (4)由阳离子和自由电子构成的物质(金属晶体):金属单质、合金
中国地域划分基本知识
中国地域划分、历史演变以及地域特征 1、目前中国地域划分 目前,东部地区包括的11个省级行政区没变。中部地区有8个省级行政区,分别是山西、吉林、黑龙江、安徽、江西、河南、湖北、湖南;西部地区包括的省级行政区共12个,分别是四川、重庆、贵州、云南、西藏、陕西、甘肃、青海、宁夏、新疆、广西、内蒙古; 现在全国区域划分为东部、中部、西部和东北。 东部包括:北京、天津、河北、上海、江苏、浙江、福建、山东、广东、海南 中部包括:山西、安徽、江西、河南、湖北、湖南 西部包括:内蒙古、广西、重庆、四川、贵州、云南、西藏、陕西、甘肃、青海、宁夏、新疆 2、历史演变 将我国划分为东部、中部、西部三个地区的时间始于1986年,由全国人大六届四次会议通过的“七五”计划正式公布。 东部地区包括北京、天津、河北、辽宁、上海、江苏、浙江、福建、山东、广东和海南等11个省(市);中部地区包括山西、内蒙古、吉林、黑龙江、安徽、江西、河南、湖北、湖南、广西等10个省(区);西部地区包括四川、贵州、云南、西藏、陕西、甘肃、青海、宁夏、新疆等9个省(区)。 1997年全国人大八届五次会议决定设立重庆市为直辖市,并划入西部地区后,西部地区所包括的省级行政区就由9个增加为10个省(区、市)。由于内蒙古和广西两个自治区人均国内生产总值的水平正好相当于上述西部10省(市、区)的平均状况,2000年国家制定的在西部大开发中享受优惠政策的范围又增加了内蒙古和广西。 3、我国东、中、西部地区是怎样划分的?以及各区域的特点。 我国大陆区域经济的产生,应该说是依据其经济发展水平与地理位置相结合长期演变而形成的,我国大陆区域整体上可划分为三大经济地区(地带)。三大
2020年化学物质之分类观
专题讲座 化学物质之分类观 ——物质的分类方法和分类依据复习目标: 考纲要求要求层次考点细化 (1)从组成上对物质进行分类,如: 混合物和纯净物、单质和化合物、金属和非金属等 (2)根据物质组成和性质理解酸、碱、盐、氧化物的分类及其相互联系Ⅱ Ⅱ 1.根据物质的分类方法,掌握物质的类别的 判断。 2.根据物质的类别,初步学会物质性质推测 的基本方法。 【引言】分类的思想是中学化学中的一种基本的、也是最重要的思想方法。它可以帮助我们整体把握学科知识体系、理解学科基本概念和系统掌握化学各板块知识,所以它在中学化学的学习中有着极其重要的作用。 【讲解】我们必须弄明白:为什么要分类?如何来分类? (1)化学物质有很多,在研究中,我们总是利用同类物质具有“相似性质”,来推测物质的性质,然后有目的地验证这些性质,最终认识物质的性质。简单地说,给物质分类就是归纳物质的共性,为推测“陌生物质”性质服务。 (2)分类的依据: 根据物质之间的共同点 ...和差异性,把研究的对象区分为不同种类的逻辑方法。 一般来说,凡是归为同一类的对象,它们必然在质上有共性,必然有质的内在联系,异类必有质的差异性。即同类物质具有相似点,这些“相似点”包括: 物质的组成、物质的结构、物质的性质、物质的其他特征等。 (3)分类方法:树状分类法(可以理解为:系统中的“包含与被包含”的关系) 交叉分类法 【活动一】下列物质:金属铁、金属锌、木炭、CuO、CaCO3、H2SO4、NaOH、Ba(O H)2、NaCl、CuSO4。有人根据不同的依据进行了如下分类,请指出分类的依据和物质类别。 分类依据分类类别名称 类别一:金属铁、金属锌、木炭 类别二:CuO、CaCO3、H2SO4、NaOH、 Ba(OH)2、NaCl、CuSO4 类别一:SO2、SO3、N2O5 类别二:CuO、Fe2O3、Na2O 类别三:Al2O3、ZnO 类别四:NO、CO 类别一:稀H2SO4、NaCl(aq) 类别二:Fe(OH)3胶体、鸡蛋白液、淀粉液 类别三:Cu(OH)2浊液 类别一:NH3、CO2、NO、Cl2O7、CH3CH2OH
高中化学--物质的分类
物质的分类【结构框图】
【知识精讲】 一、物质的分类:分类是学习和研究化学物质及其变化的一种常用的科学方法。分类并没有唯一性,它会根据分类的标准不同而不同。一般常用交叉分类法和树状分类法。 【交叉分类法】分类角度多样,物质类别间有相交叉部分。 【交叉分类法举例】 【树状分类法定义】对同类事物进行再分类的一种方法。 【树状分类法分类原则】同一层次的物质类别间一般是相互独立,没有交叉的。 【分类一般步骤】确定分类标准选择分类方法得出正确的分类。 【分类原则】行之有效,简单易行。 【分类注意】 1、非金属氧化物不一定是酸性氧化物(NO、CO、NO 2、N2O4、H2O),酸性氧化物也不一定是非金属氧 化物(Mn2O7); 2、酸性氧化物一定为酸酐;酸酐不一定为酸性氧化物(乙酸酐(CH3CO)2O)。 3、金属氧化物不一定是碱性氧化物(Al2O3,Mn2O7),但碱性氧化物一定是金属氧化物。 【典型例题】 1、分类是学习和研究化学的一种重要方法,下列分类合理的是() A. K2CO3和K2O都属于盐 B.H2SO4和HNO3都属于酸 C.KOH和Na2CO3都属于碱 D.Na2O和Na2SiO3都属于氧化物 【答案】B 【解析】A前者属于盐,后者属于金属氧化物,C前者属于碱,后者属于盐,D前者属于氧化物后者是盐,只有B是正确的。
2、下列关于氧化物的叙述正确的是() A.酸性氧化物都是非金属氧化物 B.非金属氧化物都是酸性氧化物 C.碱性氧化物肯定是金属氧化物 D.金属氧化物肯定是碱性氧化物 【答案】C 【解析】本题把氧化物的两种分类方法放在一起,考查对氧化物概念理解的准确性。 氧化物是由氧元素和其它元素组成,它只含有两种元素。氧化物分类有: 按元素组成分为金属氧化物和非金属氧化物。 也可按性质分为酸性氧化物,碱性氧化物,两性氧化物,不成盐氧化物等。 A错误:“酸性氧化物都是非金属氧化物”,说法不对。如有些变价金属的高价氧化物,如等是酸性氧化物。 B错误:“非金属氧化物都是酸性氧化物”,说法也不对。如NO、CO、H2O、H2O2等非金属氧化物,就不是酸性氧化物。 C正确:“碱性氧化物肯定是金属氧化物”,碱性氧化物肯定是金属氧化物,但金属氧化物不一定全是碱性氧化物。所以C是正确的。 D错误:“金属氧化物肯定是碱性氧化物”,说法也不对。如:在金属氧化物中,有碱性氧化物(CaO)、酸性氧化物()、两性氧化物()、过氧化物()等,这些变价金属的高价的氧化物、两性氧化物,过氧化物都不属于碱性氧化物。 【错题门诊】 1、下列判断正确的是 A. 酸酐一定是氧化物 B. 碱性氧化物一定是金属氧化物 C. 离子化合物只能在熔化状态下能导电 D. 共价化合物一定是非电解质 试题答案:B
2010高考二轮复习化学教学案:专题一《物质的组成、性质和分类 化学用语》
《专题一物质的组成、性质和分类化学用语》〉 【专题要点】 物质的组成、性质和分类、化学用语是化学最基础的主干知识,是对物质及其变化的本质特征的反映。它们涉及的化学概念、物质的分类方法和它们相互转化的方式,是中学化学最基本的知识,也是学生从化学视觉观察和思考问题的必备知识,同时也是高考的重点内容。复习本考点是应深刻理解化学概念的内涵和外延,掌握不同概念间的区别和联系,掌握物质的分类方法及物质间相互转化的方式和转化条件;要理解各个化学用语的的实际含义,掌握反应的条件与本质,正确、科学、规范的进行运用。本考点在高考中的题型主要以选择题为主,常常结合元素化合物来进行考查。从09年和08年高考考题来看高考题除了直接考查基本概念外,还考查以物质组成和分类的概念为出发点,以反映高新科技和人们普遍关注的社会问题为切入点,逐步向环保、高科技、生产等方面渗透发展。除此之外我们还可以看出来元素、物质的组成与分类、化学用语,以成为高考的一个热点,而且融入其他专题进行考查。 【考纲要求】 1.理解分子、原子、离子、元素等概念的涵义,初步了解原子团的定义。 2.理解物理变化与化学变化的区别和联系 3.理解混合物和纯净物、单质和化合物、金属和非金属的概念 4.了解同素异形体的概念,注意其与同位素、同系物、同分异构体等的区别。 5.理解酸、碱、盐、氧化物的概念及其相互联系。 6. 熟记并正确书写常见元素的名称、符号、离子符号 7. 熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),或根据化学式判断化合价。 8. 了解原子结构示意图、分子式、结构式和结构简式的表示方法 9. 掌握溶液、悬浊液、乳浊液、胶体的概念,区别及鉴别它们的方法; 10.掌握胶体的本质特征及性质; 【教法指引】 复习此专题时要做到―准确‖、―系统‖、―灵活‖,可以从三点入手: 1.以高考的热点、考点、难点为依据,合理设置复习内容和练习题,熟练掌握解题思路、注 重方法、技巧,不求面面俱到,但求在某些考点的深度和广度的挖掘上有所突破 2.加强区别相似概念的异同,理顺不同概念间的联系,进而形成连贯的知识系统。
化学 说课稿:物质的分类
《物质的分类》说课稿 各位评委老师上午好,我是化学....号, .....,我今天说课的题目是《物质的分类》。 (板书:课题、作者),下面我将从教材、教法和学法、教学过程、板书设计四个方面来对本课进行说明。 一、教材分析 (一)教材内容的地位和作用 《物质的分类》是人教版高一年级第一册第二章中的第一节内容,如果说第一章是从化学科学研究手段、化学实验方面展开化学科学的话,那么,本章则是从化学学科内容方面展开化学科学,是连接初中化学与高中化学的纽带和桥梁,对于发展学生的科学素养,引导学生有效地进行高中阶段的化学学习,具有承前启后的作用。对大量繁杂的事物进行合理的分类是一种科学、方便的工作方法,它在学习和研究化学当中有不可替代的作用。本章的基本线索就是对化学物质及其变化的分类。因此,本章在全书中占有特殊的地位,具有重要的功能,是整个高中化学的教学重点之一。 结合单元要求和本节课特点,依据新课标的要求,我将本课的教学目标确定为以下三维目标: 1.知识和能力目标 能根据物质的组成和性质对物质进行分类,知道分类的多样性,知道交叉分类法和树状分类法。 2.过程与方法 从日常生活中学生所遇见的一些常见的分类事例入手,采用合作学习的方式,让学生将所学过的化学知识从自己熟悉的角度进行分类,将不同的知识通过某种关系联系起来,从而加深对知识的理解与迁移。并进一步通过探究活动,学习与他人合作交流,共同研究、探讨科学问题的方法。 3.情感态度与价值观 初步建立物质分类的思想,体会掌握科学方法能够有效提高学习效率和效果,体验活动探究的喜悦,感受化学世界的奇妙与和谐,增强学习化学、探究物质变化的奥秘的兴趣。 (二)学情分析 教学对象是刚上高一的学生,处于初高中过渡时期,生活经验和知识基础还很少。在初中化学的学习中,学生只是简单掌握了一些化学物质和化学反应。其实,初中阶段纯净物、混合物及酸、碱、盐等的学习,就是物质分类方法的具体应用.但在思维上,学生正从直觉型经验思维向抽象型思维过渡,学生还没有把分类形成一种方法,没有形成化学学习的思想。本部分教学内容正好对初中化学中学习过的化学物质及反应进行总结和归纳,并进行适当的拓展和提高,帮助学生更好地认识化学物质,进而掌握分类方法,形成分类观 (三)教学重点、难点 本课的重点是:帮助学生形成物质分类思想上。 由于学生的生活经验和基础知识还很少的难点确定为:在掌握交叉分类和树状分类的基础上,学会找标准。 二、教法和学法 科学合理的教学方法能使教学效果事半功倍,达到教与学的和谐完美统一,基于此,我采用的教学法是教授法,点拨法,讲授法教师可以系统的传授知识,
高中化学物质的分类汇总
高中化学物质的分类汇总 高中化学物质的分类知识点总结 1、物质的组成、性质和分类: (一)掌握基本概念 1. 分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒。 (2)按组成分子的原子个数可分为: 单原子分子:Ne 、C、 He 、Kr…… 双原子分子:H2 、O2、HCl、No…… 多原子分子:H2O、P4 、C6H12O6…… 2. 原子 原子是化学变化中的最小微粒,确切的说,化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子组成的。 3. 离子 离子是指带电荷的原子或原子团。 (1)离子可分为阳离子和阴离子 阳离子:Li+、Na+、H+、NH4+…… 阴离子:Cl-、O2-、OH-、SO4-…… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、CaSo4…… ②电解质溶液中:盐酸、氯化钠溶液中…… ③金属晶体中:钠、铁、钾、铜…… 4. 元素 元素是具有相同核电荷数的(即质子数)的同一类原子的总称。 (1)元素与物质、分子、原子的区别与联系;物质是由元素组成的(宏观看);物质是由原子、分子、或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)同素异形体。(3)各元素在地壳中质量分数各不相同,占前五位的是:O、Si、Al、
Fe、Ga。 5. 同位素 同位素指同一元素不同核素之间互称同位素,即具有相同质子数不同中子数的同一类原子互称为同位素。如氢(H)有三种同位素:11H、 21H、31H(氕、氘、氚)。 6. 核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素,可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但他们质子数与电子数相同。核外电子排布相同,因而他们的化学性质几乎相同。 7. 原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有以下几种类型:根(如SO42-、OH-、CH3COO-等)、官能团(有机物分子中能反应物质特殊性质的原子团,如-OH、 -NO2、-COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。 8. 基 化合物中具有特殊性质的一部分原子或原子团,或化合物分子中去掉某些原子或原子团后剩下的原子团。 (1)有机物的官能团是决定物质主要性质的基,如醇的羟基(-OH)和羧酸的羧基(-COOH)。 (2)甲烷(CH4)分子中去掉一个氢原子后剩余部分(·CH3)含有未成对的价电子,称为甲基或甲基游离基,也包括单原子的游离基(·Cl)。 基(羟基):电中性,不能独立存在,只能和其他基或原子团相结合。根(氢氧根):带负电,能独立存在于溶液或离子化合物中。 9. 物理性质和化学性质 物理性质 (1)概念:(宏观)物质不需要发生化学变化就能表现出的性质。(2)实质:(微观)物质的分子组成和结构没有发生变化时所呈现的性质。 (3)物理性质一般包括:颜色、状态、气味、味道、密度、熔点、沸点、溶解性、导电性、导热性、延展性等。 化学性质
高中化学知识点总结:物质的组成、性质和分类
高中化学知识点总结:物质的组成、性质和分类 (一)掌握基本概念 1.分子 分子是能够独立存在并保持物质化学性质的一种微粒。 (1)分子同原子、离子一样是构成物质的基本微粒. (2)按组成分子的原子个数可分为: 单原子分子如:He、Ne、Ar、Kr… 双原子分子如:O2、H2、HCl、NO… 多原子分子如:H2O、P4、C6H12O6… 2.原子 原子是化学变化中的最小微粒。确切地说,在化学反应中原子核不变,只有核外电子发生变化。 (1)原子是组成某些物质(如金刚石、晶体硅、二氧化硅等原子晶体)和分子的基本微粒。 (2)原子是由原子核(中子、质子)和核外电子构成的。 3.离子 离子是指带电荷的原子或原子团。 (1)离子可分为: 阳离子:Li+、Na+、H+、NH4+… 阴离子:Cl–、O2–、OH–、SO42–… (2)存在离子的物质: ①离子化合物中:NaCl、CaCl2、Na2SO4… ②电解质溶液中:盐酸、NaOH溶液… ③金属晶体中:钠、铁、钾、铜… 4.元素 元素是具有相同核电荷数(即质子数)的同—类原子的总称。 (1)元素与物质、分子、原子的区别与联系:物质是由元素组成的(宏观看);物质是由分子、原子或离子构成的(微观看)。 (2)某些元素可以形成不同的单质(性质、结构不同)—同素异形体。 (3)各种元素在地壳中的质量分数各不相同,占前五位的依次是:O、Si、Al、Fe、Ca。5.同位素 是指同一元素不同核素之间互称同位素,即具有相同质子数,不同中子数的同一类原子互称同位素。如H有三种同位素:11H、21H、31H(氕、氘、氚)。 6.核素 核素是具有特定质量数、原子序数和核能态,而且其寿命足以被观察的一类原子。 (1)同种元素、可以有若干种不同的核素—同位素。 (2)同一种元素的各种核素尽管中子数不同,但它们的质子数和电子数相同。核外电子排布相同,因而它们的化学性质几乎是相同的。 7.原子团 原子团是指多个原子结合成的集体,在许多反应中,原子团作为一个集体参加反应。原子团有几下几种类型:根(如SO42-、OHˉ、CH3COOˉ等)、官能团(有机物分子中能反映物质特殊性质的原子团,如—OH、—NO2、—COOH等)、游离基(又称自由基、具有不成价电子的原子团,如甲基游离基·CH3)。
中国各省份地区划分(整理)
北京(京)天津(津)上海(沪)重庆(渝)内蒙古自治区(内蒙古)维吾尔自治区(新)西藏自治区(藏)宁夏回族自治区(宁)广西壮族自治区(桂)香港特别行政区(港)澳门特别行政区(澳)黑龙江省(黑)吉林省(吉)辽宁省(辽)河北省(冀)山西省(晋)青海省(青)山东省(鲁)河南省(豫)江苏省(苏)安徽省(皖)浙江省(浙)福建省(闽)江西省(赣)湖南省(湘)湖北省(鄂)广东省(粤)台湾省(台)海南省(琼)甘肃省(甘或陇)陕西省(陕或秦)四川省(川或蜀)贵州省(贵或黔)云南省(云或滇)dian 华东:山东、江苏、江西、安徽、浙江、上海 华南:湖南、广东、广西、福建 华北:北京、天津、河北、内蒙、山西 西南:云南、贵州、四川、重庆、西藏 西北:陕西、甘肃、宁夏、新疆、青海 中国各省份简称的由来 四个直辖市 1、北京(京)北京有据可查的第一个名称为“蓟”(ji),是春秋战国时燕国的都城。辽金是将北京作为陪都,称为燕京。金灭辽后,迁都于此,
称中都。元代改称大都。明成祖朱棣从南京迁都于此,改称“北京”。名称一直沿用至今。1949 年设为直辖市。取全称中的“京”字作为简称。 2、天津(津)唐宋以前,天津称为直沽。金代形成集市称“直沽寨”。元代设津海镇,这是天津建城的开始。明永乐 2 年(1404 年)筑城设卫,始称天津卫,取“天子经过的渡口”之意。1949 年设为直辖市。取全称中的“津”字作为简称。 3、上海(沪)上海之称始于宋代,当时上海已成为我国的一个新兴贸易港口,那时的上海地区有十八大浦,其中一条叫上海浦,它的西岸设有上海镇。1292 年,上海改镇为县。这是上海这一名称的由来。1949 年,上海设为直辖市。古时,上海地区的渔民发明了一种竹编的捕鱼工具“扈”,当时还没有上海这一地名,因此,这一带被称为“沪渎”,故上海简称“沪”。春秋战国时上海是楚春申君黄歇封邑的一部分,故上海别称“申”。 4、重庆(渝)重庆古称“巴”。秦时称江州。隋称渝州。北宋称恭州。重庆之名始于1190 年,因南宋光宗赵敦先封恭王,后登帝位,遂将恭州升为重庆府,取“双重喜庆”之意。1997 年,重庆设为直辖市。隋时,嘉陵江称渝水,重庆因位于嘉陵江畔而置渝州,故重庆简称“渝”。 五个自治区 1、内蒙古自治区(内蒙古)(呼和浩特市) 蒙古原为部落名,始见于唐代记载。1206 年,成吉思汗统一蒙古各部,建立蒙古国。元灭后,蒙古族退居塞北。明清形成内、外蒙古之称。晚清以后,泛指大漠以南、长城以北、东起哲里木盟、西至套西厄鲁特所以盟旗为内蒙古。取全称中“内蒙古”三字作为简称。
初中化学常见物质的分类
一、初中化学常见物质的分类 1、单质:非惰性气体一般由两个原子组成: F2,O2,H2,Cl2 2、惰性气体:一般由一个原子组成:He,Ne,Ar,Kr,Xe 3、化合物:氢化物居多:H2S,HCl,H3P,HF,HBr,HI 二、初中化学常见物质的颜色 (一)、固体的颜色 1、红色固体:铜,氧化铁 2、绿色固体:碱式碳酸铜 3、蓝色固体:氢氧化铜,硫酸铜晶体 4、紫黑色固体:高锰酸钾 5、淡黄色固体:硫磺 6、无色固体:冰,干冰,金刚石 7、银白色固体:银,铁,镁,铝,汞等金属 8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭) 9、红褐色固体:氢氧化铁 10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜, 五氧化二磷,氧化镁 (二)、液体的颜色 11、无色液体:水,双氧水 12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液 13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液 14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液 15、紫红色溶液:高锰酸钾溶液 16、紫色溶液:石蕊溶液 (三)、气体的颜色 17、红棕色气体:二氧化氮 18、黄绿色气体:氯气 19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢等气体。 三、初中化学敞口置于空气中质量改变的 (一)质量增加的 1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸; 2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜; 3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙;(二)质量减少的 1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水; 2、由于风化而减少的:碳酸钠晶体。 四、初中化学物质的检验 (一)、气体的检验 1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.
