第十一章 教案52 实验数据的处理分析

学案52实验数据的处理分析
[考纲要求]能分析和处理实验数据,得出合理的结论。
热点1实验数据筛选与处理
实验所得的数据,可分为有用、有效数据,正确、合理数据,错误、无效数据,及无用、多余数据等。能从大量的实验数据中找出有用、有效、正确、合理的数据是实验数据分析处理题的一个重要能力考查点,也是近年来命题变化的一个重要方向。b5E2RGbCAP
解题策略
对实验数据筛选的一般方法和思路为“五看”:一看数据是否符
合测量仪器的精度特点,如用托盘天平测得的质量的精度为0.1g,若精度值超过了这个范围,说明所得数据是无效的;二看数据是否在误差允许范围内,若所得的数据明显超出误差允许范围,要舍去;三看反应是否完全,是否是过量反应物作用下所得的数据,只有完全反应时所得的数据,才能进行有效处理和应用;四看所得数据的测试环境是否一致,特别是气体体积数据,只有在温度、压强一致的情况下才能进行比较、运算;五看数据测量过程是否规范、合理,错误和违
反测量规则的数据需要舍去。p1EanqFDPw (2018·江苏,21B>B.对硝基甲苯是医药、染料等工
典例导悟1业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化
剂,通过甲苯的硝化反应制备。DXDiTa9E3d
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,
固体NaHSO4为催化剂(可循环使用>,在CCl4溶液中加入乙酸酐(有脱水作用>, 45℃反应1h。反应结束后,过滤,滤液分别用5%NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。RTCrpUDGiT
(1>上述实验中过滤的目的是__________________。
(2>滤液在分液漏斗中洗涤静置后,有机层处于________层(填“上”或“下”>;放液时,若发现液体流不下来,其可能原因除分
液漏斗活塞堵塞外,还有5PCzVD7HxA ________________________________________________________
________________。jLBHrnAILg
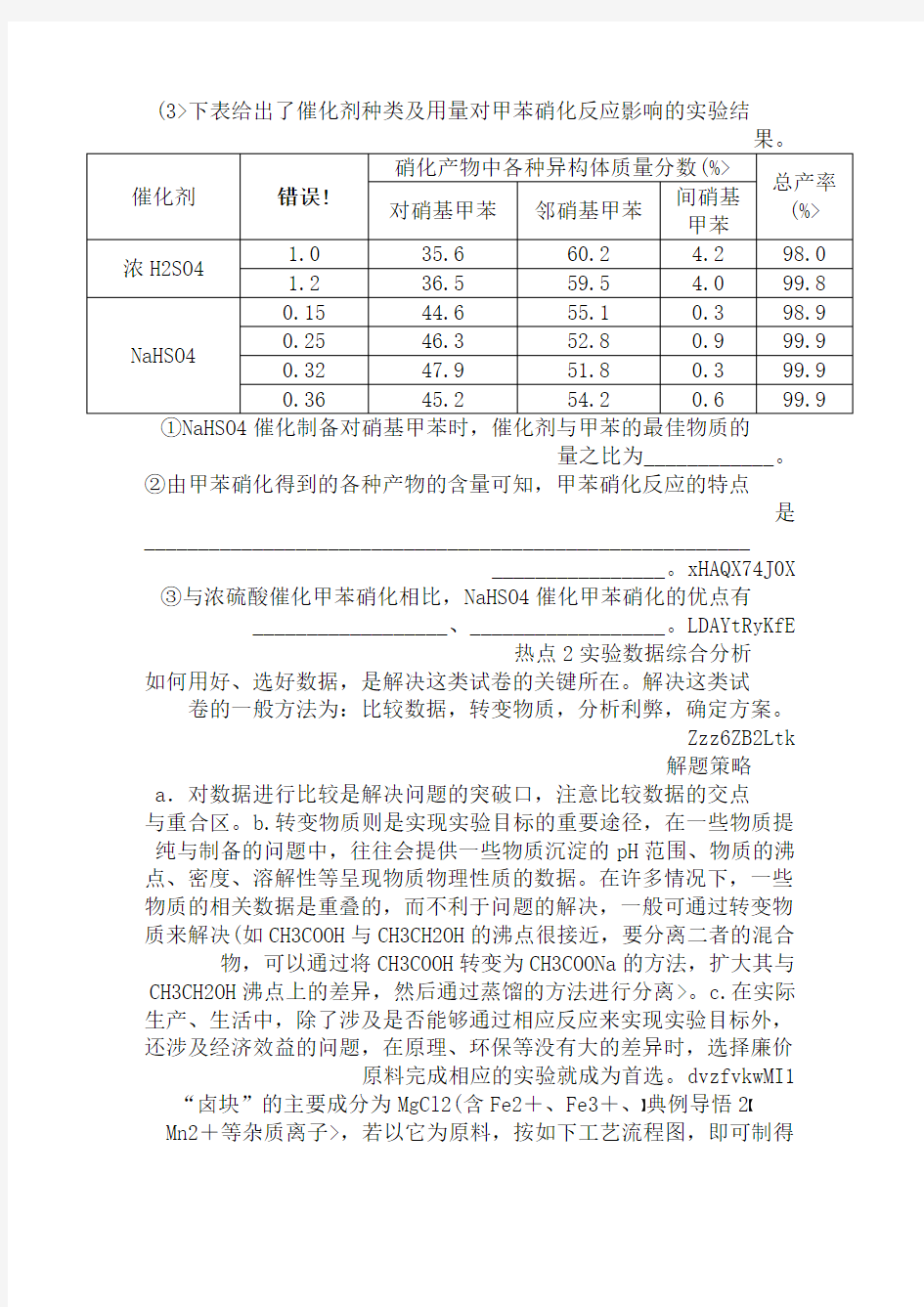
(3>下表给出了催化剂种类及用量对甲苯硝化反应影响的实验结
量之比为____________。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点
是________________________________________________________
________________。xHAQX74J0X ③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有
__________________、__________________。LDAYtRyKfE
热点2实验数据综合分析
如何用好、选好数据,是解决这类试卷的关键所在。解决这类试卷的一般方法为:比较数据,转变物质,分析利弊,确定方案。
Zzz6ZB2Ltk
解题策略a.对数据进行比较是解决问题的突破口,注意比较数据的交点
与重合区。b.转变物质则是实现实验目标的重要途径,在一些物质提纯与制备的问题中,往往会提供一些物质沉淀的pH范围、物质的沸点、密度、溶解性等呈现物质物理性质的数据。在许多情况下,一些物质的相关数据是重叠的,而不利于问题的解决,一般可通过转变物质来解决(如CH3COOH与CH3CH2OH的沸点很接近,要分离二者的混合物,可以通过将CH3COOH转变为CH3COONa的方法,扩大其与CH3CH2OH沸点上的差异,然后通过蒸馏的方法进行分离>。c.在实际生产、生活中,除了涉及是否能够通过相应反应来实现实验目标外,还涉及经济效益的问题,在原理、环保等没有大的差异时,选择廉价
原料完成相应的实验就成为首选。dvzfvkwMI1
典例导悟2“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、
Mn2+等杂质离子>,若以它为原料,按如下工艺流程图,即可制得
“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或pH值控制可参考下列附表确定。rqyn14ZNXI
表2
Ω注:Fe2
氧化成为Fe3+,生成Fe(OH>3沉淀而去除之。请填写以下空白:EmxvxOtOco
(1>在步骤②加入试剂X,最佳选择应是________,其作用是
____________________________。
(2>在步骤③加入的试剂Y应是__________________,之所以要控制pH=9.8,其目的是____________________________________________________________ ____________SixE2yXPq5
________________________________________________________ ________________。6ewMyirQFL
(3>在步骤⑤时发生的化学反应方程式是
________________________________________________________ ________________kavU42VRUs
________________________________________________________ ________________。y6v3ALoS89
热点3变量探究实验
典型的变量探究型实验,往往涉及有关影响化学反应速率、化学平衡移动规律等方面的内容。
解题策略
处理相关实验问题时,需要注意以下内容:一是要选择合适的化学反应,所选择的反应不能太灵敏,也不能太迟钝。二是反应物的浓度要适当,不能太大,而探索浓度变量时,浓度间的差别也不能太大。三是反应体系的温度,要有规律地设计不同的反应体系的温度,也要注意物质的相应性质,不能选择会引起反应发生变化的体系温度。四是对变量要进行适当的组合,组合的一般原则是“变一定多”,即保持其他变量不变,改变其中一个变量的值进行实验,测定数据,通过系列实验,找出变量对反应的影响。M2ub6vSTnP 典例导悟3控制变量法是化学实验的一种常用方法,下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点后一位>。分析以下数据,回答下列问题:
一规律进行研究的实验还有一组是____________________(填实验序号>。eUts8ZQVRd
(2>下列说法正确的是________。
A.t1<70B.m1<m2
C.m6=19.3D.t1>t4
(3>本实验还可以研究____________________对化学反应速率的影响。
(4>稀硫酸的物质的量浓度是________mol·L-1,实验6生成硫酸锌的质量m5=______________。
sQsAEJkW5T
1.(2009·广东,19>某实验小组利用如下装置(部分固定装置略>制备氮化钙(Ca3N2>,并探究其实验式。GMsIasNXkA
(1>按图连接好实验装置。检查装置的气密性,方法是
________________________________________________________
________________TIrRGchYzg ________________________________________________________
________________。7EqZcWLZNX
(2>反应过程中末端导管必须始终插入试管A的水中,目的是
________________________________________________________
________________lzq7IGf02E ________________________________________________________
________________。zvpgeqJ1hk (3>制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃
酒精灯,进行反应;③反应结束后,________________________________________________________
________________NrpoJac3v1
________________________________________________________
________________;1nowfTG4KI
④拆除装置,取出产物。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
________________________________________________________ ________________。fjnFLDa5Zo
2.(2009·安徽理综,28>Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。tfnNhnE6e5 [实验设计]控制p-CP的初始浓度相同,固定实验温度在298K或313K(其余实验条件见下表>,设计如下对比实验。HbmVN777sL
[数据处理]实验测得p-CP的浓度随时间变化的关系如上图。
(2>请根据上图实验①曲线,计算降解反应在50~150s内的反应
速率:
v(p-CP>=________mol·L-1·s-1。
[解释与结论] (3>实验①、②表明温度升高,降解反应速率增大。但温度过高
时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度
分析原因:V7l4jRB8Hs ________________________________________________________
________________。83lcPA59W9
(4>实验③得出的结论是:pH等于10时,
________________________________________________________
________________。mZkklkzaaP
[思考与交流] (5>实验时需在不同时间从反应器中取样,并使所取样品中的反
应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方
法:AVktR43bpw ________________________________________________________
________________ORjBnOwcEd ________________________________________________________
________________。2MiJTy0dTT
1.TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元
素组成,与氢气的相对分子质量之比为120。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。其主要过程为在足量氧气流中将4.80gTMB样品氧化(氮元素转化为N2>,再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热
装置等已略去,其他用品可自选>。gIiSpiue7A
(1>将所选用的仪器(可重复选用,C、D之间及D后的空栏不一
定表示只有一栏>连接顺序由上到下依次填入下表,并写出该仪器中
应加入的试剂的名称及作用。uEh0U1Yfmh
(2>
完全的>质量依次增加 3.60g、14.08g、0.14g,则TMB的分子式为__________________________。IAg9qLsgBX
2.某研究性学习小组的同学进行了如下的实验探究,将适量1.00mol·L-1CuSO4溶液和2.00mol·L-1NaOH溶液混合,过滤后得到一种浅绿色碱式盐沉淀A[aCu(OH>2·bCuSO4]。将9.08gA隔绝空气在1000℃以上加强热,得到了 5.76g红色固体B,同时得到xmol的混合气体;再将5.76gB溶于稀硫酸得到2.56g另一种红色固体C(已知铜的化合价有+1和+2>。WwghWvVhPE
(1>甲同学认为A中含有杂质Na+,作出此判断的理由是
________________________________________________________ ________________,asfpsfpi4k
验证此判断正确的方法是
________________________________________________________ ________________,ooeyYZTjj1
除去此杂质的方法是
________________________________________________________ ________________BkeGuInkxI
________________________________________________________ ________________。PgdO0sRlMo
(2>B与稀硫酸反应的离子方程式为
________________________________________________________ ________________3cdXwckm15
________________________________________________________ ________________。h8c52WOngM
(3>通过计算确定A的组成为
________________________________________________________ ________________。v4bdyGious
(4>x的取值范围:____________。
3.已知某固体混合物可能含有镁、铝、铁、硅、二氧化硅中的几种或全部,为确定其组成,某研究性学习小组的同学取17.1g固体混合物进行如下实验:J0bm4qMpJ9
(1>甲同学认为,由红褐色固体C知,混合物中一定存在
__________,由固体B知一定存在______________,但肯定不存在____________,其他物质是否存在无法确定。XVauA9grYP (2>乙同学认为,仅由上述信息,可以完全确定上述五种物质是
否存在,则乙同学确定甲同学推断外的其他物质的过程是
bR9C6TJscw ________________________________________________________
________________pN9LBDdtrd ________________________________________________________
________________DJ8T7nHuGT ________________________________________________________
________________。QF81D7bvUA
(3>反应③的离子方程式为
________________________________________________________
________________4B7a9QFw9h ________________________________________________________
________________,ix6iFA8xoX
反应④的化学方程式为
________________________________________________________
________________wt6qbkCyDE ________________________________________________________
________________。Kp5zH46zRk 4.某实验小组用0.50mol·L-1NaOH溶液和0.50mol·L-1硫
酸溶液反应,进行中和热的测定。Yl4HdOAA61
Ⅰ.配制0.50mol·L-1NaOH溶液。(1>若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固
体________g。
(2>从表中选择称量NaOH固体所需要的仪器是(填字
母>________。
(1>写出该反应的热化学方程式(中和热为57.3kJ·mol-1>:
________________________________________________________
________________。ch4PJx4BlI (2>取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表
所示。
的密度都是1g·cm-3,中和后生成溶液的比热容c=4.18J·g-1·℃-1。则中和热ΔH=__________(取小数点后一位>。
qd3YfhxCzo ③上述实验结果与57.3kJ·mol-1有偏差,产生偏差的原因可
能是(填字母>______。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温
度5.在0℃、1.01×105Pa时进行下列实验:甲、乙、丙三组实验
各取30.0mL同浓度的盐酸,加入同一种镁铝合金粉末产生气体,有
E836L11DO5
(2>合金中各成分的质量分数。
(3>在丙组实验之后,若剩余合金中的铝粉恰好完全溶解,还需
向容器中加入1.00mol·L-1的NaOH溶液________mL。(设剩余合金
与原合金成分相同>S42ehLvE3M
学案52 实验数据的处理分析
【热点探究区】
典例导悟
1.(1>回收NaHSO4 (2>下分液漏斗上口塞子未打开(3>①0.32②甲苯硝化主要得到
对硝基甲苯和邻硝基甲苯③在硝化产物中对硝基甲苯比例提高催化剂
用量少且能循环使用501nNvZFis 解读本题主要考察的是物质的性质和制备,同时考查了数据的处
理与分析能力,能够迅速在表中提取到有用信息,利用信息解决有关问题的能力。(1>NaHSO4在该反应中作为催化剂,因此反应后过滤的目的是为了回收NaHSO4。(2>该反应是以CCl4作为有机溶剂,CCl4的密度比水大,故有机层在下层;分液漏斗里的液体放不下来,除了分液漏斗堵塞,还有可能是分液漏斗上口活塞未打开。(3>①从题给数据分析,当催化剂与甲苯的比例为0.32时,总产率最高且对硝基甲苯的含量最高;②从题给数据可以看出,无论以何种比例反应,产物中的主要成分主要是对硝基甲苯和邻硝基甲苯;③用NaHSO4作催化剂的优点是在硝化物中对硝基甲苯的比例提高,同时催化剂用量少
且能循环使用。jW1viftGw9 2.(1>漂白液将Fe2+氧化成Fe3+(2>NaOH将除Mg2+以外的各种杂质金属离子都生成相应的氢氧化物沉淀,以便过滤除去
(3>MgCO3+H2O错误!Mg(OH>2↓+CO2↑xS0DOYWHLP
解读从表1可以看出,加入烧碱控制pH=9.8时即可除去Fe2+、Fe3+、Mn2+,此时Mg2+也会因生成部分Mg(OH>2而进入沉淀
中,但因卤块价格低,损失不大,这样做可以保证产品的纯度。为将Fe2+氧化成Fe3+,可采用漂白液或H2O2,从价格上看,前者比后
者便宜得多,故应选漂白液。LOZMkIqI0w
氯化镁制成氧化镁有两条路线:烧碱路线:MgCl2错误!Mg(OH>2错误!MgOZKZUQsUJed
纯碱路线:MgCl2错误!MgCO3错误!MgOdGY2mcoKtT 烧碱路线不可取,因为烧碱比纯碱的价格高,生成的中间产物
Mg(OH>2是胶状沉淀,会造成过滤困难。纯碱价格低,生成的中间产物MgCO3呈粗颗粒状,易过滤,它在
水中经一定时间加热后会有一部分水解,生成CO2。CO2的产生可使沉淀变得疏松,灼烧沉淀后可得到轻质MgO。rCYbSWRLIA 3.(1>温度实验3和实验4 (2>AC (3>硫酸的浓度和催化剂
(或压强> (4>2.49.9解读(1>实验1与实验2的条件只有温度不同,故可表明温度对
化学反应速率有影响,同样可知实验3与实验4的反应条件也是温度不同。(2>其他条件相同时,锌采用粉末状比采用颗粒状的反应速率快,故对比实验3、5的数据可知t1<70;因实验1、2采用锌的质量相同且全部溶解在稀硫酸中,故生成的硫酸锌等量,即m1=m2;由实验8、10的数据可知,在加入8.0gZn时,稀硫酸已经耗尽,故m6=19.3;实验5中加入锌的质量小于实验8的,随着反应的进行,硫酸浓度变小,反应速率变慢,故t1<t4。(3>本实验还可以研究硫酸的浓度、催化剂(或压强>等对反应速率的影响。(4>由稀硫酸耗尽
时产生硫酸锌的质量可求出50.0mL稀硫酸中含有n(H2SO4>≈0.12mol,故c(H2SO4>=2.4mol·L-1;实验6中稀硫酸未耗尽,故可由4.0gZn(全部转化为ZnSO4>求出m5=
4×161/65≈9.9。FyXjoFlMWh
【热点集训区】
高考集训1.(1>关闭活塞,微热反应管,试管A中有气泡冒出,停止加热。冷却后若末端导管中水柱上升且高度保持不变,说明装置气密性
良好TuWrUpPObX
(2>防止空气中的氧气通过末端导管进入实验装置,氧化单质
钙,生成氧化钙,引入杂质(3>熄灭酒精灯,待反应管冷却至室温,停止通入氮气,并关闭
活塞
(4>①2.80②x<3,产物中生成了CaO
解读(2>要保证整个装置不能混入其他气体;(3>一定要使玻璃
管冷却后再停止通入氮气流;(4>要确定x值必须求出钙和氮的原子
个数比,根据题目所给的数据可做如下计算①m(Ca>=(15.08-
14.90> g=0.28g,m(N>=(15.15-15.08> g=0.07g,则n(Ca>∶n(N>=错误!∶错误!=7∶5,则x=错误!;②若通入的N2中混有少量O2,则产物中就有可能混有了CaO,而Ca3N2中钙的质量分数为81.08%,CaO中钙的质量分数为71.43%,所以产物中混有了CaO会导致钙的质量分数减小,x的值偏小。7qWAq9jPqE
(3>过氧化氢在温度过高时迅速分解
(4>反应速率趋向于零(或该降解反应趋于停止>
(5>将所取样品迅速加入到一定量的NaOH溶液中,使pH约为
10(或将所取样品骤冷等其他合理答案均可>llVIWTNQFk 解读(1>实验①是参照实验,所以与实验①相比,实验②和③
只能改变一个条件,这样才能起到对比实验的目的。实验②是探究温度对反应速率的影响,则T=313K,pH=3,c(H2O2>=6.0mol·L-1,c(Fe2+>=0.30mol·L-1;实验③显然是探究pH的大小对反应速率的影响;(2>在50~150s内,Δc(p-CP>=0.8mol·L-1,则v(p-CP>=0.08mol·L-1·s-1;(3>温度过高时,H2O2分解,c(H2O2>浓度减小,导致反应速率减小;(4>从图中看出,pH=10时,c(p-CP>不变,即反应速率为零,说明碱性条件下,有机物p-CP 不能降解;(5>从第(4>题可以得出,在反应液中加入NaOH溶液,使
溶液的pH迅速增大,反应停止。yhUQsDgRT1
热点集训
解读(1>TMB氧化后得到CO2、H2O、N2,再利用吸收剂分别吸收H2O和CO2,以确定一定量的TMB中所含碳、氢原子数目。实验中必须确保碳元素全部转化为CO2,因此在用氧气氧化后再使用氧化铜作保障;为防止氧气产生时所带水蒸气的影响,要先用浓硫酸对氧气进行干燥。(2>因A中吸收剂只有固体,应选用无水CaCl2或P2O5吸收水,然后再用碱石灰吸收CO2,因此装置质量增加的 3.60g为水、14.08g为CO2、0.14g为吸收空气中的CO2、H2O。3.60gH2O中含0.4molH+、14.08gCO2中含0.32mol碳,由此可求出4.80gTMB中含有0.04molN,故C、H、N原子最简整数比为8∶10∶1,再结合其相对分子质量可求出分子式。MdUZYnKS8I
2.(1>过滤所得沉淀中含有水,水中溶解有Na+做焰色实验,观察到黄色火焰向漏斗中加蒸馏水至刚浸没沉淀,让水自然流下,重复此操作2~3次09T7t6eTno
(2>Cu2O+2H+===Cu+Cu2++H2O
(3>3Cu(OH>2·CuSO4或Cu4(OH>6SO4
(4>0.1 解读(1>过滤所得沉淀A是湿润的,水中会溶解有可溶性物质,因此会含有Na+杂质,可通过焰色反应实验验证Na+,除去Na +的方法是洗涤沉淀。e5TfZQIUB5 (2>红色固体B应该是Cu2O,Cu2O在酸性条件下发生反应生成单质铜,依据氧化还原反应理论知还应有硫酸铜生成。s1SovAcVQM (3>A的摩尔质量为(98a+160b>g·mol-1,B(Cu2O>的摩尔质量为144g·mol-1,假设有1molA,则由铜元素守恒知B的物质的量为0.5(a+b>mol,故有(98a+160b>∶[144×0.5(a+b>]=9.08∶5.76,即可得a∶b=3∶1,所以A为3Cu(OH>2·CuSO4或Cu4(OH>6SO4。GXRw1kFW5s (4>9.08gA的物质的量是0.02mol,由3Cu(OH>2·CuSO4错误! 2Cu2O+3H2O↑+SO3↑+O2↑知0.02mol3Cu(OH>2·CuSO4完全分解可得到0.06molH2O(g>、0.02molSO3、0.02molO2,三种气体共 高温 0.1mol,但因高温下SO3会分解,由2SO32SO2+O2知,SO3全部分解会使气体增加0.01mol,故x的取值范围为0.1 3.(1>铁铝镁 (2>由固体B、C质量知混合物中含有2.7gAl,5.6g铁;经分析,只含有SiO2或只含有Si都与题意不符,故混合物中硅、SiO2质量之和为8.8g,结合固体A的质量及Si~SiO2可求出原混合物中含硅 2.8g、SiO26g8PQN3NDYyP (3>Al3++3NH3·H2O===Al(OH>3↓+3NH错误! 4Fe(OH>2+2H2O+O2===4Fe(OH>3 解读由C的颜色知C是Fe(OH>3,则原混合物中含有0.1molFe,质量为5.6g;因镁、铁不溶于NaOH溶液,故原固体混合物与NaOH 溶液反应后剩余的固体可能是Mg、Fe,又因为Mg(OH>2是白色,故原固体混合物中没有镁。铝、硅、SiO2均溶于NaOH溶液,生成相应的可溶性盐溶液,加入足量盐酸后仍能得到沉淀,则该沉淀是硅酸,灼烧时得到SiO2,反应③得到的固体是Al(OH>3,灼烧得到Al2O3,由2Al~Al2O3知,原固体混合物中含有0.1molAl,质量为2.7g;若A全部来源于原固体混合物中的SiO2,则SiO2、Fe、Al三者质量之和大于17.1g,这不可能;若A全部来源于原固体混合物中的Si,则Si、Fe、Al三者质量之和小于17.1g,故原混合物中含有硅与SiO2,二者质量之和为17.1g-2.7g-5.6g=8.8g。通过一系列反应硅变成SiO2,使质量之和由8.8g变成12g,增加了3.2g,由Si~SiO2关系可求出原混合物中含硅2.8g、SiO26g。反应③是Al3+与NH3·H2O之间的反应,反应④是Fe(OH>2被氧化成Fe(OH>3的反应。mLPVzx7ZNw 4.Ⅰ.(1>5.0(2>abe Ⅱ.(1>错误!H2SO4(aq>+NaOH(aq>===错误!Na2SO4(aq>+H2O(l>ΔH=-57.3 kJ·mol-1AHP35hB02d (2>①4.0②-53.5kJ·mol-1③acd 解读Ⅰ.(1>使用245mLNaOH溶液,但需要配制250mL,m(NaOH>=40g·mol-1×0.25L×0.50mol·L-1=5.0g。NDOcB141gT (2>NaOH易潮解,应放在小烧杯中称量,要用药匙取用NaOH,用托盘天平称量。 Ⅱ.(1>根据中和热的定义,可以写出表示稀硫酸和氢氧化钠溶液反应的热化学方程式:错误!H2SO4(aq>+NaOH(aq>===错误! Na2SO4(aq>+H2O(l>1zOk7Ly2vA ΔH=-57.3kJ·mol-1。 (2>①第2组实验温度差为6.1℃,属于操作失误,处理数据时应舍去;其他3组的温度差平均值为(4.0℃+3.9℃+4.1℃>/3= 4.0℃。fuNsDv23Kh ②Q=cmΔt=4.18J·g-1·℃-1×(50g+30g>×4.0℃=1337.6J。ΔH=-错误!=-错误!≈-53.5kJ·mol-1。tqMB9ew4YX ③实验结果比57.3kJ·mol-1小的原因可能是量热计保温、隔热效果差,a对;仰视读数会造成所取NaOH溶液偏大,在反应过程中放出热量增多,计算的ΔH偏大,b错;实验中若分多次将NaOH 倒入硫酸中,则会使热量散失较多,造成测量值ΔH偏小,c对;测量NaOH溶液的温度计未用水清洗便立即去测硫酸的温度,致使酸、碱提前发生中和反应,造成热量损失,从而使Δt偏小,最终使ΔH 偏小,d对。HmMJFY05dE 5.(1>2mol·L-1 (2>Mg:47.1%Al:52.9% (3>78 解读对比甲、乙、丙三组数据,说明甲组中的盐酸过量;丙组中加入的合金比乙组多,但放出的气体一样多,可知丙组中合金过量;乙组中放出672mL气体,需合金的质量是:510×672/560=612(mg>,则乙组中的合金也过量。ViLRaIt6sk (1>求盐酸的浓度时应按乙组或丙组的数据来计算,即:2HCl~H2,n(HCl>=2n(H2>=2×0.672/22.4 mol=0.06 mol,c(HCl>=0.06 mol/0.03L=2mol·L-1。9eK0GsX7H1 (2>求合金中各物质的质量分数时应按甲组数据来计算。设该组合金中镁的物质的量为x,铝的物质的量为y,则有:24x+27y=0.510g,x+3y/2=0.560 L/22.4L·mol-1,联立解得:x=y=0.01mol,w(Mg>=0.24g/(0.24g+0.27g>×100%≈47.1%,w(Al>≈52.9%。naK8ccr8VI (3>丙组实验中合金过量,按题设可知剩余合金与原合金成分相同,故加入NaOH溶液发生的化学反应为MgCl2+2NaOH===Mg(OH>2↓+2NaCl,AlCl3+4NaOH===NaAlO2+3NaCl+2H2O,2Al+2NaOH+2H2O===2NaAlO2+3H2↑。B6JgIVV9ao 依据(2>中的结论可知,918mg合金中含n(Mg>=n(Al>≈0.018mol。由(2>知,放出672mLH2消耗Mg、Al的物质的量均为672/560×0.01 mol=0.012 mol。故剩余n′(Mg>=n′(Al>=0.006 mol,需n(NaOH>=2n(Mg2+>+4n(Al3+>+n′(Al>= 2×0.012+4×0.012+0.006=0.078 mol,V(NaOH>=0.078/1.00L=0.078L,即78mL。P2IpeFpap5 申明: 所有资料为本人收集整理,仅限个人学习使用,勿做商业用途。 第二十章数据的分析 20.1数据的代表 20.1.1平均数(第一课时) 一、教学目标: 1. 使学生理解数据的权和加权平均数的概念 2. 使学生掌握加权平均数的计算方法 3. 通过本节课的学习,还应使学生理解平均数在数据统计中的意义和作用:描述一组数据集中趋势的特征数字,是反映一组数据平均水平的特征数. 二、重点、难点和难点突破的方法: 1. 重点:会求加权平均数 2. 难点:对“权”的理解 3. 难点的突破方法: 首先应该复习平均数的概念:把一组数据的总和除以这组数据的个数所得的商,叫做这组数据的平均数.复习这个概念的好处有两个:一则可以将小学阶段的关于平均数的概念加以巩固,二则便于学生理解用数据与其权数乘积后求和作为加权平均数的分子. 在教材P124“讨论”栏目中要讨论充分、得当,排除学生常见的思维障碍.讨论问题中的错误做法是学生常见错误,尤其是中差生往往按小学学过的平均数计算公式生搬硬套.在讨论过程中教师应注意提问学生平均数计算公式中分子是什么、分母又是什么?学生由前面复习平均数定义可答出分子是数据的总和、分母是数据的个数,这时教师可递进设疑:那么,题目中涉及的每个数据是每个占有耕地面积还是人均占有耕地面积呢?数据个数是指A ,B ,C 三个县还是三个县的总人数呢?这样看来小明的做法有道理吗,为什么? 通过以上几个问题的设计为学生充分思考和相互讨论交流就铺好了台阶. 要使学生更好的去理解权的意义,可以再举一些生活、学习中的例子.比如:初二(五)班有4个小组,在一次测验中第一组有7名同学得了99分,1名同学得了61分,第二组有1名同学得到了100分、7名同学得62分.能否由 2 62 10026199+< +得出第二小组平均成绩这样的结论?为什么?这个例子简单明了又便于学生想象理解,能够让学生从中体会到得 99分的7个人比1个得61分的学生对平均成绩影响更大,从而理解权的意义. 在讨论栏目过后,引出加权平均数.最好让学生将公式与小学学过的平均数计算公式作比较看看意义上是否一致,这样做利于学生把新旧知识联系起来,利于对加权平均数公式的理解,也利于理解“权”的意义. 三、例习题意图分析 1. 教材P124的问题及讨论栏目在教学中起到的作用. (1)这个问题的设计和讨论栏目在此处安排最直接和最重要的目的是想引出权的概念和加权平均数的计算公式. (2)这个讨论栏目中的错误解法是初学者常见的思维方式,也是已学者易犯的错误.在这里安排讨论很得当,起揭示思维误区,警示学生、加深认识的作用. (3)客观上,教材P124的问题是一个实际问题,它照应了本节的前言——将在实际问题情境中,进一步探讨它们的统计意义,体会它们在解决实际问题中的作用,揭示了统计知识在解决实际问题中的重要作用. (4)P125的云朵其实是复习平均数定义,小方块则强调了权意义. 2. 教材P125例1的作用如下: (1)解决例1要用到加权平均数公式,所以说它最直接、最重要的目的是及时复习巩 实验数据的处理与分析 1. 0.80 g CuSO 4·5H 2O 样品受热脱水过程的热重曲线(样品质 量随温度变化的曲线)如下图所示。 请回答下列问题: (1)试确定200 ℃时固体物质的化学式________________________________________ ________________________________________________________________________; (要求写出推断过程)。 (2)取270 ℃所得样品,于570 ℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为________________________;把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为________,其存在的最高温度是________。 答案 (1)CuSO 4·H 2O CuSO 4·5H 2O=====200 ℃ CuSO 4·(5-n )H 2O +n H 2O 250 18n 0.80 g 0.80 g -0.57 g =0.23 g 可列式:2500.80 g =18n 0.23 g ,求得n ≈4,200 ℃时产物为CuSO 4·H 2O 晶体。 (2)CuSO 4=====570 ℃ CuO +SO 3↑ CuSO 4·5H 2O 102 ℃ 解析 (1)分析CuSO 4·5H 2O 受热脱水过程的热重曲线可知,200 ℃时和113 ℃时的产物相同,可根据113 ℃时样品质量确定脱水产物,设113 ℃时产物为CuSO 4·(5-n )H 2O ,则有 CuSO 4·5H 2O=====200 ℃CuSO 4·(5-n )H 2O +n H 2O 250 18n 0.80 g 0.80 g -0.57 g =0.23 g 可列式:2500.80 g =18n 0.23 g ,求得n ≈4,200 ℃时产物为CuSO 4·H 2O 晶体。 (2)根据灼烧产物是黑色粉末可知分解生成CuO ,则具有氧化性的另一产物为SO 3,所以灼烧时反应方程式为CuSO 4=====570 ℃ CuO +SO 3↑,CuO 溶于稀硫酸得CuSO 4溶液,结晶时又生成CuSO 4·5H 2O ,由脱水过程的热重曲线可知其存在的最高温度为102 ℃。 2.现有一份CuO 和Cu 2O 的混合物,用H 2还原法测定其中的CuO 质量x g ,实验中可以测定以 下数据:①W :混合物的质量(g)、②W (H 2O):生成水的质量(g)、③W (Cu):生成Cu 的质量(g)、④V (H 2):标准状况下消耗H 2的体积(L)。 (已知摩尔质量:Cu :64 g·mol -1、CuO :80 g·mol -1、Cu 2O :144 g·mol -1、 H 2O :18 g·mol -1) (1)为了计算x 至少需要测定上述4个数据中的________个,这几个数据的组合共有________种。请将 科研常用的实验数据分析与处理方法 对于每个科研工作者而言,对实验数据进行处理是在开始论文写作之前十分常见的工作之一。但是,常见的数据分析方法有哪些呢?常用的数据分析方法有:聚类分析、因子分析、相关分析、对应分析、回归分析、方差分析。 1、聚类分析(Cluster Analysis) 聚类分析指将物理或抽象对象的集合分组成为由类似的对象组成的多个类的分析过程。聚类是将数据分类到不同的类或者簇这样的一个过程,所以同一个簇中的对象有很大的相似性,而不同簇间的对象有很大的相异性。聚类分析是一种探索性的分析,在分类的过程中,人们不必事先给出一个分类的标准,聚类分析能够从样本数据出发,自动进行分类。聚类分析所使用方法的不同,常常会得到不同的结论。不同研究者对于同一组数据进行聚类分析,所得到的聚类数未必一致。 2、因子分析(Factor Analysis) 因子分析是指研究从变量群中提取共性因子的统计技术。因子分析就是从大量的数据中寻找内在的联系,减少决策的困难。因子分析的方法约有10多种,如重心法、影像分析法,最大似然解、最小平方法、阿尔发抽因法、拉奥典型抽因法等等。这些方法本质上大都属近似方法,是以相关系数矩阵为基础的,所不同的是相关系数矩阵对角线上的值,采用不同的共同性□2估值。在社会学研究中,因子分析常采用以主成分分析为基础的反覆法。 3、相关分析(Correlation Analysis) 相关分析(correlation analysis),相关分析是研究现象之间是否存在某种依存关系,并对具体有依存关系的现象探讨其相关方向以及相关程度。相关关系是一种非确定性的关系,例如,以X和Y 分别记一个人的身高和体重,或分别记每公顷施肥量与每公顷小麦产量,则X与Y显然有关系,而又没有确切到可由其中的一个去精确地决定另一个的程度,这就是相关关系。 4、对应分析(Correspondence Analysis) 对应分析(Correspondence analysis)也称关联分析、R-Q 型因子分析,通过分析由定性变量构成的交互汇总表来揭示变量间的联系。可以揭示同一变量的各个类别之间的差异,以及不同变量各个类别之间的对应关系。对应分析的基本思想是将一个联列表的行和列中各元素的比例结构以点的形式在较低维的空间中表示出来。 5、回归分析 研究一个随机变量Y对另一个(X)或一组(X1,X2,…,Xk)变量的相依关系的统计分析方法。回归分析(regression analysis)是确定两种或两种以上变数间相互依赖的定量关系的一种统计分析方法。运用十分广泛,回归分析按照涉及的自变量的多少,可分为一 第二十章数据的分析 数据的代表 20.1.1平均数(第一课时) 一、教学目标: 、使学生理解数据的权和加权平均数的概念 、使学生掌握加权平均数的计算方法 、通过本节课的学习,还应使学生理解平均数在数据统计中的意义和作用:描述一组数据集中趋势的特征数字,是反映一组数据平均水平的特征数。 二、重点、难点和难点突破的方法: 、重点:会求加权平均数 、难点:对“权”的理解 三、例习题意图分析 、教材的问题及讨论栏目在教学中起到的作用。 ()、这个问题的设计和讨论栏目在此处安排最直接和最重要的目的是想引出权的概念和加权平均数的计算公式。 ()、这个讨论栏目中的错误解法是初学者常见的思维方式,也是已学者易犯的错误。在这里安排讨论很得当,起揭示思维误区,警示学生、加深认识的作用。 ()、客观上,教材的问题是一个实际问题,它照应了本节的前言——将在实际问题情境中,进一步探讨它们的统计意义,体会它们在解决实际问题中的作用,揭示了统计知识在解决实际问题中的重要作用。 ()、的云朵其实是复习平均数定义,小方块则强调了权意义。 、教材例的作用如下: ()、解决例要用到加权平均数公式,所以说它最直接、最重要的目的是及时复习巩固公式,并且举例说明了公式用法和解题书写格式,给学生以示范和模仿。 ()、这里的权没有直接给出数量,而是以比的形式出现,为加深学生对权的意义的理解。 ()、两个问题中的权数各不相同,直接导致结果有所不同,这既体现了权数在求加权平均数的作用,又反映了应用统计知识解决实际问题时要灵活、体现知识要活学活用。 、教材例的作用如下: ()、这个例题再次将加权平均数的计算公式得以及时巩固,让学生熟悉公式的使用和书写步骤。 ()、例与例的区别主要在于权的形式又有变化,以百分数的形式出现,升华了学生对权的意义的理解。 ()、它也充分体现了统计知识在实际生活中的广泛应用。 四、课堂引入: 、若不选择教材中的引入问题,也可以替换成更贴近学生学习生活中的实例,下举一例可供借鉴参考。 求该校初二年级在这次数学考试中的平均成绩下述计算方法是否合理为什么 x 4 1 () 五、例习题分析: 例和例均为计算数据加权平均数型问题,因为是初学尤其之前与平均数计算公式已经作过比较,所以这里应该让学生搞明白问题中是否有权数,即是选择普通的平均数计算还是加权平均数计算,其次若用加权平均数计算,权数又分别是多少例的题意理解很重要,一定要让学生体会好这里的几个百分数在总成绩中的作用,它们的作用与权的意义相符,实际上这几个百分数分别表示几项成绩的权。 六、随堂练习: 、老师在计算学期总平均分的时候按如下标准:作业占、测验占、期中占、期末考试占,小关 (单位:小时) 求这些灯泡的平均使用寿命 实验设计与数据处理心得体会 刚开始选这门课的时候,我觉得这门课应该就是很难懂的课程,首先我们做过不少的实验了,当然任何自然科学都离不开实验,大多数学科(化工、化学、轻工、材料、环境、医药等)中的概念、原理与规律大多由实验推导与论证的,但我觉得每次到处理数据的时候都很困难,所以我觉得这就是门难懂的课程,却也就是很有必要去学的一门课程,它对于我们工科生来说也就是很有用途的,在以后我们实验的数据处理上有很重要的意义。 如何科学的设计实验,对实验所观测的数据进行分析与处理,获得研究观测对象的变化规律,就是每个需要进行实验的人员需要解决的问题。“实验设计与数据处理”课程就就是就是以概率论数理统计、专业技术知识与实践经验为基础,经济、科学地安排试验,并对试验数据进行计算分析,最终达到减少试验次数、缩短试验周期、迅速找到优化方案的一种科学计算方法。它主要应用于工农业生产与科学研究过程中的科学试验,就是产品设计、质量管理与科学研究的重要工具与方法,也就是一门关于科学实验中实验前的实验设计的理论、知识、方法、技能,以及实验后获得了实验结果,对实验数据进行科学处理的理论、知识、方法与技能的课程。 通过本课程的学习,我掌握了试验数据统计分析的基本原理,并能针对实际问题正确地运用,为将来从事专业科学的研究打下基础。这门课的安排很合理,由简单到复杂、由浅入深的思维发展规律,先讲单因素试验、双因素试验、正交试验、均匀试验设计等常用试验设计 方法及其常规数据处理方法、再讲误差理论、方差分析、回归分析等数据处理的理论知识,最后将得出的方差分析、回归分析等结论与处理方法直接应用到试验设计方法。 比如我对误差理论与误差分析的学习:在实验中,每次针对实验数据总会有误差分析,误差就是进行实验设计与数据评价最关键的一个概念,就是测量结果与真值的接近程度。任何物理量不可能测量的绝对准确,必然存在着测定误差。通过学习,我知道误差分为过失误差,系统误差与随机误差,并理解了她们的定义。另外还有对准确度与精密度的学习,了解了她们之间的关系以及提高准确度的方法等。对误差的学习更有意义的应该就是如何消除误差,首先消除系统误差,可以通过对照试验,空白试验,校准仪器以及对分析结果的校正等方法来消除;其次要减小随机误差,就就是要在消除系统误差的前提下,增加平行测定次数,可以提高平均值的精密度。 比如我对方差分析的理解:方差分析就是实验设计中的重要分析方法,应用非常广泛,它就是将不同因素、不同水平组合下试验数据作为不同总体的样本数据,进行统计分析,找出对实验指标影响大的因素及其影响程度。对于单因素实验的方差分析,主要步骤如下:建立线性统计模型,提出需要检验的假设;总离差平方与的分析与计算;统计分析,列出方差分析表。对于双因素实验的方差分析,分为两种,一种就是无交互作用的方差分析,另一种就是有交互作用的方差分析,对于这两种类型分别有各自的设计方法,但就是总体步骤都与单因素实验的方差分析一样。 数据分析实验报告 文稿归稿存档编号:[KKUY-KKIO69-OTM243-OLUI129-G00I-FDQS58- 第一次试验报告 习题1.3 1建立数据集,定义变量并输入数据并保存。 2数据的描述,包括求均值、方差、中位数等统计量。 分析—描述统计—频率,选择如下: 输出: 统计量 全国居民 农村居民 城镇居民 N 有效 22 22 22 缺失 均值 1116.82 747.86 2336.41 中值 727.50 530.50 1499.50 方差 1031026.918 399673.838 4536136.444 百分位数 25 304.25 239.75 596.25 50 727.50 530.50 1499.50 75 1893.50 1197.00 4136.75 3画直方图,茎叶图,QQ 图。(全国居民) 分析—描述统计—探索,选择如下: 输出: 全国居民 Stem-and-Leaf Plot Frequency Stem & Leaf 5.00 0 . 56788 数据分析实验报告 【最新资料,WORD 文档,可编辑修改】 2.00 1 . 03 1.00 1 . 7 1.00 2 . 3 3.00 2 . 689 1.00 3 . 1 Stem width: 1000 Each leaf: 1 case(s) 分析—描述统计—QQ图,选择如下: 输出: 习题1.1 4数据正态性的检验:K—S检验,W检验数据: 取显着性水平为0.05 分析—描述统计—探索,选择如下:(1)K—S检验 结果:p=0.735 大于0.05 接受原假设,即数据来自正太总体。 (2 )W 检验 结果:在Shapiro-Wilk 检验结果972.00 w ,p=0.174大于0.05 接受原假设,即数据来自正太总体。 习题1.5 5 多维正态数据的统计量 数据: 第二章 实验数据误差分析和数据处理 第一节 实验数据的误差分析 由于实验方法和实验设备的不完善,周围环境的影响,以及人的观察力,测量程序等限制,实验观测值和真值之间,总是存在一定的差异。人们常用绝对误差、相对误差或有效数字来说明一个近似值的准确程度。为了评定实验数据的精确性或误差,认清误差的来源及其影响,需要对实验的误差进行分析和讨论。由此可以判定哪些因素是影响实验精确度的主要方面,从而在以后实验中,进一步改进实验方案,缩小实验观测值和真值之间的差值,提高实验的精确性。 一、误差的基本概念 测量是人类认识事物本质所不可缺少的手段。通过测量和实验能使人们对事物获得定量的概念和发现事物的规律性。科学上很多新的发现和突破都是以实验测量为基础的。测量就是用实验的方法,将被测物理量与所选用作为标准的同类量进行比较,从而确定它的大小。 1.真值与平均值 真值是待测物理量客观存在的确定值,也称理论值或定义值。通常真值是无法测得的。若在实验中,测量的次数无限多时,根据误差的分布定律,正负误差的出现几率相等。再经过细致地消除系统误差,将测量值加以平均,可以获得非常接近于真值的数值。但是实际上实验测量的次数总是有限的。用有限测量值求得的平均值只能是近似真值,常用的平均值有下列几种: (1) 算术平均值 算术平均值是最常见的一种平均值。 设1x 、2x 、……、n x 为各次测量值,n 代表测量次数,则算术平均值为 n x n x x x x n i i n ∑==+???++=121 (2-1) (2) 几何平均值 几何平均值是将一组n 个测量值连乘并开n 次方求得的平均值。即 n n x x x x ????=21几 (2-2) (3)均方根平均值 n x n x x x x n i i n ∑==+???++= 1 222221均 (2-3) (4) 对数平均值 在化学反应、热量和质量传递中,其分布曲线多具有对数的特性,在这种情况下表征平均值常用对数平均值。 设两个量1x 、2x ,其对数平均值 《数据分析》实验报告 班级:07信计0班学号:姓名:实验日期2010-3-11 实验地点:实验楼505 实验名称:样本数据的特征分析使用软件名称:MATLAB 实验目的1.熟练掌握利用Matlab软件计算均值、方差、协方差、相关系数、标准差与变异系数、偏度与峰度,中位数、分位数、三均值、四分位极差与极差; 2.熟练掌握jbtest与lillietest关于一元数据的正态性检验; 3.掌握统计作图方法; 4.掌握多元数据的数字特征与相关矩阵的处理方法; 实验内容安徽省1990-2004年万元工业GDP废气排放量、废水排放量、固体废物排放量以及用于污染治理的投入经费比重见表6.1.1,解决以下问题:表6.1.1废气、废水、固体废物排放量及污染治理的投入经费占GDP比重 年份 万元工业GDP 废气排放量 万元工业GDP 固体物排放量 万元工业GDP废 水排放量 环境污染治理投 资占GDP比重 (立方米)(千克)(吨)(%)1990 104254.40 519.48 441.65 0.18 1991 94415.00 476.97 398.19 0.26 1992 89317.41 119.45 332.14 0.23 1993 63012.42 67.93 203.91 0.20 1994 45435.04 7.86 128.20 0.17 1995 46383.42 12.45 113.39 0.22 1996 39874.19 13.24 87.12 0.15 1997 38412.85 37.97 76.98 0.21 1998 35270.79 45.36 59.68 0.11 1999 35200.76 34.93 60.82 0.15 2000 35848.97 1.82 57.35 0.19 2001 40348.43 1.17 53.06 0.11 2002 40392.96 0.16 50.96 0.12 2003 37237.13 0.05 43.94 0.15 2004 34176.27 0.06 36.90 0.13 1.计算各指标的均值、方差、标准差、变异系数以及相关系数矩阵; 2.计算各指标的偏度、峰度、三均值以及极差; 3.做出各指标数据直方图并检验该数据是否服从正态分布?若不服从正态分布,利用boxcox变换以后给出该数据的密度函数; 4.上网查找1990-2004江苏省万元工业GDP废气排放量,安徽省与江苏省是 否服从同样的分布? 课题:20.1.1 平均数1知识与技能:1、使学生理解数据的权和加权平均数的概念 2、使学生掌握加权平均数的计算方法 过程与方法:3、通过本节课的学习,使学生理解平均数在数据统计中的意义和作用:描述一组数据集中趋势的特征数字,是反映一组数据平均水平的特征数。 情感态度与价值观:能灵活应用一组数据平均水平解决实际问题 教学重点:会求加权平均数 教学难点:对“权”的理解 教学方法:创设情景观察思考分析讨论归纳总结得出结论 教学过程: 一课堂导入: 问题1:一家公司打算招聘一名英文翻译。对甲、乙两名应试者进行了听、说、读、写的英语水平测试,他们的各项成绩如下: 应试者听说读写 甲85 78 85 73 乙73 80 82 83 1、如果这家公司想招一名综合能力较强的翻译,计算两名应试者平均成绩,从他们的成绩看,应该录取谁? 2、如果这家公司想招一名笔译能力较强的翻译,听、说、读、写的成绩按照2:1:3:4的比确定,计算两名应试者平均成绩,从他们的成绩看,应该录取谁? 学生思考、讨论解答,教师更正 解:1、甲的平均成绩=《85+78+85+73>/4=80.25 乙的平均成绩=《73+80+82+83>/4=79.5 因为..的平均成绩比..的高,所以应该录取...。 2、甲的平均成绩=....................................... 乙的平均成绩=.....................................? 因为..的平均成绩比..的高,所以应该录取...。 二、合作探究: 1、议一议 :上叙问题1是利用平均数的公式计算平均成绩,其中每个数据一样重要。问题2呢? 学生思考、分组讨论,之后,看课本p112面,理解“权”的意义, 以及加权平均数的公式。 三、交流展示: 例1:课本p112面例题1 学生分组讨论,小组发言,学生演板 小结:1、 解决例1要用到加权平均数公式,所以说它最直接、最重要的目的是 及时复习巩固公式,并且举例说明了公式用法和解题书写格式,给学生以示范和模仿。 2、例1与问题1的区别主要在于权的形式又有变化,以百分数的形式出现,升华了学生对权的意义的理解。 (3)、它也充分体现了统计知识在实际生活中的广泛应用。 求该校初二年级在这次数学考试中的平均成绩?下述计算方法是否合理?为什么? x =4 1(79+80+81+82)=80.5 学生分组讨论,小组发言,学生演板 四、归纳小结: 1、平均数 2、加权平均数的公式 3、权的意义 五、当堂训练: 一、必作题 : 1、某人打靶,有a 次打中x 环,b 次打中y 环,则这个人平均每次中靶 环。 数据的分析全章教案 第1课时 课题:6.1.1 从平均数到加权平均数(1) 学习目标: 1、认识平均数与加权平均数的关系; 2、掌握加权平均数的意义与计算方法; 3、培养学生对数学的感悟能力。 学习重点:理解权数的性质,以及加权平均数的计算方法。 学习难点:理解加权平均数的概念及其与普通平均数的区别。 学习过程: 一、观察,创设问题情景。 甲、乙两组各有8名同学,测量他们的身高,得到下面两组数据(单位:米):甲组:1.60,1.55,1.71,1.56,1.63,1.53,1.68,1.62。 乙组:1.60,1.64,1.60,1.60,1.64,1.68,1.68,1.68。 1、这两组数据有什么不同? A、甲组中的8个数都不相同:每个数只出现一次。 B、乙组中含有相同的数:1.60出现3次1.64出现2次,1.68出现3次,重复出现的次数(频数)不同,反映了数据之间的差异。 2、分别计算甲、乙两组同学的平均身高。 A、甲组同学的平均身高为: (1.60+1.55+1.71+1.56+1.63+1.53+1.68+1.62)÷8=1.61(米) B、乙组同学的平均身高为: (1.60+1.64+1.60+1.60+1.64+1.68+1.68+1.68)÷8=1.64(米) 3、想一想,计算乙组同学的平均身高,有没有别的方法? A 、重复出现的数相加,可以用乘法,乙组同学的身高也可以这样计算: (1.60×3+1.64×2+1.68×3)÷8=1.64(米) B 、根据乘法分配律,这个式子也可以写成: (1.60×3+1.64×2+1.68×3) ×81 =1.60×833/8+1.64×82 +1.68×81 =1.64(米) 二、探索研究、建立数模 1、在乙数数据的8个数中: 频数 频率(比率) 1.60 有3个,占83 ;1.64 有2个,占41 ;1.68 有3个占83。 83,1/4,8 3分别表示1.60,1.64,1.68 这3个数在乙组数据的8个数中所占的比例,分别称它们为这3个数的权数。 A 、在乙组数据中: 1.60的权数是(83); 1.64的权数是(41 ); 1.68的 权数是(8 3 )。 B 、3个权之和是(83+41+8 3 )=1 C 、小结:一般地,权数是一组非负数, 权数之和为1。 2、按算式1.60×83+1.64×41 +1.68×83=1.64算得的平均数,称为1.60, 1.64,1.68分别以83,41,8 3 为权的加权平均数。 三、思索、应用、拓展 1、比较下面的两种说法: A 、1.64是1.60,1.60,1.60,1.64,1.64,1.68,1.68,1.68的平均数。 实验数据的处理分析 [考纲要求] 能分析和处理实验数据,得出合理的结论。 热点实验数据筛选与处理 实验所得的数据,可分为有用、有效数据,正确、合理数据,错误、无效数据,及无用、多余数据等。能从大量的实验数据中找出有用、有效、正确、合理的数据是实验数据分析处理题的一个重要能力考查点,也是近年来命题变化的一个重要方向。 解题策略 对实验数据筛选的一般方法和思路为“五看”:一看数据是否符合测量仪器的精度特点,如用托盘天平测得的质量的精度为,若精度值超过了这个范围,说明所得数据是无效的;二看数据是否在误差允许范围内,若所得的数据明显超出误差允许范围,要舍去;三看反应是否完全,是否是过量反应物作用下所得的数据,只有完全反应时所得的数据,才能进行有效处理和应用;四看所得数据的测试环境是否一致,特别是气体体积数据,只有在温度、压强一致的情况下才能进行比较、运算;五看数据测量过程是否规范、合理,错误和违反测量规则的数据需要舍去。 典例导悟(·江苏,).对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。 一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体为催化剂(可循环使用),在溶液中加入乙酸酐(有脱水作用), ℃反应。反应结束后,过滤,滤液分别用溶液、水洗至中性,再经分离提纯得到对硝基甲苯。 ()上述实验中过滤的目的是。 ()滤液在分液漏斗中洗涤静置后,有机层处于层(填“上”或“下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有。 ②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是。 ③与浓硫酸催化甲苯硝化相比,催化甲苯硝化的优点有、。 热点实验数据综合分析 如何用好、选好数据,是解决这类试卷的关键所在。解决这类试卷的一般方法为:比较数据,转变物质,分析利弊,确定方案。 解题策略 数据分析实验报告 【最新资料,WORD文档,可编辑修改】 第一次试验报告 习题1.3 1建立数据集,定义变量并输入数据并保存。 2数据的描述,包括求均值、方差、中位数等统计量。 分析—描述统计—频率,选择如下: 输出: 方差1031026.918399673.8384536136.444百分位数25304.25239.75596.25 50727.50530.501499.50 751893.501197.004136.75 3画直方图,茎叶图,QQ图。(全国居民) 分析—描述统计—探索,选择如下: 输出: 全国居民Stem-and-Leaf Plot Frequency Stem & Leaf 9.00 0 . 122223344 5.00 0 . 56788 2.00 1 . 03 1.00 1 . 7 1.00 2 . 3 3.00 2 . 689 1.00 3 . 1 Stem width: 1000 Each leaf: 1 case(s) 分析—描述统计—QQ图,选择如下: 输出: 习题1.1 4数据正态性的检验:K—S检验,W检验数据: 取显着性水平为0.05 分析—描述统计—探索,选择如下:(1)K—S检验 单样本Kolmogorov-Smirnov 检验 身高N60正态参数a,,b均值139.00 标准差7.064 最极端差别绝对值.089 正.045 负-.089 Kolmogorov-Smirnov Z.686 渐近显着性(双侧).735 a. 检验分布为正态分布。 b. 根据数据计算得到。 结果:p=0.735 大于0.05 接受原假设,即数据来自正太总体。(2)W检验 授课教案 班级:17计1班课程:office2010 授课教师:黄媚 ?教学过程设计 教学环节及 时间分配 教学内容师生活动设计意图导入新课 ( 3分钟) 讲授新课 ( 20分 钟) 通过一个与该节相同的例子观看, 导入本次新课。 第七章电子表格中的数据处理 7、2 数据处理与分析 7.2.1 数据的查找与替换 1、数据查找 单击任意单元格-开始-【编辑】组-查 找和替换-查找-在“查找和替换”的对 话框输入查找内容-选择“查找全部” 2、数据替换 单击任意单元格-开始-【编辑】组-查 找和替换-替换-在“查找和替换”的“替 换”对话框输入查找内容和替换内容- 选择“全部替换” 教师示范操作 学生认真听课并回 答教师提出的问 题。 当堂的师生互动 能让学生更能加 深对操作步骤的 印象,对其中运用 到的按钮印象更 深刻 序 选 7.2.2 数据排序 1、使用排序按钮快速排序 开始-【编辑】组-排序和筛选 表示数据按递增顺序排列,使最小值位于列的顶端 表示数据按递减顺序排列,使最大值位于列的顶端 2、使用“排序”对话框进行排序 选择需要排序的单元格-数据-【排序和筛选】组-排序-确定 列——选择要排序的列 排序依据——选择排序类型 次序——选择排序方式 数据包含标题——排序时保留字段名称 通过学生自主练习,提高学生动手操作能力。 7.2.3 数据筛选 1、自动筛选 按值列表、按格式、按条件 选择所需单元格-数据-【排序和筛选】组- “筛选”下拉按钮-选择所需值-确定 2、自定义筛选 选择所需的单元格区域或表-数据-【排序和筛选】组-筛选 讲座 实验误差及数据处理 教学要求 1、了解实验误差及其表示方法; 2、掌握了解有效数字的概念,熟悉其运算规则; 3、初步掌握实验数据处理的方法。 重点及难点 重点:实验误差及其表示方法;有效数字;实验数据处理。 难点:有效数字运算规则;实验数据的作图法处理。 教学方法与手段 讲授,ppt演示。 教学时数 4学时 教学内容 引言 化学实验中经常使用仪器对一些物理量进行测量,从而对系统中的某些化学性质和物理性质作出定量描述,以发现事物的客观规律。但实践证明,任何测量的结果都只能是相对准确,或者说是存在某种程度上的不可靠性,这种不可靠性被称为实验误差。产生这种误差的原因,是因为测量仪器、方法、实验条件以及实验者本人不可避免地存在一定局限性。 对于不可避免的实验误差,实验者必须了解其产生的原因、性质及有关规律,从而在实验中设法控制和减小误差,并对测量的结果进行适当处理,以达到可以接受的程度。 一、误差及其表示方法 1.准确度和误差 ⑴准确度和误差的定义 准确度是指某一测定值与“真实值”接近的程度。一般以误差E表示, E=测定值-真实值 当测定值大于真实值,E为正值,说明测定结果偏高;反之,E为负值,说明测定结果偏低。误差愈大,准确度就愈差。 实际上绝对准确的实验结果是无法得到的。化学研究中所谓真实值是指由有经验的研究人员同可靠的测定方法进行多次平行测定得到的平均值。以此作为真实值,或者以公认的手册上的数据作为真实值。 ⑵绝对误差和相对误差 误差可以用绝对误差和相对误差来表示。 绝对误差表示实验测定值与真实值之差。它具有与测定值相同的量纲。如克、毫升、百分数等。例如,对于质量为0.1000g的某一物体。在分析天平上称得其质量为0.1001g,则称量的绝对误差为+0.0001g。 只用绝对误差不能说明测量结果与真实值接近的程度。分析误差时,除要去 人教版八年级(下)数学教案《数据的分析》 单元教案 学习目标 1.进一步理解平均数、中位数和众数等统计量的统计意义; 2.会计算加权平均数,理解“权”的意义,能选择适当的统计量表示数据的集中趋势; 3.会计算极差和方差,理解它们的统计意义,会用它们表示数据的波动情况; 4.能用计算器的统计功能进行统计计算,进一步体会计算器的优越性; 5.会用样本平均数、方差估计总体的平均数、方差,进一步感受抽样的必要性,体会用样本估计总体的思想; 6.从事收集、整理、描述和分析数据得出结论的统计活动,经历数据处理的基本过程,体验统计与生活的联系,感受统计在生活和生产中的作用,养成用数据说话的习惯和实事求是的科学态度。 (二)重、难点分析 统计中常用的平均数有算数平均数(简单算数平均数和加权算数平均数)、调和平均数、几何平均数等。根据《标准》的要求,本章着重研究了加权平均数。 内容分析 本章主要研究平均数(主要是加权平均数)、中位数、众数以及极差、方差等统计量的统计意义,学习如何利用这些统计量分析数据的集中趋势和离散情况,并通过研究如何用样本的平均数和方差估计总体的平均数和方差,进一步体会用样本估计总体的思想。 下面是本章知识展开的结构框图。 本章知识的展开顺序如下图: (四)课时分配 全章教学约需15课时(不包括选学内容的课时数),具体内容和课时分配如下: 18.1 数据的代表约6课时 18.2 数据的波动约5课时 18.3 课题学习约2课时 数学活动 小结约2课时 数据的代表 18.1.1平均数(第一课时) 一、教学目标: 1、使学生理解数据的权和加权平均数的概念 2、使学生掌握加权平均数的计算方法 3、通过本节课的学习,还应使学生理解平均数在数据统计中的意义和作用:描述一组数据集中趋势的特征数字,是反映一组数据平均水平的特征数。 二、重点、难点分析: 1、重点:会求加权平均数 2、难点:对“权”的理解 三、课程类型:新授课 方法手段:启发式教学法 四、课堂引入: 1、若不选择教材中的引入问题,也可以替换成更贴近学生学习生活中的实例,下举一例可供借鉴参考。 某校初二年级共有4个班,在一次数学考试中参考人数和成绩如下: 数据的统计与分析教案 Statistics and analysis of data teaching plan 数据的统计与分析教案 前言:小泰温馨提醒,数学是研究数量、结构、变化、空间以及信息等概念的一门学科,从某种角度看属于形式科学的一种,在人类历史发展和社会生活中,数学发挥着不可替代的作用,是学习和研究现代科学技术必不可少的基本工具。本教案根据数学课程标准的要求和针对教学对象是初中生群体的特点,将教学诸要素有序安排,确定合适的教学方案的设想和计划、并以启迪发展学生智力为根本目的。便于学习和使用,本文下载后内容可随意修改调整及打印。 数据的统计与分析 教学内容:本节课的内容安排是七上第四章的一点补充,即在学习了数据的分析的基础上带学生到网络教室利用网络和excel 平台对生活和社会中的一些热点问题的相关数据进行统计和分析 并得出相应的信息 教材分析:数据的处理和分析是社会生活中较为普遍的一个 知识点,与我们的生活息息相关,也是北师大版新教材每学期都要 涉及的一个重要内容。本节课不仅仅要让学生回顾和掌握所学的 相关知识,还要通过动手实做了解信息技术在数据处理中的作用。 学校及学生状况分析:重庆外国语学校是全国首批创办的八 所外国语学校之一,重庆市教委直属xxx中学,全国享受20%保送名额的13所外国语学校之一,学校设备先进一流,实现了校园网络化,学生来自全国各地,素质普遍较高,由于我校是国家级课题“z+z智能教育平台运用与国家数学课程改革的实验研究”实验学校,学生有在网络教室上数学课的实际体验。 学习目标: 认知目标:经历综合运用已有知识解决问题的过程,加深对数据的认识,体会数学与现实生活的联系。 能力目标:经历观察、比较、估计、推理、交流等过程,发展获得一些研究问题与合作交流的方法与经验。让学生实际操作,了解信息技术在数据处理中的作用。 情感目标:设置丰富的问题情景与活动,激发学生的好奇心和自动学习的欲望,让学生想学,会学,乐学;体验数学与日常生活密切相关。 重点:通过对数据的分析从而得出相应的一些信息 难点:比较、估计、推理等方法的应用 教具:采用多媒体教学(powerpoint和excel展示)并让学生在网络教室动手实做。 教法:运用多种教学方法,既有老师的讲解,又有学生探索、师生共做,学生小组合作及动手实做。 教学过程: 我们今天生活的这个世界,是一个充满信息、瞬息变化的世界,而表达信息的重要方式之一就是数据。如果大家看看报纸、电视,就会发现无论是新闻、经济论坛、天气预报、广告或者是体育比赛,很多地方都十分频繁地使用着数据。请大家从自己的身边选取一两个有意义的数据,并想一想从中可以获得哪些信息? (学生会从自己的身边举出许多的数据,老师关键是引导学 数据分析与挖掘实验报告 《数据挖掘》实验报告 目录 1.关联规则的基本概念和方法 (1) 1.1数据挖掘 (1) 1.1.1数据挖掘的概念 (1) 1.1.2数据挖掘的方法与技术 (2) 1.2关联规则 (5) 1.2.1关联规则的概念 (5) 1.2.2关联规则的实现——Apriori算法 (7) 2.用Matlab实现关联规则 (12) 2.1Matlab概述 (12) 2.2基于Matlab的Apriori算法 (13) 3.用java实现关联规则 (19) 3.1java界面描述 (19) 3.2java关键代码描述 (23) 4、实验总结 (29) 4.1实验的不足和改进 (29) 4.2实验心得 (30) 1.关联规则的基本概念和方法 1.1数据挖掘 1.1.1数据挖掘的概念 计算机技术和通信技术的迅猛发展将人类社会带入到了信息时代。在最近十几年里,数据库中存储的数据急剧增大。数据挖掘就是信息技术自然进化的结果。数据挖掘可以从大量的、不完全的、有噪声的、模糊的、随机的实际应用数据中,提取隐含在其中的,人们事先不知道的但又是潜在有用的信息和知识的过程。 许多人将数据挖掘视为另一个流行词汇数据中的知识发现(KDD)的同义词,而另一些人只是把数据挖掘视为知识发现过程的一个基本步骤。知识发现过程如下: ·数据清理(消除噪声和删除不一致的数据)·数据集成(多种数据源可以组合在一起)·数据转换(从数据库中提取和分析任务相关的数据) ·数据变换(从汇总或聚集操作,把数据变换和统一成适合挖掘的形式) ·数据挖掘(基本步骤,使用智能方法提取数 据模式) ·模式评估(根据某种兴趣度度量,识别代表知识的真正有趣的模式) ·知识表示(使用可视化和知识表示技术,向用户提供挖掘的知识)。 1.1.2数据挖掘的方法与技术 数据挖掘吸纳了诸如数据库和数据仓库技术、统计学、机器学习、高性能计算、模式识别、神经网络、数据可视化、信息检索、图像和信号处理以及空间数据分析技术的集成等许多应用领域的大量技术。数据挖掘主要包括以下方法。神经网络方法:神经网络由于本身良好的鲁棒性、自组织自适应性、并行处理、分布存储和高度容错等特性非常适合解决数据挖掘的问题,因此近年来越来越受到人们的关注。典型的神经网络模型主要分3大类:以感知机、bp反向传播模型、函数型网络为代表的,用于分类、预测和模式识别的前馈式神经网络模型;以hopfield 的离散模型和连续模型为代表的,分别用于联想记忆和优化计算的反馈式神经网络模型;以art 模型、koholon模型为代表的,用于聚类的自组 表1-1:不同频率下的遏止电压表 λ(nm)365 404.7 435.8 546.1 577 v(10^14)8.219 7.413 6.884 5.493 5.199 |Ua|(v) 1.727 1.357 1.129 0.544 0.418 表1-2:λ=365(nm)时不同电压下对应的电流值 U/(v)-1.927 -1.827 -1.727 -1.627 -1.527 -1.427 -1.327 I/(10^-11)A-0.4 -0.2 0 0.9 3.9 8.2 14 -1.227 -1.127 -1.027 -0.927 -0.827 -0.727 -0.718 24.2 38.1 52 66 80 97.2 100 表1-3:λ=404.7(nm)时不同电压下对应的电流值 U/(v) -1.477 -1.417 -1.357 -1.297 -1.237 -1.177 -1.117 I/(10^-11)A -1 -0.4 0 1.8 4.1 10 16.2 -1.057 -0.997 -0.937 -0.877 -0.817 -0.757 -0.737 24.2 36.2 49.8 63.9 80 93.9 100 表1-4:λ=435.8(nm)时不同电压下对应的电流值 U/(v)-1.229 -1.179 -1.129 -1.079 -1.029 -0.979 -0.929 I/(10^-11)A-1.8 -0.4 0 2 4.2 10.2 17.9 -0.879 -0.829 -0.779 -0.729 -0.679 -0.629 -0.579 -0.575 24.8 36 47 59 71.6 83.8 98 100 表1-5:λ=546.1(nm)时不同电压下对应的电流值 U/(v)-0.604 -0.574 -0.544 -0.514 -0.484 -0.454 -0.424 I/(10^-11)A-4 -2 0 3.8 10 16.2 24 -0.394 -0.364 -0.334 -0.304 -0.274 -0.244 -0.242 34 46 56.2 72 84.2 98.2 100 表1-6:λ=577(nm)时不同电压下对应的电流值 U/(v)-0.478 -0.448 -0.418 -0.388 -0.358 -0.328 -0.298 I/(10^-11)A-3.1 -1.8 0 2 6 10.2 16.1 -0.268 -0.238 -0.208 -0.178 -0.148 -0.118 -0.088 -0.058 22.1 31.8 39.8 49 58 68.2 79.8 90.1 -0.04 100第二十章 数据的分析 全章教案
实验数据的处理与分析
科研常用的实验数据分析与处理方法
数据的分析全章教案-人教版(精品教案)
实验设计与数据处理心得
数据分析实验报告
实验数据误差分析和数据处理
数据分析实验报告
八年级数学下册第二十章数据的分析教案
数据的分析全章备课教案
实验数据的处理分析
数据分析实验报告
数据处理与分析教案
实验数据的记录和处理
第二十章-数据的分析教案全章(精品)
数据的统计与分析教案
数据分析与挖掘实验报告
光电效应实验报告数据处理 误差分析
