化学平衡有关计算简单版

1.碳酸钠是一种重要的化工原料,主要采用氨碱法生产.回答下列问题:
(2)已知:①2NaOH (s )+CO 2(g )═Na 2CO 3(s )+H 2O (g )△H 1=﹣127.4kJ?mol ﹣1 ②NaOH (s )+CO 2(g )═NaHCO 3(s )△H 1=﹣131.5kJ?mol ﹣1
反应2NaHCO 3(s )═Na 2CO 3(s )+H 2O (g )+CO 2(g )的平衡常数表达式K= . 2.Bodensteins
研究了下列反应:
2(g)+I 2(g)在716 K 时,气体混合物中碘化氢的物质的量分数x (HI)与反应时间t
①根据上述实验结果,该反应的平衡常数
K 的计算式为_______________。 ②上述反应中,正反应速率为v 正=k
正
x 2
(HI),
逆反应速率为v 逆=k 逆x (H 2)x (I 2),其中k 正、k 逆为速率常数,则k 逆为________(以K 和k 正表示)。若
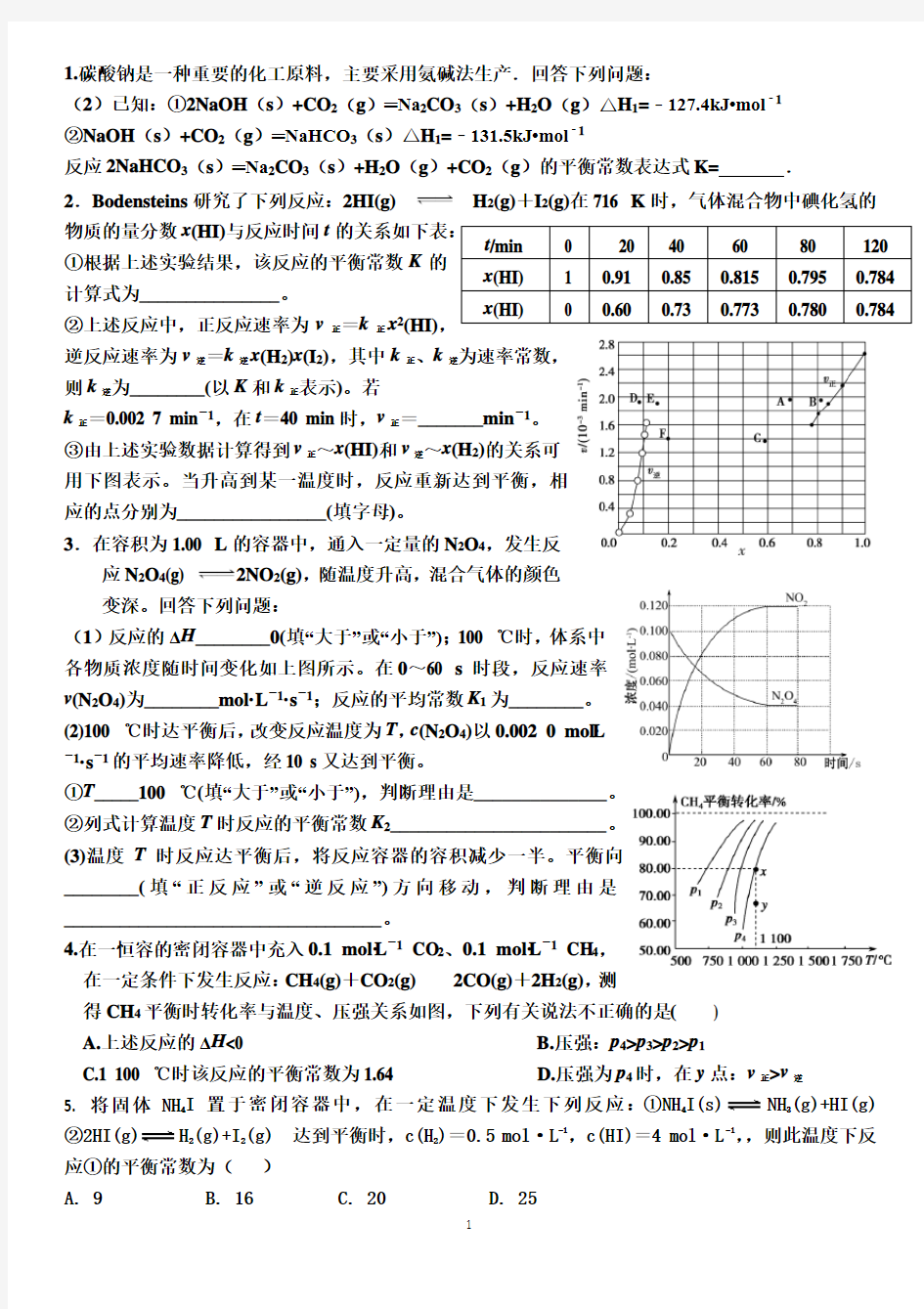
k 正=0.002 7 min -1,在t =40 min 时,v 正=_______min -1。 ③由上述实验数据计算得到v 正~x (HI)和v 逆~x (H 2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为________________(填字母)。
3.在容积为1.00 L 的容器中,通入一定量的N 2O 4,发生反
应N 2O 4(g)
2NO 2(g),随温度升高,混合气体的颜色
变深。回答下列问题:
(1)反应的ΔH ________0(填“大于”或“小于”);100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s 时段,反应速率v (N 2O 4)为________mol·L -1·s -1;反应的平均常数K 1为________。 (2)100 ℃时达平衡后,改变反应温度为T ,c (N 2O 4)以0.002 0 mol·L
-1
·s -1的平均速率降低,经10 s 又达到平衡。
①T _____100 ℃(填“大于”或“小于”),判断理由是______________。 ②列式计算温度T 时反应的平衡常数K 2_______________________。 (3)温度T 时反应达平衡后,将反应容器的容积减少一半。平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是__________________________________。
4.在一恒容的密闭容器中充入0.1 mol·L -1 CO 2、0.1 mol·L -1 CH 4,在一定条件下发生反应:CH 4(g)+CO 2
+2H 2(g),测
得CH 4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( ) A.上述反应的ΔH <0 B.压强:p 4>p 3>p 2>p 1
C.1 100 ℃时该反应的平衡常数为1.64
D.压强为p 4时,在y 点:v 正>v 逆 5. 将固体NH 4I 置于密闭容器中,在一定温度下发生下列反应:①NH 4I(s)NH 3(g)+HI(g)
②2HI(g)
H 2(g)+I 2(g) 达到平衡时,c(H 2)=0.5 mol·L -1,c(HI)=4 mol·L -1,,则此温度下反
应①的平衡常数为( )
A. 9
B. 16
C. 20
D. 25
6.顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化: 该反应的速率方程可表示为:v (正) =k (正)c (顺)和v (逆)=k (逆) c (反),k (正)和k (逆)在一定温度时为常数,分别称作正,逆反应速率常数。回答下列问题:
(1)已知:t 1温度下,k (正)=0.006s —1,k (逆)= 0.002s —1,该温度下反应的平衡常数值K 1=_____;该反应的活化能E a (正)小于E a (逆),则△H ________0(填“小于”“等于”或“大于”)。 (2)t 2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_______(填曲线编号),
平衡常数值K 2=_____;温度t 2___t 1(填“小于”“等于”或“大于”),判断理由是______。
7.N 2O 5是一种新型硝化剂,在一定温度下可发生下列反应:2N 2O 5(g )
2(g )+ O 2(g ) △H >0,T 1温度下的部分实验数据为:下列说法不正确...的是 A .500s 内N 2O 5分解速率为2.96×10—3
mol/(L · s)
B .T 1温度下的平衡常数为K 1 =125,1000s 时转化率为50%
C .其他条件不变时,T 2温度下反应到1000s 时测得N 2O 5(g )浓度为2.98 mol/L ,则T 1 D .T 1温度下的平衡常数为K 1,T 3温度下的平衡常数为K 3,若K 1> K 3,则T 1 >T 3 8.在一定温度下,将气体X 和气体Y 各0.16mol 充入10L 恒容密闭容器中,发生反应 △H <0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是 A .反应前2min 的平均速率ν(Z)=2.0×10—3mol·L —1·min —1 B .其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正) C .该温度下此反应的平衡常数K =1.44 D . 其他条件不变,再充入0.2molZ ,平衡时X 的体积分数增大 9.一定量的CO 2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO 2(g)2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:已知:气体分压(p 分)=气体总压(p 总)×体积分数。下列说法正确的是 ( ) A.550℃时,若充入惰性气体,v 正、v 逆均减小,平衡不移动 B.650℃时,反应达平衡后CO 2的转化率为25.0% C.T ℃时,若充入等体积的CO 2和CO,平衡向逆反应方向移动 D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数K p =24.0p 总 10.相同温度下体积均为1.5 L 的两个恒容容器中发生可逆反应:X 2 (g)+3Y 2(g)2XY 3(g) ΔH=- 92.6 kJ·mol -1,实验测得有关数据如下表: 下列叙述不正确的是( )A .容器①中达 到平衡时,Y 2的转化率为50% B .Q=27.78 kJ C .容器①、②中反应的平衡常数相等,K= D .相同温度下,起始时向容器中充入1.0 X 2 mol 、3.0 mol Y 2和2 mol XY 3,反应达到平衡前v(正)>v(逆) 1627 K(正)K(逆) CH 3CH 3H H CH 3CH 3 H H 顺式反式 11.已知t ℃时,反应FeO(s)+CO(g) Fe(s)+CO 2(g)的平衡常数K =0.25。 (1)t ℃时,反应达到平衡时n (CO)∶n (CO 2)=________。 (2)若在1 L 密闭容器中加入0.02 mol FeO(s),并通入x mol CO ,t ℃时反应达到平衡。此时FeO(s)转化率为50%,则x =________。 12.在10L 恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)M(g)+N(g),所得实验数据 如下表: 下列说法正确的是 A .实验①中,若5min 时测得 =0.050mol ,则0至5min 时间内,用N 表示的平均反应速率υ(N)1.0×10-2 mol/(L·min) B .实验②中,该反应的平衡常数=2.0 C .实验③中,达到平衡是,X 的转化率为60% D .实验④中,达到平衡时,b >0.060 13. 温度为T 时,向2.0L 恒容密闭容器中充入1.0 molPCl 5,反应PCl 5(g) PCl 3(g)+Cl 2(g)经 一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是 A.反应在前50 s 的平均速率为v (PCl 3)=0.0032 mol · L -1·s -1 B.保持其他条件不变,升高温度,平衡时,c(PCl 3)=0.11 mol ·L -1, 则反应的△H <0 C.相同温度下,起始时向容器中充入1.0molPCl 5、0.20molPCl 3和0.20molCl 2,达到平衡前v (正)> v (逆) D.相同温度下,起始时向容器中充入2.0molPCl 3、2.0molCl 2,达到平衡时,PCl 3的转化率小于80% 14.一定温度下,在三个体积均为2.5L 的恒容密闭容器中发生反应:CO 2(g )+H 2S (g (g ) +H 2O (g )下列说法正确的是 A .该反应正反应为放热反应 B .607K 时该反应的平衡常数为2.50×10-3 C .容器Ⅱ达到平衡时容器中COS 的物质的量为0.02mol D .容器Ⅲ达平衡时,再充入少量氦气,平衡将向正反应方向移动 15.已知:MgCO 3(s) MgO(s)+CO 2(g) ΔH >0,在密闭容器中投入过量碳酸镁在温度T 下达 到平衡,p (CO 2)=4 MPa 。 (1)该平衡常数表达式K =________。 (2)若反应体系的体积不变,升高温度,则p (CO 2)将________(填“增大”“减小”或“不变”)。 (3)若反应温度T 不变,将反应体系的体积缩小至原来的一半,则p (CO 2)变化范围为________。 16.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应: 2NO 2(g )+NaCl (s )NaNO 3(s )+ClNO (g ) K 1 ?H < 0 (I ) 2NO (g )+Cl 2(g )2ClNO (g ) K 2 ?H < 0 (II ) (1)4NO 2(g )+2NaCl (s )2NaNO 3(s )+2NO (g )+Cl 2(g )的平衡常数K= (用K 1、K 2 表示)。 (2)为研究不同条件对反应(II )的影响,在恒温条件下,向2L 恒容密闭容器中加入0.2mol NO 和0.1mol Cl 2,10min 时反应(II )达到平衡。测得10min 内v (ClNO )=7.5×10-3mol?L -1?min -1,则平衡后n (Cl 2)= mol ,NO 的转化率а1= 。其它条件保持不变,反应(II )在恒压条件下进行,平衡时NO 的转化率а2 а1(填“>”“<”或“=”),平衡常数K 2 (填“增大”“减小”或“不变”。若要使K 2减小,可采用的措施是 。 (2)某研究小组在实验室探究氨基甲酸铵(NH 2COONH 4)分解反应平衡常数的测定。将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH 2COONH 4(s) 2NH 3(g)+C O 2(g)。实验测得不同温度下的平衡数据列于下表:根据表中数据,写出15 ℃时的分解平衡常数计算表达式及结果(结果保留三位有效数字): 。 17.在 1.0 L 密闭容器中放入1.0 mol X(g),在一定温度进行如下反应:X(g) Y(g)+Z(g) ΔH =a kJ ·mol -1。反应时间(t )与容器内气体总压强(p )的数据见下表,回答下列问题: (1)实验测得,随温度的升高反应的平衡常数K 增大,则ΔH ________0(填“>”“<”或“=”)。 (2)其他条件不变时,为使平衡向右移动,采用的下列措施可行的是________。 A .缩小容器容积 B .及时分离出Y 、Z C .使用合理的催化剂 D .升高体系温度 (3)计算平衡时X 的转化率为________,该温度下反应的平衡常数值为________。 (4)由总压强p 和起始压强p 0 表示反应体系的总物质的量n (总 )和反应物X 的物质的量n (X),则n (总)=________mol ,n (X)=________mol ,反应物X 的转化率α(X)的表达式为________。 18.在一定条件下发生反应4NO 2(g)+O 2(g) 2N 2O 5(g) ΔH <0,T 1时,向体积为2 L 的恒容密闭 容器中通入NO 2和O 2,部分实验数据如表所示。下列说法不正确的是( ) A .0~5 s 内N 2O 5的平均反应速率为0.148 mol·L -1·s -1 B .其他条件不变,将容器体积压缩一半,则重新达到平衡时c (N 2O 5)<2 mol·L -1 C .设T 1时平衡常数为K 1,T 2时平衡常数为K 2,若T 1 则K 1>K 2 D .T 1时平衡常数为0.125,平衡时NO 2和O 2的转化率均为50% 19.甲醇水蒸气重整制氢(SRM )是用于驱动电动汽车的质子交换膜燃料电池的理想氢源,当前研究主要集中在提高催化剂活性和降低尾气中CO 含量,以免使燃料电池Pt 电极中毒。重整过程发生的反应如下:反应I CH 3OH(g)+H 2O(g)CO 2(g)+3H 2(g) ΔH 1 反应Ⅱ CH 3 OH(g) CO(g)+2H 2(g) ΔH 2 反应Ⅲ CO(g)+H 2O(g) CO 2(g)+H 2(g) ΔH 3 其对应的平衡常数分别为K 1、K 2、K 3,其中K 2、K 3随温度变化如下表所示:请回答:(1)反应Ⅱ能够自发进行的条件_______(填“低温”、 “高温”或“任何温度”),ΔH 1____ΔH 3 (填“>”、“<”或“=”)。 (2)相同条件下,甲醇水蒸气重整制氢较甲醇直接分解制氢(反应Ⅱ)的先进之处在于__________________。 (3)在常压、Cat.1催化下,CH 3OH 和H 2O 混和气体(体积比1∶1.2,总物质的量2.2mol )进行反应,t l 时刻测得CH 3OH 转化率及CO 、CO 2选择性随温度变化情况分别如图所示(CO 、CO 2的选择性:转化的CH 3OH 中生成CO 、CO 2的百分比)。注:曲线a 表示CH 3OH 的转化率,曲线b 表示CO 的选择性,曲线c 表示CO 2的选择性 ① 下列说法不正确... 的是__________。 A .反应适宜温度为300℃ B .工业生产通常在负压条件下进行甲醇水蒸气重整 C .己知Cat.2催化剂具有更高催化活性,可提高甲醇平衡转化率 D .添加CaO 的复合催化剂可提高氢气产率 20.二氧化碳与氢气催化合成甲醇,发生的反应为:CO 2(g )+3H 2(g )CH 3OH (g )+H 2O (g )ΔH=-46 kJ·mol -1 (3)一定条件下,往2L 恒容密闭容器中充入 1.2molCO 2和3.6molH 2,在不同催化剂作用下的反应I 、反应II 与反应III ,相同时间内CO 2转化率随温度 变化的数据如表所示,据表中数据绘制下右图: (T 5时,图中C 点转化率为66.67%,即转化了2/3) ① 催化剂效果最佳的反应是________________(填“反应I”,“反应II”,“反应III”)。 ② T 3的b 点v (正)______v (逆)(填 “>”, “<”, “=” )。 ③ T 4的a 点转化率比T 5 的c 点高的原因是____________________________。 ④ 求温度为T 5时,该反应的平衡常数K =_______。 化学反应速率和化学平衡 【专题目标】 1.了解化学反应速率的概念及表示方法,掌握同一反应中不同物质的化学反应速率与化学方程式中各物质的化学计量数的关系。 (1)概念:通常用单位时间内反应物浓度的减小或生成物浓度的增加来表示。 (2)表达式:t c v ??=(A) (A);单位:mol/(L ·min)或mol/(L ·s)。 (3)在同一反应中,用不同的物质表示反应速率的数值之比等于它们在化学方程式中的化学计量数之比。 2.了解化学反应的可逆性,理解化学平衡的特征,了解化学平衡与化学反应速率之间的内在联系。 (1)概念:在一定条件下的可逆反应里,正反应和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态叫做化学平衡状态,简称化学平衡。 (2)化学平衡状态的特征: ①“动” :化学平衡是动态平衡,即:v 正=v 逆≠0 ②“等” :达到化学平衡时v 正=v 逆,即同一物质的消耗速率等于生成速率 ③“定” :外界条件不变时,处于化学平衡状态的各物质的浓度、质量分数或体积分数保持不变 ④“变” :可逆反应的平衡状态是相对的,暂时的,当影响平衡的条件改变时,化学平衡即被破坏,并在新的条件下建立新的平衡状态 3.理解浓度、压强和温度等条件对化学平衡的影响,理解平衡移动原理的涵义。 理解勒夏特列原理:如果改变影响化学平衡的一个条件(如浓度、压强或温度等),平衡就会向着能够减弱这种改变的方向移动。 4.学会应用建立等效平衡的思维方式解决化学平衡中的常见问题。 【经典题型】 一、化学反应速率 题型一:根据化学计量数之比,计算反应速率 【例1】反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率) (X v(反应物的消耗速率或产物的生成速率)可表示为(C ) A.) mol/(L 0.010 ) (NH 3 s v? =B.) mol/(L 0.001 ) (O 2 s v? = C.) mol/(L 0.001 (NO)s v? =D.) mol/(L 0.045 O) (H 2 s v? = 【方法点拨】速率之比化学计量数之比 题型二:以图象形式给出条件,计算反应速率 【例2】某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:该反应的化学方程式为___3X+Y_______2Z_______。反应开始至2min,用Z表示的平均反应速率为__0.05mol/(L·min)__________。 题型三:根据已知的浓度、温度等条件,比较反应速率的大小 【例3】把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( B ) A.10℃20mL 3mol/L的X溶液 B.20℃30mL 2mol/L的X溶液 C.20℃10mL 4mol/L的X溶液 D.10℃10mL 2mol/L的X溶液 二、化学平衡 题型四:已知一个可逆反应、一种起始状态 考点过关(上)考点5 化学平衡计算 化学平衡是中学化学重要基础之一,是中学化学所涉及的溶解平衡、电离平衡、水解平衡等知识的核心,对很多知识的学习起着指导作用。而化学平衡计算是高考中的热点之一,此类试题常把基本概念和基础知识融汇在一起,具有知识联系广、灵活度大、隐含条件多、概念性强、思维层次高的特点。化学平衡的计算一般涉及到各组分的物质的量、浓度、转化率、百分含量、气体混合物的密度、平均摩尔质量、压强等,通常的思路是写出平衡式,列出相关量(起始量、变化量、平衡量),确定各量之间的关系,列出比例式或等式或依据平衡常数求解。 1.计算模式:化学平衡计算的最基本的方法模式是“平衡三段式法”。具体步骤是在化学方程式下写出有关物质起始时的物质的量、发生转化的物质的量、平衡时的物质的量(也可以是物质的量浓度或同温同压下气体的体积),再根据题意列式求解,起始、转化、平衡是化学平衡计算的“三步曲”,三步是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol、mol/L,也可用L。 m A(g)+n B(g)p C(g)+q D(g) n(起始)/mol ab00 n(转化)/mol mxnxpxqx n(平衡)/mol a-mxb-nxpxqx 反应可从左向右开始,也可以从右向左开始,也可以多种物质同时充入。可逆反应达到平衡状态时各物质浓度间的关系。反应物:平衡浓度=起始浓度-转化浓度;生成物:平衡浓度=起始浓度+转化浓度,其中各物质的转化浓度之比等于它们在化学方程式中各物质的化学计量数之比。 2.解题思路:具体题目要具体分析,灵活设立,一般设某物质的转化量为x;根据反应物、生成物及变化量的三者关系代入未知数确定平衡体系中各物质的起始量、变化量、平衡量并按“模式”列表;明确了“始”、“变”、“平”三个量的具体数值,再根据相应关系求平衡时某成分的浓度、反应物转化率等,得出题目答案。 3.计算公式: (1)变化量之比等于化学计量数之比v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q(未达到平衡时,用于确定化学方程式中未知的化学计量数)。 化学平衡常数及其计算训练题 1.O 3是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O 3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生的反应如下: 反应① O 3 2 +[O] ΔH >0 平衡常数为K 1; 反应② [O]+O 32 ΔH <0 平衡常数为K 2; 总反应:2O 3 2 ΔH <0 平衡常数为K 。 下列叙述正确的是( ) A .降低温度,总反应K 减小 B .K =K 1+K 2 C .适当升温,可提高消毒效率 D .压强增大,K 2减小 解析:选C 降温,总反应平衡向右移动,K 增大,A 项错误;K 1= c 2 c c 3 、 K 2= c 2 2 c c 3 、K =c 3 2c 2 3 =K 1·K 2,B 项错误;升高温度,反应①平衡向右移动, 反应②平衡向左移动,c ([O])增大,可提高消毒效率,C 项正确;对于给定的反应,平衡常数只与温度有关,D 项错误。 2.将一定量氨基甲酸铵(NH 2COONH 4)加入密闭容器中,发生反应NH 2COONH 4 3 (g)+CO 2(g)。该反应的平衡常数的负对 数(-lg K )值随温度(T )的变化曲线如图所示,下列说法中不正确的是( ) A .该反应的ΔH >0 B .NH 3的体积分数不变时,该反应一定达到平衡状态 C .A 点对应状态的平衡常数K (A)的值为10-2.294 D .30 ℃时,B 点对应状态的v 正 考纲要求 1.了解化学平衡常数(K)的含义。2.能利用化学平衡常数进行相关计算。 考点一化学平衡常数 1.概念 在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,用符号K表示。 2.表达式 对于反应m A(g)+n B(g)p C(g)+q D(g), K=c p?C?·c q?D? c m?A?·c n?B? (固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中)。3.意义及影响因素 (1)K值越大,反应物的转化率越大,正反应进行的程度越大。 (2)K只受温度影响,与反应物或生成物的浓度变化无关。 (3)化学平衡常数是指某一具体反应的平衡常数。 4.应用 (1)判断可逆反应进行的程度。 (2)利用化学平衡常数,判断反应是否达到平衡或向何方向进行。 对于化学反应a A(g)+b B(g)c C(g)+d D(g)的任意状态,浓度商:Q c=c c?C?·c d?D? c a?A?·c b?B? 。 Q<K,反应向正反应方向进行; Q=K,反应处于平衡状态; Q>K,反应向逆反应方向进行。 (3)利用K可判断反应的热效应:若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。 深度思考 1.正误判断,正确的打“√”,错误的打“×” (1)平衡常数表达式中,可以是物质的任一浓度() (2)催化剂能改变化学反应速率,也能改变平衡常数() (3)平衡常数发生变化,化学平衡不一定发生移动() (4)化学平衡发生移动,平衡常数不一定发生变化() (5)平衡常数和转化率都能体现可逆反应进行的程度() (6)化学平衡常数只受温度的影响,温度升高,化学平衡常数的变化取决于该反应的反应热() 2.书写下列化学平衡的平衡常数表达式。 (1)Cl2+H2O HCl+HClO (2)C(s)+H2O(g)CO(g)+H2(g) (3)CH3COOH+C2H5OH CH3COOC2H5+H2O (4)CO2-3+H2O HCO-3+OH- (5)CaCO3(s)CaO(s)+CO2(g) 3.一定温度下,分析下列三个反应的平衡常数的关系 ①N2(g)+3H2(g)2NH3(g)K1 ②1 2N2(g)+ 3 2H2(g)NH3(g)K2 ③2NH3(g)N2(g)+3H2(g)K3 (1)K1和K2,K1=K22。 (2)K1和K3,K1=1 K3。 题组一平衡常数的含义 1.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)K1 化学平衡常数和化学平衡计算 1.在密闭容器中将CO和水蒸气的混合物加热到800℃时,有下列平衡:CO+H22+H2,且K=1。若用2molCO和10mol H2O相互混合并加热到800℃,则CO的转化率为 ( ) A.16.7% B.50% C.66.7% D.83.3% 2.在容积为1L的密闭容器里,装有4molNO2,在一定温度时进行下面的反应: 2NO22O4(g),该温度下反应的平衡常数K=0.25,则平衡时该容器中NO2的物质的量为A.0mol B.1mol C.2mol D.3mol 3.某温度下H2(g)+I2的平衡常数为50。开始时,c(H2)=1mol·L-1,达平衡时,c(HI)=1mol·L-1,则开始时I2(g)的物质的量浓度为 ( ) A.0.04mol·L-1 B.0.5mol·L-1 C.0.54mol·L-1D.1mol·L-1 4.在一个容积为 6 L的密闭容器中,放入 3 L X(g)和2 L Y(g),在一定条件下发生反应: 4X(g)+n+6R(g)反应达到平衡后,容器内温度不变,混合气体的压强比原来增 加了5%,X的浓度减小1/3,则该反应中的n值为( ) A.3 B.4 C.5 D.6 5.在一定条件下,可逆反应X(g)十达到平衡时,X的转化率与Y的转化率之比为1∶2,则起始充入容器中的X与Y的物质的量之比为( ) A.1∶1 B.1∶3 C.2∶3 D.3∶2 6.将等物质的量的CO和H2O(g)混合,在一定条件下发生反应:CO(g)+H22(g)+H2(g),反应至4min时,得知CO的转化率为31.23%,则这时混合气体对氢气的相对密度为A.11.5 B.23 C.25 D.28 7.在一固定容积的密闭容器中,加入 4 L X(g)和6 L Y(g),发生如下反应:X(g)+n +W(g),反应达到平衡时,测知X和Y的转化率分别为25%和50%,则化学方程式中的n值为A.4 B.3 C.2 D.1 8.将固体NH4I置于密闭容器中,在某温度下发生下列反应:NH43(g)+HI(g), 2(g)+I2(g)。当反应达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则 NH3的浓度为( ) A.3.5mol·L-1 B.4mol·L-1 C.4.5mol·L-1D.5mol·L-1 9.体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应A(g)+。若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中C气体的体积占10%。下列判断中正确的是 ( ) A.原混合气体的体积为 1.2V L B.原混合气体的体积为 1.1V L C.反应达到平衡时气体A消耗掉0.05V L D.反应达到平衡时气体B消耗掉0.05V L 10.在n L密闭容器中,使1molX和2molY在一定条件下反应:a X(g)+b c Z(g)。达到平衡时,Y的转化率为20%,混合气体压强比原来下降20%,Z的浓度为Y的浓度的0.25倍,则a,c的值依次为( ) A.1,2 B.3,2 C.2,1 D.2,3 11.在一定条件下,1mol N2和3mol H2混合后反应,达到平衡时测得混合气体的密度是 同温同压下氢气的5倍,则氮气的转化率为( ) A.20% B.30% C.40% D.50% 12.已知CO(g)+H22(g)+H2(g)的正反应为放热反应,850℃时K=1。 (1)若温度升高到900°C,达平衡时K________1(填“大于”、“小于”或“等于”)。 (2)850℃时,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)=0.01mol·L-1,c(H2O)=0.03mol·L-1,c(CO2)=0.01mol·L-1,c(H2)=0.05mol·L-1。则反应开始时,H2O消耗速率比生成速率________(填“大”、“小”或“不能确定”)。 化学平衡计算题求解技巧 知识体系和复习重点 一、化学平衡常数(浓度平衡常数)及转化率的应用 1、化学平衡常数 (1)化学平衡常数的数学表达式 (2)化学平衡常数表示的意义 平衡常数数值的大小可以反映可逆反应进行的程度大小,K 值越大,反应进行越完全,反应物转化率越高,反之则越低。 2、有关化学平衡的基本计算 (1)物质浓度的变化关系 反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度 其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。 (2)反应的转化率(α):α=(或质量、浓度) 反应物起始的物质的量(或质量、浓度)反应物转化的物质的量×100% (3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时: ;恒温、恒压时:n 1/n 2=V 1/V 2 (4)计算模式(“三段式”) 浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g) 起始 m n O O 转化 ax bx cx dx 平衡 m-ax n-bx cx dx A 的转化率:α(A)=(ax/m )×100% C 的物质的量分数:ω(C)=×100% 技巧一:三步法 三步是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol 、mol/L ,也可用L 。 例1、X 、Y 、Z 为三种气体,把a mol X 和b mol Y 充入一密闭容器中,发生反应X + 2Y 2Z ,达到平衡时,若它们的物质的量满足:n (X )+ n (Y )= n (Z ),则Y 的转化率为( ) A 、%1005?+b a B 、%1005)(2?+b b a C 、%1005)(2?+b a D 、%1005)(?+a b a 解析:设Y 的转化率为α X + 2Y 2Z 起始(mol ) a b 0 转化(mol ) αb 2 1 αb αb 平衡(mol )-a αb 21 -b αb αb 依题意有:-a αb 21+ -b αb = αb ,解得:α= %1005)(2?+b b a 。故应选B 。 技巧二:差量法 差量法用于化学平衡计算时,可以是体积差量、压强差量、物质的量差量等等。 例2、某体积可变的密闭容器,盛有适量的A 和B 的混合气体,在一定条件下发生反应:A + 3B 2C ,若维持温度和压强不变,当达到平衡时,容器的体积为V L ,其中C 气体的体积占10%,下列推断正确的是( ) (a)已知初始浓度和平衡浓度求平衡常数和平衡转化率 例1:对于反应2SO 2(g)+ O2(g) 2SO3(g) ,若在一定温度下,将0.1mol的SO2(g)和0.06mol O2(g)注入一体积为2L的密闭容器中,当达到平衡状态时,测得容器中有0.088mol的SO3(g)试求在该温度下(1)此反应的平衡常数。 (2)求SO2(g)和O2(g)的平衡转化率。 (b)已知平衡转化率和初始浓度求平衡常数 例2:反应SO 2(g)+ NO2(g) SO3(g)+NO(g) ,若在一定温度下,将物质的量浓度均为2mol/L的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为60%,试求:在该温度下。 (1)此反应的浓度平衡常数。 (2)若SO2(g) 的初始浓度均增大到3mol/L,则SO2转化率变为多少? (c)知平衡常数和初始浓度求平衡浓度及转化率 练习1、在密闭容器中,将NO2加热到某温度时,可进行如下反应:2NO 2 2NO+O2,在平衡时各物质的浓度分别是: [NO2]=0.06mol/L,[NO]=0.24mol/L, [O2]=0.12mol/L.试求: (1)该温度下反应的平衡常数。 (2)开始时NO2的浓度。 (3)NO2的转化率。 练习2:在2L的容器中充入1mol CO和1mol H2O(g),发生反应:CO(g)+H 2O(g) CO2(g)+H2(g) 800℃时反应达平衡,若k=1.求:(1)CO的平衡浓度和转化率。 (2)若温度不变,上容器中充入的是1mol CO和2mol H2O(g),CO 和H2O(g),的平衡浓度和转化率是多少。 (3)若温度不变,上容器中充入的是1mol CO和4mol H2O(g),CO 和H2O(g),的平衡浓度和转化率是多少。 (4)若温度不变,要使CO的转化率达到90%,在题干的条件下还要充入H2O(g) 物质的量为多少。 练习1、 已知一氧化碳与水蒸气的反应为 CO + H 2O(g) CO2 + H2 在427℃时的平衡常数是9.4。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01mol/L,计算一氧化碳在此反应条件下的转化率。 练习2、 合成氨反应N 2+3H22NH3在某温度下达平衡时,各物质的浓度是:[N2]=3mol·L-1,[H2]=9 mol·L-1,[NH3]=4 mol·L-1。求该温度时的平衡常 化学平衡常数解题策略 ————————————————————————————————作者: ————————————————————————————————日期: 化学平衡常数解题策略 化学平衡常数与化学平衡及其影响因素的关系是高考命题的趋势之一。化学平衡常数的引入,对判 断化学平衡移动方向带来了科学的依据。平衡常数是表征反应限度的一个确定的定量关系,是反应 限度的最根本的表现。平衡常数的使用,从定量的角度解决了平衡的移动。 一、化学平衡常数 在一定温度下,可逆反应无论从正反应开始还是从逆反应开始,无论反应混合物的起始浓度是多少, 当反应达到平衡状态时,正反应速率等于逆反应速率,反应混合物中各组成成分的含量保持不变,即 各物质的浓度保持不变。生成物浓度的幂次方乘积与反应物浓度的幂次方乘积之比是常数,这个常数 叫化学平衡常数,用K表示。 化学平衡常数的计算公式为: 对于可逆反应:mA(g)+ nB(g)pC(g) + qD(g) 二、化学平衡常数意义 1、化学平衡常数K表示可逆反应进行的程度。 (1)化学平衡常数K只针对达到平衡状态的可逆反应适用,非平衡状态不适用。 (2)化学平衡常数K的表达式与可逆反应的方程式书写形式有关。对于同一可逆反应,正反应的平衡 常数等于逆反应的平衡常数的倒数,即:K正=1/K逆。 (3)K值越大,表示反应进行的程度越大,反应物转化率或产率也越大。 (4)K值不随浓度或压强的改变而改变,但随着温度的改变而改变。 (5)一般情况下,对于正反应是吸热反应的可逆反应,升高温度,K值增大;而对于正反应为放热 反应的可逆反应,升高温度,K值减少。 2、由于固体浓度为一常数,所以在平衡常数表达式中不再写出。 3、由于水的物质的量浓度为一常数(55.6 mol·L-1),因平衡常数已归并,书写时不必写出。 化学平衡计算题求解技巧 一、化学平衡常数(浓度平衡常数)及转化率的应用 1、化学平衡常数 (1)化学平衡常数的数学表达式 (2)化学平衡常数表示的意义 平衡常数数值的大小可以反映可逆反应进行的程度大小,K 值越大,反应进行越完全,反应物转化率越高,反之则越低。 2、有关化学平衡的基本计算 (1)物质浓度的变化关系 反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度 其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。 (2)反应的转化率(α):α= (或质量、浓度) 反应物起始的物质的量(或质量、浓度) 反应物转化的物质的量×100% (3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时: ;恒温、恒压时:n 1/n 2=V 1/V 2 (4)计算模式(“三段式”) 浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g) 起始 m n O O 转化 ax bx cx dx 平衡 m-ax n-bx cx dx A 的转化率:α(A)=(ax/m )×100% C 的物质的量分数:ω(C)= ×100% 技巧一:三步法 三步是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol、mol/L,也可用L。 例1、X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X + 2Y2Z,达到平衡时,若它们的物质的量满足:n(X)+ n(Y)= n (Z),则Y的转化率为() 技巧二:差量法 差量法用于化学平衡计算时,可以是体积差量、压强差量、物质的量差量等等。 例2、某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A + 3B 2C,若维持温度和压强不变,当达到平衡时,容器的 体积为V L,其中C气体的体积占10%,下列推断正确的是() ①原混合气体的体积为1.2VL ②原混合气体的体积为1.1VL ③反应达平衡时,气体A消耗掉0.05VL ④反应达平衡时,气体B消耗掉 0.05V L A、②③ B、②④ C、①③ D、①④ 技巧三:守恒法 1、质量守恒 例3、a mol N 2与b mol H 2 混合,要一定条件下反应达到平衡,生成了c mol NH 3,则NH 3 在平衡体系中质量分数为() 考纲要求 1.了解化学平衡常数(K)的含义。 2.能利用化学平衡常数进行相关计算。 考点一化学平衡常数 1.概念 在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,用符号K表示。 2.表达式 对于反应m A(g)+n B(g)p C(g)+q D(g), K=c p?C?·c q?D? c m?A?·c n?B? (固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中)。 3.意义及影响因素 (1)K值越大,反应物的转化率越大,正反应进行的程度越大。 (2)K只受温度影响,与反应物或生成物的浓度变化无关。 (3)化学平衡常数是指某一具体反应的平衡常数。 4.应用 (1)判断可逆反应进行的程度。 (2)利用化学平衡常数,判断反应是否达到平衡或向何方向进行。 对于化学反应a A(g)+b B(g)c C(g)+d D(g)的任意状态,浓度商:Q c=c c?C?·c d?D? c a?A?·c b?B? 。 Q<K,反应向正反应方向进行; Q=K,反应处于平衡状态; Q>K,反应向逆反应方向进行。 (3)利用K可判断反应的热效应:若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。 深度思考 1.正误判断,正确的打“√”,错误的打“×” (1)平衡常数表达式中,可以是物质的任一浓度() (2)催化剂能改变化学反应速率,也能改变平衡常数() (3)平衡常数发生变化,化学平衡不一定发生移动() (4)化学平衡发生移动,平衡常数不一定发生变化() (5)平衡常数和转化率都能体现可逆反应进行的程度() (6)化学平衡常数只受温度的影响,温度升高,化学平衡常数的变化取决于该反应的反应热() 2.书写下列化学平衡的平衡常数表达式。 (1)Cl2+H2O HCl+HClO (2)C(s)+H2O(g)CO(g)+H2(g) (3)CH3COOH+C2H5OH CH3COOC2H5+H2O (4)CO2-3+H2O HCO-3+OH- (5)CaCO3(s)CaO(s)+CO2(g) 3.一定温度下,分析下列三个反应的平衡常数的关系 ①N2(g)+3H2(g)2NH3(g)K1 ②1 2N2(g)+ 3 2H2(g)NH3(g)K2 ③2NH3(g)N2(g)+3H2(g)K3 (1)K1和K2,K1=K22。 (2)K1和K3,K1=1 K3。 题组一平衡常数的含义 1.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应: 2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g)K1 2NO(g)+Cl2(g)2ClNO(g)K2 则4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(用K1、K2表示)。 2.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示: t/℃700 800 830 1 000 1 200 K0.6 0.9 1.0 1.7 2.6 化学平衡计算题求解技巧 知识体系和复习重点 一、化学平衡常数(浓度平衡常数)及转化率的应用 1、化学平衡常数 (1)化学平衡常数的数学表达式 (2)化学平衡常数表示的意义 平衡常数数值的大小可以反映可逆反应进行的程度大小,K 值越大,反应进行越完全,反应物转化率越高,反之则越低。 2、有关化学平衡的基本计算 (1)物质浓度的变化关系 反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度 其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。 (2)反应的转化率(α):α= (或质量、浓度) 反应物起始的物质的量(或质量、浓度) 反应物转化的物质的量×100% (3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论: 恒温、恒容时:;恒温、恒压时:n 1/n 2 =V 1 /V 2 (4)计算模式(“三段式”) 浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g) 起始 m n O O 转化 ax bx cx dx 平衡 m-ax n-bx cx dx A的转化率:α(A)=(ax/m)×100% C的物质的量分数:ω(C)=×100% 技巧一:三步法 三步是化学平衡计算的一般格式,根据题意和恰当的假设列出起始量、转化量、平衡量。但要注意计算的单位必须保持统一,可用mol、mol/L,也可用L。 例1、X、Y、Z为三种气体,把a mol X和b mol Y充入一密闭容器中,发生反应X + 2Y2Z,达到平衡时,若它们的物质的量满足:n(X)+ n(Y)= n (Z),则Y的转化率为() 化学平衡中转化率变化的判断技巧 () 100%() ?某反应物反应的物质的量或者物质的量浓度平衡转化率=该反应物初始的物质的量或者物质的量浓度 解转化率变化的题目时,审题过程要特别关注以下四点:一要关注化学反应是否可逆,二要关注容器是否可变,三要关注各物质的状态是否都为气体,四要关注反应两边气体体积是否相等。下面就化学平衡移动导致转化率的变化用具体实例进行分析讨论: 一、增大或减少某反应物浓度判断转化率的变化 对于可逆反应aA(g)+bB(g) cC(g)+dD(g),若增大某一反应物浓度可使另一反应物转化率增大,而 自身转化率下降。 【例1】.在557℃时,密闭容器中进行下列反应CO+H 2O CO 2+H 2。 若CO 起始浓度为2mol/L (1),水蒸气浓度为3mol/L (2),达到平衡时,测得CO 2的浓度为1.2mol/L 。求CO 及H 2O 的转化率。 分析:在掌握起始浓度、转化率、平衡浓度之间的关系和正确理解转化率概念的基础上,抓住转化浓度,利用常规解题方法。 CO + H 2O (g) CO 2 + H 2 起始浓度 mol/L 2 3 0 0 转化浓度 mol/L 1.2 1.2 1.2 1.2 平衡浓度 mol/L 0.8 1.8 1.2 1.2 所以,CO 的转化率= 1.2100%2?=60% ; H 2O (气)的转化率=1.2100%3 ?=40% 【例2】.若将例1中的划线部分(2)改成水蒸气浓度为6mol/L ,而其他条件不变,达到平衡时,测得CO 2的浓度为1.5mol/L 。同样按上述方法求算,可得CO 转化率为75%,H 2O 的转化率为25%。 【例3】.若将例1中的划线部分(1)改成CO 起始浓度为1mol/L ,而其他条件不变,达到平衡时,测得CO 2的浓度为0.75mol/L 。同样按上述方法求算,可得CO 转化率为75% ,H 2O 的转化率为25%。 以上三小题转化率可归纳为: 化学平衡 基础知识 一、化学平衡状态标志 1、速率标志: 2、含量标志 3、特殊标志:P M ρ 二、平衡移动方向 浓度 温度 压强 三、化学平衡图像 (1)浓度—时间 如A(g)+B(g)AB(g) (2)含量—时间—温度(压强) (C%指产物的质量分数,B%指某反应物的质量分数) (3)恒压(或恒温)线 (α表示反应物的转化率,c 表示反应物的平衡浓度) 图①,若p 1>p 2>p 3,则正反应为气体体积减小的反应,ΔH <0; 图②,若T 1>T 2,则正反应为放热反应。 四、化学平衡计算 m A(g)+n B(g) p C(g)+q D(g),令A 、B 起始物质的量浓度分别为a mol·L -1、b mol·L -1,达到平衡后消耗A 的物质的量浓度为mx mol·L -1。 m A(g)+n B(g) p C(g)+q D(g) c 始/(mol·L -1) a b 0 0 c 转/(mol·L - 1) mx nx px qx c 平/(mol·L - 1) a -mx b -nx px qx 明确三个量的关系 (1)三个量:即起始量、变化量、平衡量。 (2)关系 ①对于同一反应物,起始量-变化量=平衡量。 ②对于同一生成物,起始量+变化量=平衡量。 ③各转化量之比等于各反应物的化学计量数之比。 掌握四个公式 (1)反应物的转化率=n (转化)n (起始)×100%=c (转化)c (起始) ×100%。 (2)混合物组分的百分含量=平衡量平衡时各物质的总量 ×100%。 (3)某组分的体积分数=某组分的物质的量混合气体总的物质的量 。 ⑷P 平/P 初=n 平/n 初 ⑸温度不变K 值相等 ⑹已知平衡时物质的量或浓度(注意如何从图像中找平衡量:横坐标为时间的转折点为平衡 化学平衡常数练习 一、单选题 1.在一密闭容器中,反应aX(g)+bY(g)cZ(g)达到平衡时平衡常数为K1;在温度不变得条件下向容器中通入一定量得X与Y气体,达到新得平衡后Z得浓度为原来得1、2倍,平衡常数为K2,则K1与K2得大小关系就是( ) A.K1<K2?B.K1=K2?C.K1〉K2D。无法确定 2.在300 mL得密闭容器中,放入镍粉并充入一定量得CO气体,一定条件下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应平衡常数与温度得关系如下表: 下列说法不正确得就是( ) A.上述生成Ni(CO)4(g)得反应为放热反应 B。在25 ℃时,反应Ni(CO)4(g)?Ni(s)+4CO(g)得平衡常数为 2×10-5 C.在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均为0、5 mol·L-1,则此时v正>v逆 D.在80 ℃达到平衡时,测得n(CO)=0、3 mol,则Ni(CO)4得平衡浓度为2 mol·L-1 3.在一定温度下,改变反应物中n(SO2),对反应2SO2(g)+O2(g)?2SO3(g) ΔH<0得影响如图所示,下列说法正确得就是() A。反应b?c点均为平衡点,a点未达到平衡且向正反应方向进行B.a?b?c三点得平衡常数Kb>K c〉K a C.上述图象可以得出SO2得含量越高得到得混合气体中SO3得体积分数越高 D.a?b?c三点中,a点时SO2得转化率最高 4。下列关于化学平衡常数得说法中,正确得就是() A。可以用化学平衡常数来定量描述化学反应得限度 B.在平衡常数表达式中,反应物浓度用起始浓度表示,生产物浓度用平衡浓度表示 C.平衡常数得大小与浓度、压强、催化剂有关 D.化学平衡发生移动,平衡常数必定发生变化 5.在一定温度下,向2L体积固定得密闭容器中加入1molHI,发生反应:2HI(g)?H2(g)+I2(g) ?H>0,测得得物质得量随时间变化如表,下列说法正确得就是() 1 2 3 化学平衡状态 1.可逆反应 (1)概念:在同一条件下,同时向正、反两个方向进行的化学反应称为可逆反应。 (2)对可逆反应概念的理解 1)可逆反应的特征:“两同”是指条件相同、同时进行。 2)表示方法:在可逆反应的化学方程式中用“”表示可逆反应。 3)可逆反应的重要特征是转化率永远不可能达到100%,也就是反应一旦开始,那 么,就不可能只存在反应物,或只存在生成物。 4)存在平衡状态 2.化学平衡状态 在一定条件下的可逆反应里,当正反应速率与逆反应速率相等时,反应混合物中各组分的浓度保持一定的状态,叫做化学平衡状态,简称化学平衡。 (1)定义中的要点关系 化学平衡的研究对象:可逆反应。 “平衡”是在一定条件下建立起来的,对于一个给定的可逆反应,若起始条件相同则平衡状态也相同,不同的起始条件,平衡状态不同。 “v(正)= v(逆)”是平衡的本质,“百分含量保持一定”,“浓度保持一定”是化学平衡的现象。 (2)化学平衡的特征 “逆”:是可逆反应。 “动”:是动态平衡。 “等”:平衡的v(正)= v(逆) >0。 “定”:平衡时组分的百分含量不变。 “变”:若改变条件,平衡可被打破,并在新的条件下建立新的化学平衡。 化学平衡的移动 A:化学平衡的移动 化学平衡是有条件的动态平衡,当影响化学平衡的条件改变时,原来的平衡被破坏,进而在新的条件下逐渐建立新的平衡,这个原平衡向新平衡的转化过程叫做化学平衡的移动。 化学平衡移动研究的对象是可逆化学反应的化学平衡状态。从正逆化学反应速率的角度来看: (1)若外界条件改变,引起v正>v逆时,正反应占优势,化学平衡向正反应方向移动; (2)若v正 化学平衡常数K(Kp)的计算和应用教学设计 广州市第三中学魏勤 高考情况分析: 在近几年全国卷中,直接计算平衡常数K的题目有8道。它们在《题型训练》中的位置分别是: 原理题1(2013全国甲卷28题)P178 原理题3(2014全国甲卷26题)P182 原理题4(2014全国乙卷28题)P183 原理题5(2015全国甲卷27题)P185(只写表达式) 原理题6(2015全国乙卷28题)P187(只写计算式) 原理题8(2016全国乙卷27题)P191 原理题11(2017全国乙卷28题)P196 原理题12(2017全国丙卷28题)P198 专题目标 习惯依赖计算器的学生,对于化学试卷中的计算有一种恐惧,经常是直接放弃,特别是二卷中的计算。平衡常数和压强平衡常数还涉及转化率等有关平衡的相关计算,既是化工生产中必须关注的,也是高考的必考考点和热点。 不管是速率、起始(或平衡)浓度(或物质的量)、转化率,还是平衡常数的计算,都涉及到三段式,这是学生最容易想到的方法。通过本训练,希望学生能够熟练应用三段式,掌握平衡常数和压强平衡常数的计算方法,从而克服对计算的恐惧心理。 引出问题1——直接利用数据或列三段式计算K或K p 例1.题型训练P182(2014全国甲卷26题)——直接代数型 在容积为的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。 回答下列问题: (1)……反应的平衡常数K1为。 (2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以 mol?L-1?s-1的平均速率降低,经10s又达到平衡。…… ②列式计算温度T是反应的平衡常数K2:。 答案:L L 【变式训练1】 上题(1)中, 若起始压强为MPa,则平衡压强p总= ;分压p(NO2)= ,p(N2O4)= ,压强平衡常数K p= 。 答案: 方法指导:根据压强平衡常数的公式,分别求出总压强分压Kp 例2.题型训练P191 (2016·新课标全国Ⅰ,27)——给出三段式部分数据 (2)CrO2-4和Cr2O2-7在溶液中可相互转化。室温下,初始浓度为 m ol·L-1的Na2CrO4溶液中c(Cr2O2-7)随c(H+)的变化如图所示。 ②用离子方程式表示Na2CrO4溶液中的转化反应 化学平衡计算的技巧 化学平衡的一般计算要采用平衡计算模式,模式中的三种量可用物质的量,物质的量浓度,对于气体,还可用体积。对于气体的相关计算,可涉及压强、体积、相对密度和平均相对分子量,故可用到相关规律,如压强比等于物质的量之比,气体体积比等于物质的量之比,质量守恒定律。采用求平均量的计算公式或三角正弦法等。 如果已知平衡时总的物质的量或总体积,或平衡时的物质的量与初始物质的量之比,或平衡时与初始的压强之比,或平衡时的平均相对分子量,则要设未知数写出模式,列代数方程式求解。若是已知平衡时的平均相对分子量,则要根据质量守恒定律列代数式求解。 例1:在容积为2 L 的恒容密闭容器中充入4 mol N 2O 3,恒温t ℃时发生反应:N 2O 3(g) N 2O(g)+O 2(g)、N 2O 3(g)+O 2(g) N 2O 5(g),达平衡时,测得c (N 2O 5)为0.7 mol / L ,c (O 2)为0.5 mol / L ,则 ( BD ) A. c (N 2O 3)=0.8 mol / L B. c (N 2O 3)=0.1 mol / L C. c (N 2O)=0.5 mol / L D. c (N 2O)=1.2 mol / L 解析: N 2O 3(g) N 2O(g)+O 2(g) N 2O 3(g) + O 2(g) N 2O 5(g) 0 0 1.2 0 1.2 1.2 1.2 0.7 0.7 0.7 1.2 1.2 0.5 0.7 c (N 2O 3)=( 42-1.2-0.7) mol / L =0.1 mol / L 例2:一定条件下,在一密闭容器中通入一定量SO 2和O 2的混合气体,发生如下反应: 。反应达平衡后SO 2、O 2和SO 3的物质的量之 比为3∶4∶6,保持其它条件不变,降低温度后达到新的平衡时,O 2和SO 3的物质的量分别是1.1 mol 和2.0 mol ,此时容器内SO 2的物质的量应是 ( A ) A . 0.7 mol B . 0.9 mol C . 1.1 mol D . 1.3 mol 解析:一法:设第一种平衡状态下O 2为x ,则SO 3为23 ,变成第二种平衡时O 2变化量 为y , 2SO 2(g )+O 2(g ) 2SO 3(g )+Q x 23 x 23x +2y =2.0 解得: x =1.2 mol y 2y x -y =1.1 y =0.1 mol 1.1 2.0 可得:2SO 2(g )+O 2(g ) 2SO 3(g )+Q 0.9 1.2 1.8 0.2 0.1 0.2 0.7 1.1 2.0 二法:用等效平衡办法,将SO 3转变为SO 2和O 2,使原初始量比相同。 2SO 2(g )+O 2(g ) 2SO 3(g ) 2SO 2(g )+O 2(g ) 2SO 3(g ) 3 4 6 x 1.1 2.0化学反应速率和平衡知识点归纳
化学平衡计算
化学平衡常数及其计算训练题
化学平衡常数及其计算
化学平衡常数和化学平衡计算练习题
化学平衡计算题求解技巧-教师
有关化学平衡常数的计算
化学平衡常数解题策略
化学平衡计算题求解技巧
(完整版)化学平衡常数及其计算
化学平衡计算题求解技巧
化学平衡中转化率的变化
化学平衡解题技巧
化学平衡常数及计算练习(附答案)
高中化学平衡总结
平衡常数K(Kp)的计算和应用
化学平衡计算的技巧
