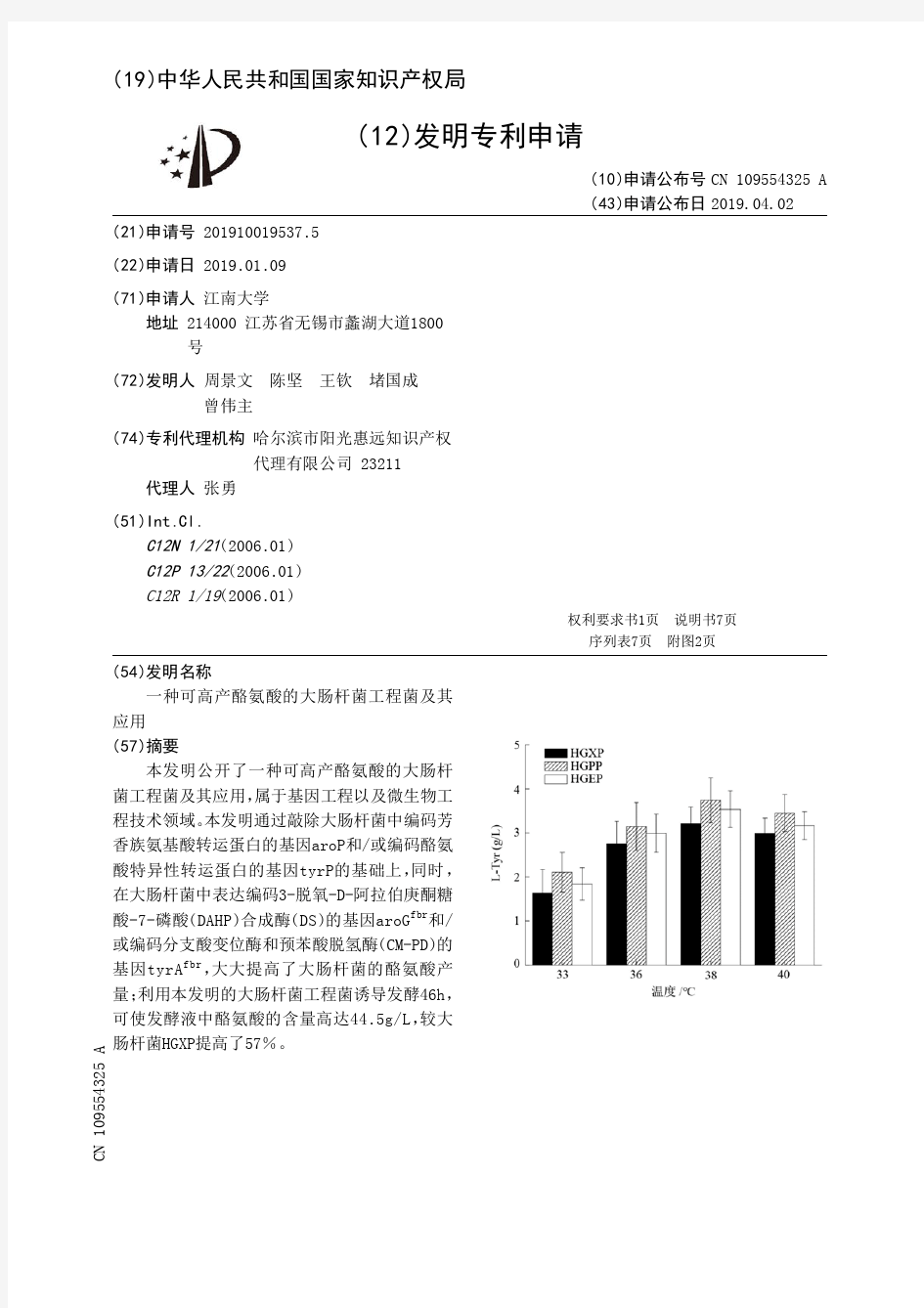
【CN109554325A】一种可高产酪氨酸的大肠杆菌工程菌及其应用【专利】

基因工程及其在大肠杆菌生产人干扰素中的应用
基因工程及其在大肠杆菌生产人干扰素中的应用 一、课程设计目的 了解工业生产中的新型育种技术并比较不同育种技术的优势; 学习理解基因工程育种技术及其操作原理; 研究基因工程育种技术在人干扰素生产中的创新。 二、课程设计题目描述与要求 本文介绍一种二十世纪七十年代发展起来的一种新型生物技术——基因工程,介绍其在育种中的应用。文中重点介绍了基因工程育种的一般步骤,以及近年来出现的运用基因工程进行定向育种的主要新技术:基因的定点突变,易错PCR,DAN重排及基因组重排。之后,应用基因工程育种技术重组大肠杆菌BL21(pBAI)生产人干扰素a2b, 通过优化补料分批培养时葡萄糖的流加策略,提高了hIFNa2b的表达量和表达速率。不同的葡萄糖流加方式有各自的优点,采用恒速流加葡萄糖的方式,hIFNa2b的表达量达到6 540 mg/L,高于目前已知文献中hIFNa2b的最高表达量5 200 mg/L。
三、课程设计报告内容 引言 基因工程是二十世纪七十年代发展起来的一种新型生物技术,其发展从根本上改变了生物技术的研究和开发应用模式。1972年美国的Berg和Jackson等人将猿猴病毒基因组SV 40DNA、λ噬菌体基因以及大肠杆菌半乳糖操纵子在体外重组获得成功。翌年,美国斯坦佛大学的Cohen和Boyer等人在体外构建出含有四环素和链霉素连个抗性基因的重组质粒分子,将之导入大肠杆菌后,该重组质粒得以稳定复制,并赋予受体细胞相应的抗生素抗性,由此宣告了基因工程的诞生。在二十世纪八十年代以来,随着大批大批成果的出现及应用,基因工程带来了一场新的革命。 利用这些技术,可以直接地、有针对性地在DNA分子水平上改造生物的遗传性状。通过转入外源基因,微生物和动、植物细胞可以产生出自身原来没有的蛋白质。同样,利用重组DNA技术,也可以使一些原来存在量极低但有重要工业或医学用途的小分子(抗生素)或蛋白质之外的大分子物质得以大量生产。特别是随着重组DNA技术的完善和发展,以基因水平为核心的现代分子定向育种技术越来越受到工业微生物育种学家的关注,并展示了良好的应用前景。 1、基因工程育种 基因工程育种是在基因水平上,运用人为方法将所需的某一供体生物的遗传物质提取出来,在离体条件下用适当的工具酶进行切割后,与载体连接,然后导入另一细胞,使外源遗传物质在其中进行正常复制和表达引,与前几种育种技术相比,基因工程育种技术是人们在分子生物学指导下的一种自觉的、能像工程一样可预先设计和控制的育种新技术,它可实现超远缘杂交,因而是最新最有前途的一种育种新技术。基因工程技术的全部过程一般包括目的基因DNA片段的取得、DNA片段与基因载体的体外连接、外源基因转入宿主细胞和目标基因的表达等主要环节。 1.1 基因工程育种的一般步骤是: (1)目的基因的获得:一般通过化学合成法、物理化学法(包括密度梯度离心法、单链酶法、分子杂交法)、鸟枪无性繁殖法、酶促合成法(逆转录法)、Norther
(完整版)大肠杆菌培养基配制及培养方法
大肠杆菌培养 一、菌种冻存液的制备 含有足量细菌的液体培养基离心后在沉淀中加入等量40%甘油,-80o C冻存。 二、培养基制备 LB培养基配方(胰化蛋白胨(Trypton):10 g/L;酵母提取物(Yeast Extract):5 g/L;NaCl:10 g/L;pH 7.4) 液体培养基 胰化蛋白胨 10.0g 酵母粉 5.0g 氯化钠 10.0g 水 1000ml pH 7.4 固体培养基在液体培养基的基础上再加入1.5%-2.0%的琼脂 三、平板的制备 1)称取胰化蛋白胨10.0g,酵母粉5.0g,NaCl 10.0g,加入800mL二次水溶解,并用玻璃棒搅拌均匀,用1mol/L的NaOH调pH至7.4左右,定容至1L,调pH 7.4(若溶液pH大于7.4,用1mol/L HCl回调)。 2)分装在锥形瓶中,每瓶量不宜太多,没过瓶底一指左右。如需固体培养基在分装后的液体培养基内加入约2%的琼脂(150mL液体培养基加入2.5g琼脂)。3)在锥形瓶口依次覆盖带滤纸通气小孔的塑料膜和硬质纸,用皮筋捆好。所有锥形瓶如上述操作。用记号笔注明培养基名称、配制日期。 4)高压蒸汽灭菌锅121 oC灭菌15min。 5)灭菌后的培养基取出置电热鼓风干燥器内60oC烘干,待锥形瓶的封口纸干燥后取出。液体培养基可直接保存或使用,此时加有琼脂的培养基不会凝固,可在预先紫外杀菌30min以上的无菌操作台上,将培养基倒入培养皿内,每个培养皿培养基约10-15mL(直径90mm),在培养皿中厚度大约4mm左右。将平皿叠放在无菌操作台上,放置10min左右,待琼脂基本凝固可涂平板。6)若平板不直接使用,灭菌后将培养基在锥形瓶中保存,待需制备平板时,微波炉中火加热约3min,使琼脂熔化,室温冷却20min至不烫手可制备平板。 四、接种大肠杆菌 1)取实验室储备的大肠杆菌BL21冻存液,管口用酒精灯灼烧,打开离心管。2)接种方法一:用灭菌枪头蘸取冻存液在平板边缘上划横条,每三道为一组,旋转平皿一圈,最后中间划之字;接种方法二:用移液枪吸取100uL溶液于平板上,用酒精灯灭菌厚的涂抹棒划十字,涂布平板。 3)因实验一般都要求挑取单菌落,故涂平板适应考虑冻存液内细菌数量,若菌量过大应适当稀释。一般方法一获得单菌落的可能性比较大。涂平板应在酒
最新大肠杆菌发酵经验总结
大肠杆菌发酵经验总结 首先,补料速率与比生长速率直接影响着乙酸的生成速率和积累量(主要是补料速率与比生长速率影响发酵液中的残糖量,进而影响),所以适当的控制补料速率和比生长速率,对于控制乙酸的量有很好的效果。 其次,必须要保证充足的溶氧,并严格控制pH值,而且补酸碱的速率尽量缓和,不能太快;温度对于蛋白的表达也有很重要的影响,较低的发酵温度下所生产出的蛋白大多是有活性的,而较高的发酵温度下产生的蛋白大多一包涵体形式存在。 第三,选取合理的诱导时间非常重要,一般的诱导时间选在指数生长后期,而且诱导时的比生长速率最好能控制在0.2之内,选在此时诱导,1.将菌体的快速生长期与蛋白合成期分开,使这两个阶段互不影响,有利于蛋白的高表达;2.已经得到了大量的菌体,而且菌体的生物量基本接近稳定,不论是从动力学角度,还是能耗,物料成本方面,都比较合理。 第四,补料过程中的碳氮比也很重要。若氮源过高,会使菌体生长过于旺盛,pH偏高,不利于代谢产物的积累,氮源不足,则菌体繁殖量少从而影响产量;碳源过多,则容易刑场较低的pH,抑制菌体生长,碳源不足,则容易引起菌体的衰老和自溶。另外,碳氮比不当还会引起菌体按比例的吸收营养物质,从而直接影响菌体的生长和产物的合成。 根据自己的经验,一般情况下,对于一个稳定的发酵工艺下,如果总是在固定的发酵时间段出现溶菌现象,而且能排除噬菌体和染菌的可能性后,那就可能是因为碳氮比不合理造成的。可以适当调整碳氮比。 大家讨论得较多的是关于代谢副产物乙酸对大肠杆菌发酵的影响,针对我们论坛所发的帖,我先总结以下几点,并作出相应解决措施。 一、代谢副产物-乙酸 乙酸是大肠杆菌发酵过程中的代谢副产物,在多大的浓度下产生抑制作用各种说法不一,一般认为在好气性条件下,5~10g/L 的乙酸浓度就能对滞后期、最大比生长速率、菌体浓度以及最后蛋白收率等都产生可观测到的抑制作用。当乙酸浓度大于10或20g/L 时,细胞将会停止生长,当培养液中乙酸浓度大于12g/L 后外源蛋白的表达完全被抑制。 预防乙酸产生的措施: 1、通过控制比生长速率来减少乙酸的产生: 比生长速率越高,乙酸产生越多,当比生长速率超过某个值时,乙酸开始产生。可以通过降低温度,调节酸碱度,控制补料等方法来降低比生长速率。 2、透析培养: 在大肠杆菌的培养过程中可以用透析技术除去发酵液中的有害物质,降低乙酸含量从而实现重组菌的高密度发酵和产物的表达。 3、控制葡萄糖的浓度: 葡萄糖是大肠杆菌发酵过程中重要的碳源之一,用其作碳源是要将其控制在一个较低的水平上,以减少乙酸的产生。 常用的控制方法主要有: 恒pH法:大肠杆菌会代谢葡萄等产生乙酸,使pH 值下降。因此可通过pH值的高低作为控制葡萄糖的指标,该法的缺点是pH 的变化不完全是由葡萄糖代谢的结果,容易造成补料体系出错。恒溶氧法:菌体代谢时会消耗氧,使溶氧下降,当葡萄糖浓度低到一定程度时菌体代谢下降,消耗氧能力下降,溶氧上升。因此,根据溶氧曲线补加葡萄糖,保持溶氧恒定,可以控制葡萄糖在一定的水平。 二、温度 大肠杆菌发酵最适温度是37 C,当温度最适菌体生长时,比增长速率将会增大。随温度上升细
大肠杆菌基因工程菌常用类型
1、大肠杆菌DH5a菌株 DH5a是世界上最常用的基因工程菌株之一。由于DH5α是DNA酶缺陷型菌株,有利于基因克隆,保存质粒,但该菌株的蛋白酶没有缺陷,表达的蛋白容易被降解,因此通常不作为表达菌株。E.coli DH5a在使用pUC系列质粒载体转化时,可与载体编码的β-半乳糖苷酶氨基端实现α-互补。可用于蓝白斑筛选鉴别重组菌株。 基因型:F-,φ80dlacZΔM15,Δ(lacZYA-argF)U169,deoR,recA1,endA1,hsdR17(rk-,mk+),phoA,supE44,λ-,thi-1,gyrA96,relA1 2、大肠杆菌BL21(DE3) 菌株 该菌株用于高效表达克隆于含有噬菌体T7启动子的表达载体(如pET系列)的基因。T7噬菌体RNA聚合酶位于λ噬菌体DE3区,该区整合于BL21的染色体上。该菌适合表达非毒性蛋白。 基因型:F-,ompT,hsdS(rBB-mB-),gal,dcm(DE3) 3、大肠杆菌BL21(DE3) pLysS菌株 该菌株含有质粒pLysS,因此具有氯霉素抗性。PLysS含有表达T7溶菌酶的基因,能够降低目的基因的背景表达水平,但不干扰目的蛋白的表达。该菌适合表达毒性蛋白和非毒性蛋白。 基因型:F-,ompThsdS(rBB-mB-),gal,dcm(DE3,pLysS,Camr 4、大肠杆菌JM109菌株 该菌株在使用pUC系列质粒载体进行DNA转化或用M13 phage载体进行转染时,由于载体DNA产生的LacZa多肽和JM09编码的LacZΔM15进行α-互补,从而显示β-半乳糖苷酶活性,由此很容易鉴别重组体菌株。 基因型:recA1,endA1,gyrA96,thi-1,hsdR17,supE44,relA1,Δ(lac-proAB)/F’[traD36,proAB+,lacIq,lacZΔM15] 5、大肠杆菌TOP10菌株 该菌株适用于高效的DNA克隆和质粒扩增,能保证高拷贝质粒的稳定遗传。 基因型:F- ,mcrAΔ(mrr-hsd RMS-mcrBC),φ80 ,lacZΔM15,△lacⅩ74,recA1 ,araΔ139Δ(ara-leu)7697,galU,galK,rps,(Strr) endA1,nupG 6、大肠杆菌HB101菌株 该菌株遗传性能稳定,使用方便,适用于各种基因重组实验。 基因型:supE44,hsdS20(rB-mB-),recA13,ara-14,proA2,lacY1,galK2,rpsL20,xyl-5,mtl-1,leuB6,thi-1 7.XL10-Gold菌株:所制备的感受态细胞是目前转化效率最高的感受态细胞,缺失几乎所有已知的限制酶切系统;同时缺失核酸内切酶(endA),提高了质粒DNA的产量和质量;重组酶缺陷型(recA)减少插入片段的同源重组概率,保证了插入DNA的稳定性,提高感受态转化效率及大质粒转化能力的宿主菌基因型。
重组人IL-2大肠杆菌工程菌质粒稳定性的研究
重组人IL-2大肠杆菌工程菌质粒稳定性的研究 摘要 基因工程菌中质粒稳定性对于基因工程菌的发酵有着重要影响,但基因工程菌在传代中经常出现质粒不稳定遗传的现象。本试验通过在工程菌的培养过程中添加抗生素这一选择压力和诱导表达目的蛋白的方式来提高基因工程菌的稳定性,并通过双酶切电泳分析及高效率的诱导表达外源蛋白来进行检测,得出工程菌在LB(-)和LB(+)平板上都能生长且形态相似;电泳图平行、酶切片段的位置大致一致;诱导表达的外源基因的质粒稳定。提高质粒稳定性有利于外源蛋白表达,以满足大规模生产发酵。 关键词:基因工程菌;质粒;稳定性 -I-
Study on the stability of plasmid of recombinant human IL-2 E.coli bacteria Abstract Escherichia coli. plasmid stability for the genetic engineering of bacteria fermentation has important implications genetically engineered bacteria in the mid-recurring genetic instability of the plasmid. This experiment in engineering from the training course to add the option of antibiotic pressure and protein expression induced by way of reference high genetically engineered bacteria stability and digested by electrophoresis and high efficiency induced expression of foreign proteins to detect, the virus can grow in the panel of LB(-) and LB(+), and the morphology is similar; The electrophoregram is parallel, and the position of the fragment is consistenct roughly; Inducible expression of foreign genes is stabile. We improve the stabilization of the foreign gene in order to meet the large-scale fermentation. Key words: Genetic engineering ; plasmid ; stability -II-
大肠杆菌发酵经验总结
大肠杆菌发酵经验总结-CAL-FENGHAI.-(YICAI)-Company One1
大肠杆菌发酵经验总结 大肠杆菌发酵经验总结 首先,补料速率与比生长速率直接影响着乙酸的生成速率和积累量(主要是补料速率与比生长速率影响发酵液中的残糖量,进而影响),所以适当的控制补料速率和比生长速率,对于控制乙酸的量有很好的效果。 其次,必须要保证充足的溶氧,并严格控制pH值,而且补酸碱的速率尽量缓和,不能太快;温度对于蛋白的表达也有很重要的影响,较低的发酵温度下所生产出的蛋白大多是有活性的,而较高的发酵温度下产生的蛋白大多一包涵体形式存在。 第三,选取合理的诱导时间非常重要,一般的诱导时间选在指数生长后期,而且诱导时的比生长速率最好能控制在之内,选在此时诱导,1.将菌体的快速生长期与蛋白合成期分开,使这两个阶段互不影响,有利于蛋白的高表达;2.已经得到了大量的菌体,而且菌体的生物量基本接近稳定,不论是从动力学角度,还是能耗,物料成本方面,都比较合理。 第四,补料过程中的碳氮比也很重要。若氮源过高,会使菌体生长过于旺盛,p H偏高,不利于代谢产物的积累,氮源不足,则菌体繁殖量少从而影响产量;碳源过多,则容易刑场较低的pH,抑制菌体生长,碳源不足,则容易引起菌体的衰老和自溶。另外,碳氮比不当还会引起菌体按比例的吸收营养物质,从而直接影响菌体的生长和产物的合成。 根据自己的经验,一般情况下,对于一个稳定的发酵工艺下,如果总是在固定的发酵时间段出现溶菌现象,而且能排除噬菌体和染菌的可能性后,那就可能是因为碳氮比不合理造成的。可以适当调整碳氮比。 大家讨论得较多的是关于代谢副产物乙酸对大肠杆菌发酵的影响,现总结以下几点,并作出相应解决措施。 一、代谢副产物-乙酸 乙酸是大肠杆菌发酵过程中的代谢副产物,在多大的浓度下产生抑制作用各种说法不一,一般认为在好气性条件下,5~10g/L 的乙酸浓度就能对滞后期、最大比生长速率、菌体浓度以及最后蛋白收率等都产生可观测到的抑制作用。当
质粒转化大肠杆菌
质粒DNA的转化操作步骤 该实验主要有两个用途: 1.重组质粒的鉴定。当质粒的重组或其它载体重组后,通常会发生质粒的重组失败,包括质粒的自身环化。因而要求进行筛选,把重组成功的质粒找出来。在目前常用的质粒和其它载体中含有相应的抗生素抗性基因,一旦重组成功,质粒环化(包括自身环化),抗生素抗性基因表达,被转化的大肠杆菌便具备抗相应抗生素的能力,可以含该抗生素的培养基中生长传代,不然,重组失败,大肠杆菌便不能抵抗该抗生素而死亡。 2.为扩增质粒和其它载体作准备。由于大肠杆菌繁殖快,在适宜的条件下繁殖一代仅需要20~30分钟,而且常用质粒可以在大肠杆菌中达到几百个拷贝,因此,通过对转化成功的大肠杆菌培养,可以在短时内极大地扩增目的质粒。(作为分子生物学用大肠杆菌,是经过实验室改造过的工程菌。) 【原理】 转化是将外源DNA分子导入到受体细胞,使之获得新的遗传特性的一种方法。转化所用的受体细胞一般是限制-修饰系统缺陷变异株,即不含限制性内切酶和甲基化酶(R-, M-)。将对数生长期的细菌(受体细胞)经理化方法处理后,细胞膜、的通透性发生暂时性改变,成为能允许外源DNA分子进入的感受态细胞。进入受体细胞的DNA分子通过复制和表达实现信息的转移,使受体细胞具有了新的遗传性状。将经过转化的细胞在筛选培养基上培养,即可筛选出转化子(带有异源DNA分子的细胞)。 本实验采用CaCl2法制备感受态细胞。其原理是细胞处于0~4℃,CaCl2低渗溶液中,大肠杆菌细胞膨胀成球状。转化混合物中的DNA形成抗DNA酶的羟基-钙磷酸复合物粘附于细胞表面,经42℃90秒热激处理,促进细胞吸收DNA得合物。将细菌放置在非选择性培养基中(无抗LB培养液)于37℃振动培养一段时间,可使细菌复苏,表达质粒编码的抗生素抗性基因,在转化过程中获得的新的表型,提高转化效率。如氨苄青霉素耐药(Ampr)得到表达,然后将此细菌培养物涂在含Amp的选择性培养基上,倒置培养过夜,即可获得细菌菌落。 本实验是将[ 某]重组质粒转化DH5α扩增菌,转化后在含Amp的培养基上进行筛选,生长的菌落即为含重组质粒的工程菌。含[ 某]重组质粒的DH5α菌用于质粒DNA的扩增,获得的质粒将作为限制性内切酶的酶切底物DNA。 【实验步骤】 自-70℃冰箱中取出受感态大肠杆菌,插入湿冰中溶解约15分钟,轻轻混匀。吸取50ul移入1.5ml管,并立刻将细菌放回-70℃冰箱。 细菌50 ul 质粒1 ul 轻轻混匀,静置冰上30分钟。 于42℃水浴中热休克细菌90秒,迅速移入湿冰中,静置3分钟,加入700ul无抗LB 培养液,放入37℃恒温箱摇床,220rpm摇晃培养45min。取30-200ul涂于含氨卞青霉素的LB琼脂平板皿上,待干燥后,倒置,存放于37℃的培养箱中过夜。 次日,检查各培养皿中是否出现菌落。
大肠杆菌发酵经验总结
大肠杆菌发酵经验总结 大肠杆菌发酵经验总结 首先,补料速率与比生长速率直接影响着乙酸的生成速率和积累量(主要是补料速率与比生长速率影响发酵液中的残糖量,进而影响),所以适当的控制补料速率和比生长速率,对于控制乙酸的量有很好的效果。 其次,必须要保证充足的溶氧,并严格控制pH值,而且补酸碱的速率尽量缓和,不能太快;温度对于蛋白的表达也有很重要的影响,较低的发酵温度下所生产出的蛋白大多是有活性的,而较高的发酵温度下产生的蛋白大多一包涵体形式存在。 第三,选取合理的诱导时间非常重要,一般的诱导时间选在指数生长后期,而且诱导时的比生长速率最好能控制在0.2之,选在此时诱导,1.将菌体的快速生长期与蛋白合成期分开,使这两个阶段互不影响,有利于蛋白的高表达;2.已经得到了大量的菌体,而且菌体的生物量基本接近稳定,不论是从动力学角度,还是能耗,物料成本方面,都比较合理。 第四,补料过程中的碳氮比也很重要。若氮源过高,会使菌体生长过于旺盛,pH偏高,不利于代产物的积累,氮源不足,则菌体繁殖量少从而影响产量;碳源过多,则容易刑场较低的pH,抑制菌体生长,碳源不足,则容易引起菌体的衰老和自溶。另外,碳氮比不当还会引起菌体按比例的吸收营养物质,从而直接影响菌体的生长和产物的合成。 根据自己的经验,一般情况下,对于一个稳定的发酵工艺下,如果总是在固定的发酵时间段出现溶菌现象,而且能排除噬菌体和染菌的可能性后,那就可能是因为碳氮比不合理造成的。可以适当调整碳氮比。 大家讨论得较多的是关于代副产物乙酸对大肠杆菌发酵的影响,现总结以下几点,并作出相应解决措施。 一、代副产物-乙酸 乙酸是大肠杆菌发酵过程中的代副产物,在多大的浓度下产生抑制作用各种说法不一,一般认为在好气性条件下,5~10g/L 的乙酸浓度就能对滞后期、最大比生长速率、菌体浓度以及最后蛋白收率等都产生可观测到的抑制作用。当乙酸浓度大于10或20g/L 时,细胞将会停止生长,当培养液中乙酸浓度大于12g/L 后外源蛋白的表达完全被抑制。 预防乙酸产生的措施:
大肠杆菌培养方法
大肠菌群测定的操作细则 大肠菌群系指一群能发酵乳糖、产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。该菌主要来于人畜粪便,故以此作为粪便污染指标来评价食品的卫生质量,推断食品中有否污染肠道致病菌的可能。食品中大肠菌群数系以100mL(g)检样内大肠菌群最可能数(MPN)表示。 1 设备和材料 1.1 温箱:36±1℃。 1.2 冰箱:0~4℃。 1.3 恒温水浴:44.5±0.5℃。 1.4 天平。 1.5 显微镜。 1.6 均质器或乳钵。 1.7 平皿:直径为90mm。 1.8 试管。 1.9 吸管。 1.10 广口瓶或三角烧瓶:容量为500mL。 1.11 玻璃珠:直径约5mm。 1.12 载玻片。 1.13 酒精灯。 1.14 试管架。 2 培养基和试剂 2.1 乳糖胆盐发酵管:按GB 4789.28中4.9规定。 2.2 伊红美蓝琼脂平板:按GB 4789.28中4.25规定。
2.3 乳糖发酵管:按GB 4789.28中4.10规定。 2.4 EC 肉汤:按GB 4789.28中4.11规定。 2.5 磷酸盐缓冲稀释液:按GB 4789.28中 3.22规定。 2.6 生理盐水。 2.7 革兰氏染色液:按GB 4789.28中2.2规定。 3 操作步骤 3.1 检样稀释 3.1.1 以无菌操作将检样25mL(或g)放于有225mL灭菌生理盐水或其他稀释液的灭菌玻璃瓶内(瓶内予置适当数量的玻璃珠)或灭菌乳钵内,经充分振摇或研磨做成1:10的均匀稀释液。固体检样最好用均质器,以8 000-10 000 r/min的速度处理1min,做成1:10的均匀稀释液。 3.1.2 用1mL灭菌吸管吸取1:10稀释液1mL,注入含有9mL灭菌生理盐水或其他稀释液的试管内,振摇试管混匀,做成1:100的稀释液。 3.1.3 另取1mL灭菌吸管,按上条操作依次做10倍递增稀释液,每递增稀释一次,换用1支1mL灭菌吸管。 3.1.4 根据食品卫生标准要求或对检样污染情况的估计,选择三个稀释度,每个稀释度,接种3管。3.2 乳糖发酵试验 将待检样品接种于乳糖胆盐发酵管内,接种量在1mL以上者,用双料乳糖胆盐发酵管,1mL及1mL以下者,用单料乳糖胆盐发酵管。每一稀释度接种3管,置36±1℃温箱内,培养24±2h,如所有乳糖胆盐发酵管都不产气,则可报告为大肠菌群阴性,如有产气者,则按下列程序进行。 3.3 分离培养 将产气的发酵管分别转种在伊红美蓝琼脂平板上,置36±1℃温箱内,培养18-24h,然后取出,观察菌落形态,并做革兰氏染色和证实试验。
大肠杆菌高密度培养2014018093
大肠杆菌高密度培养 生物1401谢宇忱2014018093 1大肠杆菌高密度培养的影响因素 1.1菌种 不同的E.coli菌株由于自身代谢系统的不同,在培养条件、对外界环境耐受能力等方面都存在着较大的差异。例如E.coli K系列菌株和E.coli B系列菌株均为较常用的培养菌株,进行了乙酸代谢研究,发现前者的乙酸积累仅为后者的1/4,菌体密度也高出25%。 1.2接种量 接种量会影响菌体在发酵罐中的生长速度。较大的接种量可以缩短菌体生长达到最高值的时间,这是因为种子液中含有大量胞外水解酶类,有利菌体对基质的快速充分利用,缩短生长延迟期。但是接种量过大也会使菌体生长过快,菌体生长持续的时间缩短,自溶也较快,反而影响后期的生长。 1.3培养基 高密度培养的目的是尽可能多地获得菌体生物量和表达产物,这就需要提供数倍于生物量的营养物质,才能满足菌体大量生长繁殖及分泌表达产物的需要。但基质中营养物质的浓度也不能太高,否则就会产生抑制效应,不利于高密度培养。 1.3.1碳源 不同微生物对碳源的需求各不相同,碳源的种类和浓度对菌体的生长代谢也有不同的影响。葡萄糖E.coli发酵中最常用的碳源。但以葡萄糖作为碳源易产生代谢抑制物质———乙酸,研究表明以甘油代替葡萄糖作为E.coli生长的碳源可以减少乙酸的积累,更易达到高密度。在发酵过程中补加麦芽糖和甘油,菌体密度和产物量都提高了2.5倍。 1.3.2氮源 大量研究表明应对发酵过程中的氮源加以控制,氮源浓度过高对菌体的生长和产物的表达合成都可能产生负面影响。培养E.coli时常用氨水作为主要的氮源,在培养过程中以流加的方式加入培养液,既可用来充当氮源又可用来调节发酵液的pH值,但氨水加入过多会导致细胞的产率下降。 1.3.3微量元素 E.coli对钙、钴、铁、铝、锰、锡等微量元素的需求量虽然很小,但微量元素对微生物的生长及活性所起的作用不可忽视,在高密度培养时应在培养基中添加适量的微量元素。1.4培养条件 1.4.1温度 温度对E.coli的生长繁殖有很大的影响E.coli的最适生长温度为37℃,但在近期的一些研究中,经常以低于37℃的温度来培养E.coli,当培养温度从37℃下降至30℃左右时,可使细胞的营养物摄入率和比生长速率减小,减少有害抑制产物的积累和代谢热的产生。 1.4.2溶氧 氧是一种难溶气体,常温常压下氧在纯水中的溶解度仅为7mg·L^-1。因此溶氧很容易成为E.coli高密度培养的限制因素,尤其是在高密度培养的后期,发酵液中菌体密度很大,耗氧量极大。在高密度培养时,可以通过提高发酵通气量、搅拌速度、通入纯氧等方法来控制溶氧;还可以通过使用氧溶解度高的载体来提高溶氧。 1.4.3pH值 微生物一般能够在3~4个pH值单位的范围内生长,细菌最适生长pH值为6.5~7.5,在pH值5.0以下或8.5以上就不能生长。培养液中pH值的变化会影响细胞
