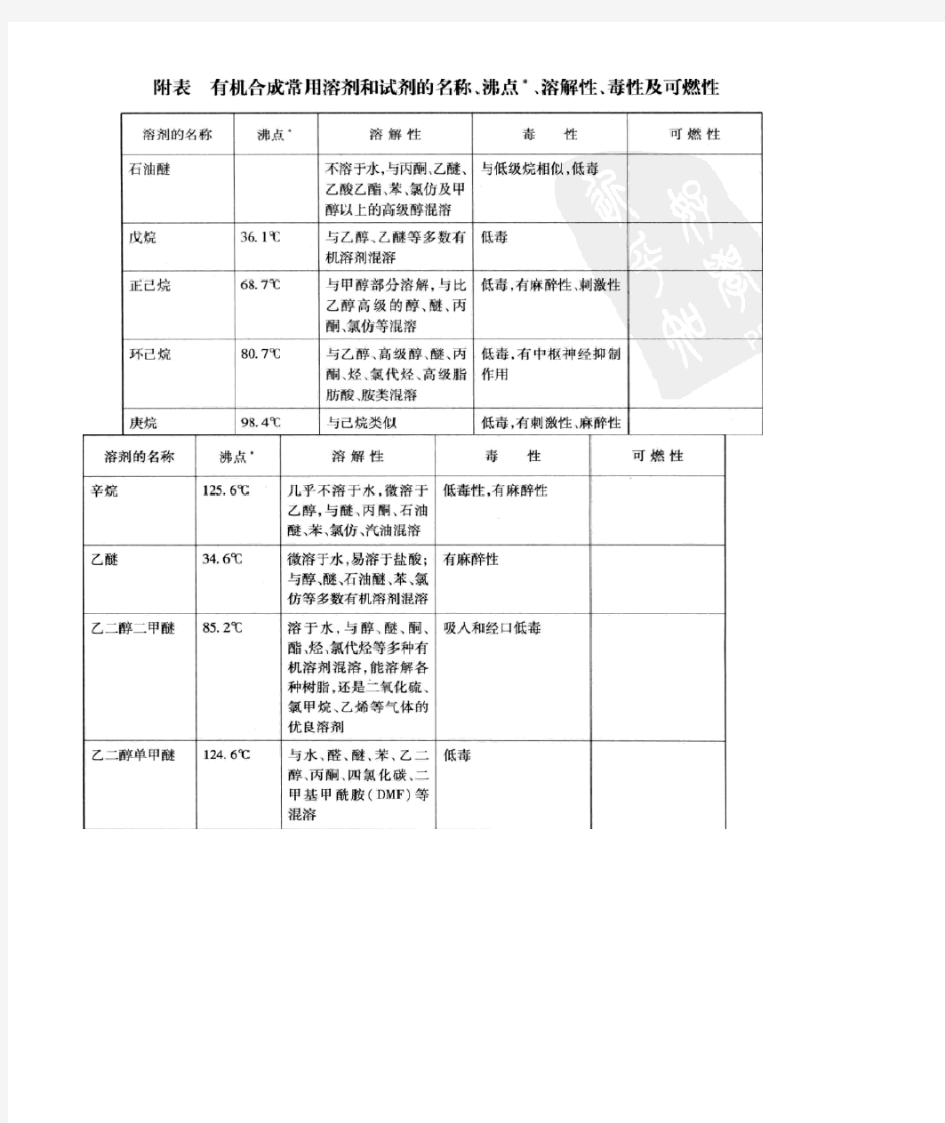
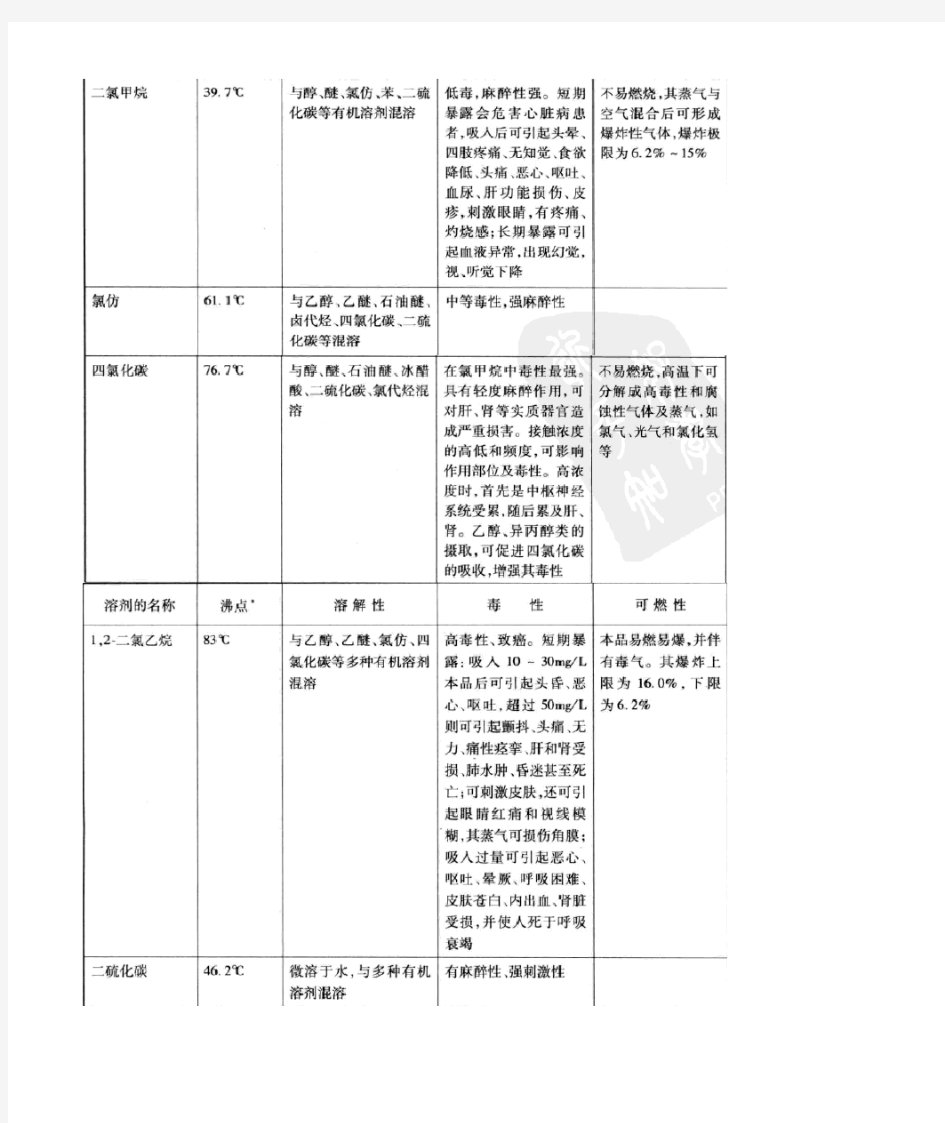
有机合成常用溶剂和试剂
转载]知识精要?化学实验常用仪器及其使用3 知识精要·化学实验常用仪器及其使用 中学化学实验常用的仪器有20多种,对这些仪器应该在反复使用和训练规范操作的基础上,努力做到“三会”,即:会识别仪器的名称和能恰当地选用仪器(仪器的种类和必要的规格);会正确地使用仪器进行实验;会画常用仪器的剖面图。 按照中学化学实验常用仪器的用途,大致可分为计量仪器、分离物质仪器、可加热的仪器、加热仪器、存放物质的仪器和其它仪器六类。现对这些仪器的名称、规格、用途和操作要领分述如下。 1.计量仪器 (1)量筒 量筒用于量度一定体积的液体。量筒的容积常见的有10mL、50mL、100mL等多种,其分度(最小刻度每格)依次为0.2mL、1mL、1mL。应该根据需要量取液体的体积大小,选用适当规格的量筒;量取液体时,以液面的弯月形最低点为准;量筒不能加热,不能作反应容器(量筒是有刻度的玻璃容器,温度的变化会使刻度不准确,且量筒受热可能引起炸裂,因此,量筒不能用做反应容器或用来稀释浓硫酸、溶解强碱,也不能量取过热的液体或用于加热等)。量取液体时,应先往量筒里注液体到接近刻度然后改用滴管,将液体逐滴加入,直到指定量。读数时量筒必须方平视线必须与量筒内液体凹液面最底处保持水平。俯视使读数偏高;仰视使读数偏低。如右图 (2)托盘天平 固体药品称量使用托盘天平,一般能精确到0.1克。 使用步骤注意事项:①先调整零点;②称量物和砝码的位置为“左物右码”;③称量物不能直接放在托盘上,干燥的药品放在洁净的纸上称量,易潮解的和有腐蚀性的药品放在小烧杯等玻璃器皿里称量;④砝码 用镊子夹取(“先大后小”)⑤称量结束后,应使游码归零,砝码放回砝码盒。 2.分离物质的仪器 漏斗漏斗内放滤纸用于过滤,也可通过漏斗向小口容器中转移液体。漏斗不能直接加热;过滤时应 固定在铁架台的铁环上或固定在漏斗架上。 3.可加热的仪器 1.试管用来盛放少量药品,常温或加热情况下进行少量试剂反应的容器,可用于制取或收集少 量气体。 使用注意事项:①可直接加热,用试管夹夹在距试管口1/3管长处。②加热后不能骤冷,防止炸裂。③加热时试管口不能对着任何人;给固体加热时,试管要横放,管口略向下倾斜。 ④加入试管内的液体,不加热时不超过试管容积的l/2,加热时不超过l/3。 2.烧杯用作配置溶液和加大试剂的反应容器,在常温或加热时使用。 使用注意事项:①烧杯外壁擦干后方可用于加热,加热时应放置在石棉网上,使受热均匀,盛放液体的容量通常不超过容积的1/3。②溶解物质搅拌时,玻璃棒不能触及杯壁或杯底。 3.烧瓶用于试剂量较大而又有液体物质参加反应的容器,还可制作洗瓶。可分为圆底烧瓶、平底烧瓶和蒸馏烧瓶。它们都可用于装配气体发生装置。蒸馏烧瓶用于分离互溶的沸点不同的物质。 使用注意事项:①圆底烧瓶和蒸馏烧瓶可用于加热,加热时要垫石棉网,也可用于其它热浴(如水浴加热等)。②液体加入量不要超过烧瓶容积的1/2。③使用时(制气体或有机 合成等),应固定在铁架上,烧瓶夹应垫石棉绳或套橡皮管。 4.蒸发皿用于蒸发液体或浓缩溶液。 使用注意事项:①可直接加热,但不能骤冷。②盛液量不应超过蒸发皿容积的2/3. ③
溶剂危害性分类 一类溶剂:应避免 致癌物;备受怀疑的致癌物;环境危害物 二类溶剂:设定残余量,限量使用 非基因性动物致癌物;可能导致不可逆中毒,比如神经性中毒,畸形;可能导致其他可逆性中毒 三类溶剂: 低毒 对人体有潜在毒性,可以接触,但不超过50mg/day。 Solvent Other Names Structure Class Acetic acid Ethanoic acid CH3COOH三类溶剂 2-Propanone Acetone CH3COCH3三类溶剂 Propan-2-one Acetonitrile CH3CN二类溶剂 Anisole Methoxybenzene三类溶剂 Benzene Benzol一类溶剂 n-Butyl alcohol 1-Butanol CH3(CH2)3OH三类溶剂 Butan-1-ol sec-Butyl alcohol 2-Butanol CH3CH2CH(OH)CH3三类溶剂 Butan-2-ol Butyl acetate Acetic acid butyl ester CH3COO(CH2)3CH3三类溶剂 tert-Butylmethyl ether2-Methoxy-2-methyl- propane(CH3)3COCH3三类溶剂Carbon tetrachloride Tetrachloromethane CCl4一类溶剂 Chlorobenzene二类溶剂Chloroform Trichloromethane CHCl3二类溶剂 Isopropylbenzene Cumene 三类溶剂 (1-Methyl)ethylbenzene Cyclohexane Hexamethylene二类溶剂 1,2-Dichloroethane sym-Dichloroethane CH2ClCH2Cl一类溶剂
专题有机合成题的一般解题方法 【复习目标】熟悉有机合成中需要具备的基础知识(有机物的组成、结构、性质、相互衍生关系,官能团的引入和消去,碳链的增减,官能团的保护等),掌握有机合成的思路方法。 【机化学基础(选修5,人教版)P64-65:以有机反应为基础的有机合成,是有机化学的一个重要内容。它是利用简单、易得的原料,通过有机反应,生成具有特定结构和功能的有机化合物。有机合成的任务包括目标化合物分子骨架的构建和官能团的转化,其过程就象建筑师建造一座大厦,从基础开始一层一层地向上构建。利用简单的试剂作为基础原料,通过有机反应连上一个官能团或一段碳链,得到一个中间体;在此基础上利用中间体上的官能团,加上辅助原料,进行第二步反应,合成出第二个中间体……经过多步反应,按照目标化合物的要求,合成具有一定碳原子数目、一定结构的目标化合物。 逆合成分析法是在设计复杂化合物的合成路线时常用的方法,它是将目标化合物倒退一步寻找上一步反应的中间体,该中间体同辅助原料反应可以得到目标化合物。而这个中间体的合成与目标化合物的合成一样,是从更上一步的中间体得来的。依次倒推,最后确定最适宜的基础原料和最终的合成路线。所确定的合成路线的各步反应其反应条件必须比较温和,并具有较高的产率,所使用的基础原料和辅助原料应该是低毒性、低污染、易得和廉价的。】 (一)有机物合成的基础知识 1.有机合成中官能团的引入和消去 (1)在分子中引入官能团的方法 ①引入卤原子 a.烯烃、炔烃的加成反应 b.取代反应 ②引入羟基 a.加成反应(烯加水、醛酮加氢) b.水解反应酯的水解 ③引入双键 a.加成反应(炔烃的加氢) b.消去反应(卤代烃、醇的消去) ④引入醛基或酮基:由醇羟基通过氧化反应可得到醛基或酮基。 (2)从分子中消除官能团的方法 ①经加成反应消除不饱和键 ②经取代、消去、酯化、氧化等反应消去-OH ③经加成或氧化反应消除-CHO ④经水解反应消去酯基。 ⑤经过水解、消去反应消去-X 2.有机合成中碳链的增减 (1)增长碳链的方法:①不饱和化合物间的加成、聚合(如乙烯→聚乙烯)、不饱和烃与HCN的加成后水解等。②酯化反应(如乙酸与乙醇转化为乙酸乙酯等)。③有机合成题中碳链的增长,也有可能以信息给出,此类问题中应高度重视反应物与产物中的碳原子数的比较及连接位置关系等。 (2)缩短碳链的方法,其方法主要有:①烃的裂化裂解(石油的裂化、裂解)。②某些烃的氧化(如苯的同系物、烯烃等)。③羧酸的脱羧反应。④酯的水解反应 3. 有机合成中官能团的保护 在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下产生副反应,这样就不能达到预计的合成目标,因此,必须采取措施保护某些官能团,待完成反应后再除去保护基,使其复原。(备考指南P125-6) 例如为防止一OH被氧化可先将其酯化,为保护C=C不受氧化可先将其与HBr加成或与水加成,在含有C=C和-CHO的化合物中欲用溴水检验C=C,应先将-CHO用弱氧化剂(银氨溶液、新制Cu(OH)2氧化)等。 (二)有机物合成的途径 (1)一元合成路线:RCH=CH2→一卤代烃→一元醇→一元醛→一元羧酸→酯 (2)二元合成路线:RCH=CH2→二卤代烃→二元醇→二元醛→二元羧酸→酯(链酯、环酯、 —CH3—CH2Cl —CH2OH —COOH
化学实验常见仪器 各种化学仪器都有一定的使用范围。有的玻璃仪器可以加热用,如试管、烧杯、烧瓶、蒸发皿等;有的不能加热,如量筒、集气瓶、水槽等。有的仪器可以做量具用。有的仪器在实验装置中起支撑作用。有些仪器外观很相似,容易混淆,应该通过对比加以分辨。化学仪器在做化学实验时经常用到,学会正确使用这些仪器的方法,是十分重要的。每种仪器,根据它的用途不同,有着不同的使用要求。因此,在使用各种化学仪器前都应该明确它的要求及这种要求的原因。 一.容器与反应器 1.可直接加热 (1)试管 主要用途: ①常温或加热条件下,用作少量试剂的反应容器。 ②收集少量气体和气体的验纯。 使用方法及注意事项: ①可直接加热,用试管夹夹住距试管口1/3处。
②试管的规格有大有小。试管内盛放的液体不超过容积1/3。 ③加热前外壁应无水滴;加热后不能骤冷,以防止试管破裂。 ④加热时,试管口不应对着任何人。给固体加热时,试管要横放,管口略向下倾斜。 ⑤不能用试管加热熔融NaOH等强碱性物质。 (2)蒸发皿 主要用途: ①溶液的蒸发、浓缩、结晶。 ②干燥固体物质。 使用方法及注意事项: ①盛液量不超过容积的2/3。 ②可直接加热,受热后不能骤冷。 ③应使用坩埚钳取放蒸发皿。 2.垫石棉网可加热
(1)烧杯 主要用途: ①用作固体物质溶解、液体稀释的容器。 ②用作较大量试剂发生反应的容器。 ③冷的干燥的烧杯可用来检验气体燃烧有无水生成;涂有澄清石灰水的烧杯可用来检验CO2气体。 使用方法及注意事项: ①常用规格有50mL、100mL、250mL等,但不用烧杯量取液体; ②应放在石棉网上加热,使其受热均匀;加热时,烧杯外壁应无水滴。 ③盛液体加热时,一般以不要超过烧杯容积的1/2为宜。 ④溶解或稀释过程中,用玻璃棒搅拌时,不要触及杯底或杯壁。 (2)烧瓶 主要用途:
常用有机溶剂分类及干燥 第一类溶剂 是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。在可能的情况下,应避免使用这类溶剂。如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如: 苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。 第二类溶剂 是指无基因毒性但有动物致癌性的溶剂。按每日用药10克计算的每日允许接触量如下: 2-甲氧基乙醇(50ppm)、氯仿(60ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、1,2,3,4-四氢化萘(100ppm)、2-乙氧基乙醇(160ppm)、环丁砜(160ppm)、嘧啶(200ppm)、甲酰胺(220ppm)、正己烷(290ppm)、氯苯(360ppm)、二氧杂环己烷(380ppm)、乙腈(410ppm)、二氯甲烷(600ppm)、乙烯基乙二醇(620ppm)、N,N-二甲基甲酰胺(880ppm)、甲苯(890ppm)、N,N-二甲基乙酰胺(1090ppm)、甲基环己烷(1180ppm)、1,2-二氯乙烯(1870ppm)、二甲苯(2170ppm)、甲醇(3000ppm)、环己烷(3880ppm)、N-甲基吡咯烷酮(4840ppm)、。第三类溶剂 是指对人体低毒的溶剂。急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。在无需论证的
情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。这类溶剂包括: 戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。 除上述这三类溶剂外,在药物、辅料和药品生产过程中还常用其他溶剂,如1,1-二乙氧基丙烷、1,1-二甲氧基甲烷、2,2-二甲氧基丙烷、异辛烷、异丙醚、甲基异丙酮、甲基四氢呋喃、石油醚、三氯乙酸、三氟乙酸。这些溶剂尚无基于每日允许剂量的毒理学资料,如需在生产中使用这些溶剂,必须证明其合理性。 一些溶剂因为种种原因总是含有杂质,这些杂质如果对溶剂的使用目的没有什么影响的话,可直接使用。可是在进行化学实验和进行一些特殊的化学反应时,必须将杂质除去。虽然除去全部杂质是有困难的,但至少应该将杂质减少到对使用目的没有妨碍的限度。除去杂质的操作称为溶剂的精制,故溶剂的精制几乎都要进行脱水,其次再除去其他的杂质。 1.溶剂的脱水干燥: 溶剂中水的混入往往是由于在溶剂制造,处理或者由于副反应时作为副产物带入的,其次在保存的过程中吸潮也会混入水分。水的存
化学反应中有机溶剂的选择原则和经验
一、溶剂的选择原则和经验 1、常用溶剂: DMF、氯苯、二甲苯、甲苯、乙腈、乙醇、THF、氯仿、乙酸乙酯、环己烷、丁酮、丙酮、石油醚。 2、比较常用溶剂:DMSO、六甲基磷酰胺、N-甲基吡咯烷酮、苯、环己酮、丁酮、环己酮、二氯苯、吡啶、乙酸、二氧六环、乙二醇单甲醚、1,2-二氯乙烷、乙醚、正辛烷。 3、一个好的溶剂在沸点附近对待结晶物质溶解度高而在低温下溶解度又很小。DMF、苯、二氧六环、环己烷在低温下接近凝固点,溶解能力很差,是理想溶剂。乙腈、氯苯、二甲苯、甲苯、丁酮、乙醇也是理想溶剂。 4、溶剂的沸点最好比被结晶物质的熔点低50℃。否则易产生溶质液化分层现象。 4、溶剂的沸点越高,沸腾时溶解力越强,对于高熔点物质,最好选高沸点溶剂。 5、含有羟基、氨基而且熔点不太高的物质尽量不选择含氧溶剂。因为溶质与溶剂形成分子间氢键后很难析出。 6、含有氧、氮的物质尽量不选择醇做溶剂,原因同上。 7、溶质和溶剂极性不要相差太悬殊。水>甲酸>甲醇>乙酸>乙醇>异丙醇>乙腈>DMSO>DMF>丙酮>HMPA>CH2Cl2>吡啶>氯仿>氯苯>THF>二氧六环>乙醚>苯>甲苯>CCl4>正辛烷>环己烷>石油醚。 二、重结晶操作
1、筛选溶剂:在试管中加入少量(麦粒大小)待结晶物,加入0.5 mL根据上述规律所选择溶剂,加热沸腾几分钟,看溶质是否溶解。若溶解,用自来水冲试管外测,看是否有晶体析出。初学者常把不溶杂质当成待结晶物!如果长时间加热仍有不溶物,可以静置试管片刻并用冷水冷却试管(勿摇动)。如果有物质在上层清液中析出,表示还可以增加一些溶解。若稍微浑浊,表示溶剂溶解度太小;若没有任何变化,说明不溶的固体是一种东西,已溶物质又非常易溶,不易析出。 2、常规操作:在锥形瓶或圆底烧瓶中加入溶质和一定溶剂,装上球冷,加热10分钟,若仍有不溶物,继续从冷凝管上口补加溶剂至完全溶解再补加过量30%溶剂。用折叠滤纸(折叠滤纸和三角漏斗要提前预热)趁热过滤入锥形瓶。滤液自然冷却后用布氏漏斗抽滤(用滤液反过来冲洗锥形瓶!)。如果物质在室温溶解度很小,滤饼可以用少量冷的溶剂淋洗(先撤掉减压,加少量溶剂润湿滤饼,再减压抽干。注意:用玻璃塞把滤饼压实有助于除掉更多溶剂!)。如果所用溶剂不易挥发,可以在常压下加入少量易挥发溶剂淋洗滤饼,如DMF可用乙醇洗,二氯苯、氯苯、二甲苯、环己酮可以用甲苯洗。初学者常遇到问题:大量结晶在滤纸上析出,原因是漏斗和滤纸预热不好、溶剂过量太少、过滤时间太长。如产品贵重,可将三角漏斗和滤纸置于锥形瓶上用蒸气预热,边过滤边用已经过滤的滤液蒸气保温,但上述操作比较危险,甲苯、醚类、石
07-08学年度第二学期高二化学:有机合成的常规方法与解题思路 (附答案) 如何从原料出发去合成有机物呢?一种是通过对比,找出原料与目标产物的区别点,区别点就是变化点,然后从原料出发去合成目标产物。还可以从目标产物入手。分析若得到此产品,最后一步应是什么反应,这步反应的反应与原料又有什么样的关系,这样从后往前将原料与产品联系起来。记住合成题的正确解答必须有扎实的有机基础知识作前提。 一、总的解题思路 关键在于: 1. 选择出合理简单的合成路线。 2. 熟练掌握好各类有机物的组成、结构,性质,相互衍变关系以及重要官能团的引入和消去等基础知识。 合成路线的推导,一般有两种方法:“直推法”和“反推法”,而“反推法”较常用,该方法的思维途径是: (1)首先确定所要合成的有机物属于何类型,以及题中所给定的条件与所要合成的有机物之间的关系。 (2)以题中要求的最终产物为起点,考虑这一有机物如何从另一有机物甲经过一步反应而制得。如果甲不是所给的已知原料,再进一步考虑甲又是如何从另一有机物乙经一步反应而制得,一直推导到题目中所给定的原料为终点,同时结合题中给定的信息。 (3)在合成某一产物时,可能会产生多种不同的方法和途径,应当在兼顾原料省、产率高的前提下选择最合理、最简单的方法和途径。 二、解题的基本规律和基本知识 1.掌握有机合成路线 有机合成往往要经过多步反应才能完成,因此确定有机合成的途径和路线时,就要进行合理选择。选择的基本要求是原料价廉,原理正确,路线简捷,便于操作、条件适宜、易于分离,产率高,成本低。中学常用的合成路线有四条。 (1)一元合成路线(官能团衍变) R —CH═CH 2 →卤代烃→一元醇→一元醛→一元羧酸→酯 (2)二元合成路线 OH H C OH H C Cl H C Cl H C CH CH OH CH CH 2|2|O H 2|2|Cl 22O H 23222-??→?-??→?=??→?++-水解 加成消去 (3)芳香化合物合成路线 ⑷改变官能团的位置 3|3HBr 23HBr 223CH Br H C CH CH CH CH Br CH CH CH +-??→?=??→?加成消去 2. 官能团的引入 ⑴引入羟基(—OH )方法: 、 、 、 等。
有机实验室常用仪器设备与使用 一、有机化学实验常用仪器、设备和应用范围 现将有机化学实验中所用的玻璃仪器、金属用具、电学仪器及一些其它设备分别介绍如下: 1、玻璃仪器 有机实验玻璃仪器(见图2.1、图2.2),按其口塞是否标准及磨口,而分标准磨口仪器及普通仪器两类。标准磨口仪器由于可以相互连接,使用是既省时方便又严密安全,它将逐渐代替同类普通仪器。使用玻璃仪器皆应轻拿轻放。容易滑动的仪器(如圆底烧瓶),不要重叠放置,以免打破。
图2.1普通玻璃仪器 除试管、烧杯等少数玻璃仪器外,一般都不能直接用火加热。锥形瓶不耐压,不能作减压用。厚壁玻璃器皿(如抽滤瓶)不耐热,故不能加热。广口容器(如烧杯)不能贮放易挥发的有机溶剂。带活塞的玻璃器皿用过洗净后,在活塞与磨口间应垫上纸片,以防粘住。如已粘住可在磨口四周涂上润滑剂或有机溶剂后用电吹风吹热风,或用水煮后再用木块轻敲塞子,使之松开。 此外,不能用温度计作搅拌棒用,也不能用来测量超过刻度范围的温度。温度计用
后要缓慢冷却不可立即用冷水冲洗以免炸裂。 有机化学实验,最好采用标准磨口的玻璃仪器。这种仪器可以和相同编号的磨口相互连接,即可免去配塞子及钻孔等手续,也能免去反应物或产物被软木塞或橡皮塞所玷污。标准磨口玻璃仪器口径的大小,通常用数字编号来表示,该数字是指塞(或橡皮塞)所玷污。标准磨口玻璃仪器口径的大小,通常用数字编号来表示,该数字是指磨口最大端直径的毫米整数。常用的有10,14,19,24,29,34,40,50等。有时也用两组数字来表示,另一组数字表示磨口的长度。例如14/30,表示此磨口直径最大处为14mm,磨口长度为30mm。相同编号的磨口、磨塞可以紧密连接。有时两个玻璃仪器,因磨口编号不同无法直接连接时,则可借助不同编号的磨口接头(或称大小头)[见图2.2(9)]使之连接。 图2.2 标准口玻璃仪器
常用有机溶剂的纯化(蒸馏法) 二硫化碳 沸点46.25℃,折光率1.631 9,相对密度1.2632。 二硫化碳为有毒化合物,能使血液神经组织中毒。具有高度的挥发性和易燃性,因此,使用时应避免与其蒸气接触。 对二硫化碳纯度要求不高的实验,在二硫化碳中加入少量无水氯化钙干燥几小时,在水浴55℃~65℃下加热蒸馏、收集。如需要制备较纯的二硫化碳,在试剂级的二硫化碳中加入0.5%高锰酸钾水溶液洗涤三次。除去硫化氢再用汞不断振荡以除去硫。最后用2.5%硫酸汞溶液洗涤,除去所有的硫化氢(洗至没有恶臭为止),再经氯化钙干燥,蒸馏收集。 DMF N,N-二甲基甲酰胺沸点149~156℃,折光率1.430 5,相对密度0.948 7。无色液体,与多数有机溶剂和水可任意混合,对有机和无机化合物的溶解性能较好。 N,N-二甲基甲酰胺含有少量水分。常压蒸馏时有些分解,产生二甲胺和一氧化碳。在有酸或碱存在时,分解加快。所以加入固体氢氧化钾(钠)在室温放置数小时后,即有部分分解。因此,最常用硫酸钙、硫酸镁、氧化钡、硅胶或分子筛干燥,然后减压蒸馏,收集76℃/4800Pa(36mmHg)的馏分。其中如含水较多时,可加入其1/10体积的苯,在常压及80℃以下蒸去水和苯,然后再用无水硫酸镁或氧化钡干燥,最后进行减压蒸馏。纯化后的N,N-二甲基甲酰胺要避光贮存。 N,N-二甲基甲酰胺中如有游离胺存在,可用2,4二硝基氟苯产生颜色来检查。 DMSO 沸点189℃,熔点18.5℃,折光率1.4783,相对密度1.100。二甲基亚砜能与水混合,可用分子筛长期放置加以干燥。然后减压蒸馏,收集76℃/1600Pa(12mmHg)馏分。蒸馏时,温度不可高于90℃,否则会发生歧化反应生成二甲砜和二甲硫醚。也可用氧化钙、氢化钙、氧化钡或无水硫酸钡来干燥,然后减压蒸馏。也可用部分结晶的方法纯化。 二甲基亚砜与某些物质混合时可能发生爆炸,例如氢化钠、高碘酸或高氯酸镁等应予注意。 乙醇 沸点78.5℃,折光率1.361 6,相对密度0.789 3。 制备无水乙醇的方法很多,根据对无水乙醇质量的要求不同而选择不同的方法。 若要求98%~99%的乙醇,可采用下列方法: ⑴利用苯、水和乙醇形成低共沸混合物的性质,将苯加入乙醇中,进行分馏,在64.9℃时蒸出苯、水、乙醇的三元恒沸混合物,多余的苯在68.3与乙醇形成二元恒沸混合物被蒸出,最后蒸出乙醇。工业多采用此法。 ⑵用生石灰脱水。于100mL95%乙醇中加入新鲜的块状生石灰20g,回流3~5h,然后进行蒸馏。 若要99%以上的乙醇,可采用下列方法: ⑴在100mL99%乙醇中,加入7g金属钠,待反应完毕,再加入27.5g邻苯二甲酸二乙酯或25g草酸二乙酯,回流2~3h,然后进行蒸馏。 金属钠虽能与乙醇中的水作用,产生氢手和氢氧化钠,但所生成的氢氧化钠又与乙醇发生平衡反应,因此单独使用金属钠不能完全除去乙醇中的水,须加入过量的高沸点酯,如邻苯二甲酸二乙酯与生成的氢氧化钠作用,抑制上述反应,从而达到进一步脱水的目的。 ⑵在60mL99%乙醇中,加入5g镁和0.5g碘,待镁溶解生成醇镁后,再加入900mL99%乙醇,回流5h
溶剂的定义 溶剂(solvent)这个词广义指在均匀的混合物中含有的一种过量存在的组分。狭义地说,在化学组成上不发生任何变化并能溶解其他物质(一般指固体)的液体,或者与固体发生化学反应并将固体溶解的液体。溶解生成的均匀混合物体系称为溶液。在溶液中过量的成分叫溶剂;量少的成分叫溶质。 溶剂也称为溶媒,即含有溶解溶质的媒质之意。但是在工业上所说的溶剂一般是指能够溶解油脂、蜡、树脂(这一类物质多数在水中不溶解)而形成均匀溶液的单一化合物或者两种以上组成的混合物。这类除水之外的溶剂称为非水溶剂或有机溶剂,水、液氨、液态金属、无机气体等则称为无机溶剂。 溶解现象 溶解本来表示固体或气体物质与液体物质相混合,同时以分子状态均匀分散的一种过程。事实上在多数情况下是描述液体状态的一些物质之间的混合,金与铜、铜与镍等许多金属以原子状态相混合的所谓合金也应看成是一种溶解现象。所以严格地说,只要是两种以上的物质相混合组成一个相的过程就可以称为溶解,生成的相称为溶液。一般在一个相中应呈均匀状态,其构成成分的物质可以以分子状态或原子状态相互混合。 溶解过程比较复杂,有的物质在溶剂中可以以任何比例进行溶解,有的部分溶解,有的则不溶。这些现象是怎样发生的,其影响的因素很多,一般认为与溶解过程有关的因素大致有以下几个方面: ⑴相同分子或原子间的引力与不同分子或原子间的引力的相互关系(主要是范德华引力); ⑵分子的极性引起的分子缔合程度; ⑶分子复合物的生成; ⑷溶剂化作用; ⑸溶剂、溶质的相对分子质量; ⑹溶解活性基团的种类和数目。 化学组成类似的物质相互容易溶解,极性溶剂容易溶解极性物质,非极性溶剂容易溶解非极性物质。例如,水、甲醇和乙醇彼此之间可以互溶;苯、甲苯和乙醚之间也容易互溶,但水与苯,甲醇与苯则不能自由混溶。而且在水或甲醇中易溶的物质难溶于苯或乙醚;反之在苯或乙醚中易溶的却难溶于水或甲醇。这些现象可以用分子的极性或者分子缔合程度大小进行判断。纤维素衍生物易溶于酮、有机酸、酯、醚类等溶剂,这是由于分子中的活性基团与这类溶剂中氧原子相互作用的结果。有的纤维素衍生物在纯溶剂中不溶,但可溶于混合溶剂。例如硝化纤维素能溶于醇、醚混合溶剂;三乙酸纤维素溶于二氯乙烷、甲醇混合溶剂。这可能是由于在溶剂之间,溶质与溶剂之间生成分子复合物,或者发生溶剂化作用的结果。总之,溶解过程能够发生,其物质分子间的内聚力应低于物质分子与溶剂分子之间的吸引力才有可能实现。 溶液浓度的表示方法 溶质在溶剂中溶解的多少,彼此间存在着相对量的关系,通常用以下几种方法表示:⑴质量分数 即混合物中某一物质的质量与混合物的质量之比,符号为ω。 物质B的质量分数(ωB)=物质B的质量(mB)/溶液的质量(m) 例如:氯化钠的质量分数ω(NaCl)=15%,即表示100g该溶液中含有NaCl 15g。 ⑵体积分数 通常用于表示溶质为液体的溶液浓度(略) ⑶物质的量的浓度
有机化学实验常用的仪 器 https://www.360docs.net/doc/e917851819.html,work Information Technology Company.2020YEAR
有机化学实验常用的仪器和装置 一、有机化学实验常用的玻璃仪器 玻璃仪器一般是由软质或硬质玻璃制作而成的。软质玻璃耐温、耐腐蚀性较差,但是价格便宜,因此,一般用它制作的仪器均不耐温,如普通漏斗、量筒、吸滤瓶、干燥器等。硬质玻璃具有较好的耐温和耐腐蚀性,制成的仪器可在温度变化较大的情况下使用,如烧瓶、烧杯、冷凝管等。 玻璃仪器一般分为普通和标准 磨口两种。在实验室,常用的普通 玻璃仪器有非磨口锥形瓶、烧杯、 布氏漏斗、吸滤瓶、普通漏斗等, 见图1-1(a)。常用标准磨口仪器 有磨口锥形瓶、圆底烧瓶、三颈 (1)圆底烧瓶;(2) 三口烧瓶;(3)磨 口锥形瓶;(4)磨 口玻璃塞; (5)U 型干燥管; (6)弯头;(7)蒸馏 头;(8)标准接 头;(9)克氏蒸馏 头;(10)真空接收 管;(11)弯形接收 管;(12)分水器; (13)恒压漏斗; (14)滴液漏斗; (15)梨形分液漏 斗;(16)球形分液 漏斗;(17)直形冷 凝管;(18)空气冷 凝管;(19)球形冷 凝管;(20)蛇形冷 凝管;(21)分馏 柱;(22)刺形分馏 头;(23)Soxhlet
图1-1(b)常用标准磨口玻璃仪器 标准磨口玻璃仪器是具有标准磨口或磨塞的玻璃仪器。由于口塞尺寸的标准化、系统化,磨砂密合,凡属于同类规格的接口,均可任意互换,各部件能组装成各种配套仪器。当不同类型规格的部件无法直接组装时,可使用变接头使之连接起来。使用标准磨口玻璃仪器既可免去配塞子的麻烦手续,又能避免反应物或产物被塞子沾污的危险;口塞磨砂性能良好,使密合性可达较高真空度,对蒸馏尤其减压蒸馏有利,对于毒物或挥发性液体的实验较为安全。每一种仪器都有特定的性能和使用: 1)烧瓶: 2)冷凝管:(1)圆底烧瓶(a):能耐热和承受反应物(或溶液)沸腾以后所发生的冲击震动。在有机化合物的合成和蒸馏实验中最常使用,也常用作减压蒸馏的接收器。(2)梨形烧瓶(b):性能和用途与圆底烧瓶相似。它的特点是在合 成少量有机化合物时在烧瓶内保持较高的液面,蒸馏时残留在烧瓶中的液体少。 (3)三口烧瓶(c):最常用于需要进行搅拌的实验中。中间瓶口装搅拌器,两个侧口装回流冷凝管和滴液漏斗或温度计等。 (4)锥形烧瓶(简称锥形瓶)(d):常用于有机溶剂进行重结晶的操作,或有固体产物生成的合成实验中,因为生成的固体物容易从锥形烧瓶中取出来。通常也用作常压蒸馏实验的接受器,但不能用作减压蒸馏实验的接受器。 (5)二口烧瓶(e):常用于半微量、微量制备实验作为反应瓶,中间口接回流冷凝管、微型蒸馏头、微型分馏头等,侧口接温度计、加料管等。 (6)梨形三口烧瓶(f):用途似三口烧瓶,主要用于半微量、小量制备实验中,作为反应瓶。
常用溶剂的沸点、溶解性和毒性 溶剂名称沸点(101.3kPa)溶解性毒性 液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐 易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、***** 、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 ***** 34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶***** 性 戊烷36.1 与乙醇、***** 等多数有机溶剂混溶低毒性员?婷疋0? 二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,***** 性强 二硫化碳46.23 微溶与水,与多种有机溶剂混溶***** 性,强刺激性 溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大 丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性 氯仿61.15 与乙醇、***** 、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强***** 性 甲醇64.5 与水、***** 、醇、酯、卤代烃、苯、酮混溶中等毒性,***** 性 四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、***** 、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。***** 性,刺激性 三氟代乙酸71.78 与水,乙醇,*****, 丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷74.0 与丙酮、、甲醇、***** 、苯、四氯化碳等有机溶剂混溶低毒类溶剂 四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,***** 性 乙醇78.3 与水、***** 、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,***** 性 丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、***** 、、四氯化碳、二硫化碳、丙酮、甲苯、二 甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性 乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃 混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒 异丙醇82.40 与乙醇、***** 、氯仿、水混溶微毒,类似乙醇 1,2-二氯乙烷83.48 与乙醇、***** 、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌 乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。能溶解各种树脂, 还是二氧化硫、氯代甲烷、乙烯等气体的优良溶剂吸入和经口低毒 三氯乙烯87.19 不溶于水,与乙醇.***** 、丙酮、苯、乙酸乙酯、脂肪族氯代烃、汽油混溶有机有毒品_ 三乙胺89.6 水:18.7 以下混溶,以上微溶。易溶于氯仿、丙酮,溶于乙醇、***** 易爆,皮肤黏膜刺 激性强 丙睛97.35 溶解醇、醚、DMF 、乙二胺等有机物,与多种金属盐形成加成有机物高度性,与氢氰 酸相似 庚烷98.4 与己烷类似低毒,刺激性、***** 性
有机合成中常见郁闷操作 1. 爬板时,忘记取出TLC板,直到溶剂爬到头。 2. 忘记称量瓶重。 3. 分液时忘记及时关闭分液漏斗的旋塞,回头一看什么都没了。 4. 过柱子的时候把产物给弄没了。 5. 柱子走干了。 6. 旋蒸的时候,含产物的烧瓶一头扎进水浴锅。 7. 旋蒸的时候忘开真空…..。 8. 旋蒸时不停的暴沸。 9. 把反应液倒进旋开塞子的分液漏斗。 10. 搅拌子连同反应液一起到进分液漏斗,结果搅拌子搞破分液漏斗。 11. 做NMR时,仅有氘代溶剂,忘加…。 12. 相信自己的记忆力很好,多个样品不写标签,第二天后悔莫及。 13. 忘记开循环水。 14. 相信溶剂绝对纯净绝对无水。 15. 直道要处理反应时,发现少加一底物。 16. 投料时,加错原料。 17. 投料前不确认原料。 18. 投料的过程中,发现反应瓶小了。 19. 淬灭反应时,发现反应瓶太小了。 20. 取样时,搞破瓶子。 21. 计算投料配比时,没有考虑原料的含量。 22. 计算投料配比时,搞错一个小数点。
23. 相信一个不可靠的反应能发生奇迹。 24. 分液时,把产物层丢弃。 25. 搅拌子打破瓶子。 26. 为取出产物,惟有搞破瓶子。 27. 反应瓶滑进油浴锅。 28. 多组分平行试验,混乱了批号。 29. 过夜反应时,循环水管从冷凝器上脱落。 30. 洗瓶子时打破瓶子。 31. 在封闭的体系中进行有气体释放的反应。 32. 萃取时,死活不分层。 33. 切钠块时,打了一个喷嚏。 34. 打开冰箱,忘记关;从冰箱取出试剂,忘记归。 35. 别人拿走你称量好的瓶子。 36. 温控失灵。 37. 冲料。 38. 减压蒸馏暴沸。 39. 使用乙醚,老打瞌睡。 40. 爬板时,别人偷偷的把你的板掉个头。 41. 做减压蒸馏,突然跳闸,倒吸了
有机合成常用的技巧 湖州中学刘羽中 关键词:有机推断有机合成 如果说有机化学是化学中的王冠的话,有机合成是则是王冠上最璀璨的明珠。有机合成和推断是有机中的精华。也是高考化学中的必考体型。 有机推断、有机合成的常用方法: 1.官能团的引入 (1)引入双键 ①通过消去反应得到C=C双键,如醇、卤代烃的消去反应 ②通过氧化反应得到--,如烯烃、醇的氧化 (2)引入-OH ①加成反应:烯烃与水的加成、醛酮与H2的加成 ②水解反应:卤代烃水解、酯的水解、醇钠(盐)的水解 (3)引入-COOH ①氧化反应:醛的氧化②水解反应:酯、蛋白质、羧酸盐的水解 (4)引入-X ①加成反应:不饱和烃与HX加成②取代反应:烃与X2、醇与HX的取代 2.官能团的改变 (1)官能团之间的衍变如:伯醇醛羧酸酯 (2)官能团数目的改变 如: (3)官能团位置的改变 3.官能团的消除 (1)通过加成可以消除C=C或C≡C(2)通过消去、氧化、酯化可以消除-OH (3)通过加成(还原)或氧化可以消除--H(4)通过水解反应消除--O-(酯基) 4.碳骨架的增减 (1)增长:有机合成题中碳键的增长,一般会以信息形式给出,常见方式有酯化、有机物与HCN反应以及不饱和化合物间的加成、聚合等。 (2)变短;如烃的裂化裂解、某些烃(如苯的同系物、烯烃)的氧化、羧酸盐脱羧反应等。 三个重要相对分子质量增减的规律 1.RCH2OH RCHO RCOOH
M M-2M+14 2.RCH2OH CH3COOCH2R M M+42 3.RCOOH RCOOCH2CH3 M M+28 (关系式中M代表第一种有机物相对分子质量) 反应条件不同、产物不同的几种情况 应对策略 一、利用结构性质推断 有机物性质是与其所具有的官能团相对应的,可根据有机物的某些性质(如反应对象、反应条件、反应数据、反应特征、反应现象、反应前后分子式的差异等等)。首先确定其中的官能团及位置,然后再结合分子式价键规律、取代产物的种类、不饱和度等确定有机物的结构简式,再根据题设要求进行解答。 例化合物A(C8H8O3)为无色液体、难溶于水、有特殊香味的物质,从A出发可发生如图所示的一系列反应,
1)烧瓶: (1)圆底烧瓶(a):能耐热与承受反应物(或溶液)沸腾以后所发生的冲击震动。在有机化合物的合成与蒸馏实验中最常使用,也常用作减压蒸馏的接收器。 (2)梨形烧瓶(b):性能与用途与圆底烧瓶相似。它的特点就是在合成少量有机化合物时在烧瓶内保持较高的液面,蒸馏时残留在烧瓶中的液体少。 (3)三口烧瓶(c):最常用于需要进行搅拌的实验中。中间瓶口装搅拌器,两个侧口装回流冷凝管与滴液漏斗或温度计等。 (4)锥形烧瓶(简称锥形瓶)(d):常用于有机溶剂进行重结晶的操作,或有固体产物生成的合成实验中,因为生成的固体物容易从锥形烧瓶中取出来。通常也用作常压蒸馏实验的接受器,但不能用作减压蒸馏实验的接受器。 (5)二口烧瓶(e):常用于半微量、微量制备实验作为反应瓶,中间口接回流冷凝管、微型蒸馏头、微型分馏头等,侧口接温度计、加料管等。 (6)梨形三口烧瓶(f):用途似三口烧瓶,主要用于半微量、小量制备实验中,作为反应瓶。 2)冷凝管: (1)直形冷凝管 (a):蒸馏物质的沸点在140℃以下时,要在夹套内通水冷却;但超过140℃时,冷凝管往往会在内管与外管的接合处炸
裂。微量合成实验中,用于加热回流装置上。 (2)空气冷凝管 (b):当蒸馏物质的沸点高于140℃时,常用它代替通冷却水的直形冷凝管。 (3)球形冷凝管 (c):其内管的冷却面积较大,对蒸气的冷凝有较好的效果,适用于加热回流的实验。 3) 漏斗: 二、 有机 化学 实验 常用 装置 其中常用的反应装置的性能与使用如下: 1)回流冷凝装置:
2)滴加回流冷凝装置: 3)回流分水反应装置: 4) 滴加蒸出反应装置: 5)搅拌反应装置:
常用用有机溶剂的相对极性 常用用有机溶剂的相对极性 solvent polarity Viscosity(cp20℃) Boiling point(℃) UV cutoff(nm) i-pentane戊烷 0.00 -- 30 -- n-pentane 0.00 0.23 36 210 Petroleum ether石油醚0.01 0.30 30-60 210 Hexane己烷0.06 0.33 69 210 Cyclohexane环己烷 0.10 1.00 81 210 Isooctane异辛烷 0.10 0.53 99 210 Trifluoroacetic acid三氟乙酸 0.10 -- 72 -- Trimethylpentane三甲基戊烷0.10 0.47 99 215 Cyclopentane(环戊烷) 0.20 0.47 49 210 n-heptane(庚烷) 0.20 0.41 98 200 Butyl chloride (丁基氯; 丁酰氯) 1.00 0.46 78 220 Trichloroethylene (三氯乙烯; 乙炔化三氯) 1.00 0.57 87 273 Carbon tetrachloride (四氯化碳) 1.60 0.97 77 265 Trichlorotrifluoroethane (三氯三氟代乙烷) 1.90 0.71 48 231 i-propyl ether (丙基醚; 丙醚) 2.40 0.37 68 220 T oluene(甲苯) 2.40 0.59 111 285 p-xylene(对二甲苯) 2.50 0.65 138 290 Chlorobenzene(氯苯) 2.70 0.80 132 -- o-dichlorobenzene (领二氯苯) 2.70 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.90 0.23 35 220 Benzene(苯) 3.00 0.65 80 280 Isobutyl alcohol(异丁醇) 3.00 4.70 108 220 Methylene chloride(二氯甲烷) 3.40 0.44 40 245 Ethylene dichloride(二氯化乙烯)3.50 0.79 84 228 n-butanol(丁醇) 3.90 2.95 117 210 n-butyl acetate(醋酸丁酯; 乙酸丁酯)4.00 --- 126 254 n-propanol(丙醇) 4.00 2.27 98 210 Methyl isobutyl ketone 4.20 -- 119 330 T etrahydrofuran( 四氢呋喃)4.20 0.55 66 220 ethanol 4.30 1.20 79 210 Ethyl acetate 4.30 0.45 77 260 i-propanol(丙醇) 4.30 2.37 82 210 Chloroform(氯仿) 4.40 0.57 61 245 Methyl ethyl ketone(甲基乙基酮)4.50 0.43 80 330
一、乙醇(ethyl alcohol,ethanol) 1.理化性质: (1)分子式C2H6O (2)相对分子质量46.07 (3)结构式CH3CH2OH (4)外观与性状:无色液体,有酒香。 (5)熔点(℃):-114.1 (6)沸点(℃):78.3 (7)相对密度(水=1):0.79 (8)相对密度(空气=1):1.59 (9)溶解性:与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、酸酐、碱金属、胺类。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):12 (3)引燃温度(℃):363 (4)爆炸下限(%):3.3 (5)爆炸上限(%):19.0 二、甲醇(methyl alcohol,Methanol) 1. 理化性质: (1)分子式CH4O (2)相对分子质量32 (3)结构式CH3OH (4)外观与性状:无色澄清液体,有刺激性气味。 (5)熔点(℃):-97.8 (6)沸点(℃):64.8 (7)相对密度(水=1):0.79 (8)相对密度(空气=1):1.11 (9)溶解性:与水混溶,可混溶于醇、醚等多数有机溶剂。 (10)禁忌物:强氧化剂、酸类、酸酐、碱金属。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):11 (3)引燃温度(℃):385 (4)爆炸下限(%):5.5 (5)爆炸上限(%):44.0
乙酸乙酯,醋酸乙酯(ethyl acetate,acetic ester) 1.理化性质: (1)分子式:C4H8O2 (2)相对分子质量88.10 (3)结构式 CH3-C-OCH2CH3 (4)外观与性状:无色澄清液体,有芳香气味,易挥发。 (5)熔点(℃):-83.6 (6)沸点(℃):77.2 (7)相对密度(水=1):0.90 (8)相对密度(空气=1):3.04 (9)溶解性:微溶于水,可混溶于醇、酮、醚、氯仿等多数有机溶剂。(10)禁忌物:强氧化剂、酸类、碱类。 危险类别: (1)燃烧性:易燃 (2)闪点(℃):-4 (3)引燃温度(℃):426 (4)爆炸下限(%):2.0 (5)爆炸上限(%):11.5 二氯甲烷(dichloromethane) 1.理化性质: (1)分子式:CH2Cl2 (2)相对分子质量84.94 (3)结构式H2CCl2 (4)外观与性状:无色透明液体,有芳香气味。 (5)熔点(℃):-96.7 (6)沸点(℃):39.8 (7)相对密度(水=1):1.33 (8)相对密度(空气=1):2.93 (9)溶解性:微溶于水,溶于乙醇、乙醚。 (10)禁忌物:碱金属、铝。 危险类别: (1)燃烧性:可燃 (2)闪点(℃): (3)引燃温度(℃):615 (4)爆炸下限(%):12 (5)爆炸上限(%):19
