高中化学必修1和必修2双向细目表
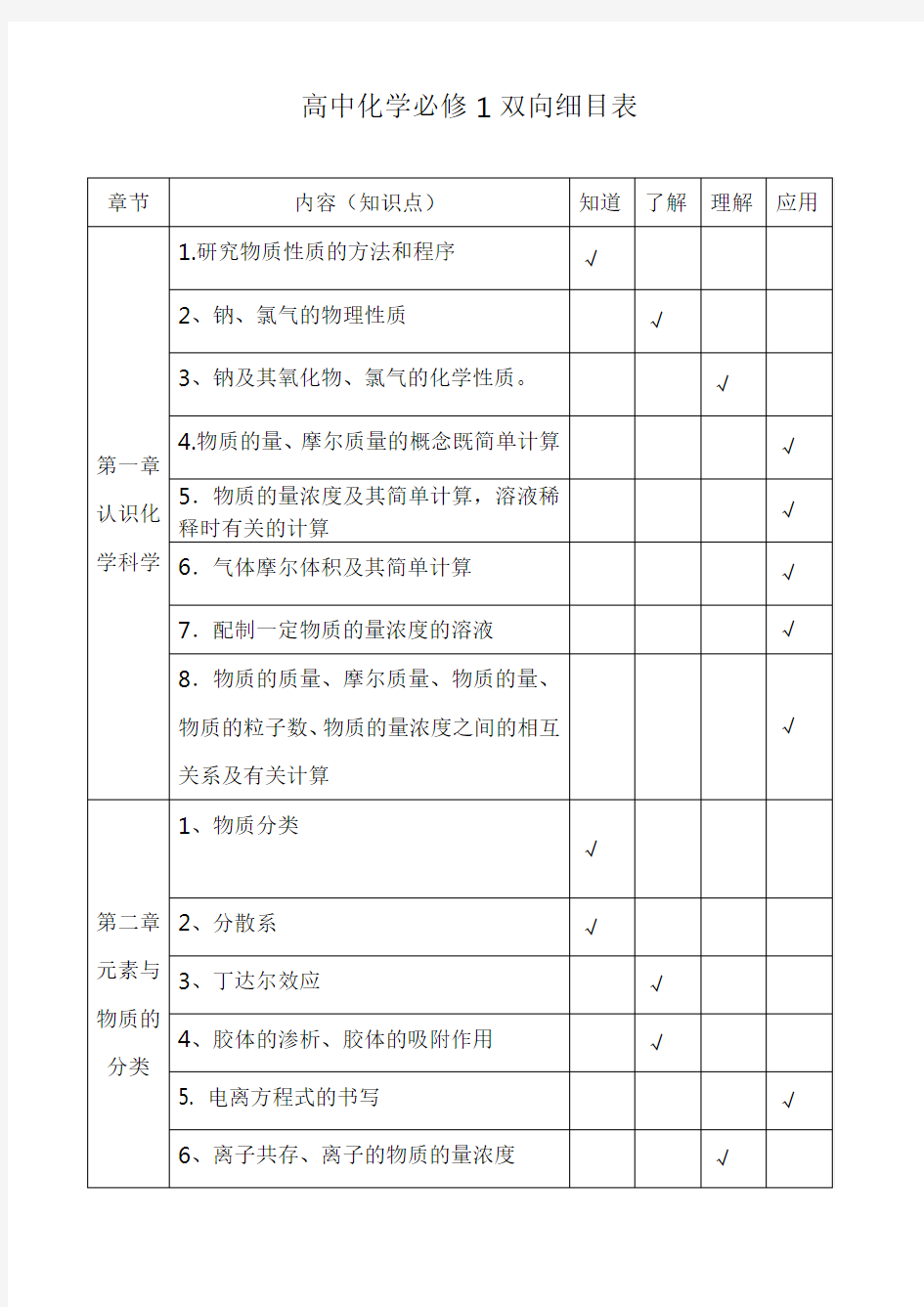
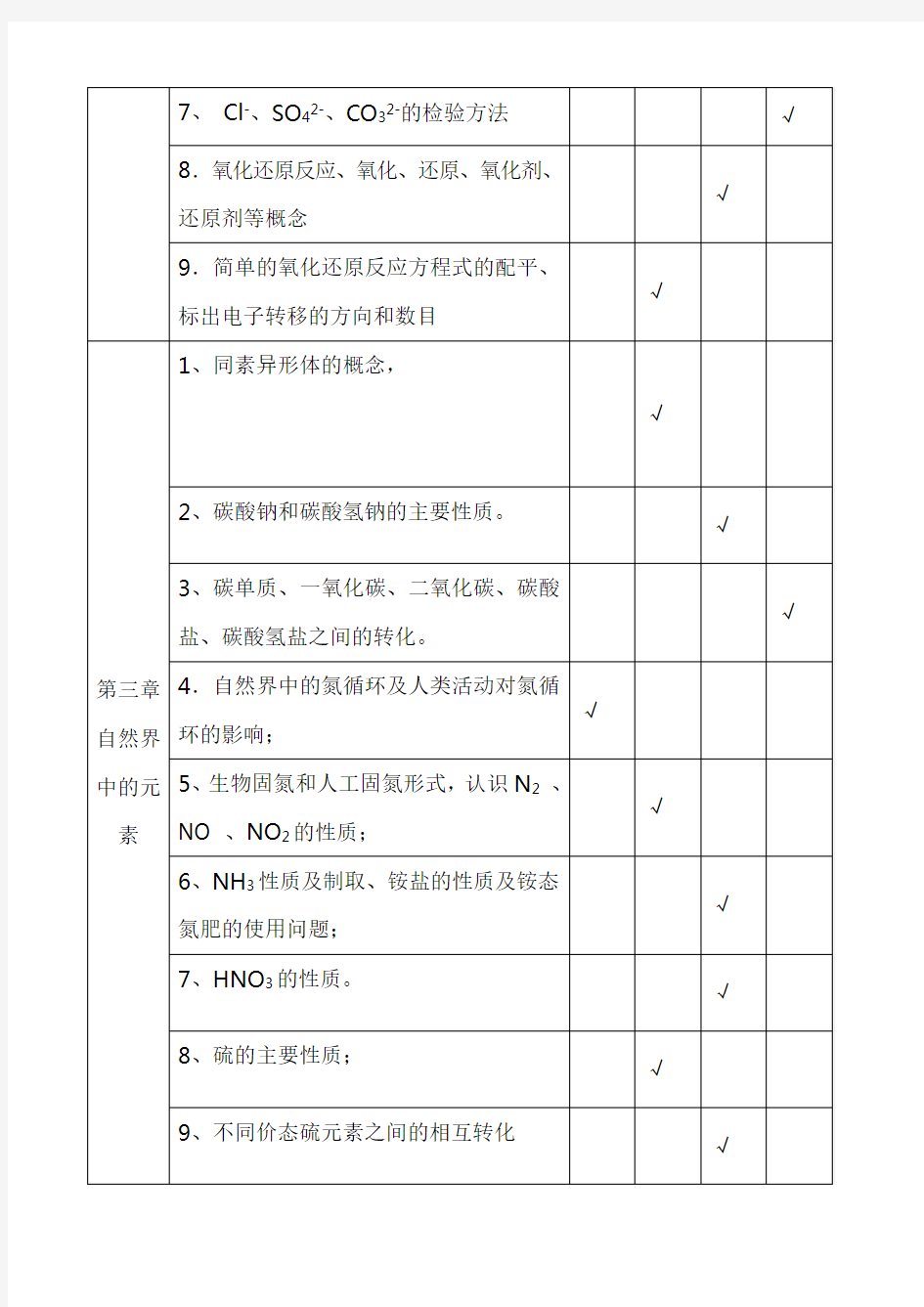
高中化学必修1双向细目表
章节内容(知识点)知道了解理解应用
第一章认识化学科学1.研究物质性质的方法和程序√
2、钠、氯气的物理性质√
3、钠及其氧化物、氯气的化学性质。√
4.物质的量、摩尔质量的概念既简单计算√
5.物质的量浓度及其简单计算,溶液稀
释时有关的计算
√6.气体摩尔体积及其简单计算√7.配制一定物质的量浓度的溶液√8.物质的质量、摩尔质量、物质的量、
物质的粒子数、物质的量浓度之间的相互
关系及有关计算
√
第二章元素与物质的分类1、物质分类
√
2、分散系√
3、丁达尔效应√
4、胶体的渗析、胶体的吸附作用√
5. 电离方程式的书写√
6、离子共存、离子的物质的量浓度√
7、 Cl-、SO42-、CO32-的检验方法√8.氧化还原反应、氧化、还原、氧化剂、
还原剂等概念
√
9.简单的氧化还原反应方程式的配平、
标出电子转移的方向和数目
√
第三章自然界中的元素1、同素异形体的概念,
√
2、碳酸钠和碳酸氢钠的主要性质。
√
3、碳单质、一氧化碳、二氧化碳、碳酸
盐、碳酸氢盐之间的转化。
√4.自然界中的氮循环及人类活动对氮循
环的影响;
√
5、生物固氮和人工固氮形式,认识N2、
NO 、NO2的性质;
√
6、NH3性质及制取、铵盐的性质及铵态氮
肥的使用问题;
√
7、HNO3的性质。
√
8、硫的主要性质;
√
9、不同价态硫元素之间的相互转化
√
10、二氧化硫和浓硫酸的主要性质。
√11、硫及其化合物在生产中的应用及酸雨
的危害
√
12、镁单质的还原性和重要用途。
√
13、氯、溴、碘单质的氧化性和氧化性递
变顺序及溴单质和溴的化合物的重要用
途。
√
14、海水中微量元素的存在和应用及在工
业生产和高科技领域的潜在价值,认识到
综合开发利用海水化学资源的重要意义。
√
第四章元素与材料世界1、硅的存在及用途。√
2、二氧化硅的物理、化学性质及其用途。√
3、硅酸的性质(弱酸性、水溶性、硅胶
的吸水性)及制备方法。
√
4.硅酸钠(Na2SiO3)的性质、用途。√
5.硅酸盐工业√
6.铝及其重要化合物的化学性质;√7、氧化铝和氢氧化铝的两性,认识与其
他常见金属及其化合物的不同。
√8.不锈钢不易锈蚀原理。√
9.金、银、铜的主要性质以及它们作为材
料在工业生产和高科技领域的应用。
√
10.了解合金的概念。√
11、认识常见的复合材料及其用途,√
12、复合材料的概念,√
13、复合材料的基本组成、优点。√
高中化学必修2双向细目表
章节内容(知识点)知道了解理解应用
第一章原子结构元素周期律1、原子核的构成,质量数与质子数、中子数的关系;
质子数、核电荷数、核外电子数的关系,能说出A
Z
X
的含义。
√
2、举例说明什么是元素、什么是核素、什么是同位
素;核素在医疗、新能源开发等方面的应用。
√
3、原子核外电子的排布规律,写出1~18号元素的原
子结构示意图及相关离子的表示方法
√4、能举例说明原子的最外层电子排布与元素性质
(原子的得失电子能力、化合价)的关系。
√5、元素原子最外层电子排布、原子半径、元素最高
化合价和最低化合价的周期性变化,认识元素周期
律。
√
6、元素周期表的结构(周期、族)以及1~18号元素
在周期表中的位置。
√
7、列举各主族的常见元素。√
8、元素周期表中金属元素、非金属元素的分布。√
9、主族元素的名称、元素符号和原子序数。√
10、原子半径、离子半径与原子结构的关系。√
11、IIA族、VA族和过渡金属元素中某些元素的主要
性质和用途。
√
12、能以第三周期元素和IA族、VIIA族元素为例,
掌握同周期、同主族元素性质递变规律,并能运用原
子结构理论初步解释这些递变规律。
√
13、主族元素在元素周期表中的位置、原子结构、元
素性质三者之间的关系,初步学会运用元素周期表。
√
14、判断元素原子得失电子能力的方法,并能进行简
单应用。
√15、元素周期律和元素周期表对其他与化学相关的科
学技术具有指导作用。
√
第二章化学键化学反应与能
量1、认识相邻原子间存在强烈的相互作用,化学键的
含义。
√
2、化学键包括离子键和共价键;离子键和共价键的
含义;可以根据化学键类型把化合物分为离子化合物
和共价化合物;能举出典型的离子化合物和共价化合
物的例子。
√
3、能用化学键的观点分析化学反应中物质变化和能
量变化的实质,知道化学反应中的能量可以转化为其
它形式的能量。
√
4、认识提高燃料的燃烧效率、开发新能源的重要性;
培养学生节约能源及保护环境的意识。
√
5、了解化学反应速率的概念;知道浓度、温度和催
化剂对化学反应速率的影响。
√
6、知道什么是可逆反应;了解化学平衡的特征,建
立化学平衡的观点。
√
7、知道外界条件会改变化学平衡状态。并能说明改
变反应条件对化学反应的调控作用。
√
8、化学平衡状态的标志及判断方法。
√
9、知道人们利用化学反应来制造新的物质和提供能
量。
√
10、能以氯气制取为例体会如何利用化学反应来制备
新的物质。
√
11、了解实验室制取氯气的原理、装置、收集方法和
尾气吸收方法。
√
12、知道电池是利用氧化还原反应将化学能转化为电
能的装置,能简单分析原电池的工作原理。
√
第三章重要的有机化合物13、初步认识有机化合物种类繁多的原因。
√
14、通过对甲烷燃烧、甲烷与氯气光照下反应等演示
实验的观察、思考、分析、推论,引导学生掌握甲烷
的化学性质,知道甲烷与氯气的反应属于取代反应。
√
15、学会书写1—5个碳原子烷烃的结构式、结构简
式,了解同分异构现象,能写出丁烷和戊烷的同分异
构体的结构简式。
√
16、以甲烷为例,认识有机化合物分子具有立体的结
构,初步培养学生空间想象能力。
√
17、引导学生了解乙烯、苯的分子结构、主要物理化
√学性质和重要应用。
18、知道石油炼制的方法、主要产物。
√
19、知道煤的干馏及其主要产物。
√
20、知道乙烯与溴的反应属于加成反应
√
21、知道乙醇的主要物理性质;能写出乙醇的结构式
√
和结构简式;了解乙醇的主要化学性质及其应用。
22、知道乙酸的主要物理性质、结构和酸性、酯化反
√
应。
23、知道乙酸乙酯的水解和酯、油脂在生产生活中的
√
应用。
24、知道糖类物质的代表物;知道葡萄糖的结构及糖
√
类的水解反应和葡萄糖与新制氢氧化铜悬浊液的反
应。
25、知道蛋白质的组成元素,基本性质和水解产物。
√
26、知道几种常见的天然高分子化合物。
√
27、了解酯化反应的实例。
√
28、初步认识有机高分子化合物的结构、性质,了解
√
合成高分子化合物的主要类别及其在生产、生活、现
代科技发展中的广泛运用。
29、认识加聚反应,能写出简单的加聚反应的化学方
√
程式。
30、学习和认识由塑料废弃物所造成的白色污染和防
√
治、消除白色污染的途径和方法。
31、了解塑料、合成橡胶、合成纤维的主要品种以及
√
它们的原料来源与石油化工、煤化工的密切联系。
高中化学必修2双向细目表
高中化学必修2双向细目表 序号内容知了理应 道解解用 第一章第一节 1、元素周期表的结构以及周期、族 ? 物质结构元素周期等概念 元素周期表 2、原子结构与元素在周期表中位置 ? 律间的关系 3、通过对碱金属、卤族元素性质的 ? 探究,理解元素性质与原子结构以及 元素在周期表中的位置的相互关系, 掌握碱金属和卤族元素的相似性和 递变性 4、原子核结构,理解质量数的含义, ? 构成原子的微粒间的关系,元素、核 素、同位素的涵义 第二节 1、原子核外电子的排布规律,1~20 ? 元素周期号元素的原子结构示意图;原子最外 律层电子排布与元素的原子得失电子 能力和化合价的关系 2、元素原子核外电子排布,原子半 ? 径,主要化合价的周期性变化。 3、第三元素和?A族,?A族元素为 ? 例,掌握同周期,同主族元素性质的 递变规律,并能运用原子结构理论初 步解释这些递变规律 4、原子结构、元素性质及该元素在 ? 周期表中的位置三者间的关系,学会 运用周期表
第三节 1、化学键的含义及离子键和共价键 ? 化学键的形成,进一步认识物质的构成 2、离子化合物和共价化合物的概念, ? 能区分离子化合物和共价化合物 3、书写常见简单化合物、单质的电 ? 子式;能用电子式表示简单物质的形 成过程 第二章第一节 1、断裂化学键要吸收能量,生成化 ? 化学反应化学能与学键要放出能量 与能量热能 2、化学能和热能是相互转化的,并 ? 且符合能量守恒 3、什么是吸热反应和放热反应,并 ? 通过实验亲身体验放热反应和吸热 反应,记住常接触的化学反应中哪些 是放热反应,哪些是吸热反应。 4、物质变化和能量变化是普遍存在 ? 的,它们符合质量守恒和能量守恒定 律 第二节 1、火力发电中的能量转化 ? 化学能与 电能 2、原电池的原理 ? 3、氧化还原反应是使化学能转换为 ? 电能的关键 4、通过对原电池装置的分析,掌握 ? 原电池正、负极判断方法 5、通过原电池装置来判断金属的活 ? 动性顺序 6、几种发展中的化学电源 ? 7、学会自己设计原电池 ? 第三节 1、化学反应速率的涵义及表示方法, ? 化学反应并能进行化学反应速率的简单计算的速率和2、浓度、温度、固体的表面积、催 ? 限度化剂等条件对化学反应速率的影响 3、建立化学平衡的观点 ?
最新六年级语文期末命题试卷(附意图、答案、双向细目表-可直接打印)
最新六年级语文期末命题试卷(附意图、答案、双向细目表-可直接打印) 姓名:成绩 积累与运用(40分)阅读(30分)习作(30分) 一、积累与运用.(50分) 1、看拼音写汉字,组成词语.(5分) jiān jùn yùn xiān yì ( ) 苦( )工( ) 含( )起()力 ( ) 灭险( ) 音( ) ()维()立 【意图:区别同音字. 】 2、改正词语中的错别字.(先把错别字画上“о”,再在括号里写上正确的字.)(4分) 莫明其妙()再接再励()自做自受()眼急手快() 德高忘重()穿流不息()兴高彩烈()愤不顾身() 【意图:检查对汉字掌握情况.】 3、给带点的字选择正确的解释,把序号填在括号里.(3分) 绝:①断绝②穷尽③走不通④独一无二的⑤极、最⑥绝对 伯牙绝弦( ) 斩尽杀绝( ) 绝无此意( ) 美妙绝伦( ) 绝大多数( ) 悬崖绝壁( ) 【意图:检测对多义字的掌握. 】 4、根据语境,选择恰当的成语填空.(4分) 执著的故事不老——愚公移山,夸父追日,_____________(守株待兔精卫填海);执著的人物不朽——闻鸡起舞的祖逖,_____________ (卧薪尝胆悬梁刺股)的勾践,面壁静修的达摩.执著是_____________(坚持不懈直言不讳),是_____________(艰苦卓绝锲而不舍),是一支永无休止符的进行曲. 【意图:考查对成语的理解和辨析能力.】5、按要求完成下面的句子.(1+1+1+4=7分) (1)、通过体育锻炼,使我的体质增强了.(在原句上修改病句) 【意图:检查修改病句的掌握情况.】 (2)、生活在海边农村的闰土的心里有无穷无尽的希奇的事.(缩写句子) _____________________________________________【意图:检查抓住句子主干的能力.】(3)、叔叔对我说:“等到了秋天,我请你到我家的果园摘桃子.”(改为转述句)
2018年高考生物全国卷一双向细目表.doc
知识内容 新课标I 必修I 蛋白质的结构和功能 2AC 核酸的结构和功能 2AC 糖类的种类和作用 脂质的种类和作用 水和无机盐的作用 多种多样的细胞☆☆ 细胞膜系统的结构和功能 主要细胞器的结构和功能☆☆☆☆ 1A 细胞核的结构和功能 1A 物质进出细胞的方式☆☆☆☆ 3A 酶在代谢中的作用 ATP 在能量代谢中的作用 光合作用的基本过程 影响光合作用速率的环境因素☆☆☆ ★30AC 细胞呼吸☆☆☆☆ 细胞的无丝分裂 细胞的有丝分裂 细胞的生长 细胞的分化☆☆ 细胞的全能性 细胞的衰老和凋亡与人体健康的关系 癌细胞的主要特征及防治 实验察DNA 、RNA 在细胞中的分布 生物组织中还原糖、脂肪和蛋白质 观察线粒体和叶绿体察植物细胞的质壁分离和复原探究影响酶活性的因素 6A 叶绿体色素的提取和分离 观察细胞的有丝分裂 4B 必修II 细胞的减数分裂 配子的形成过程 人类对遗传物质的探索过程 DNA 分子结构的主要特点☆☆ DNA 分子的复制 遗传信息的转录和翻译☆☆☆☆ 基因的分离规律和自由组合规律☆☆ ★32AB 基因与性状的关系☆☆☆☆ ★32AB 伴性遗传☆☆☆☆ ★32AB 基因突变的特征和原因6A
染色体结构变异和数目变异☆☆ 生物变异在育种上的应用☆☆ 人类遗传病的类型 现代生物进化理论的主要内容 实验低温诱导染色体加倍 必修III植物生长素的发现和作用 其他植物激素☆☆ 植物激素的应用 人体神经调节的结构基础和调节过程 神经冲动的产生和传导 人脑的高级功能 动物激素的调节 稳态的生理意义☆☆☆☆ 神经、体液调节在维持稳态中的作用 体温调节、水盐调节、血糖调节☆☆31AB 人体免疫系统在维持稳态中的作用 种群的特征☆☆☆☆5A 种群的数量变动☆☆☆ 群落的结构特征☆☆☆☆ 群落的演替☆☆☆☆ 生态系统的结构☆☆☆☆ 生态系统中的物质循环和能量流动 生态系统中的信息传递 生态系统的稳定性★29AC 人口增长对环境的影响 全球性生态环境问题 生物多样性保护的意义和措施★29A 选修1、微生物的分离和培养☆☆☆☆ ★37AB 某种微生物数量的测定 ★37AB 培养基对微生物的选择作用☆☆☆☆ 微生物发酵以及微生物应用 酶的存在与简单制作方法 酶活力测定的方法 酶在食品制造和洗涤等方面的应用 制备和应用固相化酶 从生物材料中提取某些特定的成分 运用发酵加工食品的基本方法 植物的组织培养 合计18个考点,
小学数学五年级下册期末检测双向细目表、试卷、答案
小学数学五年级下册期末检测双向细目表
小学数学五年级下册期末测试卷 学校 姓名 得分 一、填空( ?分,每空 分) 、在下面的( )里分别填上适当的分数。 ?分 ( )小时 ???毫升 ( )升 、2 9 里面有( )个 1 9 ,再加上( )个这样的分数单位是最小的质 数。 、在2 9 、 3 7 、 21 12 、 15 10 中,真分数有( ),假分数有( )。 、 ÷ ?8 () () 40 () 64 、把 米长的的绳子,平均截成 段,每段占全长的( ),每段长( )米。 、 和 的最大公因数是( ), 和 ?的最小公倍数是( ), 和 ?的最小公倍数是( ),最大公因数是( )。 、中国长征运载火箭至今已进行了 ?次发射,其中只有 次发射失败,发射成功的占总数的( )。 、在○里填上“﹥”、“﹤”或“ ”。 5 3 ○ 5 4 1 2 ○ 4 7 、用铁丝做一个长方体框架,长宽都是 ???高 ???至少需要铁丝( )???长方体框架的体积是( )??
?、用( )个 立方厘米的小正方体可以拼成一个 立方分米的正方体,把这些小正方体紧挨在一起排成一排,全长( )米。 ?、在 ???????????????????????????? ?????这几个数据中,众数是( ),中位数是( )。二、判断( 分) 、因为甲数÷乙数 ?,所以甲数和乙数的最小公倍数是甲数( )。 、两段同样长的绳子,第一段剪下4 7 米,第二段剪下全长的 4 7 ,那么两段剪下 的一样长。( )。 、 5 1 8 有 个这样的分数单位。 ( ) 、如果一个长方体,四个面完全一样,那么另外两个面一定是正方形。( ) 、棱长是 ??的正方体,它的表面积和体积相等。( )。 三、选择( 分) 、一个长是 ??,宽是 ??,棱长总和是 ???的长方体,它的高是( )??。 ???? ??? ??? ??? 、下面的平面图形中( )不能折成正方体。 、下面各分数中,不能化成有限小数的是( )。 ?? 5 8 ?? 8 15 ?? 7 20 ?? 1 8 、张师傅 小时做 个玩具,李师傅 ?小时做 ?个玩具,做得快是( )。 ??张师傅 ??李师傅 ??一样快 ??无
中考化学试卷双向细目表
初中毕业学业水平考试 试卷双向细目表 学科:化学命题时间: 单元难度 A B 考试水平 C D 难度分布 (%) 合计 a 身边的 化学物质 b c 10 4 6 2 16.7 10 10 22 a42315 物质构成 的奥秘 b2 1.611 c a54218.3 物质的 化学变化 b c 4 4 6.7 6.7 19 a22 6.7 化学与 社会发展 b4 6.78 c a 科学探究 b 4 2 7 2 19(渗透 在上述 c4 内容中)考试水平合计153******** 整卷难度分布(%):a(容易)68.3;b(中等难度)21.7;c(较难)10.
芜湖市初中毕业学业水平考试 试题情况分析 试卷名称:化学命题时间:2010年6月 题号题型知识点章/节 考试 水平 难度 估计 分值 1 2 3 4选择 选择 选择 选择 物质的变化 物质的分类 营养素 实验基本操作 2、3 2、3 12 1 B B B B 0.7 0.75 0.75 0.75 2 2 2 2 5 6选择化学式的意义 选择物质的微粒性 3 4-2 B A 0.7 0.75 2 2能根据原子序数在元素周期表 7选择 中找到指定元素 8选择与化学有关的安全知识 合成材料对人类、环境的影响;9选择 新材料对人类、社会发展的关系 4B0.72 8-1、8-3A0.752 12-3A0.72 10选择对溶解度(曲线)7-2B0.52 11填空物质的化学性质、化学变化的类1-1、1-1、B0.724 2 12填空 化学用语、混合物提纯与分离、5-2、12-1 实验分析A B C 0.65 0.8 0.6 3 2 3 7 化学用语、燃料的利用、生活中4-2、5-2A0.83 13填空6 B0.651常见的物质、分析评价6-3、7-3C0.652 14填空实验室制取气体9 3-2、5-2、A0.753
高中化学双向细目表
高中化学必修1双向细目表 章节内容(知识点)知 道了 解 理 解 应 用 第一章认识化学科学1.研究物质性质的方法和程序√ 2、钠、氯气的物理性质√ 3、钠及其氧化物、氯气的化学性质。√ 4.物质的量、摩尔质量的概念既简单计算√ 5.物质的量浓度及其简单计算,溶液稀 释时有关的计算 √6.气体摩尔体积及其简单计算√7.配制一定物质的量浓度的溶液√8.物质的质量、摩尔质量、物质的量、 物质的粒子数、物质的量浓度之间的相互 关系及有关计算 √ 第二章元素与物质的分类1、物质分类 √ 2、分散系√ 3、丁达尔效应√ 4、胶体的渗析、胶体的吸附作用√
5. 电离方程式的书写√ 6、离子共存、离子的物质的量浓度√ 7、Cl-、SO42-、CO32-的检验方法√8.氧化还原反应、氧化、还原、氧化剂、 还原剂等概念 √9.简单的氧化还原反应方程式的配平、 标出电子转移的方向和数目 √ 第三章自然界中的元素1、同素异形体的概念, √ 2、碳酸钠和碳酸氢钠的主要性质。 √3、碳单质、一氧化碳、二氧化碳、碳酸 盐、碳酸氢盐之间的转化。 √ 4.自然界中的氮循环及人类活动对氮循 环的影响; √ 5、生物固氮和人工固氮形式,认识N2、 NO 、NO2的性质; √ 6、NH3性质及制取、铵盐的性质及铵态 氮肥的使用问题; √ 7、HNO3的性质。 √
8、硫的主要性质; √ 9、不同价态硫元素之间的相互转化 √ 10、二氧化硫和浓硫酸的主要性质。 √11、硫及其化合物在生产中的应用及酸雨 的危害 √ 12、镁单质的还原性和重要用途。 √13、氯、溴、碘单质的氧化性和氧化性递 变顺序及溴单质和溴的化合物的重要用 途。 √ 14、海水中微量元素的存在和应用及在工 业生产和高科技领域的潜在价值,认识到 综合开发利用海水化学资源的重要意义。 √ 第四章元素与材料世界1、硅的存在及用途。√ 2、二氧化硅的物理、化学性质及其用途。√ 3、硅酸的性质(弱酸性、水溶性、硅胶 的吸水性)及制备方法。 √ 4.硅酸钠(Na2SiO3)的性质、用途。√5.硅酸盐工业√6.铝及其重要化合物的化学性质;√
2018年中考化学双向细目表
(化学)2018年初中毕业生毕业升学考试双向细目表 一级主题二 级 主 题 三 级 主 题 题型 能力 层次 难 度 分 值 选 择 题 填 空 题 简 答 题 实 验 题 计 算 题 A B C 科学探究 增进对科学探究的理解√7、2 发展 科学 探究 能力 能对一些实验进行探究 6 √2、1 6 学习 基本 的实 验技 能 药品的取用、仪器的连 接、加热 1 √ 7、2 1 选择实验仪器和药品√7 会配制溶液 1 √7、2 1 指示剂、PH试纸的使用√7、2 检验和区分常见物质0.25 √7、2 0.25 气体制取的装置和方法 4 √7 4 过滤、蒸发分离物质 1 2 √7 3 身边的化学物质地球 周围 的空 气 空气成分及作用 1 √√7 1 氧气和很多物质发生氧 化反应 1 √7 1 氧气、二氧化碳、一氧化 碳的性质、用途 0.5 1 √ √ 7、2、1 1.5 氧气、二氧化碳的实验室 制法 √7、2 水与 常见 的溶 液 水的组成,硬水和软水0.25 √7 0.25 常见水的净水方法 1 √7 1 溶解现象,溶液的组成0.25 √√7 0.25 饱和溶液、溶解度 5 √7、2 5 溶质质量分数的计算 1 √ 1 1 结晶现象√7 乳化√7 金属 与金 属矿 金属的物理特征,主要化 学性质,及防腐蚀方法 1 √√7、 2 1 常见的铁矿石炼铁√7 合金性能,生铁和钢√7
物金属材料作用√7 金属资源的保护√7、2 生活中常见的化合物酸碱的性质和用途,腐蚀 性 2.25 √√√2、1 2.25 常见酸碱的稀释方法√7 酸碱性对人体、农作物的 影响 √7 常见盐的用途 1 √7 1 常见化肥种类及作用 1 √7 1 常见有机物及有机物的 重要性 √√7、2 碳酸根、铵根的检验√7、2、1 常见物质的颜色及溶解 性 1.75√7 1.75 物质构成的奥秘化学 物质 的多 样性 物质的三态转化0.25√7、2 0.25 物质的分类 1 √√√7、2、1 1 微粒 构成 物质 构成物质的微粒 1.75√7 1.75 用微粒观点解释现象 4 √7 4 原子的构成 2 √7 2 微粒间的转化,核外电子 在化学反应中的作用 1 √√ 2 1 认识 化学 元素 常见元素名称及符号√7 元素的简单分类 1 √7 1 元素周期表的简单应用√7 物质 组成 的表 示 常见元素的化合价 1 √7 1 书写化学式 3 √7、2、1 3 化学式的简单计算 1 √7、2 1 商品标签的元素组成及 含量√7、2 物质的化学变化学 变化 的基 本特 征 化学变化的特征及本质0.75√7 0.75 化学变化中的能量变化 1 √7、2 1 催化剂的作用0.5 √7 0.5
小学科学毕业考试命题双向细目表2012
小学科学六年级毕业考试试卷 (满分100分,考试时间60分钟) 第一部分知识检测站 一、填空题(每格1分,共12分) 1.水银有的性质,所以水银温度计能测量出体温的高低。 2. 、、等动物一般通过卵的孵化繁殖后代。 3.关于月球环形山的成因,目前人们普遍公认的观点是。 4.1969年7月,美国的载人飞船在月球上成功着陆,宇航员阿姆斯特朗在月球上留下了人类第一个足印。2010年10月1日,中国的探月卫星也发射成功,探测到的有关月球的数据将更加详实。 5.太阳系中唯一的恒星是;唯一适合人类居住的行星是。 6. 小学科学最后一篇课文中提到的当今世界存在的三个环境问题是、、。 二.判断题(对的打“√”,错的打“×”;每小题2分,共20分) 1.()安全帽做成拱形,能提高抗撞击能力。 2.()人摇动发电机可以发电使电灯发光。说明能量是可以转换的。 3.()为了保护丽水生物的多样性,最好能引进全国各地的动植物。 4.()要区分我和同学指纹的差异,最好把手指放在显微镜下观察。 5.()动物和植物都是由细胞构成的,微生物不是由细胞构成的。 6.()柴火燃烧会发光发热,这些都是化学变化伴随的现象。 7.()人类消耗煤和石油会向大气排放二氧化碳。 8.()夜空中的星星大多数是恒星,这些恒星永远存在不会消亡。 9.()工业废水只要经过沉淀就可以成为无害水回归自然环境了。 10.()家里过期药品最好送到附近的药店统一回收处理。 三.选择题(选择合适的序号填写在后面的括号里,共计18分) 1.每个晴天的夜晚都可见星座移动,形成这种现象的原因是()浙江省夏天炎热冬天寒冷,形成这种现象的原因是() A 地球公转 B 地球自转 C 星座绕地球公转 2.不能影响电磁铁磁极方向的是() A 铁芯摆放的方向B电流的方向 C 线圈缠绕的方向 3.班里的同学根据发际、眼皮、耳垂这三个性状的差异可以分成() A 3类 B 6类 C 8类 4. 在载物台放好载玻片后,从目镜里看却是黑乎乎的,这是因为() A 显微镜没摆放平坦 B 没有调节准焦螺旋 C 没有调节反光镜 5.下列现象属于物理变化的是() A 米饭烧焦变黑 B 米饭被嚼碎 C 米饭咀嚼多次有甜味 6.下列变化属于化学变化的是()
(完整版)高考化学知识点双向细目表.doc
高考化学知识点双向细目表 (依据安徽 2011 年高考说明) 黄山市田家炳实验中学程培红2011年 8月 31日 理综 题型 分类序 知识点内容 了解合 号解掌应 填空题 选择题 握用 物质 1 分子、原子、离子、元素等概念的含义;√ 的组 2 原子团的定义√ 成、3 物理变化与化学变化的区别与联系。√√ 性质 4 混合物和纯净物、单质和化合物、金属和非金属的概念√√ 和分 类 5 同素异形体的概念。√ 6 酸、碱、盐、氧化物的概念及其相互联系。√√ 7 熟记并正确书写常见元素的名称、符号、离子符号。√√ 化 熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式), 8 √√ 或根据化学式判断化合价。 学 基9 原子结构示意图、分子式、结构式和结构简式的表示方法。√√√化学 本 用语概 及常念 用计化 量学 基 本 理 论 溶液 物 质 结 构10 质量守恒定律的含义。√ 11 正确书写化学方程式、离子方程式,并能进行有关计算。√√√ 12 相对原子质量、相对分子质量的定义,并能进行有关计算。√√ 13 物质的量的单位 -- 摩尔( mol ),摩尔质量、气体摩尔体积。√√√ 14 物质的量浓度( mol·L-1 )、阿伏加德罗常数的含义。√√√ 根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标 15 准状况下)之间的相互关系进行有关计算。 √√√ 16 溶液的含义。√ 17 溶解度、饱和溶液的概念。√ 18 溶液的组成。√ 19 溶液中溶质的质量分数的概念,并能进行有关计算。√√ 20 胶体是一种常见的分散系√√ 21 元素、核素和同位素的含义。√√ 原子构成。原子序数、核电荷数、质子数、中子数、核外电子数 √√√22 以及它们之间的相互关系 23 元素周期律的实质。√
自编小学数学期末测试题(内含期末试卷、双向细目表、试卷分析表、参考答案和评分意见)
人教版小学五年级数学(下册)期末测试双向细目表姓名:谢xx 专业:xxxx 学号:xxxx
2011年度上学期五年级数学期末试卷参考答案及评分意见 一、填空题 1、1 42 45 3 2、15 35 3、89 99 191 4、40 8 136 80 5、912 12 16 18÷24 0.75 6、 53 7 4 4 7、10 12 14 (注意,此题答案位置不可颠倒,题干中已经说明) 8、50.24 9、> 10、78 二、选择题 1、 D 2、C 3、A 4、B 5、C 三、判断题 1、× 2、× 3、 × 4、 √ 5、 × 四、计算题 1、1 0 43 53 95 83 121 6 5 (注意:本题只需写出最后结果) 2、 43 2 20 7 5 (注意:本体需有一些解题过程) 3、920 57 710 15 (注意:此题需按照方程的标准求解步骤求解)
五、作图题 1、 注:该题比较开放, 答案并不唯一教师视情况, 可酌情给分。 2、注意:该题需要步骤,学生不能直接做出最后图形,须有过程。 六、应用题 1、12 2、 15 4 3、55(分钟) 4、480元 5、150.72平方米 6、本班学生的体重,整体情况趁较集中的趋势分布,最大值和最小值差距不是特别大,整体水平稳定。
附三: 2011年上学期五年级数学期末试卷 试卷分析表
2011年上学期五年级数学期末试卷 (满分100 命题人:谢xx ) 学校 班级 姓名 学号 一、填空题(共28分,每空1分) 1、5和8的最大公因数是( ),6和42的最小公倍数是( ),9和15的最小公倍数是( ),最大公因数是( )。 2、3米长的绳子剪成相等的5段,每段长是这根绳子的) () (,每段长) () (米。 3、分数单位是1 9 的最大真分数是( ),最小假分数是( ),最小带分数是 ( )。 4、一个长方体文具盒,已知它的长为10cm ,宽为4cm,高为2cm,那么,这个文具盒最大面的面积是( ),最小面的面积是( ),它的表面积是( ),以及体积是( )。 5、3÷4=( )12 =12( ) =18÷( )=( )(填小数) 6、23 +1=( ), 2 - 14 =( ),84 +10 5 =( )。 7、三个连续偶数的和是36,这三个数安从小到大的顺序排列,它们分别是( ),( ),( )。 8、一个圆形的水池,周长是25.12米,它的面积是( )平方米。 9、若在()里填上“>”、“<”或“=”。那么,当x=16 时, 15 -x ( ) 131 。 10、小红本学期5次数学诊断的成绩分别是:76,82,88,80,64。那么,小红本学期的平均 成绩是( )。 二、选择题(请将正确答案填在括号里,共5分,每题1分) 1、下列现象中,属于图形平移的是( )。 A 、转动着的电风扇 B 、扔出的铅笔 C 、山路上行驶的汽车 D 、笔直航行的轮船 2、今年“国庆七日长假”,陆老师想参加“千岛湖双日游”,哪两天去去呢,陆老师共有( )种不同的选择。 A 、4种 B 、5种 C 、6种 3、把两根分别长为45厘米和30厘米的彩带剪成长度一样的短彩带且没有剩余,每根短彩带最长是( )厘米。 A 、15 B 、5 C 、30 4、两个连续奇数的和是24,这两个数的最大公因数是( )。 A 、1 B 、2 C 、无法确定 5、如果正方体的边长扩大3倍,那么他的面积将扩大( )倍。 A 、3倍 B 、6倍 C 、9倍
生物试卷双向细目表
高中生物《必修一模块》试卷编制 姓名:XXX 学号:XXXXXXXX 一、双向细目表(满分50分)
二、试题内容 (一)单选题(每题2分,共20分) 1、对构成蛋白质的氨基酸结构的描述,不正确的是() A.20种氨基酸的不同在于R基不同 B.每种氨基酸都只含有一个氨基和一个羧基 C.在氨基酸中,都有一个氨基和一个羧基连接在同一个碳原子上 D.氨基酸是一种具有酸、碱两种性质的化合物 2、下列哪一项不是构成蛋白质多样性的原因() A.氨基酸的数目成百上千 B.氨基酸形成肽链时,不同种类氨基酸的排列顺序千变万化 C.肽链的盘曲、折叠方式及其形成的空间结构千差万别 D.氨基酸的种类多达百种 3、下外关于水的生理功能的叙述中,不正确的是( ) A.自由水是良好的溶剂B.结合水是细胞结构的重要组成成分 C.水溶液可运输代谢废物到排泄器官D.水分解能释放能量供生命活动需要 4、真核生物的遗传物质存在于() A.细胞核内B.细胞质中的细胞器内C.细胞质基质中D.细胞核和细胞质内 5、人在补钙的同时,最好吃一点鱼肝油,其原因是() A.鱼肝油中含有维生素A,有利于钙的吸收 B.鱼肝油中含有更多的钙 C.鱼肝油中含有维生素D,有利于钙的吸收 D.鱼肝油中含有较多的脂质,有利于钙的吸收 6、淀粉、核酸、脂肪、蛋白质共有的化学元素是( ) A. C、H、O B. C、H、O、N C.C、H、O、N、S D. C、H、O、N、S 7、以下是几位同学写的氨基酸结构通式,请判断其中不符合要求的是() 8、某22肽被水解成1个4肽,2个3肽,2个6肽,则这些多肽的氨基总数的最小值及肽键总数依次是() A.6、18 B.5、18 C.5、17 D.6、17 9、如图1是细胞中3种化合物含量的扇形图,图2是活细胞中元素含量的柱形图,下列说法不正确的是() A.若图1表示正常细胞,则A、B化合物共有的元素中含量最多的是a
中学生物必修二双向细目表.docx
乌鲁木齐中学考试双向细目表 考试时间:100分钟总分:120分 考试范围:生物必修二全部及必修三第一章(期中考试) 测验内容识记理解应用综合 分数小计知识点(章、节)(分)(分)(分)(分) 第一章遗传因子的发现10(1)孟德尔遗传实验的科学方法2 (2)基因的分离规律2 (3)自由组合规律222 第二章基因和染色体的关系18 (1)精子的形成过程和减数分裂的2 概念 (2)精子和卵细胞形成的区别2 ( 3)减数分裂过程中染色体数目和22 行为的变化 (4)减数分裂和有丝分裂的比较2 (5)受精作用 (6)基因在染色体上2 (7)伴 X显、隐性遗传病的特点24 第三章基因的本质12(1)人类对遗传物质的探索过程2 (2) DNA 分子结构的主要特点(有22 关计算) (3) DNA分子的复制过程、条件22 (4)基因的概念2 (5)基因、 DNA与染色体的关系
第四章基因的表达 (1)遗传信息的转录和翻译 (2)中心法则的提出及其发展 (3)基因、蛋白质与性状的关系第五章基因突变与其他变异 (1)基因突变的特征和原因 (2)基因重组及其意义 (3)染色体结构变异和数目变异第六章从杂交育种到基因工程(1)杂交育种的原理 (2)杂交育种和诱变育种的优缺点(3)基因工程的概念及原理 第七章现代生物进化理论现 代生物进化理论的由来必修 三稳态与环境 第一章人体内的环境与稳态 (1)内环境的的概念及理化性质 (2)内环境稳态概念及其重要意义第二章动物和人体生命活动的调节(1)神经调节 (2)激素调节 (3)神经调节和体液调节的关系 (4)免疫调节 10 222 2 2 12 24 2 22 16 22 224 22 4 22 14 222 242 24 224 24 2 224 分数小计34343610
(完整版)高中化学高考试卷双向细目表分析
精典样卷分析 姓名:__ 分值:_____ _ 一、试卷与命题 1、命题依据和原则 依据:本套试题在设计要求按照新课程理念要求,依据广东省考试大纲,以能力考查为基本出发点,立足基础知识,重点加强对重要化学知识、实验与探究能力的考查。重点考查了元素化合物重要性质、电解质溶液、原电池、元素周期表及元素周期律、化学平衡、氧化还原反应和有机化学等化学主干知识,知识回忆与化学计算相结合,无机与有机相结合,考查考生思维的灵活性、广阔性和全面性。 原则:本着试卷要有较高信度,效度,适宜难度,和很好区分度的原则,全套试卷考查范围须知识点全面,不偏不倚,较少或没有重复考查,没有偏题怪题,能很好地区分各类水平的学生。 2、命题特点(指出优点和不足) 本套试卷覆盖知识点全面,考查知识点均为考试大纲中重要考查要点。题量题型均符合考纲要求。整张试卷的试题体现了考生对重要知识点的理解掌握能力,和对所学化学知识的全面了解熟悉程度以及考生对知识理解延伸能力。整体考试难度处于中点偏上水平,对考生能力和水平的考查有良好的信度,效度,区分度。不足在于,同类型题目出得略有重复(如选择题中图像考查);无机推断题涉及太多没学的化学方程式(可设计1,2个未学方程式,但这道题有4个),导致普遍考生推断困难。实验题考查题目设计不够严谨,给考生模棱两可的理解,和下笔困难的感觉。
3、试卷结构及双向细目表
二、学生考试基本情况分析 本试卷既考查了学生的基础知识,又考查了学生对高中化学所学重要知识点的掌握和熟悉程度。还侧重了学生对所学知识的延伸思考和学习能力。学生普遍对试卷中考查的重要知识点掌握良好,如阿伏伽德罗常数;化学反应原理及化学反应平衡;离子检验;元素周期律的知识点等。但对思维要求能力偏高如最后一道有机推断题的推断和填写这类解题能力有待提高;对知识延展思维能力考核的题目如无机推断题的推断和掌握都有所欠缺;另外对实验题的解题能力和技巧以及题型的应变处理能力都需要努力地提高。 三、学生具体答题情况分析 经过随机抽选的50份卷子统计,学生选择题的正确率在84%左右,对考查的基本知识点如有机物的认识,基本性质;元素周期律及性质;阿伏伽德罗常数;晶体的认识都掌握良好;对中难度知识点如电解池电极反应,反应配比及其计算等都能应付良好;而对能力要求稍高的爬坡提如对反应图像及性质,化学平衡原理的考查则处理困难,60%的同学都在这两题中失分。在第一道大题离子检验题(15分)中,学生得分率都较高,在11分到15分这个区间内,失分主要是在存在离子的判断和不确定离子的检验和实验步骤设计上。在第二道大题无机推断(15分)中,学生得分情况在7到13分之间,学生在前几小题电子式的书写,无机物的推断都能得分,失分存在于能力要求较高的推断化学方程式的书写,和细节反应物状态的填写,此题具备一定的爬坡度和区分度,属于难题。而在第三道大题实验题(15分)中,学生得分率基本在6到15之间,两极分化较为严重,学生要么得分很高,要么失分严重;此题侧重考察对学生思维的严密性,逻辑的流畅性。实验题一直属于考查学生的难题,此道实验题要求根据题意设计实验
高考生物知识双向细目表及考点细化表
知识内容 蛋白质的结构和功能 核酸的结构和功能 糖类的种类和作用 脂质的种类和作用 水和无机盐的作用 细胞学说建立的过程 多种多样的2017届高考生物考点双向细目表细分及训练情况记载 考纲 知识点细分训练情况记载要求 蛋白质的含量、元素组成和基本单位 列举氨基酸的种类 写出氨基酸的分子结构通式并说明其结构特点 简述氨基酸通过脱水缩合形成蛋白质的过程(计算、能量) 简述蛋白质的化学结构(肽键,肽链)和空间结构 解释蛋白质分子结构多样性的原因 Ⅱ概述蛋白质的在生命活动中的主要功能 列举导致蛋白质变性的原因、变性的结果、盐析 认同蛋白质的结构和功能的关系,清楚蛋白质结构和功能的 多样性(统一) 关注蛋白质研究的新进展 简述鉴定蛋白质的实验原理,尝试检测组织中的蛋白质的一 般方法 (合成蛋白质在细胞内外、细胞核内、细胞膜更新) 说出核酸的元素组成和基本单位(、连接方式) 列举核酸的种类及主要存在部位 DNA的平面结构,碱基互补配对原则的应用和计算 DNA的空间结构及特点、功能、结构和功能的关系(、多样 性原因) Ⅱ认同核酸是细胞内携带遗传信息的物质,在生物体的遗传、 变异和蛋白质的生物合成过程中具有极其重要的作用(核酸 功能) 知道 DNA和RNA的分布和功能(、区别与联系), RNA的分 类 简述检测核酸的实验原理,观察DNA和RNA在细胞中的分布 说出糖类的组成元素 列举糖类的主要类别 Ⅱ 说明动植物细胞中主要的单糖、二糖、多糖的分布、作用、 相互关系及各自功能(动植物特有的糖类) 认同糖类是主要的能源物质(功能) 简述鉴定还原糖的实验原理,尝试组织中还原糖的检测方法 说出脂质的种类及组成元素 Ⅱ 举例说出脂质是细胞内良好的贮能物质 列举出脂肪、类脂和固醇的主要作用。 简述鉴定脂肪的实验原理,尝试生物组织中脂肪的检测方法 Ⅰ 说出水在细胞中的含量、存在形式和作用 说出无机盐在细胞中的含量、存在形式和主要作用 细胞的发现 分析细胞学说建立的过程(主要时期、代表性科学家) Ⅰ细胞学说的主要内容 认同细胞学说的建立是一个开拓、继承、修正和发展的过程 举例说明技术进步在科学发展中的作用 Ⅱ使用高倍显微镜观察各种不同的生物材料
高中化学双向细目表
高中化学必修2双向细目表 序号内容知 道 了 解 理 解 应 用 第一章 物质结构元素周期律 第一节 元素周期表 1、元素周期表的结构以及 周期、族等概念√ 2、原子结构与元素在周期 表中位置间的关系 √ 3、通过对碱金属、卤族元 素性质的探究,理解元素性 质与原子结构以及元素在 周期表中的位置的相互关 系,掌握碱金属和卤族元素 的相似性和递变性 √ 4、原子核结构,理解质量 数的含义,构成原子的微粒 间的关系,元素、核素、同 位素的涵义 √ 第二节 元素周期律 1、原子核外电子的排布规 律,1~20号元素的原子结构 示意图;原子最外层电子排 √
布与元素的原子得失电子 能力和化合价的关系 2、元素原子核外电子排布, 原子半径,主要化合价的周 期性变化。 √ 3、第三元素和ⅰA族,ⅶA 族元素为例,掌握同周期, 同主族元素性质的递变规 律,并能运用原子结构理论 初步解释这些递变规律 √ 4、原子结构、元素性质及 该元素在周期表中的位置 三者间的关系,学会运用周 期表 √ 第三节化学键1、化学键的含义及离子键 和共价键的形成,进一步认 识物质的构成 √ 2、离子化合物和共价化合 物的概念,能区分离子化合 物和共价化合物 √ 3、书写常见简单化合物、 单质的电子式;能用电子式 表示简单物质的形成过程 √ 第二章化学 第一节 化学能与热能 1、断裂化学键要吸收能量, 生成化学键要放出能量 √
反应与能量 2、化学能和热能是相互转 化的,并且符合能量守恒 √ 3、什么是吸热反应和放热 反应,并通过实验亲身体验 放热反应和吸热反应,记住 常接触的化学反应中哪些 是放热反应,哪些是吸热反 应。 √ 4、物质变化和能量变化是 普遍存在的,它们符合质量 守恒和能量守恒定律 √ 第二节 化学能与电能 1、火力发电中的能量转化√ 2、原电池的原理√ 3、氧化还原反应是使化学 能转换为电能的关键 √ 4、通过对原电池装置的分 析,掌握原电池正、负极判 断方法 √ 5、通过原电池装置来判断 金属的活动性顺序 √
2020年中考化学双向细目表
(化学)2020年初中毕业生毕业升学考试双向细目表 一级主题二 级 主 题 三 级 主 题 题型 能力 层次 难 度 分 值 选 择 题 填 空 题 简 答 题 实 验 题 计 算 题 A B C 科学探究 增进对科学探究的理解√7、2 发展 科学 探究 能力 能对一些实验进行探究 6 √2、1 6 学习 基本 的实 验技 能 药品的取用、仪器的连 接、加热 1 √ 7、2 1 选择实验仪器和药品√7 会配制溶液 1 √7、2 1 指示剂、PH试纸的使用√7、2 检验和区分常见物质 0.2 5 √7、2 0.25 气体制取的装置和方法 4 √7 4 过滤、蒸发分离物质 1 2 √7 3 身边的化学物质地球 周围 的空 气 空气成分及作用 1 √√7 1 氧气和很多物质发生氧 化反应 1 √7 1 氧气、二氧化碳、一氧 化碳的性质、用途 0.5 1 √ √ 7、2、1 1.5 氧气、二氧化碳的实验 室制法 √7、2 水与 常见 的溶 液 水的组成,硬水和软水 0.2 5 √7 0.25 常见水的净水方法 1 √7 1 溶解现象,溶液的组成 0.2 5 √√7 0.25 饱和溶液、溶解度 5 √7、2 5 溶质质量分数的计算 1 √ 1 1 结晶现象√7 乳化√7 金属 金属的物理特征,主要 化学性质,及防腐蚀方 法 1 √√7、 2 1
与金属矿物 常见的铁矿石炼铁√7 合金性能,生铁和钢√7 金属材料作用√7 金属资源的保护√7、2 生活中常见的化合物酸碱的性质和用途,腐 蚀性 2.2 5 √√√2、1 2.25 常见酸碱的稀释方法√7 酸碱性对人体、农作物 的影响 √7 常见盐的用途 1 √7 1 常见化肥种类及作用 1 √7 1 常见有机物及有机物的 重要性 √√7、2 碳酸根、铵根的检验√7、2、1 常见物质的颜色及溶解 性 1.7 5 √7 1.75 物质构成的奥秘化学 物质 的多 样性 物质的三态转化 0.2 5√7、2 0.25 物质的分类 1 √√√7、2、1 1 微粒 构成 物质 构成物质的微粒 1.7 5 √7 1.75 用微粒观点解释现象 4 √7 4 原子的构成 2 √7 2 微粒间的转化,核外电 子在化学反应中的作用 1 √√ 2 1 认识 化学 元素 常见元素名称及符号√7 元素的简单分类 1 √7 1 元素周期表的简单应用√7 物质 组成 的表 示 常见元素的化合价 1 √7 1 书写化学式 3 √7、2、1 3 化学式的简单计算 1 √7、2 1 商品标签的元素组成及 含量√7、2 物质化学化学变化的特征及本质0.7√7 0.75
生物试卷双向细目表
高中生物《必修一模块》试卷编制姓名:XXX 学号:XXXXXXXX 一、双向细目表(满分50分)
4 / 1. 二、试题内容 (一)单选题(每题2分,共20分) 1、对构成蛋白质的氨基酸结构的描述,不正确的是() A.20种氨基酸的不同在于R基不同 B.每种氨基酸都只含有一个氨基和一个羧基 C.在氨基酸中,都有一个氨基和一个羧基连接在同一个碳原子上 D.氨基酸是一种具有酸、碱两种性质的化合物 2、下列哪一项不是构成蛋白质多样性的原因() A.氨基酸的数目成百上千 B.氨基酸形成肽链时,不同种类氨基酸的排列顺序千变万化 C.肽链的盘曲、折叠方式及其形成的空间结构千差万别 D.氨基酸的种类多达百种 3、下外关于水的生理功能的叙述中,不正确的是( ) A.自由水是良好的溶剂B.结合水是细胞结构的重要组成成分 C.水溶液可运输代谢废物到排泄器官D.水分解能释放能量供生命活动需要 4、真核生物的遗传物质存在于() A.细胞核内B.细胞质中的细胞器内C.细胞质基质中D.细胞核和细胞质内 5、人在补钙的同时,最好吃一点鱼肝油,其原因是() A.鱼肝油中含有维生素A,有利于钙的吸收 B.鱼肝油中含有更多的钙 C.鱼肝油中含有维生素D,有利于钙的吸收 D.鱼肝油中含有较多的脂质,有利于钙的吸收 6、淀粉、核酸、脂肪、蛋白质共有的化学元素是( ) A. C、H、O B. C、H、O、N C.C、H、O、N、S D. C、 H、O、N、S 7、以下是几位同学写的氨基酸结构通式,请判断其中不符合要求的是() 8、某22肽被水解成1个4肽,2个3肽,2个6肽,则这些多肽的氨基总数的
