第二药物合成实验

COOH
O
H +△
O —COCH 3
COOH
COOH
O —COCH 3
第二章 药物合成实验
2.1 阿斯匹林的制备
一、实验目的:
1.了解阿司匹林制备的反应原理和实验方法。
2.通过阿司匹林制备实验,初步熟悉有机化合物的分离、提纯等方法。
3.巩固称量、溶解、加热、结晶、洗涤、重结晶等基本操作。
二、实验原理
水杨酸分子中含羟基(—OH )、羧基(—COOH ),具有双官能团。本实验采用以强酸为硫酸[1]为催化剂,以乙酐为乙酰化试剂,与水杨酸的酚羟基发生酰化作用形成酯。反应如下: M=138.12 M=102.09 M=180.15
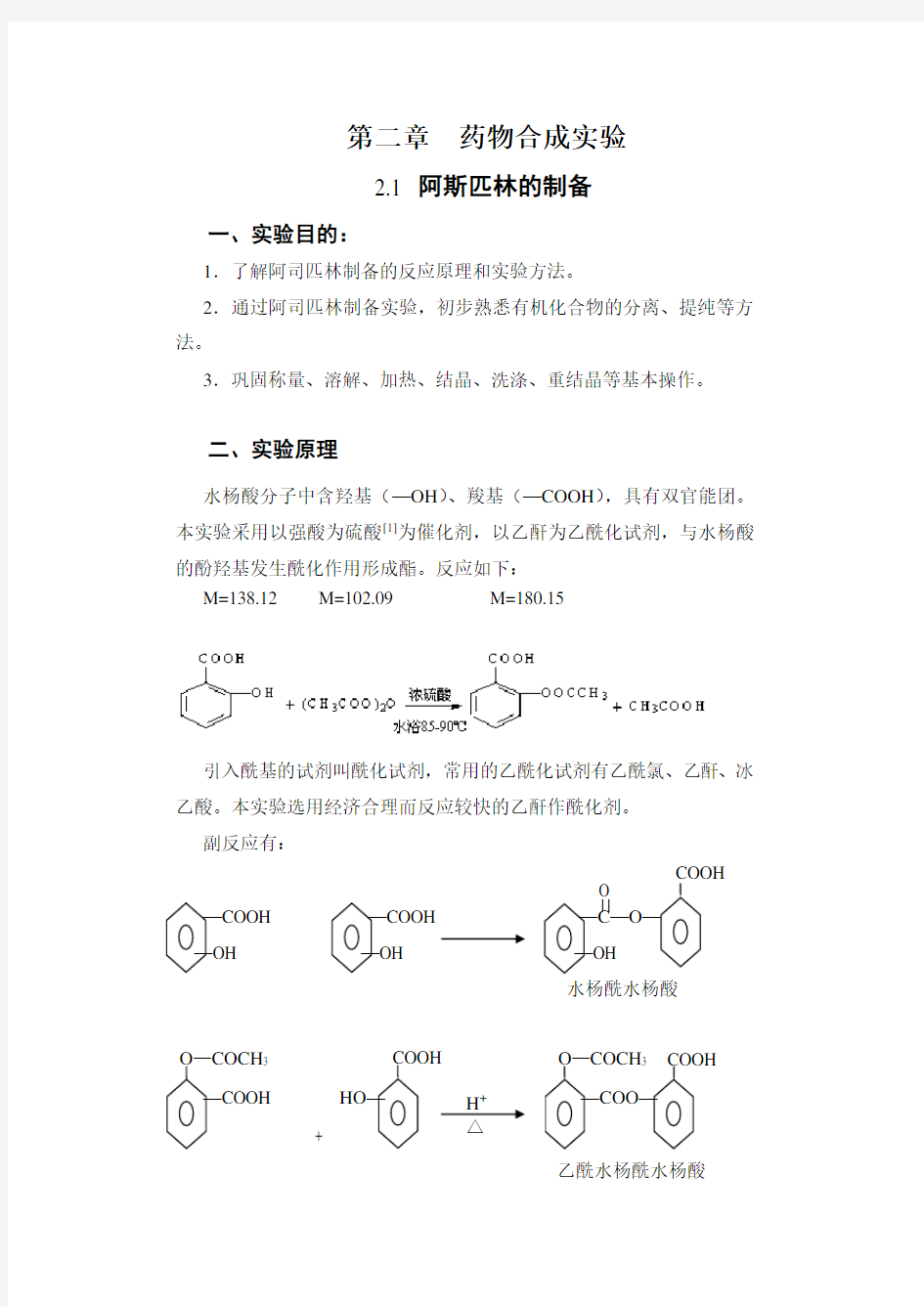
引入酰基的试剂叫酰化试剂,常用的乙酰化试剂有乙酰氯、乙酐、冰乙酸。本实验选用经济合理而反应较快的乙酐作酰化剂。 副反应有:
—COOH —COOH —C —O —
—OH —OH —OH 水杨酰水杨酸 —COOH HO —
—COO — +
乙酰水杨酰水杨酸
制备的粗产品不纯,除上面两副产品外,可能还有没有反应的水杨酸等杂质。
本实验用FeCl3检查产品的纯度,此外还可采用测定熔点的方法检测纯度。杂质中有未反应完酚羟基,遇FeCl3呈紫蓝色。如果在产品中加入一定量的FeCl3,无颜色变化,则认为纯度基本达到要求。
利用阿斯匹林的钠盐溶于水来分离少量不溶性聚合物。
三、实验试剂
水杨酸2.00g(0.015mol),乙酸酐5mL(0.053mol),饱和NaHCO3(aq),4mol/L盐酸,浓流酸,冰块,95%乙醇,蒸馏水,1%FeCl3 。
四、实验仪器
150mL锥形瓶,5mL吸量管(干燥,附洗耳球),100mL、250mL、500mL烧杯各一只,加热器,橡胶塞,温度计,玻棒,布氏漏斗,表面皿,药匙,50mL量筒,烘箱。
五、实验步骤及注意事项
注释:
1、参考数据:
1)实验在通风橱中进行,因为乙酸酐具有强烈刺激性,并注意不要粘在皮肤上。
2)仪器要全部干燥,药品也要实现经干燥处理。
3)醋酐要使用新蒸馏的,收集139~140℃的馏分。长时间放置的乙酸酐遇空气中的水,容易分解成乙酸。
4)要按照书上的顺序加样。否则,如果先加水杨酸和浓硫酸,水杨酸就会被氧化。
5)水杨酸和乙酸酐最好的比例为1:2或1:3
6)本实验中要注意控制好温度(85-90℃),否则温度过高将增加副产物的生成,如水杨酰水杨酸、乙酰水杨酰水杨酸、乙酰水杨酸酐等。
7)将反应液转移到水中时,要充分搅拌,将大的固体颗粒搅碎,以防重结晶时不易溶解。
3、思考题
1、反应容器为什么要干燥无水?
2、为什么用乙酸酐而不用乙酸?
3、加入浓硫酸的目的是什么?
4、本实验中可产生什么副产物?
5、那么副产物中的高聚物如何出去呢?
6、水杨酸可以在各步纯化过程和产物的重结晶过程中被除去,如何检验水杨酸已被除尽?
2.2 扑炎痛的合成
一、目的要求
1、了解拼合原理在药物化学中的应用,以及酯化反应在药物化学结构修饰中的应用。
2、掌握扑热息痛及阿司匹林的合成和纯化操作。
3、通过本实验,了解酯化的方法,掌握无水操作的技能。
二、反应式
+(CH 3CO)2
O
3
80~85℃
+(CH 3CO)2O CH 3CONH CH 3CONH HAc 回流
NaOH H 2O
3 +SOCl 2 +HCl ↑ +SO 2↑ 3 3
COCl
+ CH 3CONH 3
NHCOCH 3
-+NaCl
三、操作步骤与实验方法
(一)扑热息痛的制备:
1、原料与试剂
2、操作步骤
在一干燥的250ml圆底瓶中加入氨基酚25g,醋酐31g和冰醋酸44g,油浴上加热回流(110-115℃)4小时后,改成蒸馏装置,减压蒸去冰醋酸,残留物倾入约等量的冰水中1),搅拌均匀,静置使结晶。结晶后抽滤,滤饼用冰水洗(2)至中性、提干,得粗品。
粗品用适量的热水溶解(0.1g约2ml水),但产量不纯时,用水量少得多,此与原料的质量有关,PH约6。加适量活性炭,煮沸,脱色lOmin,趁热抽滤,脱色后的滤液冷却,析晶、抽滤,用少量冰水洗涤,抽干。干燥称重、计算收率,mp168-170℃。
3、本品性状
本品为白色或类白色结晶性粉末,无臭,味微苦,易溶于热于,乙醇,溶于丙酮,微溶于冷水,饱和水溶液呈弱酸性,PH约6,在PH=6时稳定,酸或碱可催化其水解。
3.附注(必须注意):
(1)蒸馏出大部分冰醋酸即可,千万不能蒸的太干,否则瓶内产物结块不易倒出。同时应注意趁热倒出产物,以免其在烧瓶内冷却结晶倒不出来。
(2)洗涤时,应先打开放空阀停抽真空,然后加少量溶剂在滤饼上,溶剂用量以使晶体刚好湿润为宜,再将溶剂抽干。
(二)乙酰水杨酸的准备
取实验1.1 所制备得到的乙酰水杨酸,经重结晶后,充分干燥备用。
(三)扑炎痛的制备
1、主要原料规格及用量
2、操作步骤(1)
在装有回流冷凝器(上端附有氯化钙干燥管排气导管通入NaOH吸收液中),温度计的250ml三颈瓶中,加入止爆剂,阿斯匹林9g,氯化亚矾5ml(实际用7ml)(2),吡啶1滴(3),置油浴上缓缓加热,约50分钟升至75℃,维持70-75℃,搅拌至无气体逸出(约2-3小时),反应毕以水泵减压蒸除过量的氯化亚砜后,冷却,得乙酰水杨酰氯,加入无水丙酮60ml,混匀密封备用。
另在装有搅拌、恒压滴液漏斗、温度计的250ml三颈瓶中,加入扑扑息痛8.6g,水50ml,保持10-15℃,缓缓加入氢氧化钠液18ml(3.3g氢氧化钠加水至18ml)降温至8-12℃,慢慢加入上述乙酰水杨酰氯无水丙酮液(约20分钟滴毕),调PH=9-10,于20-25℃搅拌1.5-2小时(保持PH=8-10),反应完毕,抽滤,滤渣用水洗至中性,烘干,得粗品,以(1:8)95%乙醇精制,约得精品5-7g,mp174-178℃,收率:44%。
3、注意:
(1)酰氯化反应,所用仪器必须干燥,反应温度不宜超过80℃,以70-75℃为佳。
(2)为了便于搅拌、观察内温、使以应更趋完全,可适当增加氯化
亚砜量至6-7ml。玻璃仪器必须是干燥的,否则氯化亚砜会产生大量烟雾。
(3)吡啶仅起催化作用,不得过多,否则影响产品色泽。
2.3 苯佐卡因的合成
一、目的要求
1. 通过苯佐卡因的合成,了解药物合成的基本过程。
2. 掌握氧化、酯化和还原反应的原理及基本操作。
二、实验原理
苯佐卡因为局部麻醉药,外用为撒布剂,用于手术后创伤止痛,溃疡痛,一般性痒等。苯佐卡因化学名为对氨基苯甲酸乙酯,化学结构式为:
COOC 2H 52
苯佐卡因为白色结晶性粉末,味微苦而麻;mp.88~90℃;易溶于乙醇,极微溶于水。
合成路线如下:
CH 3
2
2COOH
22COOC 2H 5
2
COOC 2H 5
COOC 2H 5
2
H 2SO 424
Na 2Cr 2O 7Na 2SO 4Cr 2(SO 4)3H 2O
H 2O
H 2O
Fe Fe 3O 4
++++++++C 2H 5OH
++
三、实验方法
(一) 对硝基苯甲酸的制备(氧化) 1、 仪器与试剂准备
250 mL 三颈瓶,球型冷凝管,滴液漏斗,烧杯若干,布氏漏斗,抽滤瓶等。
重铬酸钠18g ,对硝基甲苯6 g ,浓硫酸30 mL ,5% 硫酸35 mL ,
5% 氢氧化钠溶液76 mL,15% 硫酸60 mL,50%乙醇等。
2、步骤(1)
向装有球形冷凝管、滴液漏斗(2)、搅拌棒装置的250ml三口烧瓶中加入8g研碎的对硝基甲苯、24g重铬酸钠和50ml水,开启搅拌器。在滴液漏斗中放32ml浓硫酸,然后慢慢滴加入浇瓶(3)。随着浓硫酸的加入,氧化反应随之开始,反应温度迅速上升,料液颜色逐渐变深(4)。注意要严格控制滴加浓硫酸的速度,严防反应混合物高于沸腾温度(滴加时间约20~30分钟)(5)。硫酸加完后,关闭滴液漏斗,稍冷后再将烧瓶用小火加热,使反应混合物微微沸腾半小时。停止加热。冷却后,慢慢向烧瓶中加入80ml冷水(6),然后关闭搅拌器。将混合物抽滤,压碎粗产物,用20ml水分两次洗涤,粗制的对硝基苯甲酸呈深黄色固体。
为了除去粗产物夹杂的铬盐,将滤渣转移到烧杯中,加入5% 硫酸35 mL,在沸水浴上加热10 min,并不时搅拌,冷却后抽滤,滤渣溶于76ml 5%氢氧化钠溶液,温热(不超过60℃)使粗产物溶解。50℃左右抽滤(8)。在玻璃棒搅拌下将滤液慢慢倒入盛有60ml 15%硫酸的另一大烧杯中,浅黄色沉淀立即析出。用试纸检验溶液是否呈酸性。呈酸性后抽滤,固体用少量水洗至中性,抽干后放置晾干、而后称重。必要时再用50%乙醇重结晶,可得到浅黄色小针状晶体。
产量:约6g。
纯对硝基苯甲酸为浅黄色单斜叶片状晶体,熔点242℃。
实验时间:4~5小时
注意:
(1)本氧化反应十分激烈。采用机械搅拌和滴加硫酸的方法可使反应较平稳、安全。装置安装完毕后应经教师检查无误后再加料使用。
(2)滴液漏斗在使用前要检查其考克的密封性是否完好。
(3)若滴加硫酸时烧瓶内有较多白色烟雾或火花出现,则应迅速减慢或暂停滴加,必要时用冷水浴冷却烧瓶。
(4)反应温度过高,一部分对硝基苯甲酸会挥发,冷结于冷凝管内壁上。此时可适当关小冷凝水,让其熔融滴入。
(5)观察沸腾情况时,可将搅拌器暂停片刻,当看到反应物在微微起泡则可继续搅拌反应。若因故无法搅拌,也可以采用分批加硫酸、不断振荡烧瓶的方法进行实验。
(6)也可将反应混合物在玻棒搅拌下倒入水中。但由于反应物较干粘而难以倒净,反之加入水时可以充分利用搅拌器。
(7)反应式为:Cr2(SO4)3+6NaOH 2Cr(OH)3+3Na2SO4而
Cr(OH)
是两性物质,在温度较高时又会溶于碱中:
3
2Cr(OH)3+NaOH NaCrO2+2H2O,故加热溶解时温度须在60度以下。
(8)在用5% 氢氧化钠处理滤渣时,温度应保持在50℃左右,若温度过低,对硝基苯甲酸钠会析出而被滤去。本产品也可用升华法精制。
(二)对硝基苯甲酸乙酯的制备(酯化)
1、仪器与试剂准备
250 mL三颈瓶,球型冷凝管,烧杯若干,布氏漏斗,抽滤瓶,干燥管等
对硝基苯甲酸6 g(由上制备),无水乙醇24 mL,浓硫酸2 mL,氯化钙,5%碳酸钠溶液10 mL。
2、步骤(1)
在干燥的250 mL圆底瓶中加入对硝基苯甲酸6 g,无水乙醇24 mL,逐渐加入浓硫酸2 mL,振摇使混合均匀,装上附有氯化钙干燥管的球型冷凝器,油浴加热回流80 min(油浴温度控制在100~120℃);稍冷至80℃左右,将反应液倾入到100 mL冷水中并加以搅拌(2)(3),抽滤;滤渣移至研钵中,研细(4),加入5%碳酸钠溶液10 mL(由0.5 g碳酸钠和10 mL 水配成),研磨5 min以除去未酯化的对硝基苯甲酸,测pH值(检查反应物是否呈碱性),抽滤,用少量水洗涤,干燥,计算收率。
产量:4~5g。
纯对硝基苯甲酸乙酯为无色结晶,熔点57℃。
实验时间:3~4小时
注意:
(1)酯化反应须在无水条件下进行,如有水进入反应系统中,收率将降低。无水操作的要点是:原料干燥无水;所用仪器、量具干燥无水;反应期间避免水进入反应瓶。
(2)对硝基苯甲酸乙酯及少量未反应的对硝基苯甲酸均溶于乙醇,但均不溶于水。反应完毕,将反应液倾入水中,乙醇的浓度降低,对硝基苯甲酸乙酯及对硝基苯甲酸便会析出。这种分离产物的方法称为稀释法。
(3)必须随时搅拌,这样析出的固体粒子比较细,便于以后处理。
(4)如粒子很细,可不在研钵内研磨,只要在烧杯中用5%碳酸钠溶液洗涤就可以了。
(三)对氨基苯甲酸乙酯的制备(还原)
在装有搅拌棒及球型冷凝管的250 mL三颈瓶中,加入30 mL水,2.0 mL冰醋酸和已经处理过的铁粉7.2 g(1),开动搅拌,加热至95~98℃反应5 min,稍冷,加入对硝基苯甲酸乙酯5 g和95% 乙醇30 mL(2),在激烈搅拌下,回流反应90 min(3)。稍冷,在搅拌下,分次加入温热的碳酸钠饱和溶液(由碳酸钠2.5 g和水25 mL配成),搅拌片刻,立即抽滤(布氏漏斗需预热)(4),滤液冷却后析出结晶,抽滤,产品用稀乙醇洗涤,干燥得粗品。
实验时间:4小时左右
注意:
(1)还原反应中,因铁粉比重大,沉于瓶底,必须将其搅拌起来,才能使反应顺利进行,故充分激烈搅拌是铁酸还原反应的重要因素。所用的铁粉需预处理,方法为:称取铁粉10 g置于烧杯中,加入2% 盐酸25 mL,在石棉网上加热至微沸,抽滤,水洗至pH 5~6,烘干,备用。
(2)用95%乙醇作溶剂,既可溶解对硝基本甲酸乙酯,使还原反应容易进行,又可使反应物控制在80度以下搅拌回流,以免产物在沸水中分解。
(3)在加热回流过程中,先有红棕色氢氧化铁生成,最后反应物呈深棕色偏黑,这是因为有Fe3O4存在所致。
(4)滤集四氧化三铁残渣中可能夹杂着少量产品,大量制备时可用热水或稀醇洗一次,以减少损失。
(四)精制
将粗品置于装有球形冷凝器的100 mL圆底瓶中,加入10~15倍(mL/g)50% 乙醇,在电炉上小火加热溶解。稍冷,加活性碳脱色(活性碳用量视粗品颜色而定),加热回流20 min,趁热抽滤(布氏漏斗、抽滤瓶应预热)。将滤液趁热转移至烧杯中,自然冷却,待结晶完全析出后,抽滤,用少量50% 乙醇洗涤两次,压干,干燥,测熔点,计算收率。
纯对氨基苯甲酸乙酯为白色针状晶体,熔点92℃。
(五)结构确证
1. 红外吸收光谱法、标准物TLC对照法。
2. 核磁共振光谱法。
思考题:
1. 氧化反应完毕,将对硝基苯甲酸从混合物中分离出来的原理是什么?
2. 酯化反应为什么需要无水操作?
3. 铁酸还原反应的机理是什么?
药物合成反应实验讲义
药物合成反应实验讲义 编写教师:王曼张云凤
目录 实验1 苯妥英钠(Phenytoin Sodium)的合成 (1) 一、目的要求 (1) 二、实验原理 (1) 三、仪器与试剂 (2) 四、实验步骤 (3) 五、结构确证 (3) 思考题: (4) 实验2 尼群地平的合成 (5) 一、实验目的 (5) 二、方案提示 (5) 三、要求 (5) 实验3 阿昔洛韦的合成研究 (6) 一、目的 (6) 二、要求 (6)
实验1 苯妥英钠(Phenytoin Sodium)的合成 (综合性实验11学时) 一、目的要求 1. 学习安息香缩合反应的原理和应用氰化钠及维生素B1为催化剂进行反应的实验方法。 2. 了解剧毒药氰化钠的使用规则。 二、实验原理 苯妥英钠为抗癫痫药,适于治疗癫痫大发作,也可用于三叉神经痛,及某些类型的心律不齐。苯妥英钠化学名为5,5-二苯基乙内酰脲,化学结构式为: H N N ONa O 苯妥英钠为白色粉末,无臭、味苦。微有吸湿性,易溶于水,能溶于乙醇,几乎不溶于乙醚和氯仿。 合成路线如下: CHO 催化剂C CH O [O]C C O O C C O +C O NH2 NH2 NaOH H N N ONa O 2
三、仪器与试剂 1、主要仪器 磁力搅拌器、温度计、球形冷凝管、三口烧瓶、水浴锅、真空泵、布氏漏斗、抽滤瓶、圆底烧瓶、滴管、量筒、烧杯、玻璃棒、小漏斗等。 2、试剂 名称规格用量 苯甲醛 C.P. 7.5ml NaOH 2mol/L 7.5ml 乙醇 C.P. 20ml VB1 C.P. 2.7g NaOH C.P. 适量 硝酸65%—68%25ml NaOH 15%25ml 醋酸钠 C.P. 1g 尿素 C.P. 3g 乙醇95%40ml 活性炭工业少量95%乙醇-乙醚混合液1:1 少量
新实验药物合成实验报告
实验一TLC铺板、干燥、活化、色谱用硅胶柱的填装 1.硅胶薄层色谱板的制备、干燥和活化 薄层色谱中的吸附剂是铺在玻璃、塑料或金属片或薄板上的较薄的、均匀的一层细粉状物质,因支持剂的种类、制备方法和选用溶剂的不同,可按吸附、分配或二者结合的方式达到分离化合物的目的。可以通过比较斑点的R f值,或将未知样品与对照品在同一板上展开至同样高度,对样品进行初步的鉴定。还可通过比较可见斑点的大小进行半定量的判断。还可以通过光密度测量法实现定量测定。 TLC中涂布的物质与柱色谱用的吸附剂非常相似,如硅胶、氧化铝、聚酰胺等,只是它们的颗粒更细一些,一般直径为5~40μm。有些还含有石膏、淀粉等粘合剂以增强涂层与薄板的粘合力。有时里面还含有荧光指示剂(如硅酸锌等),在254或365nm的紫外光下能显示荧光,可借此对分离的斑点进行检测。到目前为止,硅胶是最常用的薄层色谱吸附剂。 在涂布吸附剂时,用于排列和放置薄板的排列盘和具有平整表面的薄板是必需的。而涂布器也很常用,当它从玻璃板上移过时,会在板的表面均匀铺上所需厚度的吸附剂涂层。 (1)实验目的 掌握硅胶薄层色谱板的制备方法。 (2)仪器和试剂 ①玻璃板(5×10cm或10×20cm,洁净且干燥); ②薄层色谱用硅胶G; ③%羧甲基纤维素钠水溶液; (3)实验步骤 ①把玻璃板在排列盘中依次相邻放好,置涂布器于其中一端。 ②在具塞锥形瓶中把一份硅胶G和2~3份CMC-Na溶液混合,并用力振摇30秒。 ③把混好的糊倒入涂布器中,均匀地移动涂布器至排列盘的另一端后,移开涂布器。 ④铺好的板静置5分钟,然后把它们面朝上移至一个水平的平面上,阴干。 ⑤把阴干后的板在105℃的烘箱中烘30分钟。 ⑥待板凉至室温后,置干燥器中保存。 2.色谱用硅胶柱的填装 液相柱色谱可以是液-固色谱或液一液色谱。如果固定相是吸附剂,也称为液相吸附色谱.若为离子交换物质,就称为离子交换色谱;若为非离子的聚合物,如聚苯乙烯或hadex,则称为凝胶渗透色谱、凝胶过滤色谱或分子排阻色谱。在柱中或纸上的液一液分配色谱可以进一步分为正相分配色谱(极性固定液)和反相分配色谱(固定相非极性)。 对于液相吸附色谱来说,固定相是填入柱中的表面活性固体(如氧化铝、硅胶和活性炭
药物合成反应 Mannich反应
Mannich 反应 在本学期的《药物合成反应》中,我学到了许多单元反应,了解了这些反 应的机理,还学到了这些反应在实际药物合成中的应用,在这些反应中,我对Mannich 反应印象最深。下面,我就Mannich 反应详细的说说我所学到的。 摘要:本文简单的概述了曼尼希反应的发现历史,反应的机理,在药物合成中的应用。很多生物碱都是通过曼尼希反应合成的,它具有很强的反应性,可 以使很多在通常条件下难以进行的反应得以顺利进行。正是Mannich 反应反应原料的多变性,以及它在药物合成中的广泛应用,使我对它产生了浓厚的兴趣。关键词:Mannich 反应;机理;应用 0 引言 Mannich 反应,亦称α-氨烷基化反应,是具有活性氢的化合物与甲醛(或 其他醛)、胺进行反应,生成氨甲基衍生物的反应,得到的 -氨基酮类化合物常称为Mannich碱。 1 Mannich 反应的历史 早在1895年便有人发现以酚作酸组分的曼尼希碱,并申请了专利。之后,Tollens、L. Henry、Duden、Franchimont等人发现了其他类型的曼尼希反应,包括以硝基烷和伯硝胺作酸组分的反应,但都没有意识到这些反应所具有的普 遍意义。 1912年,卡尔·曼尼希用沙利比林和乌洛托品反应,得到了一个难溶于水的沉淀。此产物的结构在一年内得到了解释,促使了他对这一类含活泼氢化合物、甲醛和胺之间的反应进行了深入的研究,从而奠定了曼尼希反应的基础。很多 生物碱都是通过曼尼希反应合成的。 托品酮的合成是曼尼希反应的经典例子,被认为是全合成中的经典反应之一。1901年,Willstätter首先合成了这个化合物,用的是环庚酮作原料,通过14步反应,总产率仅为0.75%。1917年,罗伯特·鲁宾逊以丁二醛、甲胺和3-氧代戊二酸为原料,在仿生条件下,利用了曼尼希反应,仅通过一步反应便得到了托品酮。反应的初始产率为17%,后经改进可增至90%。 2 Mannich 反应机理 2.1反应物
南开大学20秋学期《药物合成反应》在线作业答案资料
[南开大学]20秋学期《药物合成反应》在线作业 提示:请认真学习本资料,并完成课程复习!!100 一、单选题 (共 20 道试题,共 40 分) 1.下面所列的路易斯酸,哪个催化活性最高? A.AlBr? B.SbCl? C.SnCl4 D.ZnCl? [本题参考选择是]:A 2.根据反应历程,下列反应中生成的中间体不是碳正离子的是? A.丙烯与氯化氢的加成反应 B.甲苯的磺化反应 C.1,3-丁二烯与溴化氢的加成反应 D.溴甲烷与氢氧化钠水溶液的反应 [本题参考选择是]:D 3.鉴别甲酮基通常用? A.Tollens试剂 B.Fehling试剂 C.羰基试剂 D.碘的氢氧化钠溶液 [本题参考选择是]:D 4.羧酸的卤置换反应中,下列哪类卤化试剂的活性最高? A.三氯氧磷 B.五氯化磷 C.氧氯化磷 D.氯化锌 [本题参考选择是]:B 5.与乙烷发生卤代反应活性最强的是 A.F? B.Cl? C.I? D.Br? [本题参考选择是]:A 6.醇和卤化氢反应中,下列条件,哪条不利于反应的进行? A.增加醇的浓度 B.增加卤化氢的浓度 C.反应体系中加入水
D.除去反应体系中的水 [本题参考选择是]:C 7.醇的卤代反应属于哪类反应? A.亲电取代 B.亲电加成 C.亲核取代 D.自由基取代 [本题参考选择是]:C 8.{图} A.A B.B C.C D.D [本题参考选择是]:A 9.{图} A.A B.B C.C D.D [本题参考选择是]:C 10.在有机合成中常用于保护醛基的方法是? A.和苯肼反应 B.形成缩醛 C.碘仿反应 D.催化加氢反应 [本题参考选择是]:B 11.醇的烃化反应中,下面的卤代烃,哪个活性最高? A.CH?I B.CH?Br C.CH?Cl D.CH?F [本题参考选择是]:A 12.{图} A.A B.B C.C D.D [本题参考选择是]:A
药物化学实验讲义
药物化学实验讲义 前言 药物化学实验是依据药物化学教学大纲的要求编写的,目的是通过实验加深理解药物化学的基本理论和基本知识,掌握合成药物的基本方法;掌握对药物进行结构修饰的基本方法,了解拼合原理在药物化学中的应用;进一步巩固有机化学实验的操作技术及有关理论知识,培养学生理论联系实际的作风,实事求是,严格认真的科学态度与良好的工作习惯。 本实验教材是在药化教研室教学经验的集体总结并结合其他兄弟院校的实验素材下编写而成的,限于水平,难免有误,我们要在使用过程中不断总结经验,进一步修正提高。
2005年10月 目录 实验室基本知识 (3) 实验一苯妥英钠的合成 (6) 实验二扑热息痛的合成 (9) 实验三The Preparation of Acetylsalicylic Acid (11) 实验四苯乐来的合成 (13) 实验五盐酸普鲁卡因的合成 (16) 实验六磺胺醋酰钠的合成 (20) 实验七美沙拉秦的合成 (22)
实验室基本知识 一、实验室安全 药物化学和有机化学一样是一门实践性很强的学科,因此,在进入实验室工作之前,希望参加实验者必须对实验课程的内容,要有充分的准备,而且要通晓实验室的一些基本规则,遵守实验室安全操作须知,才能避免可能发生的一些危险情况。 (一)眼睛安全防护 在实验室中,眼睛是最容易受到伤害的。飞溅出的腐蚀性化学药品和化学试剂,进入眼睛会引起灼伤和烧伤;在操作过程中,溅出的碎玻璃片或某些固体颗粒,也会使眼睛受到伤害。为了安全起见,在某些实验中,需戴防护目镜。 倘若有化学药品或酸、碱液溅入眼睛,应赶快用大量的水冲洗眼睛和脸部,并赶快到最近的医院进行治疗。若有固体颗粒或碎玻璃粒进入眼睛内,请切记不要揉眼睛,并赶快到最近的医院进行诊治。 (二)预防火灾 有机药物合成实验室中,由于经常使用挥发性的,易燃性的各种有机试剂或溶剂,最容易发生的危险就是火灾。因此在实验中应严格遵守实验室的各项规章制度,从而可以预防火灾的发生。 在实验室内禁止吸烟。实验室中使用明火时应考虑周围的环境,如周围有人使用易燃易爆溶剂时,应禁用明火。 一旦发生火灾,不要惊慌,须迅速切断电源、熄灭火源,并移开易燃物品,就近寻找灭火的器材,扑灭着火。如容器中少量溶剂起火,可用石棉网、湿抹布或玻璃盖住容器口,扑灭着火;其他着火,采用灭火器进行扑灭,并立即报告有关部门或打119火警电话报警。 在实验中,万一衣服着火了,切勿奔跑,否则火借风势会越烧越烈,可就近找到灭火喷淋器或自来水龙头,用水冲淋使火熄灭。 (三)割伤,烫伤和试剂灼伤处理 1.割伤 遇到割伤时,如无特定的要求,应用水充分清洗伤口,并取出伤口中碎玻璃或残留固体,用无菌的绷带或创口贴进行包扎、保护。大伤口应注意压紧伤口或主血管,进行止血,并急送医疗部门
药物合成反应习题集
《药物合成技术》 习题集 适用于制药技术类专业 第一章概论 一、本课程的学习内容和任务是什么?学好本课程对从事药物及其中间体合成工作有何意义? 二、药物合成反应有哪些特点?应如何学习和掌握? 三、什么是化学、区域选择性?举例说明。 四、什么是导向基?具体包括哪些类型?举例说明。 五、药物合成反应有哪些分类方法?所用试剂有哪些分类方法?举例说明。 六、查资料写一篇500字左右的短文,报道药物合成领域的新技术及发展动态? 第二章卤化技术(Halogenation Reaction) 一、简答下列问题 1.何为卤化反应?按反应类型分类,卤化反应可分为哪几种?并举例说明。 2.在药物合成中,为什么常用卤化物作为药物合成的中间体? 3.在较高温度或自由基引发剂存在下,于非极性溶剂中,Br 2 和NBS都可用于烯丙位和苄位的溴取代,试比较它们各自的优缺点。 4.比较X 2 、HX、HOX对双键离子型加成的机理、产物有何异同,为什么? 5.解释卤化氢与烯烃加成反应中,产生马氏规则的原因(用反应机理)。为什么Lewis酸能够催化该反应? 6.解释溴化氢与烯烃加成反应中,产生过氧化效应的原因? 7.在羟基卤置换反应中,卤化剂(HX、SOCl 2、PCl 3 、PCl 5 )各有何特点,它们的 使用范围如何? 二、完成下列反应 三、为下列反应选择合适的试剂和条件,并说明原因。 四、分析讨论 1.试预测下列各烯烃溴化(Br 2/CCl 4 )的活性顺序。
2.在乙胺嘧啶中间体对氯氯苄的制备中,有如下两条路线,各有何特点?试讨论其优缺点。 3.以下是三种制备溴乙烷的方法,其中哪种适合工业生产,哪种适合实验室制备? 4.在氯霉素生产过程中,对-硝基-α-溴代苯乙酮的制备时, (1)反应有无催化剂?若有,属于哪种催化剂? (2)将对硝基苯乙酮与溶于氯苯中,加热至24-25℃,滴加少量溴,当有HBr生成并使反应液变色则可继续加溴,否则需升温至50℃直至反应开始方可继续滴加溴,为什么? (3)反应毕开大真空排净溴化氢,反应过程中溴化氢也不断移走,是不是移得越净越有利于反应?为什么? (4)生产过程中,影响因素有哪些? 第三章烷基化技术 (Hydrocarbylation Reaction ,Alkylation) 一、解释概念及简答 1.常用的烃化剂有哪些?进行甲基化及乙基化时,应选择哪些烃化剂?引入较大烃基时应选用哪些烃化剂? 2.什么叫相转移催化反应?其原理是什么?采用相转移催化技术有什么优点? 3.利用Gabriel反应与Delepine反应制备伯胺时,有什么相同与不同点? 4.什么是羟乙基化反应?在药物合成中有什么特别的意义? 5.进行F-C烃化反应时,芳香族化合物结构、卤代烃对反应有何影响?常用哪些催化剂?如何选择合适的催化剂。 6.若在活性亚甲基上引入两个烃基,应如何选择原料和操作方法?并解释原因。 二、利用Williamson法制混合醚时,应合理选择起始原料及烃化试剂,试设计下列产品的合成方法,并说明原因,掌握其中的规律。 三、完成下列反应 四、为下列反应选择适当的原料、试剂和条件,并说明依据。 五、利用所给的原料,综合所学知识合成下列产品 1.以甲苯、环氧乙烷、二乙胺为主要原料,选择适当的试剂和条件合成局麻药盐酸普鲁卡因。 2.以乙苯为主要原料,选择适当的试剂和条件合成氯霉素中间体对硝基-α-胺基
药物的合成实验
药物合成实验 实验一苯佐卡因的制备 一、实验目的 1、通过制备对氨基苯甲酸了解酯化反应的原理和方法。 2、掌握回流、重结晶、萃取等基本操作技能。 二、实验原理 本实验以对氨基苯甲酸为原料,在强酸性条件下与乙醇发生酯化反应,生成目标产物对氨基苯甲酸乙酯。 三、主要仪器与试剂 仪器:圆底烧瓶、直形冷凝管、分液漏斗、抽滤装置 试剂:对氨基苯甲酸、浓硫酸、95%乙醇、10%碳酸钠溶液、乙醚、无水硫酸镁 四、实验步骤 在50mL圆底烧瓶中加入2g对氨基苯甲酸和25mL 无水乙醇,振摇烧瓶
使大部分固体溶解。将烧瓶置于冰水浴中冷却,加入2mL 浓硫酸,立刻产生大量沉淀(在接下来的回流中沉淀将逐渐溶解),将反应混合物在水浴上加热回流 1.5h ,并不时振摇。 回流结束后将反应混合物转入烧杯中,冷却后分批(缓慢?)加入固体碳酸钠粉末,可观察到有气体逸出,并产生泡沫(发生了什么反应?),直至无明显气泡产生。检查溶液pH 值,再加入少量碳酸钠溶液至pH 为9左右(用pH 试纸检查pH 值)。在中和过程当有少量固体沉淀产生(是什么?)时,将溶液转入分液漏斗中,并用少量乙醚洗涤残余固体,并入分液漏斗中。在分液漏斗中用20mL 乙醚分两次进行萃取,振摇后分出醚层并用无水硫酸钠干燥。过滤后,在水浴上蒸去乙醚和大部分乙醇,至残余油状物约有2mL 为止。残余液用乙醇-水进行重结晶,得到最终产物约1g ,熔点90℃。 纯粹对氨基苯甲酸乙酯的熔点为91~92℃。 实验装置图 图1 普通回流装置 1-圆底烧瓶; 2-冷凝管
五、思考题 1、什么叫回流?回流的作用是什么? 2、什么叫蒸馏?回流与蒸馏有何不同? 3、酯化反应结束后,为什么要用Na2CO3溶液而不用NaOH溶液进行中和?为什么中和时不使pH=7而是pH=9? 实验二抗癫痫药——苯妥英的制备 实验I 安息香的辅酶合成 一.实验目的 1. 学习安息香缩合反应的原理。 2. 了解维生素B1的催化原理。 3. 掌握应用以VB1为催化剂合成安息香的实验方法。 二. 实验原理 安息香(二苯羟乙酮)在有机合成常作为反应中间体,既可被氧化成α-二酮(二苯乙二酮),后经浓碱处理,发生重排反应,生成二苯羟乙酸;也可被还原成二醇、烯、酮等。安息香缩合:采用氰化钾(钠)作催化剂,在碳负离子作用下,芳香醛(如苯甲醛)发生分子间缩合反应生成。但氰化物是剧毒品,危害性较强。20世纪70年代后,开始采用具有生物活性的辅酶维生素B1 代替氰化物作催化剂进行缩合反应,反应条件温和、无毒且产率高。维生素B1又称硫胺素或噻胺,它是一种生物辅酶,常作为生物化学反应的催化剂。
药物合成反应实验
药物合成反应实验 南京中医药大学药学院 2013.12.11
目录 实验一二苯甲醇的制备 (2) 实验二苯氧乙酸的制备 (3) 实验三查耳酮的制备 (4) 实验四1,2-苯并吡喃酮的制备 (5)
实验一二苯甲醇的制备 一、目的要求 了解酮的还原反应机理、还原剂的种类和特点。 二、实验原理 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗; 药品:二苯甲酮、硼氢化钠、TLC、10%HCl 四、实验操作 于装搅拌器、回流冷凝管、温度计的三颈瓶中,加入二苯甲酮3.0g,95%乙醇20ml,油浴加热至反应物全溶,冷却至室温,搅拌下分批加入硼氢化钠0.35g,加入速度以反应温度保持在50度以下为宜,加毕,回流反应1h,冷却至室温,加入20ml水稀释,加入10%稀盐酸分解未反应的硼氢化钠,待冷却至室温后抽滤,水洗滤饼,抽滤,石油醚(30-60度)重结晶得精品。 TLC判断终点,展开剂:石油醚/乙酸乙酯=10:1. 实验二苯氧乙酸的制备 一、目的要求 熟悉williamsons醚化反应的方法,了解其在药物化学结构修饰中的应用。掌握卤代烃的反应活性顺序。 二、实验原理 三、原料规格及配比
仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗、烧杯; 药品:氯乙酸、碳酸钠、苯酚、浓盐酸。 四、实验操作 将装有回流管、滴液漏斗的三颈瓶中加入氯乙酸3.8g和水5ml,缓慢滴加饱和碳酸钠溶液至pH7-8,然后加入苯酚2.6g,缓慢滴加30%氢氧化钠溶液至pH=12,回流0.5h,冷却倒入烧杯中,搅拌下滴加浓盐酸至pH=3-4,冷却结晶,抽滤,粗品用冷水洗涤,干燥称重,计算收率。 实验三查耳酮的制备 一、目的要求 了解Aldol缩合反应的机理、特点及反应条件。 二、实验原理 CHO+COCH3 2H C C H CO 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗、烧杯 药品:苯甲醛、苯乙酮、乙醇、氢氧化钠 四、实验操作 于装有电磁搅拌器、回流冷凝管、温度计、滴液漏斗的100 mL三颈瓶中,加入氢氧化钠水溶液(2.2g溶于20ml水)、95%乙醇15 mL及苯乙酮5.2g,水浴控制20o C,滴加苯甲醛4.6g,滴加过程中控制反应温度在20-25o C。加毕,于该温度下继续搅拌反应0.5h,加入少量的查耳酮做晶种,继续搅拌1.5h,析出沉淀,抽滤、水洗至中性,真空干燥,称重,计算收率。
药物合成反应重要人名反应整理
1.Hunsdriecke反应:羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。 2.Sandmeyer反应:用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。 3.Gattermann反应:将上面改为铜粉和氢卤酸。 4.Shiemann反应:将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或芳胺直接用亚硝酸纳和氟硼酸进行重氮化,此重氮盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。 5.Williamson合成:醇在碱(钠,氢氧化钠,氢氧化钾)存在下与卤代烃反应生成醚。 6.Gabriel合成:将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾生成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,肼解或酸水解即可得纯伯胺。 7.Delepine反应:用卤代烃与环六亚甲基四胺(乌洛托品)反应得季铵盐,然后水解可得伯胺。
8.Leuckart反应:用甲酸及其铵盐可以对醛酮进行还原烃化,得各类胺。 9.Ullmann反应:卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。 10.Friedel-Crafts反应:在三氯化铝催化下,卤代烃及酰卤与芳香族化合物反应,再环上引入烃基及酰基。 11.Meerwein芳基化反应:芳基自由基可与烯反应,引致烯键的碳原子上。 12.Gomberg-Bachmann反应:芳香自由基与过量存在的另一芳香族化合物发生取代反应,得到联苯。 方向自由基的来源主要有三种:最常用重氮离子的分解;其次为N-亚硝基乙酰苯胺类及芳酰过氧化物的分解 13.Hoesch反应:腈类化合物与氯化氢在Lewis酸催化剂ZnCl2的存在下与具有烃基或烷氧基的芳烃进行反应可生成相应的酮亚胺,在经水解则得具有羟基或烷氧基的芳香酮。 14.Gattermann反应:将具有羟基或烷氧基的芳烃在三氯化铝或氯化锌催化下与氰化氢及氯化氢作用生成相应芳香醛的反应。
药物合成反应期末试题
08级试题 一、填空7 1.药物合成反应的特点之一是具有较高的反应选择性,主要体现在如下三方面 选择性、 选择性、 选择性。 2.不对称烯烃与卤化氢的加成反应方向与其加成反应机理及卤化氢种类有关,此类加成反应机理大致分两类,即 加成、 加成,反应遵循马氏规则的是 加成;而当卤化氢为 时发生反马氏规则加成反应。 二、选择5 1.化学药品生产中最常见的反应器为 。 A.塔式反应器 B.釜式反应器 C.流化床反应器 D.管式反应器 2.下列试剂中属于亲核试剂的是 。 A.RO · B.C+ C.RNH 2 D.AlCl 3 3.下列醇中与HX 易发生S N 1卤置换反应的是 。 A.ROH B.R 2CHOH C.R 3COH D.CH 3OH 4.下列自由基稳定性最强的是 。 A.RCH 2· B.H 3C · C.ArCH 2· D.H 2C=CH —CH 2· 5.生成醚的反应是 。 A.Gabriel 反应 B.Williamson 反应 C.Delepine 反应 D.F-C反应 三、判断正误4 1.S N 1反应会导致卤代产物构型翻转。( ) 2.羰基α-H表现出一定的酸性,易被卤素或烃基取代。( ) 3.酚的酸性比醇强,因此酚的O-烃化反应比醇更容易。( ) 4.路易斯碱常被用于Friedel —Crafts 反应的催化剂。( ) 四、简答2 1.活化导向基 2.Phase Transfer Catalysis Reaction 五、完成反应式(填充反应条件或产物)2 1. C H 3CH 3 Cl 2CH 2Cl 2/0℃ C H 3CH 3 2. △ Me2CHCH2CH2Br NaOEt/EtOH Me2CHCH2CH2 Et C(COOEt)2CH2(COOEt)2
药物合成反应实验
药物合成反应实验 Company number:【WTUT-WT88Y-W8BBGB-BWYTT-19998】
药物合成反应实验 南京中医药大学药学院 目录 实验一二苯甲醇的制备 一、目的要求 了解酮的还原反应机理、还原剂的种类和特点。 二、实验原理 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗; 药品:二苯甲酮、硼氢化钠、TLC、10%HCl 四、实验操作 于装搅拌器、回流冷凝管、温度计的三颈瓶中,加入二苯甲酮,95%乙醇20ml,油浴加热至反应物全溶,冷却至室温,搅拌下分批加入硼氢化钠,加入速度以反应温度保持在50度以下为宜,加毕,回流反应1h,冷却至室温,加入20ml水稀释,加入10%稀盐酸分解未反应的硼氢化钠,待冷却至室温后抽滤,水洗滤饼,抽滤,石油醚(30-60度)重结晶得精品。 TLC判断终点,展开剂:石油醚/乙酸乙酯=10:1. 实验二苯氧乙酸的制备 一、目的要求
熟悉williamsons醚化反应的方法,了解其在药物化学结构修饰中的应用。掌握卤代烃的反应活性顺序。 二、实验原理 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗、烧杯; 药品:氯乙酸、碳酸钠、苯酚、浓盐酸。 四、实验操作 将装有回流管、滴液漏斗的三颈瓶中加入氯乙酸和水5ml,缓慢滴加饱和碳酸钠溶液至pH7-8,然后加入苯酚,缓慢滴加30%氢氧化钠溶液至pH=12,回流,冷却倒入烧杯中,搅拌下滴加浓盐酸至pH=3-4,冷却结晶,抽滤,粗品用冷水洗涤,干燥称重,计算收率。 实验三查耳酮的制备 一、目的要求 了解Aldol缩合反应的机理、特点及反应条件。 二、实验原理 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶100ml、温度计、回流管、抽滤瓶、布氏漏斗、烧杯 药品:苯甲醛、苯乙酮、乙醇、氢氧化钠 四、实验操作 于装有电磁搅拌器、回流冷凝管、温度计、滴液漏斗的100 mL三颈瓶中,加入氢氧化钠水溶液(溶于20ml水)、95%乙醇15 mL及苯乙酮,水浴控制20o C,滴加苯甲醛,滴加过程中控制反应温度在20-25o C。加毕,于该温度下继续搅拌反应,加入少量的查耳酮做晶种,继续搅拌,析出沉淀,抽滤、水洗至中性,真空干燥,称重,计算收率。 实验四 1,2-苯并吡喃酮的合成 一、目的要求 掌握Knoevenagel反应制备香豆素的原理。了解酯水解法制备羧酸。 二、实验原理 三、原料规格及配比 仪器:磁力搅拌器、圆底烧瓶、温度计、回流管、抽滤瓶、布氏漏斗、烧杯、干燥管; 药品:水杨醛、丙二酸二乙酯、无水乙醇、哌啶、乙酸、KOH、盐酸、冰醋酸 四、实验操作
药物合成反应习题集
《药物合成技术》习题集适用于制药技术类专业
第一章概论 一、本课程的学习内容和任务是什么?学好本课程对从事药物及其中间体合成工作有何意义? 二、药物合成反应有哪些特点?应如何学习和掌握? 三、什么是化学、区域选择性?举例说明。 四、什么是导向基?具体包括哪些类型?举例说明。 五、药物合成反应有哪些分类方法?所用试剂有哪些分类方法?举例说明。 六、查资料写一篇500字左右的短文,报道药物合成领域的新技术及发展动 态? 第二章卤化技术(Halogenation Reaction) 一、简答下列问题 1.何为卤化反应?按反应类型分类,卤化反应可分为哪几种?并举例说明。 2.在药物合成中,为什么常用卤化物作为药物合成的中间体? 3.在较高温度或自由基引发剂存在下,于非极性溶剂中,B r2和NBS都可用于烯丙位和苄位的溴取代,试比较它们各自的优缺点。 4.比较X2、HX、HOX对双键离子型加成的机理、产物有何异同,为什么?
5.解释卤化氢与烯烃加成反应中,产生马氏规则的原因(用反应机理)。为什么Lewis 酸能够催化该反应? 6.解释溴化氢与烯烃加成反应中,产生过氧化效应的原因? 7.在羟基卤置换反应中,卤化剂(HX 、SOCl 2、PCl 3、PCl 5)各有何特点,它们的使用范围如何? 二、完成下列反应 C CH 3CH 3 CHCH 3 Ca(OCl)2/AcOH/H 2O 1. Ph 2CHCH 2CH 2OH 2.CH 3 SO 2Cl Cl /AIBN 3. OH 48%HBr 4 CH 3 CH 3 5. 2 O C O CH 3OH I 2/CaO THF/MeOH AcOK Me 2CO ? 6. 三、为下列反应选择合适的试剂和条件,并说明原因。 (CH 3)2C CHCH 3 CHCH 2Br (CH 3)2C 1. CH 3 CH CH COOH CH 3 CH CH COCl 2. HOCH 2(CH 2)4CH 2OH (CH 2)4CH 2I CH 2I 3.
药物合成反应课后翻译
1、 About 216–224 g. (1.62–1.68 moles) of powdered anhydrous aluminum chloride is added to a 1Lthree-necked flask.在1L的三口烧瓶中加入大约 216-224g(1.62–1.68 moles)的无水三氯化铝。While the free-flowing catalyst is stirred (Note 3), 81 g. (0.67 mole) of acetophenone is added from the dropping funnel in a slow stream over a period of 20–30 minutes. 自由流动的催化剂边搅拌边用滴液漏斗缓慢滴加81g苯乙酰。Considerable heat is evolved, and, if the drops of ketone are not dispersed, darkening or charring occurs. 放热反应,假如滴加的酮不能被分散,就会变黑或是碳化。When about one-third of the acetophenone has been added, the mixture becomes a viscous ball-like mass that is difficult to stir.当三分之一的乙酰苯被滴加,反应混合物变成一个很难搅拌的粘性的球状团块。Turning of the stirrer by hand or more rapid addition of ketone is necessary at this point. 在这时,改用手动搅拌或快速滴加酮是非常必要的。The addition of ketone, however, should not be so rapid as to produce a temperature above 180°. 然而,速度不能太快,当反应温度超过180℃时。Near the end of the addition, the mass becomes molten and can be stirred easily without being either heated or cooled. The molten mass, in which the acetophenone is complexed with aluminum chloride, ranges in color from tan to brown.当快滴加完时,团块开始融化,表明苯乙酰已经和三氯化铝混合完全,颜色也逐渐从黄褐色变为棕色。 Bromine (128 g., 0.80 mole) is added dropwise to the well-stirred mixture over a period of 40 minutes (Note 4). 在40分钟内在搅拌下把溴缓慢滴加到混合物中。After all the bromine has been added, the molten mixture is stirred at 80–85° on a steam bath for 1 hour.溴滴加完后,熔融混合物在80-85℃蒸气浴下搅拌1小时。The complex is added in portions to a well-stirred mixture of 1.3 l. of cracked ice and 100 ml. of concentrated hydrochloric acid in a 2-l. beaker (Note 6).反应物加入到1.3L碎冰和100ml浓盐酸的混合物中在2L的烧杯中混合均匀。Part of the cold aqueous layer is added to the reaction flask to decompose whatever part of the reaction mixture remains there, and the resulting mixture is added to the beaker.把部分的冰水层加入到烧瓶中洗涤残留物,然后合并到烧杯中。The dark oil that settles out is extracted from the mixture with four 150-ml. portions of ether 分四次把深色的油从混合物中用150ml萃取出来。The extracts are combined, washed consecutively with 100 ml. of water and 100 ml. of 5% aqueous sodium bicarbonate solution, dried with anhydrous sodium sulfate, and transferred to a short-necked distillation flask. 合并萃取液,用100ml 水和100ml 5%的小苏打洗涤,用无水硫酸钠干燥。The ether is removed by distillation at atmospheric pressure, and crude 3-bromoacetophenone is stripped from a few
药物合成实验的心得体会
学而时习之 学院:树达学院学号:200921180113 姓名:李小凤经过这几个实验,经过老师的教导,我学到了很多以前没学到的知识。才发现以前的操作有很多是不规范的,做实验也经常不会去动脑的。在几位老师的引导下,慢慢的也严格的要求自己的每一个动作的规范性,每一步骤的合理性,也学会分析在做实验时出现的问题,而不再仅仅是草草的动手做做实验,也会想想有什么方法可能更好,在哪个时间段用什么试剂,为什么要用到这个试剂,不用会出现什么现象等等……同时也对以前操作过的一些仪器或步骤的进行了回顾和温习,让自己更加熟悉每一个步骤,每一个细节。下面我将谈谈自己在三个实验中遇到的一些问题和学到了一点点知识。 实验一 甲基2,3,4,6-四-o-苯甲酰基-α-D-吡喃甘露糖苷的合成及结构表征 首先这个实验我们采用了薄层分析跟踪有机反应进程、柱层析分离纯化目标产物、了解到红外光谱法和核磁共振法。 1、薄层分析跟踪有机反应进程 在这个实验中我进一步的了解到薄层分析(TLC),即把样品点到薄层上,用适当的溶剂展开,根据各组分对固定相吸附能力的差异,从而使样品的各组分达到分离的目的。这个实验我们用的固定相是硅胶板,展开剂是乙酸乙酯和甲醇(5:3)混合溶液,然后在紫外灯光下描出点,显色方法是用的硫酸碳化法,并且在电炉上烘烤出点。利用TLC来检测反应的完全程度。Rf=原点中心至斑点中心的距离/原点中心至展开剂前沿的距离,用Rf来表示各个组分的位臵。反应完全意味着我们的溶液里面没有了原料,即TLC的原料液点不会随展开剂展开,烤板后只有两个点反应点没有原料点才表示反应完全了。 TLC还用于检测纯目标产物,经过柱层析后,将流出物点到硅胶板上,和标准物对比,在紫外光下观察是否有荧光点,如没有则代表产物还没被层析出来,在给定的紫外线范围内只有产物才有荧光点,我们大概在14管的时候才出现淡淡的荧光点的,该点和标准物在统一展开线上,总层析了20管,从第14管到
(完整word版)药物合成反应的期末试卷
药物合成反应(第三版)的期末试卷 一.选择题(本大题共10题,每空2分,共20分) 1.下列论述正确的是( A ) A吸电子基的有-CHO,-COR,-NH2,-COOH,-NO2,-COOR,-COCl,-CN B酸催化的α-卤化取代反应中,过量卤素存在下反应停留在α-单取代阶段 C一般情况下,不同结构下羧酸的置换活性是脂肪羧酸<芳香羧酸 D活性较大的叔醇、苄醇的卤置换反应倾向于S N2机理,而其他的醇反应以S N1机理为主 2.下列催化剂在F-C反应中活性最强的是 ( B ) A.AlCl3 B.SnCl4 C.ZnCl2 D.FeCl3 3.对卤化剂的影响下面正确的是( A ) A.PCl5>PCl3 >POCl3>SOCl3 B. PCl5>PCl3 >SOCl3>POCl3 C. PCl5>SOCl3>POCl3>PCl3 D. PCl3 >POCl3>SOCl3>PCl5 4.离去基团活性正确的是( D ) A. I->Br->F->Cl- B. I->Br->Cl->F- C. Br->F->I->Cl- D. Br->Cl->F->I- 7.下列哪项不是DDC的特性?( C ) A.脱水剂,吸水剂,应用范围广,用于多肽合成等 B.反应条件温和,在室温下进行 C.反应过程激烈,时间短 D.反应过程缓慢,时间长 8.为了使碘取代反应效果变好,下列哪项不行( C ) A.氧化剂 B.碱性缓冲物质 C.还原剂 D.与HI形成难溶于水的碘化物的金属氧化物 9.下列重排中不是碳原子到碳原子的重排的是( D ) A. Wangner-Meerwein重排 B. 频纳醇重排(Pinacol) C. 二苯乙醇酸型重排 D. Beckmann重排 10.下列什么反应可以用于延长碳链( A ) A.Blanc氯甲基化反应 B.芳醛的α-羟烷基化 C.芳烃的β-羟烷基化 D.β-羰烷基化反应 二.填空题 (本大题共20空,每空1分,共20分) 1.重排反应是指在同一分子内,某一原子或基团从一个原子迁移至另一原子而形成新分子的反应。其按机理可分为?亲电重排、亲核重排、自由基重排、协同重排。 2.DDC缩合法的三个特征是?吸水剂、脱水剂、应用范围广,尤其用于多肽合成;反应条件温和,温室下进行;反应过程缓慢,时间长。 3.常见的酰化试剂有?羧酸、羧酸酯、酸酐、酰氯。 4.几乎可被称为万能催化剂的是?AlCl3 5.Blanc 反应条件ArH+HCHO_ HCl/ZnCl2______ArCH2Cl 6.有机化学反应的实质是旧键的断裂和新键的形成 7.由于分子经过均裂产生自由基而引发的反应称为_自由基型反应________ 8.常用的卤代试剂:卤素、NBS、次卤酸酯、硫酰卤 三.判断题(本大题共10题,每题1分,共10分) 1.分子中存在多个羟基事,M n O2可选择性地氧化烯丙位(或苄位)羟基(对) 2.羧酸酯为酰化剂时,酸催化增强羧酸酯(酰化剂)的活性,碱催化增强醇(酰化剂)的活性(对) 3.相转移催化剂是一种与水相中负离子结合的两性物质,可以把亲核试剂转移到有机相进行亲核反应。(对)
药物合成反应
1、药物合成反应中反应类型有哪些? ①按有机分子的结构变换方式分:新基团的导入反应;取代基的转化反应;有机分子的骨架。 ②按反应机制分:极性反应(a.亲核试剂、b.亲电试剂);自由基反应;协同反应 2、药物合成反应主要研究对象:化学合成药物 3、化学品的安全使用说明书——MSDS 1、混酸硝化试剂的特点有哪些? ①硝化能力强;②氧化性较纯硝酸小;③对设备的腐蚀性小 4.硝酸与醋酸酐的混合酸特点: 1.反应条件温和使用于易被氧化或易被混酸分解的化合物的硝化反应 2.醋酸酐对大部分化合物具有较好的溶解能力,可使反应易于在均相条件下进行,促进反应进行 3.在芳香环的硝化反应中,主要发生单硝化,而且主要发生在邻对位定位基的邻位,属于领位硝化剂 4.硝化能力强 5.硝酸在醋酸酐中可以任意比例溶解,常用的浓度为含硝酸10%--30% 缺点:是不能久置,久置容易生成四硝基甲烷引起爆炸,所以必须使用前临时制备 2、硝化试剂的活泼中间离子为:硝酰正离子NO2○+(在硝酸和醋酸酐作为混合硝化剂中,除NO2○+还有N2O5,CH3COON2H○+) 重氮化反应: 1.、重氮化反应定义:含有伯氨基的有机化合物在无机酸的存在下与亚硝酸钠作用生成重氮盐的反应。 2.常用的重氮化试剂 一般是由NaNO2/HCL NoHSO4/H2SO4 CuSO4 磷酸/H2SO4 CH3OH 。 3.Sandmeyer反应(桑德迈尔反应)定义 定义:在氯化亚铜或溴化铜的存在下,重氮基被氮或溴置换的反应;重氮基被氰基置换:将重氮盐与氰化亚铜的配合物在水介质中作用,可以使重氮基被氰基置换,该反应也称Sandmeyer。 4、常用的重氮化试剂 一般是由盐酸、硫酸、过氯酸和氟硼酸等无机酸与亚硝酸钠作用产生。 5、硝化反应定义:指向有机分子结构中引入硝基(—NO2)的反应过程,广义的硝化反应包括生产(—NO2、N—NO2和O—NO2)反应。 6、重氮化反应定义:含有伯氨基的有机化合物在无机酸的存在下与亚硝酸钠作用生成重氮盐的反应。 卤化反应 卤化反应:指在有机分子中引入卤素原子的反应 8、自由基反应三阶段:链引发、链增长、链终止 1、Ph上取代基对卤化反应的影响 1.立体效应 2.电子效应:PH上有给电子基团时,使PH活化,卤化反应容易进行,甚至发生多卤化效应,产物以邻位,对位为主,芳环上有吸电子基团时,使芳环钝化,以间位产物为主(-OH,-NO2给电子基团) 3. 产生自由基的方法:1.热烈法2.光解法3.电子转移法 2、醇与HCl发生卤置换反应活性顺序 醇羟基的活性顺序:叔(苄基、烯丙基)醇>仲醇>伯醇 氢卤酸的活性顺序:HI>HBr>HCL 3、NBS的应用(N—溴代丁二酸亚胺) hv
药物合成技术
课程超市入选课程申请表
《制药工艺学》课程教学大纲 适用专业 _________ 制药工艺学 ______________ 学 时 ___________ 72 __________________ 学 分 ___________ 4 ___________________ 第一部分 课程说明 课程代码:050053 课程名称:制药工艺学 开课学期:4 课程类型:职业方向课 课程的性质和任务: 本课程是生物化工工艺专业的必修课。通过这门课程的理论和实践教学的学 习,使学生能够掌握药物合成及相关职业所必需的基本理论知识、基本方法和基本 操作技能,为毕业后很快胜任药厂不同制剂岗位群工作奠定坚实的基础。 本门课程与其他课程关系: 本课程是生物化工工艺类专业学生学习药物合成的专业课程。前导课程为《生 物化学》、《微生物》、《药物化学》和其专业相关的生产工艺类知识 第二部分教学内容纲要 教学内容及要求 第1部分: 课程内容:绪论 教学要求:1、药物合成技术的研究现象和内容 2、 制药工业的特点 3、 制药工业的现状及发展趋势 第2部分: 课程内容: 酰化反应技术 教学要求: 1、 酰化反应 2、 应用实例 阿司匹林的合成 3、 实验实训 阿司匹林的合成和精制 第3部分: 课程内容:还原反应技术 推荐教材及参考书: 《现代生物制药工艺学》 《现代生物制药工艺学》 (高职高专教材) 辛秀兰化学工业出版社 (高职高专教材) 李家洲中国轻工业出版社
教学要求: 1、还原反应 2、应用实例——对乙酰氨基酚的合成 3、实验实训——对乙酰氨基酚的实验室合成 第4 部分: 课程内容:卤化反应技术 教学要求: 1、卤化反应 2、应用实例——诺氟沙星的合成 3、实验实训——诺氟沙星的实验室合成 第5 部分: 课程内容:烃化反应技术 教学要求:1、烃化反应 2、应用实例——磺胺甲噁唑的合成 第6 部分: 课程内容:缩合反应技术 教学要求:1 、缩合反应 2、光学异构药物的拆分 3、应用实例——氯霉素的合成技术 4、氯霉素生产中的综合利用与“三废”处理 5、实验实训——氯霉素的实验室合成 第7 部分: 课程内容:氧化反应技术 教学要求:1、氧化反应及常用氧化剂 2、消除反应 3、应用实例——氢化可的松的合成技术 第8 部分: 课程内容:发酵制药技术 教学要求:1、微生物发酵制药技术 2、维生素C 概述 3、应用实例——莱氏法生产维生素 C 工艺原理和过程 4、应用实例——两步发酵法生产维生素 C 工艺过程 5、莱氏法和两步发酵法的比较及维生素 C 收率的计算 6、维生素C 生产中“三废”治理和综合利用 第9 部分: 课程内容:溶剂和催化剂应用技术 教学要求:1、溶剂对化学反应的影响 2、催化剂对化学反应的影响 3、抗生素的概述 4、半合成青霉素的合成技术
