环己烷-乙醇相图实验

数据处理:
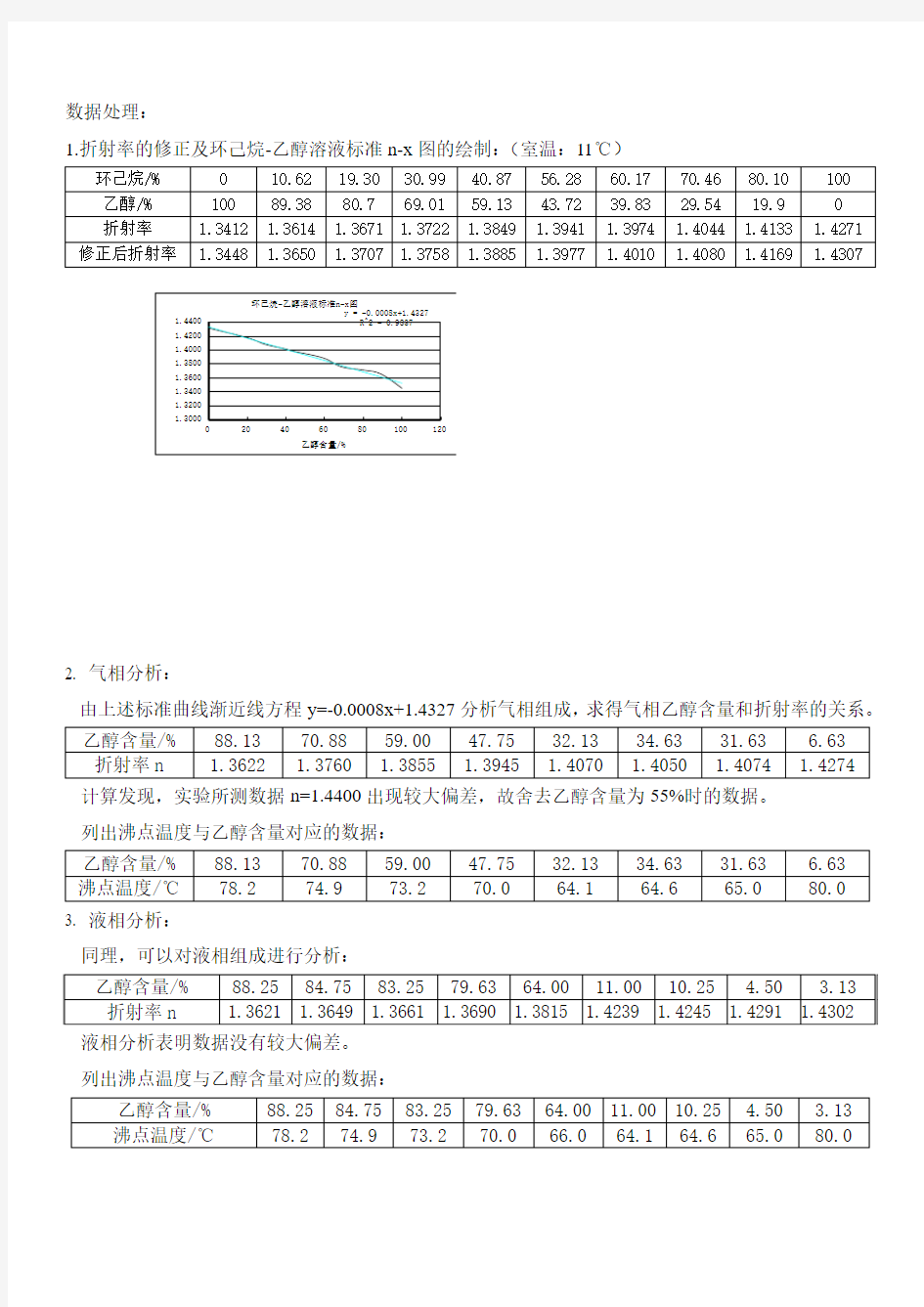
1.折射率的修正及环己烷-乙醇溶液标准n-x 图的绘制:(室温:11℃)
2. 气相分析:
由上述标准曲线渐近线方程
y=-0.0008x+1.4327分析气相组成,求得气相乙醇含量和折射率的关系。 计算发现,实验所测数据n=1.4400出现较大偏差,故舍去乙醇含量为55%
时的数据。 列出沸点温度与乙醇含量对应的数据: 3. 液相分析:
同理,可以对液相组成进行分析:
液相分析表明数据没有较大偏差。 列出沸点温度与乙醇含量对应的数据:
4.环己烷-乙醇相图的绘制及分析:
根据以上两组数据作出环己烷-乙醇的t-x图,即环己烷-乙醇体系相图:
求得其交点,即最低恒沸点的坐标(34.63,64.6),即恒沸组成:乙醇34.63%,环己烷65.37%,最低恒沸点温度约为64.6℃。
分离乙醇正丙醇混合液的精馏塔设计课程设计共46页word资料
TOC \o "1-3" \h \u 一设计任务书.. PAGEREF _Toc7399 2 二塔板的工艺设计 (5) (一)设计方案的确定 (5) (二)精馏塔的物料衡算 (5) 1.原料液及塔顶、塔釜产品的摩尔分数 (5) 2. 物料衡算 (6) (三)物性参数的计算 (6) 1.操作温度的确定 (7) 2. 密度的计算 (7) 3.混合液体表面张力的计算 (11) 4.混合物的粘度 (12) 5.相对挥发度 (13) (四)理论板数及实际塔板数的计算 (14) 1.理论板数的确定 (14) 2.实际塔板数确定 (18) (五)热量衡算 (18) 1.加热介质的选择 (18)
2. 冷却剂的选择: (19) 3.比热容及汽化潜热的计算 (19) (六)塔径的初步设计 (23) 1.汽液相体积流量的计算 (23) 2.塔径的计算与选择 (23) (七)溢流装置 (25) 1.堰长 (25) 2.弓形降液管的宽度和横截面积 (25) 3.降液管底隙高度 (26) 4.塔板分布 (26) 5. 浮阀数目与排列 (26) (八)汽相通过浮阀塔板的压降 (29) 1.精馏段 (29) 2.提馏段 (30) (九)淹塔 (30) 1.精馏段 (30) 2.提馏段 (31) (十)雾沫夹带 (31)
(十一)塔板负荷性能图 (32) 1.雾沫夹带线 (32) 2.液泛线 (34) 3.液相负荷上限线 (35) 4.漏液线 (35) 5.液相负荷下限线 (35) 三、塔总体高度计算 (38) 1.塔顶封头 (39) 2.塔顶空间 (39) 3.塔底空间 (39) 5.进料板处板间距 (40) 6.裙座 (40) 四、塔的接管 (40) 1.进料管 (40) 2.回流管 (41) 3.塔底出料管 (41) 4.塔顶蒸汽出料管 (41) 5.塔底蒸汽管 (42)
双液系的气液平衡相图
实验五双液系的气液平衡相图 摘要: 本实验利用阿贝折射仪测定液体和蒸气的组成,并用折光率确定双组分体系的组成,绘制在一大气压下水——正丙醇双液系的气液平衡相图,从而确定其最低恒沸点温度及恒沸混合物的组成。 关键词: 双液系气液平衡相图最低恒沸点 Abstract: This experiment using abbe refraction analyzer to measure liquid and the composition of the steam, and determine the refractive index of the two components system composition, draw in a water-was propanol, atmospheric pressure double liquid gas and liquid of the department of equilibrium phase diagram, so as to determine the minimum constant boiling point temperature and the composition of the azeotropic mixture. Key-words: bi-liquid system gas-liquid equilibrium phase-graph lowest constant boiling point 前言: 一、实验原理 在常温下,两液态物质混合而成的体系称为双液系。两液体若只能在一定比例范围内互相溶解,称为部分互溶双液系,若两液体能以任意比例相互溶解,则称为完全互溶双液系。例如:苯-乙醇体系,正丙醇-水体系,环己烷—乙醇体系都是完全互溶双液系,苯-水体系则是部分互溶双液系。 液体的沸点是指液体的蒸气压与外压相等时的温度。在一定的外压下,纯液体的沸点有确定的值。但对于双液系来说,沸点不仅与外压有关,而且还与双液系的组成有关,即与双液系中两种液体的相对含量有关。 双液系在蒸馏时具有另一个特点是:在一般情况下,双液系的气相组成和液相组成并不相同。因此原则上有可能用反复蒸馏的方法,使双液系中的两液体互相分离。 通常用几何作图的方法将双液系的沸点对其气相、液相组成作图,所得图形称为双液系T-x相图,在一定温度下还可画出体系的压力P与组成的P-x关系图。完全互溶双液系在恒定压力下的气液平衡相图可分为三类: 如果溶液与拉乌尔定律的偏差不大,在T—x图上,溶液的蒸汽压和沸点介于A,B两纯组分蒸汽压及沸点之间,如甲苯-苯体系(图5-1)所示,为第一类。 实际溶液由于A—B两组分的相互影响,常与拉乌尔定律有较大的偏差。在T—X图上
异丙醇-环己烷双液系相图
渤海大学学生实验报告 课程名称:任课教师: 实验室名称:物理化学实验室(二)房间号实验时间: 2013 年月日 学院化学化工与食品安全学院专业班级 姓名学号同组人 实验项目异丙醇-环己烷双液系相图组别实验成绩 一、实验目的 1、了解物理化学实验中常用的物理方法-光学方法的基本原理 2、绘制异丙醇-环己烷双液系的沸点-组成图,确定其沸点组成及衡沸温度 3、进一步理解分馏原理 4、掌握阿贝折射计的原理及使用方法 二、实验原理 在常温下两种液态以任意比例相互溶解所组成的体系称之为完全互溶双液系。在恒定压力下,表示溶液沸点与组成关系的图称之为沸点-组成图。 本实验利用回流及分析的方法来绘制相图。取不同组成的溶液在沸点仪中回流,测定其沸点及其气液组成。沸点数据可由温度计获得,气-液相组成可通过测其折射率,然后由组成-折射率曲线中最后确定。 三、仪器与试剂 沸点测定仪阿贝折射仪吸液管调压变压器温度计 移液管(1ml 10ml 25ml) 异丙醇环己烷 四、实验装置 渤海大学实验报告用纸(第页共页)
五、实验步骤 1.已知浓度溶液折射率的测定 取异丙醇和环己烷以及环己烷摩尔分数分别为0.2、0.4、0.6、0.8四种组成的溶液在25℃下,逐次用阿贝折射计测定其折射率,绘制组成-折射率的关系曲线;2,溶液沸点及气液组成的测定 (1)取25ml异丙醇于沸点测定仪之蒸馏瓶内,连好路线,打开回流冷却水,接通电源加热至沸腾。待温度恒定后,记下温度将调压变压器调至零处,停止加热充分冷却后取样,用阿贝折射计分别测定气相和液相冷凝液的折射率,按上述步骤分别测各液体的沸点及气相冷凝液和液相折射率; (2)将蒸馏瓶内的溶液倒入回馏瓶中,并用环己烷清洗蒸馏瓶,然后取25ml环己烷于蒸馏瓶内,按(1)的操作步骤进行,以后分别加入异丙醇 0.2ml,0.3ml,0.5ml,1ml,4ml,5ml,测定其沸点及气相冷凝液和液相折射 率。 六、数据记录和处理 大气压:大气压:101.56kpa; 压力校正因素:溶液沸点与大气压有关 沸点校正:△t=t/10 *(101.325-p)/101.325 t b =t+△t 编号 项目 1 2 3 4 5 6 7 8 t0c 66.4 64.6 63.9 64.1 64.3 64.6 65.7 71.6 气相n y 1 1.4029 1.4027 1.401 2 1.4005 1.3995 1.3988 1.3962 1.3842 2 1.4027 1.4028 1.4010 1.4007 1.3994 1.3987 1.3964 1.3843 平均 1.4028 1.4027.5 1.4011 1.4006 1.39945 1.39875 1.3963 1.38425 x g 41.4 42.2 45.0 45.8 47.9 49.6 61.4 69.0 液相 n x 1 1.421 2 1.4191 1.4119 1.4106 1.3891 1.3831 1.3751 1.3637 2 1.4211 1.4190 1.4120 1.4108 1.3890 1.3832 1.3750 1.3635 平均 1.42115 1.41905 1.41195 1.4007 1.38905 1.38315 1.37505 1.3636 x l 5.8 10.0 25.0 4 6.1 63.8 70.4 80.0 94.8 △t -0.0154 -0.0150 -0.0148 -0.0149 -0.0149 -0.0150 -0.0152 -0.0166 t b 66.3846 64.585 63.8852 64.0851 64.2851 64.585 65.6848 71.5834 恒沸温度校正前63.95 后63.94 恒沸组成x g = x l =45.7 渤海大学实验报告用纸(第页共页)
乙醇和正丙醇物系分离系统的设计
北京理工大学珠海学院 课程设计任务书 2011 ~2012学年第一学期 学生姓名:谢威宁专业班级:09化工1班 指导教师:李青云工作部门:化工与材料学院 一、课程设计题目乙醇和正丙醇物系分离系统的设计 二、课程设计内容(含技术指标) 1.设计条件 生产能力:25000吨/年(每年按300天生产日计算) 原料状态:苯含量40%(wt%);温度:25℃;压力:100kPa;泡点进料; 分离要求:塔顶馏出液中苯含量99%(wt%);塔釜苯含量2%(wt%)操作压力:100kPa 其它条件:塔板类型:浮阀塔板;塔顶采用全凝器;R=1.9R m 2.具体设计内容和要求 (1)设计工艺方案的选定 (2)精馏塔的工艺计算 (3)塔板和塔体的设计 (4)水力学验算 (5)塔顶全凝器的设计选型 (6)塔釜再沸器的设计选型 (7)进料泵的选取 (8)绘制流程图 (9)编写设计说明书 (10)答辩
三、进度安排 时间设计安排 10.26—10.28 设计动员,下达任务书,查阅资料,拟定设计方案,方案论证,物性数据计算 10.28—11.11 工艺计算(物料衡算、确定回流比、计算理论板层数、实际板层数、实际进料板位置) 11.11—11.18 塔结构设计(物性数据的计算、塔径计算、塔结构尺寸的计算、水力学性能校验、负荷性能图及塔高的计算) 11.18—11.25 热量衡算;附属设备的选型和计算 11.25-12.02 绘制带控制点的工艺流程图(CAD图) 12.02—12.09 绘制带控制点的工艺流程图,(借图板和丁字尺,手工绘制图)12.09—12.16 编写设计说明书,答辩要求 2012.01.03 将说明书及图纸装订并提交 2012.1.4—1.5 答辩 四、基本要求 序号设计内容要求 1 设计工艺方案的选定精馏方式及设备选型等方案的选定和论证(包括 考虑经济性;工艺要求等)绘制简单流程图 2 精馏塔的工艺计算物料衡算,热量衡算,回流比、全塔效率、实际 塔板数、实际进料位置等的确定 3 塔板和塔体的设计设计塔高、塔径、溢流装置及塔板布置等 4 水力学验算绘制塔板负荷性能图 5 塔顶全凝器的设计选型计算冷凝器的传热面积和冷却介质的用量 6 塔釜再沸器的设计选型计算再沸器的传热面积和加热介质的用量 7 进料泵的选取选取进料泵的型号 8 绘图绘制带控制点的流程图(CAD和手工绘制) 9 编写设计说明书目录,设计任务书,设计计算结果,流程图,参 考资料等 10 答辩每班数不少于20人答辩 教研室主任签名: 2011年10 月14 日
环己烷-异丙醇双液系相图
2.6 环己烷-异丙醇双液系相图 2.6.1 实验目的 1.了解物理化学实验手段中常用的物理方法—光学方法的基本原理。 2.绘制环己烷-异丙醇双液系的沸点~组成图,并找出恒沸点及恒沸点混合物的组成。 3.进一步理解分馏原理。 4.掌握阿贝折射仪的原理及使用方法。 2.6.2 实验原理 单组分液体在一定的外压下沸点为一定值。把两种完全互溶的挥发性液体(组分A和B)混合后,在一定的温度下,平衡共存的气液两相组成通常并不相同。因此在恒压下将溶液蒸馏,测定馏出物(气相)和蒸馏液(液相)的组成,就能找到平衡时气、液两相的成分并绘出T—x图,即所谓的相图。完全互溶双液系在恒定压力下的沸点~组成图可分为三类:(1)液体与拉乌尔定律的偏差不大,沸点介于A、B两纯组分沸点之间(图6一1),如苯~甲苯体系。(2) A、B两纯组分混合后与拉乌尔定律有较大的正偏差,溶液存在最低沸点(图6一2),如水~乙醇;苯~乙醇等体系。(3)实际溶液由于A、B两纯组分相互影响,常与拉乌尔定律有较大负偏差,溶液存在最高沸点(图6一3),如盐酸~水体系;丙酮~氯仿体系。 图6—1 偏差不大的体系图6—2 正偏差很大的体系图6—3 负偏差很大的体系对(2)、(3)类体系有时被称为具有恒沸点的双液系。它与(1)类的根本区别在于,体系处于恒沸点时气、液两相的组成相同。因而也就不能象(1)类那样通过反复蒸馏而使双液系的两个组分完全分离。对(2)、(3)类的溶液进行简单的反复蒸馏只能获得某一纯组分和组成为恒沸点的相应组成的混合物。如要获得两纯组分,需采取其他方法。体系的最低或最高恒沸点即为恒沸温度,恒沸温度对应的组成为恒沸组成。环己烷-异丙醇双液系属于具有最低恒沸点一类。 为了绘制沸点~组成图,可采取不同的方法。比如取该体系不同组成的溶液,用化学 分析方法分析沸腾时该组成的气、液组成,从而绘制出完整的相图。可以想象,对于不同 的体系要用不同的化学分析方法来确定其组成,这种方法是很繁杂的。特别是对于一些体 系还无法建立起精确、有效的化学分析方法,其相图的绘制就更为困难。物理学的方法为 物理化学的实验手段提供了方便的条件,如光学方法。在本实验中的折射率的测定,就是 一种间接获取组成的办法。它具有简捷、准确的特点。 本实验就是利用回流及分析的方法来绘制相图。取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成。沸点数据可直接由温度计获得;气、液相组成可通过测其折
双液系的气—液平衡相图
实验五双液系的气—液平衡相图 一、实验目的 1、绘制在标准压力下乙醇-正丙醇体系的沸点组成图,并确定其恒沸点及恒沸组成; 2、熟练掌握测定双组分液体沸点的方法及用折光率确定二组分物系组成的方法; 3、掌握超级恒温槽、阿贝折射仪、气压计等仪器的使用方法。 二、实验原理 1、相图 任意两个在常温时为液态的物质混合起来组成的体系称为双液系。两种溶液若能按任意比例进行溶解,称为完全互溶双液系,如环已烷-乙醇、正丙醇-乙醇体系都是完全互溶体系。若只能在一定比例范围内溶解,称为部分互溶双液系,例苯-水体系。 在完全互溶双液系中,有一部分能形成理想液态混合物,如苯-甲苯系统,二者的行为均符合拉乌尔定律,但大部分双液系是非理想液态混合物,其行为与拉乌尔定律有偏差。 液体的沸点是指液体的蒸气压与外界压力相等时的温度。在一定外压下,纯液体的沸点有其确定值,但双液系的沸点不仅与外压有关,而且还与两种液体的相对含量有关。双液系两相平衡时的气相组成和液相组成并不相同。 通常用几何作图的方法将双液系的沸点对其气相和液相的组成作图,所得图形叫双液系的沸点T(或t)-组成(x)图,即T(或t)—x图。它表明了沸点与液相组成和与之平衡的气相组成之间的关系。 在恒定压力下,二组分系统气液达到平衡时,其沸点-组成(t-x)图分三类: (1)混合液的沸点介于A、B二纯组分沸点之间。这类双液系可用分馏法从溶液中分离出两个纯组分。如苯-甲苯系统,此时混合物的行为符合拉乌尔定律或对拉乌尔定律的偏差不大。如图5-1(a)所示。 (2)有最低恒沸点体系,如环已烷-乙醇体系,t—x图上有一个最低点,此点称最低恒沸点,在此点相互平衡的液相和气相具有相同的组成,此时混合物的行为对拉乌尔定律产生最大正偏差,如图5-1(b)所示。对于这类的双液系,用分馏法不能从溶液中同时分离出两个纯组分。 (3)有最高恒沸点体系,如氯仿-丙酮体系,t—x图上有一个最高点,此点称最高恒沸点,在此点相互平衡的液相和气相具有相同的组成,此时混合物的行为对拉乌尔定律产生最大负偏差,如图5-1(c)所示。对于这类的双液系,用分馏
异丙醇—环己烷双液系相图
异丙醇—环己烷双液系相图
————————————————————————————————作者:————————————————————————————————日期:
实验四异丙醇—环己烷双液系相图 一、实验目的: 1.了解物理化学实验手段中常用的物理方法—光学方法的基本原理。 2.绘制异丙醇—环己烷双液系的沸点—组成图,确定其恒沸组成及恒沸温度。 3.进一步理解分馏原理。 4.掌握阿贝折射计的原理及使用方法。 二.基本原理: 根据相律:f + φ = c + 2 ,对二组分体系:f = 4 - φ,f max = 3 (T,P,x)。 对于二组分体系,常常保持一个变量为常量,而得到立体图形的平面截面图。这种平面图可以有三种:p-x图,T-x图,T-p图。常用的是前两种。在平面图上,f*=3-φ,f*max=2,同时共存的相数φmax=3。 单组分的液体在一定外压下,它的沸点是一定值,把两种完全互溶的挥发性液体(组分A和B)互相混合后,在某一定温度下,平衡共存的气液两相的组成,通常并不相同,因此如果在恒压下将溶液蒸馏,测定馏出物(气相)和蒸馏液(液相)的折射率,就能找出平衡时气液两相的成分,并绘出沸点—组成(T—x)图线,在常温下,两种液态物质以任意比例相互溶解所组成的体系称之为完全互溶双液系。完全互溶双液系在恒定压力下的沸点—组成图可分为三类: (1)溶液沸点介于两纯组分沸点之间(如图1),(2)溶液存在最低沸点(图2)和(3)溶液存在最高沸点(图3)。 (2)、(3)被称为具有恒沸点的双液系,即体系处于恒沸点时气、液两相的组成相同,其相应的溶液称为恒沸点混合物。此时对恒沸点混合物进行蒸馏,所得气相与液相组成相同,因此我们不能用普通蒸馏方法获得任一纯组分。异丙醇—环己烷双液系属于具有最低恒沸点一类的体系。 T—x图在进行蒸馏或分馏时是必不可少的,而分馏在提纯溶剂和石油工业中也得到广泛应用,所以这种图是具有很大的实用价值的。 本实验的目的就是要绘制异丙醇—环己烷的T—x图并找出恒沸点混合物的组成。1.沸点—组成图的绘制 为了绘制沸点—组成图,可采取不同的方法。在本实验中,我们采用的是一种物理方法—通过折射率的测定,来间接的获取溶液组成,它具有简捷、准确的特点。 本实验就是利用回流及分析的方法来绘制相图。取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成。沸点数据可直接由温度计获得,气、液相组成可通过测其折射率,然后由组成—折射率曲线中最后确定。以沸点对组成作图,将所有的气、液相组成连起来,即成相图。
课程设计:分离乙醇和正丙醇(详细版)
一、课程设计题目乙醇和正丙醇物系分离系统的设计 二、课程设计内容(含技术指标) 1.设计条件 生产能力:25000吨/年(每年按300天生产日计算) 原料状态:乙醇含量35%(wt%);温度:25℃;压力:100kPa;泡点进料; 分离要求:塔顶馏出液中乙醇含量99%(wt%);塔釜乙醇含量2%(wt%)操作压力:100kPa 其它条件:塔板类型:浮阀塔板;塔顶采用全凝器;R=1.5R m 2.具体设计内容和要求 (1)设计工艺方案的选定 (2)精馏塔的工艺计算 (3)塔板和塔体的设计 (4)水力学验算 (5)塔顶全凝器的设计选型 (6)塔釜再沸器的设计选型 (7)进料泵的选取 (8)绘制流程图 (9)编写设计说明书 (10)答辩 三、进度安排
四、基本要求 教研室主任签名: 年月日 摘要 精馏是分离液体混合物最常用的一种单元操作,在化工,炼油,石油化工等领域中被广泛应用。精馏是使易挥发组分进入气相,难挥发组分进入液相,从而使液体混合物分离。本次设计任务为处理25000吨/年的乙醇和正丙醇混合物。 浮阀塔是在泡罩塔的基础上发展起来的,它主要的改进是取消了升气管和泡罩,在塔板开孔上设有浮动的浮阀,浮阀可根据气体流量上下浮动,自行调节,使气缝速度稳定在某一数值。这一改进使浮阀塔在操作弹性、塔板效率、压降、生产能力以及设备造价等方面比泡罩塔优越。但在处理粘稠度大的物料方面,又不及泡罩塔可靠。浮阀塔广泛用于精馏、吸收以及脱吸等传质过程中。本设计通过物料衡算,热量衡算,工艺计算,结构设计和校核等一系列工作来设计一个具有可行性的合理的浮阀塔。 关键词浮阀塔乙醇正丙醇回流比
最新实验五环己烷-异丙醇双液系平衡相图的绘制数据处理
实验五环己烷-异丙醇双液系平衡相图的绘 制数据处理
环己烷-异丙醇的折光率与质量分数曲线 室温:24.5℃ 大气压值:102.06kpa 异丙醇量/cm3环己烷 量/cm3沸点t/℃气相冷凝液液相冷凝液 n D w(异丙醇)%n D w(异丙醇)% 125081.8+(0.65) 1.3749+(0.0032)100 1.3749+(0.0032)100 225180.8+(0.65) 1.3771+(0.0032)95.95431 1.3750+(0.0032)99 325279.2+(0.65) 1.3829+(0.0032)83.95515 1.3761+(0.0032)98.02313 425377.48+(0.65) 1.3848+(0.0032)80.02439 1.3779+(0.0032)96.36807 525476.48+(0.65) 1.3864+(0.0032)76.71428 1.3786+(0.0032)92.85107 625575.65+(0.65) 1.3887+(0.0032)71.95599 1.3782+(0.0032)93.6786 7251071.4+(0.65) 1.3962+(0.0032)56.43984 1.3840+(0.0032)81.67944 80.22579.75+(0.65) 1.4204+(0.0032) 6.37438 1.4213+(0.0032) 4.51244 90.32578.8+(0.65) 1.4192+(0.0032)8.85697 1.4217+(0.0032) 3.68491 100.52577.48+(0.65) 1.4173+(0.0032)12.78772 1.4215+(0.0032) 4.09868 1112574.08+(0.65) 1.4103+(0.0032)27.26947 1.4218+(0.0032) 3.47803 1242570.3+(0.65) 1.4037+(0.0032)40.92368 1.4138+(0.0032)22.09742 1352570.02+(0.65) 1.4046+(0.0032)39.06174 1.4142+(0.0032)18.99419 环己烷标准折光率:1.4266折射校正值:+0.0032 异丙醇的标准沸点:82.45℃温度校正值:+0.65
乙醇正丙醇分离设计
化工原理课程设计任务书 1.设计题目: 常压连续筛板式精馏塔分离乙醇—正丙醇二元物系的设计。 2.原始数据及条件: 进料:乙醇含量0.5(摩尔分数,下同),其余为正丙醇,F=3400Kg/h,塔顶进入全凝器,塔板压降0.7Kpa。 分离要求:塔顶乙醇含量0.90;回收率为0.95;全塔效率0.55。 操作条件:塔顶压强1.03atm(绝压);泡点进料; R/Rmin=1.6 。 3.设计任务: (1)完成该精馏塔的各工艺设计,包括设备设计及辅助设备选型。(2)画出带控制点的工艺流程图、塔板版面布置图、精馏塔设计条件图。 (3)写出该精馏塔的设计说明书,包括设计结果汇总和设计评价。
摘要 在本次任务中,根据化工原理课程设计的要求设计的是乙醇----丙醇连续浮阀精馏塔,除了要计算其工艺流程、物料衡算、热量衡算、筛板塔的设计计算,以外,并对精馏塔的主要工艺流程进行比较详细的设计,并画出了精馏塔的工艺流程图和设备条件图。 本次设计选取回流比R=1.8Rmin=1.6×1.34=2.144应用图解法计算理论版数,求得理论塔板NT为12块(包括塔釜再沸器),第6块为进料板。设计中采用的精馏装置有精馏塔 ,冷凝器等设备,采用间接蒸汽加热,物料在塔内进行精馏分离,余热由塔顶产品冷凝器中的冷却介质带走,完成传热传质. 塔的附属设备中,所有管线均采用无缝钢管。预热器采用管壳式换热器。用99.97℃塔釜液加热。料液走壳程,釜液走管程。本设计采用了筛板塔对乙醇-丙醇进行分离提纯,塔板为碳钢材料,通过板压降、漏液、液泛、液沫夹带的流体力学验算,均在安全操作范围内。 关键字:乙醇-丙醇筛板塔物料衡算
异丙醇—环己烷双液系相图
实验四异丙醇—环己烷双液系相图 一、实验目的: 1.了解物理化学实验手段中常用的物理方法—光学方法的基本原理。 2.绘制异丙醇—环己烷双液系的沸点—组成图,确定其恒沸组成及恒沸温度。 3.进一步理解分馏原理。 4.掌握阿贝折射计的原理及使用方法。 二.基本原理: 根据相律: f + = c + 2 ,对二组分体系: f = 4 - ,f max = 3 (T,P,x)。 对于二组分体系,常常保持一个变量为常量,而得到立体图形的平面截面图。这种平面图可以有三种:p-x图,T-x图,T-p图。常用的是前两种。在平面图上,f*=3-,f*max=2,同时共存的相数max=3。 单组分的液体在一定外压下,它的沸点是一定值,把两种完全互溶的挥发性液体(组分A和B)互相混合后,在某一定温度下,平衡共存的气液两相的组成,通常并不相同,因此 如果在恒压下将溶液蒸馏,测定馏出物(气相)和蒸馏液(液相)的折射率,就能找出平衡 时气液两相的成分,并绘出沸点—组成(T—x)图线,在常温下,两种液态物质以任意比 例相互溶解所组成的体系称之为完全互溶双液系。完全互溶双液系在恒定压力下的沸点—组 成图可分为三类: (1)溶液沸点介于两纯组分沸点之间(如图1),(2)溶液存在最低沸点(图2)和(3)溶液存在最高沸点(图3)。 (2)、(3)被称为具有恒沸点的双液系,即体系处于恒沸点时气、液两相的组成相同, 其相应的溶液称为恒沸点混合物。此时对恒沸点混合物进行蒸馏,所得气相与液相组成相同, 因此我们不能用普通蒸馏方法获得任一纯组分。异丙醇—环己烷双液系属于具有最低恒沸点 一类的体系。 T—x图在进行蒸馏或分馏时是必不可少的,而分馏在提纯溶剂和石油工业中也得到广 泛应用,所以这种图是具有很大的实用价值的。 本实验的目的就是要绘制异丙醇—环己烷的T—x图并找出恒沸点混合物的组成。 1.沸点—组成图的绘制 为了绘制沸点—组成图,可采取不同的方法。在本实验中,我们采用的是一种物理方法—通过折射率的测定,来间接的获取溶液组成,它具有简捷、准确的特点。 本实验就是利用回流及分析的方法来绘制相图。取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成。沸点数据可直接由温度计获得,气、液相组成可通过测其折射率, 然后由组成—折射率曲线中最后确定。以沸点对组成作图,将所有的气、液相组成连起来, 即成相图。
双液系的气液平衡相图
实验3 双液系的气液平衡相图 钱佳鹏 120242119 3.1实验目的与要求 3.1.1用沸点仪测定在一大气压下环已烷-乙醇双液系的气液平衡相图,确定其最低恒沸点温度及恒沸混合物的组成。 3.1.2掌握双组分体系沸点的测定方法。通过实验进一步理解分馏原理。 3.1.3用阿贝折射仪测定液体和蒸气的组成,学会用折光率确定双组分体系的组成。 3.2预习要求 3.2.1了解绘制双液系相图的基本原理。 3.2.2了解阿贝折射仪的使用方法。 3.2.3了解本实验中的注意事项,如何判断气—液两相已达到平衡。 3.3实验原理 在常温下,两液态物质混合而成的体系称为双液系。两液体若只能在一定比例范围内互相溶解,称为部分互溶双液系,若两液体能以任意比例相互溶解,则称为完全互溶双液系。例如:苯—乙醇体系、正丙醇—水体系、环已烷—乙醇体系都是完全互溶双液系,苯—水体系则是部分互溶双液系。 液体的沸点是指液体的蒸气压与外压相等时的温度。在一定的外压下,纯液体的沸点有确定的值。但对于双液系来说,沸点不仅与外压有关,而且还与双液系的组成有关,即与双液系中两种液体的相对含量有关。 双液系在蒸馏时具有另一个特点是:在一般情况下,双液系的气相组成和液相组成并不相同。因此原则上有可能用反复蒸馏的方法,使双液系中的两液体互相分离。 通常用几何做图的方法将双液系的沸点对其气相、液相组成做图,所得图形称为双液系T —χ相图,在一定温度下还可画出体系的压力与组成的P —χ关系图。完全互溶双液系在恒定压力下的气液平衡相图可分为三类: 如果溶液与拉乌尔(Raoult )定律的偏差不大, 在T —χ相图上,溶液的蒸气压和沸点介于A-B 两纯组分蒸气压及沸点之间,如甲苯—苯体系图3—1所示,为第一类。 图3—1 完全互溶体系的一种蒸馏相图 图3—2 完全互溶双液系的另一种蒸馏相图 图3—3 完全互溶双液系的另一种蒸馏相图
异丙醇-环己烷气液平衡相图
实验七 异丙醇-环己烷气液平衡相图 一、实验目的 1. 了解绘制双液系相图的基本原理和方法; 2. 采用回流冷凝法测定不同浓度的异丙醇-环己烷体系的沸点和气液两相平衡成分,绘制常压下环己烷-异丙醇双液系的T-x图,并找出恒沸点混合物的组成和最低恒沸点; 3.学会使用阿贝折射仪。 二、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。 液体的沸点是指液体的蒸气压与外界大气压相等时的温度。在一定的外压下,纯液体有确定的沸点。而双液体系的沸点不仅与外压有关,还与双液体系的组成有关。图17-1(a)是一种最简单的完全互溶双液系的T-x图(像苯与甲苯)。图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xb (或质量百分组成),上面一条是气相线,下面一条是液相线,对应于同一沸点温度的二曲线上的两个点,就是互相成平衡的气相点和液相点,其相应的组成可从横轴上获得。因此如果在恒压下将溶液蒸馏,测定气相馏出液和液相蒸馏液的组成就能绘出T-x图。 某些完全互溶的双液体系近似遵循拉乌尔定律,其正(或负)偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间(见图17-1(a)),如甲醇与水、二硫化碳与四氯化碳等。大多数实际溶液由于A、B二组分的相互影响,常会与拉乌尔定律有较大偏差,在T-x图上会有最高或最低点出现,如图17-1(b)、(c)所示。这些点称为恒沸点,其相应的溶液称为恒沸点混合物。恒沸点混合物蒸馏时,所得的气相与液相组成不变,靠蒸馏无法改变其组成。如HCl与水、丙酮与氯仿、硝酸与水等的体系具有最高恒沸点,苯与乙醇、异丙醇与环己烷、水与乙醇等的体系则具有最低恒沸点。 具有恒沸点的双液系与理想溶液或偏差很小的近似理想溶液的双液系的根本区别在于,体系处于恒沸点时气液两相的组成相同,因而也就不能像前者那样通过反复 蒸馏而使双液系的两个组分完全分离,因为对这样的溶液进行简单的反复蒸馏智能获得某一纯组分和组成为恒沸点的混合物。 绘制沸点-成分图的简单原理如下:当总成分为x的溶液开始蒸馏时,体系的温度沿虚线上升,开始沸腾时成分为y的气相开始生成,若气相量很少,x、y二点即代表互成平衡的液、气二相成分。继续蒸馏,气相量逐渐增多,沸点沿虚线继续上升,气、液二相成分分别在气相线和液相线上沿箭头指示方向变化。当二相成分达到某一对数值x′和y′,维持二相的量不变,则体系气.液二相又在此成分达成平衡,而二相的物质数量按杠杆原理分配。 从相律来看,对二组分体系,当压力恒定时,在气、液二相共存区域中,自由度数等于1,若温度一定,气、液二相成分也就确定。当总成分一定时,由杠杆原理知,二相的相对量也一定。反之.在一定的实验装置中,利用回流的方法保持气、液二相相对量一定,则体系温度也恒定。待二相平衡后,取出二相的样品、用物理方法或化学方法分析二相的成分。给出在该温度下气、液二相平衡成分的坐标点;改变体系的总成分,再如上法找出
乙醇正丙醇精馏实验
精馏实验 一、原始数据: 液相组成x 气相组成y 沸点℃1/x 1/y 0 0 97.16 0.126 0.24 93.85 7.9365 4.1667 0.188 0.318 92.66 5.3191 3.1447 0.21 0.339 91.6 4.7619 2.9499 0.358 0.55 88.32 2.7933 1.8182 0.461 0.65 86.25 2.1692 1.5385 0.546 0.711 84.98 1.8315 1.4065 0.6 0.76 84.13 1.6667 1.3158 0.663 0.799 83.06 1.5083 1.2516 0.844 0.914 80.59 1.1848 1.0941 1 1 78.38 1.0000 1.0000 Cp KJ/Kmol/K 乙醇r KJ/Kmol 822.2064 2.9050
二、数据处理 全回流 塔顶 折光率 质量浓度 摩尔分数 温度℃ ① 1.3625 81.3 ② 1.3625 平均 1.3625 0.8364 0.8696 塔底 折光率 ① 1.3758 ② 1.3740 平均 1.3749 0.2597 0.3139 7板 折光率 ① 1.3725 ② 1.3725 平均数 1.3725 0.3713 0.4351 8板 折光率 ① 1.3741 ② 1.3752 平均数 1.3747 0.2713 0.3269 计算示例: (1)折光率3625.12 3625 .13625.1=+= n (2)质量分数8364.0209.643625.1*512.46-=+= (3)摩尔分数=8696.060 8364 .0-1468364.0468364 .0=+ 正丙醇r KJ/Kmol Cp KJ/Kmol/K 713.2920 2.7165 混合液rm KJ/Kmol Cpm KJ/Kmol/K 735.0749 2.7542 料液摩尔分数与折光率关系 料液 摩尔分数 摩尔分数 乙醇 0% 100% 折光率 1.3805 1.359
分离乙醇正丙醇混合液的精馏塔设计课程设计
一设计任务书 (2) 二塔板的工艺设计 (3) (一)设计方案的确定 (3) (二)精馏塔的物料衡算 (3) 1.原料液及塔顶、塔釜产品的摩尔分数 (3) 2. 物料衡算 (4) (三)物性参数的计算 (4) 1.操作温度的确定 (5) 2. 密度的计算 (5) 3.混合液体表面张力的计算 (11) 4.混合物的粘度 (12) 5.相对挥发度 (14) (四)理论板数及实际塔板数的计算 (15) 1.理论板数的确定 (15) 2.实际塔板数确定 (18) (五)热量衡算 (19) 1.加热介质的选择 (19) 2. 冷却剂的选择: (19) 3.比热容及汽化潜热的计算 (19) (六)塔径的初步设计 (25) 1.汽液相体积流量的计算 (25) 2.塔径的计算与选择 (26)
(七)溢流装置 (29) 1.堰长 (29) 2.弓形降液管的宽度和横截面积 (30) 3.降液管底隙高度 (31) 4.塔板分布 (31) 5. 浮阀数目与排列 (32) (八)汽相通过浮阀塔板的压降 (35) 1.精馏段 (35) 2.提馏段 (36) (九)淹塔 (37) 1.精馏段 (37) 2.提馏段 (38) (十)雾沫夹带 (38) (十一)塔板负荷性能图 (40) 1.雾沫夹带线 (40) 2.液泛线 (41) 3.液相负荷上限线 (43) 4.漏液线 (43) 5.液相负荷下限线 (44) 三、塔总体高度计算 (47) 1.塔顶封头 (47) 2.塔顶空间 (47)
3.塔底空间 (48) 5.进料板处板间距 (48) 6.裙座 (48) 四、塔的接管 (50) 1.进料管 (50) 2.回流管 (50) 3.塔底出料管 (51) 4.塔顶蒸汽出料管 (51) 5.塔底蒸汽管 (51) 五、塔的附属设备设计 (52) 1.冷凝器的选择 (52) 2.再沸器的选择 (53) 六、参考文献.............................................................. . (54) 七、设计评述.............................................................. . (55)
异丙醇环己烷双液系相图
实验 异丙醇—环己烷双液系相图 一、实验目的 1.了解物理化学实验手段中常用的物理方法——光学方法的基本原理。 2. 绘制异丙醇-环己烷双液系的沸点-组成图,确定其恒沸物组成及恒沸温度。 3. 进一步理解分馏原理。 4. 掌握阿贝折射计的原理及使用方法。 二、实验背景 根据相律绘制相图,通过相图的分析加深对所研究体系的认识,是热力学方法研究多相平衡体系的重要内容之一。相平衡是物理化学的重要教学内容,其中气液平衡是最常见,也是讨论最多的内容之一。各体系相图的绘制为生产和科研实践中对某些液体混合物的分离、提纯与精制、蒸馏、精馏等具有一定的指导意义。 完全互溶双液系的T-x图,按曲线的特征,体系可以分为三大类,理想体系,正偏差体系和负偏差体系。其中,当偏差足够大时,会出现极大点和极小点,分别对应最大负偏差和最大正偏差,对应的极值点称为恒沸点,所对应的溶液称为恒沸混合物。考虑综合因素,一般实验都选择具有最低恒沸点的异丙醇—环己烷或乙醇—环己烷体系,本实验选异丙醇—环己烷体系。 根据相平衡原理,对二组分体系,当压力恒定时,当气液两相平衡时,体系的自由度为1。当体系的温度确定时,气液两相的组成也确定。反过来,当气液两相的组成确定时,体系的平衡温度也确定。沸点仪就是根据这个原理设计的。本实验中气液相的组成通过测定对应样品的折射率来确定,因而两组分的折射率相差越大越好,同时为了避免组分因挥发而造成测量误差,还要求两组分的饱和蒸汽压相差越小越好。 目前实验教学中最常用的沸点仪如图8-2所示,结构简单,容易操作,但达到平衡时间较长。另外一类型测定装置叫平衡釜,有陆志虞平衡釜、爱立斯平衡釜、罗斯平衡釜等,平衡釜结构比较复杂。还有一种多功能沸点测定仪,具有沸点测定仪和平衡釜的双重功能,测定范围较广,除常规的气液平衡数据的测定外,还可用于含盐体系和部分互溶体系气液平衡的测定。 三、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。 液体的沸点是指液体的饱和蒸汽压和外压相等时的温度。在一定外压下,纯液体的沸点有确定的值。但对于完全互溶的双液系,沸点不仅与外压有关,而且还与双液系的组成有关。 完全互溶双液系的沸点—组成图有三种类型(见图8-1),如果液体与拉乌尔定律的偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间见图8-1 (a),而实际溶液由于A、B二组分的相互影响,常与拉乌尔定律有较大偏差,在T-x图上就会有最低或最高点出现,这些点称为恒沸点,其相应的溶液称为恒沸点混合物,如图8-1(b),8-1(c)所示。
实验十一_二组分沸点组成相图的制作
实 验 报 告 一、 数据记录和处理 1.数据记录表 T 室温= 23.4℃ 表1 室温时正丙醇-乙醇溶液的组成与折射率的对应关系数据记录表 始P = 102.7kpa 末P = 102.7kpa 表2 正丙醇-乙醇溶液沸点-组成相图各数据记录表 2. 室温时绘制正丙醇—乙醇溶液组成与其折射率标准曲线 表3 室温时正丙醇-乙醇溶液的组成与折射率的对应关系表
表3数据的计算示例: 查附表9-8表计算得到: ρ0.8013 = 正丙醇 ρ0.7865 = 乙醇 再求正丙醇-乙醇溶液中正丙醇的物质的量分数浓度X正丙醇。 由表3数据绘制标准曲线: . . 图1 正丙醇物质的量分数与折射率的标准曲线
3. 常压下正丙醇-乙醇体系的沸点-组成相图的测绘 表4 正丙醇-乙醇溶液沸点-组成相图各数据处理表 由表4数据绘制相图: 图2 正丙醇-乙醇体系的沸点-组成相图
二、回答问题 1.本实验如何判断气、液两相达到平衡?用相律加以说明。如果取样口或空气口 塞子漏气,会有什么现象?为什么? 2.折射率-组成标准曲线的测定误差可能来自哪些方面?应采取哪些措施来减小误 差? 3.实验中超级恒温槽的作用?能否换成普通恒温槽? 4.气液平衡后,气相和液相在平衡仪内的温度不同,某同学认为这样测量出的气、 液相折射率会存在误差,这种说法是否正确?为什么? 5.本实验中气液平衡仪及毛细管为什么必须干燥?本实验测得的沸点-组成相图的 误差主要来源是那些操作? 6.本实验中Ⅰ-Ⅹ号溶液的浓度应如何选择?若某一号溶液的浓度发生不大的变化, 对实验测得的相图有无影响? 7.影响纯物质沸点的因素有哪些?影响混合液沸点的因素有哪些?加入平衡仪 内液体的量的多少对沸点有影响吗?
分离乙醇-正丙醇
华北科技学院环境工程系 《化工原理》课程设计报告 设计题目 分离乙醇-正丙醇二元物系浮阀式精馏塔的设计 学生姓名 杨志荣 学 号 200801034216 指导老师 孙春峰 专业班级 化工B082班 教师评语 设计起止日期:2011年6月13日 至2011年6月26日 成 绩
化工原理课程设计任务书 1.设计题目: 分离乙醇—正丙醇二元物系浮阀式精馏塔的设计 2.原始数据及条件: 进料:乙醇含量40%(质量分数,下同),其余为正丙醇 分离要求:塔顶乙醇含量93%;塔底乙醇含量0.01% 生产能力:年处理乙醇-正丙醇混合液25000吨,年开工7200小时 操作条件:间接蒸汽加热;塔顶压强1.03atm(绝压);泡点进料; R=5 3.设计任务: (1)完成该精馏塔的各工艺设计,包括设备设计及辅助设备选型。 (2)画出带控制点的工艺流程图、塔板版面布置图、精馏塔设计条 件图。 (3)写出该精馏塔的设计说明书,包括设计结果汇总和设计评价。
目录 第一章绪论4 第二章塔板的工艺设计5 2.1精馏塔全塔物料衡算5 2.2有关物性数据的计算 5 2.3理论塔板数的计算12 2.4塔径的初步计算14 2.5溢流装置15 2.6塔板分布、浮阀数目与排列16 第三章塔板的流体力学计算18 3.1、气相通过浮阀塔板的压降18 3.2、淹塔19 3.3、雾沫夹带20 3.4、塔板负荷性能图20 3.4.1物沫夹带线20 3.4.2液泛线21 3.4.3相负荷上限21 3.4.4漏液线 22 3.4.5 相负荷下限22 3.5 浮阀塔工艺设计计算结果23 第四章塔附件的设计25 4.1接管 (25) 4.2筒体与封头 (27) 4.3除沫器 (27) 4.4裙座 (27) 4.5人孔 (27) 第五章塔总体高度的设计 (28) 5.1塔的顶部空间高度 (28) 5.2塔的顶部空间高度 (28) 5.3塔总体高度 (28) 第六章附属设备的计算 (28) 6.1冷凝器的选择 (28) 6.2再沸器的选择 (30) 主要符号说明 (32) 结论 (34) 参考文献 ..................................................................................... 错误!未定义书签。 感想 (35)
课程方案乙醇正丙醇混合液精馏塔方案
华北科技学院 化工原理课程设计 说明书 设计题目:分离乙醇 -正丙醇混合液的精馏塔设计 姓 名: 熊先清 专 业: 化学工程与工艺 班 级: 化工B091 学 号: 200901034112 指导教师: 高丽花李辰明 设计时间:2018年6月10日至 2018年6月22日 完成时间:2018年6月22日 评语: 目录 目录1 一设计任务书3 二塔板的工艺设计 3
< 一)设计方案的确定 3 <二)精馏塔的物料衡算 3 1?原料液及塔顶、塔釜产品的摩尔分数 3 2物料衡算4 (三 > 物性参数的计算4 1?操作温度的确定4 2密度的计算5 3.混合液体表面张力的计算9 4混合物的粘度10 5相对挥发度11 (四 > 理论板数及实际塔板数的计算12 1?理论板数的确定12 2?实际塔板数确定13 (五 > 热量衡算14 「加热介质的选择14 2?冷却剂的选择14 3上匕热容及汽化潜热的计算14 4?热量衡算17 (六 > 塔径的初步设计19 1?汽液相体积流量的计算19 2?塔径的计算与选择 20 (七 >溢流装置22 1堰长l w22 2?弓形降液管的宽度和横截面积22 3?降液管底隙高度23 (八 > 塔板分布、浮阀数目与排列24 1?塔板分布24 2.浮阀数目与排列24 二、塔板的流体力学计算 26 <一)汽相通过浮阀塔板的压降26 1精馏段26 2提馏段27 <二)淹塔27 1精馏段27 2提馏段28 <三)雾沫夹带28 <四)塔板负荷性能图29 1?雾沫夹带线29 2?液泛线30 3液相负荷上限线 31 4?漏液线32
5液相负荷下限线 32 三、塔总体高度计算 35 1?塔顶封头35 2?塔顶空间35 3?塔底空间35 4.人孔36 5.进料板处板间距 36 6裙座36 四、塔的接管37 1?进料管37 2回流管37 3?塔底出料管37 4?塔顶蒸汽出料管38 5.塔底蒸汽管38 五、塔的附属设备设计38 1?冷凝器的选择38 2再沸器的选择39 六、总结40 七、参考文献40 -设计任务书 【设计题目】分离乙醇-正丙醇混合液的精馏塔设计【设计条件】进料:乙醇含量 40%<质量分数,下同),其余为正丙醇 分离要求:塔顶乙醇含量 93%;塔底乙醇含量0.01% 生产能力:年处理乙醇-正丙醇混合液 25000吨,年工7200小时操作条件:间接蒸汽加 热;塔顶压强 1.03atm(绝压 > ;泡点进料;R=5 【设计计算】 二塔板的工艺设计 < 一)设计方案的确定 本设计的任务是分离乙醇 -正丙醇混合液。对于二元混合物的分离,应采用连续精馏流程。 <二)精馏塔的物料衡算1?原料液及塔顶、塔釜产品的摩尔分数
