水飞蓟素中活性黄酮的测定

竹叶黄酮的抗氧化活性研究
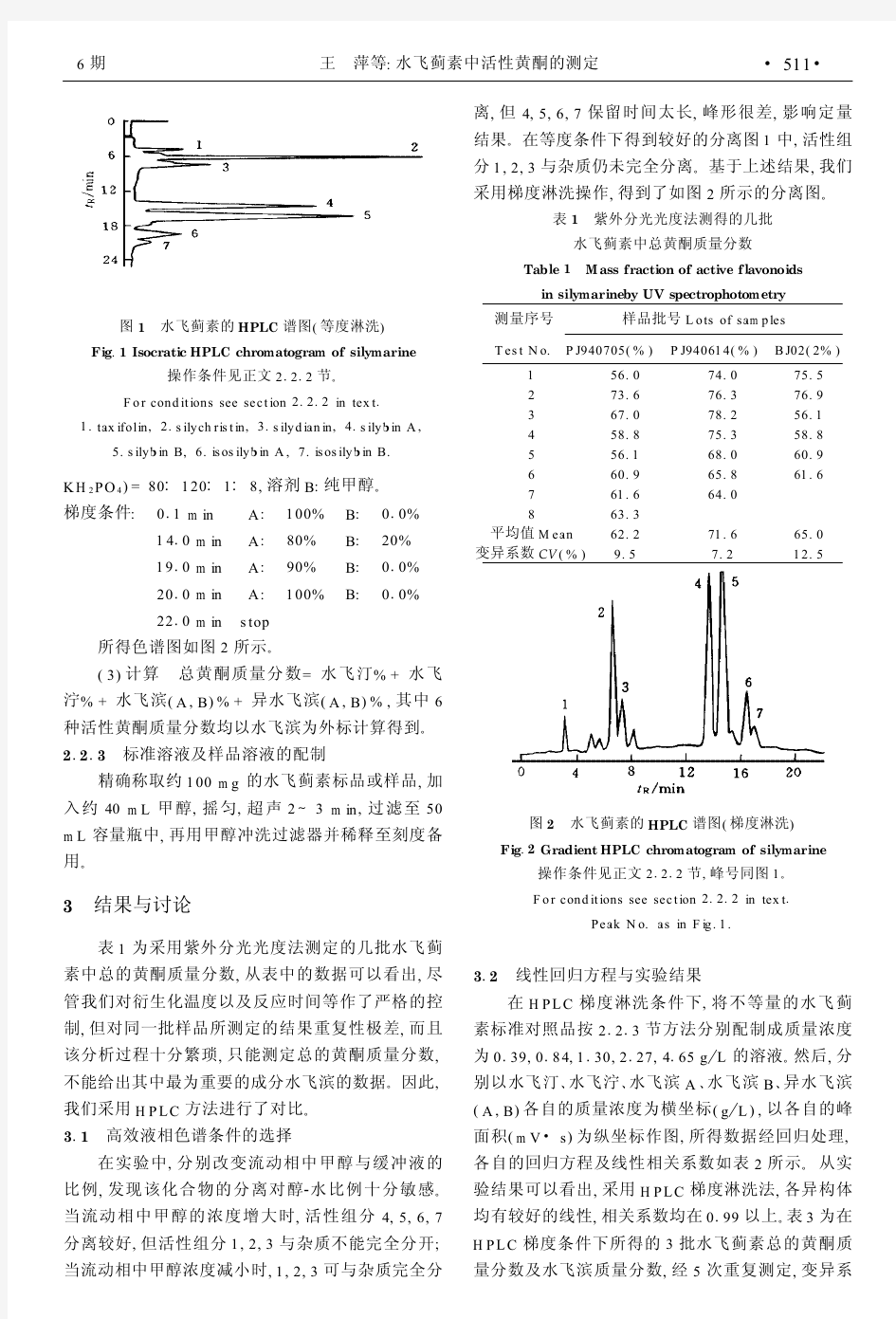
食 品 科 技 FOOD SCIENCE AND TECHNOLOGY 2011年 第36卷 第7期 提取物与应用 · 201 · 罗宇倩1,郭 辉1,胡林福2,施林巍2,钱俊青1* (1.浙江工业大学药学院,杭州 310014; 2.浙江竹类资源生物技术研究开发中心,安吉 313300) 摘要:为了有效利用竹叶中黄酮类物质,研究采用不同的方法(DPPH法、邻苯三酚自氧化法(325 nm)和 Fenton法)评价了竹叶黄酮的抗氧化活性,以Vc和茶多酚为阳性对照品。结果表明:竹叶黄酮清除超氧负离子自由基和DPPH自由基的能力比茶多酚强,其EC 50相应为11.7 μg/mL和18.3 μg/mL,分别是Vc的约1.2倍和3.4倍;竹叶黄酮在清除羟自由基效果与茶多酚相当,EC 50 为0.58 mg/mL,比Vc效果好。因此竹叶黄酮具有很强的抗氧化能力,值得深入研究其生理功能及开发利用价值。 关键词:竹叶;黄酮;抗氧化性 中图分类号:TS 202.3 文献标志码:A 文章编号:1005-9989(2011)07-0201-03 Antioxidant activity of ? avonoids from bamboo leaves LUO Yu-qian 1, GUO Hui 1, HU Lin-fu 2, SHI Lin-wei 2, QIAN Jun-qin 1* (1.College of Pharmacognosy of Zhejiang University of Technology Hangzhou 310014; 2.Biological Technology R&D Center of Bamboo Resources, Anji 313300) Abstract: The antioxidant activity of total flavonoids from bamboo leaves was determined by various assays, including DPPH radical-scavenging, self-oxidation of 1, 2, 3-phentriolassay method(325 nm) and Fenton reactions. The results showed that ? avonoids from bamboo leaves have very strong scavenging capabilities for superoxide anion and DPPH free radical, their EC 50 values are 11.7 μg/mL and 18.3 μg/mL respectively, and are approximately 1.2 times and 3.4 times as much as that of vitamin C respectively. The scavenging capability of bamboo leaves ? avonoids for hydroxyl radical is stronger than that of vitamin C, weaker than tea polyphenol, and its EC 50 is 0.58 mg/mL.Key words: bamboo leaves; ? avonoids; antioxidation 收稿日期:2010-11-07 ﹡通讯作者基金项目:浙江省制药工程重中之重开发基金项目。 作者简介:罗宇倩(1986—),女,湖南株洲人,硕士研究生,研究方向为天然药物的提取与纯化以及药理研究。 淡竹叶和淡竹沥是中医一味传统的清热解毒药,早已为我国人们所认识。竹叶中黄酮类物质是主要活性物质,含量平均在2%,主要为黄酮糖苷[1],分别是荭草苷、异荭草苷、牡荆苷和异牡荆苷,以及木犀草素苷、洋芹苷和黄酮苷类。竹叶黄酮具有明显的抗脂质过氧化[2-3]、清除羟自 由基和调节血脂功能及抗过敏、抗炎、抗菌、抗突变、抗肿瘤、抗溃疡、抗病毒、保护心血管疾病[4-5]及保肝等生理活性,是一类极具开发前景的天然有机抗氧化剂[1,6-8]。 我国竹叶资源丰富,因此充分开发利用竹叶中的黄酮类成分具有十分重要的现实经济意义。 竹叶黄酮的抗氧化活性研究
总黄酮、多酚含量的测定
燕麦总黄酮含量的测定 一、仪器 紫外-可见分光光度计、分析天平、低速离心机、超声波提取器、恒温水浴锅、粉碎机、pH计、10mL容量瓶15个、10mL具塞试管、100mL烧瓶、10mL离心管10个、试管架2个 二、药品 芦丁标准品40mg、无水乙醇1000mL、亚硝酸钠500g、硝酸铝500g、NaOH 500g 三、实验步骤 (一)、样品处理及总黄酮的提取 1. 将样品籽粒分别称取 2.5 g置于小信封里,80℃烘干24 h。 2. 研成粉末,称取500±2 mg样品于10 mL离心管中,使样品位于试管底部(重复3次)。 3. 每管加4 mL 60%乙醇,放水浴锅60℃浸提2 h。6000 r/min离心10 min,离心后取上清液于10 mL容量瓶中。 4. 再向离心管中加4 mL的60%乙醇,放水浴锅60℃浸提1 h。6000 r/min离心10 min,离心后取上清液于相应的10 mL容量瓶中。60%乙醇定容至10 mL,待测。 (二)、标准曲线绘制 1. 精确量取浓度200 μg/mL芦丁标准溶液0、0.2、0.4、0.8、1.2、1.6、 2.0 mL 分别置于10 mL容量瓶中。 2. 向容量瓶中分别加60%乙醇5、4.8、4.6、4.2、 3.8、3.4、3.0 mL。 3. 然后加5%亚硝酸钠0.3 mL,摇匀,静置6 min。 4. 再加10%硝酸铝0.3 mL,摇匀,静置6 min。 5. 加4%氢氧化钠4.0 mL,用60%的乙醇定容至刻度,摇匀,静置12 min。 6. 于510 nm波长下测定吸光度,并以芦丁标准浓度值为纵坐标,以吸光度为横坐标,绘制标准曲线。 (三)、样品提取液总黄酮含量的测定 准确吸取总黄酮提取液2.0 mL于10 mL容量瓶中,按二的方法测定吸光度,
黄酮类化合物生物活性的研究进展_王慧
黄酮类化合物生物活性的研究进展 王 慧 (山东博士伦福瑞达制药有限公司,山东 济南 250101) 摘 要:黄酮类化合物是广泛存在于自然界的一类多酚化合物,有许多潜在的药用价值。现就黄酮类化合物抗肿瘤、抗心血管疾病、抗氧化抗衰老、抗菌抗病毒、免疫调节等作用的研究进展作一综述,以期为开发利用该类药物提供参考。关键词:黄酮类化合物;生物活性;综述文献 中图分类号:R282.71 文献标识码:A 文章编号:1672-979X (2010)09-0347-04 收稿日期:2010-05-31 作者简介: 王慧(1974-),女,山东临沭人,主管药师,从事质量控制工作 E-mail : wanghui0602@https://www.360docs.net/doc/3e2025585.html, Progress in Bioactivity of Flavonoids WANG Hui (Shandong Bausch & Lomb Freda Phar. Co., Ltd., Jinan 250101, China ) Abstract: Flavonoids are polyphenols widely found in nature and they have many potential medicinal values. This paper reviews the progress in anti-tumor, anti-cardiovascular disease, anti-oxidation and anti-aging, antibacterial and antivirus, immunological regulation of flavonoids, which can provide the references for the development and utilization of flavonoids. Key Words: flavonoids; bioactivity; review 黄酮类化合物是一类低分子植物成分,具有C6-C3-C6 基本构型,为植物体多酚类代谢物。主要分为黄酮及黄酮醇类、二氢黄酮及二氢黄酮醇类、黄烷醇类、异黄酮及二氢异黄酮类、双黄酮类,以及查尔酮、花色苷等[1]。黄酮类化合物独特的化学结构使其对哺乳动物和其它类型的细胞有重要的生物活性。黄酮类化合物有高度的化学反应性,例如清除生物体内的自由基;又有抑制酶活性、抗肿瘤、抗菌、抗病毒、抗炎症、抗过敏、抗衰老、抗心血管疾病糖尿病并发症等药理作用,且无毒无害。黄酮类化合物还是茶及黄芩、银杏、沙棘等众多中草药的活性成分。因此受到广泛关注,研究进展很快。1 黄酮类化合物的理化性质 黄酮类化合物多为晶体且有颜色,少数如黄酮苷类为无定形粉末,除二氢黄酮、二氢黄酮醇、黄烷及黄烷醇有旋光性外,余者则无。黄酮类化合物的溶解度因结构及存在状态(苷或苷元、单糖苷、双糖苷或三糖苷)不同而有差异,一般游离态苷元难溶于水,易溶于甲醇、乙醇、乙酸乙酯、乙醚等有机溶剂。其中,黄酮、黄酮醇、查儿酮等平面型分子因堆砌较紧密,分子间引力较大,故更难溶于水;而二氢黄酮及二氢黄酮醇等系非平面型分子,排列不紧密,分子间引力较小,有利于水分子进入,水溶解度稍大[2]。 2 黄酮类化合物的生物活性2.1 抗肿瘤活性 黄酮类对多种肿瘤细胞有明显的抑制作用,主要表现在抑制细胞增殖、诱导细胞凋亡、干预信号转导、影响细胞 [11] Denyer S P, Baird R M. Guide to microbiological control in pharmaceuticals and medical devices[M].2nd ed. Boca Raton: CRC Press, 2006: 325-326. [12] Mao k, Masafumi U, Takeshi K, et al Evaluation of acute corneal barrier change induced by topically applied preservatives using corneal transepithelial electric resistance in vivo [J].Cornea , 2010, 29(1): 80-85. [13] Noecker R. Effects of common ophthalmic preservatives on ocular health[J]. Adv Ther , 2001, 18: 205-215. [14] Kostenbauder H B. Physical factors influencing the activity of antimicrobial agents// Block S S. Disinfection, Sterilization and Preservation[M]. 3rd ed. PhiladelpHia: Lea and Febiger, 1983: 811-828. [15] Berry H, Michaels I. The evaluation of the bactericidal activity of ethylene glycol and some of its monoalkyl ethers against Bacterium coli [J]. J Pharm Pharmacol , 1950, 2: 243-249.
总黄酮含量测定方案
总黄酮含量测定 一样品溶液的制备 70%乙醇溶液,料液比1﹕8 ,80度下回流2h。取10g样品放入圆底烧 瓶中加入80ml 70%乙醇溶液回流2h,抽滤定容至100ml备用。使用时先离心再用70%乙醇稀释10倍做样品溶液。 二芦丁标准品的配置 精密称取芦丁2mg,加无水乙醇定容至10ml。制得浓度为0.2mg/ml芦 丁标准品溶液。 三显色方法的确定 1 扫描原液分别取芦丁溶液和样品溶液各1ml,加无水乙醇定容至25ml,空白对照,全波扫描。 2硝酸铝显色法分别取芦丁对照品溶液和样品溶液各5ml,加5%亚硝酸 钠溶液(1.25g亚硝酸溶于无水乙醇中定容到25ml容量瓶中) 1ml, 摇匀,放置6min,加10%硝酸铝溶液(4,4014g硝酸铝.九水溶于无水乙醇中定容到25ml 容量瓶中) 1ml,摇匀,放置6min,加4%氢氧化钠试液(2g氢氧化钠溶于无水乙醇中定容到50ml容量瓶中)10ml, 再加无水乙醇定容至25ml,摇匀,放置15min,空白对照,全波扫描bb 。 3氯化铝显色法分别取芦丁对照溶液和样品溶液各5ml ,加1%的氯化 铝溶液(1g氯化铝溶于无水乙醇中定容到100ml容量瓶中)10ml,摇匀放置10min,空白对照,全波扫描。 4 氢氧化钾显色法分别取芦丁对照品溶液和样品溶液各5ml,加3ml10% 氢氧化钾溶液(2.5g氢氧化钾溶于无水乙醇中定容到25ml容量瓶中), 充分摇匀显色5min后,用无水乙醇定容至25ml, 摇匀,空白对照,全波 扫描。 四显色条件的确定 五标准曲线的绘制 分别取1ml,2ml,3ml,4ml,5ml,6ml芦丁对照品溶液,按所选的显色方法测定吸光度,绘制标准曲线。 六精密度实验 按标准曲线绘制方法,分别准确量取1.0ml芦丁标准液5份,按所选显色剂和所确定的最优显色条件在所选波长下测定吸光度。
总黄酮、多酚含量的测定
总黄酮含量的测定 一、仪器 紫外-可见分光光度计、分析天平、低速离心机、超声波提取器、恒温水浴锅、粉碎机、pH计、10mL容量瓶15个、10mL具塞试管、100mL烧瓶、10mL离心管10个、试管架2个 二、药品 芦丁标准品40mg、无水乙醇1000mL、亚硝酸钠500g、硝酸铝500g、NaOH 500g 三、实验步骤 (一)、标准曲线绘制 1. 芦丁标准品40mg置于称量瓶中80℃烘干至恒重,取烘干后的20mg芦丁标准品用水定容至100mL,得200μg/mL芦丁标准贮备液,精确量取上述浓度芦丁标准贮备溶液0、0.2、0.4、0.8、1.2、1.6、 2.0 mL分别置于10 mL具塞试管中。 2. 向具塞试管中分别加60%乙醇5、4.8、4.6、4.2、 3.8、3.4、3.0 mL。 3. 然后加5%亚硝酸钠0.3 mL,摇匀,静置6 min。 4. 再加10%硝酸铝0.3 mL,摇匀,静置6 min。 5. 加4%氢氧化钠4.0 mL,用60%的乙醇定容至刻度,摇匀,静置12 min。 6. 于510 nm波长下测定吸光度,并以芦丁标准浓度值为横坐标,以吸光度为纵坐标,绘制标准曲线。研究表明芦丁标准品含量在0~0.5mg 范围内与吸光度具有良好的线性关系。 (二)、样品处理及总黄酮的提取(以60%乙醇提取为例) 1. 将样品在80℃烘干24 h,粉碎后过80目筛置于干燥器中备用。 2. 称取500±2 mg样品于25 mL具塞三角瓶中,使样品位于三角瓶底部(重复3次)。 3. 每瓶加4 mL 60%乙醇,放超声波提取器提取2 h。提取液转至10 mL具塞离心管中。 4. 再向具塞三角瓶中加4 mL的60%乙醇,放超声波提取器提取1 h,提取液转至相应10 mL具塞离心管中,6000 r/min离心10 min,离心后取上清液于相应
银杏叶黄酮提取及含量测定
银杏叶黄酮提取及含量测定 一、实验目的 1、掌握银杏叶中黄酮的提取方法 2、了解银杏叶中黄酮的含量测定 二、实验原理 近几年来,随着对黄酮类化合物研究的日益深入与重视,黄酮类化合物提取技术的发展也得到了促进。目前提取黄酮类化合物的方法主要包括有机溶剂浸提法、超声波提取法、超临界流体萃取法、微波提取法和酶提取法等。 1.1有机溶剂浸提法 目前国内外使用最广泛的银杏叶中黄酮的提取方法就是有机溶剂提取法,一般可用乙酸乙酯、丙酮、乙醇、甲醇或某些极性较大的混合溶剂,如甲醇-水(1+1)溶液。由于甲醇的毒性、挥发性较大,因此一般采用乙醇作为提取剂。银杏叶干燥粉碎后用有机溶剂浸泡、提取、过滤,滤液中的溶剂经减压蒸馏除去后得银杏叶浸膏粗提物。徐桂花等[1]提取银杏叶中黄酮类化合物时,采用乙醇(70+30)溶液为提取剂,提取温度为70℃,料液质量浓度比为1g比40mL,提取时间为4h。由于乙醇提取工艺在安全性、溶剂成本、效率及杂质酚酸去除等方面都不能应对日益严酷的市场竞争,张林涛等[1]提出了以硼砂- 氢氧化钙碱水为溶剂提取银杏叶黄酮,其黄酮提取率与文献值相近,但提取工艺时间缩短为1h。 1.2超声波提取法 超声波提取法是利用搅拌作用、强烈的振动和空间效应、高的加速度等使药物有效成分进入溶剂,从而提高提取率,缩短提取时间,并能消除高温对提取成分影响的一种提取法。刘晶芝等[2]运用了超声波技术与水浸提取相结合的方法得出超声波提取的最佳工艺条件为:超声频率40kHz,超声处理时间55min,料液质量比1比100,提取温度35℃,静置3h,提取率为81.9%。郭国瑞等[3]以水为介质,超声波提取银杏叶中黄酮苷,与常规水浸提法比较,超声波提取效率大大提高,确定超声波提取的最佳工艺为:超声处理时间55min,料液质量比1比30,提取温度50℃,提取率为82.3%。 1.3超临界流体萃取法 超临界流体萃取法是一种以超临界流体代替常规有机溶剂对有效成分进行萃取和分离的新技术。可作为超临界流体的物质很多,其中二氧化碳临界温度(TC=31.3℃)接近室温,且具有无色、无毒、无味、不易燃、化学惰性、价廉、易制成高纯气体等优点而被广泛应用,特别在中药材及其制剂中更显示出其独特、简便、快速、具有较高的选择性、提取杂质少、可直接进样分析的优点。邓启焕等[4]探讨了超临界萃取银杏叶有效成分的影响因素,最佳条件为萃取压力20MPa、时间90min、粒度3.9mm、温度40℃,经测定银杏叶黄酮的质量分数为28%,高于国际公认标准。 1.4微波提取法 微波提取法是利用分子或离子在微波场中的导电效应直接对物质进行加热从而提取植物细胞内耐热物质的新工艺。曾里等[5]的研究表明以乙醇溶液作溶剂比以水作溶剂的效果好,最佳条件为以乙醇 (60+40)溶液为提取剂,解冻处理20min。张鹏等[6]对微波法提取银杏叶中黄酮类物质进行了研究,最佳提取条件为以乙醇(50+50)溶液
黄酮混合物体外抗氧化活性的相互作用
食 品 科 技FOOD SCIENCE AND TECHNOLOGY 提取物与应用· 198 ·2013年 第38卷 第2期 黄酮类化合物广泛存在于水果、蔬菜、谷物、植物来源的饮料(如红酒、绿茶等)等植物性食品中,具有保护心血管、降血压、降胆固醇、抗收稿日期:2012-08-25 基金项目:宁波职业技术学院2011年院级课题(NZ11022);宁波工程学院“北仑科技创新基金”项目。 作者简介:汤晓(1981—),女,浙江宁波人,硕士研究生,讲师,研究方向为植物有效成分提取与应用。 癌、杀菌、消炎等多种生理活性[1]。黄酮类化合物的基本结构为2个苯环通过中央三碳链连接而成,目前已确认结构的黄酮有5000多种,可划分为10汤 晓1,焦泽武1,龚淑珍1,梁 春1,方振飞1,关亚璠1,仇 丹2 (1.宁波职业技术学院应用化工系,宁波 315800 ; 2.宁波工程学院化学工程学院, 宁波 315016)摘要:测定槲皮素、异槲皮素、杨梅素、山萘酚、儿茶素、表儿茶素、芹菜素、飞燕草素-3-O-葡萄糖苷、矢车菊素-3-O-葡萄糖苷等9种黄酮类化合物及其两两混合物的体外抗氧化活性,以研究黄酮混合物的协同、拮抗与加合作用。以DPPH 清除能力、羟基自由基清除能力、总抗氧化性、还原能力为评价指标。结果表明,含有较多B 环羟基的黄酮类化合物更易发生拮抗作用,可通过调节黄酮单品的比例减小混合物的拮抗作用或是增强其协同作用,不同反应机理的评价指标所得结果不同。 关键词:黄酮;抗氧化活性;协同;拮抗;加合 中图分类号:R 285 文献标志码:A 文章编号:1005-9989(2013)02-0198-09 Interaction of flavonoids mixtures on antioxidant activities in vitro TANG Xiao 1, JIAO Ze-wu 1, GONG Shu-zhen 1, LIANG Chun 1, FANG Zhen-fei 1, GUAN Ya-fan 1, QIU Dan 2 (1.Department of Chemical Engineering, Ningbo Polytechnic College, Ningbo 315800;2.College of Chemical Engineering, Ningbo University of Technology, Ningbo 315016)Abstract: This study investigated in vitro antioxidant activities of quercetin, isoquercetrin, myricetin, kaempferol, catechin, epicatechin, apigenin, delphinidin-3-O-glucoside, cyanidin-3-O-glucoside and their pairwise mixtures to evaluate synergistic, antagonistic, and additive effects of flavonoids mixtures. DPPH radical scavenging activity, hydroxyl radical scavenging activity, total antioxidant activity and reducing power were used as evaluation indicators. The results indicate that flavonoids with more B ring hydroxyls are more influenced by antagonistic effect. Antagonistic effect could be reduced and synergistic effect could be enhanced by changing the ratio of single flavonoid in the mixture. Different reaction mechanisms could induce different experimental results.Key words: flavonoids; antioxidant activity; synergistic; antagonistic; additive 黄酮混合物体外抗氧化活性的相互作用
总黄酮测定含量
1 各批次药材含量测定 使用已经确定的总黄酮含量检测方法分别进行5个批次原料含量的测定 总黄酮含量测定:分别精密称取药材粗粉0.5g,置100ml锥形瓶中,加70%乙醇50ml,称定重量,超声60分钟,放冷,称定,加入70%乙醇补足减失重量,摇匀,过滤,弃去粗滤液,精密量取续滤液10.0ml上聚酰胺树脂,待充分吸附后,用乙醇进行洗脱,至流出液基本无色,以洗脱液定容至25ml量瓶中,备用。精密量取供试品溶液5ml,置10ml比色管中,加 5%亚硝酸钠溶液0.4ml,使混匀,放置6分钟,加10%硝酸铝溶液0.4ml,摇匀,放置6 分钟,加2mol/L氢氧化钠溶液3ml,再加30%乙醇至刻度,摇匀,放置15分钟,照分光光度法(《中国药典》2010版一部附录Ⅴ B),在504nm 的波长处测定吸收度。 表1 不同批次药材总黄酮含量测定结果 批号含量(%) 1 2 3 X±S 20140516 0.16350.16480.17010.1661±0.0035 20140516紫外扫描色谱图 2 药材总黄酮转移率研究 2.1 单个药材转移率研究
2.1.1 单个药材的转移率测定 同一批次的各药材,分别按照产品生产工艺提取得单个药材的总黄酮浓缩液样品,进行总黄酮含量检测,与“1”项下同批药材的总黄酮含量相比得出单个药材的转移率(如下式),分别进行5批次药材测定。 黄芪、桑叶、黄精、山茱萸:分别取黄芪、桑叶、黄精、山茱萸各100g,加水煎煮两次(回流),第一次加水12倍量,煎煮2.0h,过滤;第二次加水10倍量,煎煮1.0h,过滤,合并滤液浓缩至100ml,备用。 黄芪不同浓缩程度的考查:取黄芪100g,加水煎煮两次(回流),第一次加水20倍量,煎煮2.5h,过滤;第二次加水20倍量,煎煮2.0h,过滤,合并滤液,重复试验三次,分别浓缩至50ml、100ml、200ml,备用。 精密量取上述溶液5ml,加乙醇15ml,摇匀,过滤,弃去粗滤液,精密量取续滤液10.0ml上聚酰胺树脂,待充分吸附后,用乙醇进行洗脱,至流出液基本无色,以洗脱液定容至25ml量瓶中,备用。精密量取供试品溶液5ml,置10ml 比色管中,加5%亚硝酸钠溶液0.4ml,使混匀,放置6分钟,加10%硝酸铝溶液0.4ml,摇匀,放置6 分钟,加2mol/L氢氧化钠溶液3ml,再加70%乙醇至刻度,摇匀,放置15分钟,照分光光度法(《中国药典》2010版一部附录ⅤB),在504nm 的波长处测定吸收度。 表2 不同批次药材提取液总黄酮含量测定结果 批号含量(%) 1 2 3 X±S 20140516 0.16350.16480.17010.1661±0.0035
黄酮含量的测定方法
黄酮含量的测定方法 1、对照法 1) ①对照品制备:精密称取芦丁对照品20.8mg,置于100ml容量瓶中,加70%乙 醇使溶解并稀释至刻度,摇匀。 ②样品溶液制备 精密称取样品0.50g,精密加入70%乙醇50ml,称定重量,超声处理30分钟,称定重量,用70%乙醇补足减失重量,即得。 ③标准曲线的制备 精密称取对照品溶液0.0、1.0、2.0、3.0、4.0、5.0ml,分别置于25ml比色管中,加70%乙醇10ml,加5%亚硝酸钠溶液1ml,摇匀,放置6分钟,加1mol/L 氢氧化钠溶液10ml,加70%乙醇置刻度,摇匀,放置15分钟。各取10ml 置于50ml容量瓶中,用70%乙醇稀释至刻度。在510nm的波长下测定吸光度。 2) ①样品溶液的制备: 分别精确称取80℃恒温干燥的样品用50%甲醇回流提取,料液比1:15,提取两次,每次30min,将两次提取液合并浓缩至一定体积,用30%甲醇定容至50ml 容量瓶中。从其中取出12ml溶液放入100ml容量瓶中,稀释至刻度,再从100ml 容量瓶中取出1.5ml溶液,放至10ml容量瓶中,定容,为待测样品液Ⅰa和Ⅱa。 ②最大吸收波长的选择:分别作样品液Ⅰa、Ⅱa及芦丁标准品的吸收曲线,均在350 nm 处有一强吸收,因此选择350 nm为测定波长。 ③标准曲线的制定: 精密称取芦丁对照品10.3mg,用少量30%乙醇溶解后,转移至50ml容量瓶,用蒸馏水定容至刻度。分别精密量取2ml、3ml、4ml、5ml、6ml芦丁溶液置于100ml 容量瓶中,于350 nm 波长处测定吸光值,以芦丁空白为参比,以芦丁浓度为横坐标,以吸光度为纵坐标绘制标准曲线,提示在4.12~12.36mg/103ml浓度之间,吸光度值与浓度呈现良好的线性关系。 ④含量测定结果: 分别吸取2.2.1中Ⅰa和Ⅱa待测样品液各适量于石英比色池中,按标准芦丁一吸光度测定法,以样液空白参比,于350nm 波长下测定吸光值,计算各提取液中总黄酮含量。 计算公式为:样品总黄酮含量(%)=0.03692(A+0.1644)/W。 注:上式为通过回归方程转化而来,式中A为测得样品液的吸光度值,W为称样量。
黄酮体外抗氧化活性研究
1. 供试液的制备:将纯化后的黄酮用蒸馏水(可加SDS 促溶)稀释后,分别配 制10、20、30、40、50、60、70 μg/mL 溶液,4℃保存备用。(根据实际情况调整浓度) 2. 总黄酮的测定: 标准曲线的绘制:称取芦丁10.00 mg 至50 mL 容量瓶,加60%乙醇使之溶解定容至刻度,摇匀,即得芦丁标准溶液(0.2 mg/mL )。准确吸取芦丁标准溶液0、0.5、1.0、1.25、1.5、2.0 mL (相当于芦丁0、0.1、0.2、0.25、0.3、0.4 mg ),并用相应60%乙醇溶液相应补足2.0 mL ,移入10 mL 刻度比色管中,加5%亚硝酸钠溶液0.2 mL ,振摇后放置6 min ,加入10%硝酸铝溶液0.2 mL 摇匀后放置6 min ,加1.0 mol/L 氢氧化钠溶液2.0 mL 。摇匀,放置15 min ,于510 nm 波长处测定吸光度,以芦丁含量(mg )为横坐标,以吸光度为纵坐标绘制标准曲线。 样品测定:吸取适当稀释的待测液2.0 mL ,按标准曲线制备操作步骤于 510nm 处进行吸光度的测定(样液如有沉淀,应过滤后测定)。 结果计算:根据标准工作曲线,求出相当于样品吸光度的芦丁含量,按下式求出总黄酮含量: 10010 3121????=V m V m X 式中:X ——样品中总黄酮含量,g/100g ; m 1——根据标准曲线计算出待测液中黄酮的量,mg ; m ——样品质量,g ; V 1——样品提取液测定用体积,mL ; V 2——样品提取液总体积,mL 。 3. 还原能力的测定: 于试管中加入1.0 mL 样液(不同质量浓度的待测物溶液)或蒸馏水,再分别加入1.0 mL 磷酸缓冲溶液(0.2 mol/L, pH6.6)及1.0 mL 铁氰化钾水溶液(1%),50℃水浴20 min 后取出快速冷却,加入1.0 mL 三氯乙酸水溶液(10%),摇匀,5000 rpm/min 离心5 min 。取1.0 mL 上清液,依次加入1.0 mL 蒸馏水,0.5 mL 三氯化铁水溶液(0.1%),充分混匀,10 min 后,在700 nm 波长处测定吸光度,吸光度越大,则说明还原能力越强。以V C 为阳性对照做参照实验。 4. DPPH 自由基清除活性: D PPH 溶液:称取8.00 mg DPPH 用100 mL 无水乙醇溶解,定容于100 mL 容量瓶中,摇匀,倒入棕色磨口瓶,作为储备液保存于4℃冰箱中,浓度为2×10-4 mol/L 。 取100 μl 待测液及100 μl 的2×10-4 mol/L DPPH 溶液加入96孔板中,摇匀。20 min 后用相应溶剂作参比在517 nm 下测定其吸光度A i ,同时测定2×10-4 mol/L
设计实验 总黄酮的提取和测定
设计性实验: 银杏叶中总黄酮的提取和测定 小组人员:袁国明郎启国赵永仓王蓉 一、目的要求 1、探究不同浓度的乙醇和在不同时间下对黄酮类化合物提取率的影响。 2、掌握从银杏叶中提取总黄酮的操作步骤和测定方法。 3、了解提取银杏叶中黄酮类化合物制备的基本原理和方法。 二、实验原理 根据超声波具有空化、粉碎、搅拌等特殊作用,对银杏叶的细胞有破坏现象,使乙醇溶液能渗透到银杏叶中,以便让总黄酮溶解在乙醇中,在通过分离提纯的方法,来获得总黄酮的含量。 黄酮类是含酚羟基的化合物,能够和铝离子产生黄色络合物,在碱性条件下溶液呈红色。因此,本实验所采用的方法是在碱性溶液中加铝盐显色的分光光度法。其具体操作是在所测定的溶液中加入5%NaNO2;10%A1(NO3)3;5%NaOH溶液,在500nm波长下,用紫外分光光度法测定所提溶液中总黄酮的含量。 三、试剂和器材 1、试剂 芦丁标准品;5%NaNO2;10%A1(NO3)3;5%NaOH;30%、40%、50%、60%、70%、80%的乙醇(用95%的酒精31.91ml、42.55ml、53.19ml、68.83ml、74.47ml、85.11ml );及蒸馏水等。 2、材料 新鲜的银杏叶 3、器材 容量瓶25ml(×1) 100ml(×6);吸管0.5ml(×2)1ml(×2),2ml(×1),5ml (×1)粉碎机;超声波清洗机;高速离心机;三角锥形瓶50ml(×6);滤纸;分光光度
计;烧杯;具塞刻度试管;分析天平;20ml量筒等 四、操作方法 1、银杏叶的处理 把新鲜的银杏叶低温烘干,使水分小于8%,制成干粉,待用。 2、制作标准曲线 准确称取芦丁标准品5mg,用80%乙醇溶解,定容于25mL容量瓶中,摇匀,得0.2mg /mL的标准溶液。 移液管精确吸取标准溶液0.0、0.2、0.4、0.6、0.8、1.0、1.2ml,分别置于10mL容量瓶中,加入5%NaNO2 0.4mL,摇匀,放置5min;加入10%A1(NO3)3 0.4mL,摇匀,放置6min;加入5%NaOH 4.0mL,再加蒸馏水至刻度,摇匀,在80℃水浴中保温10min。以试剂空白作为参比溶液。用1cm比色皿,在510nm波长处测定吸光度,绘制标准曲线(标样浓度和吸光度的关系)。 表1-1 标准曲线制作 管号 1 2 3 4 5 6 7 芦丁标准液(mL)0.0 0.2 0.4 0.6 0.8 1.0 1.2 5%NaNO2(mL)0.4 0.4 0.4 0.4 0.4 0.4 0.4 放置时间(min) 5 5 5 5 5 5 5 0.4 0.4 0.4 0.4 0.4 0.4 0.4 10%Al(NO3)3 (mL) 放置时间(min) 6 6 6 6 6 6 6 5%NaOH(mL) 4.0 4.0 4.0 4.0 4.0 4.0 4.0 蒸馏水(mL) 5.2 5.0 4.8 4.6 4.4 4.2 4.0 3、探究不同时间对黄酮提取的影响 分别称取6分1g的银杏叶粉末,放在50mL的三角锥形瓶中,并作相应标记,分别加入70%的乙醇溶液各20mL,在超声波清洗机(500W)超声30 min、35 min 、40min、45 min、50min、 55min将溶液用高速离心机离心后除去滤渣,得到粗产品,用量筒量体积做记录,等待备用。 4、探究不同浓度的乙醇对总黄酮提取的影响
植物总黄酮的提取与测定
试验植物总黄酮的提取与测定 摘要本实验采用紫外分光光度法测定芹菜体内总黄酮含量,利用黄酮类化合物与铝盐反应生成红色络合物。以芦丁为标准品在510nm处测定吸光度。得出标准曲线,然后计算样品的黄酮量。下面会就本实验出现的一些状况作出详尽想分析。 材料与方法 材料新鲜芹菜叶 方法 试剂的配制 标准品芦丁;甲醇;石油醚;磷酸;95%乙醇;硝酸铝;亚硝酸钠;氢氧化钠;去离子水 步骤 1 总黄酮提取称取新鲜芹菜叶子10.0g,研磨后于回流装置中用70ml 95%乙醇回流2h,过滤,然后用石油醚做溶剂萃取1~2次去脂溶物。溶剂用量为提取液的1/2,除脂后浓缩并定容至50ml。 2 芹菜黄酮含量的测定吸取10ml置25ml容量瓶中,加30%乙醇2.5ml,再加入5%亚硝酸钠溶液0.75ml摇匀,放置5min,加10%硝酸铝液0.75ml,摇匀,放置5min,再加1mol/L NaOH溶液10ml,摇匀,加30%乙醇至刻度,放置10min,在510nm波长处测定吸光度。同时,取上述稀释液10ml,置于25ml容量瓶中,
加30%乙醇至刻度,作为对照溶液。根据测得的吸光度得出标准曲线 3 标准溶液配制精确称取与120℃真空干燥至恒重的芦丁标准品20mg,置100ml容量瓶中,加60%乙醇溶液,稀释至刻度,精确量取25ml,置于50ml容量瓶中,稀释至刻度,摇匀既得每1ml 含芦丁0.1mg的标准溶液。 4标准曲线制作精确量取标准溶液0。0,2.5,5.0,7.5,10.0,12.5ml,分别置于25ml容量瓶中,加30%乙醇补足至12.5ml,加5%亚硝酸钠溶液0.75ml摇匀,放置5min,精确加入10%硝酸铝液0.75ml,摇匀,放置5min,再精确加入1mol/L氢氧化钠液10ml,用30%乙醇稀释至刻度,以第一管为空白,与510nm波长下测定吸光度,以吸光度为纵坐标,浓度为横坐标,绘制标准溶液。 结果 标准:A1=0.000;A2=0.121;A3=0.266;A4=0.394;A5=0.530;A6=0.673 样品:A(1)=0.000;A(2)=0.036
黄酮类化合物抗氧化特性的研究进展【综述】(精)
Review: 黄酮类化合物的抗氧化活性 王仲承 0930******* 【摘要】 黄酮类化合物作为一种广泛分布于植物界的天然化合物, 具有治疗心血管疾病、抗氧化、消炎杀菌等多种药用意义。本文挑选其抗氧化的特性进行分析, 着力于揭示其在抗衰老、癫痫等神经性疾病的治疗等方面的药物开发前景与意义。 【关键词】 黄酮 , 天然物提取 , 天然药物 , 抗衰老 , 抗氧化 【正文】 1 黄酮类化合物简介 黄酮类化合物(flavonoids 是一类存在于自然界的、具有 2-苯基色原酮(flavone 结构的化合物。它们分子中有一个酮式羰基,第一位上的氧原子具碱性, 能与强酸成盐, 其羟基衍生物多具黄色,故又称黄碱素或黄酮。 黄酮类化合物以黄酮(2-苯基色原酮为母核而衍 生的一类黄色色素,包括黄酮的同分异构体及其氢化的
还原产物。黄酮类化合物在植物界分布很广,在植物体 中通常与糖结合成苷类,小部分以游离态(苷元的形 式存在。绝大多数植物体内都含有黄酮类化合物,它在 植物的生长、发育、开花、结果以及抗菌防病等方起着 重要的作用。天然黄酮类化合物母核上常含有羟基、甲 氧基、烃氧基、异戊烯氧基等取代基。由于这些助色团的存在,使该类化合物多显黄色。又由于分子中γ-吡酮环上的氧原子能与强酸成盐而表现为弱碱性, 因此曾称为黄碱素类化合物。 [1] 根据三碳键结构的氧化程度和β环的连接位置等特点,黄酮类化合物可分为下列几类:黄酮和黄酮醇;黄烷酮(又称二氢黄酮和黄烷酮醇(又称二氢黄酮醇;异黄酮;双黄酮类;异黄烷酮(又称二氢异黄酮;查耳酮;二氢查耳酮;橙酮(又称澳咔等。
黄酮类化合物中有药用价值的化合物很多。在心血管疾病治疗方面, 槐米中的芦丁和陈皮中的陈皮苷, 能降低血管的脆性, 及改善血管的通透性、降低血脂和胆固醇,用于防治老年高血压和脑溢血; 红茶绿茶中含有的儿茶酚等黄酮类物质还能 够减轻自发性高血压的症状; 由银杏叶制成的舒血宁片含有黄酮和双黄酮类, 用于 冠心病、心绞痛的治疗。在抗癌治疗方面, 黄芩苷、黄芩素和汉黄芩素对癌细胞增殖都有一定的抑制作用; 槲皮素的抗肿瘤活性与其抗氧化作用、抑制相关酶的 活性、降低肿瘤细胞耐药性、 诱导肿瘤细胞凋亡及雌激素样作 黄酮类化合物的基本结构 用等有关。在肝炎治疗方面,水飞蓟素对中毒性肝损伤、急慢性肝炎、肝硬化等有良好的治疗作用;淫羊藿黄酮、黄岑素、黄岑苷能抑制肝组织脂质过氧化、提高肝脏 SOD 活性、减少肝组织脂褐素形成, 对肝脏有保护作用。在消炎镇痛方面, 金荞麦中的双聚原矢车菊苷元有抗炎、解热、祛痰等作用; 金丝桃苷、芦丁、槲皮素及银杏叶总黄酮等有良好的镇痛作用。此外,大多数黄酮类化合物均有较强的抗氧化自由基作用,还具有降压、降血脂、抗衰老、提高机体免疫力、泻下、镇咳、祛痰、解痉及抗变态等药理活性。 [2-4] 2黄酮类化合物的抗氧化活性 多数黄酮类化合物具有一定的抗氧化作用,黄酮结构中的 2, 3 双键和 4 位羰基以及 3 或 5 位羟基对黄酮的抗氧化作用有重要贡献 [4]。黄酮类化合物在抗氧化反应中不仅能清除链引发阶段的自由基, 而且可以直接捕获自由基反应链中的自由基, 阻断自由基链反应, 起到预防和断链的双重作用 [5]。 2.1抗氧化物质清除自由基的作用原理 自由基系含有未成对电子的原子、原子团或分子。生物体内自由基的生成途径主要有三条 :
总黄酮的测定方法
总黄酮的测定方法 黄酮类化合物是广泛存在于植物界的一大类天然产物,种类繁多, 大多数黄酮类化合物与葡萄糖或鼠李糖结合成苷,部分为游离态或与鞣质结合存在。黄酮化合物系色原烷或色原酮的2-或3-苯基衍生物, 一般具有C6-C3-C6的基本骨架结构。近年来, 黄酮类化合物以其广谱的药理作用倍受青睐, 人们对含有黄酮的化合物进行大量研究, 以期获得黄酮含量较高的中草药。因此黄酮的含量测定成为研究的关键步骤。 一、方法 (一)高效液相色谱法 1. 原理植物类样品用石油醚脱脂后,经甲醇加热回流提取,以高效液相色谱法分离,在紫外检测器360nm条件下,以保留时间定性、峰面积定量。 2.仪器和试剂(1)高效液相色谱仪(2)紫外检测器(3)层析柱(4)超声波清洗仪(5)索氏提取器 (6)微孔过滤器(滤膜0.45um)(7)甲醇(色谱纯)(8)芦丁标准品 (9)石油醚,盐酸,磷酸(分析纯)。(10)去离子水 (11)芦丁标准溶液:精确称取经105℃干燥恒重的芦丁标谁品15.0mg,加甲醇溶解并定容至100ml,配成150ug/ml的芦丁标准溶液 3. 操作步骤 (1)样品处理 1)固体样品:称取2.0g干燥的固体样品,研细,置于索氏提取器中,用石油醚(60~90℃)提取脂肪等脂溶性成分,弃去石油醚提取液,剩余物挥去石油醚,加人甲醇50ml和25%HC1 5ml,80℃水浴回流水解1h,取出后快速冷却至室温,转移至50ml容量瓶中,甲醇定容,经0.45um滤膜过滤,供分析用。 2)液体样品:准确吸取样品2.0ml,直接以石油醚萃取脱脂,挥去石油醚后, 以甲醇溶解并定容,经微孔滤膜(0.45um)滤过后供测定用。 (2)色谱分离条件 色谱柱:CLC-ODS,6mm×150mm,5um; 流动相:0.3%磷酸水溶液:甲醇(V:V)=40:80,临用前用超声波脱气;流速:lml/min;柱温:40℃;检测波长:360nm;灵敏度:0.02AUFS;进样量:20ul。 (3)样品测定:准确吸取样品处理液和标准液各10ul,注入高液相色谱仪进行分离,以其标准溶液峰的保留时间定性,以其峰面积计算出样品中总黄酮的含量。4、结果计算 (二)分光光度法
黄酮含量测定
一、黄酮含量的测定方法 1、样品的处理 取材料地上部分洗净,晾晒至表面无水分,置于干燥箱中,80℃下干燥至恒重,磨成粉末,过筛待用。 2、标准曲线的绘制 准确称取芦丁对照品20mg,置于100ml容量瓶中,加体积分数70%乙醇溶解至刻度,摇匀得0.2mg/ml的对照品溶液。然后,分别吸取0、0.4、0.8、1.2、1.6、2.0、2.4ml,分别置于7支试管中,加水补齐至2.4ml,分别加入5%亚硝酸钠0.4ml,摇匀,放置6min。再加入10%硝酸铝溶液0.4ml,摇匀,放置6min。加入4.3%氢氧化钠溶液4ml,然后分别加2.2ml水,摇匀,放置15min。以空白试剂为参比,用紫外分光光度计在500nm波长处测定吸光度。 3、黄酮的提取(微波提取法) 准确称取干燥至横重的野生马齿苋粉末3份,每份1g,分别置于锥形瓶中,喷洒适量蒸馏水润湿,用中高火微波处理90s。加入一定量体积分数为70%的乙醇溶液,于80℃恒温水浴加热提取1.5h,趁热过滤,洗涤残渣,用70%乙醇定容于50ml容量瓶中,摇匀,得黄酮提取液。 4、黄酮含量的计算 吸取分别黄酮提取液1ml,加1.4ml蒸馏水,摇匀,加入5%亚硝酸钠0.4ml,摇匀,放置6min。再加10%硝酸铝溶液0.4ml,摇匀,放置 6min。加入4.3%氢氧化钠溶液4ml。加入蒸馏水2.8ml,摇匀放置15min。
以蒸馏水代替黄酮提取液的空白试剂为参比,用紫外分光光度计在500nm波长出测定吸光度。带入标准曲线中,计算黄酮含量。 总黄酮含量(mg/g)= c*v/m 式中:c为1ml样品中测得的黄酮含量(mg); v为提取液总体积(ml); m为叶片干重。 二、矿质元素的测定 每份需0.2g
