化学人教版九年级下册第十章 酸和碱
人教版九年级下册化学第十单元酸和碱知识点总结
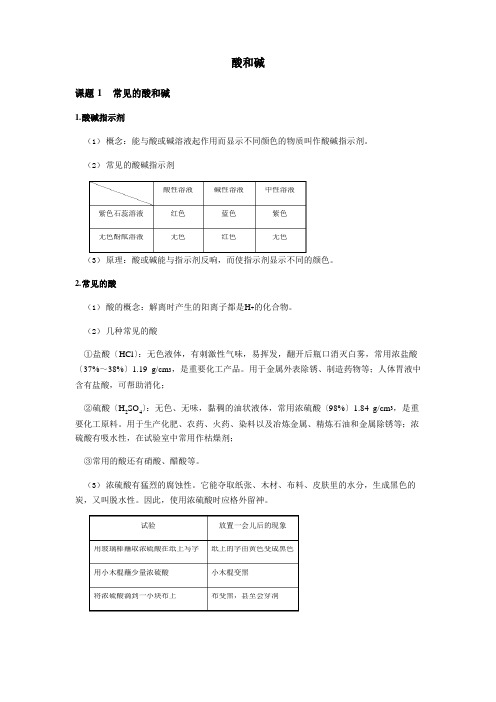
4酸性溶液碱性溶液 中性溶液 紫色石蕊溶液红色 蓝色 紫色 无色酚酞溶液 无色 红色 无色试验放置一会儿后的现象 用玻璃棒蘸取浓硫酸在纸上写字纸上的字由黄色变成黑色 用小木棍蘸少量浓硫酸小木棍变黑 将浓硫酸滴到一小块布上 布变黑,甚至会穿洞酸和碱课题 1 常见的酸和碱1. 酸碱指示剂(1) 概念:能与酸或碱溶液起作用而显示不同颜色的物质叫作酸碱指示剂。
(2) 常见的酸碱指示剂(3) 原理:酸或碱能与指示剂反响,而使指示剂显示不同的颜色。
2. 常见的酸(1) 酸的概念:解离时产生的阳离子都是H +的化合物。
(2) 几种常见的酸①盐酸〔HCl 〕:无色液体,有刺激性气味,易挥发,翻开后瓶口消灭白雾,常用浓盐酸〔37%~38%〕1.19 g/cm 3,是重要化工产品。
用于金属外表除锈、制造药物等;人体胃液中含有盐酸,可帮助消化;②硫酸〔H 2SO 〕:无色、无味,黏稠的油状液体,常用浓硫酸〔98%〕1.84 g/cm 3,是重要化工原料。
用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;浓硫酸有吸水性,在试验室中常用作枯燥剂;③常用的酸还有硝酸、醋酸等。
(3) 浓硫酸有猛烈的腐蚀性。
它能夺取纸张、木材、布料、皮肤里的水分,生成黑色的炭,又叫脱水性。
因此,使用浓硫酸时应格外留神。
42 2 2 2 2(4) 浓硫酸的稀释:稀释浓硫酸时,确定要把浓硫酸沿器壁渐渐注入水里,并用玻璃棒 不断搅拌。
假设将水注入浓硫酸,由于水的密度较小,水会浮在浓硫酸上面,溶解时放出的热能使水马上沸腾,使硫酸液滴向四周飞溅。
假设不慎将浓硫酸沾到皮肤或衣服上,应马上 用大量水冲洗,然后涂上 3%~5%的碳酸氢钠溶液。
3. 酸的化学性质①与酸碱指示剂作用:能使紫色石蕊溶液变红,使无色酚酞溶液不变色;②与活泼金属反响: Mg+2HCl =MgCl 2+H 2↑; Mg+H 2SO 4=MgSO 4+H 2↑; Zn+2HCl = ZnCl 2+H ↑;Zn+H SO =ZnSO +H ↑;Fe+2HCl =ZnCl +H ↑;Fe+H SO =FeSO +H ↑;③与金属氧化物反响:Fe 2O 3+6HCl =2FeCl 3+3H 2O ;Fe 2O 3+3H 2SO =Fe 2(SO 4)3+3H 2O 。
人教版九年级下册化学第十单元酸和碱知识点归纳

酸和碱的性质浓硫酸不慎沾到皮肤上,应先用干抹布讲其擦拭干净,再用大量的水冲洗,然后涂上3%到5%的碳酸氢钠溶液。
二.酸的化学性质:(由于酸溶液中的阳离子都是 H +,所以具有下列共性。
) 1.跟酸碱指示剂的作用酸溶液(如:盐酸、稀硫酸、稀硝酸)都能使紫色石蕊试液变红,无色酚酞试液遇酸不变色。
注意:浓硫酸和浓硝酸具有强氧化性,跟酸碱指示剂作用时,颜色变化不符合上述规律。
2.酸能跟Al 、Mg 、Fe 、Zn 等比H 活泼的金属发生置换反应生成盐和氢气。
金属 + 酸 = 盐 + 氢气 稀盐酸与金属反应:2Al + 6 HCl = 2AlCl 3 + 3 H 2↑, Mg + 2 HCl = MgCl 2 + H 2↑ Zn + 2 HCl = ZnCl 2 + H 2↑, Fe + 2 HCl = FeCl 2 + H 2↑ 稀硫酸与金属反应:2Al + 3H 2SO 4 = Al 2(SO 4)3 + 3H 2↑, Fe + H 2SO 4 = FeSO 4 + H 2↑ Zn + H 2SO 4 = ZnSO 4 + H 2↑, Mg + H 2SO 4 = MgSO 4 + H 2↑注意:①实验室用锌与稀硫酸反应制取氢气;②铁参加置换反应生成的是+2价的亚铁离子:Fe 2+;③相同质量的金属与足量的酸反应生成氢气的质量又多到少的顺序:Al 、Mg 、Fe 、Zn 。
;④金属活动顺序表:钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金。
3.酸能与一些金属氧化物(碱性氧化物)反应,生成盐和水金属氧化物+ 酸= 盐 + 水CuO + 2HCl = CuCl 2 + H 2O , CuO + H 2SO 4 = CuSO 4 + H 2OFe 2O 3 + 6HCl = 2FeCl 3 + 3H 2O , Fe 2O 3 + 3H 2SO 4 = Fe 2(SO 4)3 + 3H 2O 注意:工业上常用盐酸或稀硫酸出去铁制品表面的铁锈。
人教版九年级化学下册第十单元酸和碱复习(68张PPT)

浓盐酸
浓硫酸
(二)稀盐酸的化学性质
• 1、稀盐酸与酸碱 指示剂反应
紫色 无色 蓝色 pH 石蕊 酚酞 石蕊 试液 试液 试纸 遇酸 遇酸 遇酸
变红 不变色变红 pH<7
1.酸碱指示剂:能跟酸或碱的溶液起作用而显示 不同的颜色的物质叫做酸碱指示剂。
CaO+H2O === Ca(OH)2
高温
CaCO3===CaO+CO2
小结:NaOH溶液、Ca(OH)2溶 液的化学性质
• 1、NaOH溶液、Ca(OH)2溶液与酸碱指示 剂反应
• 2、 NaOH溶液、Ca(OH)2溶液和酸反应, 生成盐和水
• 3、 NaOH溶液、Ca(OH)2溶液与非金属氧 化物反应
氢氧化钠和氢氧化钙的物理性质和用途
氢氧化钠
氢氧化钙
俗称 颜色、状态
溶解性 其他
用途
苛性钠、火碱、烧碱 (强腐蚀性)
熟石灰、消石灰 (有腐蚀性)
白色固体
极易溶于水,放出大 量热,溶液有涩味和滑腻 感。
易潮解 (做干燥剂)
白色粉末
微溶于水 (溶液俗称石灰水)
可由生石灰加水制得(放热) CaO+H2O=Ca(OH)2
颜 色
状态
露置在空气 中的变化
在水中的溶 解情况
头发在热的氢氧化 其 钠溶液中的变化 他
氢氧 化钠
白色 固体
易潮解
极易溶于水放 出大量的热
溶解,变黄
氢氧 化钙
白色
粉末状 固体
无变化
微溶于水
氢氧化钠(NaOH) (1)暴露在空气中易潮解,因此应密封保存。 (2)俗称苛性钠、火碱或烧碱,有强烈的腐蚀性。 若不慎沾到皮肤上,应立即用大量水冲洗,再涂上硼 酸溶液。
人教版九年级下册化学第十单元 酸和碱 总复习知识点总结

第十单元酸和碱课题1 常见的酸和碱1、酸、碱、盐、的定义及举例:①酸:酸由氢离子和酸根组成的如:硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3)。
②碱:碱是由金属离子和氢氧根组成的化合物如:氢氧化钠(NaOH)、氢氧化钙Ca(OH)2 、氨水(NH3·H2O)。
③盐:由金属离子(或铵根)和酸根组成的化合物一定是盐如:氯化钠(NaCl)、碳酸钠(Na2CO3)、氯化铵(NH4Cl)。
2、酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子)。
3、拓展:酸、碱、盐、的定义电离:氯化钠(NaCl)溶解在水时,产生了能够自由移动的钠离子(Na+)和氯离子(Cl-)的过程称为电离。
可用电离方程式表示:NaCl == Na+ + Cl- (也要配平)①酸是电离时生成的阳离子全部都是氢离子(H+)的化合物。
但碳酸氢钠NaHCO3不是酸,因为NaHCO3 ==Na+ + H++ CO32-电离时生成的阳离子不是全部是氢离子。
②碱是电离时生成的阴离子全部都是氢氧根离子(OH-)的化合物。
但碱式碳酸铜Cu2(OH)2CO3不是碱,因为Cu2(OH)2CO3 == 2Cu2+ + 2 OH- + CO32-电离时生成的阴离子不是全部是氢氧根离子。
③盐是电离时生成金属离子(或铵根)和酸根离子的化合物。
碳酸氢钠NaHCO3、碱式碳酸铜Cu2(OH)2CO3也是盐,因为电离时只要有金属离子和酸根离子的化合物就是盐。
4、酸碱指示剂变色规律:石蕊溶液遇酸溶液变红色,遇碱溶液变蓝色;酚酞溶液遇酸溶液不变色,遇碱溶液变红色。
中性(大多盐如NaCl)溶液遇石蕊、酚酞溶液均不变色。
5、盐酸的物理性质、用途:“纯净”的盐酸是混合物,是无色有刺激性气味的液体,打开浓盐酸瓶盖有白雾(不是白烟)产生,说明盐酸具有挥发性,这是因为从浓盐酸中挥发出来的氯化氢气体跟空气中的水蒸气接触,形成了盐酸的小液滴。
工业盐酸因含有铁离子而呈黄色。
人教版九年级化学下册第十单元《酸和碱》教学课件

常见的酸
【典型例题8】盐酸和稀硫酸在溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是 (B ) A.打开盛有浓盐酸和浓硫酸的试剂瓶塞,在瓶口都有白雾 B.稀盐酸和稀硫酸都可用于除铁锈 C.浓硫酸和浓盐酸可用来干燥氧气 D.在稀盐酸和稀硫酸中滴加氯化钡溶液,都有白色沉淀 A、浓硫酸具有吸水性不具有挥发性,瓶口没有白雾,浓盐酸具有挥发性挥发出氯化氢气体,氯化氢 与空气中的水蒸气接触形成盐酸小液滴,所以瓶口有白雾,故A错误; B、铁锈的主要成分是氧化铁,因此稀盐酸和稀硫酸都可用于除铁锈,故B正确; C、浓盐酸不具有吸水性,不能做干燥剂;浓硫酸具有吸水性可以做干燥剂,故C错误; D、稀盐酸、稀硫酸中滴加氯化钡化钡溶液,只有硫酸中生成硫酸钡沉淀,盐酸不与氯化钡反应,没 有沉淀生成。故D错误。故选B。
(1)写出图中a、b两种仪器的名称:_____玻_璃__棒____、_量__筒____。 (2)b 容器所盛的试剂是__浓__硫_酸___(填“水”或“浓硫酸”)。 (3)稀释时,若两种试剂添加顺序颠倒,将会发生 __硫__酸__飞_溅____。 【联系与拓展】据媒体报道,2020 年5 月有一村民在家里误将装在酒瓶中的稀硫酸当成白酒喝下,造 成食道和胃严重损伤,这是因为稀硫酸具有__强_腐__蚀_性___。 这一事件警示我们,家中存放或使用药物时应注意_____贴_好__标_签__和__仔_细__阅_读__使__用_说__明____。 【解析】(1)据图可知a是玻璃棒,b是量筒;(2)浓硫酸的密度比水大且溶于水时放出大量的热,故 稀释时要将浓硫酸慢慢注入到水中,所以b中盛放的是浓硫酸;(3)浓硫酸的密度比水大且溶于水放出 大量的热,若顺序颠倒,则会使水浮在浓硫酸的上面,造成硫酸溅出,硫酸具有腐蚀性; 【联系与拓展】据媒体报道,2014年5 月有一村民在家里误将装在酒瓶中的稀硫酸当成白酒喝下,造成 食道和胃严重损伤,这是因为稀硫酸具有强腐蚀性;这一事件警示我们,家中存放或使用药物时应注意 贴好标签和仔细阅读使用说明。
九年级化学下册“第十单元 酸和碱”必背知识点

九年级化学下册“第十单元酸和碱”必背知识点一、酸和碱的定义1. 酸:电离时生成的阳离子全部是氢离子的化合物。
例如,盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)等。
2. 碱:电离时生成的阴离子全部是氢氧根离子的化合物。
例如,氢氧化钠(NaOH)、氢氧化钙[Ca(OH)2]、氨水(NH3·H2O)等。
二、酸和碱的性质1. 酸碱指示剂无色酚酞:遇酸不变色,遇碱变红色。
紫色石蕊:遇酸变红色,遇碱变蓝色。
2. 酸的通性1. 与指示剂作用:使紫色石蕊变红,无色酚酞不变色。
2. 与活泼金属反应:生成盐和氢气。
例如,Zn + H2SO4 = ZnSO4 + H2↑。
3. 与金属氧化物反应:生成盐和水。
例如,Fe2O3 + 6HCl = 2FeCl3 + 3H2O。
4. 与碱反应:生成盐和水 (中和反应)。
例如,NaOH + HCl = NaCl + H2O。
5. 与某些盐反应:生成新盐和新酸(复分解反应)。
例如,AgNO3 + HCl = AgCl↓+ HNO3。
3. 碱的通性1. 与指示剂作用:使紫色石蕊变蓝,使无色酚酞变红 (仅限于可溶性碱)。
2. 与酸性氧化物反应:生成盐和水。
例如,2NaOH + CO2 = Na2CO3 + H2O。
3. 与酸反应:生成盐和水 (中和反应)。
例如,NaOH + HCl = NaCl + H2O。
4. 与某些盐反应:生成新碱和新盐(复分解反应)。
例如,2NaOH + CuSO4 = Na2SO4 + Cu(OH)2↓。
三、酸碱度的表示方法——pH1. 定义:pH是表示溶液酸碱性强弱的一种指标。
2. 测定方法:使用pH试纸。
将少量待测液滴在干燥的pH试纸上,再与标准比色卡对照,读出溶液的pH值。
3. 范围与意义:pH = 7,溶液呈中性。
pH < 7,溶液呈酸性;pH越小,酸性越强。
pH > 7,溶液呈碱性;pH越大,碱性越强。
四、酸碱反应的应用1. 中和反应:酸和碱作用生成盐和水的反应。
人教版九年级下册化学常见的酸和碱-第一课时 指示剂

自制酸碱指示剂
收集不同颜色的新鲜花瓣或紫萝卜皮,各取适 量,研碎,加入适量水和酒精(两者体积比 为1:1),浸泡,过滤,得到植物色素提取液。 将提取液分别装入小试剂瓶中备用。 将上述植物色素提取液分别滴入白醋、蒸馏水、 澄清石灰水中,观察颜色的变化,并记录。 选择颜色变化明显的植物色素提取液作为酸碱 指示剂,并检验稀盐酸、氨水、食盐水等溶 液的酸碱性。
4.常见的碱有氢氧化钠(NaOH)、氢氧化 钙[Ca(OH)2]、氢氧化钾(KOH)、氢氧化铜 [Cu(OH)2]、氨水(NH3· H2O)等。
从名称上看都叫“氢氧化某”;从结构上 看都含有氢氧根(OH)
二、酸、碱、盐的定义
1、酸:电离生成的阳离子全都是 氢离子的化合物。 2、碱:电离生成的阴离子全都是 氢氧根离子的化合物。 3、盐:电离生成金属离子和酸根 离子的化合物。
3、下图是某同学在电脑屏幕上绘制的 酸、碱、盐电离图片,○表示H+, ●表示Na+,●表示OH-,●表示 Cl-,其中描述的是酸的电离的是 ( )
4、下图是试验物质导电性的实 验,其中灯泡不亮的是 ( )
5、含有下列离子的溶液中,溶 质全部为酸的是 ( ) A.H+、Na+、SO42- + - - B.H 、Cl 、NO3 - + 2 + C.OH 、K 、Ba D.Ag+、K+、NO3-
从紫罗兰花变色的现象中发现了 酸碱指示剂
探究 自制酸碱指示剂
1. 阅读“资料卡片——酸碱指示剂的发现”,你从 中能获得什么启示?与同学交流。
2. 自制酸碱指示剂。 (1) 取几种植物的花瓣或果实(如牵牛花、月季花、 紫甘蓝等), 分别在研钵中捣烂, 加入酒精(乙醇与水 的体积比为1 ∶ 1)浸泡; (2) 用纱布将浸泡出的汁液过滤或挤出, 得到指 示剂; (3) 试验指示剂在下列4种溶液中的颜色变化。 (每小组可以自制1~2 种指示剂)
人教版九年级下册化学 第十单元 酸和碱 常见的酸和碱

C.稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中, 并用玻璃棒不断搅拌
D.稀硫酸、稀盐酸都可以用于金属表面除锈
11.下列物质可以利用金属和稀盐酸直接制取的是(AB )
A.MgCl2
B.FeCl2
C.CuCl2
铜与盐酸
D.生Fe成Cl3
不反应
FeCl2
巩固练习
13.将锈铁钉放入稀盐酸中看到哪些现象?并写出 化学方程式。
为了防止发生事故,在稀释浓硫酸时,一 定要_将__浓_硫__酸__沿__着_杯__壁__慢__慢_注__入__水__中_____, 并不断搅拌。
巩固练习
下列说法错误的是( B )
A.浓盐酸放置一段时间后,溶液的质量会减少
B.浓盐酸在空气中会冒白烟 应该是冒白雾
C.浓硫酸敞口放置一段时间后,溶液的质量会增加 D.浓硫酸溶于水时会放出大量的热
①酸能使酸碱指示剂显示不同的颜色; ②酸能与多种活泼金属反应,生成氢气; ③酸能与某些金属氧化物反应,生成水。
练习:向放有铁锈的钉子的试管中加入过量盐酸,充分 反应后,铁锈消失, 并有气泡产生,写出有关反应的化学方 程式:__F_e_2_O_3_+__6_H_C_l_=__2_F_e_C_l_3_+_3_H__2O_、 ____F_e_+__2_H_C__l =__F_e_C_l_2_+_H__2_↑______ .
1.在不同的酸溶液中都含有相同的H+,因此不同的酸的化学 性质是相似的。
(2)酸溶液能与活泼金属反应(请回忆第八单元并填表)
与稀盐酸反应
与稀硫酸反应
镁 Mg+2HCl=MgCl2+H2 ↑ Mg+H2SO4=MgSO4+H2 ↑ 锌 Zn+2HCl=ZnCl2+H2 ↑ Zn+H2SO4=ZnSO4+H2 ↑ 铁 Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十单元酸和碱的复习课教案
竹溪县天宝乡中心学校柯昌东
一、教学目标
1.能灵活运用酸的知识、碱的知识解决老师创设的问题,达到对已有知识的回
顾,并总结构建出知识网络。
2. 学会用比较、分类、归纳、概括等方法加工信息。
3.通过酸与碱的复习,提高学生分析问题以及通过实验探究解决问题的能力。
培养学生的总结和归纳能力,并掌握学习的一些规律,提高实验探究能力。
4. 通过创设多样化学法,激发学生学习的兴趣,增强学生学习的自信心。
二、教学重难点
构建酸碱性质的知识网络,使知识形成系统化。
三、教学方法
对比与讲练相结合、实验与探究相结合
四、教学过程
(一)复习引导
1、解读2017年中考说明,让学生了解并掌握本章中考考点,理清复习思路。
2、结合导学案,回顾本章知识点。
(二)合作探究
1、通过PPT师生合作对知识点进行系统的回顾。
①、浓酸的性质和用途;
②、稀硫酸及稀盐酸的化学性质;
③、常见的碱;
④、碱的化学性质;
⑤、酸碱性及酸碱度;
⑥、酸碱中和反应;
2、针对复习进行课堂简单训练,加深对知识点的掌握。
(三)、拓展提升
冲击中考试题
五、巩固提高
六、板书设计
第十单元酸和碱
一、常见的酸与碱
1、常见的酸;
2、常见的碱;
二、酸碱的化学性质
1、酸的通性;
2、碱的通性;
三、中和反应
四、溶液酸碱性的定量表示——酸碱度。
