人教版初中化学 第五单元 化学方程式 同步练习 (含答案)
人教版九年级化学上册第五单元整章同步练习化学方程式(含答案)

人教版九年级化学上册第五单元整章同步练习化学方程式5.1 质量守恒定律1.在化学反应前后,下列物理量可能发生变化的是( )A.原子的数目B.元素的种类C.物质的总质量D.分子的数目2.将20克甲、5克乙、8克丙三种纯净物混合,在密闭容器中加热发生化学反应,经分析可知:反应后混合物中含有5克甲、16克丙,还含有一种新物质丁。
则丁物质的质量是( )A.12 g B.9 g C.4 g D.17 g3.下列验证质量守恒定律的实验中,能得出正确结论的是( )4.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反反应后,甲的“待测”值应为( )A.10 B.8 C.4 D.05.下列现象不能用质量守恒定律解释的是( )A.纸燃烧化为灰烬,灰烬的质量比纸的质量小B.镁条燃烧,生成物的质量比镁条的质量大C.水结冰质量不变D.蜡烛燃烧后质量减小5.1 质量守恒定律1.D 2.A 3.A 4.D 5.C人教版化学九年级上同步练习 5.2 如何正确书写化学方程式第一课时 化学方程式的书写1.下列对应的化学方程式书写完全正确的是( )A .用澄清的石灰水检验二氧化碳气体:CO 2+Ca(OH)2===CaCO 3↓+H 2OB .用水的电解实验测定水的组成:2H 2O=====通电2H 2+O 2C .在密闭的容器中燃烧镁条验证质量守恒定律:Mg +O 2=====点燃2MgO 2D .用胃舒平(主要成分是氢氧化铝)治疗胃酸过多:HCl +Al(OH)3===AlCl 3+H 2O2.某发电厂烟气处理的新工艺是:CH 4+2NO 2===N 2+X +2H 2O ,则X 的化学式为( ) A .CO B .CO 2 C .O 2 D .C 3.请用化学方程式表示下列反应原理。
(1)水滴入氢化钙(CaH 2)中放出氢气,并生成氢氧化钙[Ca(OH)2]:________________________________________________________________________。
人教版初中化学第五单元化学方程式单元测试题及答案

第五单元《化学方程式》测试题(一)1.本试卷包含选择题(第 1 题~第 20 题,共 40 分)、非选择题(第 21 题~第 26 题,共 60 分)两部分。
本卷满分100 分,考试时间为90 分钟。
2.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Al 27 P 31Zn 65第Ⅰ卷(选择题40分)一、选择题(本大题包含20 个小题,每题只有一个选项切合题意,请将正确答案的序号填到第Ⅱ卷的表格中。
)1.在以下各项中,化学反响前后必定没有发生改变的是()①原子的数量②分子的数量③元素的种类④物质的总质量⑤物质的种类⑥原子的种类A. ①③④⑤B.①③④⑥C.①④⑥D.①③⑤2.依据质量守恒定律判断,铁丝在氧气中完整焚烧,生成物的质量()A. 必定大于铁丝的质量B. 必定小于铁丝的质量C. 必定等于铁丝的质量D. 不可以确立3.化学方程式 3Fe + 2O2 Fe O 可读作()3 4A.铁加氧气等于四氧化三铁 B .三个铁加两个氧气等于一个四氧化三铁C.铁和氧气点燃后生成四氧化三铁 D .铁加氧气点燃等于四氧化三铁4.某物质在纯氧中焚烧生成了氮气和水蒸气,该物质必定含有()A. 氮元素和氧元素B.氢元素和氧元素C.氮元素和碳元素D.氮元素和氢元素5.以下化学方程式正确的选项是()A. S + O 2SO2↑B. 4Al +3O22Al 2 O3C. P + O 2PO2D. Mg + O2MgO26.以下反响不属于分解反响的是()A. H2 CO3== CO2↑+H2O B.2HgO2Hg+O↑C. 2HO22H2O+O2↑ D .Mg+CuO Cu+MgO7.以下反响中.有一种元素从+ 2 价变成 0 价的是 ()A. S+O2SO2B.2Mg+O2MgOC . CuO+HCu+HO D . 2HO2H ↑ +O ↑2228.化学方程式 a C H + b O 2c H 2O +d CO 配平后 a 、 b 、 c 、 d 之和为 ()2 22A . 15B .14C . 13D .109.在化学反响 X + 2Y ==== Z 中, 3g X 和足量 Y 充足反响后生成 8g Z ,则参加反响的 Y 的质量为()A. 2.5 gB. 3 gC. 5 gD. 6 g10.以下各式中,正确表示铝与稀硫酸反响的化学方程式是()A .Al + H 2SO 4 ==== AlSO 4 + H 2↑B .2Al+ 3H 2SO ==== Al (SO) 3+3H ↑424 2C. Al + 2H 2SO 4 ==== Al(SO 4) 2 + 2H 2↑D. 2Al + H 2SO ==== Al SO + H ↑424211.在 2A+B == 2C 反响中,已知 A 的相对分子质量为 24,C 的相对分子质量为 40,则 B 的 相对分子质量为()A. 16 gB. 32 gC. 16D. 3212.以下说法能用质量守恒定律解说的是()A .mg 水受热变成 mg 的水蒸气B.62g 磷和 80g 的氧反响生成 142g 五氧化二磷C .20g 食盐溶于 80g 水获得 100g 的食盐水D .拧开盛酒精的瓶盖一段时间后质量变小13.9g 水在通电条件下可生成氢气的质量是()A. 1 gB. 2 gC. 3 gD. 4 g14.在 2HO 22H 2O+O 2↑的反响中,反响前后必定发生变化的是()A .元素种类B.各样原子的数量C .氧元素的化合价D.物质的质量总和15.铝在氧气中焚烧生成氧化铝。
2022年人教版九上《第五单元 化学方程式练习》同步练习(附答案)

《第五单元化学方程式》1.在化学反响X+Y=Z中,10gY和X完全反响生成25g Z,那么参加反响的X物质的质量为__________。
2.在化学反响A+B=C+D中,5gA与10gB恰好完全反响,生成9gC,假设要生成12gD,那么参加反响的A物质的质量为__________。
3.以下现象可以用质量守恒定律来解释的是-------------------------------------------------------〔〕A.100g酒精和100g水混合在一起,质量等于200g;B.10g水可以结成10g冰C.纸在空气中燃烧后化为灰烬,灰烬质量比纸的质量小D.敞口放置的酒精,越放越少4.硝酸铵可发生如下反响:2NH4NO32N2↑+O2↑+4______。
那么______中的物质应为A.H2B.H2O C.H2O2D.HNO35.以下化学方程式书写正确的选项是--------------------------------------------------------------------〔〕A.Al+2HCl=AlCl2+H2↑B.KMnO4K2MnO4+MnO2+O2↑C.3CO+Fe2O32Fe+3CO2D.Cu+FeSO4=CuSO4+Fe6.右以下图四位同学正在讨论某一个化学方程式表示的意义,他们所描述的化学方程式是〔〕〔相对原子质量:H一1;C—12;O—16;S一32〕A.S+O2点燃SO2B.2CO+O2 点燃2CO2C.2H2 +O2 点燃2H2OD.CH4 +2O2 点燃CO2+2H2O7.在—个密封容器内有X、Y、M、N四种物质,在—定条件下反响—段时间后,测得反响前后各物质的质量如下:物质X Y M N反响前质量(g) 10 10 10 10反响后质量(g) 10 15 8 7试推断该密闭容器中发生化学反响的根本类型是------------------------------------------------〔〕A.分解反响B.化合反响C.复分解反响D.置换反响《第五单元化学方程式》1.15g;2.10g;3.C;4.B;5.C;6.C;7.B。
人教版初中九年级化学上册第五单元《化学方程式》经典练习(含答案解析)
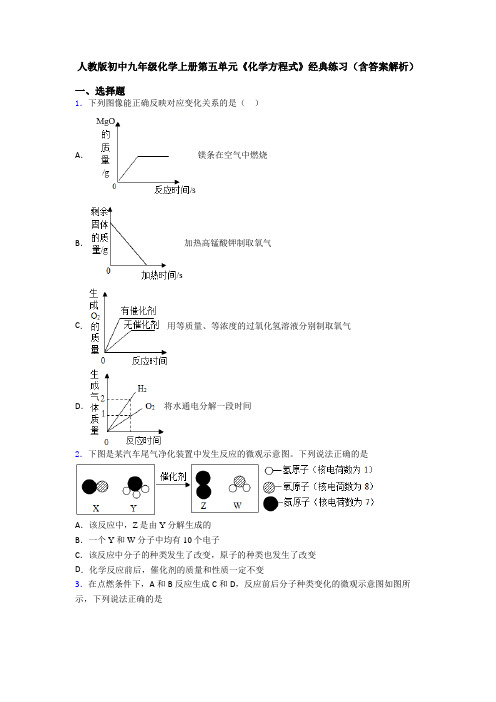
人教版初中九年级化学上册第五单元《化学方程式》经典练习(含答案解析)一、选择题1.下列图像能正确反映对应变化关系的是()A.镁条在空气中燃烧B.加热高锰酸钾制取氧气C.用等质量、等浓度的过氧化氢溶液分别制取氧气D.将水通电分解一段时间2.下图是某汽车尾气净化装置中发生反应的微观示意图。
下列说法正确的是A.该反应中,Z是由Y分解生成的B.一个Y和W分子中均有10个电子C.该反应中分子的种类发生了改变,原子的种类也发生了改变D.化学反应前后,催化剂的质量和性质一定不变3.在点燃条件下,A和B反应生成C和D,反应前后分子种类变化的微观示意图如图所示,下列说法正确的是A.图中只有两种氧化物B.生成C和D的分子个数比为1:1C.图中共有4种分子D.反应前后分子和原子的种类不变4.某化合物在4.8g氧气中完全燃烧,生成了4.4g二氧化碳和2.7g水。
关于该物质的推断中不正确的是()A.该化合物的质量为2.3gB.该化合物中一定含碳、氢、氧三种元素C.该化合物中碳、氧元素质量比为3:2D.分子中C、H原子个数比为1:25.一定条件下,将甲、乙、丙、丁四种物质放入密闭容器内充分反应,测得反应前后各物质的质量如下表所示。
下列说法正确的是:物质甲乙丙丁反应前质量/g22748反应后质量/g10.5 2.5待测8A.该反应属于化合反应B.甲和乙的质量比为21:5C.丁物质一定是该反应的催化剂D.反应后丙物质的质量为20g6.向一个密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生反应,测得有关数据如图所示。
下列说法不正确的是A.a的数值为4B.该反应为分解反应C.丁可能是反应的催化剂D.乙和丙的质量变化之比为2:17.逻辑推理是化学常用的思维方法。
下列推理正确的是A.单质由同种元素组成,所以由同种元素组成的物质一定是单质B.阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子C.氧气是由氧元素组成的,所以制取氧气的反应物中一定含有氧元素D.由同种分子构成的物质属于纯净物,所以纯净物都是由同种分子构成的8.下列由事实得出的结论正确的是()A.A B.B C.C D.D9.将一定量的炭放在含有一定质量的氧气的密闭容器中燃烧,实验数据如下表:A.①B.①②③C.②③D.①③10.推理是研究和学习化学的一种重要方法。
人教版九年级化学上册第五单元《化学方程式》测试题(含答案)
人教版九年级化学上册第五单元《化学方程式》测试题(含答案)一、选择题。
1、化学反应前后一定发生变化的是()A.原子数目B.分子数目C.物质种类D.物质的总质量2、在化学反应:2X2 + 3Y2 ===2R中,用X、Y表示R的化学式,正确的是()A.X2Y2B.X2Y3C.X4Y5D.X3Y23、用氯酸钾与二氧化锰混合加热制氧气的过程中,锰元素在固体中的质量分数随时间的变化关系正确的是()A.B.C.D.4、长途运输鱼苗时,为了防止鱼苗缺氧,常在水中加入物质X,发生反应的化学方程式为2X+2H2O2Ca(OH)2+O2↑,其中X的化学式为()A.CaOB.CaO2C.CaCO3D.CaCl25、已知A物质与B物质反应生成C物质,现有12克A与32克B恰好完全反应,则生成C物质的质量是( )A.44克B.32克C.22克D.12克6、对化学方程式4P + 5O22P2O5所表示的意义,下列说法正确的是()A.4个磷跟5个氧气反应,生成两个五氧化二磷B.磷加氧气等于五氧化二磷C.磷元素与氧元素结合生成两个五氧化二磷D.每4个磷原子可与5个氧分子反应生成两个五氧化二磷分子7、实验室通常用浓盐酸和二氧化锰在加热的条件下制取氯气。
反应的化学方程式为4HCl (浓)+MnO 2MnCl 2+2X+Cl 2↑,则X 的化学式为( )A .H 2B .O 2C .H 2OD .HClO8、21世纪初中缅油气管道天然气进口量突破50亿立方米。
天然气的主要成分是甲烷,甲烷燃烧的化学方程式为aCH 4+bO 2cCO 2+dH 2O ,则化学计量数之和等于( ) A.4B.5C.6D.79、一定质量的CH 4可与常见物质M 发生下图所示的循环反应,其中反应②为化合反应。
下列说法不.正确的是( )A .M 中铜元素的质量分数比Cu 2O 中的低B .理论上,循环过程中无需添加物质MC .反应①理论上每生成44gCO 2,同时生成18gH 2OD .总的化学表达式为:CH 4 + O 2M 一定条件CO 2 +H 2O10、已知含氢元素的物质完全燃烧后氢元素全部进入生成的水中,葡萄糖(C 6H 12O 6)和乙酸(CH 3COOH )组成的混合物240g ,在一定条件下完全燃烧,生成水的质量是( ) A .48gB .72gC .36gD .144g11、下列化学反应可用如图表示的是( )A.H 2CO 3CO 2↑+H 2OB.2H 2SO 3+O 22H 2SO 4C.2HClO2HCl+O 2↑ D.CaCO 3CaO+CO 2↑12、在反应X+2Y====R+2M 中,当1.6 g X 与Y 完全反应后,生成4.4 g R ,且反应生成的R 和M 的质量之比为11∶9,则在此反应中Y 和M 的质量之比为( )A.23∶9B.16∶9C.32∶9D.46∶913、下列实验不能直接用于验证质量守恒定律的是()A.B.C.D.14、人在剧烈运动后,血液中产生较多的乳酸(化学式为C3H6O3),使肌肉酸痛。
人教版九年级化学上册第五单元《化学方程式》测试题(含答案)

人教版九年级化学上册第五单元《化学方程式》测试题(含答案)一、单选题1.停电时,在烛光下看书学习是常有的事,长时间在烛光下看书,你的鼻孔会聚积一些黑色物质—炭黑。
此事实说明蜡烛(主要成分是石蜡)的组成中一定含有( ) A .碳元素B .氢元素C .氧元素D .铁元素2.下列说法不符合质量守恒定律的是( ) A .铜丝在火焰上灼烧后质量增加了 B .木炭燃烧后质量减少了 C .浓硫酸吸收水蒸气后质量增加了D .氢氧化钠溶液放置于空气中一段时间后质量增加了 3.下列物质对应的化学式不正确的是( ) A .氧化镁—MgOB .氯化氢—HClC .氧气—OD .氧化铜—CuO4.氯酸钾在二氧化锰的催化作用下受热分解制取氧气,其化学方程式书写正确的是( ) A . KClO 32MnO 加热KCl+O 2↑ B .2KClO 3加热2KCl+3O 2↑C .2KClO 32MnO 加热2KCl+3O 2↑ D .2KClO 32MnO 加热2KCl+3O 2↑5.下列涉及化学学科观念的说法正确的是( ) A .转化观:石墨转化为金刚石是物理变化B .微粒观:二氧化碳是由1个碳原子和2个氧原子构成的C .守恒观:1g 红磷和1g 氧气反应,生成2g 五氧化二磷D .结构观:构成水和过氧化氢的分子结构不同,故两种化合物的化学性质也不同6.下列反应的化学方程式,书写正确的是( ) A .磷在空气中燃烧:2524P+5O O P 点燃B .氧化汞加热分解:2HgO=Hg+O ↑C .硫在氧气中燃烧:22S+O SO ↑点燃D .细铁丝在氧气中燃烧:2343Fe+2O Fe O 点燃7.化学反应前后,可能发生变化的是( ) A .元素的种类B .原子的种类C .分子的数目D .物质总质量8.某化学反应的微观示意图如下图所示,下列说法正确的是镁原子( )A .该反应生成了3种物质B .反应涉及的物质中,是由原子构成的单质C .参加反应的和的微粒个数比是4:3D .反应前后元素的种类及化合价均未发生改变9.密闭容器中,一定质量的硫粉在过量的氧气中点燃,充分反应后,各相关量与时间的对应关系正确的是( )A .B .C .D .10.铜与浓硝酸反应的化学方程式为3322Cu+4HNO =Cu NO +2H O (+2X ↑)。
人教版九年级化学第五单元《化学方程式》单元测试题及答案

第五单元《化学方程式》测试题( 附答案 )可能用到的相对原子质量:H 1 C 12 O 16 N 14 Cl 35.5 S 32 Zn 65 Fe 56 Mg 24 K 39 Mn 55 一、选择题(每题只有一个答案一题 3 分,共 30 分)1.对于质量守恒定律,以下表达正确的选项是()A.煤焚烧化为灰烬,该反响不切合质量守恒定律;B.24g 镁在空气中完整焚烧生成40g 氧化镁,实质耗费空气的质量为16g;C.无数实考证明化学反响都按照质量守恒定律;D.质量守恒定律只合适于有气体或固体生成的化学反响。
2.某企业研发了一种由甲醇为原料的新式手机电池,其容量为锂电池的10 倍,可连续使用一个月才充一次电,其电池反响原理为:2CH3OH + 3X + 4NaOH == 2Na2CO3 + 6H 2O,此中 X 的化学式为()A.O2 B .CO C.CO2D.H23.如右图所示: 2 个甲分子反响生成 1 个丙分子和 3 个乙分子,以下判断不正确的选项是A、反响生成的丙物质属于单质B、参加反响的甲物质属于化合物C、该反响中原子的种类发生了改变D、依据质量守恒定律可推知, 1 个乙分子中含有 2个A原子4.在一密闭容器中,盛放A、 B、 C 三种物质各30g,加热充足反响后,各物质质量变化以下:对于此反响,以下认识不正确的选项是()A.物质有可能是单质B.变化后待测物 A 的质量为 5gC.该变化的基本反响种类是分解反响D.C物质中所含有的元素种类是A、B、D三种物质中全部元素种类之和5.在反响 A+2B=C+2D中, 9.8gA 与 8gB 完整反响,生成14.2gC,则以下结论正确的是()A、生成 D1.8gB、质量比为49∶40∶71∶ 18C、生成 D7.2gD、相对分子质量比98∶80∶ 142∶36理的是 (m 可与 n 相等,也可不相等 ) ()A.必定等于 (m+n)g B.必定小于 (m–n)gC.可能是小于或等于 (m+n)g D.以上答案都正确7:7. A 、B 两元素可形成多种化合物,已知在 A B 化合物中, A 和 B 的质量比为24,则切合 A 与 B 质量比为 7: 12 的化合物是()A、 AB2B、 A 2B3 C 、AB D、A2B58.某有机物焚烧后生成 CO2和 H2O两种物质,则此有机物的构成是()A、只含有碳、氢元素B、必定含有碳、氢元素,可能含有氧元素C、必定含有碳、氢、氧元素D、必定含有碳、氧元素9.化学方程式 aC2H2+bO2 = cH2O+dCO2则 a、b、c、d 等数之和为()A、15 B、14 C、13D、 1010.在反响2A+B=3C+D中,A和 B 的相对分子质量之比为5﹕1,已知 20 克 A 与必定质量的 B 恰巧反响,生成 5 克 D,则在此反响中 B 和 C的质量比为( )A、4﹕19B、3﹕5C、1﹕3D、2﹕17二、此题包含 3 个小题,共 27 分11(10 分).用元素符号或化学式表示( 1)氧化铁(2)2个铁离子( 3)碳酸根的化合价为 -2 价(4)4个硫酸根离子( 5)硝酸铵12( 10 分)梅县东山工业区某化工厂以食盐和水为主要原料生产多种化工产品。
人教版化学九年级上第五单元《化学方程式》测试题(含答案)

第五单元《化学方程式》测试题一、单选题1.工业上利用下列反应制取金属Hg:4HgS+4CaO=4Hg+3X+CaSO4。
该反应中X的化学式为()A.CaS B.SO2C.CaSO3D.CaSO32.某化合物完全燃烧,需要4.8g氧气,同时只生成4.4g二氧化碳和2.7g水,则该化合物中()A.只含有碳、氢两种元素B.含有碳、氢、氧三种元素C.一定含有碳、氢两种元素,可能含有氧元素D.无法确定3.下列结论不正确的是A.化学反应中一定有能量的变化 B.化学反应中一定会有新物质生成C.化学反应中元素种类一定不发生变化 D.化学反应中一定会伴随着一些现象4.某发电厂烟气处理的新工艺:CH4+2NO2=N2+2X+CO2,则X的化学式为A.H2B.H2O C.NH3D.CO5.拒报道,美国宇航局的专家发明了“月球制氧机”,这种“月球制氧机”利用聚焦太阳能产生的高温使月球土壤发生化学反应制取氧气,据此可推测月球土壤中一定含有A.氧气B.水C.氧元素D.空气6.实验室的氯酸钾中通常含有杂质。
现称取6.20g氯酸钾样品与一定量的二氧化锰混合,完全反应后冷却,将剩余固体加入17.02g的水中,得到不饱和溶液,测得溶液中溶质的质量分数为14.9%.则该样品中杂质的质量为(不考虑实验中药品的损耗,杂质不参与反应,也不溶于水)()A.3.22g B.2.98g C.1.92g D.1.30g7.乙硫醇(化学式为C2H6S)易挥发、有蒜臭味,人对该气体及其敏感,下列有关乙硫醇的说法不正确的是()A.乙硫醇的摩尔质量为62g/molB.乙硫醇由2 个C 原子、6 个H 原子与1 个S 原子构成C.硫元素的质量分数是321221632⨯+⨯+×100%D.在管道煤气中添加微量乙硫醇,可以及时发现煤气泄漏8.乙醇不完全燃烧时产生CO、CO2和H2O。
依据下表数据分析得出的结论中,不正确的是:A .表中的a 值为1.4B .在化学反应前后碳元素质量一定相等C .参加反应的乙醇和氧气的质量比为3、4D .生成的CO 和CO 2分子个数比为1、3 9.下列关于22S+O SO 点燃的理解错误的是A .参加反应的硫与氧气的质量比是2:1B .反应前后硫原子、氧原子的个数均不变C .表示硫与氧气在点燃条件下反应生成二氧化硫D .参加反应的氧气与生成的二氧化硫的分子个数比为1:1 10.如图是某化学反应的微观示意图,下列说法正确的是( )A .该反应属于化合反应B .该反应共涉及四种原子C .该反应前后,原子的种类没有发生变化D .该反应前后所有元素的化合价都没有发生变化 11.下列化学方程式书写完全正确的是( ) A .双氧水中加入少量MnO 2:H 2O 22MnO H 2↑+O 2↑B .高炉炼铁:3CO+Fe 2O 3高温2Fe+3CO 2↑C .硫酸的制备:Na 2SO 4+2HCl =2NaCl+H 2SO 4D .工业法制烧碱:Na 2CO 3+Ca (OH )2=2NaOH+CaCO 3↓ 12.对下列日常生活中的现象解释不合理...的是B纸在空气中燃烧化为灰烬,质量变小此现象不符合质量守恒定律C湿衣服在阳光下比阴凉处干得快温度升高,分子运动速度加快D石油气加压可贮存在钢瓶中分子间有间隔,加压使得间隔缩小A.A B.B C.C D.D13.已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:则下列说法正确的是()A.图示中共有4种分子B.该反应属于化合反应C.图示中的反应物都是单质D.该图示不符合质量守恒定律14.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
周周练(第五单元)
一、我会选(每小题4分,共40分)
1.下列化学方程式书写正确的是( ) A .S +O 2===SO 2 B .Cu +O 2=====△
CuO C .2Al +O 2=====点燃2AlO D .4P +5O 2=====点燃2P 2O 5
2.化学反应前后,一定没有变化的是( ) A .物质的种类 B .物质的状态
C .分子的种类和数目
D .原子的种类和数目
3.(怀化中考)铜与稀硝酸反应可产生一种气体X ,方程式为3Cu +8HNO 3===3Cu(NO 3)2+2X ↑+4H 2O ,则X 的化学式是( )
A .H 2O
B .NO
C .Cu
D .N 2
4.2015年1月29日,里约2016奥运会火炬接力标志公布,圣火传递路线将覆盖巴西全境。
此次火炬使用的燃料是丙烷(C 3H 8),其燃烧的化学方程式为C 3H 8+5O 2=====点燃
x CO 2+y H 2O ,其中x ,y 分别为( )
A .1 3
B .1 5
C .3 8
D .3 4
5.你认为下列观点不正确的是( )
A .质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关
B .化学实验是人类认识物质、改造和应用物质、推动化学科学发展的主要手段
C .化学的主要特点是在原子、分子水平上认识物质,化学可以识别、改变和创造分子
D .通过化学变化,人们改造物质世界并实现物质与能量的相互转化
6.在反应A +3B===2C +3D 中,已知A 和B 的相对分子质量之比为5∶6,2.5gA 与一定质量的B 恰好完全反应,生成3.5gD ,则反应中B 和C 的质量比为( )
A .2∶1
B .9∶8
C .3∶2
D .4∶7
7.(襄阳中考)以下是氯气与水反应的微观示意图,从示意图中获取的信息不正确的是( )
A .反应前后分子种类发生改变
B .反应前后原子的数目不发生改变
C .氯元素的化合价在反应前后没有改变
D .每个氯气分子是由两个氯原子构成的
8.(河池中考)甲、乙、丙、丁四种物质,它们在密闭容器中反应前后质量的变化关系如下表所示。
则下列说法错误的是( )
物质名称 甲 乙 丙 丁 反应前质量/g 40 10 10 0 反应后质量/g
6
m
28
16
A.甲是化合物
B .乙可能是这个反应的催化剂
C .m =38
D .此反应基本类型为分解反应
9.(成都中考)我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。
其成果
在最近的美国《科学》杂志发表。
该转化的微观示意图如下:
有关转化的说法错误的是()
A.催化剂改变了反应速率
B.反应前后原子的种类发生了变化
C.生成物之一为C2H4
D.反应物与生成物均由分子构成
10.(黔东南中考)如图是反映某个化学反应里各物质质量与时间的变化关系,下列对此变化的描述中,正确的是()
A.充分反应后,乙+丙=甲的质量
B.物质甲的相对分子质量大于乙
C.此化学反应中,不遵循质量守恒定律
D.此化学反应是分解反应
二、我会填(共33分)
11.(9分)某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝。
他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化。
请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应铝粉的质量______(填“大”“小”或“不变”)。
(2)你认为这两个反应是否遵循质量守恒定律?______(填“是”或“否”)。
(3)请写出氧化汞受热分解的化学方程式:______________________。
12.(12分)(本溪中考)如图表示的是某纯净物在氧气中燃烧的微观示意图,请根据图示回答问题:
(1)甲的化学式为________;
(2)上述微观反应图示中,不发生改变的粒子是______(填“分子”“原子”或“离子”);
(3)生成物中丙和丁两种物质的分子个数比为______。
13.(12分)某同学把3 g碳放在给定的氧气中充分燃烧,实验数据如下:
第一次第二次第三次
给定氧气的质量 6 g 13 g 8 g
生成二氧化碳的质量8.25 g 11 g 11 g
(1)通过以上数据说明,这三次实验中第______次恰好完全反应;
(2)第______次实验中碳有剩余,剩余______g;
(3)第______次实验中氧气有剩余,剩余______g;
(4)在三次化学反应过程中,是否有不符合质量守恒定律的?______。
三、我会探究(18分)
14.在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。
他们使用的实验装置和选用药品如图所示,现分别以A、B、C、D表示如下:
A 、
B 、
C 、
D 四个实验分别由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
(1)A 实验:锥形瓶底放层细沙的原因是:__________________________________________;小气球的作用是:__________;白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡。
结论是:质量不守恒。
待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。
结论是:质量守恒。
你认为结论正确的是________(填“前一种”或“后一种”),而导致另一种结论错误的原因是:
__________________________________________________________________。
(2)丙组同学认为C 实验证明了质量守恒定律。
请你从原子的角度说明为什么?
____________________________________________________________________________________________________________。
乙、丁两组同学得到的错误结论是“实验B 、D 均说明质量不守恒”。
老师引导同学们分析了B 、D 两个实验反应前后天平不平衡的原因。
你认为B 实验天平不平衡的原因是:
__________________________________________________; D 实验天平不平衡的原因是:
________________________________________________________________________________
(3)如果只是将A 装置中的药品改为少量的二氧化锰和过氧化氢,反应前后天平仍不平衡,原因是:______________________________________;结论是:参加反应的过氧化氢的质量一定______(填“等于”或“不等于”)生成的水和氧气的质量总和。
四、我会计算(9分)
15.(宿迁中考)在煤中加入适量的生石灰制成供居民采暖用的“环保煤”,以减少二氧化硫的排放,减弱二氧化硫对空气的污染。
“环保煤”燃烧时生石灰吸收二氧化硫的化学方程式为:2CaO +m SO 2+O 2===n CaSO 4;请回答下列问题:
(1)m 值是______;
(2)若煤厂一次共加入含氧化钙56 t 的生石灰,则理论上最大可吸收二氧化硫多少吨?
参考答案
1.D 2.D 3.B 4.D 5.A 6.B 7.C 8.C 9.B 10.D 11.(1)大 (2)是 (3)2HgO=====△
2Hg +O 2↑ 12.(1)C 2H 6O (2)原子 (3)3∶2 13.(1)三 (2)一 0.75 (3)二 5 (4)没有 14.(1)防止白磷燃烧产生的热量使锥形瓶底部炸裂 缓冲作用 后一种 白磷刚引燃时,装置内气体受热膨胀将气球胀大,装置受到的浮力增大 (2)化学反应的过程是反应物的原子重新组合的过程,反应前后原子的种类、数目、质量不变,因此生成物的质量也不会改变 因为反应后生成的CO 2逸出,使得天平不平衡 因为镁条燃烧消耗空气中的氧气且生成的氧化镁部分跑到空气中去,使得天平不平衡。
(3)过氧化氢分解产生的氧气将使气球胀大 等于 15.(1)2 (2)解:设理论上最大可吸收二氧化硫的质量为x 。
2CaO +2SO 2+O 2===2CaSO 4
112 128 56 t x
112 128=56 t
x x=64 t答:理论上最大可吸收二氧化硫质量为64 t。
