信号转导2012
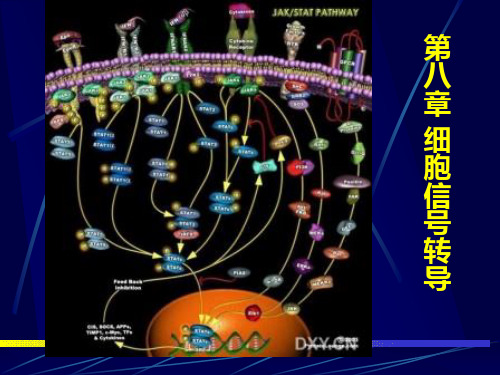
JAK_STAT信号转导在脑卒中的研究进展

·综述·JAK-STAT信号转导在脑卒中的研究进展肖霖,武衡南华大学第一附属医院神经内科,湖南衡阳421001关键词:脑卒中;JAK—STAT;信号转导;损伤;脑缺血中图分类号:R743.3文献标志码:A文章编号:1672-4208(2012)02-0058-02Janus激酶-信号转导与转录激活因子(JAK-STAT)途径,参与细胞增殖、分化、凋亡、免疫调节等多个生理病理过程,是细胞因子信号转导的一个重要的途径[1]。
以往JAK-STAT途径的研究主要集中于肿瘤、肝脏、造血系统、心血管系统。
近年来的研究表明,JAK蛋白和STAT蛋白在中枢神经系统的发育与病理过程中均有表达,如脑缺血后,STAT3和STAT1表达上调,活性显著升高,而敲除STAT1基因,则对脑卒中具有一定的神经保护作用,表明JAK-STAT信号转导途径可能与脑卒中后神经再生、胶质细胞活化等有关[2-3]。
1JAK-STAT信号转导途径有研究表明,细胞因子及JAK-STAT途径中的JAK1、JAK2、STAT1、STAT3、STAT5参与脑卒中后脑缺血的病理过程,Nakanishi M等研究表明激活后的JAK-STAT途径促进了星形胶质细胞的分化过程[4],并在星形胶质细胞间的信号通讯中起着重要的调控作用[5]。
Janus激酶(JAK)是胞质内的一类非受体型酪氨酸蛋白激酶,可溶性强,分子量在120 130之间,其mRNA的转录长度范围在5.0kb左右。
迄今为止,已发现该家族的4种成员即JAKl、JAK2、JAK3、TYK2[6]。
JAK蛋白酪氨酸激酶在细胞因子信号传递过程中发挥着重要作用,它通过与其相连的细胞因子及生长因子的受体酪氨酸磷酸化反应产生催化作用,并且形成多种含有特定SH2区信号能发生分子磷酸化反应的蛋白-受体复合物的结合位点,自身而被迅速激活,就在细胞因子的受体在相应的配基下结合而被活化后,再将另外的一种被称为是“信号转导子和转录激活子”的信号蛋白分子激活,诱导目的基因表达,发生一系列蛋白的级联反应。
细胞生物学第4版第9章细胞信号转导

第一节 细胞信号转导概述
• 细胞通讯步骤与功能
Figure 15-8 Molecular Biology of the Cell (© Garland Science 2008)
一、细胞通讯
• 化学信号通讯 • 接触依赖性通讯(contact-dependent signaling) P157 • 间隙连接(gap junction)胞间连丝(plasmodesma)
– 受体特异性识别并结合胞外信号分子 , 形成受体-配体复合物,导致受体 激活
– 受体构象改变,导致信号初级跨膜转 导,靶细胞内产生第二信使或活化的 信号蛋白
– 胞内第二信使或胞内信号蛋白复合物 装配,起始胞内信号放大的级联反应
– 细胞应答反应 – 受体脱敏或受体下调,终止或降低细
胞反应
蛋白质模式结合域(modular binding domain)
一、细胞内核受体及其对基因表达的调节
• 3 个功能域
– C 端激素结合结构域 – 中部DNA 或Hsp90 结合结构域 – N 端转录激活结构域
• 细胞内受体的本质是依赖激素激活 的转录因子。
• 信号分子的作用是将抑制性蛋白从 细胞内受体上解离,使受体上的 DNA结合位点暴露而激活。
• 激素-核受体复合物与激素反应元 件(HRE)结 合,调节基因转录。
一细胞,常见于癌变细胞。 化学突触(chemical synapse):神经递质由突触前膜释
放,经突触间隙扩散到突触后膜,作用于特定的靶细胞。
二、几个基本概念
• 信号分子 • 受体 • 第二信使 • 分子开关
1. 化学信号分子
• 根据其溶解性分类: • 亲水性信号分子——神经递质、生长因子、细胞因子
精品医学课件-细胞信号转导

52
53
多种途径逐 级磷酸化
54
2. JAK-STAT途径
• 配体:干扰素、白介素等细胞因子 • 受体:酪氨酸蛋白激酶型受体 • 效应蛋白及其作用:胞质PTK(非受体型的PTK),如JAK
(Janus kinase)。活化的JAK激活其底物信号转导子和转 录激活子(signal transducer and activator of transcription, STAT),STAT激活一系列后续蛋白质,调节基因表达。
• 两种形式:载体介导和通道介导
10
(二)主动转运(active transport)
1. 原发性主动转运
• ATP直接供能 • Na+-K+泵,ATP酶活性
11
2. 继发性主动转运或协同转运
• ATP间接供能 • Na+依赖式转运体蛋白
12
(三)胞吐与胞吞式转运
• 胞吐:通过一个耗能过程将细胞内物质分泌到细 胞外的过程。(固有性胞吐、调节性胞吐)
虽然这些微小的蛋白质看不见摸不着, 但是它们与我们的日常生活息息相关, 如果没有G蛋白偶联受体,人类根本无 法生存下去。如果没有视紫质,我们将 看不见光线;如果没有嗅觉受体,我们 将闻不见气味;如果没有β-肾上腺素受 体,我们将无法调节血糖;如果没有毒 蕈碱受体,乙酰胆碱将无法将心跳速度 限定在合理范围内;如果没有5-羟色胺 受体,我们甚至无法感受幸福……
15
(三)化学通讯
• 间接通讯方式:信 号分子→靶细胞
• 分3类:
1. 内分泌(endocrine) --血液循环 2. 旁分泌(paracrine) --扩散作用 3. 自分泌(autocrine) --同类或同一细胞 (常见于癌变细胞)
雌激素受体信号转导途径和功能_吴艳

当前雌激素替代疗法虽然在女性一级和二级心血管疾病防治中尚存在争议因此应用植物雌激素及选择性雌激素受体调节剂作为雌激素替代疗法的选择成为研究的热点之一随着基础及临床研究的更加系统与深入将有助于认识雌激素及其受体在心血管系统中的作用机制这些研究将帮助人们探讨更年期疾病治疗的最佳方法
·242·
安 徽 医 药 Anhui Medical and Pharmaceutical Journal 2012 Feb; 16( 2)
参考文献:
[1] Orshal JM,Khalil RA. Gender. sex hormones,and vascular tone[J]. Am J Physiol Regul Integr Comp Physiol,2004,286( 2) : 233 - 49.
[2] Dubey RK,Imthurn B,Barton M,et al. Vascular consequences of menopause and hormone therapy: importance of timing of treatment and type of estrogen[J]. Cardiovasc Res,2005( 66) : 295 - 306.
细胞生物学第八章细胞信号转导
内容提示
第一节 概述 第二节 细胞内受体介导的信号转导 第三节 G蛋白耦连联受体介导的信号转
导 第四节 酶连受体介导的信号转导 第五节 信号的整合与控制
第一节 概述
一、细胞通讯(cell communication)
1、概念:一个细胞发出的信息通过介质
美国科学家罗伯特· 莱夫科维茨(Robert J. Lefkowitz)和布莱恩· 克比尔卡(Brian K. Kobilka )因“G蛋白偶联受体研究”获得2012年诺贝尔化 学奖。
Robert J. Lefkowitz
Brian K.有:
肽类激素、局部介质、神经递质、氨基 酸或脂肪酸的衍生物、气味分子、光量 子、声等。50%的药物也是通过与G蛋白 偶联的受体结合发挥作用。
快速应答过程
激素
G蛋白偶联的受体 腺甘酸环化酶 cAMP依赖的蛋白激酶A cAMP 底物蛋白磷酸化
G蛋白
生物学效应
肾上腺素使血糖升高的信号通路
肾上腺素
G蛋白偶联的受体 cAMP 升高 磷酸化酶激酶被 磷酸化 糖原分解为 葡萄糖
G蛋白
激活腺甘酸环 化酶 激活cAMP依赖的蛋白激 酶A
糖原磷酸化酶 被磷酸化
第二节 细胞内受体介导的信号转导
亲脂性信号分子通过扩散进入细胞,与胞内受体
结合(前列腺素除外)。通常表现为影响细胞分 化等长期的生物学效应。 一、细胞内核受体及其对基因表达的调节 1、细胞内受体超家族的本质是依赖激素激活的 基因调控蛋白。有三个结构域。 C-端激素结合位点 三个结构域 中部的DNA或Hsp90结合位点: 富含Cys、锌指结构 N-端转录激活结构域
receptor)
(三)酶耦联的受体(enzyme-linked
在保卫细胞信号转导中MAPK级联途径

浅谈在保卫细胞信号转导中MAPK级联途径摘要:叶片表面的气孔是由保卫细胞构成的特殊结构,是气体出入植物体的主要通道。
气孔可以通过保卫细胞控制植物与外界大气的气体交换,影响光合作用和蒸腾过程,对环境和内源信号进行感知从而对胁迫环境做出响应,以此减轻胁迫程度并提高植物的抗性。
而促分裂原活化蛋白激酶(MAPK)级联在这一过程中至关重要。
促分裂原活化蛋白激酶(MAPKs)形成具有蛋白激酶和MAPK激酶激酶的三层激酶级联,其信号转导到靶蛋白是以三级激酶级联的方式进行的。
在所有真核生物中,MAPK级联基因高度保守,并且它们在各生长发育及生理过程中发挥关键作用。
在生物和非生物胁迫反应过程中,MAPK级联功能通过将受体接收的细胞外信号与胞质事件和基因表达相连接而发挥作用。
本文以MAPK级联途径在保卫细胞信号转导为侧重点,将近年来MAPK级联的特异性的研究情况加以综述并分析亟待解决的问题,对以后的研究方向提出展望,以期为进一步的深入研究提供理论参考。
关键词MAPK级联;气孔;气孔运动;保卫细胞Brief Discussion on MAPK Cascades in Guard Cell Signal Transduction Abstract: Guard cells form stomata on the epidermis and continuously respond to endogenous and environmental stimuli to fine-tune the gas exchange and transpirational water loss, processes which involve mitogen-activated protein kinase (MAPK) cascades. MAPKsform three-tiered kinase cascades with MAPK kinases and MAPK kinase kinases, bywhich signals are transduced to the target proteins. MAPK cascade genes are highlyconserved in all eukaryotes, and they play crucial roles in myriad developmental andphysiological processes. MAPK cascades function during biotic and abiotic stress responses by linking extracellular signals received by receptors to cytosolic events and gene expression. In this review, we highlight recent findings and insights into M A P K- mediated guard cell signaling, including the specificity of MAPK cascades.The future research directions were also discussed,which could offer scientific references for its rational and efficientdevelopment.Key words: MAPK cascade, stomatal pore, stomatal movement, guard cell在光合作用过程中,通过由表皮中的保卫细胞围成的气孔,植物和大气之间进行气体交换和水分蒸腾[1]。
生物化学教学课件:信号转导通路

信号转导要素:信号或配体, 受体, 信号放大
(产生第二信使), 应答和反馈调节
22
PARTⅠ
1 Basic characteristics of signal transduction 2 Four general types of signal transducers
PARTⅡ
1 Regulatory mechanisms 2 Some diseases caused by defects in the
由于衰老和疾病,多种细胞或器官需要修复;
来源? 伦理 (胚胎干细胞)?
干细胞分化: 根据组织局部 微环境的差异
而分化成 相应的细胞
Whether the specialisation of cells is reversible
in human?
2011年,Science 评出 本世纪前十年十大科学成就:
“发现成熟细胞可以重新编程而获得多能性”
iPS, induced pluripotent stem cell
诱导多能干细胞
中枢神经
上皮
软骨
脂肪
引入关键基因 体细胞重新编程
肌肉 畸胎瘤实验
iMice
iPS-derived mice
iPS在疾病治疗中的应用
优势 • 诱导简单,容易操作 • 可从自体细胞中获得,免
Time to flee!
脑:神经信号警告 眼:瞳孔
身体各部位,释放 放大,视
心脏:心率加速
激素激活肾上腺 野变窄来自肺:气管扩张,呼吸频率加快
肌肉:血量增加,
肌肉收缩
髓质 皮质醇
皮质
肾上腺素
去甲肾上腺素
肝脏:糖原分解,
糖被释放到血液
抑郁症与细胞信号转导进展

2012年12月第9卷第36期·综述·CHINA MEDICAL HERALD 中国医药导报抑郁症是严重危害人类健康的情感障碍疾病,以往人们对抑郁症发病机制的研究主要集中在神经生化方面,近年来,人们逐渐认识到抑郁患者在神经细胞信号转导分子水平也存在异常。
信号转导途径具有级联放大作用,一个原始的化学信号,通过信号传递过程的级联反应,可以在下游引起成百上千个酶蛋白的活化,产生生物学效应。
本文综述了信号转导机制在抑郁症中的研究进展,为阐明抑郁症的发病机制和研制新型抗抑郁药物提供参考。
1G 蛋白偶联的信号转导通路与抑郁症1.1G 蛋白与抑郁症G 蛋白在信息转导通路中起广泛和重要的整合、调节及放大作用,早期抑郁症信号通路的研究集中在G 蛋白上。
2002年国内学者研究发现慢性应激抑郁模型大鼠海马的Gi 蛋白表达量明显高于正常大鼠[1]。
抑郁患者Gq α下降,并常伴随神经元去分化过程,抗抑郁药能上调Gq α从而发挥抗抑郁作用。
研究表明,抑郁模型大鼠前额皮质、海马CA3区G αi 表达增高,西酞普兰抗抑郁作用靶点之一可能是调整前额皮质、海马CA3区的G αi 的表达[2]。
1.2cAMP-PKA 通路与抑郁症对抑郁症信号通路研究较多的是cAMP-PKA 通路。
研究提示抑郁症存在cAMP 系统活性下调,抗抑郁治疗可使cAMP 通路上调。
抑郁患者存在大脑去甲肾上腺素能β受体耦联的腺苷酸环化酶(AC )敏感性降低及PKA 通路的异常。
国外有资料报道,抑郁症自杀死亡者脑前额叶AC 的活性明显下降,自杀行为及抑郁性疾病可能与AC 活性改变有关。
邓沁涛等[3]建立小鼠重复应激抑郁模型,检测小鼠海马内cAMP 含量、PKA 活性及海马磷酸化反应元件结合蛋白(P-CREB )水平,发现cAMP-PKA-CREB 是咯利普兰发挥抗抑郁作用信号转导途径之一。
魏浩洁等[4]的研究显示黄精皂苷对慢性应激抑郁大鼠行为学有改善作用,可能是通过调节5-羟色胺1A 受体(5-HT 1A R )及其介导的5-HT 1A R/cAMP/PKA 通路发挥抗抑郁作用。
