期末重点复习初三化学--燃料
九年级化学上册第7单元燃料及其利用复习提纲

干粉灭火器的反应原理: 2NaHCO3
Na2CO3+H2O+CO2↑
三、 爆 炸
二氧化碳灭火器内盛装的是液态二氧化碳,使用时不会留下任何痕迹。
定义:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而 引起爆炸。
爆炸还包括物理爆炸,它们是物理变化。
除了可燃性气体能发生爆炸外,可燃性粉尘如面粉、煤粉等也能发生爆炸。
加入的物质
现象 水
SO2 加水
植物叶子或果皮
无明显变化
植物叶子或果皮变黄
镁条或锌粒
无明显变化
镁条或锌粒表面有气泡产生
大理石或石灰石
无明显变化
大理石或石灰石表面有气泡产生,并且变得粗糙
【实验结论】酸雨呈酸性,能与多种物质发生反应。
鼓气
粉尘爆炸实验
【实验操作】取一空金属罐和小塑料瓶,剪去金属罐和小塑料瓶的上部,并在金属罐和小塑料瓶的底
侧各打一个比橡皮管 外径略小的小孔。像右图那样连接好装置,在小塑料瓶中放入干燥的面粉,点燃
蜡烛,用塑料盖盖住罐。从橡皮管一端快速鼓入大量的空气,使面粉充满罐,观察现象并分析原因。 【实验现象】“砰”地一声响,伴随一团火光产生;放热;塑料盖被掀起。 【实验分析】面粉被吹起后与空气充分接触,又被蜡烛点燃。在有限的空间内发生急剧燃烧并放出大 量热,产生的气浪将塑料盖掀起,说明可燃性的粉尘在有限的空间内急剧燃烧能发生爆炸。 【注意事项】 ① 面粉应该是干燥的; ② 气囊的作用:使面粉与空气充分混合。 ③ 鼓气球与金属罐之间的连接管可稍长一些,人距离该装置远一些,以防危险。 油库、面粉加工厂、纺织厂和煤矿的矿井内等地方必须做的安全措施:通风、严禁烟火。
第 7 单元 燃料及其利用复习提纲
九年级化学燃料及其利用知识点总结

化学燃料及其利用是九年级化学内容中的一个重要知识点,下面是九年级化学燃料及其利用的知识点总结,包括什么是燃料、常见的燃料种类、燃烧反应及其特点、燃料的效能、燃料和环境的关系以及节约能源和绿色能源等方面。
一、什么是燃料燃料是指直接或间接用于产生热能或动力的物质。
燃料主要为化学物质,它们能够在适当的条件下与氧气反应产生热能。
常见的燃料有化石燃料、木炭、天然气等。
二、常见的燃料种类2.木炭:木炭是由木材等植物有机物经过热分解得到的固体燃料。
木炭燃烧时释放的热量高,但燃烧产物中会有很多固体颗粒物。
3.液体燃料:液体燃料主要指石油和汽油,它们被广泛用于交通运输和工业生产等领域,但燃烧产生的尾气对环境有污染。
4.天然气:天然气是一种主要由甲烷组成的气态燃料,它燃烧时产生的污染物相对较少,因此被认为是较为清洁的燃料。
三、燃烧反应及其特点燃烧是指物质与氧气发生化学反应,放出焓变为负的化学反应。
燃烧反应一般包括燃料和氧气的反应,产物主要有二氧化碳、水和能量(热能和光能)。
燃烧反应具有自燃性、连续性、放热性和产物不稳定性等特点。
四、燃料的效能燃料的效能指用于产生能量的燃料利用效果的好坏。
常用的衡量燃料效能的指标包括燃烧的热效率和排放的污染物。
炉具和发动机等的效能主要取决于其热损失的多少,减少热损失可以提高燃料的效能。
五、燃料和环境的关系燃料的燃烧过程中会产生大量的污染物,包括二氧化碳、二氧化硫、氮氧化物和颗粒物等。
这些污染物对环境和人类健康都有一定的危害。
因此,燃料和环境的关系十分密切,我们应该选择清洁和高效的燃料,减少污染物的排放。
六、节约能源和绿色能源近年来,随着全球能源危机的日益突出和环境保护意识的提高,节约能源和绿色能源成为了研究的热点。
节约能源主要包括提高能源利用效率、合理使用能源和开发新能源等。
绿色能源是指对环境友好、可持续利用的能源,如太阳能、风能和生物能等。
总的来说,九年级化学燃料及其利用的知识点包括了什么是燃料、常见的燃料种类、燃烧反应及其特点、燃料的效能、燃料和环境的关系以及节约能源和绿色能源等方面。
人教版九年级上册化学第七单元《燃料及其利用》知识点汇总
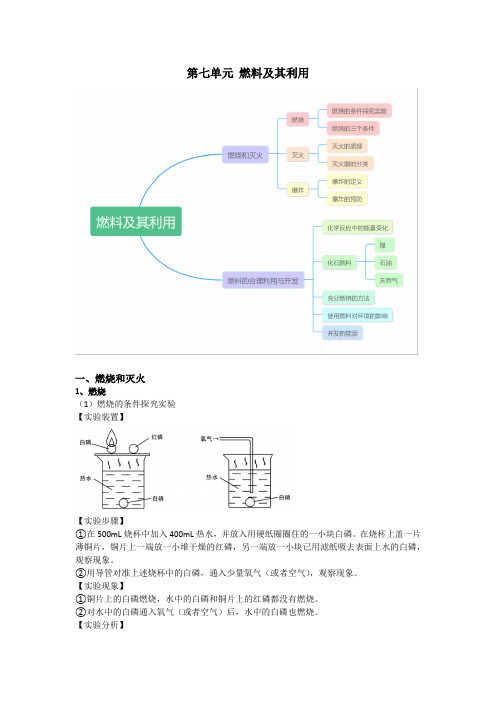
第七单元燃料及其利用一、燃烧和灭火1、燃烧(1)燃烧的条件探究实验【实验装置】【实验步骤】①在500mL烧杯中加入400mL热水,并放入用硬纸圈圈住的一小块白磷。
在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷,观察现象。
②用导管对准上述烧杯中的白磷,通入少量氧气(或者空气),观察现象。
【实验现象】①铜片上的白磷燃烧,水中的白磷和铜片上的红磷都没有燃烧。
②对水中的白磷通入氧气(或者空气)后,水中的白磷也燃烧。
【实验分析】①对比铜片上的白磷和红磷,说明燃烧需要达到一定的温度。
②对比铜片上的白磷和水中的白磷,说明燃烧需要与氧气(或者空气)接触。
③观察步骤二的现象,说明燃烧需要氧气(或者空气)。
【实验结论】燃烧需要可燃物、达到一定的温度、氧气(或者空气)。
(2)燃烧的三个条件通常情况下,可燃物与氧气发生的一种发光、发热的剧烈的氧化反应叫做燃烧。
燃烧需要三个条件:①可燃物;②氧气(或者空气);【不是所有的燃烧都需要氧气,有助燃物就行】③达到燃烧所需的最低温度(着火点)。
2、灭火(1)灭火的原理①清除或使可燃物与其他物品隔离;②隔绝氧气(或者空气);③使温度降到着火点以下。
3、爆炸(1)爆炸的定义可燃物在有限空间内急剧地燃烧,在短时间内聚积大量的热,使气体的体积迅速膨胀。
(2)爆炸的预防在油库、面粉厂、加油站等地区应该注意通风,严禁烟火。
二、燃料的合理利用与开发1、化学反应中的能量变化(1)有些化学反应会放出热量,如:(2)有些化学反应会吸收热量,如:2、化石燃料(1)煤①煤的组成煤是复杂的混合物,主要含有碳元素,此外,还含有氢元素和少量的氮、硫、氧等元素和无机矿物质。
②煤的综合利用将煤隔绝空气加强热,可以使煤分解出如焦炭、煤焦油、煤气等有用物质。
其中煤气的主要成分是氢气、甲烷、一氧化碳和其他气体。
(2)石油①石油的组成石油中主要含有碳和氢两种元素。
②石油的综合利用利用石油中各成分的沸点不同,可以分离得到不同的产品,如沥青、石蜡、润滑油、柴油、煤油、航空煤油、汽油、溶剂油等。
初三期末化学知识点总结:燃料及应用

初三期末化学知识点总结:燃料及应用初三期末化学知识点总结:燃料及应用
1.燃烧和灭火
(1)燃烧的条件:(缺一不可)
a.可燃物
b.氧气(或空气)
c.温度达到着火点
(2)灭火的原理:(只要消除燃烧条件的任意一个即可)
a.消除可燃物
b.隔绝氧气(或空气)
c.降温到着火点以下
(3)影响燃烧现象的因素:可燃物的性质、氧气的浓度、与氧气的接触面积
使燃料充分燃烧的两个条件:
a.要有足够多的空气
b.燃料与空气有足够大的接触面积。
(4)化学反应中的能量变化 CaO+H2O=Ca(OH)2 放热反应
2、化石燃料
(1)三大化石燃料:煤、石油、天然气(主要成分甲烷)
甲烷的化学式: CH4 (最简单的有机物,相对分子质量最小的有机物)
物理性质:无色,无味的气体,密度比空气小,极难溶于水。
化学性质: 可燃性
CH4+2O2点燃CO2+2H2O (蓝色火焰)
(2)乙醇汽油-汽油中加入适量的乙醇
乙醇 (俗称:酒精,化学式:C2H5OH)
化学性质: 可燃性
C2H5OH+ 3O2点燃2CO2+3H2O
优点:
a.减少环境污染
b.节约化石燃料
c.促进农业发展
(3)新能源:氢能源(最清洁的能源)、太阳能、核能、风能、地热能、潮汐能。
第七单元 燃料及其运用 期末复习课件 人教版九年级化学上册

燃烧条件的探究 实验装置
实验现象
实验分析
__小__木__块_燃烧, __小__石__块__不燃烧
小石块不属于可燃物, 小木块属于可燃物
铜片上的白磷_燃__烧___;铜片上的物质都与氧气接触,
铜片上的红磷_不__燃__烧_
但温度达到白磷的着火点, 未达到红磷的着火点
铜片上的白磷__燃_烧___, 热水中的白磷未与 热水中的白磷_不__燃__烧_ __空_气__(_或__氧_气__)__接触
2. (2017北部湾经济区5题2分)下列有关燃烧、灭火的分析,
错误的是( C )A. 火上浇油——增加可燃物B. 釜底抽薪—
—移走可燃物C. 吹灭蜡烛——降低着火点D. 油锅着火用锅 盖盖灭——隔绝空气
命题点4 能源与资源
5. (2020桂林14题2分)下列有关石油的说法,错误的是( C )A. 属于混合
2. 灭火
(1)原理:破坏_燃__烧___的条件。
(2)方法 ①清除__可__燃_物___(或使_可_燃__物___与其他物 品隔离) ②隔绝_空__气__(或__氧__气__) __
三者之中满足 一个 条件即可
③使温度降到__可_燃__物__的__着__火_点___以下
【特别提醒】着火点是物质的固有属 性,一般不随外界条件的 改变而改变。灭火时可采用降低温度至可燃物的着火点以下的方 法,而不是降低可燃物的着火点。
物
B. 属于化石燃料
C. 只含碳元素
D. 属于不可再生能源
6. (2019北部湾经济区5题2分)2019年环境日的主题是“美丽中国,我
是行动者”。下列行为与主题相符合的是( B )A. 野外焚烧垃圾B. 提
倡植树造林C. 随意丢弃电池D. 多开私家车出行
化学初三教材梳理:燃料及其利用

化学初三教材梳理:燃料及其利用通常的燃烧是指可燃物跟氧气发生的一种发光、发热的剧烈的氧化反应。
接下来小编为大家整理了化学学习相关内容,一起来看看吧!化学初三教材梳理:燃料及其利用燃烧及燃烧的条件⒈通常的燃烧是指可燃物跟氧气发生的一种发光、发热的剧烈的氧化反应。
燃烧需要同时满足三个条件:⑴可燃物;⑵与氧气(或空气)接触;⑶温度达到可燃物的着火点。
⒉着火点:达到燃烧所需的最低温度,着火点是物质本身的固有属性,因此不能说用降低着火点的方法来灭火,而只能是降温到着火点以下。
探究点1:燃烧的条件:⑴可燃物;⑵与氧气(或空气);⑶温度。
探究点2:燃烧的剧烈程度:⑴氧气的浓度;⑵接触面积(团块<粉末<气体)灭火的原理和方法⒈灭火的原理:(破坏燃烧的条件,三者破坏其一就可灭火,也可同时都破坏)⑴清除可燃物或使可燃物跟其他物品隔离;⑵隔绝氧气(或空气)⑶使温度降低到着火点以下⒉几种常用灭火器的适用范围⑴泡沫灭火器:用来扑灭木材、棉花等燃烧而引起的失火。
⑵干粉灭火器:除用来扑灭一般火灾外,还可用来扑灭油、气等燃烧引起的失火。
⑶液态二氧化碳灭火器:用来扑灭图书档案、贵重设备、精密仪器等处的失火。
易燃物和易爆物的安全知识⒈可燃物与氧气接触面积越大,燃烧越剧烈;燃烧空间越小,越危险。
⒉一切可燃性的气体(氢气、天然气、煤气等)或粉尘,在空气中达到极限遇到明火就易发生。
家用煤气一旦泄露,千万不要开动电器开关(如开灯、抽风、拨打电话、手机等),以免发生。
⒊认识一些与燃烧和有关的图标(参看课本P129)化石燃料(包括煤、石油、天然气)⒈煤:被称为“工业的粮食”。
⑴煤是一种混合物,主要含有碳元素。
⑵煤燃烧放出的热量,主要是碳元素和氧元素反应放出的。
⑶煤的综合利用:煤隔绝空气加强热——化学变化,可使煤分解成许多有用的物质,有:焦炭:冶金、炼铁等煤气:气体燃料。
它的有效成分有H2、CO等。
⒉石油:被称为“工业的血液”。
⑴石油是一种混合物,主要含有碳、氢元素。
初三化学笔记 第五章 燃料

第五章燃料第一节洁净的燃料——氢气1.物理性质无色、无味的气体,难溶于水。
密度比空气小,标准状况下,氢气的密度为0.090 g/L,是相同条件下密度最小的气体。
2.化学性质(1)可燃性:2H2+O22H2O现象:氢气燃烧时发出淡蓝色火焰,放出大量热,罩在火焰上方的烧杯内有水珠产生。
(2)还原性:H2+CuO Cu+H2O现象:黑色的粉末逐渐变成红色,并有水珠产生。
3.实验室制取氢气(1)反应原理Zn + H2SO4 = ZnSO4 + H2↑(2)反应物的选择选用锌粒和稀硫酸。
a 不使用盐酸,因为盐酸易挥发,使制得的氢气中混有HCl气体。
b 不用镁等活泼金属,因为反应速度太快,不用铁是因为反应速度太慢。
(3)发生装置和收集装置a 发生装置:固液常温型。
因为反应物中锌为固体,稀硫酸为液体,反应在常温下就能进行,所以发生装置同分解过氧化氢制取氧气的发生装置;b 收集装置:排水法收集气体的装置(原因:氢气难溶于水且不和水反应)或向下排空气法收集气体的装置(原因:氢气密度比空气小,且不和空气中成分反应)。
(4)注意事项a 用排空气法收集氢气时,不能验满!用排水法收集氢气时,如果集气瓶口出现气泡,说明氢气收集满了。
b 在点燃氢气前,一定要检验氢气的纯度。
c 可燃性气体的验纯方法:用排水法收集一试管可燃气体,用大拇指堵住试管口移近火焰点燃。
如果气体较纯,气体将会安静地燃烧,并发出“噗”声;如果气体不纯,会发出尖锐爆鸣声。
d 如果验纯时发现气体不纯,需要再收集再检验时,必须对试管进行处理(用拇指在试管口堵住一会或更换试管),以免发生爆炸。
4.氢气作为理想的高能燃料的优点氢气被认为是最清洁的燃料。
(1)以水为原料,来源广泛;(2)热值高,放热多;(3)生成物是水,无污染。
5.目前氢能源存在的问题制取成本高、贮存和运输困难。
第二节组成燃料的主要元素——碳1.“碳”和“炭”的区别“碳”指碳元素,不是具体指某种物质;而“炭”指具体的、由碳元素组成的单质。
九年级化学《燃烧与燃料》期末复习知识点

九年级化学《燃烧与燃料》期末复习知识点
九年级化学《燃烧与燃料》期末复习知识点
九年级《燃烧与燃料》期末复习知识点
(燃烧)
⑴要使物质燃烧的条件:
物质必须是可燃物、与氧气接触、要使温度达到可燃物的着火点。
⑵灭火的三种方法:
隔离可燃物与火源、
隔绝氧气、
降低温度到着火点以下。
⑶火灾中逃生的方法:
用湿毛巾捂住口鼻,伏下身体迅速逃离。
⑷氧气充分时可燃物发生完全燃烧,C、H元素转化成H2O和CO2 。
燃料利用充分。
氧气不充分时可燃物发生不完全燃烧,C、H元素转化成CO和C、H化合物,燃料利用不充分。
(质量守恒定律)
参加化学反应的各物质质量总和等于反应生成的各物质质量总和,这个规律叫质量守恒定律。
判断:反应物的'质量总和等于生成物的质量总和(×)
质量守恒定律只适用于化学变化,适用于一切化学变化。
在一切化学反应中,反应前后
①原子的种类没有改变,
②原子的数目没有增减,
③原子的质量也没有变化,所以反应前后各物质的质量总和相等。
小结:在化学反应中:
一定不变的是:
①各物质的质量总和
②元素的种类
③元素的质量
④原子的种类
⑤原子的数目
⑥原子的质量;
一定改变的是:
①物质的种类
②分子的种类;
可能改变的是:
①分子的数目
②元素的化合价.
书写化学方程式应遵守的两个原则:一是必须以客观事实为基础,二是要遵守质量守恒定律,“等号”表示两边各原子的数目必须相等。
【九年级化学《燃烧与燃料》期末复习知识点】。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
期末重点复习:初三化学--燃料知识梳理1.当今社会的三大化石燃料为________、________和________。
答案:煤石油天然气2.化石燃料是由远古时代动植物和其他生物的遗体,经几亿年时间,在地球内部的热量和压力作用下形成的,所以它属于________资源。
(填“可再生”“不可再生”)答案:不可再生3.三大化石燃料的成分(1)煤主要含_______元素,除此之外,还含有少量的______________等元素。
它是复杂的混合物。
(2)石油主要含_______元素,除此之外,还含有少量的______________等元素。
它也是复杂的混合物。
(3)天然气主要成分为______________气体。
它也属于混合物。
答案:(1)碳硫、氮(2)碳、氢硫、氮(3)甲烷4.化石燃料的燃烧煤、石油、天然气都是由碳氢化合物组成的,碳元素燃烧生成______________,氢元素燃烧生成______________。
答案:CO2H2O5.化石燃料的燃烧,造成对空气污染的原因(1)燃料中某些元素如硫、氮等燃烧时,产生空气污染物有______________等。
(2)燃料燃烧不充分,产生有毒气体______________。
答案:(1) SO2、NO2(2)CO6.化石燃料的综合利用煤、石油、天然气不仅是重要的能源,还是重要的化工资源。
试举出化石燃料综合利用的例子:(1) ________________________________________________________。
(2) ________________________________________________________。
(3) ________________________________________________________。
答案:(1)用石油为原料生产塑料、橡胶、合成纤维等(2)使煤在氧气不足的情况下发生不完全燃烧,从而转化为既可作燃料气,又可作化工原料的CO、CH4、H2等(3)把煤隔绝空气加热,将煤分解为焦炭、煤焦油、焦炉气(含有CO、CH4、H2、CO2等)疑难突破如何判断石油的分馏、煤的焦化(干馏)、煤的气化分别属于物理变化还是化学变化?剖析:(1)石油的分馏:在分馏塔内给石油加热,不同温度时分别由液体汽化出来,经冷凝分离,这种操作叫做分馏。
原理是利用石油中各物质沸点的不同,让它们逐一汽化出来。
(2)煤的焦化(干馏):把煤隔绝空气加热,将煤分解为焦炭、煤焦油、焦炉气(含有CO、CH4、H2、CO2等)的过程。
此过程中生成了多种新物质。
(3)煤的气化:使煤在氧气不足的情况下发生不完全燃烧,从而转化为既可作燃料气,又可作化工原料的CO、CH4、H2等。
此过程中也生成了多种新物质。
问题探究问题据报道:2010年全国死于煤矿瓦斯爆炸的人数达3000多,如此大的数目让人触目惊心。
安全重于一切,如何消除生产和生活中的不安全因素、学会不同恶劣环境下的逃生方法,显得尤为重要起来。
当你遇到下述紧急情况时,你应当怎样做呢?(1)发现家中煤气泄漏。
(2)进入久未开启的菜窖。
(3)进入煤矿坑道。
探究:(1)煤气主要成分为CO气体,CO有毒,主要表现在它能够结合人体内的血红蛋白,使人窒息死亡。
另外,CO气体具有可燃性,与空气混合均匀后,遇明火会发生爆炸。
要打开家中的门窗进行通风,切忌开灯或打电话报警,开灯或打电话产生的静电火花可能会引起煤气爆炸。
(2)由于菜的呼吸作用,菜窖内氧气减少,二氧化碳气体增多,人贸然进入可能会因缺氧而导致窒息死亡。
(3)煤矿坑道内有瓦斯气体,瓦斯气体是甲烷和空气的混合气体。
甲烷具有可燃性,与空气混合均匀后遇明火会发生爆炸。
根据甲烷的性质和煤矿的密封性,通风是主要的。
典题精讲例1 (2010天津中考) 某气体可能含有CO、CH4、H2、N2中的一种或两种。
该气体在足量的氧气中充分燃烧后,将全部生成物依次通过浓硫酸和氢氧化钠溶液,发现浓硫酸和氢氧化钠溶液的质量都有增加,则该气体的成分不可能是( )A.CH4B.CO和N2C.H2和COD.CO和H2“浓硫酸和氢氧化钠溶液的质量都有增加”,可断定该气体燃烧同时生成了H2O和CO2,思路解析根据题中信息:又因碳元素完全燃烧生成二氧化碳,氢元素燃烧生成水,可知该气体中必须含有碳元素和氢元素。
而氧元素无法判定因为氧气参与反应生成H2O。
答案:B例2 阅读下面短文完成下列有关问题。
我们目前使用得最多的燃料是煤、石油、天然气,它们都是由古代动植物遗体埋在地层下,并在地壳中经过一系列非常复杂的变化而逐渐形成的。
因此,它们被称为化石燃料。
这些燃料在地球上的蕴藏量是有限的,而且又都是经过亿万年才能形成的非再生能源,用一些就会少一些,最终会枯竭。
上图是我国近年来能源总消费量与人均能源消费量。
因此,如何来控制燃烧反应,使燃料充分燃烧,这对节约能源非常重要。
如果我们能把煤等燃料利用率提高一倍,就相当于将这些燃料的使用时间延长一倍。
当今世界各国能源研究的前沿课题之一就是如何提高燃烧效率,节约能源。
煤炭直接燃烧不仅产生大量烟尘,而且煤中所含的硫在燃烧时会生成SO2,这是导致酸雨形成的主要原因之一。
因此,发展洁净煤技术、减少污染物的排放、提高煤炭利用率,正成为我国乃至国际上的又一项重要研究课题。
图4-+10(1)要让煤充分燃烧,提高煤的燃烧效率,应采取的措施是______________________________。
(2)煤燃烧产生的主要污染物是________,如果煤不充分燃烧还会产生的污染物有__________。
(3)高效、清洁地利用煤的主要途径有________________________________________。
(4)二十一世纪,人类在研究开发新能源方面一定会取得重大突破,你认为无污染的能源有______________________________________________________________________。
思路解析能源问题是当今社会的热点问题,与之相关的还有环境问题。
依题意,当今社会主要的能源依然是石油、煤和天然气,本题主要解答煤的充分燃烧和消除煤燃烧所引起的污染问题。
煤的充分燃烧可由燃烧的条件和燃烧的现象等有关知识解释:一是燃烧时要有足够多的空气;二是燃料与空气要有足够大的接触面。
煤的燃烧产物中烟尘和SO2是主要污染物,如果煤不完全燃烧,还会产生CO导致空气污染。
为高效清洁地利用煤,目前采用的方法有:将煤气化,如将煤制成水煤气以提高利用率,或将煤进行脱硫处理以减少污染。
答案:(1)鼓入空气,将煤粉碎以增大与空气的接触面积(2)SO2CO(3)将煤制成水煤气;将煤进行脱硫处理(4)氢能源、核能、地热能、潮汐能、水能、风能、太阳能等例3 (2010黑龙江课改区) 当走过大庆油田时,你会发现长久都不会熄灭的巨大“火炬”,“火炬”产生的黑烟飘向空中。
其实那是为处理在原油开采过程中释放的燃气而造成的。
看到这一情景,你会想到什么?请从能源和环境两个角度谈谈你的观点。
图4-11思路解析煤、石油、天然气是不可再生能源,其储量有限。
目前,在石油开采过程中还存在巨大的能源浪费,大量的粉尘排放,燃烧过程中产生的有害气体污染了我们生存的环境。
答案:(参考答案)能源角度:①将燃气储备输送,直接供给生产、生活的能源②对燃气加工处理,提高燃料的使用效率③将燃烧放出的热量应进行综合利用环境角度:①燃烧产生的有毒、有害气体及粉尘造成空气污染②燃烧中产生大量二氧化碳气体容易造成温室效应知识导学虽然很多物质都能够燃烧,但当今社会起着主要作用的是煤、石油、天然气。
碳元素完全燃烧生成二氧化碳,氢元素燃烧生成水。
这个理论在有机物的学习中非常重要,据此可以写出各种有机物在空气中燃烧的化学方程式。
例如:乙炔(C2H2)燃烧的方程式为:2C2H2+5O2点燃4CO2+2H2O由于煤、石油中还含有硫、氮元素,硫、氮元素燃烧就会产生SO2、NO2等有毒气体,它们一方面污染空气,另一方面还会增加酸雨( H2SO4、HNO3)的形成。
其中,二氧化硫溶于水生成硫酸、二氧化氮溶于水生成硝酸。
对燃料的评价是本节的一个重点。
评价时主要从是否产生污染、是否会导致温室效应、来源、价格、放热量、是否易贮存和运输、是否安全等方面来考虑。
特别是氢气,由于其资源丰富,放热量大,燃烧产物无污染,被称为理想能源。
除上述能源外,太阳能、风能、核能、地热和潮汐等能源的开发,不仅可缓解当前的能源危机问题,还可以减少对环境的污染。
化石燃料的综合利用主要联系日常生活实际,认识它们的应用。
疑难导析这部分知识太抽象、太复杂,我们接触比较少。
要想会做这种题,必须把这左边的几个概念搞清楚。
根据物理变化和化学变化的本质区别——是否有新物质生成来判断。
首先,关于石油的分馏,要描述在分馏塔内给石油加热时,各种物质发生的变化的本质是什么,原理是什么,有无新物质生成。
其次,关于煤的焦化(干馏),要描述在该过程中发生了怎样的变化,有无新物质生成。
最后,关于煤的气化,也要描述在该过程中发生了怎样的变化,有无新物质生成。
问题导思对于这一类问题首先考虑相关的化学物质的性质,针对其化学性质,具体问题具体分析。
(1)关于家中煤气泄漏,要明确煤气由什么组成,有什么性质,对人体有什么危害,家中发生煤气泄漏,与空气混合均匀后,遇明火会发生什么危险。
针对以上分析,家中煤气泄漏,要注意哪些问题,应该采取什么措施以应对这种事故的发生。
(2)关于进入久未开启的菜窖,要描述清楚菜的呼吸作用会产生什么气体,这种气体对菜窖的环境有什么影响,人贸然进入可能会发生什么危险。
(3)关于进入煤矿坑道,要描述清楚煤矿坑道中含有什么气体,该气体有什么性质,有什么隐患,存在于煤矿坑道中,与空气混合均匀后遇明火会发生什么危险,怎样应对这种危险的发生。
对于此类问题,还要联系实际,采取相应的逃生、急救等措施。
典题导考绿色通道在有机物中,碳元素完全燃烧生成二氧化碳,氢元素燃烧生成水,硫元素燃烧生成二氧化硫,氮元素燃烧生成氮的氧化物。
又因燃烧时氧气参与了反应,生成物中的氧元素来自氧气还是有机物,无法确定。
典题变式分别写出一氧化碳、乙炔(C2H2)、乙醇(C2H6O)燃烧的化学方程式。
答案:2CO+O2点燃2CO22C2H2+5O2点燃4CO2+2H2OC2H6O+3O2点燃2CO2+3H2O典题变式一定量的石油在氧气中完全燃烧后测得产生了CO、CO2、NO、SO2、H2O(气)五种物质,由此可以推断石油中一定含___________元素,可能含___________元素。
答案:C、H、N、S O绿色通道对燃料进行评价时,主要从是否产生污染、是否会导致温室效应、来源、价格、放热量、是否易贮存和运输、是否安全等方面来考虑。
