2020届人教版高考化学:无机工艺流程二轮练题(答案不全)
2020届高考化学人教第二轮复习专题强化练:化学工艺流程题(含解析)

2020届高考化学人教第二轮复习专题强化练化学工艺流程题1、磷酸铁锂电池是新型的绿色能源电池,其简化的生产工艺流程如下。
(1)反应釜中反应的化学方程式为____________________,该反应体现出非金属性关系:P________(填“>”或“<”)C。
(2)室温下,LiH 2PO 4溶液的pH 随c (H 2PO -4)的变化如图1所示,H 3PO 4溶液中H 2PO -4的分布分数δ随pH 的变化如图2所示[δ=c H 2PO -4c总(含P 元素的粒子)]。
①由图1知,低浓度时LiH 2PO 4溶液的pH 小于7,且随着c 初始(H 2PO -4)的增大而减小,其合理的解释为____________________。
②综合上图分析,若用浓度大于1mol·L -1的H 3PO 4溶液溶解Li 2CO 3,要使反应釜中的H 3PO 4几乎全部转化成LiH 2PO 4,反应釜中需要控制溶液的pH=________。
(3)磷酸铁锂电池总反应为:LiFePO4+6C Li1-x FePO4+Li x C6,电池中的固体电解质可传导Li+。
充电时,Li+移向________(填“阳极”或“阴极”);放电时,正极反应式为___________________________________________________。
(4)磷酸铁锂电池中铁的含量可通过如下方法测定:称取1.60g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030mol·L-1重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液50.00mL。
已知:2Fe3++Sn2++6Cl-===SnCl2-6+2Fe2+4Cl-+Sn2++2HgCl2===SnCl2-6+Hg2Cl26Fe2++Cr2O2-7+14H+===6Fe3++2Cr3++7H2O①实验中加入HgCl2饱和溶液的目的是___________________。
2020届(人教版)高考化学:无机化工工艺流程二轮练题含答案

2020届(人教版)高考化学:无机化工工艺流程二轮练题含答案*无机化工工艺流程*1、Ni2O3主要用作陶瓷、搪瓷和玻璃的着色颜料,也可用于镍粉的制造,其一种生产工艺如下:(1)Ni2O3中Ni的化合价为________________。
(2)为了提高金属镍废料浸出速率,在“酸浸”时可采取的措施有_______________ _________________________________________________________________(写两条)。
(3)加入H2O2“氧化”的离子方程式为_______________________________________;加入Na2CO3溶液调pH,产生的“滤渣”是____________________________________。
(4)从滤液A中可回收利用的主要物制质是________;加入NaClO溶液和NaOH 溶液,“氧化”生成Ni2O3的离子方程式为___________________________________________。
_________________________________________________________________。
答案(1)+3(2)适当升高温度、增大盐酸的浓度、搅拌或将镍废料研成粉末等(任写两条)(3)2Fe2++H2O2+2H+===2Fe3++2H2O Fe(OH)3(4)NaCl2Ni2++ClO-+4OH-===Ni2O3↓+Cl-+2H2O2、铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:请回答下列问题:(1)若A 为H 2O(g),可以得到Fe 3O 4,写出H 2O 的电子式:________________。
2020届高考化学二轮复习专题八无机化工流程(含解析)

精品文档,欢迎下载如果你喜欢这份文档,欢迎下载,另祝您成绩进步,学习愉快!专题八 无机化工流程1、工业上采用氯化铵焙烧菱锰矿制备高纯度碳酸锰,其工艺流程如下:已知:①菱锰矿的主要成分是3MnCO ,还含有少量的Fe 、Al 、Ca 、Mg 等元素。
②氢氧化物沉淀的条件:3Al +、3+Fe 完全沉淀的pH 分别为4.7、3.2;2+Mn 、2Mg +开始沉淀的pH 分别为8.1、9.1。
③“焙烧”过程的主要反应:34MnCO +2NH Cl 2322MnCl +2NH +CO +H O ↑↑。
④常温下,几种难溶物的sp K 如下表所示: 难溶物2Mn(OH) 3MnCO 2CaF 2MgFsp K132.010-⨯ 112.010-⨯ 102.010-⨯ 117.010-⨯1.分析图1、图2、图3,推测最佳的焙烧温度、焙烧时间、4(NH Cl)()m m 菱锰矿粉分别为__________、__________、__________。
2.“除杂”过程如下:①已知几种氧化剂氧化能力的强弱顺序为3+42282222(NH )S O >H O >Cl >MnO >Fe ,则氧化剂X 宜选择___________(填字母序号)。
A.4228(NH )S O B.2MnO C.22H O D.2Cl②调pH 时,pH 可取的最低值为 _____________。
③当2CaF 、2MgF 两种沉淀共存时,若溶液中2+5(Ca ) 1.010mol/L c -=⨯,则2+(Mg )c =___________mol/L 。
3.“沉锰”过程中,不能用碳酸钠溶液代替43NH HCO 溶液的可能原因是__________。
4.测定碳酸锰粗产品的纯度。
实验步骤如下:①称取0.5000g 碳酸锰粗产品于300mL 锥形瓶中,加少量水润湿。
再加入25mL 磷酸,移到通风橱内加热至240℃。
②将上述锥形瓶中的溶液加水稀释至100mL,滴加2~3滴指示剂,然后用浓度为0.2000mol/L 的硫酸亚铁铵4242[(NH )Fe(SO )]标准溶液滴定,发生的反应为3-2+2+3+3-424[Mn(PO )]+Fe =Mn +Fe +2PO 。
2020届(人教版)高考化学:无机(化工)工艺流程二轮练习题附答案

无机(化工)工艺流程练习题*无机(化工)工艺流程*1、医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:已知:查阅资料得知氢氧化物沉淀时的pH如下表。
氢氧化物Fe(OH)3Al(OH)3开始沉淀时的pH 2.3 4.0 开始溶解:7.8完全沉淀时的pH 3.7 5.2 完全溶解:10.8(1)CaCO3与盐酸反应的离子方程式:_________________________________。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为________,目的是除去溶液中少量的Al3+、Fe3+。
检验Fe(OH)3是否沉淀完全的实验操作是________________________。
(3)过滤时需用的玻璃仪器有________。
滤渣主要成分的化学式:________。
(4)酸化时加盐酸的目的为①_______________________________________,②防止Ca2+在蒸发时发生水解。
(5)为什么蒸发结晶要保持在160 ℃:__________________________________。
(6)若所测样品CaCl2·2H2O的质量分数偏高(忽略其他实验误差),可能的原因之一为___________________________________________________________________________________________________________________________。
解析根据流程可知,加入氢氧化钙的目的是通过调节溶液的pH使Al3+、Fe3+转化为Fe(OH)3、Al(OH)3,使其沉淀完全,根据表中的数据可知,选择的pH 应使得两种离子都生成沉淀,特别要保证Al3+全部沉淀后不能再溶解,故选择pH为5.2~7.8。
检验Fe(OH)3是否沉淀完全即检验溶液中是否还存在Fe3+,可用KSCN溶液检验。
2020高三化学二轮复习高考常考题:无机化工流程图题

2020届届届届届届届届届届届—— 届届届届届届届届届届届届届届届一、单选题(本大题共20小题,共40分)1.某化学小组以铝土矿(含Al2O3、Fe2O3和SiO2)为原料进行炼铝探究(流程如下),叙述错误..的是()A. 步骤①②过程中均需过滤操作B. a、b中铝元素的化合价相同C. 反应③的化学方程式为:2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3D. d只能是氧化铝2.(NH4)2SO4是一种常见的化肥,某工厂用石膏、NH3、H2O和CO2制备(NH4)2SO4的工艺流程如下:下列说法正确的是()A. 通入NH3和CO2的顺序可以互换B. 操作2为将滤液加热浓缩、冷却结晶、过滤,可得(NH4)2SO4C. 步骤②中反应的离子方程式为Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+D. 通入的NH3和CO2均应过量,且工艺流程中CO2可循环利用3.由二氧化硅制高纯硅的流程如下,下列判断中不正确的是()A. ①②③均属于氧化还原反应B. H2和HCl均可循环利用C. SiO2是一种坚硬难熔的固体D. 硅可用于制作光导纤维4.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收Cu并制备ZnO的部分实验过程如图3所示:下列叙述错误的是()A. 合理处理废弃旧电池的铜帽既有利于节约资源,又有利于保护环境B. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2C. 加入锌粉反应的离子为Cu2+D. “过滤”操作后直接将溶液蒸发结晶、高温灼烧得到ZnO5.多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。
已知多晶硅第三代工业制取流程如图所示:下列说法错误的是()A. Y、Z分别为H2、Cl2B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1C. SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价D. Y与SiHCl3制备多晶硅的反应属于置换反应6.活性氧化锌是一种多功能性的新型无机材料。
2020届高考化学二轮备考专题辅导与测试:大题强化训练——无机工艺流程综合大题【答案+解析】

无机工艺流程综合大题1.某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中含有Ni 70.0%及一定量的Al、Fe、SiO2和有机物,镍及其化合物的化学性质与铁的类似,但Ni2+的性质较稳定)。
已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示。
沉淀物Al(OH)3Fe(OH)3Fe(OH)2Ni(OH)2pH 5.2 3.2 9.7 9.2(1)滤渣a的成分是________,用乙醇洗涤废催化剂的目的是____________________,从废渣中回收乙醇的方法是___________________________________________________________________________________ ___________。
(2)为提高酸浸速率,可采取的措施有__________________(答一条即可)。
(3)硫酸酸浸后所得滤液A中可能含有的金属离子是________________,向其中加入H2O2的目的是__________________________________________________,反应的离子方程式为___________________________________________________。
(4)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,与电镀相比,化学镀的最大优点是____________。
(5)滤液C 进行如下所示处理可以制得NiSO 4·7H 2O 。
滤液C ―――――→调pH =3 溶液D ――――→操作XNiSO 4·7H 2O ①操作X 的名称是______________。
②产品晶体中有时会混有少量绿矾(FeSO 4·7H 2O),可能是由于生产过程中__________导致Fe 2+未被完全氧化。
2020届高考化学二轮复习大题精准训练 制备类无机工艺流程题.docx
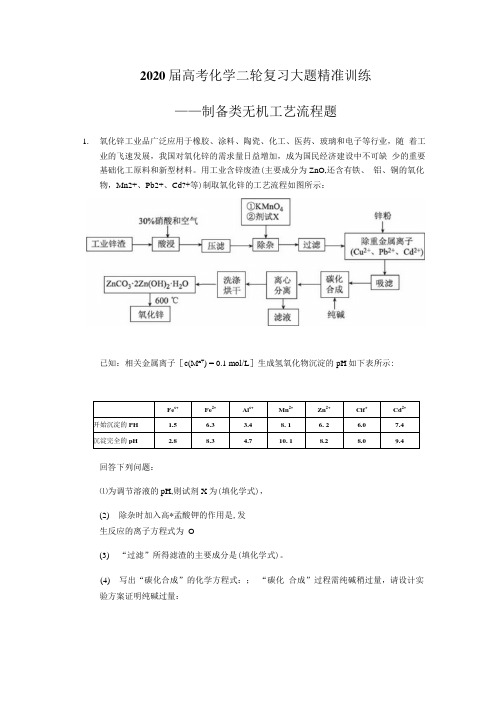
2020届高考化学二轮复习大题精准训练——制备类无机工艺流程题1.氧化锌工业品广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,随着工业的飞速发展,我国对氧化锌的需求量日益增加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。
用工业含锌废渣(主要成分为ZnO,还含有铁、铝、铜的氧化物,Mn2+、Pb2+、Cd?+等)制取氧化锌的工艺流程如图所示:已知:相关金属离子[c(M n+) = 0.1 mol/L]生成氢氧化物沉淀的pH如下表所示:回答下列问题:⑴为调节溶液的pH,则试剂X为(填化学式),(2)除杂时加入高*孟酸钾的作用是,发生反应的离子方程式为O(3)“过滤”所得滤渣的主要成分是(填化学式)。
(4)写出“碳化合成”的化学方程式:;“碳化合成”过程需纯碱稍过量,请设计实验方案证明纯碱过量:2.钛被称为继铁、铝之后的第三金属。
工业上常用硫酸酸解钛铁矿(主要成分为FeTiO3, 还含有部分Fe2O3)的方法制取金红石(TiO2),再还原Ti()2制取金属钛。
工业制取TiC)2的工艺流程图如下:回答下列问题:⑴钛酸亚铁(FeTQ)中Ti的化合价为(2)钛液1中钛以TiO2+的形式存在,则FeTiO3与硫酸反应的离子方程式为(3)为提高钛铁矿的酸解率,可添加适量氧化剂,依据下图判断,添加的最佳氧化剂为(填化学式)。
100j ▲▲90- ---------- "o o o o 8 7 6 5 la®*KMnO4 -^NaClO -*-KClC>3• I I I I I I I I I I20 30 40 50 60 70时间/min不同氧化剂对钛铁矿酸解率的影响(4)钛液1中加入的A物质是,流程中的操作a是(5)制取金红石过程中,需要测定TiO?+的含量。
取lOOmL钛液1,加铝粉,使其发生反应3TiO2+ +Al + 6H+ = 3Ti3+ + Al3+ + 3H2O,反应消耗铝1.35g,则钛液1 中TiO2+的物质的量浓度为。
2020届高三化学二轮复习高考常考题:无机化工流程图题【精编选择20+4大题】 (含解析)
2020届届届届届届届届届—— 届届届届届届届届届届届届届届届届届届届届20+4届届届一、单选题(本大题共20小题,共40分)1.某化学小组以铝土矿(含Al2O3、Fe2O3和SiO2)为原料进行炼铝探究(流程如下),叙述错误..的是()A. 步骤①②过程中均需过滤操作B. a、b中铝元素的化合价相同C. 反应③的化学方程式为:2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3D. d只能是氧化铝2.(NH4)2SO4是一种常见的化肥,某工厂用石膏、NH3、H2O和CO2制备(NH4)2SO4的工艺流程如下:下列说法正确的是()A. 通入NH3和CO2的顺序可以互换B. 操作2为将滤液加热浓缩、冷却结晶、过滤,可得(NH4)2SO4C. 步骤②中反应的离子方程式为Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+D. 通入的NH3和CO2均应过量,且工艺流程中CO2可循环利用3.由二氧化硅制高纯硅的流程如下,下列判断中不正确的是()A. ①②③均属于氧化还原反应B. H2和HCl均可循环利用C. SiO2是一种坚硬难熔的固体D. 硅可用于制作光导纤维4.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收Cu并制备ZnO的部分实验过程如图3所示:下列叙述错误的是()A. 合理处理废弃旧电池的铜帽既有利于节约资源,又有利于保护环境B. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2C. 加入锌粉反应的离子为Cu2+D. “过滤”操作后直接将溶液蒸发结晶、高温灼烧得到ZnO5.多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。
已知多晶硅第三代工业制取流程如图所示:下列说法错误的是()A. Y、Z分别为H2、Cl2B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1C. SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价D. Y与SiHCl3制备多晶硅的反应属于置换反应6.活性氧化锌是一种多功能性的新型无机材料。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020(届)人教版高考化学:无机工艺流程二轮练题(答案不全) *无机工艺流程*1、过氧乙酸()常用作纺织品漂白剂。
(1)乙醛能与O 2在一定条件下反应生成过氧乙酸,若有11.2 L O 2(标准状况下)参加反应,理论上可生成浓度为40%的过氧乙酸________ g 。
(2)某纺织厂污水中过氧乙酸含量测定:取一定量的污水加入硫酸酸化,然后加入过量KI 溶液充分反应,加入NaOH 溶液调节为弱碱性,用Na 3AsO 3标准液滴定至终点。
已知:CH 3COOOH ――→I -I 2――→AsO 3-3AsO 3-4①I -将过氧乙酸还原为乙酸的离子方程式为_______________________________________________________。
②取污水水样100.00 mL ,按上述方法测定污水中过氧乙酸含量,消耗0.010 00 mol·L -1 Na 3AsO 3标准溶液8.50 mL 。
计算污水中过氧乙酸物质的量浓度(写出计算过程)。
【答案】 (1)95(2)①CH 3COOOH +2I -+2H +===I 2+CH 3COOH +H 2O②CH 3COOOH ~I 2~AsO 3-3n(CH 3COOOH)=n(Na 3AsO 3)=0.010 00 mol·L -1×8.50×10-3 L =8.50×10-5 molc(CH 3COOOH)=8.50×10-5 mol 0.10 L=8.5×10-4 mol·L -1。
2、医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na +、Al 3+、Fe 3+等杂质)生产医用二水合氯化钙工艺流程为:已知:查阅资料得知氢氧化物沉淀时的pH如下表。
氢氧化物Fe(OH)3Al(OH)3开始沉淀时的pH 2.3 4.0 开始溶解:7.8完全沉淀时的pH 3.7 5.2 完全溶解:10.8(1)CaCO3与盐酸反应的离子方程式:_________________________________。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为________,目的是除去溶液中少量的Al3+、Fe3+。
检验Fe(OH)3是否沉淀完全的实验操作是________________________。
(3)过滤时需用的玻璃仪器有________。
滤渣主要成分的化学式:________。
(4)酸化时加盐酸的目的为①_______________________________________,②防止Ca2+在蒸发时发生水解。
(5)为什么蒸发结晶要保持在160 ℃:__________________________________。
(6)若所测样品CaCl2·2H2O的质量分数偏高(忽略其他实验误差),可能的原因之一为___________________________________________________________。
解析根据流程可知,加入氢氧化钙的目的是通过调节溶液的pH使Al3+、Fe3+转化为Fe(OH)3、Al(OH)3,使其沉淀完全,根据表中的数据可知,选择的pH应使得两种离子都生成沉淀,特别要保证Al3+全部沉淀后不能再溶解,故选择pH 为5.2~7.8。
检验Fe(OH)3是否沉淀完全即检验溶液中是否还存在Fe3+,可用KSCN 溶液检验。
(4)加入氢氧化钙除去杂质离子后,往往会有剩余的氢氧化钙,故加入盐酸的目的就是除去过量的氢氧化钙。
答案(1)CaCO3+2H+===Ca2++CO2↑+H2O(2)5.2~7.8取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全(3)烧杯、玻璃棒、普通漏斗Fe(OH)3、Al(OH)3(4)除去过量的氢氧化钙(5)温度太高CaCl2·2H2O会失水(6)Na+没除去,析出NaCl,导致测定结果偏高3、硫酸锌可作为食品锌强化剂的原料。
工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程图如下:(1)将菱锌矿研磨成粉的目的是。
(2)完成“氧化除铁”步骤中反应的离子方程式:□Fe(OH)2+□+□=□Fe(OH)3+□CI-(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,摩尔质量为89g/mol,化学式是。
以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时针铁矿转化为Fe(OH)2,该电池放电反应的化学方程式是。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______ 。
沉淀化学式Mg(OH)2Zn(OH)2MgCO3CaCO3(5)工业上从“滤液3”制取MgO过程中,合适的反应物是____________ (选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.氨水(6)“滤液4”之后的操作依次为____________、_____________、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO的质量分数不低于________3(用代数式表示)【参考答案】(1)增大反应物接触面积(或增大反应速率或使反应更充分)。
(2)2Fe(OH)2+2ClO-+H2O=2Fe(OH)3+Cl-(3)FeO(OH)(或其它合理答案);3FeO(OH)+Al+NaOH+H2O=NaAlO2+3Fe(OH)2(4)8.0≤pH<10.4(或其它合理答案)(5)bd(6)蒸发(浓缩)、(冷却)结晶(或其它合理答案)(7)125m2/99m1(或其它合理答案)4、烟气中SO2和NO x(NO及NO2)的脱除对于环境保护意义重大。
(1)湿式氨法烟气脱硫脱氮是通过氨水吸收烟气,得到含NH4+、SO32-、SO42-、HSO3-和N02的吸收液。
①用离子方程式解释吸收液中含有S03 -的原因:__ __。
②吸收液中的SO32-、HSO3-均对NO2具有吸收作用,但HSO3-对NO2的吸收能力比S032-弱。
a·SO32-与NO2反应生成NO2的离子方程式是_ ___。
b.经测定,在烟气的吸收过程巾,吸收液对N02的吸收率随烟气通入量变化的曲线如下图所示。
结合化学用语解释产生上述结果的原因:____。
(2)二氧化氯(Cl02)具有很强的氧化性,可用于烟气中SO2和NO的脱除。
①酸性条件下,电解NaCl03溶液,生成Cl02的电极反应式是__ __。
②研究表明:ClO2氧化SO2和NO的反应历程与下列反应有关。
i.NO+CIO2= NO2 +CIOii.NO +CIO=NO2 +CIiii.SO2 +CIO2=SO3 +Cl0iV.SO2 +ClO=SO3 +Cl实验测得:CIO2分别氧化纯SO2和纯NO的氧化率以及ClO2氧化SO2和NO混合气中的S02氧化率随时间的变化情况如下图所示。
a·结合上述信息,下列推论合理的是____(填字母序号)。
A.NO的存在会影响ClO2氧化SO2的反应速率B.ClO2氧化SO2的反应速率慢于ClO2氧化NO的反应速率C.反应i中生成的NO2可以加快ClO2氧化SO2的反应速率b.结合反应历程,分析混合气中SO2氧化速率较纯SO2氧化速率快的原因可能是__ _ _。
5、无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为_________________________________________________________。
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:已知:物质SiCl4AlCl3FeCl3FeCl2沸点/℃57.6 180(升华) 300(升华) 1 023_________________________________________(只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是___________________________________。
③已知:Al2O3(s)+3C(s)===2Al(s)+3CO(g)ΔH1=+1 344.1 kJ·mol-12AlCl3(g)===2Al(s)+3Cl2(g)ΔH2=+1 169.2 kJ·mol-1由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为_____________________________________________________。
④步骤Ⅲ的尾气经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为_____________________________。
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是_________________________________________________。
解析(1)AlCl3属于强酸弱碱盐,在溶液中Al3+发生水解反应生成Al(OH)3胶体:Al3++3H2O Al(OH)3(胶体)+3H+;(2)①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,可以防止后续步骤生成的AlCl3水解,同时也增大了反应物的接触面积,从而加快反应速率。
②根据物质的组成元素可知:若步骤Ⅱ中不通入氯气和氧气,则反应生成相对原子质量比Si大的单质是Fe。
③对已知两个热化学方程式由上到下依次标记为(i)和(ii),根据盖斯定律,(i)-(ii)可得所求热化学方程式:Al2O3(s)+3C(s)+3Cl2(g)===2AlCl3(g)+3CO(g)ΔH=+174.9 kJ·mol-1;④步骤Ⅲ经冷却至室温后,气体中含有Cl2、CO2、O2等,用足量的NaOH冷溶液吸收。
因此,得到的3种盐分别为NaCl、NaClO、Na2CO3。
⑤Al的活动性强于Fe,在步骤Ⅴ中加入Al粉与FeCl3发生置换反应,以除去FeCl3从而提高AlCl3的纯度。
答案(1)Al3++3H2O Al(OH)3(胶体)+3H+(2)①防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率②Fe或铁③Al2O3(s)+3C(s)+3Cl2(g)===2AlCl3(g)+3CO(g)ΔH=+174.9 kJ·mol-1④NaCl、NaClO、Na2CO3⑤除去FeCl3,提高AlCl3纯度6、(2019·高考名校联考信息优化卷)硼氢化钠(NaBH4)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33 ℃)。
