微生物检验记录表
微生物限度检查记录表格

乳糖胆盐发酵培养基(18~
24h)
EMB培养基(18~24h)
(批号:)
乳糖发酵培养基(24~
48h)
供
试
品
10-
(批号:)
(批号:)
1-
10
2-
10
3
阴性对照
阳性对照
结果
个/g(规定:<个/
微生物限度检查(根据需要在表头补充产品名称、批号,日期等)
供试液制备
取供试品g,加入pH7.0无菌氯化钠-蛋白胨缓冲液至ml,混匀。
供试液制备
取供试品g,加入pH7.0无菌氯化钠-蛋白胨缓冲液至ml,混匀。
□研钵法□振摇法
细菌、霉菌和酵母菌计数□
平皿
号
细菌数(30~35℃3天)
营养琼脂培养基(批号:)
霉菌和酵母菌数(23~28℃5天)
玫瑰红钠琼脂培养基(3
10-4
阴性对照
10-1
10-2
阴性对照
1
2
□研钵法□振摇法
细菌、霉菌和酵母菌计数□
平皿
号
细菌数(30~35℃3天)
营养琼脂培养基(批号:)
霉菌和酵母菌数(23~28℃5天)
玫瑰红钠琼脂培养基(批号:)
10-1
10-2
10-3
10-4
阴性对照
10-1
10-2
阴性对照
1
2
平均
结果
cfu/g(规定:≤cfu/g)
cfu/g(规定:≤cfu/g)
大肠埃希菌检查□培养条件:30~35℃18~24h
平均
结果
cfu/g(规定:≤cfu/g)
cfu/g(规定:≤cfu/g)
微生物检验记录表
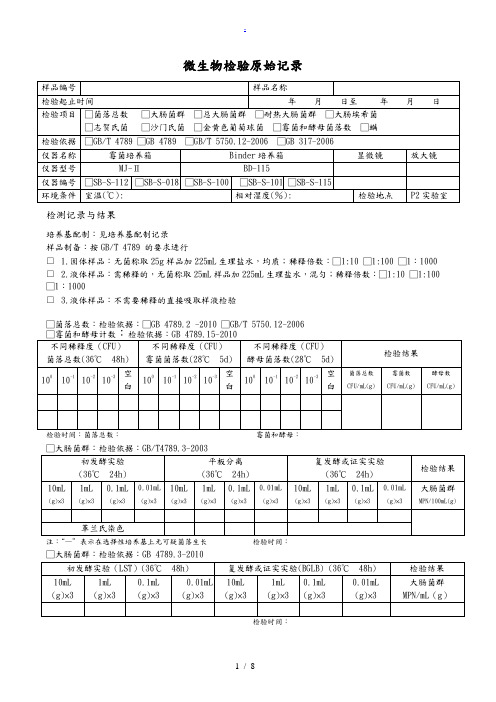
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物检验原始数据登记表
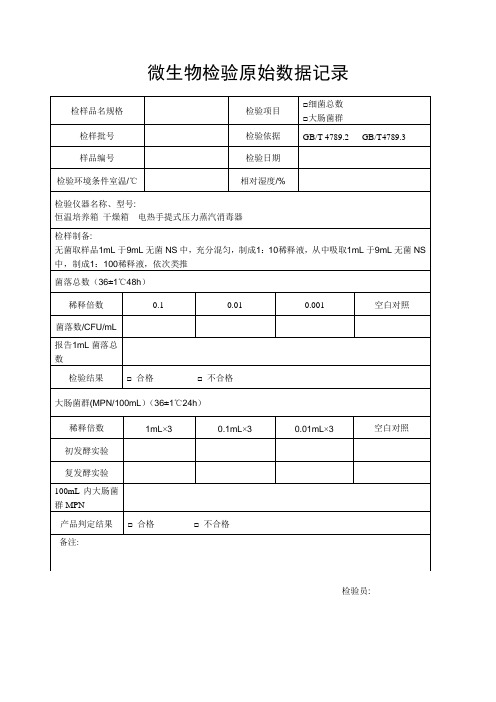
微生物检验原始数据记录
检验员:
检样品名规格 检验项目 □细菌总数 □大肠菌群
检样批号 检验依据 GB/T 4789.2 GB/T4789.3 样品编号 检验日期 检验环境条件室温/℃
相对湿度/%
检验仪器名称、型号:
恒温培养箱 干燥箱 电热手提式压力蒸汽消毒器 检样制备:
无菌取样品1mL 于9mL 无菌NS 中,充分混匀,制成1:10稀释液,从中吸取1mL 于9mL 无菌NS 中,制成1:100稀释液,依次类推 菌落总数(36±1℃48h )
稀释倍数 0.1 0.01 0.001 空白对照
菌落数/CFU/mL
报告1mL 菌落总数
检验结果
□ 合格 □ 不合格
大肠菌群(MPN/100mL )(36±1℃24h )
稀释倍数 1mL ×3
0.1mL ×3
0.01mL ×3
空白对照
初发酵实验 复发酵实验
100mL 内大肠菌群MPN
产品判定结果 □ 合格 □ 不合格 备注:。
微生物检验原始记录范本
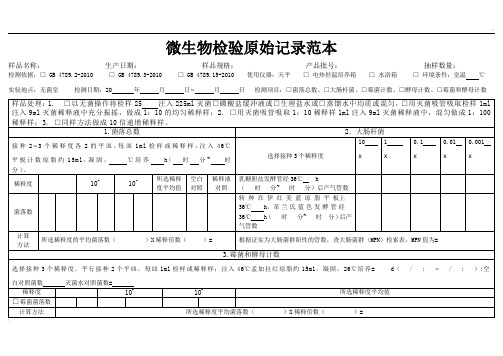
样品名称:生产日期:样品规格:产品批号:抽样数量:
检测依据:□ GB4789.2-2010□GB 4789.3-2010□GB 4789.15-2010使用仪器:天平□ 电热恒温培养箱 □ 水浴箱 □ 环境条件:室温℃
实验地点:无菌室检测日期:20年月日~月日检测项目:□菌落总数、□大肠杆菌、□霉菌计数、□酵母计数、□霉菌和酵母计数
稀释度
10-
ቤተ መጻሕፍቲ ባይዱ10-
所选稀释度平均值
□霉菌菌落数
计算方法
所选稀释度平均菌落数()X稀释倍数( )=
□霉菌菌落数
计算方法
所选稀释度平均菌落数()X稀释倍数( )=
检验菌落总数大肠菌群霉菌 酵母
结果:cfu/MPN/100计数cfu/计数cfu/
检测者: 审核者:
1.菌落总数
2.大肠杆菌
接种2~3个稀释度各2的平皿,每皿1ml检样或稀释样,注入46℃平板计数琼脂约15ml,凝固,℃培养h(时分~时分)。
选择接种3个稀释度
10
x
1
x
0.1x
0.01x
0.001x
稀释度
10-
10-
所选稀释度平均值
空白对照
稀释液对照
乳糖胆盐发酵管经36℃h
(时 分~时分)后产气管数
菌落数
转 种 在 伊 红 美 蓝 琼 脂 平 板上36℃h,革兰氏蓝色发酵管经36℃h(时分~时 分)后产气管数
计算 方法
所选稀释度的平均菌落数( )X稀释倍数( )=
根据证实为大肠菌群阳性的管数,查大肠菌群(MPN)检索表,MPN值为=
3.霉菌和酵母计数
选择接种3个稀释度,平行接种2个平皿,每皿1ml检样或稀释样;注入46℃孟加拉红琼脂约15ml,凝固,26℃培养=d( / :~/ : );空白对照菌数灭菌水对照菌数=
微生物检验记录表
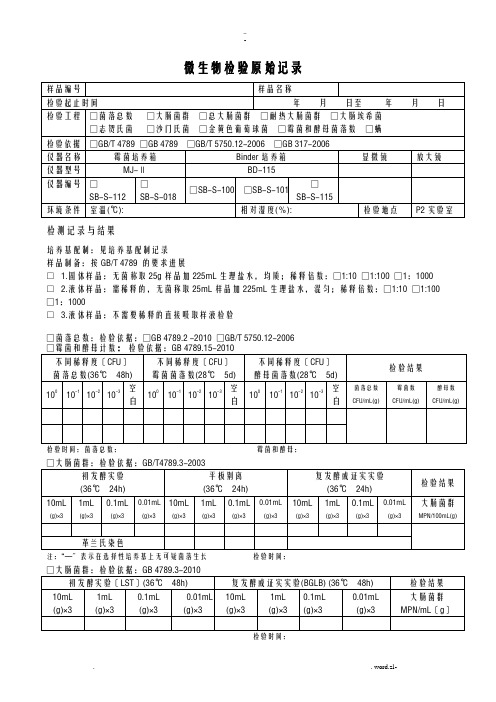
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进展
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—〞表示在选择性培养基上无可疑菌落生长检验时间:□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据GB 317.4-.10-2006
检测人:复核人:微生物限度检验记录〔复合膜〕
检验人:复核人:微生物限度检验记录〔辅料〕
检验人:复核人:
微生物限度检验记录〔铝箔、PVC硬片〕
微生物限度检验记录〔半成品、成品〕
微生物限度检验记录〔辅料〕。
微生物检验技能考试评分记录表
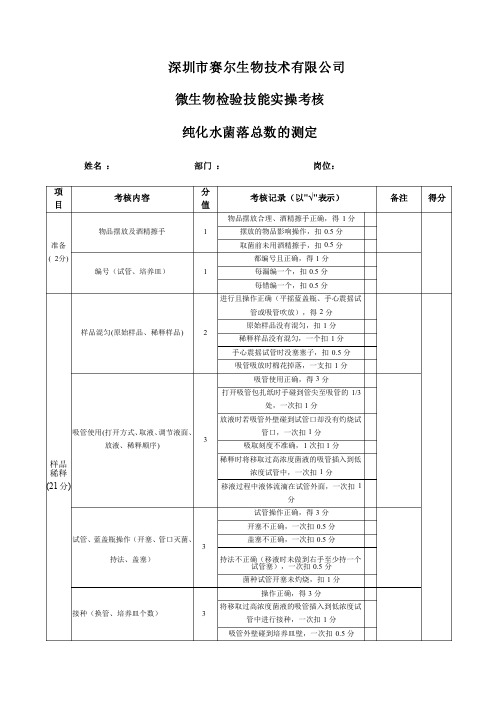
深圳市赛尔生物技术有限公司 微生物检验技能实操考核 纯化水菌落总数的测定姓名 : 部门 : 岗位: 项目考核内容分值考核记录(以"√"表示)备注得分准备准备 ( 2分) 物品摆放及酒精擦手物品摆放及酒精擦手1 物品摆放合理、酒精擦手正确,得1分摆放的物品影响操作,扣0.5分 取菌前未用酒精擦手,扣0.5分编号(试管、培养皿)编号(试管、培养皿)1 都编号且正确,得1分每漏编一个,扣0.5分 每错编一个,扣0.5分样品稀释稀释 (21分) 样品混匀(原始样品、稀释样品) 2 进行且操作正确(平摇蓝盖瓶、手心震摇试管或吸管吹放),得2分原始样品没有混匀,扣1分 稀释样品没有混匀,一个扣1分 手心震摇试管时没塞塞子,扣0.5分 吸管吸放时棉花掉落,一支扣1分吸管使用(打开方式、取液、调节液面、放液、稀释顺序) 3 吸管使用正确,得3分打开吸管包扎纸时手碰到管尖至吸管的1/3处,一次扣1分放液时若吸管外壁碰到试管口却没有灼烧试管口,一次扣1分吸取刻度不准确,1次扣1分稀释时将移取过高浓度菌液的吸管插入到低浓度试管中,一次扣1分移液过程中液体流滴在试管外面,一次扣1分试管、蓝盖瓶操作蓝盖瓶操作(开塞、(开塞、管口灭菌、持法、盖塞)持法、盖塞)3 试管操作正确,得3分开塞不正确,一次扣0.5分盖塞不正确,一次扣0.5分持法不正确(移液时未做到右手至少持一个试管塞),一次扣0.5分菌种试管开塞未灼烧,扣1分接种(换管、培养皿个数)接种(换管、培养皿个数) 3 操作正确,得3分将移取过高浓度菌液的吸管插入到低浓度试管中进行接种,一次扣1分吸管外壁碰到培养皿壁,一次扣0.5分漏接培养皿,一个扣0.5分 试管被污染,每根扣1分加培养基(培养皿持法、加入量、污染皿壁、混匀、)染皿壁、混匀、)4 正确(单手持皿,平端,两指自如开合皿盖,另一只手持培养基瓶),得4分加入培养基量低于10mL ,一次扣0.5分培养基污染皿壁,一次扣1分 培养基瓶接触平皿,一次扣0.5分 培养基有凝块、不透明,一次扣1分酒精灯附近区操作酒精灯附近区操作2 在酒精灯附近区操作,得2分未在酒精灯附近区操作,扣2分空白空白 1 进行,得1分未进行,一个扣0.5分操作熟练程度操作熟练程度3 熟练,得3分较熟练,得2分 一般,得1分 不熟练,得0分培养(3分)琼脂凝固琼脂凝固1 凝固,得1分没有凝固,1个扣0.5分 翻转培养皿翻转培养皿 2 正确培养,得2分培养时未翻转培养皿,一个扣1分清场操作操作 (2分) 实验后台面整理实验后台面整理 1 整理,得1分未整理,扣1分 器皿破损器皿破损 1 未破损,得1分破损,扣1分合计合计考核人:日 期:。
微生物限度检验记录
三糖铁琼脂培养基
供试品溶液制备
取供试品10g,加pH7.0氯化钠-蛋白胨缓冲液至100ml,混匀,作为1:10的供试液,取上液1ml,加至9mlpH7.0氯化钠-蛋白胨缓冲液,混匀,作为1:100的供试液。
检验项目
一、需氧菌总数(33℃培养5天)
二、霉菌和酵母菌总数(23℃培养7天)
麦康凯液体培养基选择培养
(42℃,48h)
麦康凯琼脂培养基分离培养
(33℃,72h)
供试品
阳性对照
阴性对照
结果
□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出)
检验项目
四、金黄色葡萄球菌
胰酪大豆胨液体培养基增菌培养
(33℃,24h)
甘露醇氯化钠琼脂培养基选择分离培养
(33℃,72h)
供试品
阳性对照
检验项目
一、需氧菌总数(33℃培养5天)
二、霉菌和酵母菌总数(23℃培养7天)
培养时间
原液
10-1
阴性对照
原液
10-1
阴性对照
皿1
皿2
皿1
皿2
皿1
皿2
皿1
皿2
皿1
皿2
皿1
皿2
菌落数
平均值
结果
CFU/100cm2标准规定
CFU/100cm2标准规定
检验项目
三、大肠埃希菌
胰酪大豆胨液体培养基增菌培养
(33℃,24h)
供试品
阳性对照
阴性对照
结果
□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出)
检验项目
四、沙门菌
胰酪大豆胨液体培养基增菌培养
(33℃,24h)
微生物检验原始记录表格式
稀释度
产气管数
(2)伊红美蓝琼脂分离培养
培养基名称
伊红美蓝琼脂
培养温度
36℃±1℃
培养时间
18~24h
空白性
(3)证实试验(凡乳糖发酵管产气、革兰氏染色为阴性的无芽孢杆菌,即可报告为大肠菌阳性)
培养基名称
乳糖发酵管
培养温度
36℃±1℃
培养时间
248±2h
空白性
阳性管数
大肠菌群(MPN/ mL)
微生物检验原始记录
样品名称:检验日期:检验人:复核人:
1.菌落总数
培养基名称
营养琼脂培养基
培养温度
36℃±1℃
培养时间
48±2h
空白性
稀释度
菌落数(1)
菌落数(2)
平均菌落数
菌落总数(cfu/mL)
2.大肠菌群
(1)乳糖胆盐发酵管初发酵试验
培养基名称
乳糖胆盐发酵管பைடு நூலகம்
培养温度
36℃±1℃
培养时间
24±2h
微生物检验记录簿表格
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨:检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人:复核人:
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
微生物限度检查记录版
表:2.1-024微生物限度检查记录(通用)1. 常规法:取供试品10為1,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
2. 薄膜过滤法:取供试品10mi ,用胰酪大豆胨液体培养基稀释至 100ml ,用匀浆仪等适宜的方法混匀,制成1:10供试液。
吸取1:10的供试液10ml ,过滤,加0.1%无菌蛋白胨水溶液 300ml 分 三次冲洗,每次100ml ;冲洗后,将滤膜正贴于胰酪大豆胨固体培养基和沙氏葡萄糖琼脂培养基 上,每种培养基平行制备 2个平皿。
按平皿法测定其菌数。
胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批)麦康凯琼脂培养基(配制批号: )供试液制备微生物限度检查记录、需氧菌总数检查30〜353〜5)、霉菌、酵母菌总数检查20C〜25C,5〜7天)三糖铁琼脂斜面穿刺接种 (18〜24h )三、控制菌检查 (30-35 C )检验者:表:2.1-024号:结论本品经按《中国药典》2015年版“非无菌产品微生物限度检查法”进行检验,结果审核者:微生物限度检查记录(丸剂)供试液制备供试液。
胰酪大豆胨增菌 (18〜24h )RV 沙门选择培养木糖赖氨酸脱氧胆酸分离培养(18〜48h )胰酪大豆胨液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)四、沙门菌检查 (30 °C 〜35C ) 胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:五、耐胆盐革兰阴性菌检杳胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:审核者:检验者: 表:2.1-024阴性对照阳性对照三、大肠埃希菌检查)、麦康凯液体培养基(配制批结果□检出大肠埃希菌□未检出大肠埃希菌(规定:不得检出/g)四、沙门菌检查(30°C〜35C)胰酪大豆东液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:、表: 2.1-024 微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)审核者:检验者:表:2.1-024 微生物限度检查记录(30〜353〜5天)、霉菌、酵母菌总数检查20C〜25C, 5〜7天)1、 口服液体药用聚酯瓶:取数个试瓶,加入1/2标示容量的氯化钠注射液,将盖旋紧,振摇1分钟,即得供试液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
微生物检验原始记录
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 得要求进行
□1、固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:10
00
□2。
液体样品:需稀释得,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10□1:100 □1:1000
□3、液体样品:不需要稀释得直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2-2010 □GB/T 5750.12-2006
检验时间:菌落总数: 霉菌与酵母:
注:“-"表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
注:“-”表示在选择性培养基上无可疑菌落生长检验时间:
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
□螨: 检验依据GB 317、4-、10-2006
ﻬ微生物限度检验记录(复合膜)
检验人: 复核人:
微生物限度检验记录(辅料)
检验人: 复核人:
微生物限度检验记录(铝箔、PVC硬片)
检验人: 复核人:
ﻬ微生物限度检验记录(半成品、成品)
检验人: 复核人:
ﻬ微生物限度检验记录(辅料)
检验人: 复核人:。
