药品生产统计表
药库、药房统计表

1.本表由药房、药库和材料 、药品领用两板块构成。 2.药库、药房数据输入:新 增药品需在药库统计表的(号、 品名、单位)输入信息。
表
材料、药品领用 内科 儿科 外科 妇科 外2科 放射、B超室 注射室 检验科 护理部 药房
由于本人个人水平有限如有不足请谅解!谢谢与我联系! 加我QQ:1207478725
表
材料、药品领用 公卫科 手术室 护工
科室分类汇总 材料、药品领用汇总
信息一致(如:号、品名、单位)。材料
品名、单位、单价)输入相应的信息。
根据规定的药品种类输入(所有科室都
了解本月各科室耗材情况;材料、药品
25@。本表为3.8M大小。
系! 加我QQ:1207478725
6 7 8 9 10
3.材料、药品领用板块的信息需与药库统计表的信息一致(如:号、品名、单位)。材料 、药品领用信息输入:在材料、药品领用汇总的(号、品名、单位、单价)输入相应的信息。 各分科室信息自动生成。材料、药品领用模板内信息根据规定的药品种类输入(所有科室都 都领用的就不用输入了)。月末,科室分类汇总能够了解本月各科室耗材情况;材料、药品 领用汇总了解本月各类耗材情况。 4.本表均有密码保护,如需修改,请 @1207478725@。本表为3.8M大小。
药品安全监管检查月统计表

零售药店
(1)是否严格按照经营范围购销药品,购进渠道是否合法,营业场所是否与其药品经营范围、经营规模相适应,是否存在私设库房或者变相从事药品批发活动的行为。
(2)是否按包装标示的温度等要求储存药品,经营冷藏药品是否有专用冷藏设备。
(3)是否购进销售回收药品,采购药品是否按规定索取发票,证、票、账、货、款是否相符一致;是否违规销售含麻黄碱类复方制剂等。
(5)对不能提供储存、运输全过程温度监测记录或者温度控制不符合要求的,是否拒绝接收或者购进,并立即报告药品监管部门、卫生健康主管部门。
(6)是否建立不合格疫苗登记制度,对包装无法识别、储存温度不符合要求、超过有效期等问题的疫苗,是否如实进行登记,并按规定统一回收至县级疾控机构集中处理。
检查对象
检查重点内容
(5)对不合格疫苗(包括包装无法识别、储存温度不符合要求、超过有效期等,下同)是否采取隔离存放、暂停发货,并标注相应警示标志等措施。
疾病预防控制机构
(1)是否按规定建立真实、完整的疫苗购进、储存、分发、供应记录,并保存至超过疫苗有效期5年备查,购进疫苗是否做到票、账、货、款一致。
(2)是否根据储存、供应、运输疫苗的需要配备冷库、冷藏运输车(疫苗运输车)、冰柜(箱)或冷藏箱(包)、温度监测器材或设备等。
检查对象
检查重点内容
互联网药品信息服务企业
(1)是否在其网站主页显著位置标注《互联网药品信息服务资格证书》的证书编号。
(2)所登载的药品信息是否符合国家的法律、法规和国家有关药品、医疗器械管理的相关规定。
(3)是否发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息。
(7)是否如实、规范记录疫苗储存、运输过程温度监测数据。对冷库、冰箱等设备是否填写《冷链设备温度记录表》,其记录是否真实、完整。
药物化学强化冲刺药品归类统计表_Q药网_2013年

磷酸可待因、磷酸苯丙哌林、右美沙芬、喷托维林 盐酸氨溴索、乙酰半胱氨酸、羧甲司坦 西咪替丁、盐酸雷尼替丁、法莫替丁、罗沙替丁、尼扎替丁 奥美拉唑、埃索美拉唑、兰索拉唑、泮托拉唑、雷贝拉唑钠 甲氧氯普胺、多潘立酮、莫沙必利、伊托必利 昂丹司琼、格拉司琼、托烷司琼、阿扎司琼、盐酸帕洛诺司琼 对乙酰氨基酚、阿司匹林、赖氨匹林、贝诺酯、安乃近 吲哚美辛、双氯芬酸钠、舒林酸、萘丁美酮、芬布芬、布洛芬、萘普生、吡罗昔康、氯诺昔 康、美洛昔康、塞来昔布、帕瑞昔布、尼美舒利 别嘌醇、丙磺舒、秋水仙碱、苯溴马隆 盐酸苯海拉明、马来酸氯苯那敏、盐酸赛庚啶、盐酸西替利嗪(左西替利嗪)、氯雷他定 (地氯雷他定)、富马酸酮替芬、诺阿司咪唑、非索非那定 醋酸可的松、氢化可的松、地塞米松、倍他米松、泼尼松、泼尼松龙、醋酸氟轻松 丙酸睾酮、甲睾酮、苯丙酸诺龙、司坦唑醇 雌二醇、苯甲酸雌二醇、炔雌醇、炔雌醚、尼尔雌醇、己烯雌酚、磷雌酚 黄体酮、醋酸甲羟孕酮、醋酸甲地孕酮、醋酸氯地孕酮、炔诺酮、左炔诺孕酮、米非司酮 胰岛素类药物 格列本脲、格列美脲、格列齐特、格列吡嗪、格列喹酮、那格列奈、瑞格列奈、米格列奈 盐酸二甲双胍、盐酸吡格列酮 阿卡波糖、米格列醇、伏格列波糖 盐酸雷洛昔芬、阿法骨化醇、骨化三醇 阿仑膦酸钠、利塞膦酸钠、帕米膦酸二钠、依替膦酸二钠 维生素A醋酸酯、维A酸、维生素D2、维生素D3、阿法骨化醇、骨化三醇、维生素E、维生素 K1 维生素B1、维生素Β 2、维生素Β 6、维生素C、叶酸
(-)平喘药 六、呼吸系统药物
六、呼吸系统药物 (二)镇咳祛痰药 (-)抗溃疡药 七、消化系统药物 (二)胃动力药和止吐药
八、影响免疫系统的药物
(-)非甾体抗炎药 (二)抗变态反应药 (-)肾上腺皮质激素类药物 (二)性激素类药物和避孕药
药品流量统计表
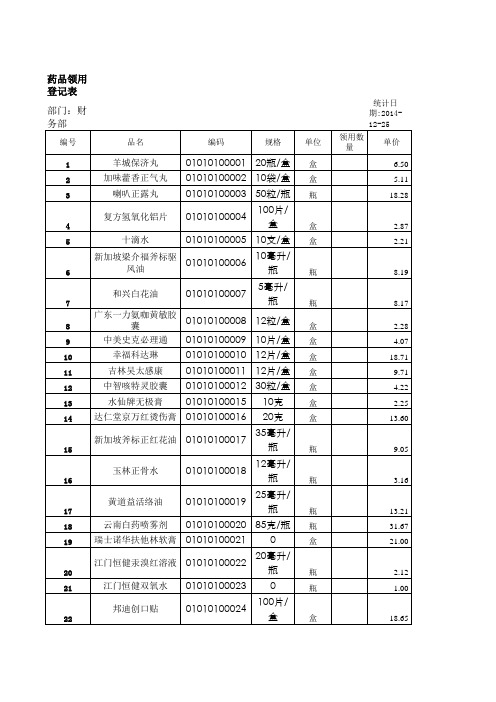
编号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 品名 编码 规格 单位 盒 盒 瓶 盒 盒 瓶 瓶 盒 盒 盒 盒 盒 盒 盒 瓶 瓶 瓶 瓶 盒 瓶 瓶 盒 瓶 盒 支 扎 包 卷 包 盒 盒 包 盒 瓶 领用数量 统计日期:2014-12-25 单价 6.50 5.11 18.28 2.87 2.21 8.19 8.17 2.28 4.07 18.71 9.71 4.22 2.25 13.60 9.05 3.16 13.21 31.67 21.00 2.12 1.00 18.65 15.11 2.30 2.10 2.06 0.94 4.25 1.41 8.25 8.19 2.00 4.00 1.00
广州卫材医用橡皮膏 01010100030
35
合计
人丹
01010100037 30粒/袋
袋 -
3.00
统计日期:2014-12-25 金额 -
-
瑞士诺华扶他林软膏 01010100021 江门恒健双氧水 邦迪创口贴 南阳蚊怕水 广东顺峰扑尔敏 体温计 外用绷带 中山苏华纱布 肇庆先锋脱脂棉球 百消膏 999皮炎平 棉签 正气水 过氧化氢溶液
江门恒健汞溴红溶液 01010100022 20毫升/瓶
01010100023
01010100024 100片/盒 01010100025 80毫升/瓶 01010100026 01010100027 01010100028 01010100029 01010100031 01010100032 01010100033 01010100034 01010100035 01010100036 0 0 0 0 0 0 0 0 0 0 0
药品抽检统计表流通环节监督

合格
17
SC201808333
江苏康缘药业股份有限公司
桂枝茯苓胶囊
60粒
170634
宁夏德立信老百姓医药彭阳兴彭店
2018-04-09
合格
奥硝唑氯化钠注射液
100毫升
1711062
彭阳县妇幼保健计划生育服务中心
2018-04-08
合格
3
SC201808351
国药集团工业有限公司
氨酚待因片
20片
20180105
宁夏德阳医药连锁有限公司彭阳老百姓药店
2018-04-09
合格
4
SC201808340
青海制药厂有限公司
氨酚待因片
20片
20170223
48片
170703
彭阳县大众康药店
2018-04-10
合格
10
SC201808321
上海信谊天平药业有限公司
左炔诺孕酮片
2片
8618010102
彭阳县妇幼保健计划生育服务中心
2018-04-09
合格
11
SC201808374
青海制药有限公司
氨酚待因片(I)
2010
合格
12
SC201808352
广东新峰药业股份有限公司
骨刺平片
100片
170105
宁夏德阳医药连锁有限公司彭阳老百姓药店
2018-04-09
合格
13
SC201808401
广东罗浮山国药股份有限公司
骨刺平片
36片
L16J251
彭阳县康乐堂药品超市
2018-04-10
合格
14
国际麻醉品管制局表C麻醉药品的生产制造消费贮存和缉获数量

2011年12月,第十六版 V .11-88073 (C)国际麻醉品管制局表C麻醉药品的生产、制造、消费、贮存和缉获数量年度统计1961年麻醉品单一公约:第1、2、13、20和27条。
修正1961年麻醉品单一公约的1972年议定书:第1和10条。
说明本表应尽快填写,至迟不能超过相关统计数据所涉及年份下一年6月30日。
可从麻管局网站下载表格。
表格填好后送交:International Narcotics Control Board Vienna International Centre P.O. Box 500 1400 Vienna Austria电话: (+43-1) 26060-4277 传真: (+43-1) 26060-5867/5868 电子邮件: secretariat@ 网址: /Page 2(表C)填表须知概述1. 本表分作四部分:第一部分:麻醉麻醉品的制造、消费、使用和贮存数量统计数据。
第二部分:麻醉麻醉品的制造数量统计数据。
第三部分:罂粟合法种植和大麻、古柯叶和阿片合法生产数量统计数据。
第四部分:麻醉麻醉品缉获量和含麻醉药品的医药产品缉获量统计数据。
2. 为确保准确填写本表,应切记根据1961年麻醉品单一公约第1条规定而列出的下述定义:(a) “消费”系指将一麻醉品供应给任何人或企业用于零售、医用或科学研究;(b) “麻醉品”系指1961年公约表一或表二所列需按公约实行特定管制措施的任何天然或合成物质;(c) “制造”系指除生产(见以下定义)以外一切可用以提取麻醉品的过程,包括精炼以及将一种麻醉品改变为另一种麻醉品;(d) “制剂”系一种含有麻醉品的固体或液体混合剂,需对其实行与所含此种麻醉品同样的管制措施。
但应指出,单一公约表三中所列的制剂免于某些管制措施;(e) “生产”系指将阿片、古柯叶、大麻和大麻树脂自其从出植物析离;(f) “贮存量”系指一国/领土为本国消费、制造其他麻醉品或出口而保存的麻醉品数量;(g) “特别贮存量”系指一国/领土政府为政府特别目的和满足特别情况需要而保存的麻醉品数量。
药品“三统一”配送情况统计表
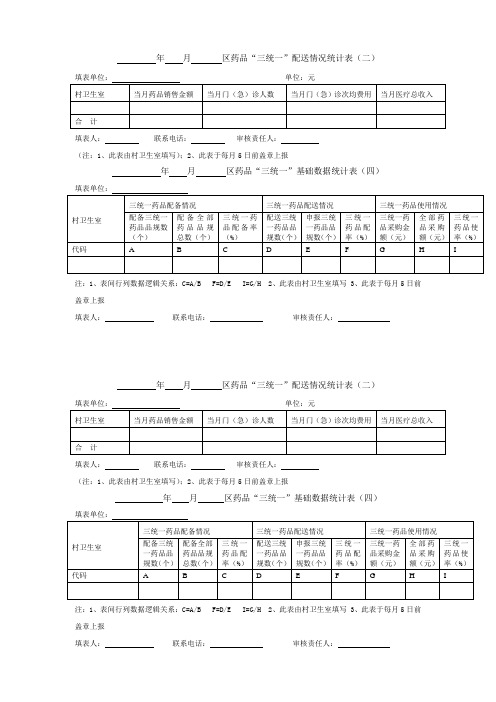
年 月 区药品“三统一”配送情况统计表(二)
填表人: 联系电话: 审核责任人: (注:1、此表由村卫生室填写);2、此表于每月5日前盖章上报
年 月 区药品“三统一”基础数据统计表(四)
注:1、表间行列数据逻辑关系:C=A/B F=D/E I=G/H 2、此表由村卫生室填写 3、此表于每月5日前盖章上报
填表人: 联系电话: 审核责任人:
年 月 区药品“三统一”配送情况统计表(二)
填表人: 联系电话: 审核责任人: (注:1、此表由村卫生室填写);2、此表于每月5日前盖章上报
年
月 区药品“三统一”基础数据统计表(四)
注:1、表间行列数据逻辑关系:C=A/B F=D/E I=G/H 2、此表由村卫生室填写 3、此表于每月5日前盖章上报
填表人: 联系电话: 审核责任人:。
有关麻醉药品登记的各种表格(全套)

有关麻醉药品登记的各种表格(全套)年度麻醉药品注射剂购用计划表药品名称规格计量单位上年度申请用量上年度实际用量本年度申请用量卫生行政部门核定用量填报医疗机构(公章) 联系电话:医疗机构法定代表人(签章)填报人:(签章)年月日卫生行政部门审批意见印章年月日说明:此表一式两份,卫生行政部门存档一份,麻醉药品及精神药品经销单位一份。
麻醉药品注射剂增补购用计划表报请时间:年月日药品名称规格计量单位上年度库存量本年度原核定用量本年度增补用量卫生行政部门核定用量填报医疗机构(公章) 联系电话:医疗机构法定代表人(签章)填报人:(签章)年月日卫生行政部门审批意见印章年月日说明:此表一式两份,卫生行政部门存档一份,麻醉药品及精神药品经销单位一份。
麻醉药品注射剂使用情况统计表医疗机构名称:期间:年月日至年月日品名规格单位批号有效期上年度库存量本年度原核定用量目前已购买量期间使用量现库存量备注总计手术用数量非手术用数量麻醉药品、第一类精神药品出入库记录药品名称:剂型:规格:生产单位:单位:日期凭证号批号有效期供货/领出单位入库验收出库结存购进数量质量情况验收结论验收人复核人保管人发出数量发药人复核人领用人数量表6 麻醉药品、第一类精神药品基数保管登记表药品名称:剂型:规格:单位:固定基数:日期生产单位批号有效期领回数量使用数量结存数量记录人备注说明:基数是指为满足门诊药房、手术室、肿瘤科室等有关科室紧急使用麻醉药品、一类精神药品的需要,医疗机构配备某固定量的麻醉药品、一类精神药品存放在这些科室内,这个限定量称为基数。
基数设定应切合实际。
表7 不合格麻醉药品、第一类精神药品报告记录报告部门:报告日期:年月日编号:品名剂型规格生产单位批号有效期单位数量不合格原因:拟处理意见:报告人:复核人:审批处理意见:审批人:审批日期:年月日(公章)处理结果:经办人:复核人:日期:年月日表8 麻醉药品、第一类精神药品空安瓿交接记录日期药品名称规格单位空安瓿批号数量是否为原批号交回部门交回人接受部门接受人换领药品数量单位说明:1、本表用于记录医院有关科室向药房、药库移交麻醉药品、第一类精神药品空安瓿、废贴情况。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
产品名称规格:计划量实际量总量
批号调整原由:
主药含量1: %2: %3: %1: %2: %3: %
辅药含量1: %2: %3: %1: %2: %3: %
PH值1:2: 3:1:2: 3:
时限统计超限原有
浓配用时合格数合格率 %应>95%
稀配用时批次白点玻璃屑纤维色块装量轧盖破瓶其他
灌装用时1
灭菌数2
包装箱数3
制表人: 日期:
生产过程:
质量分析:
备注:
大容量注射剂车间日生产统计表
+ +
补加后
灯检岗位统计(瓶)
