2014中考化学复习之化学用语专题
2014年中考化学总复习知识点总结最全的资料

GAGGAGAGGAFFFFAFAF2014年中考化學總復習知識點總結最全的資料基本概念:1、化學變化2、物理變化:沒有生成其它物質的變化3、物理性質:不需要發生化學變化就表現出來的性質((如:顏色、狀態、密度、氣味、熔點、沸點、硬度、水溶性等))4、化學性質:物質在化學變化中表現出來的性質((如:可燃性、助燃性、氧化性、還原性、酸堿性、穩定性等))5、純凈物:由一種物質組成6、混合物:由兩種或兩種以上純凈物組成,各物質都保持原來的性質7、元素:具有相同核电荷数(即质子数)8、原子:是在化學變化中的最小粒子,在化學變化中不可再分9、分子:是保持物質化學性質的最小粒子,在化學變化中可以再分10、單質11、化合物:由不同種元素組成的純凈物12、氧化物:由兩種元素組成的化合物中,其中有一種元素是氧元素GAGGAGAGGAFFFFAFAF13、化學式:用元素符號來表示物質組成的式子14、相對原子質量:以一種碳原子的質量的1/12作為標準,其它原子的質量跟它比較所得的值某原子的相對原子質量= 相對原子質量 ≈ 质子数 + 中子数 (因为原子的质量主要集中在原子核)15、相對分子質量:化學式中各原子的相對原子質量的總和16、離子:帶有電荷的原子或原子團 17、原子的結構:原子、離子的關系:注:在離子里,核電荷數 = 質子數 ≠ 核外電子數18、四種化學反應基本類型:①化合反應: 由兩種或兩種以上物質生成一種物質的反應如:A + B = AB②分解反應:由一種物質生成兩種或兩種以上其它物質的反應如:AB = A + B③置換反應:由一種單質和一種化合物起反應,生成另一種單質和另一(單位為原子原子核外電子中子质子注:在原子里,核電荷數=質陽離陰離原得失失得種化合物的反應如:A + BC = AC + B④復分解反應:由兩種化合物相互交換成分,生成另外兩種化合物的反應如:AB + CD = AD + CB19、還原反應:在反應中,含氧化合物的氧被奪去的反應((不屬于化學的基本反應類型))氧化反應:物质跟氧发生的化学反应(型)緩慢氧化:進行得很慢的,甚至不容易察覺的氧化反應自燃:由緩慢氧化而引起的自發燃燒Mn20、催化劑:在化學變化里能改變其它物質的化學反應速率,而本身的質量和化學性在化學變化前后都沒有變化的物質(注:2H2O2 === 2H2O + O2 ↑此反應MnO2是催化劑)21、質量守恒定律:參加化學反應的各物質的質量總和,等于反應后生成物質的質量總和。
中考化学专题辅导化学用语

化学用语一、化学常见物质的化学式1、单质:H2氢气O2氧气N2氮气C碳P磷S硫Fe铁Cu铜Hg汞2、化合物(1)氧化物:H2O水CO2二氧化碳CO一氧化碳SO2二氧化硫SO3三氧化硫P2O5五氧化二磷Fe2O3氧化铁Fe3O4四氧化三铁CaO氧化钙MgO氧化镁CuO氧化铜ZnO氧化锌FeO氧化亚铁MnO2二氧化锰 Na2O氧化钠(2)酸:HCl盐酸H2SO4硫酸HNO3硝酸H3PO4磷酸H2CO3碳酸H2SO3亚硫酸(3)碱:NaOH氢氧化钠KOH氢氧化钾Ca(OH)2氢氧化钙Ba(OH)2氢氧化钡Cu(OH)2氢氧化铜Fe(OH)3氢氧化铁Fe(OH)2氢氧化亚铁Al(OH)3氢氧化铝Mg(OH)2氢氧化镁(4)盐:NaCl氯化钠Na2CO3碳酸钠ZnCl2氯化锌CaCl2氯化钙KCl氯化钾Na2SO4硫酸钠CuSO4硫酸铜AgCl氯化银FeCl3氯化铁FeCl2氯化亚铁AlCl3氯化铝FeSO4硫酸亚铁Fe2(SO4)3硫酸铁ZnSO4硫酸锌CaCO3碳酸钙BaCl2氯化钡BaSO4硫酸钡KClO3氯酸钾KMnO4高锰酸钾K2MnO4锰酸钾KNO3硝酸钾Cu(NO3)2硝酸铜Hg(NO3)2硝酸汞NH4Cl 氯化铵NH4NO3硝酸铵(NH4)2SO4硫酸铵NH4HCO3碳酸氢铵NaHCO3碳酸氢钠Cu2(OH)2CO3碱式碳酸铜(5)有机物:CH4甲烷C2H5OH乙醇(酒精)CH3OH甲醇CH3COOH乙酸(醋酸)CO(NH2)2尿素,葡萄糖:C6H12O6淀粉:(C6H10O5)n二、常见物质的学名、俗名及化学式三、化学方程式按元素归类总结与氧有关的化学方程式:====2MgO 现象:燃烧、放出大量的热、同时放出耀眼的白光2Mg+O2点燃====SO2 现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激S+O2点燃性气味的气体。
====CO2 现象:生成能够让纯净的石灰水浑浊的气体C+O2点燃====2CO 现象:燃烧现象外,其他现象不明显2C+O2点燃====2P2O5 现象::生成白烟4P+5O2点燃====Fe3O4 现象:剧烈燃烧、火星四射、生成黑色的固体3Fe+2O2点燃====2H2O 现象:淡蓝色的火焰2H2+O2点燃====2H2O+O2↑现象:溶液里冒出大量的气泡2H2O2MnO2====2Hg+O2↑现象:生成银白色的液体金属2HgO△====2KCl+3O2↑现象:生成能让带火星的木条复燃的气体2KClO3MnO2====K2MnO4+MnO2+O2↑现象:同上,2KMnO4△跟氢有关的化学方程式:====2H2O 现象:淡蓝色的火焰2H2+O2点燃Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4 ==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4 ==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成△H2+CuO====Cu+H2O 现象:由黑色的固体变成红色的,同时有水珠生成高温2Fe2O3+3H2 =====2Fe+3H2O 现象:有水珠生成,固体颜色由红色变成银白色跟碳有关的化学方程式:====CO2(氧气充足的情况下) 现象:生成能让纯净的石灰水变浑浊的气体C+O2点燃====2CO(氧气不充足的情况下) 现象:不明显2C+O2点燃高温C+2CuO=====2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成高温3C+2Fe2O3=====4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的气体生成====2CO 现象:黑色固体逐渐减少CO2+C高温3C+2H2O=CH4+2CO 现象:生成的混和气体叫水煤气,都是可以燃烧的气体跟二氧化碳有关的化学方程式:====CO2 现象:生成能使纯净的石灰水变浑浊的气体C+O2点燃Ca(OH)2+CO2===CaCO3↓+H2O 现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2 现象:白色固体逐渐溶解====CaCO3↓+CO2↑+H2O 现象:生成白色的沉淀,同时有能使纯净的石灰水Ca(HCO3) △变浑浊的气体生成====2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石Cu2(OH)2CO3△灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显====CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成CaCO3高温跟一氧化碳有关的,但同时也跟二氧化碳有关:高温Fe3O4+4CO====3Fe+4CO2 现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温FeO+CO===Fe+CO2 现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温Fe2O3+3CO====2Fe+3CO2 现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温CuO+CO====Cu+CO2 现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H2O 现象:不明显HCl+AgNO3==AgCl↓+HNO3 现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O 现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O 现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O 现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O 现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成以上四个反应,盐酸、硫酸都相似,后面两类就不赘述了,读者只需写出配平即可;硝酸一般具有氧化性,所以产物一般不为H2跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O 现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致跟硝酸有关的化学方程式:Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+2HNO3==Cu(NO3)2 +H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O 现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O 现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2 现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl 现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl 现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl 现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl 现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl 现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O 现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O 现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O 现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O 现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O 现象:无明显现象2NaOH+SO2==Na2SO3+H2O 现象:无明显现象跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成BaCl2+Na2CO3==BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于盐酸和硝酸,其实也溶于硫酸,但生成硫酸钡沉淀,不容易看出来跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl 现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2 现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O 现象:生成白色沉淀跟几种金属及其盐有关的化学方程式:铜:CuSO 4•5H 2O △====CuSO 4+5H 2O ↑ 现象:固体由蓝色变为白色高温CuO+CO====Cu+CO 2 现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成△H 2+CuO====Cu+H 2O 现象:固体由黑色逐渐变成红色,同时有水珠生成 Cu+2AgNO 3==Cu (NO 3)2+2Ag 现象:铜表面慢慢生成了银白色金属 CuCl 2+2NaOH==Cu (OH) 2↓+2NaCl 现象:生成了蓝色絮状沉淀 CuO+H 2SO 4==CuSO 4+H 2O 现象:黑色固体溶解,生成蓝色溶液 Cu (OH) 2+H 2SO 4==CuSO 4+2H 2O 现象:蓝色沉淀溶解,生成蓝色溶液 Fe(Zn)+CuSO 4==FeSO 4+Cu 现象:有红色金属生成Cu 2(OH)2CO 3△====2CuO+H 2O+CO 2↑ 现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成 铁:Fe+2HCl==FeCl 2+H 2 现象:铁粉慢慢减少,同时有气体生成,溶液呈浅绿色 FeCl 2+2NaOH==Fe(OH)2↓+NaCl 现象:有白色絮状沉淀生成4Fe(OH)2+O 2+2H 2O==4Fe(OH)3 现象:氢氧化铁在空气中放置一段时间后,会变成红棕色 Fe (OH) 3+3HCl==FeCl 3+3H 2O 现象:红棕色絮状沉淀溶解,溶液呈黄色 Fe (OH) 2+2HCl==FeCl 2+2H 2O 现象:白色絮状沉淀溶解,溶液呈浅绿色 Fe+CuSO 4==FeSO 4+Cu 现象:铁溶解生成红色金属 Fe+AgNO 3==Fe(NO 3)2+Ag 现象:铁溶解生成银白色的金属 Fe 2O 3+6HCl==2FeCl 3+3H 2O 现象:红色固体溶解,生成黄色的溶液23432Fe O Fe O 点燃= 现象:铁剧烈燃烧,火星四射,生成黑色的固体Zn+FeCl2==ZnCl2+Fe 现象:锌粉慢慢溶解,生成铁银:AgNO3+HCl==AgCl↓+HNO3 现象:有白色沉淀生成,且不溶于强酸AgNO3+NaCl==AgCl↓+NaNO3现象:有白色沉淀生成,且不溶于强酸Cu+2AgNO3==Cu(NO3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色的金属生成2AgNO3+Na2SO4==Ag2SO4↓+2NaNO3 现象:有白色沉淀生成。
(人教版)中考化学考点跟踪【第25讲】专题四-化学用语(含答案)

第25讲 专题四 化学用语一、选择题1.(2014,成都)下列化学用语表示正确的是( C )A .2个氢分子-2HB .3个氧原子-O 3C .4个水分子-4H 2OD .5个钠离子-5Na +12.(2013,衡阳)符合以下四位同学所描述的化学式可能是( A )A .H 2OB .O 3C .MgOD .HClO3.(2014,雅安)下列化学符号中的数字表示的意义不正确的是( B )A .NO 2:“2”表示一个二氧化氮分子含有两个氧原子B .2Na :“2”表示两个钠元素C.Mg +2:“+2”表示镁元素的化合价为+2价D .2OH -:“2”表示两个氢氧根离子4.在化学王国里,数字被赋予了丰富的内涵。
对下列化学用语中数字“2”的说法正确的是( C )①2H ②2NH 3 ③SO 2 ④C +2uO ⑤Mg 2+ ⑥2OH - ⑦H 2O A .表示离子个数的是⑤⑥B .表示离子所带电荷数的是④⑤C .表示分子中原子个数的是③⑦D .表示分子个数的是①②5.(2014,福州)某物质的分子模型如图所示,下列说法错误的是( D )A .该物质属于有机物B .该物质的化学式为CH 4C .该物质的1个分子含5个原子D .该物质中碳、氢元素质量比为1∶46.(2013,莱芜)饮料中的果味大多来自酯类。
丁酸乙酯(C 6H 12O 2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂。
关于丁酸乙酯的说法正确的是( D ) A.相对分子质量为116 gB.由20个原子构成C.分子中碳、氢、氧原子的个数比为3∶6∶2D.氢元素质量分数最小7.(2014,连云港)对于下列化学用语,有关说法正确的是( B )①N2②Mg2+③SO2④⑤A.①可表示两个氮原子B.③中硫元素的化合价为+4C.②和⑤均表示阳离子D.④和⑤表示的微粒化学性质相同8.(2013,日照)无色混合气体可能由CH4、H2、CO、CO2和HCl中的某几种气体组成。
化学用语

2014中考化学专题训练1 化学用语A .1 B.2 C .3 D.43、我国南海海底蕴藏着丰富的锰结核——含有锰、铁、铜等金属的矿物。
已知锰原子的质子数为25,相对原子质量为55,则锰原子的电子数为A .25B .30C .55D .804、日常生活中见到的"加碘食盐"、"高钙牛奶"中的"碘、钙"应理解为 A.分子 B.原子 C.离子 D.元素5、下列对于化学式“H 20”的各种表述不正确的是A.表示水这种物质B.表示水分子由氢元素和氧元素组成C.表示1个水分子D.表示1个水分子由2个氢原子和1个氧原子构成 6、元素观是化学的重要观念之一。
下列有关元素的说法错误的是A .物质都是由元素组成的 B.同种元素的原子核内中子数相同 C .在化学变化中元素的种类不发生改变D .元素周期表中原子序数等于该元素原子核内的质子数 7、C 3 N 4是一种新型材料,它的硬度比金刚石还高,可做切割工具。
在C 3N 4中,C 的化合价为+4,则N 的化合价是 A .+5 B .+3 C .+1 D .-38、三甲醚(C 2H 6O)是一种清洁燃料,能替代柴油作车用能源,具有广阔的市场前景。
下列有关二甲醚的说法错误的是A .由C 、H 、O 三种元素组成B .一个分子中含有3个氢分子C .相对分子质量为46D .属于有机化合物 9、下列化学用语与含义相符的是A .MgCl 2——氯化镁B .Ca +2——钙离子 C .2H ——2个氢元素 D .O 2——2个氧原子 10、下列关于二甲醚(C 2H 6O )的说法错误的是A. 由碳、氢、氧三种元素组成B.相对分子质量为46C. —个二甲醚分子中含有9个原子D.碳、氢、氧三种元素的质量比为2 : 6 : 11、下列化学用语表达正确的是 A .钠原子结构示意图:B .硫离子:S —2C .两个氮分子:2ND .氧化铝:Al 2O 312、下列符号表示正确的是A .2个氮分子:2NB .2个碳酸根离子:2CO 32—﹣C .氧化铝元素的化合价:3Al 2O 3 D .4个氢原子:2H 213、对下列符号意义的表述,正确的是A .N 2 两个氮原子B .2H 两个氢元素C .2H 2O 两个水分子D .Ca 2+钙元素的化合价为+2价14、今年央视3.15晚会曝光,少数不法厂家向液化石油气中掺入了二甲醚(C 2H 6O ),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患。
化学中考复习专题化学用语及微观粒子

[键入公司名称]中考复习专题五化学用语及微观粒子化学中考复习(Xi)专题化学用语及微观粒子1、分子的(De)特点分子是(Shi)构成物质的一(Yi)种微粒,大多数(Shu)物质由分子构成。
分子(Zi)是保持物质的化(Hua)学性质的(De)一种微粒。
在化学变化中分子可分,即分子的种类一定发生改变。
2、表示方法:用化学式(分子式)表示。
3、相对大小:用相对分子质量表示。
即组成各元素的原子乘以相对原子质量的总和。
4、分子是由原子构成。
二、原子1、原子的特点原子可以直接构成物质。
如:金属单质、稀有气体、金刚石。
原子是化学变化中的最小微粒。
因为在化学变化中原子不可再分,即原子种类和大小以及质量即质子数和中子数(即原子核)都不变。
2、表示方法:用元素符号表示。
3、相对大小:用相对原子质量表示。
Ar(X)=(一个X原子真实质量/一个碳-12原子真实质量)×124、原子结构:5、原子中的几个等量关系:(1)质子数==核外电子总数==核电荷数注:核电荷数就是原子核所带正电荷的数目。
(2)相对原子质量==质子数 + 中子数。
说明原子的质量主要集中在原子核上。
(3)原子核内质子数不一定等于中子数:普通氢原子的原子核内无中子。
6、原子质量之比等于相对原子质量之比。
三、离子1、粒子的特点离子可以直接构成物质。
例如 NaCl。
离子是带电的原子或原子团。
2、表示方法:用离子符号表示。
3、相对大小:简单离子用相对原子质量表示,原子团离子用相对原子质量之和表示。
4、离子分类:阴离子(带负电的)和阳离子(带正电的)。
5、离子和原子关系:在原子变成离子过程中,原子核不变,即质子数和中子数不变。
四、联系1、分子、原子、离子它们体积很小,质量很小、它们总是在不停运动;同种粒子的化学性质相同,不同种粒子的化学性质不同。
2、分子之间有间隙:一般条件下,气体分子之间间隙最大,液体次之,固体最小。
3、同种分(Fen)子一定构成同一(Yi)种的(De)物质,同种原子可以构成不同(Tong)种的(De)物质。
中考化学 教材知识梳理 小专题(二)化学用语
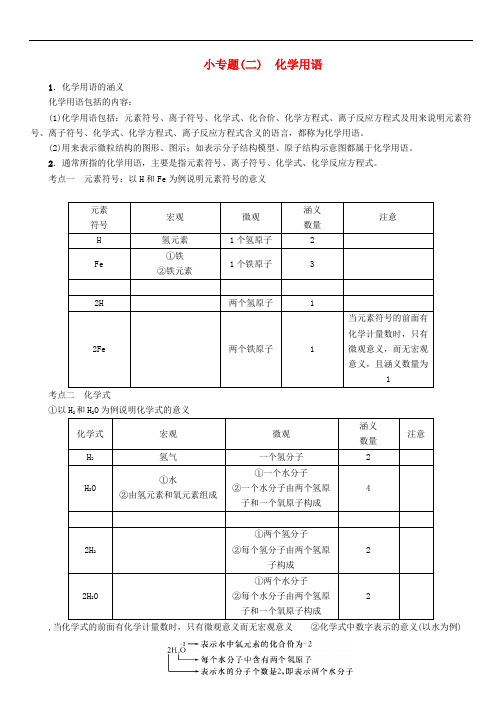
小专题(二) 化学用语1.化学用语的涵义化学用语包括的内容:(1)化学用语包括:元素符号、离子符号、化学式、化合价、化学方程式、离子反应方程式及用来说明元素符号、离子符号、化学式、化学方程式、离子反应方程式含义的语言,都称为化学用语。
(2)用来表示微粒结构的图形、图示;如表示分子结构模型、原子结构示意图都属于化学用语。
2.通常所指的化学用语,主要是指元素符号、离子符号、化学式、化学反应方程式。
考点一元素符号:以H和Fe为例说明元素符号的意义元素符号宏观微观涵义数量注意H 氢元素1个氢原子 2Fe①铁②铁元素1个铁原子 32H 两个氢原子 12Fe 两个铁原子 1 当元素符号的前面有化学计量数时,只有微观意义,而无宏观意义,且涵义数量为1考点二化学式①以H2和H2O为例说明化学式的意义化学式宏观微观涵义数量注意H2氢气一个氢分子 2H2O①水②由氢元素和氧元素组成①一个水分子②一个水分子由两个氢原子和一个氧原子构成42H2①两个氢分子②每个氢分子由两个氢原子构成22H2O①两个水分子②每个水分子由两个氢原子和一个氧原子构成2,当化学式的前面有化学计量数时,只有微观意义而无宏观意义②化学式中数字表示的意义(以水为例)考点三离子符号的意义(以Mg2+、SO2-4为例)考点四结构图、图示、模型和相关意义(常考点) ①原子结构示意图(以镁原子为例)②图示、元素周期表表中表格(以镁为例)考点五化学方程式(必考点)。
中考化学复习学案专题 化学用语
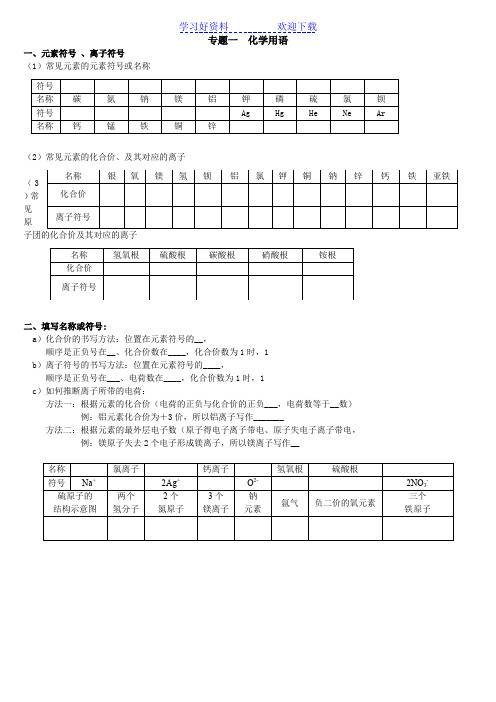
专题一化学用语一、元素符号、离子符号(1)常见元素的元素符号或名称(2)常见元素的化合价、及其对应的离子(3)常见原子团的化合价及其对应的离子二、填写名称或符号:a)化合价的书写方法:位置在元素符号的__,顺序是正负号在__、化合价数在____,化合价数为1时,1b)离子符号的书写方法:位置在元素符号的____,顺序是正负号在___、电荷数在____,化合价数为1时,1c)如何推断离子所带的电荷:方法一:根据元素的化合价(电荷的正负与化合价的正负___,电荷数等于__数)例:铝元素化合价为+3价,所以铝离子写作_______方法二:根据元素的最外层电子数(原子得电子离子带电、原子失电子离子带电,例:镁原子失去2个电子形成镁离子,所以镁离子写作__名称氯离子钙离子氢氧根硫酸根符号Na+2Ag+O2-2NO3-硫原子的结构示意图两个氢分子2个氮原子3个镁离子钠元素氩气负二价的氧元素三个铁原子符号名称碳氮钠镁铝钾磷硫氯钡符号Ag Hg He Ne Ar名称钙锰铁铜锌名称银氧镁氢钡铝氯钾铜钠锌钙铁亚铁化合价离子符号名称氢氧根硫酸根碳酸根硝酸根铵根化合价离子符号三、写出下列化学式的名称:O2N2CuO SO2 CO2CO Fe3O4FeO Fe2O3H2O H2O2NaCl HCl CaCl2FeCl2NH4Cl Cu(OH)2Al(OH)3H2CO3H2SO4 CuSO4Al2(SO4)3CaCO3NaHCO3 AgNO3Cu(NO3)2KMnO4KClO3四、写出下列物质的化学式:氢气氦气氧化汞氧化镁氧化钙氧化钠氧化铝二氧化锰氯化银氯化镁氯化锌氢氧化钙氢氧化钠氢氧化铁硝酸硫酸钠硫酸钡硫酸铁碳酸钠碳酸钡硝酸铝硝酸亚铁乙醇醋酸。
中考化学专题复习:化学用语PPT课件 通用

思路点拨
1.首先要明确表示的是物质、元素、原子、 分子、离子; 2.其次要理解化学符号周围数字的意义; 3.最后提醒:Cu和Ca; Cl和Al; Ag、Mg和Hg;I和l。
化学符号周围数字表示的意义:
表示元素 的化合价
表示微粒(分子/ 原子/离子)个数
R
+ m -
n+ b
一个离子所 带电荷数
一个分子或 原子团中所 含原子个数
阴离子 阳离子
意义和区别 定义 意义 物质变化用语 —— 化学方程式 依据 原则 写法 化学量用语 相对原子质量
相对分子质量
理清关系
理清关系
预习查漏 学生在化学用语习题中常见的问题?
1.用数字和符号填空时,如何减少错误? 2.如何提高分析化学式含义方面的选择题 的正确率? 3.如何分析化学图示(原子结构示意图、 离子结构示意图、微观模型图等)? 4.如何根据给定信息书写化学方程式?
③_______,⑤_______,
⑥_______,⑧_______。
思路点拨
⑴m为核内质子数,决定元素的种类。其数值上 等于原子序数和核电荷数。 ⑵n为最外层电子数,决定元素的化学性质,相等 时化学性质相似。 ⑶里外相等是原子,里外不等是离子; 里大外小阳离子,里小外大阴离子。 ⑷化合价的数值一般和离子所带电荷数目相同, 正负也相同。
即时突破
4.请仔细观察分析,回答下列问题: ⑴上述粒子中: ①只有一个电子层的是___(填序号,下同) ②电子层数最多的是___; ③核内质子数最多的原子是____; ④属于同一种元素的是______;
即时突破
1.(2014•泰州)下列化学用语书写正确的 是( )
A.钴元素CO
C.铵根离子NH4+
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三讲化学用语2014/3/28 1.下列试剂瓶标签上的化学式书写错误的是
A B C D
2.《美国化学会杂志》报道了中国科学家以二氧化碳和钠在一定条件下制得金刚石,其化学方程式为
2X+C(金刚石)。
则X的化学式为
3C02+4Na ℃470
80MPa
A.Na202 B.Na2CO3 C.Na2O D.Na4C206
3.芬太奴是强有力的麻醉剂,在军事上作为“非致命武器”曾被用作解救人质,其化学式为C20H24N2O,下列关于芬太奴的说法中不正确的是
A.芬太奴的每一个分子中含有47个原子
B.芬太奴是由碳、氢、氮、氧四种元素组成的物质
C.一个芬太奴分子中含有一个氮气分子
D.芬太奴中碳、氢、氮、氧元素的质量比为60:6:7:4
4.以二氧化锡(SnO2)为敏感材料制成的“气-电”转换器,可用于对有害气体的监测。
SnO2中Sn的化合价为
A.-4 B.+4C.+3D.+2
5.下列反应的化学方程式中,书写正确的是
A.电解水 H2O == H2 +O2
B.铁和稀盐酸的反应 2Fe + 6HCl == 2FeCl3 + 3H2↑
C.实验室制二氧化碳 CaCO3 + H2SO4==CaSO4 + CO2↑+ H2O
D.氢氧化钠溶液与稀硫酸的反应 2NaOH + H2SO4 == Na2SO4 + 2H2O
6.物质X是一种重要的阻燃剂。
工业上用三氧化二锑(Sb2O3)生产X的化学方程式为:
Sb2O3+2H2O2====X+2H2O。
根据质量守恒定律,推断X的化学式为
A.SbO2 B.Sb2O5 C.HSbO3 D.H3SbO4
7. 由+5价氮元素和-2价氧元素组成的化合物是()
A.N5O2
B.NO
C.NO2
D.N2O5
8.下列四个化学反应中,符合图中漫画情景的是
A. Zn+CuCl2==ZnCl2+Cu B.Fe203+3CO==2Fe+3CO2
C.2CuO+C== 2Cu十CO2↑ D.Fe+H2SO4==FeSO4+H2↑
9.“NaCl+CO 2+NH 3+H 2O=NaHCO 3↓+NH 4Cl ”是著名的“侯氏制碱法”的重要反应。
下面是4位同学对该反应涉及的有关知识发表的部分见解。
其中不正确...的是
A B C D
10.下列化学方程式正确的是
A .铁屑溶于稀硫酸:
2Fe+3H 2SO 4= Fe 2(SO 4)3+3H 2↑ B .食盐溶于硝酸钾溶液:NaCl+KNO 3=NaNO 3+KCl
C .木炭在不充足的氧气中燃烧:2C+O 2 2CO
D .过氧化氢分解:H 2O ↑+O 2↑ 11.下列化常用语中,正确的是
A .2年氮分子—2N
B .氢氧化铁的化学式—Fe(OH)2
C .H 2O 2中氧元素的化合价为-2价
D .加热高锰酸钾和二氧化锰混合物制氧气的化学方程式:2KClO 3=2KCl+3O 2 12.“齐二药”假药事件是将“二甘醇”用于药品生产造成的。
“二甘醇”在人体内可发生如下反应:C 4H 10O 3+4O 2=2X+3H 2O ,而导致人中毒。
X 的化学式为 A.C 4H 4O 8 B.C 2H 4O 4 C.C 2H 2O 2 D.C 2H 2O 4 13.下列化学方程式的书写不正确...的是 A.CaCO 高温CaO+CO 2↑ B.2KMnO 4 △ K 2MnO 4+MnO 2+O 2↑ C.Al+O 点燃Al 2O 3 D.CO 2+Ca(OH)2=CaCO 3↓+H 2O
14.二氧化铅(PbO 2)中铅元素的化合价是
A .-2
B .+1
C .+2
D . +4
15.下面是某学生学完化学用语后的一次练习的部分内容,其中不正确的是
A.2MnO 42-:表示2个高锰酸根离子
B.维生素C (C 6H 8O 6):表示该物质由三种元素组成,该分子中含20个原子
C.Ar :可表示1个氩分子由1个氩原子构成
D.2O :表示2个氧原子
16. 达菲(化学式为C 16H 28N 2O 4·H 3PO 4)是世界卫生组织推荐的抗禽流感药物。
下列有关的说法正确的是 A.达菲属于氧化物
B.达菲由碳、氢、氮、氧、磷五种元素组成
C.达菲分子中碳、氮、磷元素的质量比为16∶2∶1
D.达菲分子由碳原子、氢原子、四氧化二氮分子和磷酸分子构成
17.硝酸可发生如下反应:4 HNO 3
加热 或光照
4 NO 2↑↑+ 2H 2O 。
据此我能回答:
⑴ 中物质的化学式为 。
点燃
⑵我还可从不同角度分析,获得对HNO3的下列认识:
从组成上,;
从性质上,;
从贮存上,……
18.在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下:
⑴这一反应类型是反应;= g
由表中数据分析可知,B可能没有参加该化学反应,也可能是该反应的剂。
⑵写出一例与上述反应类型
....相同的化学方程式:。
19.只用Ca、C、O、Cl、H五种元素的一种或几种,按要求填空:
(1)各写出一个化学式:
①氧化物__________②酸__________③碱__________④盐__________
(2)各写出一个化学方程式:
①分解反应__________________________________________________
②复分解反应________________________________________________
20.(2006海南)从化学方程式2H2O22O +O2↑中,你能知道什么?(至少写出四点)
参考答案:
1.B
2.B
3.C
4.B
5.D
6.B
7.D
8.A
9.C10.C11.B12.D13.C14.D15.A16.B17.略18.⑴化合 5 催化
⑵ C+O2点燃
CO2【或 2Mg+O2
点燃
2MgO 或CO2 + H2O====H2CO3;
或CaO + H2O ==== Ca(OH)2……】
19.本题有多种可能答案,只要符合要求,且不超出所给5种元素,均按相关化学用语评分要求进行评分.举例答案:
(1)①CaO②HC l③Ca(OH)2④CaCl2
(2)①2H2O通电2H2↑+O2↑
②CaCO3+2HCl=CaCl2+ H2O+CO2↑
20.(1)反应物是H2O2(2)生成物是H2O 和O2(3)反应条件是用MnO2作催化剂(4)该反应属于分解反应(5)反应前后各元素种类不变(6)反应前后质量守恒(7)反应前后原子个数不变(8)反应物与生成物之间的质量比为 H2O2∶H2O ∶O2 =68∶36∶32(符合题意均可)。
