初三化学计算题及答案
九年级化学化学计算题题20套(带答案)及解析
九年级化学化学计算题题20套(带答案)及解析一、中考化学计算题1.小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。
请计算:第一次第二次第三次第四次加入澄清石灰水100100100100的质量/g生成沉淀的质量0.4m 1.0 1.0/g(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
【答案】0.8 10.6%【解析】【分析】第一次生成沉淀0.4g,而第三次不到0.4g的3倍,则第二次应该为0.4g的二倍,所以m=0.4g×2=0.8g,根据碳酸钙的质量和对应的化学方程式求算碳酸钠溶液中溶质的质量分数。
【详解】由分析可知,m=0.4g×2=0.8g设原Na2CO3溶液中溶质的质量分数为x。
106100=10g?x 1.0gx=10.6%答:(1)表中的m的值为 0.8。
(2)原Na2CO3溶液中溶质的质量分数是10.6%。
2.将含有杂质(不溶于水)的氯化钡样品12.5g放入39.6g水中充分搅拌,完全溶解后过滤。
取20g滤液与足量的稀硫酸完全反应,得到4.66g沉淀。
请计算:①配制的氯化钡溶液中溶质的质量分数。
②样品中氯化钡的质量分数。
【答案】20.8%;83.2%【解析】【详解】①设参加反应的氯化钡的质量为x 。
2244BaCl +H SO =BaSO +2H 208233x4Cl.66g208233=x 4.66gx= 4.16g则配制的氯化钡溶液中溶质的质量分数为 :4.16g20g×100%=20.8% ②由于20g 溶液中含有4.16g 氯化钡,则可设样品中氯化钡的质量为y 。
则4.16g y=20g-4.16g 39.6gy=10.4g样品中氯化钡的质量分数为:10.4g12.5g×100%=83.2%答:①氯化钡溶液中溶质的质量分数为20.8% ②样品中氯化钡的质量分数为83.2%。
(完整版)初三化学计算题及答案

初三化学计算题1 .用氯酸钾和二氧化镒的混合物16g,加热制取氧气,待完全反应,冷却后称量,得到11. 2g固体物质,计算原混合物中二氧化镒的质量(计算结果保留二位小数)。
2. 刘彬同学的姑父从三峡搬迁到我们家乡后,准备兴建一座碳酸钙精粉厂。
为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品(杂质不参加反应)与19g稀盐酸恰好完全反应,测得残留物为22.8g。
求:(1)依据质量守恒定律,生成二氧化碳g;(2)样品中碳酸钙的质量分数;(3)所用稀盐酸溶液中溶质的质量分数。
3、某工厂的废料中含铁和铜,需回收此废料中的铜.现取铁和铜的混合物样品10g,向其中加入废弃的稀硫酸50g恰好完全反应,产生0. 1gH2o求:①废料中铜的质量分数。
②废弃稀硫酸中硫酸的质量分数。
7.取碳酸钠和氯化钠的固体混合物13, 6g,与质量为73g的稀盐酸恰好完全反应?产生二氧化碳气体的质量为4. 4g,计算:(1)固体混合物中碳酸钠的质量(2)该稀盐酸中溶质的质量分数(3)反应所得的溶液中溶质的质量分数(最后结果保留一位小数)9. (6分)小华想测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器。
(1)你认为能测出其铜的质量分数的是合金;(2)小华取该合金的粉末32.5g,与足量该盐酸充分反应,经测定,产生了0.4g气体请求出该合金中铜的质量分数。
(3)若想测出该盐酸的质量分数,你认为实验时必须提供和测出的数据是(选填序号)。
A .参加反应的合金质量B .参加反应的稀盐酸的质量C.参加反应的稀盐酸的体积和密度D.产生气体的质量17、(本题要求写出计算过程)将1.80g不纯的氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,过滤后得到溶质质量分数为20.0%的溶液5.85g o求:(1)样品中氯化铜的质量分数(2)加入氢氧化钠溶液的质量。
答案:1.解:设原混合物中KC1O3质量为x,依题意可知完全反应后生成氧气的质量为:16g-11. 2g=4. 8g (1 分)MnO2由2KClO3=====2KCl+3O2 f (1 分)△2.443. (5分)(1)解:设质量为x的这种稀硫酸可与4.0gCuO恰好完全反应CuO + H2SO4 = CuSO4 + H2O (2 分)80 984.0g 10% x= (1 分)x = 49g (1 分)答:完全溶解这些固体产物至少需要溶质质量分数为10%的稀硫酸49g o(2) Cu2S (1 分)7.设碳酸钠的质量为,参加反应的氯化氢的质量为,反应生成的氯化钠质量为Na2CO3+2HCl = 2NaCl+H2O+CO2 f106 73 117 44x y z 4. 4g=10. 6g=7. 3g=11.7g盐酸中溶质质量分数:7. 3g x l00%= 10%最后得到的溶液中溶质质量为:(13 . 6g- 10. 6g)+ 11. 7g=14. 7g最后得到的溶液的质量为:13. 6g+ 73g-4. 4g=82.2g最后得到的溶液中溶质质量分数为:答:固体混合物中碳酸钠的质量为10. 68,该盐酸中溶质的质量分数为10%,所得到的氯化钠溶液的质量分数为17. 9%。
初三化学化学计算题题20套(带答案)含解析

初三化学化学计算题题20套(带答案)含解析一、中考化学计算题1.我市东部山区盛产石灰石,某校课外活动小组为了解石灰石资源的品质,采用两种方案对当地石材进行化学分析:方案一: 取10g 石灰石粉末样品置于下图所示装置,充分加热至质量恒定,冷却后称得固体质量为8.12g方案二:另取10g 同质地石灰石颗粒样品,置于烧杯中加足量稀盐酸,充分反应后称得混合物的总质量减少了4.27g相关资料:当地石灰石含有的主要杂技为二氧化硅,其化学性质稳定,加热不易分解且不与盐酸发生化学反应.计算出两种方案测得的石灰石中碳酸钙的质量分数:(1)方案一中碳酸钙的质量分数是_______________________;(2)方案二中碳酸钙的质量分数是_______________________.(精确到0.1%)比较两方案测量的结果,分析两方案误差较大的可能原因?______【答案】42.7% 97% 石灰石分解需要高温,两方案误差较大的原因可能是酒精灯火焰温度偏低,石灰石粉末未能充分分解,引起误差较大.【解析】【分析】【详解】(1)生成二氧化碳的质量为10g-8.12g=1.88g设生成1.88g 二氧化碳需碳酸钙的质量为x32CaCO CaO +10044x 1.88CO g高温 10044=x 1.88gx=4.27g石灰石样品中碳酸钙的质量分数为4.27g100%=42.7% 10g⨯(2)混合物的总质量减少了4.27g说明生成了4.27g二氧化碳设样品中的碳酸钙的质量为y3222CaCO+2HCl=CaCl+H O+CO10044y 4.27g↑10044=y 4.27gy=9.7g石灰石样品中碳酸钙的质量分数为9.7g100%=97% 10g⨯石灰石分解需要高温,两方案误差较大的原因可能是酒精灯火焰温度偏低,石灰石粉末未能充分分解,引起误差较大。
2.我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
初中化学计算题大全(含答案及解析)

2024年中考化学《必考经典》计算题大全(含答案及解析)1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
3.取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配成溶液,然后向其中滴加溶质质量分数为7.3%稀盐酸,直至恰好反应,共消耗稀盐酸50g。
初中化学计算题100题含答案

初中化学计算题100题含答案
1、一块铝热量发生变化时所放出的热量为?
答案:Q=m·C·ΔT
2、一次反应所需的能量是多少?
答案:ΔH=Hf-Hi
3、一克硝酸钠可与多少毫升水反应?
答案:1克硝酸钠可与25毫升水反应。
4、一克重氢氧化钠在室温时最多可溶解多少克水?
答案:一克重氢氧化钠在室温时最多可溶解5.6克水。
5、1 mol酸能把多少ml水搞碱?
答案:1 mol酸能把1000ml水搞碱。
6、醋酸的PH值是多少?
答案:醋酸的PH值为2.4
7、H2SO4形成的水溶液中,氢离子的浓度是多少?
答案:H2SO4形成的水溶液中,氢离子的浓度为1 mol/L。
8、浓硫酸中含有多少原子硫?
答案:浓硫酸中含有2个原子硫。
9、一克CuSO4能溶解多少克水?
答案:一克CuSO4能溶解37.2克水。
10、氢化钠可与100g水反应吗?
答案:可以,氢化钠可与100g水反应。
九年级化学化学计算题专项训练100(附答案)含解析

56
152 64
m
n 3.2g
m = 56 m=2.8g, 3.2g 64
n = 152 n=7.6g, 3.2g 64
滤液 a 的质量=125g-(3.2g-2.8g)=124.6g;滤液 b 的质量=98g+5.6g-0.2g=103.4g;若将滤液 a 和 b 倒入同一烧杯并得到溶质质量分数为 8%的溶液,加水的质量=(15.2g+7.6g) 8%(124.6g+103.4g)=57g; (4)参加反应 10%稀硫酸的质量=9.8g 10%=98g,用 98%的浓硫酸配制 98g10%稀硫酸, 需加水的质量=98g-9.8g 98%=88g,即 88mL; (5)过滤操作需要用到的基本仪器有:铁架台、烧杯、玻璃棒和漏斗;在漏斗内放滤纸制 作过滤器。 【点睛】 在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解答。
(l)原固体混合物中碳酸钠的质量分数 4.8g÷
=10.6g;混合物中碳酸钠的质量
分数为 10.6g÷12.6g×100%≈84.1%; (2)设盐酸中溶质的质量为 x,生成二氧化碳质量为 y
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
106 73
44
10.6g x
y
106 = 73 = 44 10.6g x y
(3)用同浓度的硫酸,与一瓶未变质、部分变质、或全部变质(杂质都是 Na2CO3)的烧碱样品 反应,需要硫酸的质量都相等.其原因是:__(从钠元素质量守恒的角度解释).
y=
44 9.0g 混合物中的碳酸钙质量为 9.0g× 5 =7.5g
6 所以 100 (4.0g-m) +m=7.5g,m=1.25g。
九年级化学化学计算题题20套(带答案)含解析
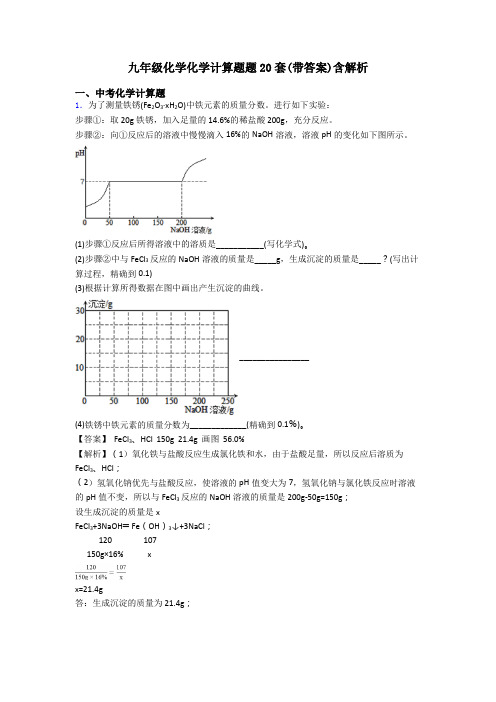
九年级化学化学计算题题20套(带答案)含解析一、中考化学计算题1.为了测量铁锈(Fe2O3·xH2O)中铁元素的质量分数。
进行如下实验:步骤①:取20g铁锈,加入足量的14.6%的稀盐酸200g,充分反应。
步骤②:向①反应后的溶液中慢慢滴入16%的NaOH溶液,溶液pH的变化如下图所示。
(1)步骤①反应后所得溶液中的溶质是___________(写化学式)。
(2)步骤②中与FeCl3反应的NaOH溶液的质量是_____g,生成沉淀的质量是_____?(写出计算过程,精确到0.1)(3)根据计算所得数据在图中画出产生沉淀的曲线。
________________(4)铁锈中铁元素的质量分数为_____________(精确到0.1%)。
【答案】 FeCl3、HCl 150g 21.4g 画图 56.0%【解析】(1)氧化铁与盐酸反应生成氯化铁和水,由于盐酸足量,所以反应后溶质为FeCl3、HCl;(2)氢氧化钠优先与盐酸反应,使溶液的pH值变大为7,氢氧化钠与氯化铁反应时溶液的pH值不变,所以与FeCl3反应的NaOH溶液的质量是200g-50g=150g;设生成沉淀的质量是xFeCl3+3NaOH═Fe(OH)3↓+3NaCl;120 107150g×16% xx=21.4g答:生成沉淀的质量为21.4g;(3)所以产生沉淀的曲线为;(4)所以铁锈中铁的质量分数为 =56%。
2.某化学兴趣小组对某铜锌合金样品进行探究实验,称取样品10.0 g,再用100.0 g稀硫酸溶液逐滴滴入,实验情况如图所示。
求:(1)铜锌合金中,Zn的质量分数是________。
(2)所用稀硫酸溶液中溶质的质量分数是__________?【答案】65% 19.6%【解析】试题分析:(1)铜锌合金与稀硫酸反应,其中只有锌与硫酸反应,故固体减少的量即为锌的质量=10g-3.5g=6.5g,则Zn%=6.5g/10g×100%=65%(2)解:设所用稀硫酸中溶质的质量分数为xZn+H2SO4=ZnSO4+H2↑65 986.5g 50gx65/98=6.5g/50gxx=19.6%答:锌的质量是65%;所用稀硫酸中溶质的质量分数为19.6%考点:合金、化学方程式计算3.某炼铝工厂想测定铝土矿中A12O3的含量,将矿石粉碎(其中杂质不溶于水,不与酸反应,且不含铝元素),进行如下实验,第一步反应的物质质量关系如坐标图所示:(1)上述实验过程中发生反应的化学方程式是_____;(2)根据已知条件列出求解第一步实验铝土矿中参加反应的A12O 3质量(x)的比例式_____ (3)铝土矿样品中A12O 3的含量_____;(4)坐标图中B 点所示溶液中溶质的化学式是_____;(5)在第二步实验结束后所得溶液中溶质的质量分数是_____(6)用1700t 此铝土矿冶炼得到540t 的铝,则在冶炼中,铝土矿的利用率是_____。
初中化学计算题(带答案)

初中化学计算题一、根据化学式的计算1、计算相对分子质量相对分子质量=化学式中各原子的相对原子质量的总和。
点拨:①计算物质的相对分子质量时,同种元素的相对原子质量与其原子个数是相乘的关系,不同种元素相对质量是相加的关系。
②计算结晶水合物的相对分子质量时,化学式中的“·”表示相加,而不表示相乘。
③化学式中原子团(或根)右下角的数字表示的是原子团(或根)的个数。
计算时先求一个原子团或根的总相对原子质量,再乘以原子团(或根)的个数,即得出几个原子团的总相对原子质量。
2、计算物质中各元素的质量比组成化合物的各元素的质量比=化合物中各元素的相对原子质量总和(即相对原子质量与原子个数乘积)之比。
点拨:①计算时一定要写清楚各元素质量比顺序,因顺序不同,比值也不同。
②计算时的结果约成最简整数比。
3、计算物质中某元素的质量分数化合物中某元素的质量×100%4、已知某化合物的质量,求某元素的质量化合物里某元素的质量=化合物的质量×化合物中某元素的质量分数化合物的质量=化合物中已知元素的质量÷化合物中已知元素的质量分数5、求化学式点拨:求物质化学式的主要类型:①由元素的相对原子质量和化合物的相对分子质量,确定化学式。
②根据化合物中某元素质量分数确定化合物的化学式。
③已知化合物中元素的质量比和相对原子质量,确定化学式。
原子个数比=元素的质量比:相对原子质量比④根据质量守恒定律确定化学式。
6、计算不纯物中某元素(或某纯净物)的质量分数计算公式:①某纯净物的质量分数= ×100%②不纯物中某元素的质量分数=不纯物中纯净物的质量分数×该纯净物中某元素的质量分数。
③某纯净物的质量分数=实际上某元素的质量分数÷化学式中该元素的质量分数×100%二、根据化学方程式的计算根据化学方程式的计算就是从量的方面来研究物质变化的一种重要的方法,其计算步骤和方法,一般分为以下几步: ①设未知量,未知量不带单位,常用X 表示.②根据题意确定反应物与生成物,写出并配平反应的化学方程式. ③在有关物质化学式下面写出相对分子质量并代入已知量和所设未知量. ④列比例式求解,写出答案.在初中阶段,根据化学方程式的计算,主要有以下几种基本类型.(1)根据化学方程式计算反应物、生成物间的质量比反应物、生成物间的质量比,就是各反应物、生成物相对分子质量×计量数之比. (2)根据化学方程式计算反应物或生成物的质量反应物或生成物质量的计算,一般是根据化学方程式中各反应物、生成物间的质量比来求算的,对某些反应,可直接依据质量守恒定律进行计算.(3)根据化学方程式进行含有一定且杂质的反应物或生成物的计算根据化学方程式的计算,其反应物或生成物的质量必须是纯物质的质量.含有一定量杂质的反应物或生成物的质量,必须换算成纯物质的质量,才能按根据化学方程式的计算步骤和方法进行计算.纯物质质量=含有一定量杂质的物质质量×该物质质量分数三、有要溶液组成的计算1.用溶质所占溶液的质量分数表示溶液的组成,其关系如下:溶质的质量分数= 溶质质量溶质+溶剂 × 100%=溶液质量溶质质量 × 100%在饱和溶液中: 溶质的质量分数=+溶解度溶解度g 100 × 100%2、有关溶液加水稀释的计算在溶液加水稀释过程中,溶质的质量分数将随溶液的稀释而改变,溶质质量分数一定的溶液加水稀释,稀释前后溶质的总质量不会发生改变.溶液加水稀释的计算,根据的就是这个道理.M 浓溶液×浓溶液的溶质质量分数=M 稀溶液×稀溶液的溶质质量分数 =(M 浓溶液+M 水)×稀溶液的溶质质量分数 3、溶质的质量分数在化学方程式的应用反应后溶液的质量=反应物的总质量(包含溶液的质量)-生成气体或沉淀的质量四、综合计算题分类解析从近几年全国各地的中考化学试题来看,化学计算已经走出了“为计算而计算”的考查误区,考题所涉及的内容更加注重与日常生活、工农业生产的联系;更加注重对同学们图表、数据、信息、实验综合分析能力的考查。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.用氯酸钾和二氧化锰的混合物16g,加热制取氧气,待完全反应,冷却后称量,得到11.2g固体物质,计算原混合物中二氧化锰的质量(计算结果保留二位小数)。
2.刘彬同学的姑父从三峡搬迁到我们家乡后,准备兴建一座碳酸钙精粉厂。
为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品(杂质不参加反应)与19g稀盐酸恰好完全反应,测得残留物为22.8g。
求:(1)依椐质量守恒定律,生成二氧化碳 g;(2)样品中碳酸钙的质量分数;(3)所用稀盐酸溶液中溶质的质量分数。
3.(5分)由硫元素和铜元素组成的一种化合物(硫化物)4.0g,高温条件下在空气中充分煅烧,只得到气体SO2和4.0g固体CuO 。
(1)要使煅烧后的固体CuO完全溶解,可加入适量稀硫酸。
计算至少需要溶质质量分数为10%的稀硫酸多少克?(要求写出计算所需的化学方程式)(2)运用所学知识和上述数据进行分析,这种硫化物的化学式为。
(2)某工厂的废料中含铁和铜,需回收此废料中的铜.现取铁和铜的混合物样品l0g,向其中加入废弃的稀硫酸50g恰好完全反应,产生0.1gH2。
求:①废料中铜的质量分数。
②废弃稀硫酸中硫酸的质量分数。
5.侯德榜是我国著名的化学家。
由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠。
现取仅含氯化钠杂质的纯碱样品33.2g,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g。
求:(1)该纯碱样品中Na2CO3的质量;(2)反应后所得溶液中溶质的质量分数。
6.(10分)某矿井采出的食盐(俗称井盐)中含有CaCl2,为设计除杂方案需测定CaCl2的含量;取上述井盐22.8g,向其中加入100g质量分数为10.69%的Na2CO3溶液恰好完全反应。
若样品检测过程在露℃的恒温下进行,此时NaCl 的溶解度为36g。
(1)取样检测后的溶液中,Na+与Cl-的数量比为。
(2)求检测后的溶液中NaCl的质量及井盐中CaCl2的质量分数(结果保留一位小数)。
(3)请通过相关计算判断,取样检测后的溶液是否为t℃时的NaCl饱和溶液?7.取碳酸钠和氯化钠的固体混合物13,6g,与质量为73g的稀盐酸恰好完全反应,产生二氧化碳气体的质量为4.4g,计算:(1)固体混合物中碳酸钠的质量(2)该稀盐酸中溶质的质量分数(3)反应所得的溶液中溶质的质量分数(最后结果保留一位小数)8.(4分) 啤酒、红酒和白酒中都含有乙醇(C2H5OH),饮酒后乙醇可进入人体血液中,科学实验表明,当乙醇在人体血液中的含量超过80mg /100mL血(每100mL血中含有80mg乙醇)时,便会影响人的驾车或操作机器的能力;已知饮用某啤酒1大杯(0.56L),会使血液中乙醇含量升高30mg/100mL血。
回答下列问题:(1)乙醇中含有________种元素。
(2)乙醇分子中碳、氢、氧原子的个数比是_____________。
(3)李明饮用了3大杯上述啤酒后,其体内每100mL血液中乙醇的含量(理论上)升高__________mg,____________(填影响或不影响)其驾车或操作机器的能力。
9.(6分) 小华想测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀盐酸和必要的仪器。
(1)你认为能测出其铜的质量分数的是____________合金;(2)小华取该合金的粉末32.5g,与足量该盐酸充分反应,经测定,产生了0.4g气体请求出该合金中铜的质量分数。
(3)若想测出该盐酸的质量分数,你认为实验时必须提供和测出的数据是_________(选填序号)。
A.参加反应的合金质量B.参加反应的稀盐酸的质量C.参加反应的稀盐酸的体积和密度D.产生气体的质量10.(6分)欲使6.5g锌跟20%的稀硫酸完全反应,需要这种稀硫酸多少克?11.(5分)游泳池常用硫酸铜溶液进行杀菌消毒。
某游泳池现需含铜4%的硫酸铜溶液消毒,试求这种溶液中溶质的质量分数?12.(6分)把12.5g含杂质20%的大理石放人盛有34.4g稀盐酸的烧杯中,恰好完全反应,反应后烧杯中物质的总质量比反应前减少了4.4g。
求反应后所得溶液中溶质的质量分数。
(大理石中的杂质不与酸反应,也不溶于水)13.(2分)用KCl和KH2PO4固体配制钾元素、磷元素、水的质量比为78:3l:10000的植物生长营养液,所耗用的KCl和KH2PO4的质量比为。
14.(4分)(1)尿素是一种常用氮肥,其化学式为CO(NH2)2。
尿素由种元素组成,其相对分子质量为--。
小林家中有一块稻田,需施15 kg尿素,他到农资公司去购买,由于尿素售完,他需购硝酸铵(化学式NH4NO3)代替尿素.他应购的硝酸铵的质量为 kg。
(2)用2%的NaOH溶液给禽舍消毒能有效杀灭”禽流感”病毒。
要配制2L2%R NaOH溶液(密度1kg/L).需NaOH的质量为 g。
15.(5分)制取22吨二氧化碳,需煅烧含碳酸钙80%的石灰石多少吨?16、据Science, Vol 303, Issue 5660, 993-997 , 13 February 2004报道:以铑的化合物为催化剂,乙醇与水的混合物部分氧化可有效地生产出氢气,同时得到另一副产物X,反应的化学方程式是2C2H5OH + 4H2O + O2 == 4X + 10H2 则X的化学式是。
乙醇的相对分子质量是;乙醇分子中氢原子的质量分数是。
17、(本题要求写出计算过程)将1.80g不纯的氯化铜样品(杂质不溶于水,也不参加反应)跟一定量的氢氧化钠溶液恰好完全反应,过滤后得到溶质质量分数为20.0%的溶液5.85g。
求:(1)样品中氯化铜的质量分数(2)加入氢氧化钠溶液的质量。
18.实验室配制300g质量分数为10%的氢氧化钠溶液,需氢氧化钠 g,水 g。
19.将一定量的石灰石放人烧杯中,加入100g稀酸恰好完全反应(杂质不溶解,也不参加反应),此时,烧杯中物质的总质量比反应前减少了8.8g,则石灰石中碳酸钙的质量为 g,所用盐酸的溶质质量分数为。
20.(1)(2分)计算碳酸氢铵(NH4HCO。
)中氮元素的质量分数。
(计算结果精确到O.1)21.(4分)盐酸和氯化坝的混合溶液40g,其中盐酸的溶质质量分数为10%.向混合溶液中加入9%的硫酸溶液20g恰好完全反应。
计算:(1)生成沉淀的质量是多少克?(2)反应后所得溶液中盐酸的质量分数。
(计算结果精确到O.1)22.(4分)油炸食品,烧烤食品等被营养专家称作“垃圾食品”,这是因为在制作过程中不仅产生大量有害气体污染环境,而且食物中还会产生一些强致癌物质,故此类食品不易多吃、常吃。
如在食物的煎炸过程中会产生一种有害物质一丙烯醛。
化学式为C2H3CH0。
试回答:(1)丙烯醛的相对分子质量是。
(2)丙烯醛中氧元素的质量分数为 (结果保留一位小数)。
(3)112g丙烯醛中碳元素的质量为。
23.(8分)我省盛产石灰石,其中含有的杂质为二氧化硅(不溶于水、高温下难以分解的酸性氧化物)。
S中学初三化学研究性学习小组的同学为了测定某矿山石灰石的纯度,取2.Og该矿山石灰石样品,将20.Og盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表。
试求。
(1)2.Og石灰石样品中杂质的质量。
(2)石灰石样品中碳酸钙的质量分数。
(3)加入的盐酸中溶质的质量分数是多少?次数1234加入盐酸质量/g5.O5.O5.O5.O剩余固体质量/g1.3O.6O.20.224.(2分)近几年脑黄金(DHA)成为人们研究的热点之一。
脑黄金在医药、食品等行业中应用前景非常广阔,脑黄金的化学式为C25H51COOH,试计算:(1)脑黄金中碳、氢、氧元素的最简质量比等到于。
(2)脑黄金中氧元素的质量分数为(精确到0.1%)25、(5分)纯铜呈紫红色,故又称紫铜。
而铜的合金有黄铜、青铜和白铜等。
其中Cu与Zn的合金称黄铜。
黄铜有优良的导热性和耐腐蚀性,可用作各种仪器零件。
为了测定某黄铜样品中铜的质量分数,取20克该黄铜样品加入到50克稀硫酸中,恰好完全反应,产生气体0.2克。
反应的化学方程式为:Zn + H2S04 == ZnS04 + H2↑。
试求:(1)该黄铜样品中铜的质量分数。
(2)原稀硫酸溶液中溶质质量分数。
参考答案1.解:设原混合物中KClO3质量为x,依题意可知完全反应后生成氧气的质量为:16g-11.2g=4.8g(1分)MnO2由 2KClO3=====2KCl+3O2↑(1分)△2.443.(5分)(1)解:设质量为x的这种稀硫酸可与4.0gCuO恰好完全反应CuO +H2SO4=CuSO4+H2O80 984.0g 10% xx=49g答:完全溶解这些固体产物至少需要溶质质量分数为10%的稀硫酸49g 。
(2)Cu2S(1分)4.(1)142;36:3:32(或72:6:64)(2)解:设废料中铁的质量为x,稀硫酸中H2SO4的质量为yFe+H2SO4=FeSO4+H2↑56 98 2x y 0.1gx=2.8gy=4.9g铜的质量分数为:=72%稀硫酸的质量分数为:9.8%答;略5.解;设样品中含Na2CO3的质量为x,生成NaCl的质量为y,依题意知产生CO2的质量为33.2g+130g-150g=13.2g。
则:Na2CO3+2HCl=2NaCl+CO2↑=H2O106 117 44x y 13.2gx=31.8gy=35.1g原样品中含NaCl 33.2g-31.8g=1.4g答:该纯碱样品中Na2CO3为31.8g,所得溶液中溶质的质量分数为24.3%。
6.(1)1:1(2)所设取样品中CaCl2的质量为x,反应生成NaCl的质量为yCaCl2+Na2CO3=CaCO3↓+2NaCl1l1 106 117x 100g×10.6% y11.1g11.7g则m(NaCl)=(22.8-11.1g)+11.7g=23.4gω(CaCl2)==48.7%(3)溶液中水的质量:100g×(100%-10.6%)=89.4g设t℃时89.4g水中NaCl的最大溶解量为m则100g:36g=89.4g:mm===32.2g>23.4g故样品检测后的溶液不是t℃时的NaCl饱和溶液7.设碳酸钠的质量为,参加反应的氯化氢的质量为,反应生成的氯化钠质量为Na2CO3+2HCl=2NaCl+H2O+CO2↑106 73 117 44x y z 4.4g=l0.6g=7.3g=11.7g盐酸中溶质质量分数:7.3g×l00%=10%最后得到的溶液中溶质质量为:(13.6g-10.6g)+11.7g=14.7g最后得到的溶液的质量为:13.6g+73g-4.4g=82.2g最后得到的溶液中溶质质量分数为:答:固体混合物中碳酸钠的质量为10.68,该盐酸中溶质的质量分数为10%,所得到的氯化钠溶液的质量分数为17.9%。
