《无菌检验原始记录》
《无菌检验原始记录》
培养天
数
菌别
1234567891011121314
需气菌
厌气菌
30~35℃薄
膜
法
样
品
阳
性
直
接
法
1
2
3
4
5
6阳
性阴性
真薄膜法
7
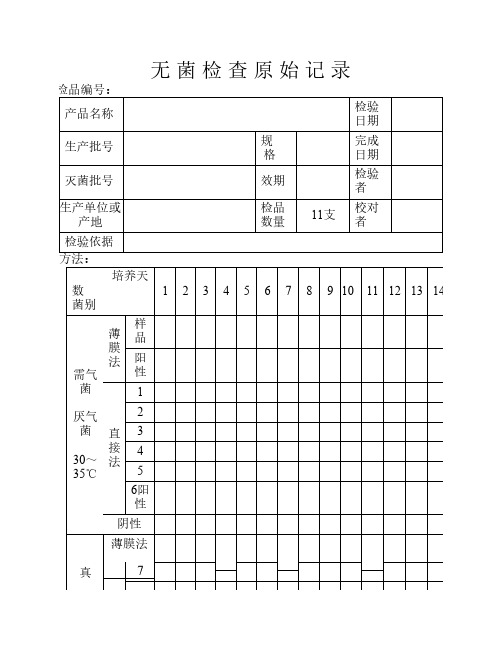
无菌检查原始记录
检品编号:
产品名称检验日期
生产批号规
格
完成
日期
灭菌批号效期检验者
生产单位或
产地检品
数量
11支
校对
者
检验依据方法:
菌 23~28℃
直接法8 9 10 11
阴性
培养基: 硫乙醇酸盐流体培养基 配制批号:
改良马丁培养基 配制批号:
稀释液、冲洗液:□ 0.1%蛋白胨水溶液 □ PH7.0氯化钠-蛋白胨缓冲液 □ 0.9%无菌氯化钠溶液
配制批号:
对照菌:
取上述对照菌新鲜培养物1ml ,用9ml0.9%无菌氯化钠溶液10倍系列稀
释,取稀释液1ml 作为对照用菌液。
第 代培养物,稀释级别 计数结果
CFU/ml
设备编号: 隔水式恒温培养箱: 霉菌培养箱: 集菌仪:
无菌室菌落培养(30~35℃)
碟号时间123(应≤1CFU/平板)24小时菌落
数 结果:
符合 □
不符合 □
48小时菌落
数 平均菌落数
检验结果
无菌检查结果判断:□符合规定□不符合规定。
无菌检验原始记录
3.供试品:细菌检测管;将5个供试品在无菌操作环境下,每个包装用50-100ml无菌0.9%生理盐水分别冲洗样品的内壁和外表,收集冲洗液于无菌容器中,用放有无菌过滤膜的无油真空泵过滤抽取冲洗液,然后将过滤膜取出接种置硫乙醇酸盐流体培养基。
5.阴性对照管:空白硫乙醇酸盐流体培养基和改良马丁培养基。
6.将接种好后硫乙醇酸盐流体培养基置30~35℃,改良马丁马丁培养基置23~28℃,培养14天观察结果。
结果记录
培养基灵敏度:
空白对照
无菌检查:
日期
供试管
阳性对照管
阴性对照管
备注:
成品检验报告:
结论:
(盖章)
检验人:复核人:
无菌检验原始记录
样品名称
样品批号
检验数量
样品数量
检验日期
灭菌批号
检验项目
无菌
方法(薄膜过滤法)
1.培养基的制备:硫乙醇酸盐流体培养基、改良马丁培养基完全溶解后置于高压蒸汽锅121℃,30min灭菌。将灭菌后培养基做灵敏度检查。
2.培养基的灵敏度检查:硫乙醇酸盐流体培养基;将生孢梭菌、枯草芽孢杆菌各2支接种置硫乙醇酸盐流体培养基同时做空白对照1支,置30~35℃培养3天,观察结果。
真菌检测管;将5个供试品在无菌操作环境下,每个包装用50-100ml无菌0.9%生理盐水分别冲洗样品的内壁和外表,收集冲洗液于无菌容器中,用放有无菌过滤膜的无油真空泵过滤抽取冲洗液,然后将过滤膜取出接种置改良马丁培养基。
4.阳性对照管:在阳性间的无菌操作环境下,将对应的阳性菌5个接种置硫乙醇酸盐流体培养基和改良马丁培养基。
商业无菌检验原始记录表2013

外观检查
马口铁容器,无泄漏或锈蚀、压痕、膨胀 马口铁容器,无泄漏或锈蚀、压痕、膨胀
保温前称重(g) 356.3
367.9
保温观察现象 无泄漏或膨胀
无泄漏或膨胀
保温后称重(g) 355.7
365.7
组织 紧密略有弹性,略粘
紧密略有弹性,略粘
形态 方块状
开
罐
色泽 不均匀的粉红色
检 查
气味 芳香,无不良异味
5 个视野
与对照样品相比, 无 明显的微生物增殖现象。数量比: 6 / 6
结封性检查见附页
校核者:
某某检验机构
商业无菌检验原始记录表
(受控文件号)************
样品流转号
食检 14-0374
样品名称
共 页第 页 午餐肉罐头
生产批号 检验地点 检验依据
培养基 检验日期
20131209
洁净实验室 508-2
GB 4789.26-2013 商业无菌检验 结晶紫染色液 20131226 无菌蒸馏水 20140313
14 年 3 月 13 日~ 3 月 23 日
仪器和设备
SC6010 电子天平 恒温培养箱 冰箱 □超净工作台 PHS-3C 酸度计 Olympus 显微镜
编号 W036 编号 W007 编号 W041 编号 W016 编号 W002 编号 W022
检验步骤
保温样品 36℃±1℃,10 d
对照样品 2℃~5℃,10 d
内壁 无锈斑
方块状 不均匀的粉红色 芳香,无不良异味 无锈斑
鉴别
无 腐败变质的迹象
pH 测定两次 等量蒸馏水混匀
7.41 7.43
平均值:7.42
7.45 7.45
无菌检查原始记录019
生孢梭菌CMCC(B)64941□
加菌量
培养基
名称:硫乙醇酸盐流体培养基
批号:
厂名:
名称:改良马丁培养基
批号:
厂名:
培养天数
1
2
3
4
5
6
7
8
9
10
11
12
13
14
阴性对照
硫乙醇酸盐流体培养基管
改良马丁
培养基管
阳性对照
结论
本品菌生长。
备注
检验人:复核人:
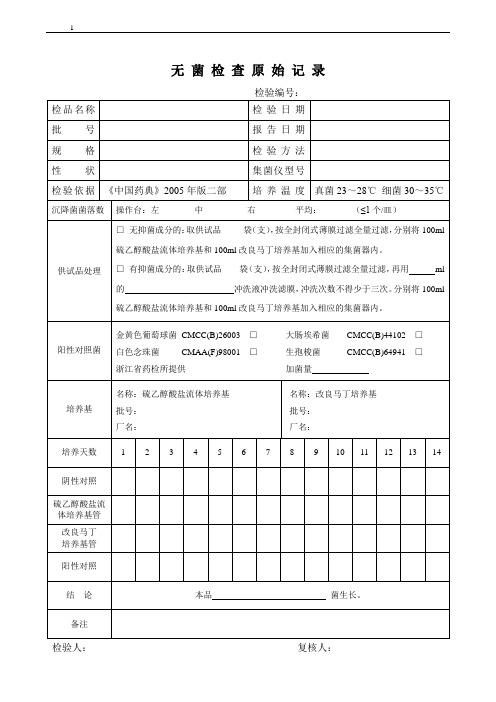
无菌检查原始记录
检验编号:
检品名称
检验日期
批号
报告日期
规格
检验方法
性状
集菌仪型号
检验依据
《中国药典》2005年版二部
培养温度
真菌23~28℃细菌30~35℃
沉降菌菌落数
操作台:左_____中_____右_____平均:_____(≤1个/皿)
供试品处理
□无抑菌成分的:取供试品_____袋(支),按全封闭式薄膜过滤全量过滤,分别将100ml硫乙醇酸盐流体培养基和100ml改良马丁培养基加入相应的集菌器内。
□有抑菌成分的:取供试品____袋(支),按全封闭式薄膜过滤全量过滤,再用ml的冲洗液冲洗滤膜,冲洗次数不得少于三次。分别将100ml硫乙醇酸盐流体培养基和100ml改良马丁培养基加入相应的集菌器内。
阳性对照菌
金黄色葡萄球菌CMCC001□
浙江省药检所提供
《无菌检验原始记录》

《无菌检验原始记录》
日期:YYYY年MM月DD日
实验目的:通过进行无菌检验,检测样品是否受到外源性微生物污染。
实验材料:
1.无菌培养基
2.无菌试管
3.无菌匀液棒
4.无菌平板
5.微生物荧光灯
6.净化工作台
实验步骤:
1.将样品取出,在净化工作台上进行操作。
2.取一支无菌试管,将培养基倒入试管中约1/4满。
3. 用无菌匀液棒沾取样品约0.1ml,并迅速划线于无菌培养基上。
4.取另一支无菌试管,使用同样的方法将培养基倒入试管中,作为对
照组。
5.将培养基涂布在无菌平板上,旋转均匀。
6.将培养基固化后,将平板放置于微生物荧光灯下观察,并记录菌落
的出现情况。
7.对照组同样进行观察,用于比对差异结果。
实验结果:
对照组观察结果:未观察到任何菌落的生长。
样品观察结果:观察到部分菌落的生长。
实验分析与讨论:
根据实验结果,对照组未观察到任何菌落的生长,说明实验的无菌操作得到了有效执行。
而样品中观察到了部分菌落的生长,表明样品中存在微生物的外源性污染。
实验结论:
根据实验结果,样品中观察到了部分菌落的生长,表明样品受到了外源性微生物污染。
为了确保样品的质量和安全性,在进一步的研究中,需要采取相应措施降低污染源,并加强无菌操作的执行。
无菌检验、观察记录
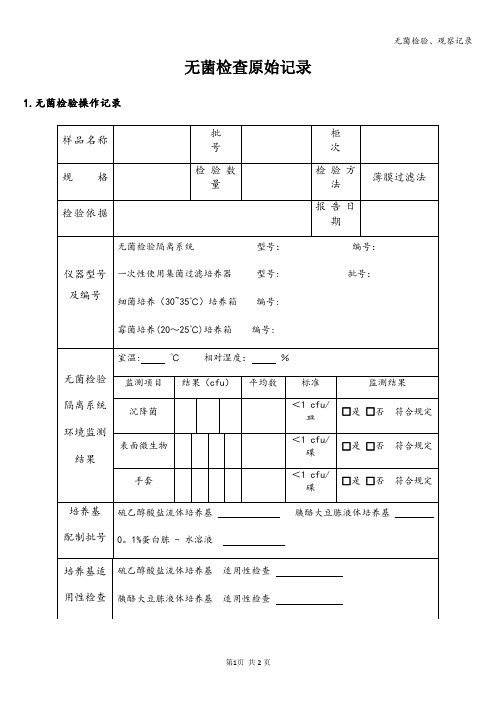
阳性对照试验情况
菌种1
菌种名称:金黄色葡萄球菌(26003)
菌种批号:培养温度:30~35℃培养时间:72h
菌种2
菌种名称:白色念珠菌(98001)
菌种批号:培养温度:20~25℃培养时间:72h
检验者:
检验日期:
复核者:
无菌检查原始记录
2.无菌检验观察记录
培养
时间(天)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
供试品
FTM
TSB
阴性对照
FTM
TSB
阳性对照
FTM
/
TSB
/
观 察 者
无菌检验观察情况:“-”表示阴性;“+”表示阳性
检验结果:
┄┄┄┄┄┄ 以下空白 ┄┄┄┄┄┄
检 验 者:复 核 者:
检验日期:复核日期:监测来自目结果(cfu)平均数
标准
监测结果
沉降菌
<1 cfu/皿
□是□否符合规定
表面微生物
<1 cfu/碟
□是□否符合规定
手套
<1 cfu/碟
□是□否符合规定
培养基
配制批号
硫乙醇酸盐流体培养基胰酪大豆胨液体培养基
0。1%蛋白胨 - 水溶液
培养基适用性检查
硫乙醇酸盐流体培养基 适用性检查
胰酪大豆胨液体培养基 适用性检查
供试品的无菌检查:取支(瓶),□直接过滤□加入适量0。1%蛋白胨—水溶液的无菌容器中,混匀,立即过滤。1个集菌器加入100ml硫乙醇酸盐流体培养基(以下简称FTM)另1个集菌器加入100ml胰酪大豆胨液体培养基(以下简称TSB)。将上述接种供试品后的培养基容器分别按各培养基规定的温度培养14天。
《无菌检验原始记录》资料
无菌检验原始记录资料1. 引言本文档为《无菌检验原始记录》资料的详细记录和分析。
无菌检验是指在无菌条件下对物品进行检验,以确定其中是否存在细菌或其他微生物的方法。
本次无菌检验涉及的物品包括药品、医疗器械、食品等。
本文档将提供检验过程的详细记录,并分析结果以评估物品的无菌性能。
2. 检验对象及目的2.1 检验对象本次无菌检验的对象为医疗器械A。
2.2 检验目的检验医疗器械A是否符合无菌要求,以评估其无菌性能。
3. 检验方法3.1 前期准备•清洁工作台:使用消毒剂对工作台进行彻底清洁,并进行适当灭菌处理。
•检验器具:收集所需的各种无菌器具,如培养皿、无菌填料等。
•培养基:准备适当的培养基。
3.2 检验步骤1.将医疗器械A放置在清洁工作台上,检查其外部是否有明显污染。
2.使用消毒液对医疗器械A进行清洁,消毒时间为10分钟。
3.将清洁后的医疗器械A放入无菌培养皿中。
4.将培养皿密封并标记,以便后续分析。
5.将培养皿放入适当的培养基中,培养时间为24小时。
6.培养结束后,观察培养皿中是否有细菌生长。
7.根据细菌生长情况,评估医疗器械A的无菌性能。
4. 实验结果经过24小时的培养,观察到培养皿中无任何细菌生长。
因此,医疗器械A符合无菌要求,具有较好的无菌性能。
5. 结论和建议根据本次无菌检验的结果,可以得出以下结论和建议:1.医疗器械A通过了无菌检验,满足无菌要求。
2.建议继续保持对医疗器械A的无菌条件管理,并进行定期检验,以确保其无菌性能。
6. 参考文献1.无菌检验技术规范,国家药典委员会、中国食品与药品监督管理局。
2.WHO《无菌技术指南》。
本文档详细记录了《无菌检验原始记录》的实验步骤、检验结果以及结论和建议。
通过本次检验,我们可以对医疗器械A的无菌性能进行初步评估,并提出后续管理建议,以确保其安全使用。
无菌检查记录
无菌检查记录
标题:无菌检查记录
引言概述:
无菌检查记录是医疗机构中非常重要的一项工作,它是确保手术室、医疗器械、药品等都符合无菌要求的重要手段。
无菌检查记录可以匡助医疗机构及时发现问题,保障患者手术安全,提高医疗质量。
一、手术室无菌检查记录的重要性
1.1 确保手术室环境无菌
1.2 预防手术感染
1.3 保障患者手术安全
二、医疗器械无菌检查记录的作用
2.1 确保医疗器械无菌
2.2 预防交叉感染
2.3 提高医疗质量
三、药品无菌检查记录的必要性
3.1 防止药品污染
3.2 保障用药安全
3.3 提高治疗效果
四、无菌检查记录的内容和方式
4.1 记录无菌检查的时间、地点、人员等信息
4.2 记录无菌检查的结果和结论
4.3 建立完善的无菌检查记录档案
五、如何做好无菌检查记录工作
5.1 建立规范的无菌检查流程
5.2 培训医护人员无菌检查知识和技能
5.3 定期检查和评估无菌检查记录的质量
结语:
无菌检查记录是医疗机构保障医疗质量、提高患者安全的重要手段,惟独做好无菌检查记录工作,才干确保医疗过程中的无菌要求得到有效执行,降低医疗事故的发生率,提升医疗服务水平。
无菌检查记录
无菌检查记录一、任务背景无菌检查是医疗机构中非常重要的一项工作,旨在确保手术器械和手术环境的无菌状态,从而减少手术感染的发生。
本文将详细介绍无菌检查记录的标准格式和内容要求。
二、标准格式无菌检查记录应包括以下内容:1. 日期和时间:记录无菌检查的具体日期和时间。
2. 检查人员信息:记录进行无菌检查的人员姓名和职务。
3. 检查项目:列出需要进行无菌检查的器械和环境项目。
4. 检查结果:对每个检查项目进行结果记录,包括“合格”、“不合格”或其他相应描述。
5. 异常情况:如有不合格的检查结果,应详细描述异常情况,包括具体的问题和发现的原因。
6. 处理措施:针对不合格的检查结果,记录采取的处理措施,包括重新清洗、更换器械或其他相应措施。
7. 复查结果:对处理后的检查项目进行复查,并记录复查结果,确保问题得到解决。
8. 备注:记录其他需要补充说明的信息。
三、内容要求1. 日期和时间:准确记录无菌检查的日期和时间,确保时间的连续性和准确性。
2. 检查人员信息:记录进行无菌检查的人员姓名和职务,确保责任的明确性。
3. 检查项目:列出需要进行无菌检查的器械和环境项目,包括手术器械、手术台、手术室空气质量等。
4. 检查结果:对每个检查项目进行结果记录,准确标注“合格”、“不合格”或其他相应描述,确保结果的准确性和可读性。
5. 异常情况:如有不合格的检查结果,应详细描述异常情况,包括具体的问题和发现的原因,以便后续处理和改进。
6. 处理措施:针对不合格的检查结果,记录采取的处理措施,包括重新清洗、更换器械或其他相应措施,确保问题得到妥善解决。
7. 复查结果:对处理后的检查项目进行复查,并记录复查结果,确保问题得到彻底解决。
8. 备注:记录其他需要补充说明的信息,如特殊情况、特殊处理等。
四、示例内容日期和时间:2022年5月10日 09:00-09:30检查人员信息:主检人员:李医生(主任医师)协检人员:王护士(护士长)检查项目:1. 手术器械:手术刀、镊子、钳子、针线等。
注射液的无菌检查原始记录.
注射液的无菌检查原始记录样品名称:规格:样品编号:生产单位:批号:样品状态:检验日期:完成日期:一检验依据二样品处理:取本品三检验方法:(1)直接接种法(2)薄膜过滤法稀释液、冲洗液:(1)0.1%蛋白胨水溶液(2)pH7.0氯化钠-蛋白胨缓冲液四无菌检查结果:洁净室动态测定∑= CFU/皿(规定100级∑≤1 CFU/皿)符合规定室温℃相对湿度 %细菌培养箱:真菌培养箱:压力蒸汽灭菌器:培养基名称:硫乙醇酸盐流体培养基(1)硫乙醇酸盐流体培养基(2)改良马丁培养基阳性对照菌:金黄色葡萄球菌 [CMCC(B)26 003] 生孢梭菌 [CMCC(B)64 941] 白色念珠菌[CMCC(F)98 001] 大肠埃希菌 [CMCC(B)44 102]注射液的无菌检查原始记录样品名称:规格:样品编号:生产单位:批号:样品状态:检验日期:完成日期:一检验依据二样品处理:取本品三检验方法:(1)直接接种法(2)薄膜过滤法稀释液、冲洗液:(1)0.1%蛋白胨水溶液(2)pH7.0氯化钠-蛋白胨缓冲液四无菌检查结果:基本信息【药品名称】通用名称:头孢呋肟商品名称:西力欣、明可欣、达力新英文名称:汉语拼音:xilixin【成份】头孢呋辛酯化学名称为:(6R,7R)-7-[2-呋喃基(甲氧亚氨基)乙酰氨基]-3-氨基甲酰氧甲基-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-羧酸,1-乙酰氧基乙酯【性状】本品为白色胶囊形薄膜衣片。
【作用类别】【规格】 250mg/片 125mg/片适应症头孢呋辛酯适用于敏感细菌造成的感染的治疗。
- 下呼吸道感染:如急性支气管炎及慢性支气管炎急性发作和肺炎。
- 上呼吸道感染:包括耳、鼻、咽喉感染,如中耳炎、鼻窦炎、扁桃体炎及咽炎。
- 生殖泌尿道感染:如肾盂肾炎,膀胱炎和尿道炎。
- 皮肤及软组织感染:如疖病,脓皮病和脓疱病。
治疗成人和12岁以上儿童的早期莱姆病,以及其后对晚期莱姆病的预防。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
稀释液、冲洗液:□0.1%蛋白胨水溶液□PH7.0氯化钠-蛋白胨缓冲液□0.9%无菌氯化钠溶液
配制批号:
对照菌:
对照菌菌液:取上述对照菌新鲜培养物1ml,用9ml0.9%无菌氯化钠溶液10倍系列稀释,取稀释液1ml作为对照用菌液。
第代培养物,稀释级别计数结果CFU/ml
设备编号: 隔水式恒温培养箱:霉菌培养箱:集菌仪:
无菌室菌落培养(30~35℃)碟号时间 Nhomakorabea1
2
3
(应≤1CFU/平板)
24小时菌落数
结果:
符合□
不符合□
48小时菌落数
平均菌落数
检验结果
无菌检查结果判断:□符合规定□不符合规定
无菌检查原始记录
检品编号:
产品名称
检验日期
生产批号
规格
完成日期
灭菌批号
效期
检验者
生产单位或产地
检品数量
11支
校对者
检验依据
方法:
培养天数
菌别
1
2
3
4
5
6
7
8
9
10
11
12
13
14
需气菌
厌气菌
30~35℃
薄膜法
样品
阳性
直接法
1
2
3
4
5
6阳性
阴性
真菌
23~28℃
薄膜法
直接法
7
8
9
10
11
阴性
培养基:硫乙醇酸盐流体培养基配制批号:
