western-blot-全过程-详细步骤复习课程
Western Blot技术详细操作步骤

Western Blot技术详细步骤蛋白质印记(Western Blot)是一种常用的生物技术,用于检测特定蛋白质在细胞提取物中的存在。
Western Blot基本步骤如下:1. 准备样品和设备:收集细胞或组织样品,然后使用适当的细胞裂解缓冲液将细胞破碎。
前处理样本并测定蛋白质浓度。
准备凝胶电泳设备,包括聚丙烯酰胺凝胶和Tris-glycine SDS运行缓冲液。
2. 凝胶电泳:将处理好的样品与样品缓冲液混合并加热,然后将其加载到凝胶孔中。
接着将预染蛋白质分子量标记也加载至凝胶中。
开始分子量依赖的电泳,使蛋白质在凝胶中分离。
3. 转印:将蛋白质从凝胶转移到结构更加稳定的膜载体,如聚偏氟乙烯 (PVDF)或者硝酸纤维素膜。
使用电转印或半干转印设备进行转移。
4. 封闭:为防止非特异性结合,使用5%无脂奶粉或BSA溶于TBST (Tris-缓冲的盐水加Tween 20)在膜上进行封闭。
一般封闭时间约为1小时,根据实验需求可调整。
5. 第一抗体孵育:将特异性的一抗稀释 (通常为多克隆或单克隆抗体),然后在封闭液中孵育膜。
根据抗体浓度与孵育时间进行相应优化。
6. 清洗:使用TBST清洗膜,以去除未结合的一抗。
通常需要清洗3次,每次5-10分钟不等,避免一抗非特异性结合。
7. 第二抗体孵育:将标记有荧光或酶的二抗稀释后,再次孵育膜。
封闭液中的二抗通常是与一抗长在不同宿主动物中的特异性抗体。
孵育时间需要优化。
8. 清洗:再次清洗膜,以去除未结合的二抗。
重复步骤6的清洗方法。
9. 检测:将膜放入检测设备中,如化学发光仪、荧光扫描仪等。
等待信号产生并记录结果。
测定蛋白质相对表达量的强度并进行定量分析。
10.数据分析:使用图像处理软件进行定量分析,如ImageJ等软件,并进行归一化处理,一般以内参蛋白(如β-actin, GAPDH等)数据为基准。
以上就是蛋白印记的基本操作步骤,具体细节及操作条件可能因实验室环境和试剂不同而有所差异。
Western-blot实验操作步骤

Western-blot实验操作步骤Western blot实验步骤一、制备蛋白样品(单层贴壁细胞总蛋白提取)1.倒掉细胞培养液,加3ml预冷的PBS洗涤细胞,重复两次,弃掉PBS 后将细胞培养瓶置于冰上。
2.裂解液RIPA(强)1ml +PMSF10ul(100:1),两者混匀后加入培养瓶中裂解细胞,冰上裂解30min,为使细胞充分裂解,培养瓶要经常来回摇动。
3.裂解完后,用细胞刮将细胞刮于一侧(动作要快),转移至ep管中.4.4度,12000rpm,离心5min.离心后取上清至新的ep管中,用于后续实验(-80保存)常用蛋白收样:倒掉细胞培养基后,预冷PBS洗涤细胞2次,弃去,再加入1ml PBS,用细胞刮轻轻刮取细胞,转移至1.5ml ep管中,12000rpm,离心5min,尽量吸净上清,沉淀于-80保存,用于后续实验。
融化蛋白样品,加入RIPA+PMSF细胞裂解液(200ul/ep管),充分混匀,冰上裂解20min,4度离心,5min ,12000rpm,小心吸取上清至新的ep管中。
二、蛋白浓度测定(BCA法)BCA(碧云天)蛋白浓度测定试剂盒灵敏度高,检测浓度下限达到25ug/ml,最小检测蛋白量达到0.5ug,待测样品体积为1-20ul。
在50-2000ug/ml浓度范围内有较好的线性关系。
标准蛋白BSA浓度:5mg/ml (-20保存) ,完全溶解蛋白标准品,取10ul 稀释至100ul,使终浓度为0.5mg/ml(ug/ul)。
蛋白样品在什么溶液中,标准品也宜用什么溶液稀释。
但为了简便起见,也可以用0.9%NaCl 或PBS稀释标准品。
1.配置BCA工作液A液: B液= 50 : 1 ,混匀 A液+B液=200ul (每个样本) 样本数量: 7个标准品 + N 个待测蛋白样本2.先将每孔加入200ul BCA工作液,再加入蛋白样本。
(96孔板),总体积为10ul.待测蛋白样本先10倍稀释。
western blot实验流程(自己整理)
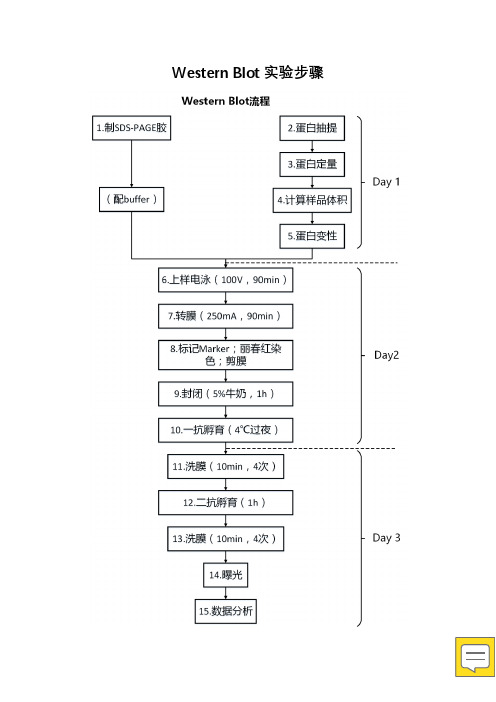
Western Blot实验步骤1.制胶2.细胞蛋白抽提步骤1.提前预冷离心机,溶解lysis buffer;2.将细胞沉淀置于冰上;1ml PBS重悬,4℃离心5min,(除去样中微量血清);3.每107cells加裂解工作液100ul,轻轻重悬细胞沉淀;4.置冰上10min,其间振荡2-3次;5.13000rpm离心10min,4℃;6.将上清转到小离心管中;7.取出1ul,用于Bradford测定蛋白浓度(ug/ul)=(样本OD值的平均值-对照OD值平均值)*斜率100℃,5min;提前预热。
中间打开盖子1~2次。
6.上样电泳(100V,90min)向电泳槽中加入电泳缓冲液,使两块玻璃内侧电泳液高于上样孔,外侧电泳槽内电泳液浸没凝胶底部。
玻璃板内侧液面高于外侧。
然后开始上样,保证每孔总蛋白量在30-50ug,总上样量小于30ul,注意上样时间尽量短,避免样品扩散。
上样完毕,盖好电泳槽的盖子,注意正负极,并选择适当的电压进行电泳。
通常在不连续的系统中,上层浓缩胶的电泳电压(建议70-80V)要低于分离胶电泳电压(建议90-110V),以达到更好的浓缩效果,使样品进入分离胶时被压缩在同一水平线上。
电泳直至溴酚蓝染料前沿下至凝胶末端处停止电泳,电泳时间约2-3 小时。
电泳时间根据具体情况定。
7.转膜(250mA,1h 30min)转膜顺序:阴极碳板+海绵+三滤+胶+膜+三滤+海绵+阳极碳板湿式电转膜1. 电泳结束后取出凝胶,在转膜缓冲液中漂洗数秒。
按“三明治”模式,打开电转印夹,每侧垫上一块专用的用转膜液浸泡透的海绵垫,再各放一块转膜液浸透的快速高效蛋白转移垫(定性滤纸),将凝胶平放在阴极侧滤纸上,最后将转膜液浸透博士德硝酸纤维素NC 膜平放在凝胶上,去除气泡,夹好电转印夹,注意NC 膜与胶,NC 膜与滤纸,滤纸与胶之间不可有气泡。
2. 转印槽加满转膜缓冲液,插入电转印夹,将转印槽放入冰箱内(-20℃),确保NC 膜最靠近正极,带负电的氨基酸和蛋白质向正极迁移。
WesternBlot操作流程

WesternBlot操作流程Western Blot操作流程本⼈将⾃⼰做WB实验时的具体操作流程,做了详细的记录并整理。
因为每个实验室的条件不⼀样,所以本流程仅供参考,具体适合⾃⼰的实验操作需要⼤家摸索。
由于知识量有限,有些描述⽤词并不专业,请⼤家谅解。
⼀、流程图制胶→→电泳跑胶(1.5-2.5h)→→转膜(3h)→→(可使⽤⽴春红检测是否蛋⽩是否成功转移)TBST清洗(10min)→→封闭(2h)→→TBST清洗(10min)→→附Ⅰ抗(内参:⼩⿏抗β-Actin,先摇床轻摇30min,再放冰箱4度过夜)→→TBST 清洗三次(10min/次)→→附Ⅱ抗(内参:⼭⽺抗⼩⿏,轻摇1.5h)→→TBST清洗三次(10min/次)→→显影⼆、物料及配制1、电泳液:⼀包电泳粉+1000ml双蒸⽔(可回收使⽤)2、10%过硫酸铵:1g过硫酸铵+10ml双蒸⽔3、转膜液:⼀包转膜粉+800ml双蒸⽔+200ml甲醇(可回收使⽤)4、TBST溶液:50ml 20*TBS+950ml双蒸⽔+1ml吐温20。
(⽆需回收)5、封闭液:购买6、Ⅰ抗(内参):将⼩⿏抗β-Actin:Ⅰ稀释液按1:500稀释待⽤,4度保存。
Ⅰ抗(⽬的蛋⽩58kDa):将smad2:Ⅰ稀释液按1:1000稀释待⽤,4度保存。
7、Ⅱ抗(内参):将⼭⽺抗⼩⿏:Ⅱ抗稀释液按1:5000稀释代⽤,4度保存。
Ⅱ抗(⽬的蛋⽩58kDa):将⼭⽺抗兔:Ⅱ抗稀释液按1:5000稀释待⽤,4度保存。
7、显影液:按说明书配制,避光可长期回收使⽤8、定影液:按说明书配制,可长期回收使⽤9、发光液:超敏发光液A液:B液=1:1三、步骤(⼀)制胶1、Tris-⽢氨酸SDS-PAGE聚丙烯酰胺凝胶电泳分离胶溶液的配制2、Tris-⽢氨酸SDS-PAGE聚丙烯酰胺凝胶电泳5%积层胶所⽤溶液3、1)将规格1.0mm或其它规格的玻璃板固定好。
2)依次将所需试剂加⼊烧杯中,加⼊TEMED之后,混匀,⽤1000ml的移液枪沿玻璃板缝左右两边的⾓交替加⼊分离胶溶液,也可从左到右连续加⼊(⽬的:两种⽅法都可以使液⾯快速达到⽔平状态)。
Western blot详细操作过程

Western BlotWestern Blot 采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,“探针”是抗体,“显色”用标记的二抗。
经过PAGE 分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄(NC )膜或聚偏二氟乙烯(PVDF )膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。
以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色以检测电泳分离的特异性目的基因表达的蛋白成分。
该技术广泛应用于检测蛋白水平的表达。
流程:蛋白样品的提取→蛋白样品定量与变性→PAGE 凝胶电泳→转膜→丽春红染色→封闭→抗体孵育→底物显色。
实验器材和试剂:一. 蛋白提取试剂1.10% SDS 裂解液:称取10g SDS 粉末加入双蒸水至90mL ,充分溶解,定容至100ml 室温保存。
2.RIPA 裂解液1ml 裂解液工作液配方: 10ul 100mmol/L PMSF (1mM) 0.2ul 10mg/ml Aprotinin (2ug/ml) 5.0ul 1mg/ml Leupeptin (5ug/ml)0.9848ml 裂解液0.5ml 裂解液工作液配方: 5ul 100mmol/L PMSF (1mM) 0.1ul 10mg/ml Aprotinin (2ug/ml) 2.5ul 1mg/ml Leupeptin (5ug/ml)0.4924ml 裂解液 PMSF 必须摇匀至无结晶时才可与裂解液混合3.蛋白酶抑制剂:100mmol/L PMSF :17.4mg PMSF 粉末溶于1ml 异丙醇(AR),分装250ul 每管后-20℃保存。
使用终浓度为1 mmol/L 。
【PMSF :在溶液中不稳定,应在临用前从储存液中现加于裂解液中。
PMSF 剧毒,严重损害呼吸道粘膜、眼睛及皮肤,吸入、吞进或通过皮肤吸收后有致命危险一旦眼睛或皮肤接触了PMSF ,应立即用大量的水冲洗。
western操作详细程序

Western blot详细步骤一、电泳1、Marker点0.8微升,72KD显红色,其它显蓝色2、100V,恒压——140V恒压,1.5h, 15%的胶,将溴酚蓝跑到外面,让带分开点。
3、转膜: PVDF膜从下到上依次是:黑板、海绵垫,两层滤纸,胶,PVDF 膜,两层滤纸,海绵垫,白板4、根据Marker把多出来的胶切掉节省。
留下14—72之间,将海绵垫与板用水洗,泡于Western转膜buffer中,剪取和脚大小合适的滤纸和膜,膜剪好后放在无水甲醇中浸泡2分钟,将滤纸润湿,两层滤纸放于海绵垫上,赶尽气泡,再铺两层滤纸,压紧夹子。
放于电转膜槽中,加冰盒,将wenstern转膜buffer倒入槽中,加满,放入4度冰箱中,100V1h, western转膜buffer可重复使用5次。
5、将膜放入封闭液中(5%脱脂奶粉,用PBS缓冲液配置)45min摇。
6、用PBST液洗膜2次,每次2min,摇(将500微升吐温20加到1000微升PBS 溶液中)将脱脂奶粉中的蛋白洗掉。
7、加一抗 Anti-His(我做的是抗His,要根据自己的蛋白选择)根据抗体说明书配置抗体稀释液,用PBS稀释,用塑料膜封膜加抗体缓冲液,封袋1.5小时反应,摇。
PBS一般PH为7.2,一抗可多次使用,直到有异味产生,可持续一个月,使用3、4次,因为比较贵,为得到较好效果,可向旧抗体缓冲液不加新液,为长久保存,可加叠氮钠,但使抗体不易结合。
脱脂奶粉可多次使用,一般为两天。
8、洗膜,4次,每次两分钟,PBST.9、加二抗,(羊抗鼠)封于小袋中摇45分钟,(二抗用辣跟过氧化物酶标记)10、PBST洗脱4次,摇11、在桌子上铺保鲜膜,将PVDF膜防御保鲜膜上,向膜上加A,B混合底物,反应1-2min,吸干底物,用保鲜膜将PVDF膜包好,放入曝光版中。
12、进入暗室操作,将胶压在膜上曝光2min(如果不行,加长曝光时间2-30min)将胶片放入显影液中2min-3min,用水漂洗一下,放入定影液2-3min(手套操作)定影液都是商品粉剂,后调配而成。
Westernblot实验操作详细步骤

Westernblot实验操作详细步骤1.样本制备:a.收集细胞或组织样本并加入提取缓冲液,破碎细胞或组织以释放蛋白质。
b.用超声波破碎机或搅拌器处理样本,使其彻底破碎。
c.避免加入蛋白酶抑制剂和磷酸酶抑制剂以防止蛋白质的降解。
2.蛋白质分离:a.将样本加入离心管中,并用高速离心分离细胞碎片和细胞核。
b.收集上清液,其中包含溶解的蛋白质。
3.蛋白质浓度测定:a. 使用BCA或Bradford等方法测定提取的蛋白质浓度。
b.根据需要调整蛋白质浓度,以确保每个样本使用相同的蛋白质量。
4.准备SDS-凝胶:a.准备解聚凝胶和浓缩凝胶以进行垂直电泳。
b.根据需要选择合适的胶百分比和凝胶组装器。
c.制备足够的凝胶和凝胶缓冲液。
5.蛋白质电泳:a.将蛋白质样本加入加载缓冲液,并在煮沸过程中使其变性。
b.将蛋白质样本加载至凝胶槽中。
c.根据需要在凝胶中加入预定分子量标记物,以便于蛋白质分子量的确定。
d.以恒定电流进行电泳,直到预定分子量标记物到达所需位置。
6.蛋白质转膜:a.选择合适的膜材料(例如聚偏氟乙烯或硝酸纤维素)。
b.用蛋白质转膜装置将凝胶上的蛋白质转移到膜上。
c.确保膜与凝胶完全贴合,并尽量避免气泡的产生。
7.阻塞和抗体孵育:a.将膜放入含有5%非脂奶粉或1%牛血清蛋白的TBST缓冲液中进行阻塞。
b.在蛋白质靶向抗体中稀释贮存液,并使用适当的稀释倍数进行孵育。
c.将膜和抗体一起放入摇床或孵育箱中,在适当的温度下进行孵育。
8.洗涤:a.用TBST缓冲液洗涤膜以去除未结合的抗体。
b.进行3至5次洗涤,每次洗涤持续5到10分钟。
9.二次抗体孵育:a.将膜放入稀释过的二抗溶液中进行孵育。
b.孵育时间和温度根据抗体种类和需求进行调整。
10.再洗涤:a.用TBST缓冲液进行大约3至5次洗涤。
b.确保彻底洗涤以去除未结合的二抗。
11.信号检测:a.使用化学发光或荧光探针对膜上的蛋白质进行检测。
b.按照探针供应商的说明进行操作。
Western blot实验技术全攻略!附详细操作步骤

随着生物学领域的不断发展,Western blot(蛋白质印迹)实验技术已成为研究蛋白质表达和相互作用的重要手段。
本文将为大家提供一份Western blot实验技术全攻略,附详细操作步骤,希望对大家的科研工作有所帮助。
Western blot实验技术全攻略第一步:制备样品Western blot实验需要使用蛋白质样品,因此首先需要制备样品。
一般来说,可以从细胞、组织或生物液中提取蛋白质。
提取蛋白质的方法有很多种,例如细胞裂解、超声波破碎、切片法等。
提取后的样品需要通过蛋白质定量方法确定蛋白质的浓度。
第二步:电泳分离蛋白质将制备好的样品经过蛋白质电泳分离,将蛋白质分离成不同的带状条带。
电泳分离可以采用SDS-PAGE或非变性PAGE方法。
SDS-PAGE适用于大多数蛋白质,这种方法可以将蛋白质分离成不同的分子量带状条带。
非变性PAGE则适用于大分子蛋白质和蛋白质复合物的分离。
第三步:转移蛋白质将分离好的蛋白质转移到聚丙烯酰胺凝胶膜(PVDF)或硝酸纤维素膜(NC)上。
转移蛋白质可以采用湿式电转移或半干式电转移方法。
湿式电转移适用于小分子蛋白质的转移,而半干式电转移则适用于大分子蛋白质的转移。
第四步:阻断和孵育将转移膜放入含有牛血清白蛋白(BSA)或非脂类干奶粉的TBST中,进行阻断。
然后将膜孵育于含有一定浓度的一抗体的TBST中,以便与目标蛋白结合。
第五步:检测和成像将膜孵育于含有适量的二抗体的TBST中,以便与一抗体结合。
二抗体通常被标记为辣根过氧化物酶(HRP)或碱性磷酸酶(AP)。
在使用HRP的情况下,将膜浸泡在ECL底物中,然后用射线或荧光成像系统观察蛋白质的信号。
在使用AP的情况下,将膜浸泡在BCIP 和NBT底物中,然后用射线或荧光成像系统观察蛋白质的信号。
下面是Western blot实验的详细操作步骤:1. 蛋白质提取:将待测样品(如细胞、组织等)进行裂解,以获得蛋白质样品。
2. SDS-PAGE电泳:将蛋白质样品进行电泳分离,以分离不同大小的蛋白质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.胶取出,在transfer buffer里泡10min
5.黑胶白膜(一层海绵,2层滤纸)
6.转膜100v,1—1.5h(黑对黑,冰板,在冰里跑)
四:封闭、一抗、二抗
1.5%脱脂奶粉(pbst溶)1h37度
2.一抗4度12h
9.加好对应的RIPA以及loding buffer后,煮蛋白5-15min,-20度保存。
二:跑胶
1.1.0玻板,洗干净
2.配制10%或者12%分离胶一块胶需要5ml
3.灌分离胶,在分离胶上层灌无水乙醇
4.配制5%浓缩胶2块胶需要4ml
5.待分离胶干后,灌浓缩胶,插梳子
6.待胶干后,将胶及玻板一起放入电泳槽,拔梳子,倒入1*running buffer(上腔灌满,下腔过电线丝)
western-blot-全过程-详细步骤
一:提蛋白:
1.PBS洗2遍,加RIPA 80-100ul(含10xcooktail)。
2.在冰上刮到离心管中,在冰上裂解20-30min。
3.4度离心,13000rpm、10-15min(准备新的离心管、配BCA 200ul/每孔(A:B=50:1)、96孔板加PBS(2个对照组20ul,实验组18ul))。
4.取上清转移到新离心管中,记住转移的体积。
5.96孔板中每孔加2ul蛋白液。
6.每孔加200ulA/B混合液。
7.37度半小时。
8.测浓度以及标化用一起在libo文件夹找模板,最后得到每组需要加的RIPA以及loding buffer,还有标化后的浓度。562波长0.046斜率(实验组值-对照组值)/斜率=浓度浓度最好在4-8ug/ul最好,跑胶时就可以只加10ul蛋白液(蛋白含量40-80ug)
3.pbst洗膜,3次,每次10min
4.二抗(1:5000)1h3300ul
PBST:1000ml’PBS+1mltween
5%脱脂奶粉:100mlPBST+5g脱脂奶粉
10*running buffer:tris30.3g甘氨酸144.1gsds10g加水至1000ml
7.预电泳,100v,10-15min
8.加样(蛋白样品及marker)10ul,marker 5ul
9.60v 10-20min,之后100-110v
三:转膜
1.配transfer buffer,用10*transfer buffer稀释10倍,并加20%甲醇
2.transfer buffer浸泡海绵、滤纸
10*transfer buffer:tris30.3g甘氨酸144.1g加水至1000ml
1*transfer buffer:100ml10*transfer buffer 200ml甲醇加水至1000ml
