化学式及离子符号书写练习
化学式及离子符号的书写训练

化学式及离子符号的书写训练
氢氧根:硝酸根碳酸根:硫酸根:铵根:
氢氧根离子:硝酸根离子:碳酸根离子:硫酸根离子:铵根离子:氢离子:银离子:钠离子:氟离子:钾离子:钙离子:镁离子:钡离子:锌离子:铁离子:亚铁离子:铜离子:
氢气:氧气:氮气:臭氧:
二氧化碳:一氧化碳:五氧化二磷:四氧化三铁:二氧化氮:一氧化氮:二氧化硫:三氧化硫:
硫酸:碳酸:硝酸:盐酸:
氯化钠:氯化钾:氯化铁:氯化亚铁:
氯化铜:氯化银:氢氧化钠:氢氧化钾:
氢氧化铁:氢氧化铜:氢氧化镁:氢氧化锌:
碳酸钠:碳酸镁:碳酸钾:碳酸钡:
硫酸钠:硫酸镁:硫酸钾:硫酸铜:
硫酸亚铁:硫酸铁:硫酸钡:硝酸钠:
硝酸钾:硝酸银:硝酸铁:硝酸钡:
氯化铵:硫酸铵:硝酸铵:碳酸铵:。
化学式书写与化学方程式配平专项练习

+2 Mg__________________________ +2MgO______________________________元素符号、原子团及化学式的书写及练习一、写出各元素的元素符号或名称及部分常见原子团离子的符号。
1、写出下列各种符号所表示的意义:“Cu” 表示①__________________ ②_________________________ “H 2O” 表示①②③④“5H” 表示①“2CO 2”表示①2、写出下列各种符号或指出符号中的“2”的意义: 三个铁原子 五个五氧化二磷分子液态氮铝离子 氯离子 二个铵根离子2Mg___________________________ Mg 2+______________________________SO 2___________________________2O,O 2-, 2.O 2-,O 2, 2. O 2 ,四、熟练书写化学式:(写出下列各种物质的化学式)1、单质: 氢气 氯气 氮气 氦气 氖气 氩气铜 锰 镁 金刚石 固态磷硫磺 臭氧气体 2 、化合物:氧化物: 一氧化碳 水 二氧化硫氧化镁氧化铁 氧化亚铁氧化铜氧化铝氧化锌 氧化亚铜 硫化物:(硫元素显示-2价)硫化镁 硫化锌硫化铁硫化亚铁硫化钠 氯化物(又称盐酸盐)氯元素显示-1价 氯化镁 氯化锌氯化铁 氯化亚铁氯化钠 氯化铜氯化铵 氯化氢(盐酸)氢氧化物(含OH )氢氧化镁 氢氧化锌 氢氧化铁氢氧化铝氢氧化钠 氢氧化铜 氢氧化钾 氢氧化钡硝酸盐(含硝酸根NO 3)硝酸镁 硝酸锌硝酸铁 硝酸钾硝酸钠硝酸铜 硝酸铵硝酸银硝酸钙硝酸铝硝酸钡硝酸亚铁硫酸盐(含SO4)硫酸镁硫酸锌硫酸铜硫酸铁硫酸钠硫酸钾硫酸铵硫酸钡碳酸盐(含CO3)碳酸镁碳酸锌碳酸钙碳酸钡碳酸钠碳酸钾碳酸氢钠碳酸氢铵磷酸盐(含PO4)磷酸镁磷酸锌磷酸铜磷酸铁磷酸钠磷酸钾磷酸铵磷酸钡酸类(H+与某些阴离子结合而成的化合物)盐酸(氯化氢)氢硫酸(硫化氢)氢氟酸(氟化氢)硫酸硝酸碳酸亚硫酸磷酸酸式盐(含HCO3或HSO4或HPO4)碳酸氢钠碳酸氢钙碳酸氢钡碳酸氢铵硫酸氢钠硫酸氢钙硫酸氢钡硫酸氢铵磷酸氢钠磷酸氢二钙磷酸氢钡磷酸氢铵配平化学方程式的专项练习一、最小公倍数法:(找出两边同种原子的个数最多的原子,然后求最小公倍数,得原子个数。
(整理)高中离子方程式经典练习题

(整理)高中离子方程式经典练习题离子反应问题及离子方程式的书写离子方程式的书写步骤:1、写:书写完全正确的化学方程式;2、拆:将能拆的化学式(完全电离的酸、碱、盐及融化态的金属氧化物)拆为离子符号;3、删:将未参加离子反应的离子从两边删掉(等个数),整理(系数应为最简整数比);4、查:⑴质量守恒、⑵电荷守恒、⑶注明“↑”“↓” ;⑷ 、为氧化还原反应时、氧化剂与还原剂得失电子数应相等。
? 书写相关知识1、完全电离的酸是指:HCl 、H 2SO 4、HNO 3、HI 、HBr 、HClO 4等强酸;中强酸(H 2SO 3、H 3PO 4),弱酸(H 2CO 3、H 2S 、HF 、HclO 、CH 3COOH 、H 2SiO 3)则不能拆。
2、完全电离的碱是指:NaOH 、KOH 、Ca(OH)2、Ba(OH)2等强碱、中强碱的溶液;而 NH 3?H 2O 及Cu(OH)2、Fe(OH)3等难溶性弱碱则不能拆。
3、完全电离的盐是指:所有易溶、可溶及微溶性的盐的溶液。
附:盐的溶解性规律:钾盐、钠盐、铵盐、硝酸盐,二元酸的酸式盐、磷酸的二氢盐均易溶。
碳酸盐、磷酸盐、硅酸盐的正盐中只有钾盐、钠盐、铵盐溶;氯化物中只有AgCl 不溶;硫酸盐中只有PbSO 4 、BaSO 4不溶,但CaSO 4、Ag 2SO 4为微溶。
4、特殊情况处理:微溶物:作反应物时,为溶液时拆,作产物时不拆。
浓硫酸作反应物时,不能拆,而浓盐酸、浓硝酸则必须拆。
酸式酸根离子只有HSO 4-必须拆,而HS -、HCO 3-、HSO 3-、HPO 42-、H 2PO 4-则不能拆。
5、凡单质、氧化物、气体、难溶固体、弱酸、弱碱、水等难电离的及非电解质均不能拆。
练习题一选择题1、下列电离方程式错误的是()A NaHCO 3 ====Na + +H ++CO 32―B NaHSO 4 ====Na + +H ++SO 42―C MgCl 2 ====Mg 2++2Cl ―D B a (O H )2 =====Ba 2++2OH ―2、离子方程式CO 32-+ 2H += H 2O + CO 2↑中的CO 32-代表的物质可以是() A 、CaCO 3 B 、NaHCO 3 C 、Na 2CO 3 D 、BaCO 33、下列化学方程式中,不能用离子方程式 Ba 2++SO 42―====BaSO 4 ↓A .Ba(NO 3)2+H 2SO 4==BaSO 4↓+2HNO 3B .BaCl 2+Na 2SO 4==BaSO 4↓+2NaClC .BaCO 3+H 2SO 4==BaSO 4↓+H 2O+CO 2↑D .BaCl 2+H 2SO 4==BaSO 4↓+2HCl4.下列各组离子反应可用H ++OH -H 2O 表示的是()A .氢氧化钡和硫酸B .氢氧化铁和盐酸C.硝酸和氢氧化钠D.硫酸氢钠和氢氧化钠5、下列离子方程式,书写正确的是()A、盐酸与碳酸钡反应 CO32-+2H+==CO2↑+H2OB、硫酸铜溶液中滴加氢氧化钡溶液Ba2++2OH-+Cu2++SO42-==BaSO4↓+Cu(OH)2↓C、硝酸银溶液中加入铜粉Ag++Cu==Cu2++Ag↓D、铁与稀盐酸反应2Fe+6H+==2Fe3++3H2↑6、下列离子方程式书写正确的是()A、氧化铜与盐酸反应O2― +2H+ ====H2OB、碳酸氢钠溶于盐酸:HCO3-+ H+ = H2O + CO2↑C、硫酸氢钠溶液与NaOH溶液混合:HSO4- + OH- = H2O + SO42-D、石灰石溶于硝酸:CO32-+ 2H+ = H2O + CO2↑7.下列反应的离子方程式中,正确的是()A.向硝酸银溶液中加盐酸Ag++C1-===AgCl↓B.碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+===Ca2++2H2O+2CO2↑C.盐酸跟氢氧化镁反应:H++OH-===H2OD.碳酸镁跟硫酸反应:MgCO3+2H+===Mg2++H2O+CO2↑8.下列离子方程式中,正确的是A.碳酸氢钙溶液与盐酸反应Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑B稀盐酸和碳酸钙反应 CO32- + 2H+ = CO2↑ + H2OC碳酸钠溶液与醋酸反应 CO32-+ 2H+ = CO2↑ + H2OD石溶于醋酸的反应CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O9.下列反应的离子方程式中,正确的是()A、氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO42-=BaSO4↓+2H2OB、氯化铁溶液中加铁粉 2Fe3+ + Fe = 3Fe2+C、过量CO2通入NaOH溶液中CO2 + 2OH-= CO32-+ H2OD、少量CO2通入NaOH溶液中CO2 + OH-= HCO3-+ H2O10.下列离子方程式中,正确的是A、氨气通入醋酸CH3COOH + NH3 = CH3COO-+NH4+B.碳酸氢镁溶液中加过量石灰水Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ C、澄清石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2OD、稀硫酸滴在铜片上:Cu+2H+==Cu2++H2↑11.下列各组中的离子,能在溶液量共存的是()A 、K+、H+、SO42-、OH-B、Na+、Ca2+、CO32-、NO3-C 、Na+、H+、CO32- Cl-D 、Na+、Cu2+、Cl、SO42-12、在无色透明强酸性溶液中,能大量共存的离子组是()A、K+、Cu2+、NO3-、SO42-B、K+、Na+、Cl-、CO32-C、Zn2+、NH4+、NO3-、Cl-D、K+、Na+、MnO4-、SO42-13、在PH=1无色透明溶液中能大量共存的离子组是()A.Al3+、Ag+、NO3-、Cl-B.Mg2+、NH4+、NO3-、Cl-C.Ba2+、K+、S2-、Cl-D.Cu2+、Na+、NO3-、SO42-14、在强酸性或强碱性溶液中都能大量共存的一组离子是()A.Ba2+,Fe3+,Br-,NO3-B.Na+,Ca2+,HCO3-,NO3-C.Al3+,NH4+,SO42-,Na+D.Na+,K+,NO3-,SO42-15、下列各组中的离子,能在溶液量共存的是()A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、CO-23、NO-3C、Na+、H+、Cl-、CO-23 D.K+、Cu2+、NO-3、SO-24、16、在强酸性无色透明溶液中,下列各组离子能大量共存的是()A、Fe3+、K+、Cl-、MnO4-B、Ag+、Na+、NO3-、Cl-C、Zn2+、Al3+、SO42-、Cl-D、Ba2+、NH4+、Cl-、HCO3-17、巳知某溶液中存在较多的H+、SO42—、NO3—,则该溶液中还可能大量存在的离子组是A.Al3+、CH3C00—、Cl—B.Mg2+、Ba2+、Br—C.Mg2+、Cl—、I—D.Na+、NH4+、Cl—18、某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子。
化学用语(元素符号、化学式、化学方程式)专题练习

“化学用语”(元素符号、化学式、化学方程式)专题练习一.说出下列符号的含义:1.H:2、2H:23、H2:4、2H2:25.H+:6、2H+:27、3Mg2+:二.说出下列符号中数字“2”的含义:1、2S:22、SO2:3、S2-:4、2S2-:5、MgO:6、SO42-:三.用数学或符号表示:1、3个铝原子:2、5个水分子:23、a个氦分子:4、b个铁离子:5、3个硫酸根离子:6、m个碳酸根离子:37、2个亚铁离子:8、氯酸钾中氯的化合价:4四.写出下列物质的化学式:1、氯化钾:2、氯酸钾:3、硫酸铜:4、硫酸锌:5、硫化锌:6、氢氧化钙:7、氯化钠:8、氧化钙:9、碳酸钠:10、硝酸铵:11、硫酸亚铁:12、氢氧化钠:五.用序号回答下列问题:1、写出下列粒子的名.称.、符号..:A:____B:_____C:_____D:____E:______2、以上粒子中,表示原子的是;表示阳离子的有__种,阴离子有__种;电子排布相同的是;五、配平下列化学方程式(反应条件忽略):1、Al + Fe3O4—- Fe + Al2O32、Al + MnO2—Mn + Al2O33、 CO + Fe3O4 —- Fe + CO 24、 C+ Fe3O4 —— Fe + CO 25、 H 2 + WO 3 —— W + H 2O6、 Fe + H 2O —— H 2 + Fe3O47、 FeS 2 + O 2 —— Fe2O3+ SO 28、 MnO 2+ HCl —— MnCl2 + Cl 2 + H 2O9、 Cl 2 + Ca (OH )2 —— CaCl2 + Ca (ClO )2 + H 2O六.(1) 3Cu+8HNO3==3Cu (NO 3)2+2X ↑+4H 2O ,求X 的化学式为 。
(2) R+3O 2==2CO 2+3H 2O 求R 的化学式为 。
化学用语过关练习修

化学符号书写过关练习※2个氢原子__;2个硫原子__;4个铁原子__;5个氧原子__;2个氮原子__2.化学式:单质:①稀有气体、金属和固态非金属氦气____氩气_____氖气____铁____汞____铜____碳_____硫______磷______②非金属气体氧气____氢气____氮气____氯气____化合物:①常见的氧化物的化学式:水_____二氧化硫____四氧化三铁_____五氧化二磷____二氧化碳_____一氧化碳_____二氧化氮___过氧化氢_____二氧化锰______氧化镁_____氧化汞_____氧化铁_____②金属和非金属组成化合物的化学式:氯化钠___氯化钾___硫化钾___氯化锌___硫化锌___③其他:高锰酸钾_____氯酸钾_______锰酸钾______※2个氢分子__4个水分子__5个二氧化碳分子__2个氮分子__3.离子符号:常见的离子:①阳离子:钾离子,钙离子,钠离子,镁离子铝离子,锌离子,铁离子,氢离子铜离子,银离子,亚铁离子②阴离子:氧离子,氯离子,氟离子,硫离子,③原子团:硝酸根离子___氢氧根离子___氯酸根离子___高锰酸根离子___碳酸根离子___硫酸根离子___锰酸根离子___铵根离子___※2个钠离子__3个镁离子__4个硫酸根离子___3个硝酸根离子___5个氢氧根离子___ 3个氯酸根离子___ 4个高锰酸根离子___3个碳酸根离子___ 4个硫酸根离子___ 4个锰酸根离子___4个铵根离子___4.化合价①请标出下列元素的常见化合价,括号中写出对应元素的化合价形成的离子符号H ( )Cl ( )Na ( )K ( )Ag ( )O ( )Ca ( )Mg ( ) Ba ( )Zn ( )Al ( )Si P Fe ( )Fe ( )Cu ( )Hg C C S S S②写出下列酸根离子硝酸根氢氧根氯酸根高锰酸根碳酸根硫酸根锰酸根磷酸根铵根5.结构示意图①请画出下列元素的原子结构示意图:氢氦碳氮氧氟氖钠镁铝硫氯氩②请画出下列离子结构示意图钠离子镁离子铝离子氧离子硫离子氯离子6.符号和数字的含义①说明下列符号的含义:O: 、2O: 2O2: O2: ①;②③;④O2-O-2②说明下列符号中数字的含义:2H: 2H 2: H 2: C 60 O 2- Mg 2+2S 2-____ 2H ++2 +2Mg MgO 7.下列化学式如有错误请改在横线上: 氧化钙Ca 2O 2 ______,氯化铁 FeCl 2 ______,氯化锌 ZnCl ______,硫化铝Al 3 S 2 ______,氢氧化铜CuOH __________,氯化钠ClNa ______,8.写出下列物质的化学式(并标出金属元素或非金属元素及原子团的化合价)。
九年级上离子符号化学式练习题
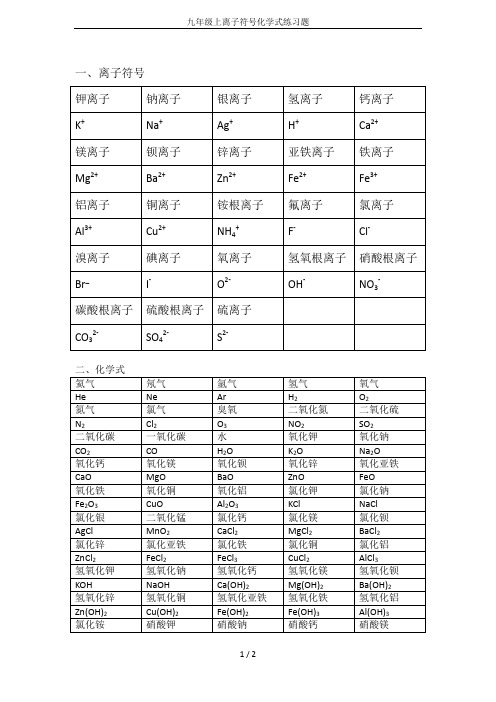
CaSO4
MgSO4
硫酸钡
硫酸锌
硫酸铜
氯化铵
硝酸
BaSO4
ZnSO4
CuSO4
NH4Cl
HNO3
盐酸
硫酸
四氯化碳
二硫化碳
二氧化氯
HCl
H2SO4
CCl4
CS2
ClO2
硝酸铵
硫酸铵
NH4NO3
(NH4)2SO4
CO32-
SO42-
S2-
二、化学式
氦气
氖气
氩气
氢气
氧气
He
Ne
Ar
H2
O2
氮气
氯气
臭氧
二氧化氮
二氧化硫
N2
Cl2
O3
NO2
SO2
二氧化碳
一氧化碳
水
氧化钾
氧化钠
CO2
CO
H2O
K2O
Na2O
氧化钙
氧化镁
氧化钡
氧化锌
氧化亚铁
CaO
MgO
BaO
ZnO
FeO
氧化铁
氧化铜
氧化铝
氯化钾
氯化钠
Fe2O3
CuO
Al2O3
一、离子符号
钾离子
钠离子
银离子Байду номын сангаас
氢离子
钙离子
K+
Na+
Ag+
H+
Ca2+
镁离子
钡离子
锌离子
亚铁离子
铁离子
Mg2+
Ba2+
Zn2+
Fe2+
Fe3+
九年级上册化学期末专练:元素符号、化合价、离子符号、化学式默写和计算

九年级上册化学期末复习专练元素符号、化合价、离子符号、化学式背写与计算➢背写部分一. 写出元素符号1.元素周期表前20个元素氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙2.常见元素:锰铁银碘钡汞铅溴铜锌金二. 背出常见元素、原子团的化合价:(用符号填写)常见元素化合价:常见原子团化合价:(一定要靠记忆来背写)练习:1. 标出下列物质中N元素的化合价,请标在N元素的正上方①N.2; ②N.O: ③N.O2: ④N.2O5; ⑤HN.O3⑥N.H4N.O32. NaSO4中S的化合价是KMnO4中Mn的化合价为三、写出下列离子的符号氢离子氧离子氟离子钠离子镁离子铝离子硫离子氯离子钾离子钙离子铁离子铜离子亚铁离子氢氧根离子硫酸根离子硝酸根离子碳酸根离子铵根离子碳酸氢根离子四、写出下列物质的化学式1、单质三原子:臭氧双原子:氧气氯气氢气碘溴单原子:稀有气体:氦气氩气氖气金属:铜银水银锌铁其他:磷金刚石硫碳石墨2、化合物氧化物:氧化铝水干冰氧化铜三氧化硫过氧化氢二氧化硫氧化钾氧化钙一氧化碳二氧化锰四氧化三铁五氧化二磷氯化物:氯化钠氯化铜氯化银氯化氢氯化镁氯化铁硫化物:硫化氢硫化钠硫化锌其他:氯酸钾 硫酸钾 碳酸钙 锰酸钾 高锰酸钾 硫酸 氢氧化钙 氢氧化钾 氢氧化铝 碳酸钠 碳酸铵 综合练习 1、看符号写含义O 5N 3H 2 C Al mC 2、按要求写出下列符号:①氧元素 ②两个氧原子 ③氧气 ④两个氧气分子 ⑤氧离子 ⑥两个氧离子 3、写出下列符号中数字2的意义。
2H Ca 2+ 2SO 3 Cl 2 2H 2O 、2MgO C +2u SO 42-➢ 计算部分一、根据化学式计算相对分子质量或相对分子质量之和1、A12(SO 4)3的相对分子质量=2、下列各相对分子质量的计算中,正确的是( ) A 、2MgO 的相对分子质量之和=2×24+16=64 B 、NO 2的相对分子质量=14×16×2=448C、2N的相对分子质量和=2(14+2)=32D、3O2的相对分子质量和=3×(16×2)=96二、根据化学式计算化合物中各元素的质量比(最简整数比)化合物中各元素的质量比等于各元素的相对原子质量的和之比1:计算硫酸铵【(NH4)2SO4】中各元素的原子个数比及各元素的质量比解:(NH4)2SO4中N、H、S、O原子个数比为:(NH4)2SO4中各元素的质量比:2、在H2SO4中氢、硫、氧三种元素的质量比的计算式正确的是( )A、(1×2):32:(16×4)B、1:32:16C、2:1:4D、(16×4):32:(1×2)三、计算化合物中某元素的质量分数例题:计算碳酸氢铵【NH4HCO3】中氮元素的质量分数。
化学式的书写专题训练

化学式的书写专题训练化学式的书写专题训练1金属单质:钾钙钠镁铝锌铁铜汞银2、稀有气体:氨气氛气氮气3、固态非金属单质:硫磷4、气态(液态)非金属单质:氢气氧气氮气5、氧化物:水双氧水二氧化碳一氧化碳二氧化硫二氧化氮二氧化硅五氧化二磷氧化钾氧化钙___________ 氧化钠_________ 氧化镁____________ 氧化铝________氧化锌___________ 氧化铁_______ 氧化亚铁___________ 四氧化三铁_______ 氧化铜________ 氧化亚铜________ 氧化汞___________ 二氧化镭__________ 6、酸(H ):盐酸硫酸硝酸碳酸磷酸7、碱(_OH)?氢氧化钾氢氧化钠氢氧化钙氢氧化镁氢氧化铁氢氧化锌氢氧化锁氢氧化铜氢氧化铝8、盐1)盐酸盐(_C1):氯化钾__________ 氯化钠__________ 氯化银__________ 氯化钙________ 氯化钞!氯化镁氯化锌氯化铝氯化亚铁氯化铁氯化铜氯化钱2)硫酸盐(_SOJ :硫酸钾硫酸钠硫酸钙硫酸顿硫酸镁硫酸锌硫酸铝硫酸铁硫酸亚铁硫酸铜硫酸讓写出下列物质的化学式(1)单质的化学式:铜,铁,汞,铝,硫,t ,磷氨气,氛气,氮气,氢气,氧气,氯气,氮气,碘,(2)化合物的化学式:①氧化物:氧化钠镁,9氧化钾,氧化钙氧化氧化铜,水,氧化铁,氧化亚铁氧化铝9②酸:硫酸,硝酸,盐酸,碳酸,磷酸9③氢氧化物:氢氧化钠,镁,氢氧化钾,氢氧化钙9氢氧化氢氧化铝,亚铁,氢氧化铜,氢氧化领,氢氧化铁氢氧化④氯化物:氯化钠,氯化钾,氯化锲,氯化钙,氯化铜9氯化铝,氯化钱,氯化亚铁,氯化银,⑤硝酸钠,硝酸钾, 硝酸铜9硝酸银9硝酸亚铁,硝酸铝, 硝酸汞9硝酸铁9⑥硫酸钾,硫酸铜,硫酸顿硫酸铝9硫酸锌,硫酸镁, 硫酸亚铁9硫酸铁9⑦氯化彼,硝酸彼, 硫酸钱9碳酸彼9⑧碳酸钾, 碳酸钙, 碳酸铝9碳酸锁f 镭酸钾高徭酸钾氯酸钾元素符号、化学式练习一.常见单质的书写1、氨气氛气氨气2、氢气氧气氮气氯气氟气漠碘3、金刚石铜磷石墨二.常见化合物的书写(一)1、水一氧化碳二氧化碳二氧化硫三氧化硫一氧化氮二氧化氮五氧化二磷过氧化氧2、氧化铜氧化钙氧化铁氧化铝氧化镁氧化钠四氧化三铁3、氯化氢硫化氢*氨气甲烷4、氯化钠氯化镁氯化钞!氯化钙氯化铜氯化铁氯化亚铁四.常见化合物的书写(二)1、硫酸盐酸硝酸碳酸2、氢氧化钠氢氧化钾氢氧化钞!氢氧化铜氢氧化铁氢氧化铝氢氧化钙氢氧化镁3、碳酸钙碳酸钠碳酸顿碳酸氢钠硫酸钠硫酸铜硫酸亚铁硫酸顿硝酸镀__________ 硝酸钾___________ 硝酸顿__________ 硝酸铜___________五、常见离子符号1、氯离子镁离子氧离子钠离子钙离子锁离子铝离子铁离子硫酸根硝酸根碳酸根氢氧根2、Fe2+HCO厂Cu2+NHZSO?-PO43-3、3个硫酸根2个锌离子六、符号的意义1、玄严表示________________________________“2C1”表示 _____________________________ ;“2Cb”表示 ___________________________ :2、“Fe”表示 _______________________________ 、3、“良0”表示 ______________________________4、下列符号的“2”各表示什么意义①H2②2H③2Hi?■④H.O⑤2CO⑥202⑦汨⑧MgO化学式练习题[日期:2012-01-04]來源:芳星园中学作者:饶利[字体:大中小]专题四:化学式的写法基础知识巩固:1、化学式的写法(1)单质化学式的书写直接用元素符号表示化学式的有_____________ 、 __________ :一般在元素符号的右下角标''2〃的有 _________(2)化合物化学式的书写i先读—写,后读—写。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学式书写练习
碳酸钠碳酸铁高锰酸钾
碳酸钡碳酸亚铁锰酸钾
碳酸钙碳酸铜亚硫酸钠
碳酸镁碳酸银亚硝酸钠
碳酸铝碳酸铵
常见离子符号
氢离子铵根离子钾离子钠离子钡离子
钙离子镁离子铝离子锌离子亚铁离子
铁离子铜离子银离子氯离子硝酸根离子
硫酸根离子氢氧根离子碳酸根离子
一、用化学用语填空
1、2个氧原子____2个氧离子 2个氧分子 2个硫酸分子
2、锌离子____ 镁离子氢离子银离子铜离子
氟离子钾离子钡离子钙离子硫离子
3、+2价的镁元素__________
4、2个氮分子__________
5、保持硫酸铜化学性质的粒子是_____构成氧化汞的微粒是
6、两个氦原子_________氖气氩原子
7、氧化钾的化学式__________
8、硫酸铁的化学式________常温下一种液态金属的化学式
9、硅元素______铅元素铂元素金元素
10、3个亚铁离子_______ 铁离子 3个碳酸分子
11、氧化铁中铁元素的化合价___硝酸铵中+5价的氮元素
12、铵根离子________4个氨分子_____铝离子 2个硫酸根离子____
硝酸根离子 m个碳酸根离子高锰酸根离子氢氧根离子
13、空气中含量最多的元素_____ 空气中含量最多的气体
二、按要求填空
1、FeSO4的名称__________ NaNO2的名称
2、构成氯化钠的微粒是________氯酸钾中的阴离子
3、右图表示的微粒是______ 画出氧原子的结构示意图
4、相对分子质量最小的氧化物________
5、人体含量最多的金属元素__________
6、地壳中含量最多的非金属元素与含量最高的金属元素组成的化合物___
7、KClO3中氯元素的化合价是_______ 3ClO2表示
8、O3中氧元素的化合价是______2Hg表示
9、Fe2+中“2”表示__________ Ca2+和S2-中“2”表示__________
10、过氧化氢中氧元素的化合价是__________。
