三氟化硼及硼酸的理化性质
三氟化硼乙酸作用机理-概述说明以及解释

三氟化硼乙酸作用机理-概述说明以及解释1.引言1.1 概述三氟化硼乙酸是一种常见的有机酸,其化学性质和反应机理引起了广泛的研究兴趣。
它具有特殊的结构和性质,能够参与多种有机化学反应,并在有机合成中发挥重要的作用。
首先,三氟化硼乙酸具有高度的酸性。
该化合物的酸性可归因于其氟化物离子的拉电子效应以及其硼-氧键的极性。
这使得它能够在反应中作为强酸进行质子转移反应以及催化反应。
由于其强酸性,三氟化硼乙酸在一些有机反应中可以替代其他酸进行催化,同时也可以促进其他有机分子的重排、环化和开环反应等。
其次,三氟化硼乙酸还具有良好的溶解性和稳定性。
由于其具有较高的极性,它能够溶解许多有机化合物,使其在反应中起到溶剂和催化剂的双重作用。
此外,三氟化硼乙酸在常温下具有较好的热稳定性和化学稳定性,能够在多种反应条件下保持其活性,使其在有机合成中具有广泛的应用前景。
最后,三氟化硼乙酸的反应机理多样且复杂。
它可以通过质子转移、酸碱催化、配体置换等多种方式参与反应。
其反应机理的深入研究可以帮助我们更好地理解和掌握有机化学反应的规律,并为合成新型有机分子提供理论指导和实验依据。
总之,三氟化硼乙酸作为一种具有特殊性质和结构的有机酸,在有机化学领域有着广泛的应用和深入的研究。
通过本文对三氟化硼乙酸的基本性质和化学反应机理的探讨,我们可以进一步揭示其作用机理,并为未来的研究提供一定的参考和指导。
1.2文章结构1.2 文章结构本文将按照以下结构进行论述三氟化硼乙酸的作用机理:第二章:正文2.1 三氟化硼乙酸的基本性质在本节中,我们将介绍三氟化硼乙酸的化学性质、物理性质以及在化学实验和工业应用中的常见用途。
我们将讨论三氟化硼乙酸的分子结构、溶解性、酸性、稳定性等方面的性质。
2.2 三氟化硼乙酸的化学反应机理这一节将深入探讨三氟化硼乙酸的反应机理。
我们将介绍三氟化硼乙酸参与的各种化学反应,包括其与有机化合物、无机化合物和水等的反应。
此外,我们还将研究不同条件下三氟化硼乙酸催化反应中的机理和速率控制步骤,以及反应中可能涉及的中间体形成和过渡态的形成。
三氟化硼;氟化硼化学品安全技术说明书MSDS
立即提起眼睑,用流动清水或生理盐水冲洗至少15分钟。就医。
吸入:
迅速脱离现场至空气新鲜处。保持呼吸道通畅。呼吸困难时给输氧。呼吸停止时,立即进行人工呼吸。就医。
防护措施
工程控制:
严加密闭,提供充分的局部排风和全面排风。
呼吸系统防护:
空气中浓度超标时,必须佩带防毒面具。紧急事态抢救或逃生时,建议佩带正压自给式呼吸器。
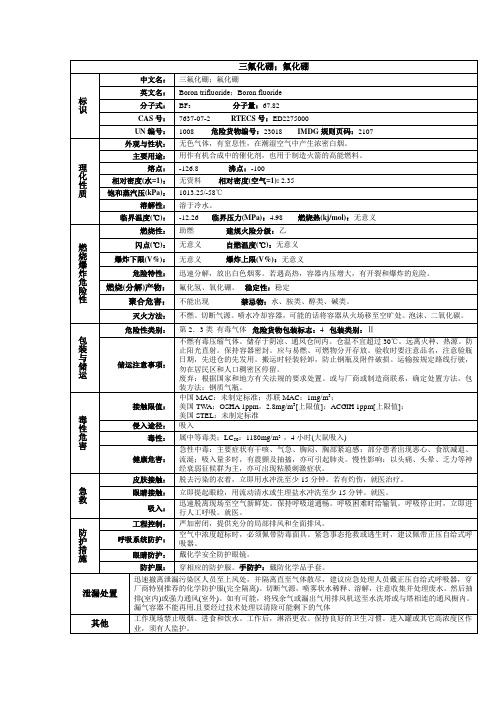
三氟化硼;氟化硼
标识
中文名:
三氟化硼;氟化硼
英文名:
Boron trifluoride;Boron fluoride
分子式:
BF3分子量:67.82
CAS号:
7637-07-2RTECS号:ED2275000
UN编号:
1008危险货物编号:23018IMDG规则页码:2107
理化性质
外观与性状:
无色气体,有窒息性,在潮湿空气中产生浓密白烟。
眼睛防护:
戴化学安全防护眼镜。
防护服:
穿相应的防护服。手防护:戴防化学品手套。
泄漏处置
迅速撤离泄漏污染区人员至上风处,并隔离直至气体散尽,建议应急处理人员戴正压自给式呼吸器,穿厂商特别推荐的化学防护服(完全隔离)。切断气源,喷雾状水稀释、溶解,注意收集并处理废水。然后抽排(室内)或强力通风(室外)。如有可能,将残余气或漏出气用排风机送至水洗塔或与塔相连的通风橱内。漏气容器不能再用,且要经过技术处理以清除可能剩下的气体
其他
工作现场禁止吸烟、进食和饮水。工作后,淋浴更衣。保持良好的卫生习惯。进入罐或其它高浓度区作业,须有人监护。
废弃:根据国家和地方有关法规的要求处置。或与厂商或制造商联系,确定处置方法。包装方法:钢质气瓶。
毒性危害
[新版]硼的制备和主要化学性质
![[新版]硼的制备和主要化学性质](https://img.taocdn.com/s3/m/fe2d7a58842458fb770bf78a6529647d26283441.png)
硼的制备和重要化学性质. 工业上一般是由硼镁矿制取硼砂,再由硼砂制取硼酸详见4.5.5.3. 若加热硼酸,脱水成B2O3,用镁或铝使之还原,可制得单质的硼。
此种条件下所制得的硼不纯,杂质为金属氧化物。
2H3BO3→B2O3+ 3H2O. B2O3+3Mg→2B+3MgO ...一、硼的存在與製備[return]1. 1.存在:硼於地殼中之含量僅0.001﹪,主要以硼酸鹽存於礦石中,由以硼砂(Na2B4O7.10H2O)最重要2. 2.製備(1)(1)多晶性的硼粉末是以金屬鎂在高溫下還原氧化硼(B2O3)而得B2O3(s)+3Mg(s)→2B(s)+3MgO(s),可以HCl(aq)除去MgO(2)(2)純度較高之黑色晶狀硼,則以氫氣於1000℃下還原三氯化硼(BCl3)而得2BCl3(s)+3H2(g)→2B(s)+6HCl(g)二、二、硼的性質與用途:硼與同族其他元素之物理性質均有顯著之不同[return]1. 1.元素硼是硬度很大的高熔點(~2300℃)物質2. 2.硼原子之電子組態為2s22p1,故氧化數與同族其他元素(如Al、Ga)一樣皆可為+3,但B因離子半徑小,游離能高,不易游離電子而與其他原子形成離子鍵(即離子化合物),故硼化物常呈共價性,如BF3等,此點與同族的鋁截然不同3. 3.常溫下,硼除了與氟(最強得氧化劑)及濃硝酸反應外,幾乎不予其他化合物反應2B+3F2→2BF3B+3HNO3(濃)→H3BO3+3NO24. 4.在高溫時,硼會與氧結合生成B2O3,與鹵素反應生成BX3(X=Cl、Br、I);亦可與不同的非金屬形成高硬度之硼化物(如碳化硼B12C3或氮化硼BN)4B+3O2→2B2O32B+3X2→2BX35. 5.元素硼與熔化的強鹼反應可生成硼酸鹽及氫氣2B(s)+6NaOH(l)→2Na3BO3(s)+3H2(g)6. 6.添加少量硼於金屬中會增強材料的硬度,並減低腐蝕性7.7.製造p-型半導體,常加入硼為電子對之受體三、三、硼的同素異性體[return]1. 1.硼有三種不同的同素異性體,除非晶性硼外,屬於晶體的部份有α-斜方硼、β-斜方硼及α-四方硼,均是以B12為基本組成單位的巨分子構造,故元素硼是硬度很大之高熔點物質2. 2.B12:(1)(1)12個硼原子形成一個20面體(2)(2)20面體有12個角,各角上均有一硼,每個面均為正三角形,呈幾何對稱,B的配位數為5(3)(3)各B原子間之共價鍵頗強(4)(4)各20面體間再以不同鍵結聯結成三種同素異性體四、四、硼的重要化合物[return]1. 1.硼酸H BO(1)(1)製備:由硼砂(Na2B4O7.10H2O)之水溶液酸化而得B4O72-+2H++5H2O→4H3BO3(2)(2)性質白色晶狀物質,熔點約為184℃‚為單質子弱酸H3BO3+H2O H++B(OH)4-,Ka=6.0×10-10ƒ硼酸可形成分子間氫鍵…硼酸受熱(169℃)可得偏硼酸H3BO3→HBO2+H2O(3)(3)用途:最為消毒劑及眼藥水之成份2. 2.四硼酸H2B4O7與硼砂Na2B4O7.10H2O(1)(1)H2B4O7為一種弱酸(2)(2)Na2B4O7.10H2O為四硼酸的鈉鹽俗稱硼砂,可由硼酸鹽之礦物製得,用於清潔劑及洗滌用之藥品(3)(3)硼砂之水溶液呈鹼性B4O72-+H2O 4H3BO3+2OH- (水解)3. 3.三氟化硼BF(1) (1) 具高腐蝕性的氣體(2) (2) 製備:由氧化硼、氟化鈣(CaF 2,俗稱螢石)與H 2SO 4反應而得B 2O 3(s)+3CaF 2(s)+3H 2SO 4(aq)→3BF 3(g)+3CaSO 4(s)+3H 2O (l)(3) (3) 可與NH 3起化合反應(由N 提供電子對給B)BF 3+NH 3B FFFN H H H,BF 3為路易士酸工業上常利用此種BF 3可接受電子之本性作為酸性觸媒以提煉石油4. 4. 碳化硼與氮化硼均為高熔點及高硬度之固體,其硬度僅次於鑽石,可用作研砵,研杵或磨石之用5. 5. B 2H 6乙硼烷或二硼烷由兩個BH 3形成三中心鍵之二聚體2BH 3 B 2H 6,為立體型分子B 軌域為sp 3,有兩個H(於平面之外),作為氫橋,餘為共價鍵。
各种硼化物 气化温度

各种硼化物气化温度
元素硼:元素硼在常温下为固态,气化温度为2500℃以上。
硼酸(H3BO3):硼酸在常温下为固态,其气化温度为200℃以上。
硼酸酐(B2O3):又称氧化硼、三氧化二硼,常温下为白色固体,无气味,有吸湿性。
气化温度在1800℃以上。
三氟化硼(BF3):在常态下三氟化硼是气体,气化温度为150℃左右。
三氯化硼(BCl3):在常态下三氯化硼是液体,沸点为12.9℃。
碳化硼(B4C):碳化硼在常温下为灰色固体,硬度仅次于金刚石,气化温度在2700℃以上。
氮化硼(BN):氮化硼在常温下为白色固体,具有超硬、耐高温、抗化学腐蚀等特性。
气化温度在3000℃以上。
铝硼合金:铝硼合金是一种金属间化合物,其气化温度取决于具体的成分和工艺条件,一般在1000℃以上。
铁硼合金:铁硼合金是一种具有高磁性能的合金材料,其气化温度通常在1200℃以上。
需要注意的是,这些气化温度可能会受到压力、气氛、杂质等因素的影响而有所变化。
因此在实际应用中,需要根据具体条件进行测定和评估。
三氟化硼乙醚络合物的理化性质和危险特性
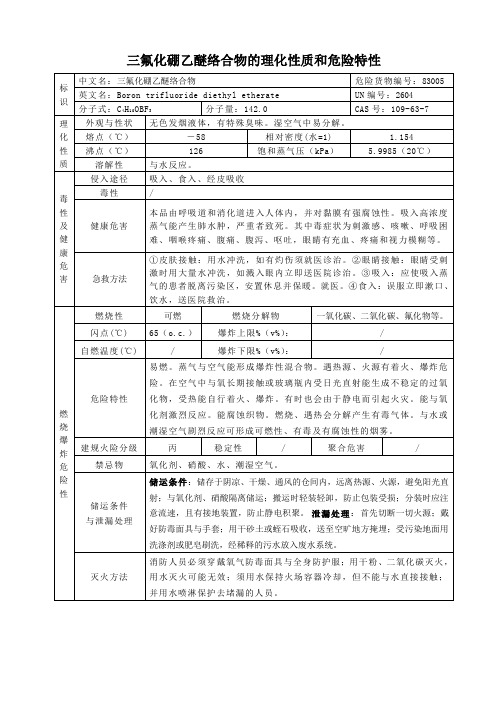
相对密度(水=1)
1.154
沸点(℃)
126
饱和蒸气压(kPa)
5.9985(20℃)
溶解性
与水反应。
毒性及健康危害
侵入途径
吸入、食入、经皮吸收
毒性
/
健康危害
本品由呼吸道和消化道进入人体内,并对黏膜有强腐蚀性。吸入高浓度蒸气能产生肺水肿,严重者致死。其中毒症状为刺激感、咳嗽、呼吸困难、咽喉疼痛、腹痛、腹泻、呕吐,眼睛有充血、疼痛和视力模糊等。
急救方法
①皮肤接触:用水冲洗,如有灼伤须就医诊治。②眼睛接触:眼睛受刺激时用大量水冲洗,如溅入眼内立即送医院诊治。③吸入:应使吸入蒸气的患者脱离污染区,安置休息并保暖。就医。④食入:误服立即漱口、饮水,送医院救治。
燃烧爆炸危险性
燃烧性
可燃
燃烧分解物
一氧化碳、二氧化碳、氟化物等。
闪点(℃)
65(o.c.)
三氟化硼乙醚络合物
标识
中文名:三氟化硼乙醚络合物
危险货物编号:83005
英文名:Boron trifluoride diethyl etherate
UN编号:2604
分子式:C4H10OBF3
分子量:142.0
CAS号:109-63-7
理化性质
外观与性状
无色发烟液体,有特殊臭味。湿空气中易分解。
熔点(℃)
爆炸上限%(v%):
/
自燃温度(℃)
/
爆炸下限%(v%):
/
危险特性
易燃。蒸气与空气能形成爆炸性混合物。遇热源、火源有着火、爆炸危险。在空气中与氧长期接触或玻璃瓶内受日光直射能生成不稳定的过氧化物,受热能自行着火、爆炸。有时也会由于静电而引起火灾。能与氧化剂激烈反应。能腐蚀织物。燃烧、遇热会分解产生有毒气体。与水或潮湿空气剧烈反应可形成可燃性、有毒及有腐蚀性的烟雾。
三氟化硼结构

三氟化硼结构三氟化硼(BF3)是一种无机化合物,具有三角形平面形状,是一种化学气体。
它的化学式为BF3,分子量为67.81g/mol。
三氟化硼的熔点为-127.8°C,沸点为-100.3°C。
在常温下,它是一种无色、无味、无毒的气体,其密度为1.24g/L。
三氟化硼分子的结构是三角形平面构型,由一个硼原子和三个氟原子组成。
硼原子处于分子平面的中心,三个氟原子在平面的三个角落上。
硼的轨道杂化为sp2,几何构型为三角形平面分子分子。
氟原子与硼原子通过共价键结合。
三氟化硼分子具有高度的惰性和不稳定性,是一种高反应性的化合物。
由于其带有不平衡的电子对,在空气中容易被水蒸气和空气中的其他分子攻击而分解,因此在实验室中通常要在氮气或氩气中进行。
三氟化硼的化学性质:三氟化硼是一种具有强酸性和强氧化性的气体,可以与氨等一些碱性物质反应,生成盐类。
它可以和各种有机化合物反应,从而发生氟化反应,有时能够完成芳香烃的氟化反应。
三氟化硼还能与一些配体形成配位化合物,形成分子配合物。
三氟化硼的工业应用三氟化硼主要用于无机合成、有机合成、催化剂、制备氟化物等方面。
其中,主要的应用包括:1. 用于冶炼金属和裂解纤维素等工艺中的催化剂。
2. 用于聚合物和脂肪酸的合成。
3. 用作原子化学气相沉积制备高质量硅等相关的化学合成过程。
4. 作为氟化剂来合成带有氟酰基的有机化合物。
总的来说,三氟化硼具有优异的化学性质和广泛的应用,其在工业中有着重要的地位。
同时,三氟化硼也是一个重要的研究对象,它的独特反应性质可以为化学研究提供宝贵的参考。
硼酸理化性质及危害特性

硼酸理化性质及危害特性硼酸是一种化学品,中文名称为硼酸,英文名称为boric acid,CAS号为-35-3,其分子式为H3BO3,分子量为61.84.该化学品的健康危害主要表现为口服引起急性中毒,包括胃肠道症状、脱水、休克、昏迷、急性肾功能衰竭等,重者甚至会导致死亡。
皮肤接触也会引起中毒,出现广泛鲜红色疹和剥脱性皮炎。
长期吸收小量该品会导致消化道症状、皮炎、秃发、肝肾损害等慢性中毒。
因此,该品的操作注意事项包括密闭操作、加强通风、佩戴自吸过滤式防尘口罩、化学安全防护眼镜、防毒物渗透工作服和橡胶手套等。
储存时应存放于阴凉、通风的库房,远离火源、热源,并与碱类、钾分开存放,切忌混储。
在紧急情况下,应该隔离泄漏污染区,限制出入,戴防尘面具(全面罩)、穿防毒服,用砂土、干燥石灰或苏打灰混合,小心扫起,转移至安全场所,若大量泄漏,用塑料布、帆布覆盖,收集回收或运至废物处理场所处置。
淋、高温。
在运输过程中,应遵守相关法规和规定。
为了保护自己的健康,我们需要采取一些预防措施。
其中之一就是在工作结束后要进行淋浴更衣,保持良好的卫生惯。
这可以有效地减少我们接触有害物质的机会。
这种化学物质的主要成分是纯品。
它的外观和性状是无色微带珍珠光泽的三斜晶体或白色粉末,具有滑腻手感,没有臭味。
其熔点为185℃(分解),沸点为300℃,相对密度为1.44(15℃)。
它可以溶于水,乙醇、乙醚和甘油。
这种化学物质有多种用途。
它可以用于玻璃、搪瓷、医药、化妆品等工业,也可以用于制备硼和硼酸盐,并且可以用作食品防腐剂和消毒剂等。
但需要注意的是,它不能与碱类、钾等物质混合使用。
这种化学物质的急性毒性和刺激性较低,但仍需注意安全使用。
对于废弃物的处置,应遵循国家和地方的相关法规,或与制造商联系确定正确的处理方法。
在运输过程中,应注意包装完整、稳妥,避免与碱类、钾、食品等混装混运,同时遵守相关法规和规定。
三氟化硼的特性及安全措施和应急处置原则

三氟化硼的特性及安全措施和应急处置原则三氟化硼,化学式为BF3,是一种无色、有刺激性的气体。
它具有以下特性:
1. 强的酸性:三氟化硼在水中会形成强酸——氢氟酸,具有强烈的刺激性和腐蚀性,对皮肤、眼睛、呼吸道等部位都有较大的危害。
2. 低沸点:三氟化硼在常压下沸点为-100℃,易于气态扩散,有爆炸危险。
3. 可燃性:三氟化硼具有一定的可燃性,不能与有机物混合使用,避免发生火灾和爆炸事故。
在使用三氟化硼时,应当采取以下安全措施:
1. 注意通风:使用三氟化硼时必须在通风良好的地方进行,防止气体积聚而引发事故。
2. 使用防护措施:应当穿戴防护眼镜和手套等防护措施,避免接触到身体而引起损伤。
3. 避免混合使用:三氟化硼不应与有机物混合使用,以免引起化学反应,导致事故发生。
在发生三氟化硼泄漏事故时,应当采取应急处置措施:
1. 疏散周围人员:及时将周围的人员疏散到安全区域。
2. 切断气源:尽可能地切断三氟化硼的气源,以避免事故的进一步扩大。
3. 空气监测:使用气体检测仪等工具对气体进行监测,确定泄漏物质的浓度和范围。
4. 启动应急处理计划:按照事先制定好的应急处理计划,采取相应的措施进行处理,控制泄漏、清除污染等。
三氟化硼是一种具有危险性的化学品,应当在使用过程中注意安全措施,一旦发生事故应当迅速采取应急处置措施,以保障人员的安全。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三氟化硼及硼酸的理化性质
1、三氟化硼理化性质
三氟化硼(Boron trifluoride)是一种无色气体,吸入可窒息。
其可与潮湿空气发生化学反应而生成白色烟雾。
三氟化硼的晶体结构是平面三角形。
其中的硼原子受极性共价键作用,且为spasp杂化,使其分子间结构具备一定的对称性,偶极矩被完全抵消,表现为非极性分子性质。
三氟化硼性质较为活泼,能与多种物质反应,其理化性质见表1。
表1三氟化硼理化性质
三氟化硼易溶于浓硫酸、三氯甲烷和四氯化碳等常见有机溶剂,可以与水反应而生成氟硼酸和硼酸,是放热反应。
三氟化硼气体可与某些金属及有机物发生反应,亦可与某些物质发生加成反应或络合反应。
其酸碱性表现为路易斯酸,因此可与氟化物或醚类物质发生酸碱反应。
三氟化硼能作为酯化、烷基化等有机反应的催化剂,也能作为防氧化剂来生产某些合金,其作为原料亦可生产卤化硼、单质硼、硼烷等硼相关产品。
高纯三氟化硼在电子、核工业及光纤工业中有重要的应用,同时作为重要掺杂源,在半导体工艺中也有广泛的应用。
除此之外,硼化合物可以作为固化剂应用于环氧树脂中,在光纤预制件中也有一定使用。
三氟化硼是一种高毒物质,兼具硼与氟化氢两者毒性,气体具有强刺激性,在加热条件
下或接触潮湿空气会发生反应而生成有毒且有腐蚀性的白烟(HF) ,可以腐蚀眼睛、皮肤等器官,如不慎吸入毒烟可导致死亡。
与其接触后表观感受为咽喉刺痛、呼吸困难、视力模糊等症状。
2、硼酸理化性质
硼酸(H}BO})多为白色粉末状晶体,味微酸而略带甜味,相对密度1.43 5g/cm3(15℃),熔点185℃(可分解),3 00℃时失水而生成硼醉,无臭味。
能溶于常见有机溶剂中,如酒精、乙醚、甘油等。
硼酸在水中的溶解度与温度成正比,常温下,其溶解度较低。
同时,硼酸在溶液中的溶解度会因某些无机酸的存在而显著降低。
硼酸作为溶质通常不解离,以B(OH)3分子的形式存在于水溶液中,而在某些硼酸盐溶液中则通常以B(OH)4一离子的形式存在。
通常,硼酸在其水溶液中会按式(1)进行电离:
(1)
硼酸溶液具有一定的挥发性。
常压下,沸腾的硼酸水溶液产生的蒸汽中,有约千分之三浓度的硼酸随蒸汽挥发而损失。
硼酸在176℃, 201℃和236℃时可分别生成三种不同变体。
加热硼酸至107.5℃时,如上文的氧化硼三水合物会失去部分结晶水,首先生成偏硼酸,继续失去部分结晶水而最终生成正硼酸。
随着结晶水的失去,挥发性随之增大,在3 00℃时完全失去结晶水而生成硼酸醉(B203),如果继续加热,会继续脱水完全而最终生成氧化硼,其完全熔化的温度为450℃。
将无定型氧化硼加热至325℃时开始软化,当温度升高至500℃时则以液态形式存在,因此,熔点对于无定型氧化硼来说是不固定的。
硼酸是一元弱酸,电离常数为,当其分子浓度达到0.llg时,溶液的pH约为5左右。
因此,可利用置换反应以某些无机酸为原料来制备硼酸,无机酸亦可选择某些弱酸,如碳酸及硫化氢之类仍可保证置换反应进行。
某些多经基化合物可以与硼酸进行反应而生成硼酸络合物,由于络合物离解度较大,因此一定程度上强化了硼酸的酸性。
如甘
露醇与硼酸反应生成的络合物离解常数为,比硼酸的电离常数高104倍。
硼酸水溶液中加入某些中性盐也可以大大提高其酸性,尤其是某些含高水合物的中性盐。
硼酸在某些酸作为催化剂或脱水剂存在下可以与某些低级醇反应而生成酯化物。
例如,在浓硫酸存在时,硼酸会与甲醇反应生成硼酸三甲酯。
硼酸作为反应物可与HF发生反应而生成一种中,同时硼酸与氢氧化物或金属氧化物亦可形成氟硼酸盐。
硼酸也会和磷酸反应生成磷酸硼,此时的硼酸会表现出微弱的碱性。
硼酸有毒,会影响消化器官及神经中枢等人体组织。
吸入硼酸的中毒表现为食欲不振、腹痛腹泻、虚脱等症状。
最低致死量:皮肤接触8600mg/kg,口服640mg/kg,静脉注射29mg/kg,最高允许浓度为l0mg/m3。
