卡尔费休水分测定原始记录
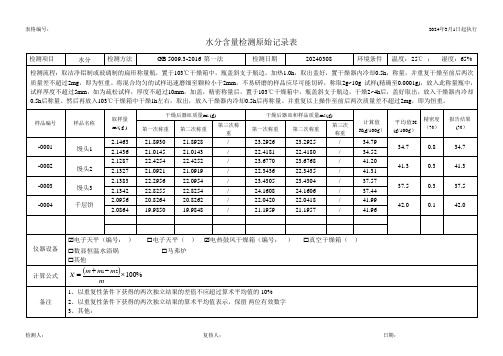
水分含量检测原始记录表
/
22.4181
22.4180
/
23.6770
23.6768
/
22.3436
22.3435
/
23.4305
23.4304
/
24.1608
24.1606
/
22.0420
22.0418
/
21.1959
21.1957
/
计算值 X(g/100g)
34.79 34.52 41.20 41.31 37.57 37.44 41.99 41.96
平均值X 精密度 (g/100g) (%)
34.7
0.8
41.3
0.3
37.5
0.3
42.0
0.1
报告结果 (%)
34.7 41.3 37.5 42.0
仪器设备 计算公式
备注
电子天平(编号: ) 电子天平( ) 电热鼓风干燥箱(编号: )
数显恒温水浴锅 其他
X m m1 m2 100%
m
马弗炉
1、以重复性条件下获得的两次独立结果的差值不应超过算术平均值的 10% 2、以重复性条件下获得的两次独立结果的算术平均值表示,保留 两位有效数字 3、其他:
真空干燥箱( )
检测人:
复核人:
日期:
样品编号
-0001 -0002 -0003 -0004
样品名称
馒头1 馒头2 馒头3 千层饼
取样量 m/( g )
2.1463 2.1436 2.1287 2.1327 2.1383 2.1342 2.0956 2.0864
干燥后器皿质称重
第三次称 重
21.8930
21.8928
/
卡尔费休法测水分

卡尔费休自动滴定仪
双炉串联型或互换型
带三通阀的气体入口
滴定
用单刻度移液管量取10ml的甲醇样品萃取液至滴定管中,进行滴定。滴定结束后,排出滴定液并用甲醇清洗滴定瓶。重复滴定,计算含水量,若两次结果差值不大于0.5%,计算平均值,否则重复测定。
用滴定管向吸收池中缓慢加入卡尔费休溶液。在迅速变化点上选择一电流(30μA~40μA)作终点。继续滴定至此电流保持30s为止。每隔10min加一次卡尔费休溶液,直到恢复初测电流值并维持30s,它所需的增加量不大于0.05ml.
在105℃±2℃的氮气中加热预干燥使吸湿水释放出来。继续在另一950℃炉内加热,用乙二醇—甲醇混合液收集释放的化合水。
试样粒度小于100μm
取样过程中保证气流温度高于露点温度,必要时取样装置可加热。
试剂
分析纯试剂
三级水
无吡啶卡尔费休试剂
分析纯试剂
去离子水或同等பைடு நூலகம்度的水
卡尔费休试剂在使用当日需标定
卡尔费休专用试剂
卡尔费休法测水分
被测物
项目
烟草及烟草制品
GB/T 23357-2009
铁矿石化合物
GB/T 24190-2009
天然气(库伦法)
GB/T 18619.1-2002
可测含水量
2%~55%
0.05%~10%
5mg/cm3~5000mg/cm3
样品前处理
无水甲醇震荡萃取
样品粒径小雨4mm(不能研磨剪切,可能造成水分的损失,可惨用低温技术予以处理)
打开电磁搅拌器,通过三通阀吹扫样品管线,并放空至大气。转动三通阀使气体直接进入滴定池,并将气体流速调节到30L/h之间。用湿式气体流量计在滴定池出口测量气体流速,气体的进样体积取决于其水含量。当预定体积的气体通过滴定池后,将三通阀转向先前的位置。
karl fisher

水分测定
1935年卡尔 费休 年卡尔·费休 年卡尔 费休(KarlFj scher) 提出的测定水分的容量分拆方法 提出的测定水分的容量分拆方法
Karl fisher
费休法是对水最专一、 费休法是对水最专一、 最专一 最准确的方法 最准确的方法
经改进,提高了准确度, 经改进,提高了准确度,扩大了 测量范围, 测量范围,已被列为许多物质 中水分测定的标准方法 中水分测定的标准方法
C
注意的损失
搅拌充分且 均匀 注意被测定的 试样中是否有 能与卡尔费休试剂 足够的吡啶 生成水的物质 和甲醇量
D
定 仪 器 好 的 测
综上所述
操 作 细 心
测 量 结 果
准 确 的
目录
滴定原理 滴定步骤 注意事项 综上所述
A
滴定原理
I2十S02十2H2O=2HI十 I2十S02十2H2O=2HI十H2SO4
费休试剂
碘 1:
二氧化 硫
吡啶 3:
甲醇 1
1:
B
滴定步骤
取样时应尽量取均匀有代表性的样品 对于无色试液可用目视法判定, 一般采用的摩尔比为碘:二氧化硫:吡啶: 由于化合物性质的差异 ,故在测定前 根据试样含水量的多少决定取样量大小 如果是带有颜色或呈浑浊状的试液 甲醇=1:3:10:50 需对其分类,从而选择直接或非直接的 特别要注意进样时注射器中是否存在小 ,则需用水停滴走法或电位滴定法 标定方法一般有纯水标定、含水甲酵标准溶 测定方法 气泡, 以防产生严重的测量误差 判定终点 液标定和稳定的结晶水合物标定三种
卡尔费休水分测定全面信息

卡尔费休氏水分测定法对样品中水分的含量测定建立在R.W.Bunsen描述的下面这个反应上:I2+SO2+2H2O 2HI+H2SO4Karl Fischer首先发现这个反应可以在非水环境中用来测定水分含量,反应系统中包含有过量的SO2,甲醇可以被选作理想的溶剂。
但反应是可逆的,为了使反应向右进行,Karl Fischer用吡啶来吸收反应生成的HI和H2SO4.Smith,Bryanz 和 Mitchell 将这个反应描述成两步:I2+SO2+H2O+3B5C5N → 2B5C5NH+I- + B5C5N.SO3B 5C5N.SO3+CH3OH → B5C5N H+CH3SO4-在第一步反应中,KF试剂和水反应生成的B5C5N.SO3不稳定,容易分解成吡啶和二氧化硫,甲醇可以和其反应生成稳定的B5C5N H+CH3SO4-。
由此可见,甲醇作溶剂有防止副反应发生的作用。
在醇溶剂中,碘和水反应的化学计量数为1:1。
在无醇的溶剂中,碘和水反应的化学计量数为1:2:I 2+SO2+H2O+3 B5C5N → 2 B5C5N H+I- + B5C5N.SO3(不稳定)B 5C5N.SO3+H2O → B5C5N H+HSO4-(稳定)卡尔.费休试剂的基本成份是碘、二氧化硫、溶剂和有机碱,溶剂主要是醇类。
通常,试剂中二氧化硫、有机碱和醇类物质都是过量的,试剂中碘与水以固定的化学计量数1:1进行反应,所以我们在进行实验前应先确定滴定剂中碘的浓度,也即对滴定剂进行标定,这是本实验定量的基础。
用已知浓度的卡氏试剂滴定样品中的水分,由消耗滴定剂的体积和称样量,即可求出样品的含水量。
以前,卡氏试剂中用的有机碱主要是有毒、恶臭的吡啶,但更重要的是如果我们不能确定反应到底受那些方面的影响的话,我们就无法用其来进行定量分析。
后来,E.Barenrecht和J.Cverhoff对Karl Fisher反应进行了更进一步的研究后,得出了如下结论:◎吡啶不直接参加反应,也就是说它只起调节PH值和缓冲剂的作用,可以用其它的有机碱替代。
卡尔费休法测定丙酮中微量水分

412 PCO2 垂直分布:在船上在20 ℃浴温下做平衡,得出的PCO2 ( 20 ℃) 垂直分布如图2a 。
换算到现场温度下PCO2 如图2b 。
PCO2 ( 现场) 随深度变化与TC O2 相似, 也在300 —400m 达最大值。
由温度降低造成向下减少,在135°E 以西与TC O2 一致。
从表层到1000m TCO2 值小于停泊点值。
停泊点上: 0 —100m , PCO2 ( 20 ℃) 在400m 可达1000uat m 左右,500m 出现个最小值, 以后又增加, 从600m 以下变化不大。
11 月26 日—11 月30 日, 再到2 月份, PCO2 值逐步减少。
垂直分布规律与以前相同。
从PCO2 (现场温度) 与TCO2 的关系图(图略) 可见在现场温度下当PCO2 大于μat m , TCO2 小于μmo l/ kg , 即对应着400m 以下深度时, PCO2 与TCO2 呈正相关趋势。
400m 以上与TCO2 不成正相关且PCO2 变化范围很大,显然是由于上层水温度变化影响增大的缘故。
参考文献:1 David W. Chip man and Jo hn G o ddard , Tachnical manual f o r ga schro matograp hic syst em f o r high p recisio n measurement of carbo n dio xide partical p ressures in discret e ocean wat er and air samples , R , New Y o r k , L amo nt - D o hert y G e ological Observato ry of Columb.马黎明,热带西太平洋海—气C02 交换与碳化学量的分布〈, 热带西太平洋海气相互作用综合研究〉M , 北京, 海洋出版社, 1993 ,156 - 173 .乔然, 马黎明, 张滨, 高精度测量海水和大气二氧化碳分压( PC02) 气相色谱系统的完善和应用, C , 微量元素研究进展( 1995 . 07) ,北京,化学工业出版社,1995 ,229 - 234 .乔然,海水二氧化碳分压的取样手段和分析计算方法, J , 北京, 海洋预报,1993 ,1 ( 1) 1 ,77 - 79 .234卡尔2费休法测定丙酮中微量水分代丽斌(北京燕山石油化工公司研究院,北京102500)摘要:本文采用乙二醇甲醚、吡啶、二氧化硫和碘配制成卡尔2费休试剂,在以乙二醇甲醚与吡啶( 4¬1) 的混和液作为本底溶剂的条件下,用其测定丙酮中的水分。
容量法卡尔费休法测定硬糖样品中水分的含量

容量法卡尔费休法测定硬糖样品中水分的含量
目的:
本实验用甲醇和甲酰胺的混合溶液作为溶剂增加硬糖样品在溶剂中的溶解度,使用AKF-1水分仪直接测定硬糖中水分的含量,验证AKF-1在硬糖样品中水分检测的可行性、准确度和重复性。
仪器配置:
1、AKF-1卡尔费休水份测定仪主机;
2、全封闭安全滴定池组件;
3、双铂片电极
4、滴定池搅拌台
5、10μL微量进样针
6、电子天平(0.1mg)
试剂:
1、滴定剂:容量法单组份卡尔费休试剂
2、溶剂:无水甲醇
3、辅助试剂:甲酰胺
测定方法:
1、向滴定池内加入甲醇和甲酰胺的混合溶液(甲醇:甲酰胺=2:1);
2、使用仪器中“标定”选项的“打空白”功能滴定至终点,彻底除去滴定池和
溶剂中的水分;
3、选择“试剂标定”功能,用经过干燥处理的微量进样针精确抽取10 μL纯水,
拭干针头后将针头插入滴定池内加样,加样结束后输入加样质量为10 mg,开始标定;
4、重复步骤3,反复测量3-5次,仪器后自动保存标定结果并计算出平均值作为
试剂的滴定度;
5、将硬糖样品用研钵粉碎细化后,称取硬糖样品约0.3 g加入滴定池,将样品的
进样质量输入仪器,并开始测量。
仪器参数
1、计量管体积:20 mL
2、终点电流值:60 μA
3、最小进液量:0.002 mL
4、滴定延时:90 s
5、终点延时:10 s
6、漂移扣除:On
7、终点保持:On
卡尔费休水份测定仪样品测定记录。
卡尔费休水分测定---原始记录
数
据
处
理
编号
样品
□质量m,g
□体积V2,μL
试样耗卡尔.费休体积V1,mL
V1平均值
结果计算
□X=(V1×T)/m*100 □X=(V1×T)/(V2×ρ)*100
样品结果:
编号
X%
T=M/V最低检出限浓度为____;液体样品的密度ρ=____g/mL
备注
(1)水分含量≥1g/100g时,计算结果保留三位有效数字,水分含量<1g/100g时,计算结果保留两位有效数字:
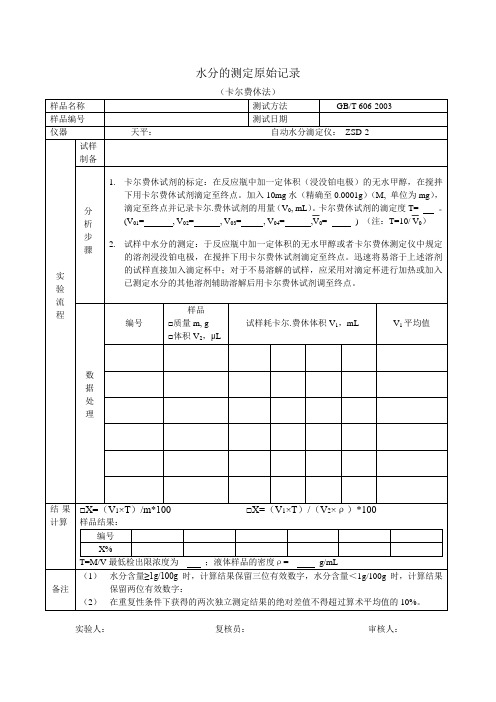
水分的测定原始记录
(卡尔费休法)
样品名称
测试方法
GB/T 606-2003
样品编号
测试日期
仪器
天平:自动水分滴定仪:ZSD-2
实
验
流
程
试样
制备
分ห้องสมุดไป่ตู้
析
步
骤
1. 卡尔费休试剂的标定:在反应瓶中加一定体积(浸没铂电极)的无水甲醇,在搅拌下用卡尔费休试剂滴定至终点。加入10mg水(精确至0.0001g)(M,单位为mg),滴定至终点并记录卡尔.费休试剂的用量(V0,mL)。卡尔费休试剂的滴定度T=____。(V01=__,V02=,V03=,V04=,V0=____)(注:T=10/V0)
(2)在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
实验人:复核员:审核人:
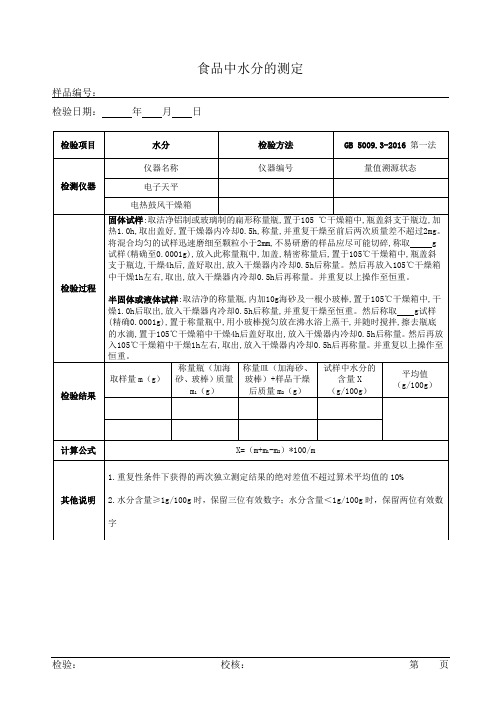
食品水分原始记录
样品编号:
检验项目
水分
检验方法
GB 5009.3-2016第一法
检测仪器
仪器名称
仪器编号
量值溯源状态
电子天平
电热鼓风干燥箱
检验过程
固体试样:取洁净铝制或玻璃制的扁形称量瓶,置于105℃干燥箱中,瓶盖斜支于瓶边,加热1.0h,取出盖好,置干燥器内冷却0.5h,称量,并重复干燥至前后两次质量差不超过2mg。将混合均匀的试样迅速磨细至颗粒小于2mm,不易研磨的样品应尽可能切碎,称取g试样(精确至0.0001g),放入此称量瓶中,加盖,精密称量后,置于105℃干燥箱中,瓶盖斜支于瓶边,干燥4h后,盖好取出,放入干燥器内冷却0.5h后称量。然后再放入105℃干燥箱中干燥1h左右,取出,放入干燥器内冷却0.5h后再称量。并重复以上操作至恒重。
半固体或液体试样:取洁净的称量瓶,内加10g海砂及一根小玻棒,置于105℃干燥箱中,干燥1.0h后取出,放入干燥器内冷却0.5h后称量,并重复干燥至恒重。然后称取g试样(精确0.0001g),置于称量瓶中,用小玻棒搅匀放在沸水浴上蒸干,并随时搅拌,擦去瓶底的水滴,置于105℃干燥箱中干燥4h后盖好取出,放入干燥器内冷却0.5h后称量。然后再放入105℃干燥箱中干燥1h左右,取出,放入干燥器内冷却0.5h后再称量。并重复以上操作至恒重。
样品编号:
检验日期:年月日
检验项目
水分
检验方法
GB 5009.3-2016第三法
检测仪器
仪器名称仪器编号Βιβλιοθήκη 量值溯源状态电子天平
试剂配制
甲苯或二甲苯制备:取甲苯或二甲苯,先以水饱和后,分去水层,进行蒸馏,收集馏出液备用。
检验过程
试样制备:粉末和结晶试样直接称取;较大块硬糖经研钵粉碎,混匀备用。
