反应工程习题答案
化学反应工程练习题解答

第一章习题1有一反响在间歇反响器中进行,经过8min 后,反响物转化掉80%,经过18min 后,转化掉90%,求表达此反响的动力学方程式。
解2A A min 18A0min 8A0AA A0d d 219.019.0181)(218.018.081)(11kc tc kc kc x x c kt =-=-⋅==-⋅=-⋅=为假设正确,动力学方程 2在间歇搅拌槽式反响器中,用醋酸与丁醇生产醋酸丁酯,反响式为:()()()()S R B A O H H COOC CH OH H C COOH CH 2943SO H 94342+−−→−+反响物配比为:A(mol):B(mol)=1:4.97,反响在100℃下进行。
A 转化率达50%需要时间为24.6min ,辅助生产时间为30min ,每天生产2400kg 醋酸丁酯〔忽略别离损失〕,计算反响器体积。
混合物密度为750kg·m -3,反响器装填系数为0.75。
解3313111111i 1.2m 0.750.8949总体积反应0.8949m 0.910.9834有效体积反应0.91hr6054.6折合54.6min 3024.6总生产时间hr 0.9834m 750737.5换算成体积流量hr 737.5kg 634.1103.4总投料量hr 634.1kg 744.97724.1B 4.97:1B :A hr 103.4kg 601.724折算成质hr 1.724kmol 0.50.862的投料量A ,则50%转化率hr 0.862kmol 116100hr 100kg 2400/24R 116 74 60 M S R B A ==⨯==+=⋅=+⋅=⨯⨯=⋅=⨯⋅=⋅=⋅=+→+-------器器投料量则量流量产量3反响(CH 3CO)2O+H 2O →2CH 3COOH 在间歇反响器中15℃下进行。
一次参加反响物料50kg ,其中(CH 3CO)2O 的浓度为216mol·m -3,物料密度为1050kg·m -3。
反应工程课后习题参考答案

1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+ 32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)反应的选择性;(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),当进入反应器的总原料量为100mol 时,则反应器的进料组成为2由甲醇的转化率达72%2y x +=72%; 4.27x=69.2% 解得x=18.96; y=0.77 所以,反应器出口气体组成为: CH 3OH:%100221004.27⨯++--y x yx =6.983%空气:%1002210023279.54⨯++--y x y x =40.19% 水: %10022100281.17⨯++++y x y x =34.87%HCHO: %10022100⨯++y x x=17.26%CO 2: %10022100⨯++y x y=0.6983%1.2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩机后与原料气混合返回合成塔中。
下图是生产流程示意图放空气体 Akmol/h原料气和冷凝分离后的气体组成如下:组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 21.460.82CH40.55 3.62N22.92 10.29粗甲醇的组成为CH3OH 89.15%,(CH3)2O 3.55%,C3H9OH 1.10%,H2O 6.20%,均为重量百分率。
(完整版)化学反应工程课后习题答案.

积分之
2.10在催化剂上进行三甲基苯的氢解反应:
反应器进口原料气组成为66.67%H2,33.33%三甲基苯。在0.1Mpa及523K下等温反应,当反应器出口三甲基苯的转化率为80%时,其混合气体的氢含量为20%,试求:
(1)(1)此时反应器出口的气体组成。
(2)(2)若这两个反应的动力学方程分别为:
组分
摩尔分率yi0
摩尔数ni0(mol)
CH3OH
2/(2+4+1.3)=0.2740
27.40
空气
4/(2+4+1.3)=0.5479
54.79
水
1.3/(2+4+1.3)=0.1781
17.81
总计
1.000
100.0
设甲醇的转化率为XA,甲醛的收率为YP,根据(1.3)和(1.5)式可得反应器出口甲醇、甲醛和二氧化碳的摩尔数nA、nP和nc分别为:
组分
摩尔质量
摩尔分率yi
CO
28
15.49
H2
2
69.78
CO2
44
0.82
CH4
16
3.62
N2
28
10.29
总计
100
其中冷凝分离后气体平均分子量为
M’m=∑yiMi=9.554
又设放空气体流量为Akmol/h,粗甲醇的流量为Bkg/h。对整个系统的N2作衡算得:
5.38B/28×1000+0.1029A=2.92 (A)
20
30
40
50
60
70
试求当进口原料气体流量为50ml/min时CO的转化速率。
解:是一个流动反应器,其反应速率式可用(2.7)式来表示
化学反应工程课后习题答案

1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)(1)反应的选择性;(2)(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),当进入反应器的总原料量为100mol设甲醇的转化率为X A,甲醛的收率为Y P,根据(1.3)和(1.5)式可得反应器出口甲醇、甲醛和二氧化碳的摩尔数n A、n P和n c分别为:n A=n A0(1-X A)=7.672 moln P=n A0Y P=18.96 moln C=n A0(X A-Y P)=0.7672 mol结合上述反应的化学计量式,水(n W)、氧气(n O)和氮气(n N)的摩尔数分别为:n W=n W0+n P+2n C=38.30 moln O=n O0-1/2n P-3/2n C=0.8788 moln N=n N0=43.28 mol所以,反应器出口气体组成为:1. 1.2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩机后与原料气混合返回合成塔中。
下图是生产流程示意图原料气Bkg/h 粗甲醇Akmol/h100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 22.9210.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。
(完整版)反应工程课后答案完整版.
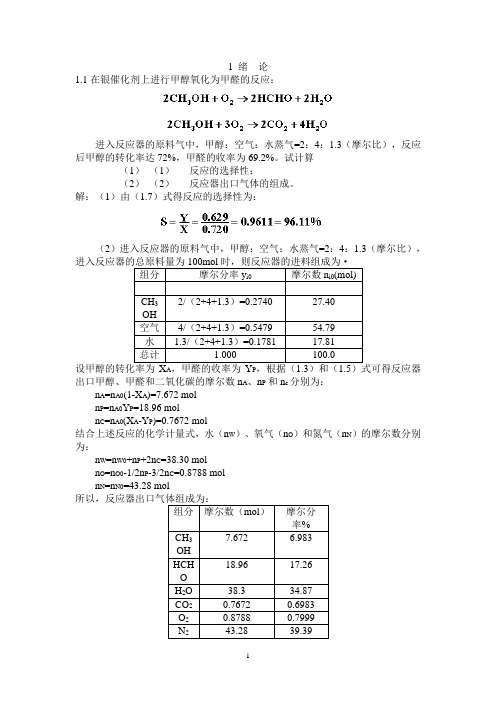
1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)(1)反应的选择性;(2)(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),组分摩尔分率y i0 摩尔数n i0(mol)CH32/(2+4+1.3)=0.2740 27.40OH空气4/(2+4+1.3)=0.5479 54.79水 1.3/(2+4+1.3)=0.1781 17.81总计 1.000 100.0A P出口甲醇、甲醛和二氧化碳的摩尔数n A、n P和n c分别为:n A=n A0(1-X A)=7.672 moln P=n A0Y P=18.96 moln C=n A0(X A-Y P)=0.7672 mol结合上述反应的化学计量式,水(n W)、氧气(n O)和氮气(n N)的摩尔数分别为:n W=n W0+n P+2n C=38.30 moln O=n O0-1/2n P-3/2n C=0.8788 moln N=n N0=43.28 mol组分摩尔数(mol)摩尔分率%7.672 6.983CH3OH18.96 17.26HCHOH2O 38.3 34.87CO2 0.7672 0.6983O2 0.8788 0.7999N2 43.28 39.392 反应动力学基础2.4在等温下进行液相反应A+B→C+D,在该条件下的反应速率方程为:若将A和B的初始浓度均为3mol/l的原料混合进行反应,求反应4min时A的转化率。
解:由题中条件知是个等容反应过程,且A和B的初始浓度均相等,即为1.5mol/l,故可把反应速率式简化,得由(2.6)式可知代入速率方程式化简整理得积分得解得X A=82.76%。
2.6下面是两个反应的T-X图,图中AB是平衡曲线,NP是最佳温度曲线,AM是等温线,HB是等转化率线。
化学反应工程教材课后习题答案-李绍芬-天津大学

0.76 6.1
0.125mol
/
l .h
由(2.6)式可知反应物的水解速率为
rA
dC A dt
0.125mol
/ l.h
2.2 在一管式反应器中常压 300℃等温下进行甲烷化反应:
CO 3H2 CH4 H2O
催化剂体积为 10ml,原料气中 CO 的含量为 3%,其余为 N2,H2 气体,改变进口原料 气流量 Q0 进行实验,测得出口 CO 的转化率为:
0.65 0.04 0.34
1.79
故 CO 的转化速率为
C A0
PA0 RT
0.1013 0.03 8.314 103 573
6.38 104 mol / l
rA
C A0
dX A d (VR / Q0
)
6.38
104
1.79
1.14
103
mol
/
l . min
2.3 已知在 Fe-Mg 催化剂上水煤气变换反应的正反应动力学方程为:
解:利用(2.10)式及(2.28)式可求得问题的解。注意题中所给比表面的 单位换算成 m2/m3。
(1)kv bkw 1.13 103 0.0535 60.46kmol / m3 .h
(2)kg
b av
kw
b
b 30 103
kw
1.78 106kmol
/ m2.h
(3)k p
(
1 P
1绪 论
1.1 在银催化剂上进行甲醇氧化为甲醛的反应:
2CH3OH O2 2HCHO 2H2O 2CH3OH 3O2 2CO2 4H2O
李绍芬《反应工程》课后习题答案

李绍芬《反应工程》课后习题答案1 绪 论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+ 32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1) (1) 反应的选择性;(2) (2) 反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),组分 摩尔分率y i0 摩尔数n i0(mol) CH 3OH 2/(2+4+1.3)=0.2740 27.40 空气 4/(2+4+1.3)=0.5479 54.79 水 1.3/(2+4+1.3)=0.1781 17.81 总计 1.000 100.0A P 出口甲醇、甲醛和二氧化碳的摩尔数n A 、n P 和n c 分别为:n A =n A0(1-X A )=7.672 mol n P =n A0Y P =18.96 moln C =n A0(X A -Y P )=0.7672 mol结合上述反应的化学计量式,水(n W )、氧气(n O )和氮气(n N )的摩尔数分别为:n W =n W0+n P +2n C =38.30 mol n O =n O0-1/2n P -3/2n C =0.8788 mol n N =n N0=43.28 mol组分 摩尔数(mol ) 摩尔分率% CH 3OH 7.672 6.983 HCHO 18.96 17.26 H 2O 38.3 34.87 CO 2 0.7672 0.6983 O 2 0.8788 0.7999 N 2 43.28 39.391. 1. 2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+ 242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩原料气 Bkg/h 粗甲醇 Akmol/h100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 2 2.92 10.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。
化学反应工程习题答案__梁斌

习题2.5
CNO
PNO RT
CO 2
PO2 RT
rA
kcCNO2CO 2
kc
PNO RT
2
PO2 RT
kc RT
P P2
3 NO O2
• 反应速率常数的kp值:
kP
kc
RT 3
1.661012
m3
mol s Pa3
• 知识点:化学反应速率常数
习题2.6
• 有一反应,已知下列速率常数:
惰性物料是否存在无关.
习题2.5
• NO和O2氧化为NO2的反应是一个三级反 应,2NO+O2=2NO2,在30℃及1kg/cm2下测得 其反应速率常数为kc=2.65×104 L2/(mol2·s). 如果将速率方程表示为分压的函 数:rA=kppNO2pO2,请问反应速率常数的kp值和单 位是什么?
习题2.7
• CH3COOH+C2H5OH=H2O+CH3COOC2H5
• CA0
CB0
Cp0
t=0
• CA0(1-x) CB0-CA0x Cp0+CA0x CA0x
t=t
rA
dCA dt
k1CA0 (1 x)(CB0
CA0 x) k2 (Cp0
CA0 x)CA0 x
rA
dCA dt
RgT
RT
rA kCA 0.0063(mol /(m3 s)) rp 0.5kCA 0.00314(mol /(m3 s))
• 知识点: 反应速率: • Arrhenius law:
(rA
)
dC A dt
E k k0 exp( RT )
习题2.3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学反应工程习题(第五章)5.1乙炔与氯化氢在HgCl 2-活性炭催化剂上合成氯乙烯的反应2223C H HCl C H Cl +↔()A ()B ()C其动力学方程式可有如下种种形式:(1) 2(/)/(1)A B C A A B B C C r p p p K K p K p K p κ=-+++ (2) /(1)(1)A B A B B B C C A A r K K p p K p K p K p κ=+++ (3) /(1)A A B A A B B r K p p K p K p κ=++(4) /(1)B A B B B C C r K p p K p K p κ=++试说明各式所代表的反应机理和控制步骤。
解:(1) A A σσ+↔B B σσ+↔A B C σσσσ+↔+ (控制步骤) C C σσ↔+(2) 11A A σσ+↔22122111B B A BC C C σσσσσσσσ+↔+→+↔+(控制步骤) (3) A A σσ+↔B B σσ+↔A B C σσ+→+ (控制步骤)(4) B B σσ+↔A B C σσ+→ (控制步骤) C C σσ↔+经验:①看分母,含有哪些物质的吸附平衡常数,可以确定哪些物质有吸附或脱附过程;②看分母,含有几个式子相乘,就有几个活性中心参与反应,式子相同,说明活性中心相同,式子不同,说明活性中心不同; ③看分子,含有哪些物质的吸附平衡常数,可以推出哪些物质与活性中心吸附后参与了控制步骤的反应;④看分子,有“-”号,说明控制步骤为可逆反应,反之则为不可逆反应。
5.2 在Pd-Al 2O 3催化剂上用乙烯合成醋酸乙烯的反应为 243222321C H CH COOH O CH COOC H H O 2++↔+实验测得的初速率数据如下[功刀等,化工志,71,2007(1968).] 115℃, AcOH 200p mmHg =,292O p mmHg =。
24()C H p mmHg70 100 195 247 315 4655010(/)r mol hr g ⨯⋅催化剂3.94.4 6.0 6.6 7.255.4注:1mmHg=133.322Pa 如反应机理设想为2424242422423223232222O ()O O+AcOH AcOH C H C H AcOH C H HC H OAc O O HC H OAc O C H OAc H C H OAc C H OAc H H σσσσσσσσσσσσσσσσ+↔+↔+↔++↔+→+↔+↔控制步骤试写出反应速率并检验上述部分数据能与之符合否。
解: 243222321C H CH COOH O CH COOC H H O 2++↔+ (A ) (B ) (C ) (E ) (F )A A A V K P θθ=B B B V K P θθ=C Vθ=1D s A B A B V k K K P P θθ= E E E VK P θθ= F F F V K P θθ=2D C 102''22323()()V s A AA A r k K P P r K K P K K P θθθ======++=''23A K K P +24()C H p mmHg70 100 195 247 315 4655010(/)r mol hr g ⨯⋅催化剂3.94.4 6.0 6.6 7.255.4310- 1.34 1.51 1.80 1.93 2.08 2.93A P 作图,基本上为一直线。
∴上述数据与反应速度式基本符合。
5.3某反应A R S −−→+,其动力学方程式为 (/)/(1)A A A R S A A R R r kK p p p K K p K p -=-++试导出平推流式的等温积分反应管中转化率X A 与W/F AO 的关系式。
解:设总压不变且0000(0)A R S p p p p p ==== 2111A δ-== 000(1)(1)(1)1(1)(1)A A A A A A A A A A A A p x x x p p p y x x x δ---===+++同理: 1AR s Ax p p p x ==+ 将各p 值代人题中给出的动力学方程式,并简化得:222(1)/()A r a x bx cx d -=-++式中: 21p a k =+1()/R A A b K K kK p=+- 2()/R A c K kK p =+ 1()/A A d K kK p=+ A x x =并设A r -是以单位床层体积为基准的,反应管中堆积密度为B p 。
22222220000111ff f x x x A BW x x d b dx c dx d dx F a x a x a x ρ=++---⎰⎰⎰ 2200000222112121121211ln ln(1)212f f f f f x x x x x f f ff b x b x x d d dx dx c dx dx dxa ax a ax a x ax axax b d c a x bx a ax a=-+++-+--+++=----⎰⎰⎰⎰⎰5.4在200℃下,苯在Ni 催化剂上加氢。
已知催化剂微孔的平均孔径4.0mm ,求总压分别为0.1Mpa 及3.5MPa 下氢的扩散系数。
解:由陈甘棠(81版)表5.3-4查得:266:/59.7:/412.3H k C H k ξξ== 102.827105.349mσσ-=⨯=设本系统可由苯与氢的二组分系统代表,则由(5.3-62)及(5.3-63)式,得:1/21/211()(2.827 5.349) 4.08822()(59.7412.3)157.0AB A B ABA B k kσσσξξξ=+=+===⨯=故: /473/157.030.1AB kT ξ==由表5.3-3查得: 0.9483AB Ω=代入(5.3-61)式:2663/22211()0.8602.01678.110.001858(473)/(4.088)(0.9483)H C H D cm s p p -+==当p=0.1MPa=1atm 时 266220.860/0.860/1H C H D cm s cm s -== 当p=3.5MPa=35atm 时 266220.860/0.02457/35H C H D cm s cm s -== 至于努森扩散则由(5.3-65)式计算,它与总压是无关的。
1/224739700(0.4)()59431.5/2.016K D cm s == 由此可知,由于孔径较大,努森扩散的影响可以忽略。
解法2:由于孔径4mm 很大,因此直接用分子扩散的公式(参考朱炳晨的书)5.5 异丙苯在催化剂上裂解而生成苯,如催化剂为微球状,d p =0.4cm ,ρp =1.06g/cm 3, εp =0.52, S g =350m 2/g ,求在500℃,0.1Mpa 时,异丙苯的微孔中的有效扩散系数。
设已知微孔的曲折因子τ=3,异丙苯-苯的分子扩散系数为0.155cm 2/s 。
解: 742220.52 2.8101.0635010g ggp gV a cm S S ξρ-⨯====⨯⨯⨯ 孔径很小属努森扩散区:73232333250027397009700 2.810 6.8910/120116.6010/111/1/0.1556.89100.52 6.6010 1.1410/3k k k ABD e D cm s D cm s D D D D D cm sξτ------+==⨯⨯=⨯===⨯≈++⨯⨯⨯===⨯迷宫因子是催化剂中的一种加速或者减弱催化的酶的催化系数,这个系数决定了催化的速度。
5.6兹有直径为0.2cm 高0.2cm 及直径为0.8cm 高0.8cm 的两种催化剂粒子分别在等温的管中进行测试,填充体积为150cm 3,床层空隙率0.40,所用气体流量均为3cm 3/s ,粒子孔隙率均为0.35,迷宫因子0.20,反应为一级不可逆,对直径为0.2cm 催化剂,达到的转化率为66%,而对直径为0.8cm 的催化剂则为30%,如气体密度不变,问: (1)这两种床层催化剂有效系数是多少? (2)气体真实的扩散系数为多少? 解:(1)设等比表面当量球半径R p1, R p2:22224222423p P R R R R R R R πππππ⨯+⨯=⨯ ,故P R R = ∴ 110.2/20.1P R R cm ===,220.8/20.4P R R cm ===, 120.10.250.4P P R R == 一级反应催化剂有效系数与浓度无关,分别设为η1,η2'00'0011ln (1)1AfAf x x pA A v A Af v Af Adx dx c c k c x k x r τηη===---⎰⎰ 式中'A r -,'p τ均以催化剂粒子体积为基准:'211ln1.07910.66p k τη==-, '221ln 0.35710.3p k τη==-121212/ 3.02//0.25P P R R ηηϕϕ=⎧⎨==⎩ 根据式(5.3-91)计算,311()tan ss sηϕϕϕ=-,用试差法求得: 1 3.29ϕ= 213.16ϕ= 10.637η= 20.211η= 此算法均是将圆柱子化作当量球形求解。
(2)'11.079v p k τη=(或'20.357p τη) '0(1)1500.630()3R p V s V ετ-⨯=== 21.0795.6510(1/)300.637v k s -==⨯⨯由式(5.3-78)222521215520.1 5.6510 5.2210/3.2920.2 5.22102.9810/0.35P ve e pR k D cm sD D cm sϕτε----⨯⨯===⨯⨯⨯===⨯5.7 某组分A 在540℃下的催化剂上反应,其速率式为132()8.3610A A r p --=⨯ /m o l s g ⋅催化剂φA 的单位为Pa 。
如催化剂颗粒的密度为0.8g/cm 3,当量直径为0.3cm ,颗粒外表面上A 的分压为p A,s =1.2×104Pa ,A 的组分在粒内的扩散系数为0.020cm 2/s,求催化剂的有效系数。
解:用浓度表示时 13222()8.3610()A p A v Ar RT c k c ρ--=⨯= 故:1322528.3610(0.80)(8.314813) 3.055610v A Ak c c --=⨯⨯=⨯ 又R=0.3cm 代入(5.3-77)0.01562s φ==== 于是从图5.3-11中查得:η=0.91。
