米氏常数测定(精)
米氏常数实验报告

米氏常数实验报告米氏常数实验报告引言:米氏常数是物理学中的一个重要常数,它描述了光在真空中的传播速度。
在本次实验中,我们将通过测量光的传播时间和光程差来确定米氏常数的数值。
通过这个实验,我们将更深入地了解光的性质和光在空间中的传播规律。
实验目的:本实验的目的是通过测量光的传播时间和光程差来确定米氏常数的数值,并验证光在真空中的传播速度是否恒定。
实验器材:本实验所需的器材包括:激光器、分光镜、反射镜、光电探测器、计时器等。
实验步骤:1. 首先,我们将激光器置于实验室的一端,并将其打开。
确保激光器产生的光束是稳定的。
2. 接下来,我们将分光镜放置在激光器的光路中,并调整其角度,使得光束被分光镜分为两束相等的光束。
3. 将两束光束分别引导至反射镜,并使其分别反射回来。
4. 在光束返回的路径上,我们将安装光电探测器,并将其与计时器相连。
5. 开始实验时,我们同时启动激光器和计时器,并记录下光束从激光器发出到光电探测器接收到的时间。
6. 重复实验多次,取平均值作为最终的测量结果。
实验结果:通过多次实验测量,我们得到了光的传播时间和光程差的数据。
根据这些数据,我们可以计算出米氏常数的数值。
讨论与分析:在本次实验中,我们得到了光的传播时间和光程差的数据,进而计算出了米氏常数的数值。
通过比较实验结果与已知的米氏常数数值,我们可以验证光在真空中的传播速度是否恒定。
此外,本实验还可以用于研究光在不同介质中的传播速度。
通过将光束传播到不同介质中,我们可以测量光的传播时间和光程差,并计算出不同介质中的米氏常数。
这有助于我们更深入地了解光在不同介质中的传播规律。
结论:通过本次实验,我们成功地测量了光的传播时间和光程差,并计算出了米氏常数的数值。
实验结果与已知的米氏常数数值相符,验证了光在真空中的传播速度是恒定的。
此外,本实验还为研究光在不同介质中的传播速度提供了一种方法。
总结:米氏常数实验是一项重要的实验,通过测量光的传播时间和光程差,我们可以确定光在真空中的传播速度。
酵母蔗糖酶米氏常数的测定
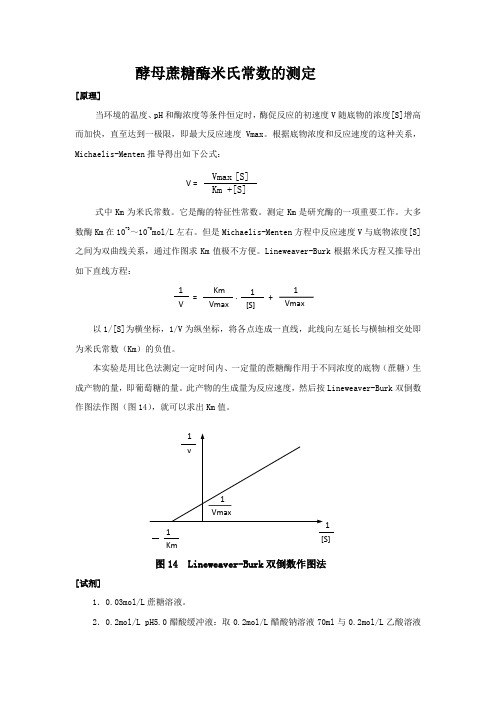
酵母蔗糖酶米氏常数的测定[原理]当环境的温度、pH 和酶浓度等条件恒定时,酶促反应的初速度V 随底物的浓度[S]增高而加快,直至达到一极限,即最大反应速度Vmax 。
根据底物浓度和反应速度的这种关系,Michaelis-Menten 推导得出如下公式:式中Km 为米氏常数。
它是酶的特征性常数。
测定Km 是研究酶的一项重要工作。
大多数酶Km 在10-3~10-5mol/L 左右。
但是Michaelis-Menten 方程中反应速度V 与底物浓度[S]之间为双曲线关系,通过作图求Km 值极不方便。
Lineweaver-Burk 根据米氏方程又推导出如下直线方程:以1/[S]为横坐标,1/V 为纵坐标,将各点连成一直线,此线向左延长与横轴相交处即为米氏常数(Km )的负值。
本实验是用比色法测定一定时间内、一定量的蔗糖酶作用于不同浓度的底物(蔗糖)生成产物的量,即葡萄糖的量。
此产物的生成量为反应速度,然后按Lineweaver-Burk 双倒数作图法作图(图14),就可以求出Km 值。
图14 Lineweaver-Burk 双倒数作图法[试剂]1.0.03mol/L 蔗糖溶液。
2.0.2mol/L pH5.0醋酸缓冲液:取0.2mol/L 醋酸钠溶液70ml 与0.2mol/L 乙酸溶液V =Vmax [S] Km +[S]1 V = · 1 Vmax 1 [S] + Km Vmax1 [S] 1 Km30ml相混合。
3.蔗糖酶溶液:干酵母2.5g置研钵中,加蒸馏水4ml,用力研磨10分钟,转移到离心管中,用25ml蒸馏水洗研钵,并将洗涤液一起转移到离心管中,摇匀,静置50分钟,离心(2000r/min 5min),小心取出上清夜备用。
置冰箱保存。
实验时根据需要用蒸馏水适当稀释。
(约25倍稀释)4.碱性硫酸铜溶液:取无水Na2CO340g溶于400ml蒸馏水中;酒石酸7.5g溶于350ml 蒸馏水中;结晶硫酸铜(CuSO4·5H2O)4.5g溶于200ml蒸馏水中,以上分别加热促溶。
米氏常数测定实验报告

一、实验目的1. 理解并掌握米氏常数(Km)及其与最大反应速度(Vmax)的关系。
2. 通过实验测定酶的米氏常数,了解酶与底物之间的亲和力。
3. 学习并掌握酶促反应动力学的基本原理和实验方法。
二、实验原理米氏常数(Km)是酶的特征性常数,表示酶与底物结合的亲和力。
在一定的实验条件下,酶促反应的初速度(v)与底物浓度([S])之间的关系可用米氏方程表示:\[ v = \frac{V_{max} [S]}{Km + [S]} \]当底物浓度很低时,酶促反应速度与底物浓度成正比,随着底物浓度的增加,反应速度逐渐加快,但增速逐渐减慢。
当底物浓度增加到一定程度时,反应速度达到最大值(Vmax),此时酶已全部被底物饱和。
本实验采用分光光度法测定酶的米氏常数。
实验中,通过改变底物浓度,测定不同浓度下酶促反应的初速度,根据米氏方程绘制v/[S]对1/[S]的曲线,通过线性回归分析求出曲线的斜率和截距,进而计算出Km和Vmax。
三、实验材料与仪器材料:1. 酶制剂(如蔗糖酶、淀粉酶等)2. 底物溶液(如葡萄糖溶液、淀粉溶液等)3. 碳酸盐缓冲液4. 4-氨基安替比林5. 铁氰化钾6. 0.1 mol/L NaOH溶液7. 葡萄糖标准溶液仪器:1. 分光光度计2. 移液管3. 移液器4. 恒温水浴5. 试管6. 比色皿四、实验步骤1. 制备酶溶液:将酶制剂溶解于适量的碳酸盐缓冲液中,调节pH值至最适值,稀释至一定浓度。
2. 制备底物溶液:将底物溶液稀释至不同浓度,备用。
3. 测定酶促反应初速度:a. 将不同浓度的底物溶液分别加入试管中,加入适量的酶溶液。
b. 将试管放入恒温水浴中保温一段时间。
c. 取出试管,立即加入适量的4-氨基安替比林和铁氰化钾,充分混匀。
d. 在分光光度计上测定溶液的吸光度,记录数据。
4. 数据处理:a. 以底物浓度[S]为横坐标,酶促反应速度v为纵坐标,绘制v/[S]对1/[S]的曲线。
b. 对曲线进行线性回归分析,求出曲线的斜率和截距。
碱性磷酸酶米氏常数测定
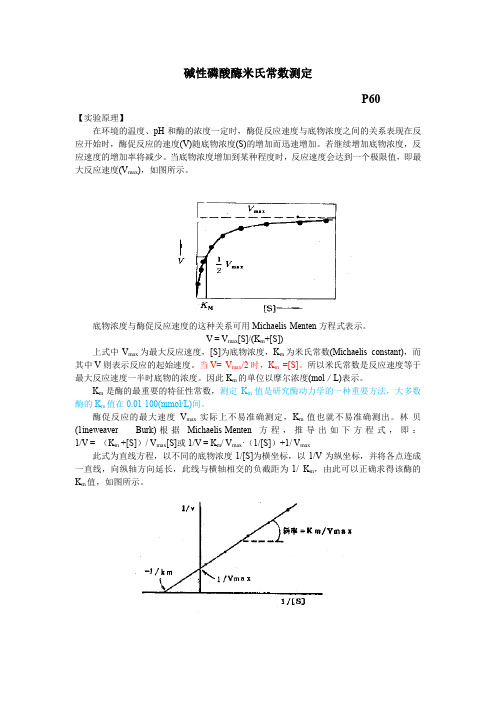
碱性磷酸酶米氏常数测定P60【实验原理】在环境的温度、pH和酶的浓度一定时,酶促反应速度与底物浓度之间的关系表现在反应开始时,酶促反应的速度(V)随底物浓度(S)的增加而迅速增加。
若继续增加底物浓度,反应速度的增加率将减少。
当底物浓度增加到某种程度时,反应速度会达到一个极限值,即最大反应速度(V max),如图所示。
底物浓度与酶促反应速度的这种关系可用Michaelis-Menten方程式表示。
V = V max[S]/(K m+[S])上式中V max为最大反应速度,[S]为底物浓度,K m为米氏常数(Michaelis constant),而其中V则表示反应的起始速度。
当V= V max/2时,K m=[S]。
所以米氏常数是反应速度等于最大反应速度一半时底物的浓度。
因此K m的单位以摩尔浓度(mol/L)表示。
K m是酶的最重要的特征性常数,测定K m值是研究酶动力学的一种重要方法,大多数酶的K m值在0.01-100(mmol/L)间。
酶促反应的最大速度V max实际上不易准确测定,K m值也就不易准确测出。
林-贝(1ineweaver - Burk)根据Michaelis-Menten方程,推导出如下方程式,即:1/V = (K m +[S])/ V max[S]或1/V = K m/ V max·(1/[S])+1/ V max此式为直线方程,以不同的底物浓度1/[S]为横坐标,以1/V为纵坐标,并将各点连成一直线,向纵轴方向延长,此线与横轴相交的负截距为-1/ K m,由此可以正确求得该酶的K m值,如图所示。
本实验以碱性磷酸酶为例,测定不同底物浓度的酶活性,再根据Lineweaver-Burk法作图,计算其K m值。
可以作为碱性磷酸酶底物的物质很多,底物反应的酶对于不同的底物有不同的K m值。
本实验以磷酸苯二钠为底物,由碱性磷酸酶催化水解,生成游离酚和磷酸盐。
酚在碱性条件下与4-氨基安替比林作用,经铁氰化钾氧化,生成红色的醌衍生物,颜色深浅和酚的含量成正比。
六、脲酶米氏常数简易测定2010(精)

米氏常数的意义
• 由米氏方程可知,当反应速度等于最大反应速度一半时, 即V = 1/2Vmax时, Km = [S] 。 • 上式表示,米氏常数是反应速度为最大值的一半时的底物 浓度。 • 因此,米氏常数的单位为mol· L-1。 • 不同的酶具有不同Km值,它是酶的一个重要的特征物理常 数。 • Km值只是在固定的底物,一定的温度和pH条件下,一定的 缓冲体系中测定的,不同条件下具有不同的Km值。 • Km值表示酶与底物之间的亲和程度:Km值大表示亲和程度 小,酶的催化活性低; Km值小表示亲和程度大,酶的催化 活性高。 • 通过Km值的测定,可鉴定酶的各种底物,Km值最小者为酶 最佳底物,即天然底物。
充分摇匀,室温下静置5min,过滤,另取5支试管,同上编号,加入以下试剂 滤液(ml) 双蒸水(ml) 显色液(ml) 1 2 0.75
迅速摇匀,用分光光度计在420nm下测定各管A值。
4.2 数据处理
• 各管在420nm测定OD420nm值。 • 由于光密度(OD420nm)与显色,显色与底物浓度成正比, 反应时间均为15min。故以1/A取代1/V为纵坐标作图。 • 测定所用单位为Km单位g· L-1 。 • 由1/A对1/[S]作图,求得回归方程,计算α-淀粉酶催化 可溶性淀粉溶解的米氏常数Km。
V max [ S ] V Km [ S ]
• 其中,V为酶促反应速度;Vmax为最大反应反应速度(与V 的单位相同, mol· L-1· min-1); [S]为底物浓度(mol· L-1); Km为米氏常数,是酶促反应速度V为最大酶促反应速度值一 半时的底物浓度,即V = 1/2Vmax时, Km = [S] 。 • 在酶促反应中,底物在低浓度情况下,反应相对于底物是 一级反应(first order reaction);而当底物浓度处于 中间范围时,反应(相对于底物)是混合级反应(mixed order reaction);当底物浓度增加时,反应由一级反应 向零级反应(zero order reaction)过渡;当底物浓度[S] 逐渐增大时,速度V相对于[S]的曲线为一双曲线。下图为 米氏方程的模拟作图:
米氏常数的测定(精)

v
1 Km
1
[S]
6 反应速度v的测定
18 16 14 12 10 8 6 4 2 0 0 5 10 时间 15 20
产物量
系列1
7 胰蛋白酶的性质 胰蛋白酶催化蛋白质中碱性氨基酸(L-精氨酸和L-赖氨酸) 的羧基所形成的肽键水解,产生自由氨基。 8 氨基的测定 甲醛滴定法。 COOCH2 NH2
底物浓度对酶促反应速度的影响 ——米氏常数的测定
目的要求:
1. 了解底物浓度对酶促反应的影响。 2. 掌握测定米氏常数Km的原理和方法
原理: 1. Km定义: Km值等于酶促反应速度达到最大反应速度一半时所对应的 底物浓度。 2 Km的意义
Km是酶的特性常数之一,不同的酶Km值不同,同一种酶与 不同底物反应Km值也不同。 Km值可近似的反应酶与底物的亲和力大小: Km值大,表明 亲和力小;Km值小,表明亲和力大。 测定Km值是酶学研究的一个重要方法。大多数纯酶的Km值 在0.01-100mmol/L。
思考题: 1. 试述底物浓度对酶促反应速度的影响。 2. 试述在何种条件下,测定酶的Km值可以作为鉴定酶的一种 手段。 3 米氏方程中的Km值的实际应用是什么? 4 本实验中的注意事项是什么?
4 米氏方程: V[S] v = Km + [S ] v : 反应初速度 (微摩尔浓度变化/min) V : 最大反应速度 (微摩尔浓度变化/min) [S]:底物浓度 (mol/L) Km: 米氏常数 (mol/L)
此方程表明,当已知Km及V时,酶反应速度与底 物浓度 之间的定量关系。
5 双倒数作图法测定Km值: 1 Km 1 1 v V [S] V
HCHO
COOCH2 NHCH2OH
HCHO
淀粉酶米氏常数测定

三 仪器和试剂
试剂
(1)酶液:精确称取酶制剂0.1g(以大约2000 U/g计),先用少量40℃ 蒸馏水溶解、浸提。将上层液小心倾入500ml容量瓶内,沉淀再加水 捣研。如此重复,最后全部移入容量瓶中,定容后摇匀,用四层纱布 过滤,滤液供测试定用
(2)原碘液 称取碘11 g,碘化钾(KI)22 g,先用少量蒸馏水使碘-碘化 钾完全溶解,定容至500 mL,贮于棕色瓶内。
试剂
瓶号
1
2
3
4
5
6
4%可溶性淀粉(ml) 0.5
1
1.5
2
2.5
3
H2O(ml) 缓冲液(ml)
3.5
3
2.5
2
1.5
1
0.75 0.75 0.75 0.75 0.75 0.75
60℃放置,预热5min
酶液(ml)
0.25 0.25 0.25 0.25 0.25 0.25
充分摇匀,60℃放置10min
1 Km 1 1 v Vm [S] Vm
酶促反应v-[S]曲线
以1/v对1/[S]作图,可得一条直 线,所得直线的截距是1/Vm, 斜率为Km/ Vm。通过 Lineweaver-Burk作图法作图后 可方便的求出Km值。
三 仪器和试剂
试管 移液抢 秒表 吸耳球 恒温水浴锅 7200型分光光度计。
一、 实验目的
了解并掌握米氏常数的意义和测定方法
二、 实验原理
推导出米氏方程为: v Vm[S ] Km [S]
米氏常数Km是酶的一个基本特征常 数,它包含着酶与底物结合和解离的 性质。特别是同一种酶能够作用于几 种不同底物时,米氏常数Km往往可以 反映出酶与各种底物的亲和力的强弱。
【米氏常数】米氏常数测定实验报告.docx

【米氏常数】米氏常数测定实验报告.docx【米氏常数】米氏常数测定实验报告此人姓米,单名兰,却没有米兰那种碧绿盎然,幽香沁人的素雅。
她的身高同十几年前参军时,相差无几—1.55米。
3号军装穿在身上,仍旧如长袍加身,宽大得令人忍俊不禁。
第一个对米兰发表看法的,是化验科的金云。
金云姑娘,确如行于天穹的云霞,轻盈高挑的身材,朗若明月的脸庞,使她这只“鹤”,高立于我们这所医院的所有兵姑娘之中。
姑娘对自己的美都是敏感的,“大兵”也不例外。
更何况金云的仰慕者不计其数。
不知何故,却一概吃了闭门羹,落得个没趣。
这个金云啊,美丽使她的嘴变得尖酸起来。
于是乎,米兰也逃不出她那双带着讥讽的笑盈盈的大眼睛。
从医校毕业分到化验科的第2周,金云在医学论文宣读会上,见到了比讲台高不了多少的米兰。
“米兰?嘻嘻!”她一眨黑白分明的眸子,咬着身边另一位护士的耳朵,“米氏常数。
嗯?”“米氏常数?”“酶的底物浓度取决于米氏常数。
它在同等条件下是恒定的。
你瞧,她多恒定,永远只比讲台高半尺。
咯咯!”周围的姑娘们八成听见了。
否则,各种无法揣测的眼神,为什么都聚向站在讲台后面,涨红了脸的米兰?金云矜持地向周围扫了一眼,她为自己的想象力而暗暗自得。
这位以全优成绩毕业的姑娘,连头发梢都是高傲的。
“……是个沉痛的教训。
”米兰颤动着嘴角,向幻灯投影机插进一张照片。
金云低呼了一声,礼堂里那些抄录笔记的大夫们,也交头接耳起来—幕布上一张奇丑无比的脸。
严重烧伤使患者分不清男女,辨不全五官。
变形的脸上爬满了蚯蚓似的斑痕。
又是一张照片,仍旧是一张奇丑的脸。
“手术没有获得预期效果。
主要教训是……”金云无心去关心那位没有恢复容貌的患者,也不再留神米兰那些专科术语了。
她痴呆呆地盯住米兰—“真是太一般啦!”五官似乎是符合解剖位置,但安在米兰宽大的脸庞上,总那么别扭。
又黑又硬的头发从无沿帽下“炸”开来,象一道狭窄的帽檐。
金云下意识地拂拂自己额前那蓬微微弯曲、浓密地偏向一侧的刘海。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
COOCH2 NHCH2OH
HCHO
COOCH2 NH(CH2OH)2
试剂器材
试剂
1. 10~40g/L酪蛋白溶液(pH8.5): 四种不同[S]的酪蛋白标准溶液。 2. 中性甲醛溶液:75mL分析纯甲 醛加15mL 0.25%酚酞乙醇溶液, 以0.1M NaOH滴至微红,密闭于 玻璃瓶中。(自己配制) 3. 0.25%酚酞乙醇溶液: 4. 标准0.1M NaOH溶液。 5.胰蛋白酶溶液(已配好)
液,重复上述操作,分别测出V30、V20、V10。
利用上述结果,以1/v对1/[s]作图,即求出V与 Km值。
注意事项
(1 )实验表明,反应速度只在最初一段时间内保持恒定, 随着反应时间的延长,酶促反应速度逐渐下降。原因有多种, 如底物浓度降低,产物浓度增加而对酶产生抑制作用并加速 逆反应的进行,酶在一定pH及温度下部分失活等。因此,研 究酶的活力以酶促反应的初速度为准。
此方程表明,当已知Km及V时,酶反应速度与底 物浓度 之间的定量关系。
双倒数作图法测定Km值: 1 Km 1 1 v V [S] V
胰蛋白酶的性质 胰蛋白酶催化蛋白质中碱性氨基酸(L-精 氨酸和L-赖氨酸)的羧基所形成的肽键水解, 产生自由氨基端。
氨基的测定
甲醛滴定法
COOCH2 NH2
HCHO
实验十六
底物浓度对酶促反应速度的影响 ——米氏常数的测定
目的要求
(1)了解底物浓度对酶促反应的影响。
(2)掌握测定米氏常数Km的原理和方法
实验原理
Km定义: Km值等于酶促反应速度达到最大反应速度一半时 所对应的底物浓度。
Km的意义
Km是酶的特性常数之一,不同的酶Km值不同,同
一种酶与不同底物反应Km值也不同。
器材:
碱式滴定管
操作方法
1 .取 50mL三角瓶 4 个,加入 5mL 甲醛与 1 滴酚酞,以 0.1M 标准 NaOH滴定至微红色, 4 个瓶颜色应当一致,编 号。 2 .量取 40g/L 酪蛋白 50mL,加入一 150mL 三角瓶, 37℃保温10分钟,同时胰蛋白酶液也在37℃保温10分钟, 然后吸取5mL酶液加到酪蛋白液中。(同时计时!)充分 混合后立即取出10mL反应液(定为0时样品)加入一含甲 醛的小三角瓶中(1号)加10滴酚酞;以0.1M NaOH滴定 至微弱而持续的微红色。在接近终点时,按耗去的 NaOHmL数,每mL加一滴酚酞,再继续滴至终点,记下 耗去的0.1M标准NaOH mL数。
(2 )本实验是一个定量测定方法,为获得准确的实验结 果,应尽量减少实验操作中带来的误差。因此配制各种底物 溶液时应用同一母液进行稀释,保证底物浓度的准确性。各 种试剂的加量也应准确,并严格控制准确的酶促反应时间。
思考题
1. 试述底物浓度对酶促反应速度的影响。 2. 试述在何种条件下,测定酶的Km值可以作为鉴 定酶的一种手段。 3 米氏方程中的Km值的实际应用是什么? 4 本实验中的注意事项是什么?
3.在2分钟、4分钟、6分钟时,分别取出10mL反应 液,加入2号、3号、4号小三角瓶,同上操作,记下耗 去NaOH mL数。 以滴定度(即耗去的NaOH mL数)对时间作图,
得一直线,其斜率即初速度为V40(相对于40g/L
的酪蛋白浓度)。 然后分别量取30g/L、20g/L、10g/L的酪蛋白溶
Km值可近似的反应酶与底物的亲和力大小: Km 值大,表明亲和力小;Km值小,表明亲和力大。 测定Km值是酶学研究的一个重要方法。
米氏方程: V[S] v = Km + [S ]
v : 反应初速度 (微摩尔浓度变化/min) V : 最大反应速度 (微摩尔浓度变化/min) [S]:底物浓度 (mol/L) Km: 米氏常数 (mol/L)
