溶液 溶解度解题技巧及练习测试题
最新溶液 溶解度专题(含答案)经典

最新溶液溶解度专题(含答案)经典一、溶液选择题1.列表和作图是常用的数据处理方法.结合材料所绘图表判断下列说法正确的是( )A.表格与图象均能反映温度对固体物质溶解度的影响,表格比图像更直观体现变化规律B.由表格数据可知,物质的溶解度只受温度影响C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成【答案】A【解析】A.通过分析溶解度表和溶解度曲线可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点是变化规律更直观,故A错误;B.由表格数据可知,物质的溶解度受温度和溶剂影响,故B错误;C.40℃时,氢氧化钠在水中的溶解度是129g,氢氧化钠在酒精中的溶解度是40g,所以将50gNaOH分别投入到100g水和酒精中,在水中不能形成饱和溶液,故C错误;D.40℃时,碳酸钠在酒精中难溶,所以将CO2通入饱和的NaOH酒精溶液中有沉淀生成,故D正确;故选D。
点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
2.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )A.50℃时,氯化铵的溶解度大于硝酸钾B.a℃时,氯化铵与硝酸钾溶液的质量分数相等C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【答案】D【解析】【分析】【详解】A、从图中看出,50℃时,硝酸钾的溶解度大于氯化铵的,故A不正确;B、a℃时,硝酸钾和氯化铵的溶解度曲线相交,此时两物质的溶解度相等,则其饱和溶液的溶质质量分数相等,其不饱和溶液的质量分数是否相等无法确定,故B不正确;C、硝酸钾的溶解度随温度的升高明显增大,将60℃时硝酸钾饱和溶液降温后会析出晶体,剩余的溶液仍然是低温下的饱和溶液,故C不正确;D、40℃时,硝酸钾的溶解度为64g,则50g水中最多溶解硝酸钾32g,所得溶液的溶质质量分数为32g100%39%32g+50g⨯≈,故D正确。
溶液 溶解度解题技巧及练习测试题(word)1

溶液溶解度解题技巧及练习测试题(word)1一、溶液选择题1.请根据右图的溶解度曲线图,判断下列说法正确的是()A.a、b两物质的溶解度相等B.t1℃时,向20g a固体加入50g 水,充分搅拌后固体能全部溶解C.将t2℃时a、b饱和溶液降温到t1℃时,两者的溶质质量分数相等D.b中含有少量a,可以用冷却热饱和溶液的方法提纯b【答案】C【解析】试题分析:A 根据溶解度曲线可知,只有在℃时两物质溶解度相等;B t 1℃时,a物质的溶解度为36g,也就是说此温度下100g水中最多可以溶解36g a物质;C 从t2℃降温至t1℃时,两物质溶解度相等,且都为饱和溶液,因此质量分数相等;D a、b两物质溶解度变化随温度变化相差较大,因此可以用冷却热饱和溶液的方法提纯a,不可以用来提纯b。
考点:溶解度曲线的意义点评:关于溶解度曲线的题目一直是中考的必考点,常在双选中出现,得分率不是很高,注意仔细审题,避免粗心。
2.甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是A.甲的溶解度比乙的大B.t1℃时,甲和乙的饱和溶液中溶质的质量分数一定相等C.将t2℃时甲的不饱和溶液变为饱和溶液,可采取升温的方法D.分别将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量一定大【答案】B【解析】A.根据物质的溶解度分析;B.根据饱和溶液溶质质量分数分析;C.根据根据饱和溶液与不饱和溶液的互相转换分析;D.根据溶液质量是否相等分析。
解:A.物质的溶解度受温度的影响,温度不同,溶解度不同,故错误;B. t 1℃时,甲和乙的溶解度相等,故饱和溶液中溶质的质量分数一定相等,正确;C.甲的溶解度随温度的升高而增大。
将t 2℃时甲的不饱和溶液变为饱和溶液,升高温度,溶解度变大,此时仍为不饱和溶液,错误;D. 甲、乙的饱和溶液的质量不一定相等,故分别将甲、乙的饱和溶液从t 2℃降到t 1℃,析出甲的质量不一定大,错误。
故本题选B 。
点睛:饱和溶液与不饱和溶液,溶质质量分数。
【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)

【化学】初三化学《溶液》解题技巧及经典题型及练习题(含答案)一、选择题1.NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是A.乙为NH4Cl B.t3应介于40℃﹣50℃C.55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙 D.等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等【答案】C【解析】A. 据溶解度表可知,NH4Cl的溶解度随温度升高而增大,故乙是NH4Cl,正确;B、40℃时,Na2SO4的溶解度是48.4g,50℃时,溶解度变小,是47.5g,且t3℃时两种物质的溶解度相等,故t3应介于40℃﹣50℃,正确;C、据溶解度表分析可知,55℃时,NH4Cl的溶解度大于Na2SO4的溶解度,故分别将两饱和溶液蒸发等质量的水,得到固体质量乙>甲,错误;D、两种物质的溶解度从t3降温到t1时,溶解度变化相同,故等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等,正确。
故选C。
2.如图是甲、乙两种固体物质在水中的溶解度曲线。
下列说法正确的是A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等B.由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多C.t2℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90gD.t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙多【答案】A【解析】A、一定温度下,饱和溶液溶质的质量分数=s100g s×100%。
t1℃时,甲、乙的溶解度相等,甲、乙两种饱和溶液的溶质质量分数相等,正确;B、没有确定溶液的质量无法比较甲、乙饱和溶液析出晶体的质量,错误;C、t2℃时,甲的溶解度为50g,即100g水中最多溶解50g的甲,40g甲加入50g水中,充分溶解后只能溶解25g,所得的溶液质量为75g,错误;D、t2℃时,甲的溶解度大于乙的溶解度,配制等质量饱和溶液,甲所需要水的质量比乙少,错误。
溶液 溶解度试题和答案经典1
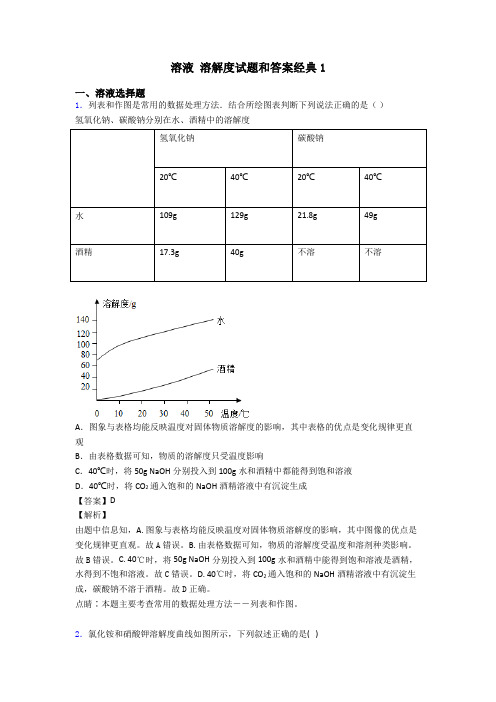
溶液溶解度试题和答案经典1一、溶液选择题1.列表和作图是常用的数据处理方法.结合所绘图表判断下列说法正确的是()氢氧化钠、碳酸钠分别在水、酒精中的溶解度氢氧化钠碳酸钠20℃40℃20℃40℃水109g129g21.8g49g酒精17.3g40g不溶不溶A.图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观B.由表格数据可知,物质的溶解度只受温度影响C.40℃时,将50g NaOH分别投入到100g水和酒精中都能得到饱和溶液D.40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成【答案】D【解析】由题中信息知,A. 图象与表格均能反映温度对固体物质溶解度的影响,其中图像的优点是变化规律更直观。
故A错误。
B. 由表格数据可知,物质的溶解度受温度和溶剂种类影响。
故B错误。
C. 40℃时,将50g NaOH分别投入到100g水和酒精中能得到饱和溶液是酒精,水得到不饱和溶液。
故C错误。
D. 40℃时,将CO2通入饱和的NaOH酒精溶液中有沉淀生成,碳酸钠不溶于酒精。
故D正确。
点睛∶本题主要考查常用的数据处理方法--列表和作图。
2.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )A.50℃时,氯化铵的溶解度大于硝酸钾B.a℃时,氯化铵与硝酸钾溶液的质量分数相等C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【答案】D【解析】【分析】【详解】A、从图中看出,50℃时,硝酸钾的溶解度大于氯化铵的,故A不正确;B、a℃时,硝酸钾和氯化铵的溶解度曲线相交,此时两物质的溶解度相等,则其饱和溶液的溶质质量分数相等,其不饱和溶液的质量分数是否相等无法确定,故B不正确;C、硝酸钾的溶解度随温度的升高明显增大,将60℃时硝酸钾饱和溶液降温后会析出晶体,剩余的溶液仍然是低温下的饱和溶液,故C不正确;D、40℃时,硝酸钾的溶解度为64g,则50g水中最多溶解硝酸钾32g,所得溶液的溶质质量分数为32g100%39%32g+50g⨯≈,故D正确。
溶液 溶解度解题技巧及练习测试题1

溶液溶解度解题技巧及练习测试题1一、溶液选择题1.甲和乙两种固体的溶解度曲线如图所示.下列说法中,正确的是A.10℃时,甲的溶解度大于乙的溶解度B.通过降温可以将甲的饱和溶液变为不饱和溶液C.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数D.30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液【答案】D【解析】A.10℃时,甲的溶解度小于乙的溶解度,不是大于,故A错误;B.通过升温可以将甲的饱和溶液变为不饱和溶液,不是降温,故B错误;C.20℃时,在甲乙的饱和溶液中,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数,必须指明在饱和溶液中,故C 错误;D.30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液,因为在20℃,甲、乙的溶解度相等,都是40g,故D正确;故选D。
点睛:根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,10℃时,甲的溶解度小于乙的溶解度;通过升温可以将甲的饱和溶液变为不饱和溶液;20℃时,在甲乙的饱和溶液中,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数;30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液,因为在20℃,甲、乙的溶解度相等,都是40g。
2.不含结晶水的甲、乙两种固体物质的溶解度曲线如图所示。
下列说法正确的是A.t1℃时,甲、乙饱和溶液中含溶质的质量相等B.t1℃时,甲、乙两种物质各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70 gC.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙【答案】B【解析】A、t1℃时,甲、乙溶解度相等,所以等质量的饱和溶液中含溶质的质量相等,故A错误;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t2℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定大于乙溶液的溶质质量分数,故C错误;D、t2℃时甲、乙的饱和溶液的质量不确定,所以降温到t1℃时,析出晶体的质量甲不一定大于乙,故D错误。
【化学】溶液 溶解度难题及答案(word)

【化学】溶液溶解度难题及答案(word)一、溶液选择题1.试管中分别盛装甲、乙的饱和溶液,向烧杯中加入一定量NaOH固体后,A试管中变浑浊,结合图象,下列说法正确的是()A.A试管中是甲溶液B.t1℃时,甲的饱和溶液溶质质量分数为10%C.将t3℃时甲、乙饱和溶液降温至t2℃,溶质的质量分数甲=乙D.t3℃时,等质量的甲、乙饱和溶液中,溶剂质量甲<乙【答案】D【解析】【详解】A、由于氢氧化钠溶于水时溶液的温度升高,向烧杯中加入一定量NaOH固体后A试管中变浑浊,说明了溶质的溶解度随温度的升高而减小,由溶解度曲线可知,A试管中是乙的溶液,故A错误;B、由溶解度曲线可知,在t1℃时,甲的溶解度是10g,饱和溶液溶质质量分数为:≈9%,故B错误;C、将t3℃时甲、乙饱和溶液降温至t2℃,甲的溶解度随温度的降低而减小,成为t2℃的饱和溶液,乙的溶解度随温度的降低而增大,成为t2℃的不饱和溶液,与t3℃时溶质的质量分数相同,由于在t2℃甲的溶解度大于t3℃时乙的溶解度,所以溶质的质量分数甲>乙,在故C错误;D、由溶解度曲线可知,在t3℃时,甲的溶解度大于乙的溶解度,所以等质量的甲、乙饱和溶液中,溶剂质量甲<乙,故D正确。
故选D。
2.不含结晶水的甲、乙两种固体物质的溶解度曲线如图所示。
下列说法正确的是A.t1℃时,甲、乙饱和溶液中含溶质的质量相等B.t1℃时,甲、乙两种物质各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70 gC.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙【答案】B【解析】A、t1℃时,甲、乙溶解度相等,所以等质量的饱和溶液中含溶质的质量相等,故A错误;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t2℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定大于乙溶液的溶质质量分数,故C错误;D、t2℃时甲、乙的饱和溶液的质量不确定,所以降温到t1℃时,析出晶体的质量甲不一定大于乙,故D错误。
最新 溶液 溶解度解题技巧及练习测试题经典

【解析】碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为 CaCO3+2HCl═CaCl2+H2O+CO2↑ 、 K2CO3+2HCl═2KCl+H2O+CO2↑ , 由 上 述 化 学 方 程 式 可 知 , 碳 酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相 对原子质量的和是 71,碳酸根的相对原子质量的和是 60,差是 11,即完全反应后质量增 加了 11 份质量.实际反应后固体质量增加了 82.7g-75g=7.7g,设原混合物中含碳酸根的 质量为 x,则 60:11=x:7.7g,x=42g;则所含金属元素质量为 75g-42g=33g,原混合物中
金属元素的质量分数为 33g ×100%=44%。 75g
点睛:掌握反应前后金属元素的质量不变、看成碳酸根离子被两个氯离子取代是正确解答 本题的关键,碳酸钾和碳酸钙的固体混合物 75g,与 500g 质量分数为 14.6%的盐酸充分反 应,充分反应后盐酸可能有剩余,蒸发时剩余的盐酸挥发掉,故不能用稀盐酸中氯元素的 质量进行计算;碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为 CaCO3+2HCl═CaCl2+H2O+CO2↑ 、 K2CO3+2HCl═2KCl+H2O+CO2↑ , 由 上 述 化 学 方 程 式 可 知 , 碳 酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,由与金属离子结 合的酸根离子的相对原子质量的差,进行分析解答即可。
溶液溶解度测试题及答案1

溶解度为36g ,也就是说此温度下100g 水中最多可以溶解 36g a 物质;C 从t z C 降温至t i C时,两物质溶解度相等,且都为饱和溶液,因此质量分数相等; 随温度变化相差较大,因此可以用冷却热饱和溶液的方法提纯 D a 、b 两物质溶解度变化 a ,不可以用来提纯b o考点:溶解度曲线的意义点评:关于溶解度曲线的题目一直是中考的必考点,常在双选中出现,得分率不是很高, 注意仔细审题,避免粗心。
溶液溶解度测试题及答案(word ) 1一、溶液选择题1 •请根据右图的溶解度曲线图,判断下列说法正确的是()A. a 、b 两物质的溶解度相等B. t i C 时,向20g a 固体加入50g 水,充分搅拌后固体能全部溶解C. 将t 2C 时a 、b 饱和溶液降温到t i C 时,两者的溶质质量分数相等D.b 中含有少量a ,可以用冷却热饱和溶液的方法提纯 b【答案】C 【解析】试题分析:A 根据溶解度曲线可知,只有在 -C 时两物质溶解度相等;B t i C 时,a 物质的甲 乙 丙 丁A. 用装置甲收集氧气B. 用装置乙溶解完全反应后的固体C. 用装置丙分离MnO 2和KCI 溶液D.用装置丁蒸发分离后的溶液得 KCI 晶体【答案】D2.实验室用KCIQ 制氧气并回收 MnO 2和KCl ,下列操作不规范的是()【解析】【分析】【详解】A、氧气的密度比空气大,可用向上排空气法收集,故A正确;B、氯化钾易溶于水,二氧化锰难溶于水,溶解用玻璃棒搅拌以加快溶解速率,故B正确;C过滤时要用玻璃棒引流,故C正确;D、蒸发时要变加热边搅拌,故D不正确。
故选D o3. 右图是a、b、c三种物质的溶解度曲线,下列分析不正确的是A. t2C时,a、b、c三种物质的溶解度由大到小的顺序是a> b> cB. t2C时,将50ga物质放入100g水中充分溶解恰好得到a的饱和溶液(a物质不含结晶水)C. 将t2C时a、b、c三种物质的饱和溶液降温至t i C时,所得溶液的溶质质量分数关系b> c= aD. 将c的饱和溶液变为不饱和溶液,可采用降温的方法【答案】C【解析】【详解】A. 通过分析溶解度曲线可知,t2C时,a、b、c三种物质溶解度由大到小的顺序是a> b> c,故A正确;B. t2C时,a物质的溶解度是50g,所以将50g a物质(不含结晶水)放入100g水中充分溶解得到150ga的饱和溶液,故B正确;C. t1C时,b物质的溶解度最大,a物质次之,降低温度,a、b物质会析出晶体,c物质降低温度不会析出晶体,应该按照50 C时的溶解度进行计算,所以将50 C时a、b、c三种物质的饱和溶液降温至20C时,这三种溶液的溶质质量分数的大小关系是b> a> c,故C错误;D. c物质的溶解度随温度的升高而减小,所以将c的饱和溶液变为不饱和溶液,可采用降低温度的方法,故D正确;故选C O4. 如图是KNQ、MgSO4、NaCl三种物质的溶解度曲线。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【详解】 A、由甲、乙两种固体物质的溶解度曲线图可知,t2℃时甲的溶解度比乙的大,故 A 正确; B、将等质量甲、乙的饱和溶液从 t2 降到 t1,析出甲的质量大,故 B 不正确; C、甲的溶解度随温度升高而增大,升高温度可以将甲的饱和溶液变成不饱和溶液,故 C 正确; D、t1℃时,两种物质的溶解度相等,甲和乙的饱和溶液各 100g,其溶质的质量一定相等, 故 D 正确。 故选 B。
【解析】
s A、一定温度下,饱和溶液溶质的质量分数= 100g s ×100%。t1℃时,甲、乙的溶解度相
等,甲、乙两种饱和溶液的溶质质量分数相等,正确;B、没有确定溶液的质量无法比较 甲、乙饱和溶液析出晶体的质量,错误;C、t2℃时,甲的溶解度为 50g,即 100g 水中最多 溶解 50g 的甲,40g 甲加入 50g 水中,充分溶解后只能溶解 25g,所得的溶液质量为 75g,
5.一定温度下,向盛有 100g 蔗糖溶液的烧杯中再加入 5 克蔗糖,充分搅拌后一定不变的
是
A.溶质的质量
B.溶液的质量
C.溶质的质量分数 D.蔗糖的溶解度
【答案】D
【解析】
【分析】
溶液由溶质和溶剂组成,溶液的质量等于溶质和溶剂的质量和,被溶解的物质叫溶质。
【详解】
在一定温度下,向盛有 100 克蔗糖溶液的烧杯中再加入 5 克蔗糖,不确定蔗糖是否溶解,
3.如图是甲、乙两种固体物质在水中的溶解度曲线。下列说法正确的是
A.t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等 B.由 t2℃降温到 t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多 C.t2℃时,将 40g 甲物质加入 50g 水中,充分溶解后溶液的质量为 90g D.t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙多 【答案】A
误;C. 降低温度,可以使甲溶液变成饱和溶液,硝酸钾溶解度随温度升高而增大,故 C 正
确;D. 硝酸钾溶解度随温度升高而增大,升高温度,甲、乙两溶液的质量分数都不变,故
D 错误。
点睛∶硝酸钾溶解度随温度升高而增大,影响固体溶解度的因素是温度,溶质和溶剂本身
的性质。
7.a、b、c 三种物质的溶解度曲线如下图所示。取等质量 ℃的 a、b、c 三种物质的饱和 溶液,分别蒸发等量水后恢复至 ℃。下列说法不正确的是
2.甲、乙两种固体物质的溶解度曲线如图所示。下列有关叙述中错误的是
A.t2℃时甲的溶解度比乙的大 B.将甲、乙的饱和溶液从 t2℃降到 t1℃,析出甲的质量大 C.升高温度可将甲的饱和溶液变成不饱和溶液 D.t1℃时,甲和乙的饱和溶液各 100g,其溶质的质量一定相等 【答案】B 【解析】 【分析】 由甲、乙两种固体物质的溶解度曲线图可知,甲的溶解度受温度的影响较大,乙的溶解度 受温度的影响较小。
金属元素的质量分数为 33g ×100%=44%。 75g
点睛:掌握反应前后金属元素的质量不变、看成碳酸根离子被两个氯离子取代是正确解答 本题的关键,碳酸钾和碳酸钙的固体混合物 75g,与 500g 质量分数为 14.6%的盐酸充分反 应,充分反应后盐酸可能有剩余,蒸发时剩余的盐酸挥发掉,故不能用稀盐酸中氯元素的 质量进行计算;碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为 CaCO3+2HCl═CaCl2+H2O+CO2↑ 、 K2CO3+2HCl═2KCl+H2O+CO2↑ , 由 上 述 化 学 方 程 式 可 知 , 碳 酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,由与金属离子结 合的酸根离子的相对原子质量的差,进行分析解答即可。
是饱和溶液;降温到 t1℃,c 溶液就变为不饱和溶液
8.下图是不含结晶水的甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.t1℃时,100g 甲的饱和溶液中含有 50g 甲 B.t1℃时,配制甲乙两种物质的饱和溶液,需要相同体积的水 C.t1℃时,将等质量的甲、乙的饱和溶液升温至 t2℃,溶液质量仍然相等 D.要从含少量乙的甲中提纯甲,通常可采用蒸发结晶的方法 【答案】C 【解析】 A.由图知 t1℃时,甲物质的溶解度是 50g,即 100g 水中最多能溶解甲物质 50g,故 A 错误; B. t1℃时,甲、乙两物质的溶解度都是 50g,但是不知道所配甲乙两种物质的饱和溶液的质 量是否相等,故需要的水的体积也不一定相等,故此选项错误;C. 因两物质的溶解度都是 随温度的升高而增大,故当 t1℃时,将等质量的甲、乙的饱和溶液升温至 t2℃,两溶液都 变为不饱和溶液,故溶液质量仍然相等,此选项正确。D.因甲物质的溶解度受温度影响较 大,所以应采用降温结晶的方法。故错误。 答案为 C。
A、由溶解度曲线可知,MgSO4 的溶解度不是始终随温度的升高而减小,故 A 错误; B、t1℃时,氯化钾和硫酸镁的溶解度相等,如果两种溶液是饱和溶液,并且溶液质量相 等,则溶质质量一定相等,但题目未告知两溶液质量是否相等,故 B 错误; C、t2℃时,溶解度的含义是 100g 水中最多能溶解 ag 氯化镁,因此 100gMgCl2 的饱和溶液 中含有氯化镁的质量小于 ag,故 C 错误; D、氯化钾的溶解度随着温度的升高而增大,将 t1℃时的 KCl 饱和溶液升温到 t2℃,溶液由 饱和溶液变成不饱和溶液,故 D 正确。 故选:D。
溶液 溶解度解题技巧及练习测试题
一、溶液选择题
1.实验室有碳酸钾和碳酸钙的固体混合物 75g,使之与 500g 质量分数为 14.6%的盐酸充分 反应,将反应后的溶液蒸干得到 82.7g 固体。则原混合物中金属元素的质量分数为 A.44% B.50% C.55% D.68% 【答案】A 【解析】碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为 CaCO3+2HCl═CaCl2+H2O+CO2↑ 、 K2CO3+2HCl═2KCl+H2O+CO2↑ , 由 上 述 化 学 方 程 式 可 知 , 碳 酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相 对原子质量的和是 71,碳酸根的相对原子质量的和是 60,差是 11,即完全反应后质量增 加了 11 份质量.实际反应后固体质量增加了 82.7g-75g=7.7g,设原混合物中含碳酸根的 质量为 x,则 60:11=x:7.7g,x=42g;则所含金属元素质量为 75g-42g=33g,原混合物中
溶解度是指在一定温度下,某固态物质在 100g 溶剂中达到饱和状态时所溶解的溶质的质
80g 量,叫做这种物质在这种溶剂中的溶解度。A.该温度下,KNO3 的溶解度为 20g 20g =
100g ,x=50g,故 A 错误;B. 乙溶液的质量分数为 50g ×100%=33.3%,故 B 错
x
100g 50g
错误;D、t2℃时,甲的溶解度大于乙的溶解度,配制等质量饱和溶液,甲所需要水的质量 比乙少,错误。故选 A。
s
点睛:一定温度下,饱和溶液溶质的质量分数=×100%。100g s
4.甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )
A.t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙 B.t2℃时,30g 甲物质加入 50g 水中,充分搅拌后,所得溶液的溶质的质量分数为 37.5% C.将相同质量的甲、乙、丙三种物质的饱和溶液从 t2℃降温到 t1℃,析出晶体最多的是甲 D.欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法 【答案】B 【解析】 【详解】 A、通过分析溶解度曲线可知,t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是: 乙>甲=丙,故 A 正确;B、t2℃时,甲物质的溶解度是 50g,所以 30g 甲物质加入 50g 水
10.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中不正确的是( )
A.降低温度能使接近饱和的丙溶液变为饱和溶液 B.t2℃时,甲物质的溶解度大于乙物质的溶解度 C.t1℃时,甲、丙两物质的饱和溶液中溶质质量分数相等 D.将甲、乙、丙的饱和溶液从 t2℃降至 t1℃,溶质质量分数由大到小的顺序是乙>甲>丙 【答案】A 【解析】A.丙物质的溶解度随温度的升高而减小,所以降低温度能使接近饱和的丙溶液 变为饱和溶液,故 A 错误;B.通过分析溶解度曲线可知,t2℃时,甲物质的溶解度大于乙 物质的溶解度,故 B 正确;C.t1℃时,甲、丙两物质的溶解度相等,所以饱和溶液中溶质 质量分数相等,故 C 正确;D.t1℃时,乙物质的溶解度最大,甲物质的溶解度次之,较大 温度,甲、乙物质会析出晶体,丙物质不会析出晶体,应该按照 t2℃时的溶解度进行计 算,所以将甲、乙、丙的饱和溶液从 t2℃降至 t1℃,溶质质量分数由大到小的顺序是乙> 甲>丙,故 D 正确;故选 A。 点睛:根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质 的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量 分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸 发结晶的方法达到提纯物质的目的。
中,充分搅拌后,所得溶液的溶质的质量分数为 ×100%=33.3%,故 B 错误;C、将相同 质量的甲、乙、丙三种物质的饱和溶液从 t2℃降温到 t1℃,甲物质的溶解度变化最大,所 以析出晶体最多的是甲,故 C 正确;D、丙物质的溶解度随温度的升高而减小,所以欲将 丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法,故 D 正确。故选 B。 【点睛】 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解 性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的 大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶 的方法达到提纯物质的目的。
A.原饱和溶液中,溶质的质量分数 a>b="c" B.恢复至 t2℃时,析出溶质的质量 a>b=c C.恢复至 t2℃时,三种溶液一定都是饱和溶液 D.若继续降温至 t1℃,三种溶液一定都是饱和溶液 【答案】D 【解析】 a、b、c 三种物质的溶解度,a 的随温度的升高而增大,b 的受温度的变化影响不大,c 的 随温度的升高而降低。由于 t2℃时,Sa>Sb=Sc, 故溶质质量分数 a>b=c;由于温度没有变,因 此 S 不变,故恢复到 t2℃时,析出溶质的质量 a>b="c" ;蒸发后,都有固体析出,因此还
