高考化学 物质的量综合试题及答案
高考化学物质的量(大题培优 易错 难题)含答案

【详解】
(1)在该反应中,Mn元素化合价由反应前KMnO4中的+7价变为反应后MnCl2中的+2价,化合价降低,得到5个电子,Cl元素化合价由反应前HCl中的-1价变为反应后Cl2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO4、MnCl2前的系数是2,HCl前的系数是10,Cl2前的系数是5,根据原子守恒,KCl的系数是2,这样反应中有6个Cl原子未参加氧化还原反应,所有Cl原子都是由HCl提供,因此HCl前的系数为10+6=16,结合H原子反应前后相等,可知H2O的系数是8,用“双线桥”表示电子转移为: ;
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为______mL。
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:_______________。
【答案】0.250.4 mo•L-12.240.1532 g•mol-1500mL容量瓶8.2将浓硫酸沿烧杯内壁缓缓注入盛有水的烧杯中并用玻璃棒不断搅拌
(2)在标准状态下,2.24LCl2的物质的量n(Cl2)= =0.1mol。
①根据反应的化学方程式可知:生成0.1molCl2时,参与反应的KMnO4的物质的量为0.1mol× =0.04mol,则参与反应的KMnO4的质量m(KMnO4)=0.04mol×158g/mol=6.32g;
②由反应化学方程式可知,HCl被氧化后生成Cl2,因此根据Cl元素守恒可知:被氧化的HCl的物质的量n(HCl)氧化=0.1mol×2=0.2mol。
(3)在标准状况下,1.7 g氨气所占的体积约为_________L,与_____mol H2S含有相同的氢原子数。
高考化学 物质的量综合试题附答案

高考化学物质的量综合试题附答案一、高中化学物质的量1.①同温同压下,同体积的氨气和硫化氢气体(H2S)的质量比为_________;②同质量的氨气和硫化氢气体的体积比为_______________,其中含有的氢的原子个数比为___________;③若二者氢原子数相等,它们的体积比为_____________;④在相同条件下,在5.6g氮气中应添加___________g氨气所组成的混合气体与16g氧气所占的体积相等。
【答案】1:2 2:1 3:1 2:3 5.1【解析】【分析】【详解】①同温同压下,气体体积之比等于其物质的量之比,根据m=nM可知,同体积的氨气和硫化氢气体(H2S)的质量比为17g/mol:34g/mol= 1:2 ;②根据n=mM可知,同质量的氨气与硫化氢的物质的量之比为34g/mol: 17g/mol=2:1;相同条件下,气体体积之比等于其物质的量之比,二者体积之比为2:1,所含氢原子数目之比为(2⨯3):(1⨯2)=3:1;③假设H原子为3mol,氨气为1mol,硫化氢为1.5mol,二者体积之比为1mol: 1.5mol=2:3;④氮气物质的量n=5.6g0.2mol28g/mol=,氧气物质的量n=16g32g/mol= 0.2mol,则氨气物质的量为=0.5mol-0.2mol=0.3mol ,氨气的质量为0.3mol⨯17g/mol=5.1g。
2.设N A代表阿伏加德罗常数的数值,判定下列说法是否正确,打√或×?①22.4L(标准状况)氩气含有的质子数为18N A__________②标准状况下,11.2 LCH4和C2H4混合物中含氢原子数目为2N A__________③标准状况下,2.24LN2和O2的混合气体中分子数为0.2N A__________④1mol的CO和N2混合气体中含有的质子数为14N A__________⑤标准状况下,5.6LCO2气体中含有的氧原子数目为0.5N A__________⑥1.6g由O2和O3组成的混合物中含有的O原子数目为0.1N A__________⑦常温常压下,8g O2含有的电子数为4N A__________⑧常温常压下,22.4LNO2和CO2的混合气体中O原子数目为2 N A__________⑨标准状况下,22.4LCCl4中含有的CCl4分子数为N A__________⑩常温常压下,18 g H2O中含有的原子总数为3N A__________⑪标准状况下,11.2LCH3CH2OH中含有的分子数目为0.5N A__________⑫常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1N A__________【答案】√√ × √√√√ × × √ × ×【解析】【分析】运用n=m/M、V=n×V m、n= V/ V m等公式的应用转换,先求出物质的量,然后求出分子的总个数,在根据这个分子中含有多少个相关微粒。
高考化学专题题库∶物质的量的综合题附详细答案

高考化学专题题库∶物质的量的综合题附详细答案一、高中化学物质的量练习题(含详细答案解析)1.用98%的浓硫酸(其密度为1.84g/cm3,物质的量浓度为18.4 mol·L-1)配制100mL1.0mol·L-1稀硫酸,现有下列实验仪器备用:A.100mL量 B.托盘天平 C.玻璃棒D.50mL容量瓶 E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶。
请回答:(1)通过计算,需用量筒量取浓硫酸的体积为________mL;(2)实验时选用的仪器有______(填序号),使用容量瓶时第一步的操作是________________;(3)配制过程中,下列情况会使配制结果偏高的是________(填序号);①定容时俯视刻度线观察液面②容量瓶使用时未干燥③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线(4)实验步骤如下:①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解④恢复至室温⑤转移、洗涤⑥定容、摇匀⑦装瓶贴标签。
其中,第⑤步中“洗涤”操作的目的是_______________________。
【答案】5.4 CFGEH 检查容量瓶是否漏水①减少溶质损失,减小实验误差【解析】【分析】⑴根据稀释前后溶质物质的量不变进行计算。
⑵配制溶液时需要用到100mL容量瓶、玻璃棒、10mL量筒、胶头滴管、50mL烧杯,使用容量瓶前要检漏。
⑶①定容时俯视刻度线观察液面,溶液体积偏小,溶液溶度偏高;②容量瓶使用时未干燥,与结果无影响;③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线,溶液体积偏大,浓度偏低。
⑷溶质黏在烧杯内壁或玻璃棒上,要洗涤。
【详解】⑴用物质的量浓度为18.4 mol·L-1的浓硫酸配制100mL 1.0mol·L-1稀硫酸,根据稀释前后溶质物质的量不变得到18.4 mol·L−1 ×V= 1.0 mol·L−1×0.1 L,V=0.0054L =5.4mL,因此需用量筒量取浓硫酸的体积为5.4mL;故答案为:5.4。
高考化学物质的量的综合题试题及答案解析
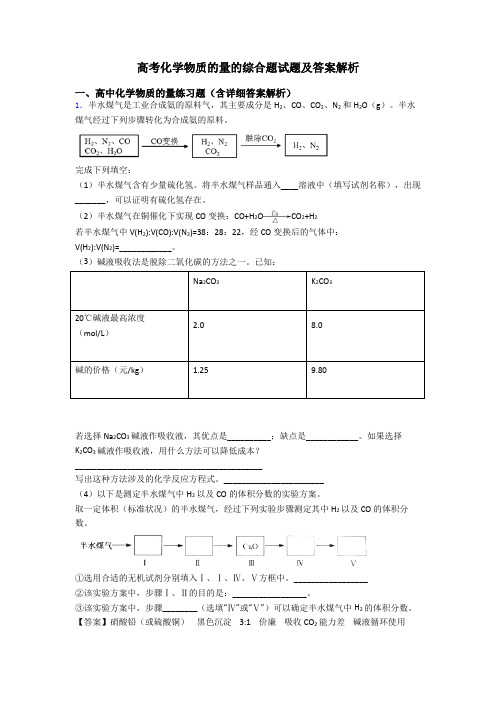
高考化学物质的量的综合题试题及答案解析一、高中化学物质的量练习题(含详细答案解析)1.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。
半水煤气经过下列步骤转化为合成氨的原料。
完成下列填空:(1)半水煤气含有少量硫化氢。
将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O CO2+H2若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。
已知:Na2CO3K2CO320℃碱液最高浓度(mol/L)2.08.0碱的价格(元/kg) 1.259.80若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。
如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?___________________________________________写出这种方法涉及的化学反应方程式。
_______________________(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
_________________②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。
【答案】硝酸铅(或硫酸铜)黑色沉淀 3:1 价廉吸收CO2能力差碱液循环使用2KHCO3→K2CO3+CO2↑+H2O除去半水煤气中的CO2(包括H2S)和H2O IV【解析】【分析】【详解】(1)硫化氢能与重金属生成沉淀,所以将半水煤气样品通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀可以证明有硫化氢存在。
高考化学物质的量(大题培优)附答案解析

高考化学物质的量(大题培优)附答案解析一、高中化学物质的量1.在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。
反应:2KMnO 4+16HCl=2KCl+2MnCl 2+5Cl 2↑+8H 2O(1)“双线桥法”标出电子转移情况________ 。
(2)若生成2.24L 标准状况时的氯气,请计算(写出必要的计算过程):①理论上需要多少克KMnO 4参加反应?________。
②被氧化的HCl 的物质的量为多少?________。
【答案】 6.32g 0.2 mol【解析】【分析】(1)根据元素化合价升降数目等于反应过程中电子转移数目分析,标出电子转移情况;(2)先计算Cl 2的物质的量,然后根据方程式中KMnO 4、HCl 与Cl 2之间的反应转化关系计算。
【详解】(1)在该反应中,Mn 元素化合价由反应前KMnO 4中的+7价变为反应后MnCl 2中的+2价,化合价降低,得到5个电子,Cl 元素化合价由反应前HCl 中的-1价变为反应后Cl 2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO 4、MnCl 2前的系数是2,HCl 前的系数是10,Cl 2前的系数是5,根据原子守恒,KCl 的系数是2,这样反应中有6个Cl 原子未参加氧化还原反应,所有Cl 原子都是由HCl 提供,因此HCl 前的系数为10+6=16,结合H 原子反应前后相等,可知H 2O 的系数是8,用“双线桥”表示电子转移为:;(2)在标准状态下, 2.24LCl 2的物质的量n(Cl 2)=m V 2.24L V 22.4L /mol=0.1mol 。
①根据反应的化学方程式可知:生成0.1molCl 2时,参与反应的KMnO 4的物质的量为0.1mol×25=0.04mol ,则参与反应的KMnO 4的质量m(KMnO 4)=0.04mol×158g/mol=6.32g ; ②由反应化学方程式可知,HCl 被氧化后生成Cl 2,因此根据Cl 元素守恒可知:被氧化的HCl 的物质的量n(HCl)氧化=0.1mol×2=0.2mol 。
高考化学专题题库∶物质的量的综合题及详细答案

高考化学专题题库∶物质的量的综合题及详细答案一、高中化学物质的量1.将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
(1)写出Al与NaOH溶液反应的化学方程式___________________;(2)镁和铝的总质量为________g;(3)b点溶液中的溶质为__________,硫酸的物质的量浓度为___________mol/L;(4)生成的氢气在标准状况下的体积为__________L;(5)c点溶液中通入足量的CO2的反应化学方程式为___________。
【答案】2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 9 Na2SO4 2.5 10.08NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3【解析】【分析】由图象可知,从开始至加入NaOH溶液20mL,没有沉淀生成,说明原溶液中硫酸溶解Mg、Al后有剩余,溶液的溶质为H2SO4、MgSO4、Al2(SO4)3,此时发生的反应为:H2SO4+2NaOH=Na2SO4+2H2O;当V(NaOH溶液)=200mL时,沉淀量最大,此过程中Mg2+、Al3+与OH-反应生成Mg(OH)2和Al(OH)3,溶液溶质为Na2SO4;从200mL到240mL,NaOH溶解固体Al(OH)3,发生反应:OH-+ Al(OH)3=AlO2-+2H2O,据此分析解答。
【详解】(1)Al与NaOH溶液反应产生NaAlO2和H2,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(2)根据图象可知Mg(OH)2和Al(OH)3的物质的量之和为0.35mol,从200mL到240 mL,NaOH溶解Al(OH)3,当V(NaOH溶液)=240mL时,沉淀不再减少,此时全部为Mg(OH)2,物质的量为0.15mol,Al(OH)3的物质的量为0.35mol-0.15mol=0.2mol,由元素守恒可知n(Al)=n[Al(OH)3]=0.20mol,n(Mg)=n[Mg(OH)2]=0.15mol,所以镁和铝的总质量为m(Al)+m(Mg)=0.20mol×27g/mol+0.15mol×24g/mol=9g;(3)沉淀量最大时为Mg(OH)2和Al(OH)3,溶液中溶质为Na2SO4,根据钠元素守恒可知此时n(Na2SO4)等于200mLNaOH溶液中含有的n(NaOH)的0.5倍,所以n(Na2SO4)=0.5×5mol/L×0.2L =0.5mol,所以H2SO4的物质的量浓度c(H2SO4)=0.50.2Lmol=2.5mol/L;(4)根据以上分析,n(Al)=0.2mol,n(Mg)=0.15mol,由于Al是+3价金属,Mg是+2价的金属,所以金属失去电子的物质的量n(e-)=3n(Al)+2n(Mg)=0.2mol×3+ 0.15mol×2=0.9mol,根据反应过程中得失电子守恒,可知反应产生氢气的物质的量n(H2)=12n(e-)=0.45mol,则在标准状况下的体积V(H2)=0.45mol×22.4L/mol=10.08L;(5)在b点时溶液中溶质为Na2SO4,沉淀量为Mg(OH)2和Al(OH)3,在b→c过程中发生反应:NaOH+Al(OH)3=NaAlO2+2H2O,至c点,该反应恰好反应完全,故c点溶液的溶质为Na2SO4、NaAlO2,由于酸性:H2CO3>Al(OH)3,所以c点溶液中通入足量的CO2,NaAlO2、CO2、H2O反应产生Al(OH)3和NaHCO3,反应的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3。
全国高考化学物质的量的综合高考真题汇总附详细答案

全国高考化学物质的量的综合高考真题汇总附详细答案一、高中化学物质的量1.按要求完成下列填空I.(1)给定条件下的下列四种物质:a.10g氖气b.含有40mol电子的NH3c.标准状况下8.96LCO2d.标准状况下112g液态水则上述物质中所含分子数目由多到少的顺序是________________(填序号)。
(2)标准状况下,0.51g某气体的体积为672mL,则该气体摩尔质量为______。
(3)将100mL H2SO4和HCl的混合溶液分成两等份,一份中加入含0.2molNaOH溶液时恰好中和完全,向另一份中加入含0.05molBaCl2溶液时恰好沉淀完全,则原溶液中c(Cl-)=____ mol/L。
II.现有以下物质:①铝;②二氧化硅;③液氯;④NaOH溶液;⑤液态HCl;⑥NaHCO3晶体;⑦蔗糖;⑧熔融Na2O;⑨Na2O2固体;⑩CO2。
回答下列问题(用相应物质的序号填写):(1)其中可以导电的有__________。
(2)属于电解质的有_______,非电解质有__________。
(3)写出向⑨与⑩反应的化学方程式___________。
(4)写出①与④的离子方程式_____________。
(5)写出⑤的水溶液与⑥的水溶液反应的离子方程式___________________ 。
(6)写出②与④反应的离子方程式_______________________________ 。
【答案】d>b>a>c 17g/mol 2 ①④⑧⑤⑥⑧⑨②⑦⑩ 2Na2O2 + 2CO2=2Na2CO3 + O2 2Al + 2H2O + 2OH- = 2AlO2- + 3H2 H+ + HCO3- = H2O + CO2 SiO2 + 2OH- = SiO32- + H2O【解析】【分析】I.利用n=mM=ANN=mVV计算。
II.①铝能导电,既不是电解质,也不是非电解质;②二氧化硅不能导电,为非电解质;③液氯不能导电,既不是电解质,也不是非电解质;④NaOH溶液能导电,为混合物,既不是电解质,也不是非电解质;⑤液态HCl不能导电,为电解质;⑥NaHCO3晶体不能导电,为电解质;⑦蔗糖不能导电,为非电解质;⑧熔融Na2O能导电,为电解质;⑨Na2O2固体不能导电,为电解质;⑩CO2不能导电,为非电解质。
全国高考化学物质的量的综合高考真题汇总含答案解析

全国高考化学物质的量的综合高考真题汇总含答案解析一、高中化学物质的量练习题(含详细答案解析)1.某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2。
实验步骤如下:①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95 g.②连接好实验装置,检查装置的气密性.③加热,开始反应,直到不再有气体产生为止.④测量排入量筒中水的体积为285.0 mL,换算成标准状况下氧气的体积为279.7 mL.⑤准确称量试管和残留物的质量为15.55 g.根据上述实验过程,回答下列问题:(1)如何检查装置的气密性?______________________________________________。
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒的高度使广口瓶和量筒内的液面高度相同②使试管和广口瓶内气体都冷却至室温③读取量筒内液体的体积这三步操作的正确顺序是________(请填写步骤代码。
进行③的实验操作时,若仰视读数,则读取氧气的体积________(填“偏大”、“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是________mol;实验测得氧气的摩尔体积是________(保留小数点后两位)。
【答案】往广口瓶中注满水,塞紧橡胶塞,按装置图连接好装置,用手将试管底部捂热,若观察到广口瓶中长玻璃管内液面上升,松开手后,过一会儿长玻璃管内的液面下降,则证明该装置不漏气②①③偏小0.012522.38 L/mol【解析】【分析】【详解】(1)往广口瓶中装满水,使装置左侧形成密闭体系,通过捂热试管看广口瓶中长导管内液面高度的变化来判断装置的气密性;综上所述,本题答案是:往广口瓶中注满水,塞紧橡胶塞,按装置图连接好装置,用手将试管底部捂热,若观察到广口瓶中长玻璃管内液面上升,松开手后,过一会儿长玻璃管内的液面下降,则证明该装置不漏气。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.(1)1mol H2SO4中含有_____个硫原子,_____mol O。
(2)写出下列物质在水溶液中的电离方程式
HCl:_______________NaHSO4:____________________
【解析】
【分析】
(1)根据物质结构进行计算;
(2)强电解质完全电离;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;氢氧化亚铁白色沉淀迅速变为灰绿色,最终变为红褐色为氢氧化亚铁与氧气、水反应生成氢氧化铁;铜与氯化铁溶液反应生成亚铁离子和铜离子;
(4)根据化合价升降法及化合价只靠拢不相交的原则配平;
(5)还原剂,失电子,化合价升高,发生氧化反应,产物为氧化产物;氧化剂得电子,化合价降低,产物为还原产物。
【点睛】
本题考查了物质检验实验方案的设计以及化学方程式的书写、溶质物质的量浓度的计算,明确硫酸根离子、碳酸根离子的性质是解题的关键。
3.按要求完成下列各小题
(1)在同温同压下,相同质量的N2和H2S气体的体积比为____。
(2)0.8molCO和0.4molCO2中电子数目之比为___,含有氧原子物质的量之比为___,相同条件下两物质的密度之比为___。
【解析】
【分析】
根据阿伏伽德罗定律进行分析解答;根据氧化还原反应进行判断。根据溶解规律和离子的特征选择除杂试剂。如Na2SO4中的Na2CO3目的是除去CO32-离子,所以选择H2SO4进行除杂。
【详解】
(1)相同质量的N2和H2S的物质的量之比为 ,根据阿伏伽德罗定律,在同温同压下,气体体积之比等于物质的量之比,因此相同质量的N2和H2S气体的体积比为17:14。答案:17:14;
(2)电子数目之比等于电子的物质的量之比。0.8molCO中电子的物质的量为0.8 mol×(6+8)=11.2mol,0.4molCO2中电子的物质的量为0.4mol×(6+8×2) =8.8mol,电子数目之比为11.2:8.8=14:11;含有氧原子物质的量之比为0.8:0.4 2=1:1,根据阿伏伽德罗定律的推论可知,相同条件下,气体的密度与摩尔质量成正比,所以相同条件下两物质的密度之比为:28:44=7:11。答案:14:11 1:1 7:11;
【点睛】
掌握有关硝酸反应的计算,一般用守恒方法,如电子守恒,反应中氮元素得到电子物质的量等于铜失去电子的物质的量,也等于铜离子结合的氢氧根的物质的量,据此计算即可。
2.I.NaCl溶液中混有Na2CO3、Na2SO4,为检验两种物质的存在,请你根据所选择的试剂,按实验步骤的先后顺序写出相应的化学方程式:
【答案】Na2CO3+2HCl=2NaCl+CO2↑+H2OCO2+Ca(OH)2=CaCO3↓+H2OBaCl2+Na2SO4=BaSO4↓+2NaCl0.3mol/L
【解析】
【分析】
I.首先加入过量HCl,有气泡产生,该气体能够使澄清石灰水变浑浊,说明有Na2CO3,再滴加过量BaCl2溶液,最终有白色沉淀证明有Na2SO4;
高考化学 物质的量综合试题及答案
一、高中化学物质的量
1.NH3、NO、NO2都是常见重要的无机物,是工农业生产、环境保护、生命科学等方面的研究热点。
(1)写出氨在催化剂条件下与氧气反应生成NO的化学方程式_____。
(2)氮氧化物不仅能形成酸雨,还会对环境产生的危害是形成_____。
(3)实验室可用Cu与浓硝酸制取少量NO2,该反应的离子方程式是_____。
故答案为:4NH3+6NO 5N2+6H2O;
(5)n(NO2)=n(NO)=2.24L÷22.4L/mol=0.1mol,根据电子转移守恒,可知n(Cu)= =0.2mol,由Cu原子守恒可得氢氧化铜的物质的量为0.2mol,生成Cu(OH)2沉淀的质量为0.2mol×98g/mol=19.6g,故答案为:19.6。
II.混合溶液加入过量的氯化钡溶液,发生反应:BaCl2+Na2SO4=BaSO4↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl,得到16.84g白色沉淀为BaSO4、BaCO3,沉淀用过量稀HNO3处理,发生反应:BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O,最终6.99g沉淀为BaSO4,根据n= 计算BaSO4的物质的量,而n(Na2SO4)=n(BaSO4),再根据c= 计算c(Na2SO4)。
(3)写出下列化学反应的方程式
呼吸面具中过氧化钠与二氧化碳反应的化学方程式_________________
氢氧化亚铁白色沉淀迅速变为灰绿色,最终变为红褐色的反应的化学方程式____________________
印刷电路板处理时铜与氯化铁溶液反应的离子方程式_______________________
(3)卤素单质的氧化性为F2>Cl2>Br2>I2,单质的氧化性越强,其对应的离子的还原性越弱,所以还原性Br->Cl-,还原性最弱的阴离子是Cl-;金属单质的金属性越强,其离子的氧化性越弱,所以氧化性最强的离子是Cu2+;属于中间价态的元素既有氧化性又有还原性,所以Fe2+既有氧化性又有还原性的;答案:Cl-Cu2+Fe2+;
B.19.6磷酸(H3PO4)的物质的量为 =0.2mol,则0.2NA个硫酸分子与19.6磷酸(H3PO4)含有的氧原子数均为0.8NA,故B#43;6H2O光化学烟雾Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O4NH3+6NO 5N2+6H2O19.6
【解析】
【分析】
(1)氨气和氧气在催化剂的条件下反应生成一氧化氮和水;
(2)氮氧化物还可以形成光化学烟雾,破坏臭氧层;
(3)铜和浓硝酸反应生成硝酸铜、二氧化氮和水,浓硝酸和硝酸铜都能写成离子形式;
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.0.2NA个硫酸分子与19.6磷酸(H3PO4)含有相同的氧原子数
C.常温下,28克N2和CO的混合物,含有2NA个原子
D.标准状况下,33.6 L氧气中含有9.03×1023个氧气分子
【答案】A
【解析】
【详解】
A.稀有气体为单原子分子,含有NA个氦原子的氦气物质的量为1mol,标准状况下的体积约为22.4L,故A错误;
(4)根据氧化还原反应中,化合价只靠拢不相交的原则,碘离子变为0价,碘酸根离子变为0价,则最小公倍数为5,则离子方程式为5 I-+IO3-+ 6H+=3I2+3H2O;
高氯酸铵自身发生氧化还原反应,N、O的化合价升高,Cl的化合价降低,根据电子得失守恒,则4NH4ClO4=2N2↑+5O2↑+4HCl+6H2O;
(4)配平下列方程式:
_____I-+_____IO3-+_____H+—_____I2+_____H2O
_____NH4ClO4——_____N2↑+_____O2↑+_____HCl+_____H2O
(5)用单线桥法或双线桥法表示该反应转移电子的方向和数目并填空:
Cu+4 HNO3(浓)= Cu(NO3)2+2 NO2↑+2H2O__________________
HNO3的作用是__________,发生氧化反应,氧化产物是__________。
【答案】NA4HCl=H++Cl-NaHSO4= Na++ H++SO42-2Na2O2+2CO2=2Na2CO3+O24Fe(OH)2+O2+2H2O=4Fe(OH)32Fe3++Cu=2Fe2++Cu2+5163342546 氧化性和酸性Cu(NO3)2
【详解】
I.首先向该物质的水溶液中滴加过量盐酸,有气体产生,该气体能够使澄清的石灰水变浑浊,证明溶液中含有Na2CO3,反应方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O,CO2+Ca(OH)2=CaCO3↓+H2O,然后向溶液中加入过量BaCl2溶液,产生白色沉淀,证明含有Na2SO4,发生该反应的化学方程式为:Na2SO4+BaCl2=2NaCl+BaSO4↓;
(4)氨气使一氧化氮转化为两种无毒气体,其中一种是水蒸气,另外一种为氮气;
(5)根据电子转移守恒计算铜的物质的量,由铜原子守恒可得氢氧化铜的物质的量,在根据m=nM计算。
【详解】
(1)氨气与氧气在催化剂条件下生成NO与水,反应方程式为:4NH3+5O2 4NO+6H2O,
故答案为:4NH3+5O2 4NO+6H2O;
(2)氮氧化物还可以形成光化学烟雾、破坏臭氧层等,故答案为:光化学烟雾;
(3)Cu与浓硝酸反应生成硝酸铜、二氧化氮与水,浓硝酸、硝酸铜都写成离子形式,反应离子方程式为:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O,答案为:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2O;
(4)NH3使NO转化为两种无毒气体,其中之一是水蒸气,另外一种为氮气,反应方程式为:4NH3+6NO 5N2+6H2O,
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式为2Na2O2+2CO2=2Na2CO3+O2;氢氧化亚铁白色沉淀迅速变为灰绿色,最终变为红褐色为氢氧化亚铁与氧气、水反应生成氢氧化铁,方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;铜与氯化铁溶液反应生成亚铁离子和铜离子,离子方程式为2Fe3++Cu=2Fe2++Cu2+;
