原子的结构和电子构型ppt课件
人教版教材《原子结构》优秀课件1

值越大,能级越高。 D.羧基、酚羟基可以与金属钠反应;羧基、酚羟基可以与NaOH发生反应;NaHCO3只能与羧基发生反应。1 mol该物质最多消耗Na
、NaOH、NaHCO3的物质的量之比为2:2:1,D正确。
3d54S1 d区
3S1
S区
3d104S1 ds区
根据某离子的外层电子分布式,指出元素所处区
+1价 3S23P6
S区
+2价 3S23P63d5 d区
例4:某元素为金属,最高氧化数为+6,原子半径 是同族中最小的。请写出:
(1) 原子的电子分布式。 (2) 原子的外层电子分布式。 (3) +3 价离子的外层电子分布式。 (4) 该元素所在的周期、族、区、元素名称。
注意对于过渡金属离子: 如 Fe2+:3d6 ( ╳ ) 应该将电子层写完整:3s23p63d6
(4)例外:并不是所有的核外电子排布都满 足以上规则。根据光谱实验的结果,发现 Ru,Nb,Rh,Pd,W,Pt及镧系和锕系的一些元 素的核外电子排布并不符合以上规则。
如:
41: 铌,Nb: 4d45s1 44:钌,Ru: 4d75s1 45: 铑,Rh: 4d85s1 74: 钨, W: 5d46s2 78: 铂, Pt: 5d96s1 注意:不需要掌握以上内容
D. KW/c(H+)=0.1 mol·L-1的溶液中:Ca2+、NH4+、CH3COO-、HCO3-
过渡元素:写出(n-1)d ns轨道的 5.下列有关实验装置或操作正确的是
【解析】
9.【解答】解:无色时可排除 Cu2+、Fe2+、Fe3+、MnO4﹣等有色离子的存在,
原子的结构和电子构型

原子的结构和电子构型原子是构成物质的最基本单位,它由质子、中子和电子组成。
质子和中子位于原子的核心,称为原子核,而电子则围绕着原子核旋转。
原子核是原子的中心,由质子和中子组成。
质子带正电荷,质子数决定了元素的原子序数。
中子不带电荷,其数量会影响原子的质量。
电子壳是电子的运动区域,分为n个主量子能级(n=1,2,3...)。
第一主量子能级(K壳)离原子核最近,第二主量子能级(L壳)紧随其后,以此类推。
每个主量子能级可以容纳不同数量的电子。
电子轨道是电子在主量子能级中的运动路径。
每个主量子能级可以含有不同数量的电子轨道,分别以s、p、d和f来表示。
s轨道是最简单的电子轨道,每个s轨道可以容纳最多2个电子。
s轨道有一个球形的分布,出现在所有主量子能级上。
p轨道比s轨道复杂一些,每个p轨道可以容纳最多6个电子。
p轨道有三个不同的方向(xyz轴),分别以px、py、pz表示。
d轨道相对更复杂,每个d轨道可以容纳最多10个电子。
d轨道有五个不同的方向,分别以dxy、dyz、dzx、dx2-y2和dz2表示。
f轨道更加复杂,每个f轨道可以容纳最多14个电子。
f轨道有七个不同的方向,分别以fxyz、fx2-y2、fyz2、fzx2、fz3和fx3-y2表示。
当电子填充到原子中时,要遵循一定的顺序。
这一顺序可以通过洪特规则和泡利不相容原理来确定。
洪特规则指出,当电子填充到电子轨道中时,首先填充最低能级的轨道。
泡利不相容原理指出,每个电子轨道上的电子应具有相反的自旋方向。
根据这些规则,我们可以确定原子的电子构型。
以氧(O)原子为例,氧原子有8个电子,因此电子构型为1s22s22p4、这意味着氧原子的电子首先填充到1s轨道中,然后填充到2s轨道中,最后填充到2p轨道中。
电子构型对于理解原子性质和化学反应非常重要。
它可以帮助我们预测原子的化学行为和物理性质,以及解释元素周期表的排列。
《结构化学》课件

contents
目录
• 结构化学简介 • 原子结构与性质 • 分子的电子结构与性质 • 晶体结构与性质 • 结构化学实验结构化学的定义
总结词
结构化学是一门研究物质结构与 性质之间关系的科学。
详细描述
结构化学主要研究原子的排列方 式、电子分布和分子间的相互作 用,以揭示物质的基本性质和行 为。
晶体的电导率、热导率等性质取决于其内 部结构,不同晶体在这些方面表现出不同 的特性。
晶体的力学性质
晶体材料的应用
晶体的硬度、韧性等力学性质与其内部原 子排列密切相关,这些性质决定了晶体在 不同工程领域的应用价值。
晶体材料广泛应用于电子、光学、激光、 半导体等领域,如单晶硅、宝石等。了解 晶体的性质是实现这些应用的关键。
分子的选择性
分子的选择性是指分子在化学反应中对反应物的选择性和对产物的选择性。选择性强的分 子可以在特定条件下优先与某些反应物发生反应,产生特定的产物。
04
晶体结构与性质
晶体结构的基础知识
晶体定义与分类
晶体是由原子、分子或离子在空 间按一定规律重复排列形成的固 体物质。根据晶体内部原子、分 子或离子的排列方式,晶体可分 为七大晶系和14种空间点阵。
电子显微镜技术
• 总结词:分辨率和应用 • 电子显微镜技术是一种利用电子显微镜来观察样品的技术。相比光学显微镜,
电子显微镜具有更高的分辨率和更大的放大倍数,因此可以观察更细微的结构 和组分。 • 电子显微镜技术的分辨率一般在0.1~0.2nm左右,远高于光学显微镜的分辨 率(约200nm)。因此,电子显微镜可以观察到更小的晶体结构、病毒、蛋 白质等细微结构。 • 电子显微镜技术的应用范围很广,例如在生物学领域中,可以用于观察细胞、 病毒、蛋白质等生物样品的结构和形态;在环境科学领域中,可以用于观察污 染物的分布和形态;在材料科学领域中,可以用于观察金属、陶瓷、高分子等 材料的表面和断口形貌等。
第八章 原子结构(2)
电负性( P)变化
主 族 元 素
元素的原子半径变化趋势
第四周期元素 r/pm 第五周期元素
Sc 161 Y
Ti 145 Zr
V 132 Nb
Cr 125 Mo
r/pm 第六周期元素 r/pm
181 Lu 173
160 Hf 159
143 Ta 143
146 W 137
镧系元素从左到右,原子半径减小幅 度更小,这是由于新增加的电子填入外数 第三层上,对外层电子的屏蔽效应更大, 外层电子所受到的 Z* 增加的影响更小。镧 系元素从镧到镱整个系列的原子半径减小 不明显的现象称为镧系收缩。
同一周期:
短周期:从左到右,Z*显著增加。 长周期:从左到右,前半部分有Z*增加 不多,后半部分显著增加。 同一族:从上到下,Z*增加,但不显著。
2. 原子半径
在同一周期中,从左到右减小 主 由于核电荷的增加,核外电子受核的引 族 力增大,原子半径减小。 元 素 在同一族中,从上到下增加 由于主量子数 n 的增加,原子半径一般增 加。 过渡元素:从左到右r 缓慢减小; 从上到下r略有增大。
Z=56,Ba: [Xe] 6s2 。
四个量子数小结:
原子中每个电子的运动状态可以用n,l,m, ms四个量子数来描述:主量子数n决定电子层 数和主要电子的能量;角量子数l决定原子轨道
的形状,同时也影响电子的能量;磁量子数m
决定原子轨道在空间的伸展方向;自旋量子数
ms决定电子自旋的方向。四个量子数确定后,
3. 电离能
第一电离能——处于基态的1mol气态原子失去 1mol电子成为气态一价正离子所需的能量,称 为该元素的第一电离能。 同一周期中 自左至右,第一电离能一般增加,但有一 些波动。当电子结构为全充满或半充满时, 其第一电离能相应较大。 同一族中 主族,自上而下第一电离能依次减小。
原子的结构完整版PPT课件

工业领域应用
放射性同位素可用于材料 检测、无损探伤、辐射加 工等。
其他领域应用
放射性同位素还可用于科 学研究、环境保护、农业 生产等领域。
放射性同位素对环境影响及安全防护措施
对环境影响
放射性同位素衰变产生的射线会对环境和生物体造成危害,如污 染空气、水源和土壤等。
安全防护措施
为了保障人类和环境安全,需要采取一系列安全防护措施,如合 理选址、屏蔽防护、废物处理等。
放射性同位素概念及来源
放射性同位素定义
01
具有相同原子序数但质量数不同的同位素,能自发地放出射线
并转变为另一种元素。
放射性同位素来源
02
天然放射性元素和人工合成放射性元素。
放射性同位素衰变类型
03
α衰变、β衰变和γ衰变。
放射性同位素在医学、工业等领域应用
医学领域应用
放射性同位素可用于诊断 和治疗疾病,如放射性碘 治疗甲状腺疾病、PET扫 描等。
过渡元素位于周期表中间部分, 包括3~12列的元素。它们具有 多种氧化态和丰富的化学性质, 是构成众多合金和催化剂的重要
成分。
稀有气体元素
稀有气体元素位于周期表的最右 侧,它们具有稳定的8电子构型 (氦为2电子构型),化学性质 极不活泼,一般不易与其他物质
发生化学反应。
04
化学键与分子间作用 力
化学键类型及特点
分子间作用力影响物质的物理性质
分子间作用力主要影响物质的熔点、沸点、密度、硬度等物理性质。一般来说,分子间作用力越强,物质的熔点 、沸点越高,密度越大,硬度也越大。例如,氢键的存在使得水的熔沸点异常高,范德华力则主要影响由分子构 成的物质的物理性质。
05
原子光谱与能级跃迁
第四章原子结构简介

18
【例如】n=3, l=0,1,2 l 可以有三个取值。也就是说,第三电子层有
三个亚层,分别是:3s、3p、3d。 同一层中(n相同),l 越大,则轨道的能量越高。
E3s E3p E3d
另外,l 不同的原子轨道,形状不一样。
08:28
19
角量子数与电子亚层、轨道形状的对应关系
角量子数 亚层符号 轨道形状
鲍林原子轨道能级图★
08:28
29
08:28
30
E4s E4p E4d E4f
08:28
31
08:28
32
从鲍林近似能级图可以看出,各轨道能级次序如下:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f< 5d<6p<7s<5f<6d<7p
08:28
能量相同的轨道称为简并轨道(或等价轨道), 如:3px、3py、3pz 互相称为等价轨道。
08:28
23
l=2,m=-2,-1,0,+1,+2 五个取值,说明d 轨道在空间有5个不同取向 的原子轨道:
dz2 、dxy 、dxz 、dx2 y2 、d yz
08:28
24
根据n、l、m三个量子数的取值范围,可以 确定每个电子层中原子轨道的数目。
理奖 量子概念是1900年普朗克首先提出的,到今天已经一百多年 了。期间,经过玻尔、德布罗意、玻恩、海森柏、薛定谔、 狄拉克、爱因斯坦等许多物理大师的创新努力,到20世纪30 年代,初步建立了一套完整的量子力学理论
08:28
4
§4-1 氢原子光谱和玻尔理论
高考一轮复习化学课件原子结构核外电子排布规律

电子云概念及形状
电子云概念
电子在原子核外很小的空间内作高速运动,其运动规律跟 一般物体不同,没有确定的运动轨道,只能用电子云来描 述。
电子云形状
s电子云是球形对称的,在核外半径方向呈现球对称分布 ;p电子云是纺锤形,并不是电子运动轨迹,而是表示电 子出现的几率大小;d电子云是花瓣形。
电子云伸展方向
领域。
02
核外电子排布原理
能量最低原理与电子排布顺序
01
能量最低原理
电子在原子核外排布时,总是尽可能排布在能量最低的电子层里。
02
电子排布顺序
即电子层顺序,遵循1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、
5p、6s、4f…的顺序。
03
电子层与能级
电子层可用n(n=1、2、3…)表示,n值越小,电子层离核越近,能量
非金属元素
非金属元素的原子最外层电子数一般较多,容易得到电子形成阴离子,或与其 他非金属元素共用电子形成共价键。其核外电子排布通常具有较少的电子层, 且最外层电子数接近或达到稳定构型。
过渡元素核外电子排布特征
过渡元素
过渡元素是指元素周期表中d区的一系列金属元素,其核外电 子排布特点是具有未填满的d电子层。这些元素的原子最外层 通常只有1-2个电子,而次外层(即d层)电子数则依次增加 。
高考一轮复习化学课
件原子结构核外电子
排布规律 汇报人:XX
20XX-02-04
• 原子结构基本概念 • 核外电子排布原理 • 原子核外电子排布规律 • 典型元素核外电子排布分析 • 化学键与分子结构基础 • 高考一轮复习策略与技巧
目录
01
原子结构基本概念
原子组成与性质
01
原子结构

电子在确定的轨道上,能量状态确定,称为定态。
En = -B /n2 , B = 2.18×10-18J
n = 1时轨道能量最低,称为基态,n=2, 3, 4….的状态称为激发态。 轨道跃迁假设
ΔE = En2-En1 = B(1/n12 –1/n22) = hν
25
1s 2s
z
3s
z
z
x
x
y
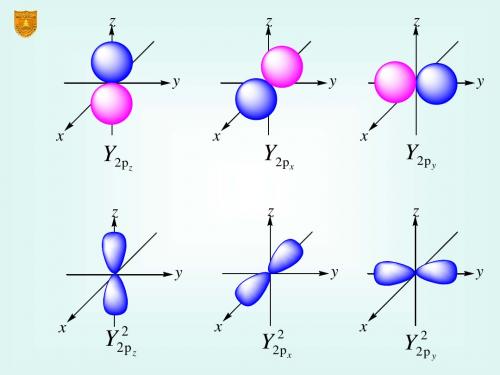
2pz
2px
2py
y
z
z
z
y
x
x
y
x
x
3dxy
3dxz
3dyz
3dz2
3dx2-y2
26
核外电子几率分布和径向分布
D = |ψ2| dV
电子出现几率
该函数存在极值现象。
27
核外电子出现几率的径向分布图
D
1) n-l 个极值;
0.5
2) n 相同,l越小,小峰、离核越近,
12
Lyman Balmer Paschen
紫外 可见 红外 光区 光区 光区
13
玻尔理论的意义和局限性
成功解释了原子的稳定性氢原子光谱。 不能解释多电子原子光谱,不能解释光谱在磁场中的分裂。
还没有认识到波粒二象性是微观粒子的运 动的普遍特征。
14
9.2 单电子原子的波函数
薛定谔方程
2ψ +
x2
自旋量子数ms
与电子自旋状态相关的参数。取值为±(1/2),以↑和↓表示。
23
单电子原子中电子的可能运动状态与四个量 子数之间的关系
nl 10
0 2
1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
规则2:泡利不相容原理
一个轨道最多仅能填充两个电子,且必须自旋相反
规则3:洪特规则
在能量相等的轨道上,自旋平行的电子数目最多时,原 子的能量最低。所以在能量相等的轨道上,电子尽可能 自旋平行地多占不同的轨道。
完整版课件
7
一些元素的基态
1s22s22p63s23p3
Na 11
1s22s22p63s1
O 8
1s22s22p4
2p
2s
1s
完整版课件
8
此课件下载可自行编辑修改,供参考! 感谢您的支持,我们努力做得更好!
能级的划分是因为电子能量不同,一般来 说,电子先排在能量较低的轨道,再排能量 高的轨道
电子在原子中处于不同的能层
完整版课件
3
电子在原子中如何分布?
每个圆圈表示一个能级,每一行对应一个能层,各圆圈连接 线方向表示随核电荷数递增而增加的电子填入能级顺序
完整版课件
4
电子在原子中如何分布?
多电子原子轨道能级
原子的结构和电子构型
完整版课件
1
原子的结构
原子示意图:密集的、带正电荷的原子核包含了原子的大部 分质量,它被带负电荷的电子包围
完整版课件
2
电子在原子中如何分布?
原子核外的电子是分层排布的,每一层都 可以叫做能层,可以分为K.L.M.N.O.P.Q这7 个能层,每个能层最多能排2n2个电子,每 个能层又可以为多个能级。
完整版课件
能级交错 ?
E3d>E4s
钻穿效应和屏蔽效应
5
电子在原子中如何分布?
s能级的原子轨道图 ns能级的各有1个轨道,呈球形
p能级的原子轨道图
np能级的各有3个轨道,呈哑铃 形, 3个轨道相互垂直
完整版课件
6
原子核外电子排布规律
规则1:能量最低原理
按1s→2s → 2p → 3s → 3p → 4s → 3d顺序,先填充
