化合价与化学式(讲义及答案)
初中常见化合价、化学式、化学方程式
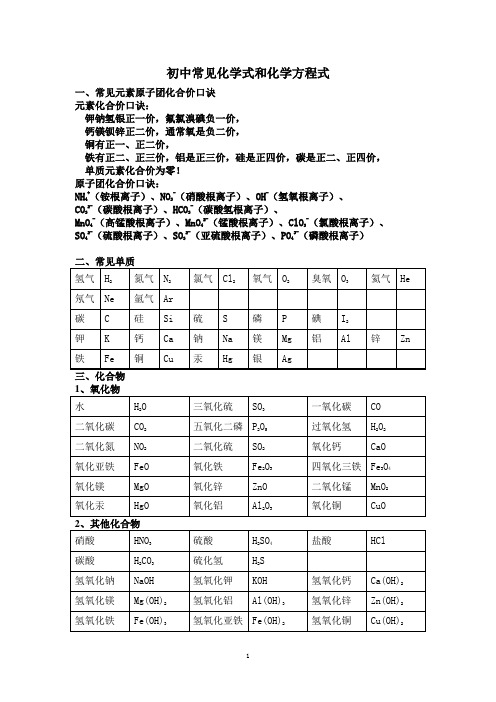
初中常见化学式和化学方程式一、常见元素原子团化合价口诀元素化合价口诀:钾钠氢银正一价,氟氯溴碘负一价,钙镁钡锌正二价,通常氧是负二价,铜有正一、正二价,铁有正二、正三价,铝是正三价,硅是正四价,碳是正二、正四价,单质元素化合价为零!原子团化合价口诀:NH4+(铵根离子)、NO3-(硝酸根离子)、OH-(氢氧根离子)、CO32-(碳酸根离子)、HCO3-(碳酸氢根离子)、MnO4-(高锰酸根离子)、MnO42-(锰酸根离子)、ClO3-(氯酸根离子)、SO42-(硫酸根离子)、SO32-(亚硫酸根离子)、PO43-(磷酸根离子)初中常见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P + 5O2 2P2O52、氢气在空气中燃烧生成水:2H2 + O22H2O3、硫磺在空气(或氧气)中燃烧:S + O2 SO24、镁条在空气(或氧气)中燃烧:2Mg + O22MgO5、铁丝在氧气中燃烧:3Fe + 2O2 Fe3O46、木炭在空气(或氧气)中完全燃烧:C + O2 CO27、木炭不充分燃烧:2C + O22CO8、一氧化碳燃烧:2CO + O2 2CO29、二氧化碳和水反应生成碳酸:CO2 + H2O == H2CO310、二氧化碳通过灼热的炭层:CO2 + C 2CO点燃点燃点燃点燃点燃点燃点燃高温点燃11、生石灰作为干燥剂:CaO + H2O == Ca(OH)2二、分解反应11、高锰酸钾制氧气:2KMnO4 K2MnO4+ MnO2+ O2↑12、氯酸钾制氧气:2KClO3 2KCl + 3O2↑13、双氧水制氧气:2H2O22H2O + O2↑14、电解水:2H2O 2H2↑+ O2↑15、碳酸分解:H2CO3H2O + CO2↑16、高温煅烧石灰石(工业制取二氧化碳):CaCO3 CaO +CO2↑三、置换反应17、铜和硝酸银溶液反应:Cu + 2AgNO3 == 2Ag + Cu(NO3)218、铁和硫酸铜溶液反应:Fe + CuSO4 == Cu + FeSO419、锌和硫酸反应制取氢气:Zn + H2SO4== ZnSO4+ H2↑20、铝和稀硫酸反应:2Al + 3H2SO4== Al2(SO4)3+ 3H2↑21、木炭还原氧化铁:3C + 2Fe2O34Fe + 3CO2↑木炭还原氧化铜:C + 2CuO 2Cu + CO2↑木炭还原四氧化三铁:2C + Fe3O43Fe +2CO2↑氢气还原氧化铜:H2 + CuO Cu + H2O四、复分解反应(一)酸 + 碱→盐 + 水22、氢氧化钠与盐酸反应:NaOH + HCl == NaCl + H2O23、氢氧化钠与硫酸反应:2NaOH + H2SO4== Na2SO4+ 2H2O24、氢氧化铝治疗胃酸过多:Al(OH)3 + 3HCl == AlCl3+ 3H2O25、氢氧化镁与硫酸反应:Mg(OH)2 + H2SO4== MgSO4+ 2H2O(二)酸 + 盐→新酸 + 新盐26、盐酸与硝酸银溶液反应:HCl + AgNO3 == AgCl↓+ HNO3△MnO2△MnO2通电高温高温高温高温高温27、氯化钡溶液与硫酸溶液反应:BaCl2 + H2SO4== BaSO4↓+ 2HCl28、碳酸钠与稀盐酸:Na2CO3+ 2HCl == 2NaCl+ H2O + CO2↑碳酸氢钠与稀盐酸:NaHCO3 + HCl == NaCl+ H2O + CO2↑29、石灰石与稀盐酸反应(实验室)制取二氧化碳:CaCO3+2HCl = CaCl2+H2O+CO2↑(三)碱 + 盐→另一种碱 + 另一种盐30、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓31、氯化铁溶液和氢氧化钠溶液反应:FeCl3+3NaOH==Fe(OH)3↓+3NaCl(四)盐 + 盐→两种新盐32、硝酸银溶液与氯化钠溶液反应:AgNO3 + NaCl == AgCl↓+ NaNO333、氯化钡溶液与碳酸钠溶液反应:BaCl2+ Na2CO3= BaCO3↓+ 2NaCl(五)金属氧化物 + 酸→盐 + 水34、稀盐酸清洗铁锈:6HCl + Fe2O3== 2FeCl3+ 3H2O35、氧化铜与稀硫酸反应:CuO + H2SO4== CuSO4+ H2O五、非金属氧化物 + 碱→盐 + 水36、二氧化碳通入澄清石灰水中:CO2 + Ca(OH)2== CaCO3↓+ H2O37、氢氧化钠在空气中变质:CO2+ 2NaOH = Na2CO3+ H2O38、氢氧化钠溶液吸收二氧化硫:SO2 + 2NaOH==Na2SO3+ H2O39、氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH==Na2SO4+ H2O六、其他反应类型40、一氧化碳还原氧化铜:CO + CuO Cu + CO241、一氧化碳还原氧化铁:3CO + Fe2O32Fe + 3CO2↑42、一氧化碳还原四氧化三铁:4CO + Fe3O43Fe + 4CO2↑43、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O44、甲烷燃烧:CH4 + 2O2CO2+ 2H2O△点燃点燃高温高温。
初三化学 化合价与化学式

化合价与化学式一.化合价口诀:钾钠氢银+1价,钙镁钡锌+2价;氢氧、铵根、硝酸根,氟氯溴碘-1价,通常氧是-2价;都是1价铵为正;铜+1、2 铝+3,铁有+2和+3;硫酸(根)碳酸根-2,碳有+2和+4,硫有-2、+4、6 。
-3价有磷酸根;还有氯酸根-1,高锰酸根也-1。
二. 根据化合价书写化合物的化学式:十字交叉法:一排序二标价三约分四交叉五检查。
一排:将元素(或原子团)符号按正价写前,负价写后的顺序排列;二标:将元素(或原子团)的化合价标在符号的正上方;三约:将正、负化合价的绝对值约成最简整数比;四交:将化合价数值的最简整数比交叉写在另一元素(或原子团)符号的右下角。
注意:①当原子数为1时,1不写出来;②含原子团的化合物,当原子团的个数为2个或2个以上时,要先用括号将原子团符号括起来,再在括号的右下角标明其个数。
五查:检查正、负化合价的代数和是否等于零。
三.化合物的命名规则:1.由两种元素组成的化合物,一般从右向左读作“某化某”。
如:Na2S 读作:硫化钠;AlCl3读作:氯化铝2.由金属元素与氢氧根(OH)组成的化合物,读作“氢氧化某”如:KOH读作:氢氧化钾;Zn(OH)2读作:氢氧化锌3.由氢元素与含氧酸根(SO4、NO3、CO3 等)组成的化合物,读作“某酸”。
(其“某”为除氢、氧元素外的第三种元素的名称)如:H2SO4读作:硫酸;H3PO4读作:磷酸;HClO3读作:氯酸4.由金属元素与含氧酸根(SO4、NO3、CO3 等)组成的化合物,从右向左读作“某酸某”。
如:Na2SO4读作:硫酸钠;Ca(NO3)2读作:硝酸钙5.含铁、铜的化合物应注意,含高价铁(+3)、高价铜(+2)的化合物,直接按上述1、2、4点规则命名,含低价铁(+2)、低价铜(+1)的化合物按上述1、2、4点规则命名时必须在铁、铜名称前加“亚”字。
如:FeCl3读作:氯化铁Cu(OH)2读作:氢氧化铜FeCl2读作:氯化亚铁CuOH读作:氢氧化亚铜四、练习2.写出下列物质的化学式:氧化钾氯化钡硝酸钾氢氧化钙氧化锌氯化钙硝酸锌氢氧化锌氧化铁氯化铵碳酸钾氢氧化钾硫化钾氟化钙碳酸钙氢氧化钡硫化铜氟化钾碳酸银硫化氢硫化亚铜氟化铝碳酸钡氨气硫酸钠硫酸钡硫酸锌盐酸氯酸钾高锰酸钾锰酸钾碳酸二氧化锰五氧化二磷四氧化三铁二氧化硫。
化合价讲义

化合价和化学式一、化合价掌握元素的化合价,请注意以下几点:(1)记住常见元素的化合价,掌握元素化合价的一些规律,如:①在化合物中,通常氢显+1价;氧显-2价;②单质里元素的化合价为零;③一些元素有变价,其化合价的确定,可以通过不变价元素按化合价规则求得。
(2)使用化合价的规则是:在化合物里,元素正负化合价的代数和为零。
(3)掌握常见原子团的化合价。
原子团是在化学反应中相对稳定的原子集团,又叫做根。
下表是一些常见原子团的化合价:根的名称根的符号化合价根的名称根的符号化合价氢氧根OH -1锰酸根-2硝酸根-1碳酸根-2高锰酸根-1硫酸根-2+1碳酸氢根-1 铵根氯酸根-1【例题1】下列物质中均含有氯元素,它们的氯元素的化合价按下列顺序排列:①KCl;②;③HClO;④X;⑤。
根据这种排列规律,X不可能是()A.AgClB.C.D.二、化学式的意义和书写1.化学式的意义①表示一种物质;②表示该物质的组成元素;③由分子构成的物质的化学式可以表示该物质的一个分子及该分子的构成。
2.化学式的书写①单质化学式书写一般用元素符号表示,但像氢气、氧气、氮气、氯气等非金属单质是双原子分子,要在其元素符号的右下角加2;②化合物化学式书写时,正价元素写在左边,负价元素写在右边;正负价总数的代数和为0;③含有原子团的物质,可将原子团看成是一个原子来书写化学式,如氢氧化镁〔〕。
【例题2】请在下表中应用横行和纵行的原子或原子团,进行两两组合,写出正确的化学式,完成表中的空白:AlCuKCl三、关于化学式的计算利用化学式可进行下列各种计算:①相对分子质量;②物质组成元素的质量比;③物质中某元素的质量分数。
【例题3】木糖醇()常用于制造口香糖。
下列有关木糖醇的说法中不正确的是()A.该物质中含碳元素的质量分数是39.47%B.该物质分子中碳、氢、氧原子个数比为5∶12∶5C.该物质中碳、氢、氧三种元素的质量比为5∶12∶5D.该物质的相对分子质量为152中考链接【例题1】(2004·广东省)如下图所示是乙醇分子的模型,则下列说法正确的是()A.该物质是氧化物B.该物质的化学式是C.该物质含有四个碳原子D.大量饮用该物质对人体有益【答案】B【例题2】(2005·江苏省海门市)我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质,常常需要寻找它们之间的内在规律。
初中化学人教版九年级上册精品讲义:4.4 化学式与化合价(学生版)

4.4 化学式与化合价 讲义核心素养学习目标1.通过对化学式的概念、意义、写法及读法的学习,使学生进一步掌握化学语言。
2.通过对化合价的本质及应用的学习,增进学生对物质化学式的认识。
3.通过对化学式的有关计算的学习,培养学生的计算能力和解题的标准性。
1.了解化学式的含义,初步掌握化学式的书写及其意义,会读出简单化合物的名称。
2.让学生掌握化合价中元素化合价的一些规律,熟记一些常见的化合价,并学会根据化学式计算化合价的方法,能利用化合价推求化学式。
3.了解相对分子质量的涵义,并能利用相对原子质量和相对分子质量计算物质的组成。
4.能看懂某些商品、药品标签或说明书上标示的物质成分和含量。
5.通过讨论交流,培养学生利用所学的知识解决实际问题的能力和基本计算能力。
1.概念:用_______________________________表示物质组成的式子叫作化学式。
由分子构成的物质,一般将它们的______作为其化学式。
2.化学式量:化学式中_________________,就是化学式量。
对于由分子构成的物质,其化学式量也叫相对分子质量。
可见化学式量在本质上也是分子的实际质量与碳12原子质量的进行比较而得出的比值,其单位是1(一般不写出来)。
3.原子团有些化合物中的某些原子常作为一个整体参加化学反应,在反应中的表现如同一个原子,化学上用“______”来命名这些原子集合体,常见根的化合价为:氢氧根______、硝酸根______、硫酸根______、碳酸根______、铵根______。
4.化合价的一般规律(1)化合物中元素的化合价有______和______。
金属元素通常显______,非金属元素通常显______。
(2)氧元素通常显______价,氢元素通常显______价。
(3)有些元素在不同的化合物中显示不同的化合价。
(4)在化合物中,各元素的正负化合价之和为______。
(5)单质中,元素的化合价为______。
初三化学预习讲义--第十二讲 化学式与化合价(一)(解析版)

第十二讲化学式与化合价(一)【学习目标】1、了解化学式和化合价的含义,并能准确判断化学式中元素化合价。
2、牢记常见元素化学价及化学式的书写规则和一些常见物质的化学式。
3、熟练化学式的相关计算。
【基础知识】【想一想】什么是化学式?一、化学式1.概念:用化学符号来表示物质组成的式子。
①任何物质都有化学式吗?②同种物质可以有不同的化学式吗?③一个化学式是不是只表示一种物质?④化学式可以任意的书写吗?2、化学式的意义化学式表示的意义:既可表宏观意义,又可表微观意义①宏观意义:A、表示一种物质; B、表示物质的元素组成;②微观意义:C、表示一个分子;D、表示一个分子的微观构成如:H2O 表示水;水是由氢元素和氧元素组成;一个水分子;一个水分子是由2个氢原子和1个氧原子构成1、符号H、2H、H2、2H2各具有什么意义?①H一个氢原子氢元素②2H2个氢原子③H2氢气氢气是由氢元素和氧元素组成一个氢分子一个氢分子由2个氢原子构成④2H22个氢分子2.书写:化学式书写原则:①以客观事实为基础,不可臆造②遵守化合价规则和化合物中正负化合价代数和为零的原则(1)单质:①由原子构成的单质,直接用元素符号表示A:通常用元素符号表示。
例如:铁:Fe;红磷:P②由分子构成的单质,如气态或液态非金属单质,用元素符号及其右下角的数字表示,如O2、N2、H2、Br2。
B:氢气、氮气、氧气、氟气、氯气、溴、碘这七种单质:在元素符号右下角加2表示。
例如:氢气:H2、氧气:O2(2)化合物:①氧化物化学式写法:一般氧元素写在右边, 另一元素写在左边.如: H2O , CO2 , HgO氧右, 非氧左②金属和非金属组成的化合物:一般金属元素排在左边,非金属元素排在右边.如:NaCl , KCl , ZnS.金左, 非金右根据名称从右写到左。
若已读出原子个数的就直接写;若未读出原子个数的需根据化合价来正确书写。
3.化学式的读法:化合物一、两种元素组成的物质读为“某化某”如:CaCl2MgO二、由非金属元素和氧元素组成的物质,读为“几氧化几某”如:P2O5SO2三、金属元素和原子团组成的物质,读为“某酸某”如:CaCO3CuSO4NaNO3四、氢原子和原子团组成的物质,读为“某酸”。
第2讲 化学式与化合价

第2讲 化学式与化合价,百色五年中考命题规律)近五年百色中考考情分析2020年中考预测年份 考点题型 题号 分值本讲考查的重点是化学式的书写及意义,化合价、有关化学式的计算、化学符号的书写及意义,预计2020年百色中考仍会以选择题或计算题考查化学式的意义或有关计算。
2019 化合价、化学式的计算选择、计算题 14、22、30 4 2018 化学式、化学符号及意义、化学式的计算 选择、填空、 计算题 7、22、30 9 2017 化合价、化学符号、化学式的计算 选择、填空、 计算题 11、22、30 9 2016 化合价、化学符号、化学式的计算 选择、填空、 计算题 10、22、30(1) 8 2015化合价、化学符号、化学式的计算选择、填空、 计算题7、22、30(1)9,知 识 清 单)化学式1.化学式:用 元素符号 和 数字 的组合表示物质组成的式子。
2.化学式的意义(以CO 2为例)意义 实例宏观①表示一种 物质 CO 2表示二氧化碳这种物质 ②表示物质的元素组成 CO 2表示二氧化碳由 碳元素 和氧元素 组成微观,表示物质的1个分子,CO 2表示1个 二氧化碳分子 表示物质的分子构成,CO 2表示1个二氧化碳分子是由 1个碳原子和2个氧原子 构成特别提醒 化学式前面的计量数不为1时,化学式只具有微观意义,如2CO 2只能表示2个二氧化碳分子。
3.化学式的书写 (1)单质化学式①组成特点:由同种元素组成。
②(2)化合物的化学式的写法①根据物质的名称(带有数字),直接写出化学式,如五氧化二磷写出P 2O 5即可。
②根据化合价写化学式。
写化合物的化学式一般正价在左,负价在右,用“十”字交叉法写出。
例如,写氧化铝的化学式:(化合价请见考点二)一般步骤(口诀):左正右负写符号 标价步骤不能少 交叉标出原子数 化简、检验即得到写完化学式进行检验(+3)×2+(-2)×3=0,所以书写正确。
化学式与化合价知识点讲解

化学式与化合价专题讲解一、化学式:1、定义:用元素符号和数字的组合表示物质组成的式子叫化学式。
如:Fe、C、P、H2O、O2、H2、NaCl等2、化学式表示的意义:①由分子构成的物质,其化学式意义(以CO2为例):②由原子构成的物质,其化学式的意义(以Fe为例):微观:表示该物质的一个原子:一个铁原子。
3、化学式的读写方法:化学式在初中主要有以下五种形式,各种化学式的读写方法既有规则发也有约定发。
说明:有些物质化学式读法是特定的:如:H2O(水)、CH4(甲烷)等二、化合价:1、化合价含义:元素的化合价是元素的原子在形成化合物时表现出来的一种性质,他用来表示原子之间相互化合的数目。
反映化合物中固定的原子个数比。
2、化合价与离子符号的书写区别:数字位置不同,正负号位置不同,化合价的“1”不能省略联系:同种元素(或原子团)的化合价和离子的电荷,通常数值相等,正、负号相同,只是位置不同。
3、规律:氧元素通常显-2价,氢元素通常显+1价;金属一般显正价,非金属一般先负价;一些元素在不同的化合物中可显不同的化合价。
单质中元素的化合价为零;化合物中各元素的化合价分别乘以他们的脚标(个数),最后相加之和为0。
4、化合价的应用:(1) 根据化合价书写化学式:一般把正价元素或原子团写在左边,负价元素或原子团写在右边;将正负化合价绝对值相约至最简整数后,将其交叉写在元素符号或原子团的右下角。
(2) 根据化学式确定化合价:依据化合物中正负化合价代数和为零的原则;依据原子团中正负化合价代数和为根价的原则,计算确定。
三、相对分子质量及其计算:(1)概念:化学式中各原子的相对原子质量的总和,就是相对分子质量(符号为Mr )。
(2)有关化学式的计算:①根据化学式可以计算物质的相对分子质量。
计算公式:相对分子质量=(相对原子质量×原子个数)之和。
②根据化学式可以计算物质中各元素的质量比。
计算公式:元素质量比=(相对原子质量×原子个数)之比。
化学式与化合价(知识讲解与练习)

化学式与化合价(讲解与练习)【学习目标】1.记住常见元素及原子团的化合价,并能利用化合价推求化学式。
2.会正确书写常见物质的化学式;掌握化学式的意义;能根据物质的化学式做相关的计算。
【要点梳理】要点一、化学式1.化学式的定义:用元素符号和数字的组合表示物质组成的式子,叫做化学式。
2.化学式的意义:(高清课堂《化学式与化合价》一)3.单质化学式的写法:1)单质的化学式的书写(2)化合物的化学式的书写由于化合物是由不同种元素组成的纯净物,因此在书写某化合物的化学式时不但要知道这种化合物是由哪几种元素组成的,还要知道组成这种化合物的各元素的原子个数之比。
知道了这些信息后,就可以先把组成这种物质的各元素的符号按一定顺序写在一起,然后再在元素符号右下角写上小数字来表示该物质的一个分子里所含该元素的原子个数。
把组成化合物的各元素的符号写在一起时的顺序是:①氧化物的化学式,一般把氧的元素符号写在右边,另一种元素的符号写在左边。
②由金属元素与非金属元素组成的化合物,一般把金属的元素符号写在左边,非金属元素的符号写在右边。
③学习了化合价以后,一般把显正价的元素符号写在左边,把显负价的元素符号写在右边。
标化学式里各元素的原子个数时,当原子个数是1时,1可以省略不写。
二、化合价1.化合价的概念:一种元素一定数目的原子跟其他元素一定数目的原子相互化合的性质叫做化合价。
2.化合价的主要作用:利用化合价可以推求实际存在的化合物的化学式。
3.化合价的一般规律:(1)化合价有正价和负价。
①氧元素通常显-2价,氢元素通常显+1价。
②金属元素跟非金属元素化合时,金属显正价,非金属显负价。
(2)一些元素在不同的物质中可显不同的化合价。
例如,FeO中铁显+2价,Fe2O3中铁显+3价。
(3)在化合物里正负化合价的代数和为0。
(4)在单质里元素的化合价为0。
(因为元素的化合价是元素的原子在形成化合物时表现出来的一种性质,所以在单质里元素的化合价为0)4.化合价的应用(1)根据化合价推求实际存在的物质的化学式例题1、写出氧化铝的化学式解:①写出组成氧化铝的两种元素的符号,显正价的写在左边,显负价的写在右边:AlO②求两种元素的化合价的绝对值的最小公倍数,因为铝显+3价氧显-2价:3×2=6③求化学式里个元素的原子个数:最小公倍数÷元素的化合价的绝对值=该元素的原子数,Al: 6÷3=2, O: 6÷2=3④把所求出的原子个数标在相应元素符号的右下角即得到化学式:Al2O3⑤检查化学式,当正价总数与负价总数的代数和等于0时,化学式才是正确的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化合价与化学式(讲义)
一、知识点睛
1. 化合价综合应用
依据:在单质里,元素的化合价为 。
在化合物里,正负化合价的代数和为 。
原子团的化合价为各组成元素正负化合价的。
2. 化学式计算
(1)灵活运用化学式基本计算公式,并能根据公式计算原
子个数、相对原子质量、相对分子质量、元素质量、物质质量等计算。
基本计算公式:
①相对分子质量 M r =(_ × )之和; ②原子个数比=化学式中元素符号右下角数字的 ; ③元素质量比=( × )之比; ④物质中某元素的质量分数
= 元素质量物质质量 ? 100%
= ×100%。
(2)由元素质量比或某元素质量分数确定化学式
①设出化学式,如 A x B y ;
②根据元素质量比建立等式(若出现某元素质量分数, 将其转化成元素质量比建立等式)
m A
x = 元素质量比 = y 相对原子质量比 m B A r (A)
A r (
B )
(或 x :y = m A : m B )A (r A ) A (r B )
③求出原子个数比,确定化学式。
二、精讲精练
1. 碘酸钙[Ca(IO 3)2]是食品及饲料添加剂中补碘补钙的常用试剂,则该物质中碘元素的化合价为( )
A .-1
B .+3
C .+5
D .+7
2.钛铁矿主要成分的化学式为F eTi O x,其中铁元素和钛元素均
显+3 价,则x 为()
A.2 B.3 C.4 D.6
3.三氧化二铋(Bi2O3)可用作防火纸,若铋元素的化合价不
变,则铋元素的氯化物的化学式为()
A.BiCl B.Bi3Cl C.BiCl2 D.BiCl3
4.已知R 元素的化合价为+3,下列化学式不正确的是()
A.R2O3 B.RCl3 C.R(NO3)2 D.R2(SO4)3
5.下列物质中氮元素的化合价按一定顺序排列:①NH3 ②N2
③NO ④X ⑤HNO3。
根据这种排列规律,X 可能是()
A.NO2 B.N2O C.N2O5 D.NaNO3 6.NH4+和NO3-中有关N 的化合价判断正确的是()
A.均为+1 价B.NH4+中为+3 价
C.NO3-中为-3 价D.NO3-中为+5 价
7.用实际参加化学反应的离子符号来表示化学反应的式子叫
离子方程式。
在离子方程式中,反应前后的电荷是守恒的。
现有如下离子方程式:RO3n-+F2+2OH
-RO4-+2F-+H2O,由此可知在RO3n-中,元素R 的化合价为()
A.+4 B.+5 C.+6 D.+7
8.维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人
体生长发育,增强人体对疾病的抵抗力。
下列关于维生素C 的说法错误的是()
A.维生素C 由碳、氢、氧三种元素组成
B.维生素C 的相对分子质量为176
C.维生素C 中碳、氢、氧三种元素的质量比为3:4:3 D.维生素C 中氢元素的质量分数为4.5%
9.柠檬酸是一种广泛用于食品、医疗、日化等行业的重要有机
酸。
它的分子结构如图所示,下列说法正确的是()
A.柠檬酸中含有21 个原子
B.柠檬酸的相对分子质量为192 g
C.柠檬酸中碳、氢元素的质量比为3:4 D
.柠檬酸中元素质量分数最大的为氧元素
10.治疗禽流感的特效药帕拉米韦氯化钠注射液,临床证明其对
H7N9 型的禽流感病毒有明确疗效。
帕拉米韦的化学式为
C x H28N4O4,相对分子质量为328,则x 为。
11.实验测得RO2 中R、O 的元素质量比为3:8,则R 的相对原
子质量为。
12.丙氨酸的相对分子质量是89,其中氮元素的质量分数为
15.8%,则每个丙氨酸分子中含氮原子的个数为。
13.莽草酸由碳、氢、氧三种元素组成,其中氢元素的质量分数约
为5.75%,氧元素的质量分数约为46.0%,且每个分子中含有5 个氧原子。
请回答下列问题:
(1)莽草酸的相对分子质量为;
(2)莽草酸的化学式为。
14.完成下列化学式的相关计算。
(1)丙烷的化学式为C3H8,88 g 丙烷中含氢元素的质量为
g;g 丙烷中含氢元素的质量为2 g。
(2)36 g H2O 与g H2O2 中所含氧元素质量相等。
(3)要使H2O 和H2O2 中含有相同质量的氧元素,则H2O 与H2O2 的质量比是。
15.在X、Y 两种元素组成的一种化合物中,已知X、Y 的元素
质量比为21:8,X、Y 的相对原子质量之比为7:2,则该化
合物的化学式为()
A.X2Y3 B.X2Y5 C.X3Y4 D.X2Y7 16.已知R 元素的相对原子质量为96,在其氧化物中,R、O 的
元素质量比为2:1,则该氧化物的化学式为()A.RO3 B.RO2 C.R2O3 D.RO
17.某氮的氧化物中,N、O 的元素质量比为7:20,则该物质的
化学式为()
A.NO B.NO2 C.N2O4 D.N2O5
18.已知铁的一种氧化物,其中含铁元素的质量分数为70%,则
该氧化物的化学式为()
A.FeO B.Fe2O3 C.Fe3O4 D.无法判断
【参考答案】
一、知识点睛
1.零零代数和
2.(1)①相对原子质量原子个数
②最简比
③相对原子质量原子个数
④该元素原子的相对原子质量×原子个数物质的相对分子质量
二、精讲精练
1. C
2. B
3.D
4. C
5.A
6.D
7. B
8. C
9. D
10. 15
11. 12
12. 1
13. (1)174 (2)C7H10O5
14. (1)16 11
(2)34
(3)18:17
15.C
16.A
17.D
18.B。
