2020-2021学年新教材鲁科版化学学案-2.1-第1课时-元素与物质的关系-物质的分类-含解析
近年-2020版新教材高中化学第2章第1节第1课时元素与物质的分类教案鲁科版必修第一册(最新整理)

2019-2020版新教材高中化学第2章第1节第1课时元素与物质的分类教案鲁科版必修第一册编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019-2020版新教材高中化学第2章第1节第1课时元素与物质的分类教案鲁科版必修第一册)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019-2020版新教材高中化学第2章第1节第1课时元素与物质的分类教案鲁科版必修第一册的全部内容。
第1课时元素与物质的关系物质分类与物质性质学业要求核心素养对接1。
根据物质的组成和性质可以对物质进行分类。
2.感受分类在科研和学习中的重要作用.3.能从物质的宏观特征入手对物质进行分类和表征。
1.通过对“物质的分类"的学习增强宏观辨识水平。
2。
通过“分类方法的应用”的学习,能从物质的宏观特征入手对物质及其反应进行分类和表征。
[知识梳理]知识点一元素与物质的关系盐酸(分析纯)的试剂标签通过上图可以知道,盐酸是由氢元素和氯元素组成的,里面还含有其它的杂质,它们分别由什么元素组成的,元素与物质的关系究竟怎样?请完成下列知识点:1.元素与物质的关系(1)元素是物质的基本组成成分,物质都是由元素组成的.(2)每一种元素都能自身组成单质;绝大多数元素都能与其他种类的元素组成化合物。
而且几种元素组成化合物时,有的只能组成一种,有的则能组成几种不同的化合物.同一种元素组成的物质不一定是单质,可能是混合物,如O2、O32.元素的存在形态及元素的化合价(1)游离态:元素以单质形式存在的状态,其化合价为0。
(2)化合态:元素以化合物形式存在的状态,元素的化合价一般不为0。
2020-2021年高中化学 .1《元素与物质的分类(1)》教案 鲁科版必修1.

2019-2020年高中化学 2.1《元素与物质的分类(1)》教案鲁科版必修1.一.教材分析(一)知识脉络学生在初中化学中已经认识了几种具体物质的性质和单质、酸、碱、盐、氧化物的一般性质,但他们只是从单个物质的角度认识物质的性质,尚未从一类物质的角度认识物质的性质,更未建立起元素与物质的关系。
因此,通过元素与物质的关系的研究,引导学生以元素的观点认识物质;通过研究用不同的标准对物质进行分类,使学生建立分类的观点。
在分类的基础上,研究纯净物——单质、氧化物、酸、碱、盐之间的相互关系;在学生原有的认知结构中已存在溶液、浊液等混合物的观点,进而引进一种新的混合物——胶体,建立分散系的概念,丰富学生对混合物的认识,并使学生了解胶体的一般性质,学会从粒度大小的角度对混合物进行分类。
(三)本节教材的主要特点从单个物质向一类物质过渡,体现分类思想的应用,为形成元素族奠定基础,并以概念同化的方式引入新概念——胶体。
二.教学目标(一)使学生初步接触各种元素及其化合物,知道元素以游离态和化合态两种形态在物质中存在,以及每一种物质都有自己的物质家族,建立起元素与物质家族的关系,了解110多种元素为什么能组成上千万种物质。
(二)从物质组成和性质的角度对物质进行分类,为研究物质的通性建立认识框架,同时知道可以依据不同的标准对物质进行分类。
了解单质、氧化物、酸、碱、盐之间的反应关系,掌握一类物质可能与哪些其它类物质发生化学反应。
体验了解研究一类物质与其它类物质之间反应的关系的过程方法。
(三)知道胶体是一种重要的分散系,了解胶体的丁达尔现象、电泳、聚沉等特性,能够列举生活中胶体的实例,了解胶体性质的简单应用。
三.教学重点(一)知识与技能:元素与物质的关系;胶体的性质。
(二)过程与方法:探讨各类物质的通性及其相互反应关系,学会如何以元素为核心认识物质,从多角度依据不同标准对物质进行分类并体验分类的重要意义。
(三)情感态度与价值观:体会分类的重要意义,依据不同的标准对物质进行分类;让学生树立运用化学知识,使自己生活得更健康。
鲁科版化学必修1《元素与物质的分类》学案
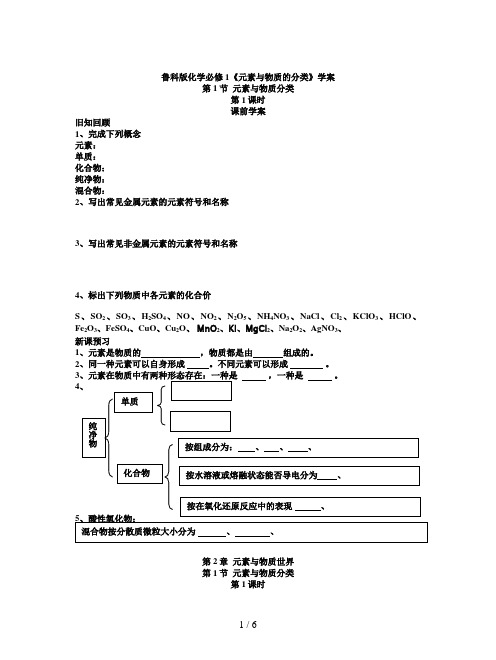
鲁科版化学必修1《元素与物质的分类》学案第1节元素与物质分类第1课时课前学案旧知回顾1、完成下列概念元素:单质:化合物:纯净物:混合物:2、写出常见金属元素的元素符号和名称3、写出常见非金属元素的元素符号和名称4、标出下列物质中各元素的化合价S、SO2、SO3、H2SO4、NO、NO2、N2O5、NH4NO3、NaCl、Cl2、KClO3、HClO、Fe2O3、FeSO4、CuO、Cu2O、MnO2、KI、MgCl2、Na2O2、AgNO3、新课预习1、元素是物质的,物质都是由组成的。
2、同一种元素可以自身形成。
不同元素可以形成。
34第2章元素与物质世界第1节元素与物质分类第1课时课堂学案重难点突破:1、元素的存在形态元素在自然界中的存在形态有两种:一种是游离态即单质,另一种是化合态。
每一种元素的单质和化合物构成了这种元素的物质家族。
金刚石碳单质石墨C60碳元素(C)氧化物:CO 、CO2氢化物:CH4、C2H4等碳的化合物含氧酸:H2CO3碳酸盐:Na2CO3、NH4HCO3等有机物:尿素CO(NH2)2、酒精C2H5OH等例1、下列元素在自然界中既有游离态又有化合态存在的是:()① N ② O ③ Cl ④ C ⑤ Na ⑥ CaA ①②③④B ①②④C ②③④⑤D 全部解析:在自然界中,活泼的金属元素和非金属元素一般以化合态存在,而不活泼的金属元素和非金属元素既可以游离态存在,也可以化合态存在。
但氧元素虽然是活泼非金属元素,空气的成分之一是O2,大气中存在臭氧(O3)层。
答案:B2、元素与物质的多样性①每种元素都能自身组成单质,许多元素还可形成不同单质,如氧元素可形成O2和O3两种单质。
②一种元素与其他元素组成化合物,元素种类不同化合物不同,元素种类相同时也可形成不同化合物,如:Na和O可形成NaO2和Na2O2两种氧化物。
由于可以按照一定的规律以不同的种类和方式进行组合,所以为数不多的元素能组成种类繁多的物质。
2024-2025学年高中化学鲁科版必修一课件2.1.1元素与物质的关系物质的分类

c.能和碱性氧化物生成盐。 CO2 + CaO ==== CaCO3
Ⅲ.大多数非金属氧化物是酸性氧化物, CO、H2O不是酸性氧化物。 个别金属氧化物也是酸性氧化物。 Mn2O7是酸性氧化物。
提醒:非金属氧化物和酸性氧化物的关系:
酸
按是否含氧 元素:
含氧酸H2SO4、HNO3、H3PO4(磷酸)
H2பைடு நூலகம்O3
无氧酸HCl、H2S(氢硫酸)
一元酸HCl、 HNO3
按电离氢离子 数目:
二元酸H2SO4 、H2CO3、 H2S
三…元…酸H3PO4
按挥发性: 挥发性酸、难挥发性酸
……
碱的分类
从是否溶 于水分
碱
从碱性强 弱分
……
可溶碱NaOH、KOH、Ca(OH) 2、 Ba(OH)2、NH3·H2O
2.说出实现各物质之间转化的化学反应。
3.由上述关系图试分析氧化钙能与哪些物质反应?
4.探究:K2O属于上述哪类物质?它可能与哪些物质反
应呢?试举出两例。
推测:下列能与SO3反应的是
A.CO2
B.CaO
C.H20
D.Ca(OH)2
一、元素与物质的关系 1.物质都是由元素组成的 2.物质种类繁多的原因 3.元素的存在形态:游离态、化合态 二、物质的分类 1.酸性氧化物、碱性氧化物 2.单质、氧化物、酸、碱、盐的关系
分类
根据研究对象的共同点和差异点,将它们区分为不同 种类和层次的科学方法。
食物的可存放时间和适宜存放温度
运用分类的实例
分类的好处
为了更全面认识、了解物质世界、研究物质世界: •认识同类的化学物质及其变化的相似性:以点带面、模仿判 断、举一反三、使知识条理化; •找到不同类化学物质及其变化的差异和规律--逻辑推理、由此 及彼,使知识系统化; •创新视角、发现规律、开辟新的知识领域
高中化学第2章元素与物质世界第1节第2课时一种重要的混合物__胶体学案第一册

第2课时一种重要的混合物--胶体发展目标体系构建1.了解分散系的含义及其种类,知道胶体是一种常见的分散系.数轴法辨析三种分散系2.知道胶体可以产生丁达尔现象.3.通过事实了解胶体的性质在生活、生产中的简单应用,体会化学的实用性。
一、分散系微点拨:二、胶体的分离和提纯1.胶体与浊液分离:用过滤的方法,胶体的分散质微粒可以通过滤纸.2.胶体与溶液分离:用渗析的方法,胶体的分散质微粒不能通过半透膜,而小分子、离子能够通过半透膜。
三、胶体的性质和应用3.聚沉错误!1.判断正误(正确的打“√”,错误的打“×")。
(1)NaCl溶液、水、鸡蛋清溶液、淀粉溶液都属于胶体。
(2)FeCl3溶液呈电中性,Fe(OH)3胶体带电,通电时可以定向移动。
()(3)可以利用丁达尔效应区分胶体和溶液。
(4)直径介于1~100 nm之间的微粒称为胶体。
[答案](1)×(2)×(3)√(4)×2.下列关于分散系的说法中不正确的是()A.分散系的稳定性:溶液>胶体>浊液B.分散质微粒的大小:溶液>胶体>浊液C.分散质微粒的直径为几纳米或几十纳米的分散系是胶体D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来B[分散质微粒的大小:浊液>胶体>溶液。
]3.下列事实与胶体性质无关的是()A.在豆浆里加入盐卤做豆腐B.盐碱地里土壤保肥能力差C.一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀D[A项属于胶体的聚沉;B项土壤胶体的分散质微粒带电,盐碱地中的电解质易使胶体聚沉;C项属于丁达尔效应;D项发生化学反应产生沉淀。
]胶体的性质及应用胶体具有一定的稳定性,具有丁达尔效应和电泳的性质(如图),在一定条件下胶体还能发生聚沉,胶体因具有这些性质而在生产和生活中具有广泛的应用。
1.胶体为什么比较稳定?提示:①主要原因是同种胶体的分散质微粒带同种电荷,胶粒相互排斥,胶粒间无法聚集成大颗粒形成沉淀从分散剂中析出.②次要原因是胶粒小,质量轻,布朗运动剧烈,能克服重力引起的沉降作用。
化学鲁科版必修1 第2章第1节元素与物质的分类第1课时 学案-word文档资料

第1节元素与物质的分类第1课时元素与物质的关系物质的分类1.物质是由______组成的。
元素在物质中有两种存在形式:______和______。
2.元素与物质的多样性(1)同一种元素可以形成单质也可以形成化合物,如氧元素可以形成单质______和______;也可以和氢元素结合形成化合物______和________。
在单质中元素是以______形式存在的,在化合物中元素是以______形式存在的。
(2)同一种元素可以形成一种或几种单质,如碳元素的单质有______、______、______,这三种物质互称为__________。
(3)相同的多种元素也可以形成一种或几种不同的化合物,如:碳、氧元素可以形成______、______等化合物。
预习交流1.“由一种元素组成的物质一定是单质”的说法正确吗?2金刚石转变成石墨是什么变化?二、物质的分类1.物质分类的意义对物质进行科学的分类,再分门别类地研究它们的______、______、______等,就容易找到有关规律,把握物质的________和________。
2.物质分类标准的研究(1)根据物质的组成分类:(2)根据物质的组成和性质对无机化合物分类:(3)根据分散物质颗粒大小,将混合物分为:________、______、______等。
(4)根据在水溶液或熔化状态下能否导电将化合物分为:______和________。
(5)根据在氧化还原反应中的表现,可将反应物分为:______和______。
3.物质分类的方法(1)交叉分类法根据______的分类标准,对同一事物进行多种分类的一种分类方法,例如:。
(2)树状分类法对同类事物按照某种属性再进行分类的方法,例如:预习交流1.CO是酸性氧化物吗?2.Na2O2是碱性氧化物吗?答案:一、1.元素游离态化合态2.(1)O2O3H2O H2O2游离态化合态(2)石墨金刚石C60同素异形体(3)CO CO2预习交流:1.答案:不正确,氧气和臭氧组成的混合物也只有一种元素。
2020-2021学年鲁科版高一化学必修2第一单元教案

第1章原子结构元素周期律1.1原子核核素教材分析:本课时是教材第一章第一节第一课时的内容,该课时包括两部分内容:原子核和核素。
首先是在初中学习原子结构的基础上,继续学习原子结构,了解质量数和同位素的基本概念。
在之前的学习中,学生已经知道了原子是由核外电子、质子和中子构成的,但是还没有质量数的概念,通过本课时的学习,学生可以建立原子结构的简单模型,为今后元素周期律的学习打下坚实的基础。
教学目标与核心素养:证据推理与模型认知:理解原子结构的微观模型,知道核素和同位素宏观辨析与微观探析:建立原子结构的微观模型科学态度与社会责任:通过学习认识化学知识的规律性,理解化学知识从实验到理论,再由理论推测出实验结果的科学精神。
教学重难点:重点:原子结构、核素、同位素难点:核素、同位素教学过程:一、知识回顾1.物质由元素组成。
2.物质由分子、原子、离子构成。
3.在化学变化中分子可以再分,原子不可再分。
4.原子是化学变化中的最小粒子。
二、导语展示课件:卢瑟福实验示意图卢瑟福通过实验和理论分析构建的核式原子模型,形象地描述了原子结构。
那么,原子核内部结构是怎样的,电子在核外空间的运动状态又是怎样的?人们对原子结构认识的不断深入,对认识元素性质有哪些帮助?板书:1.1原子核核素三、讲授新课活动一:根据初中学习的关于原子结构的知识,请同学们描述一下原子的结构。
初中化学中,我们学习了,原子是由原子核以及核外电子组成的,而原子核又由质子和中子构成。
相对于原子而言,原子核的体积很小,电子都在核外进行高速运动;原子的质量几乎都集中在原子核上,电子的质量可以忽略,而质子和中子的质量近似相等。
活动二:什么是相对原子质量?一个原子的质量与一个12C 原子质量的1/12的比值活动三:仔细研读下表数据,回答问题:电子、质子、中子的基本数据 1.在原子中,质子数、核电荷数和核外电子数之间存在怎样的关系? 2.原子的质量主要由哪些微粒决定?3.如果忽略电子的质量,质子、中子的相对质量分别取其近似整数值,那么,原子的相对质量在数值上与原子核内的质子数和中子数有什么关系?4.质子和中子为什么能结合在一起?5.原子的质量主要集中在哪儿?6.在原子中,质子数、核外电子数、中子数的关系是什么?7.什么是质量数? 交流与小结:因为微观粒子的质量太小,为了方便起见,一般用相对质量表示微观粒子的质量,例如初中学习的相对原子质量、相对分子质量等。
鲁科版,化学必修一,第二章,元素与物质的关系教案

第2章元素与物质世界第1节元素与物质的分类一. 教学目标(1)知识与技能:①初步接触各种元素及其化合物,知道元素以游离态和化合态两种形态在物质中存在,以及每一种物质都有自己的物质家族,让学生在学习一些个别物质的基础上,建立有限的元素与大量物质间的关系。
②了解110多种元素为什么能组成上千万种物质。
(2)过程与方法:从C、O、H、Na等简单元素入手,通过拼图组合游戏、“数轴法”、“阶梯法”等新颖教学方法,从抽象到直观使学生更好的了解各类物质的通性及其相互反应关系,学会如何以元素为核心认识物质。
(3)情感态度与价值观:①学生主动参与其关系的探究过程,不仅完成了知识上的再发现任务,而且更重要的是在探究过程中能获得一种体验,获得成功感,它对于提高学生的科学素养有着重要的作用。
②体会元素与物质的奇妙关系,培养学生对化学学科的兴趣。
二. 教学重点和难点(1)元素与物质的关系(2)以元素为核心认识进一步物质(3)元素观的建立三. 教学准备教学媒体及课件;用纸板做成的代表元素符号及数字的简易磁性拼图;元素周期表四. 教学方法与学习方法:教学方法——引导探究法;学习方法——合作学习法。
五. 教学过程【板书】第1节元素与物质的分类【导入新课】(展示一盒积木及几种积木组合体)一盒积木能否组合出多种物体?【学生】能【联想质疑】(展示几块类似积木原理的简易磁性拼图)(用硬纸板剪成四个圆形的纸板,分别标上H、O、C、Na代表这四类元素符号,另外小的圆纸板若干张,分别标上数字1、2、3等代表原子个数)我手上有几块代表几种元素的磁性拼图,这些元素可以组合出多少种化学物质?现在请同学们分成4人一组,讨论一下并在下发的表格中尽可能多的写出有关物质的化学式。
【学生活动】(学生讨论并填写下表)元素H、O、C、Na可组合成的常见物质【讨论】(选出一组投影播放学生讨论成果,其他小组补充讨论结果,教师引导学生纠正错误的化学式,培养学生的合作学习能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第1节元素与物质分类
第1课时元素与物质的关系物质的分类
[学习目标]
1.了解元素是物质的基本组成成分以及在物质中的两种存在形态。
2.能根据物质的组成和性质按不同的方法对物质进行分类。
(重点)
3.了解单质、氧化物、酸、碱、盐之间的相互转化关系。
授课提示:对应学生用书第26页
一、元素与物质的关系
1.元素与物质的关系
元素是物质的基本组成成分,物质均是由元素组成的。
2.元素组成物质的形式
(1)单质:由一种元素组成的纯净物叫作单质,分为金属单质和非金属单质。
(2)化合物:由多种元素组成的纯净物叫作化合物。
注意:只由一种元素组成的物质可能是纯净物(单质),也有可能是混合物,如C60和石墨的混合物。
3.元素的存在形态
(1)游离态:元素以自身形式结合成单质时的存在状态,此时元素的化合价为零。
(2)化合态:元素与另外的元素结合成化合物时的存在状态,此时元素的化合价一般为正价或负价。
二、物质的分类与物质的性质
1.物质的分类依据
(1)根据物质的组成分类
物质⎩
⎪⎪⎨⎪⎪⎧
混合物
纯净物⎩⎪⎨⎪⎧ 单质⎩
⎪⎨⎪⎧ 金属单质非金属单质化合物⎩⎪⎨⎪⎧
氧化物酸碱
盐
(2)根据性质分类
氧
化物⎩⎪⎨⎪⎧
酸性氧化物:与碱反应生成盐和水的氧化物,
如CO 2
、Mn 2
O 7
碱性氧化物:与酸反应生成盐和水的氧化物, 如Na 2
O 、Fe 2
O 3
2.根据物质类别研究物质性质
单质、氧化物、酸、碱、盐之间的相互关系
1.下列物质属于纯净物的是( ) A .漂白粉 B .液氯 C .氯水 D .盐酸
答案:B
2.符合图中阴影部分的物质是( )
A.KNO3B.KHSO4
C.K2S D.K2SO4
答案:D
3.下列说法中不正确的是()
A.一种元素可能形成两种或多种不同的单质
B.单质的种数一定多于元素的种数
C.只含一种元素的物质不一定是纯净物
D.只含碳元素的物质在氧气中燃烧只能生成一种物质
答案:D
4.将下列物质及其类别连线。
①酸性氧化物A.HCl
②碱B.NaHCO3
③碱性氧化物C.CO2
④酸D.NaOH
⑤盐E.Na2O
答案:①—C②—D③—E④—A⑤—B
授课提示:对应学生用书第27页
要点一元素与物质的关系
含碳物质的研究。
研究含有0、+2、+4的碳元素的物质,学生共同绘出下图,建立元素及其化合物家族的观念。
其中,属于游离态的是C(填化学式)。
[拓展应用]
根据下列“价—类”二维图回答问题:
其中,属于化合态的是________________(填物质类别)。
答案:氢化物、氧化物、酸、盐
要点二 物质的分类
1.物质的分类
物质⎩
⎪⎪⎪⎪⎨⎪⎪⎪
⎪⎧
混
合
物⎩
⎪⎨⎪
⎧ 均匀混合物(如空气、溶液等)非均匀混合物(如泥土等)纯净物⎩⎪⎪⎨⎪⎪⎧ 单质⎩
⎪⎨⎪
⎧ 金属单质
(如铁、铝、铜等)
非金属单质(如碳、氢气、氧气等)化合物⎩⎪⎨⎪⎧
有机化合物(如CH 3
CH 2
OH 、CH 4
等)
无机化合物
⎩⎪⎨⎪⎧ 酸(如HCl 、HNO 3等)
碱(如KOH 、NH 3
·
H 2O 等)
盐(如NaCl 、NaHCO 3等)
氧化物(如CuO 、SO 2
等)
氢化物(如NH 3
、NaH 等)
2.无机化合物的分类
题组过关] 1.关于物质分类的正确组合是()
选项碱酸盐碱性氧化物酸性氧化物
A Na2CO3H2SO4NaHCO3SiO2CO2
B NaOH HCl NaCl Na2O CO
C NaOH CH3COOH CaF2Na2O2SO2
D KOH HNO3CaCO3CaO SO3
2.奥运五环代表着全世界五大洲的人民团结在一起。
下列各项中的物质,能满足如下图中阴影部分关系的是()
①②③④
A NaCl K2SO4KCl (NH4)2SO4
B Na2SO4K2SO4KCl NH4Cl
C NaCl K2SO4KCl NH4Cl
D Na2SO4K2SO4KCl (NH4)2SO4
解析:①既是钠盐又是硫酸盐,所以是硫酸钠;②既是钾盐又是硫酸盐,所以是硫酸钾;
③既是钾盐又是盐酸盐,所以是氯化钾;④既是铵盐又是盐酸盐,所以是氯化铵。
答案:B
要点三单质、氧化物、酸、碱、盐之间的相互转化关系
⎭⎪
⎬
⎪⎫
1.金属+酸―→盐+氢气
2.金属+盐―→新金属+新盐
置换反应
⎭⎪
⎬
⎪
⎫
3.酸+碱性氧化物―→盐+水
4.酸+碱―→盐+水
5.酸+盐―→新酸+新盐
6.碱+盐―→新碱+新盐
7.盐+盐―→新盐+新盐
8.碱+酸性氧化物―→盐+水
复分解反应
9.金属+氧气―→金属氧化物化合反应
10.碳酸钙高温分解分解反应
[题组过关]
1.下列物质中不属于碱性氧化物,且与酸反应能生成盐和水的是()
A.Na2O B.Na2O2
C.Na D.CuO
解析:Na2O、CuO均是碱性氧化物,A、D不能选;Na是单质,与酸反应产生盐和氢气,C不能选;过氧化钠与酸反应生成盐和水还有氧气,所以选B。
答案:B
2.下列反应不能发生的是()
A.CaCO3+2CH3COOH===(CH3COO)2Ca+H2O+CO2↑
B.CO2+2NaOH===Na2CO3+H2O
C.AgNO3+HCl===AgCl↓+HNO3
D.2HCl+Cu===CuCl2+H2↑
解析:A.该反应是生成挥发性气体的复分解反应,也是较强酸(醋酸)与较弱酸盐(碳酸钙)生成较弱酸(碳酸)和较强酸盐(醋酸钙)的反应。
B.该反应是酸性氧化物与碱生成盐和水的反应。
C.该反应是生成沉淀的复分解反应。
D.从化学方程式形式上来看,该反应是金属置换酸中氢的反应,但是铜位于金属活动性顺序中氢的后面,它不能置换盐酸中的氢。
答案:D
[归纳总结]
1.单质、氧化物、酸、碱和盐之间的转化关系图
2.元素及其化合物转化的主线
学科素养培养(六)——宏观辨认与微观探析
授课提示:对应学生用书第28页
[培养方向]
能从不同层次认识物质的多样性,并对物质进行分类;能从元素和原子、分子水平认识
物质的组成、结构、性质和变化,形成“结构决定性质”的观念。
能从宏观和微观相结合的视角分析与解决实际问题。
[素养特训]
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可采取多种分类方法。
下列各组归类不合理的是()
解析:A项中物质均为含氧化合物;B项中物质均属于酸;C项中氢气燃烧、氧化钙变质、食物腐烂均为化学变化,而冰雪融化属于物理变化;D项中物质均为氮肥。
本题选C。
答案:C。
